使用多克隆免疫球蛋白预防或治疗急性加重的方法和组合物与流程
1.本发明属于通过向呼吸道施用多克隆免疫球蛋白,特别是通过直接应用包含多克隆免疫球蛋白的雾化组合物,预防或治疗慢性肺病例如慢性阻塞性肺病和非囊性纤维化支气管扩张中的急性加重的领域。
2.背景
3.慢性肺病,特别是牵涉其中感染为主要驱动因素的加重的慢性肺病,其特征在于受试者难以充分呼出其肺中的空气。患有此类慢性肺病的患者由于难以从肺中呼出所有空气而具有呼吸急促。由于肺部受损或肺内部气道变窄,所以呼出的空气比正常情况下放出更慢。完全呼气结束时,异常大量的空气仍可能留在肺中。慢性阻塞性肺病(copd)和非囊性纤维化支气管扩张(ncfb)为这类慢性肺病的例子。copd的特征在于持续的气流限制,其通常为渐进的,并且与气道和肺中对有害颗粒或气体的慢性炎症反应增强有关。加重和合并症导致个体患者的整体严重程度[1]。ncfb的特征在于气道病理性扩张
–
通过气道扩大的影像学表现(即通过ct扫描)进行临床鉴定[2]。加重被视为ncfb进展中的关键事件[3]。
[0004]
患有慢性肺病,例如copd和ncfb的患者经常发生呼吸道症状的急性加重。这些急性加重可能由细菌或病毒(它们可能共存)感染引起。在加重过程中,存在突然出现的炎症、充气过度增加和气体截留、呼呼吸流量减少和呼吸困难增加。其他医学状况,例如肺炎可能恶化例如copd的加重。
[0005]
慢性阻塞性肺病的全球倡议(gold)将copd的急性加重定义为患者呼吸道症状的急性恶化,其超出了正常日常变化,导致额外的治疗药物[4]。患者之间加重的发生率差异很大。copd患者加重的长期性支持气道的组织重塑,并促成了该疾病的加剧。这些急性加重与高度的系统性炎症和免疫激活相关联。随着copd严重程度恶化,加重的频率增加。反过来,急性加重可能增加copd的进展,此外,可能的是由急性加重产生的炎症状态增加对另外的、复发性急性加重的敏感性。这导致驱动copd进展的恶性循环。
[0006]
可以将ncfb的加重定义为超出正常日常变化的ncfb的一种或多种症状的急性恶化,例如在一种或多种症状例如咳嗽增加、痰量增加或恶化痰脓性存在下需要抗生素。可以将严重加重定义为需要不定期住院或急诊就诊[3]。
[0007]
患有慢性肺病,例如copd或ncfb的患者很可能出现复发的呼吸道感染,这可能触发急性加重。copd急性加重的最常见原因是上呼吸道和气管支气管树的病毒感染。在copd加重期间检测到的最常见病毒是人鼻病毒(hrv)[5],其与细菌气道微生物组的赘疣有关[6]。copd中的细菌菌群通常高度可变。许多不同的细菌与copd有关。然而,最致病的细菌包括流感嗜血杆菌(haemophilus influenza)、肺炎链球菌(streptococcus pneumonia)、卡他莫拉菌(moraxella catarrhalis)、副流感嗜血杆菌(haemophilus parainfluenzae)和金黄色葡萄球菌(staphylococcus aureus)。另外,铜绿假单胞菌(pseudomonas aeruginosa)(pa)被描述为在稳定copd和急性加重期间患有过度严重气流阻塞的患者中发现的最有害的细菌之一[7]。
[0008]
copd的治疗基于吸入性皮质类固醇(ics)、吸入性支气管扩张剂(包括长效β2激动
剂)和抗胆碱能药(包括长效毒蕈碱受体拮抗剂)及这些药物的组合。例如,具有加重的高风险的严重copd通常使用所有三类药物进行治疗。这些疗法减轻了加重,但是采取最大吸入疗法的患者继续经历加重,且因此需要新的治疗方法。实际上,ics疗法与副作用相关,包括高风险的肺炎、口腔念珠菌病、声音嘶哑和皮肤淤青。其他副作用包括新发糖尿病,糖尿病进展,白内障和肺结核的风险增加。长期使用还与copd患者骨折的风险增加有关[8]。特别地,ics疗法仅适度地降低加重的频率,并且临床试验报告在copd中使用ics增加肺炎的风险。这可能是因为ics似乎降低了抗病毒免疫性,导致粘液分泌过多和肺部细菌载量增加[9]。
[0009]
在患有慢性支气管炎的copd患者中,可以将磷酸二酯酶
‑
4酶抑制剂(例如罗氟司特)添加到所选的治疗中。罗氟司特是一种非甾类抗炎活性物质,其被设计靶向与copd相关的系统炎症和肺部炎症。其适用于作为支气管扩张剂治疗的辅助疗法,用于具有频繁加重史的成人患者的与慢性支气管炎相关的严重copd的维持治疗。
[0010]
copd的急性加重目前用药理学疗法,包括支气管扩张剂、ics和抗生素进行管理。如上所述,ics疗法与副作用相关。抗生素用于治疗细菌性呼吸道感染,以减少加重的发生和严重程度。大环内酯类药物也具有抗炎作用,并且可用于患有严重copd且有频繁加重史的患者。然而,长期大环内酯类药物疗法与微生物耐药性和心血管不良作用的风险有关。目前没有用于治疗copd中病毒感染,例如鼻病毒感染的药物。
[0011]
对于ncfb尚无可利用的治疗。ncfb的急性加重通常用抗生素治疗,以消除潜在的呼吸道感染。一些ncfb患者接受预防性抗生素疗法以防止病情加重。然而,这种疗法的功效尚未得到证实。
[0012]
本发明的一个目的在于提供慢性肺病,特别是具有与感染相关的加重的慢性肺病,例如copd和ncfb的进一步和改善的治疗,特别是预防或治疗急性加重。
[0013]
本发明的公开内容
[0014]
与现有技术基于任选地与皮质类固醇、β2激动剂和/或抗胆碱能支气管扩张剂组合的抗生素用于预防或治疗急性加重的疗法形成鲜明对比,根据本发明,通过将包含多克隆免疫球蛋白的组合物施用于人受试者的呼吸道预防或治疗急性加重。
[0015]
因此,本发明提供包含多克隆免疫球蛋白的组合物,其用于预防或治疗患有慢性肺病的人受试者的急性加重,其中将该组合物施用于受试者的呼吸道。
[0016]
本发明还提供通过向受试者的呼吸道施用包含多克隆免疫球蛋白的组合物预防或治疗患有慢性肺病的人受试者的急性加重的方法。
[0017]
本发明还提供多克隆免疫球蛋白在制备用于预防或治疗患有慢性肺病的人受试者的急性加重的药剂中的用途,其中将该药剂施用于受试者的呼吸道。
[0018]
令人惊奇地,将免疫球蛋白应用于呼吸道的粘膜上皮可以减轻炎症,驱动存在于粘膜层中的潜在致病性微生物(例如细菌和/或病毒)的免疫排斥,并且防止例如细菌胞外酶和毒素和/或病毒复制(脱落)对上皮的直接损伤。这些作用对预防或治疗可能由呼吸道感染例如细菌和/或病毒感染导致的急性加重是有利的。
[0019]
可商购的免疫球蛋白组合物通过静脉内或皮下施用,即通过系统施用来施用。例如通过气雾剂吸入局部施用于靶呼吸道组织可以实现呼吸道中对免疫球蛋白的相同暴露,但是所需的总剂量比系统施用(例如静脉内施用)所需的总剂量更小。由此这种直接向靶呼
吸道组织的局部化施用可以避免系统性副作用。另外,由于仅一部分系统性施用的免疫球蛋白终止于呼吸道,因此向呼吸道施用可以获得比系统性施用可获得的更高的局部浓度。
[0020]
此外,静脉内或皮下免疫球蛋白疗法是昂贵的。直接向呼吸道的靶向、局部施用可以需要施用更小剂量,以实现与系统施用将实现的相同的呼吸道中对免疫球蛋白(例如igg)的暴露。作为结果,直接施用至呼吸道可能更具成本效益性,因为在呼吸道中实现相同的治疗效果需要更少的组合物。
[0021]
此外,静脉内或皮下免疫球蛋白疗法通常需要健康护理专业人员的关注。例如,静脉内施用需要护士或医生,并且通常在诊所中进行。吸入气雾剂免疫球蛋白可以不需要医护人员监督,因此可适合在家中自我施用。因此,对受试者而言,直接向呼吸道施用可能更为实用,因此受试者可能更可能依从这种治疗。依从性的提高减少了可能导致例如急性加重和住院的治疗失败。
[0022]
急性加重
[0023]
本发明涉及患有慢性肺病,典型地copd或ncfb的人受试者的急性加重的预防或治疗。
[0024]
急性加重是急性事件,其特征在于患者的呼吸症状恶化,该恶化超出了正常的日常变化,并且需要额外的疗法。这种急性加重的严重性可能有所不同。
[0025]
在患有copd的受试者中,轻度急性加重是需要对该受试者进行药物改变的急性加重,特别是用短效支气管扩张剂(sabd)治疗该受试者。中度急性加重需要药物干预,特别是用sabd加抗生素和/或口服皮质类固醇治疗。严重急性加重需要住院治疗或去急诊室就诊。本发明的受试者可以患有轻度、中度或重度急性加重。典型地,受试者患有中度或重度急性加重。
[0026]
在患有ncfb的受试者中,急性加重的特征在于局部症状(咳嗽,痰液量增加或粘度变化,有或没有增加哮鸣的痰脓性增加,气喘吁吁,咳血)和/或系统性不适恶化[10]。严重急性加重可以被表征为需要不定期住院或去急诊室就诊的急性加重[3]。
[0027]
在一个实施方案中,本发明的组合物用于预防急性加重,即预防疗法。在一个具体实施方案中,本发明的组合物用于预防急性加重,其中该组合物预防和/或治疗存在于受试者呼吸道中的感染。这种预防疗法特别有效,因为它可以预防病毒感染和细菌感染,并且有效地抵抗对一种或多种抗生素具有抗性的细菌。
[0028]
因此,在一个实施方案中,本发明的组合物用于预防急性加重,特别地,通过治疗和/或预防呼吸道中潜在的感染来进行。多克隆免疫球蛋白特别适合,因为它可以治疗病毒感染和细菌感染,并且有效地抵抗对一种或多种抗生素具有抗性的细菌。
[0029]
在另一个实施方案中,本发明的组合物用于治疗急性加重。典型地,急性加重由呼吸道的病毒或细菌感染引起。多克隆免疫球蛋白识别呼吸道中广谱的潜在致病性微生物(典型地为细菌和病毒)。识别广谱细菌意味着免疫球蛋白有效治疗细菌性呼吸道感染,例如通过免疫排斥。识别广谱病毒意味着免疫球蛋白有效治疗病毒性呼吸道感染,例如通过防止病毒与宿主细胞结合,从而防止病毒复制和脱落。它也可以有效地使用,而无需诊断测试来鉴定可能引起或正在引起急性加重的特定细菌或病毒感染,这意味着可以更早地开始施用所述的组合物。
[0030]
治疗急性加重可预防急性加重恶化的严重程度。例如,治疗轻度急性加重可以预
防其进展为重度急性加重。
[0031]
本发明的组合物用于治疗或预防急性加重。为了这种急性加重的治疗或预防,本发明的组合物可以富含识别特异性病原体的抗体。在一个实施方案中,对患有急性加重的受试者进行了测试,以鉴定出引起急性加重潜在的感染的病原体(例如细菌和/或病毒),并且本发明的组合物富含对所鉴定病原体具有特异性的抗体。在一个实施方案中,通过向组合物补充对所鉴定病原体具有特异性的单克隆抗体而富集本发明的组合物。在另一实施方案中,通过补充对受试者呼吸道中已鉴定出的病原体具有特异性的单克隆抗体而富集本发明的组合物。另外,或者可替代地,该组合物可以富含对某些病原体具有特异性的多克隆免疫球蛋白,例如,其可以通过免疫已被工程化以生产人免疫球蛋白的转基因动物,或者通过筛选对所需病原体具有特异性的抗体的人抗体谱库,然后以重组方式产生鉴定的抗体来得到。
[0032]
在一个具体实施方案中,所述的组合物用于预防或治疗受试者呼吸道中的超级感染。超级感染是在呼吸道的第一次感染期间在呼吸道中发生的第二次感染。特别地,呼吸道超级感染可能存在第二种感染因子的感染,该第二种感染因子对针对第一种感染因子所用的治疗耐药。在一个实施方案中,两种感染都是细菌性呼吸道感染。在另一个实施方案中,感染包含一种细菌性呼吸道感染和一种病毒性呼吸道感染。
[0033]
在一个实施方案中,本发明的受试者具有由对至少一种抗生素具有抗性的细菌引起的呼吸道感染。特别地,所述细菌可能对多种抗生素具有抗性(多重耐药)。本发明的组合物有效抵抗这些耐药细菌,包括多重耐药细菌,因为多克隆免疫球蛋白可识别细菌上的许多表位,包括与抗生素活性和耐药机制无关的表位。
[0034]
在一个实施方案中,本发明的受试者具有由病毒引起的呼吸道感染。本发明的组合物识别病毒并治疗感染。特别地,多克隆免疫球蛋白与病毒结合并阻止病毒与其宿主细胞(例如上皮细胞)结合。多克隆免疫球蛋白可防止病毒进入宿主细胞、病毒复制和病毒脱落。由于没有用于治疗呼吸道感染的有效抗病毒剂,这种治疗可能特别有用。
[0035]
患者史
[0036]
本发明的受试者可以为患有慢性肺病的患者,其具有急性加重史。
[0037]
急性加重率在受试者之间可能不同。本发明的受试者可能具有频繁的急性加重,例如,他们每年经历两次或更多次急性加重。患有频繁急性加重的受试者的最佳预测指标之一是先前治疗过的急性加重的历史。因此,本发明的组合物对于治疗具有频繁的急性加重的风险的受试者特别有用,该受试者对应于具有加重历史的受试者。因此,在一个实施方案中,本发明的组合物用于预防或治疗受试者的急性加重,其中该受试者在预防或治疗前12个月内经历了一次或多次急性加重。优选地,该受试者在预防或治疗之前12个月中经历了两次或更多次急性加重。特别地,该受试者在预防或治疗之前12个月中,经历了3次或更多次急性加重。
[0038]
维持疗法(如下文所讨论)特别适合于具有急性加重历史的这类受试者。因此,在一个具体实施方案中,本发明的受试者在疗法前12个月内经历了至少一次急性加重,并且用该组合物治疗至少12个月。
[0039]
具体地,在copd中,患者未来急性加重频率的最强预测指标之一是前一年经历的急性加重的次数[4]。特别地,在过去一年中经历过两次或更多次急性加重的患有copd的受
试者很可能有频繁加重。因此,在一个具体实施方案中,本发明的组合物用于预防患有copd的受试者的急性加重,其中预防是患有copd的受试者的维持疗法,并且其中该受试者在维持疗法开始前12个月内经历了两次或更多次急性加重,且维持疗法持续至少12个月。
[0040]
具体地,在ncfb中,患者未来急性加重频率的最强预测因素之一是前一年经历的急性加重的次数[3]。特别地,在过去一年中经历过3次或更多次急性加重的患有ncfb的受试者可能有频繁加重。因此,在一个具体实施方案中,本发明的组合物用于预防患有ncfb的受试者的急性加重,其中预防是患有ncfb的受试者的维持疗法,并且其中该受试者在维持疗法开始前12个月内经历了3次或更多次急性加重,而维持疗法持续至少12个月。
[0041]
慢性肺病
[0042]
本发明涉及预防或治疗患有慢性肺病的受试者的急性加重的方法,该慢性肺病特别为其中感染为加重的主要驱动者的慢性肺病,典型地为copd和/或ncfb。
[0043]
copd
[0044]
患有copd的受试者典型地具有支气管扩张剂后fev1(以1s计的用力呼气量)/fvc(用力肺活量)之比小于0.7。可以通过肺量测定法,使用本领域中的标准方法[11]测定fev1和fvc。举例来说,对于支气管扩张剂后肺量测定法测量,可以如下进行肺量测定:(i)施用短效β2激动剂(400μg)后10
‑
15分钟;(ii)施用短效抗胆碱能药(160μg)后30
‑
45分钟;或(iii)施用两类药物的组合后30
‑
45分钟。
[0045]
本发明特别适合于预防或治疗患有中度至非常严重copd,即中度copd、重度copd或非常严重copd的受试者的急性加重。典型地,所述受试者具有重度或非常严重的copd。
[0046]
参考文献[1]中解释了copd严重性的这种分级,其基于受试者中气流限制的严重性。简言之,在fev1/fvc之比<0.7的受试者中,气流限制严重程度的分级基于测定的支气管扩张剂后fev1,以及该测定的值如何与健康受试者的预测值进行比较。患有轻度copd的受试者的fev1为至少预测值的80%。患有中度copd的受试者的fev1为预测值的50%至80%。患有重度copd的受试者的fev1为预测值的30%至50%。患有非常严重copd的受试者的fev1低于预测值的30%。
[0047]
使用如下公式计算健康受试者的预测fev1[12]:
[0048]
男性fev1{升}=4.30*高{米}
‑
0.029*年龄{岁}
‑
2.49
[0049]
女性fev1{升}=3.95*高{米}
‑
0.025*年龄{岁}
‑
2.60
[0050]
举例来说,年龄50岁和身高1.8m的男性受试者具有3.8l的预测fev1(4.3*1.8
–
0.029*50
–
2.49)。如果然后通过肺量测定法测量该受试者具有2.09l的支气管扩张剂后fev1,则该值将是预测fev1(3.8l)的55%,因此该受试者被视为患有中度copd。
[0051]
中度至非常严重copd难以治疗,甚至三联疗法(吸入皮质类固醇/β2激动剂/抗胆碱能支气管扩张剂)也并非始终成功。认为本发明的多克隆免疫球蛋白通过不同于当前治疗机制的机制(包括预防呼吸道感染和减轻呼吸道炎症)来预防或治疗患有copd的受试者的急性加重,因此提供了进一步和补充的治疗。
[0052]
在另一个方面,本发明的组合物用于治疗受试者的copd,其中将该组合物施用于受试者的呼吸道。急性加重促成copd的病理学情况,并且可以促成炎症与进一步感染之间的恶性循环。因此,预防急性加重是治疗copd。在患有copd的受试者中使用本发明的组合物的维持疗法(如下所讨论)特别适合于治疗copd,因为它预防急性加重(其包括降低急性加
重的发生率和/或减轻严重性)。由于类似原因,季节性施用本发明的组合物特别适合于治疗copd。
[0053]
非囊性纤维化支气管扩张
[0054]
本发明涉及治疗患有慢性肺部疾病,特别是其中感染是恶化的主要驱动者的慢性肺部疾病,典型地为ncfb的受试者中的急性加重。ncfb有多种原因,并且可能出现一系列广泛体征。其特征在于气道的病理性扩张。特别地,将其定义为气道的永久性扩张[2],可以通过射线照相术,例如通过计算机体层摄影术(ct)扫描来证明。ncfb的征象微妙地扩张到气道中的囊性变化。患者可能无症状(意外发现气道扩张),或可能出现一系列症状,例如咳嗽和/或痰液产生,伴有周期性加重。
[0055]
本发明特别适合于预防或治疗患有ncfb的受试者的急性加重。在一个实施方案中,本发明的组合物用于预防或治疗患有ncfb的受试者。该组合物特别适用于预防患有ncfb的受试者的重度急性加重。在另一个方面,本发明的组合物用于治疗受试者的ncfb,其中将该组合物施用于受试者呼吸道。急性加重促成ncfb的病理学情况,并且可以促成炎症与进一步感染之间的恶性循环。因此,预防急性加重施治疗ncfb。在患有ncfb的受试者中使用本发明的组合物的维持疗法(如下所讨论)特别适合于治疗ncfb,因为它预防急性加重(包括降低急性加重的发生率和/或减轻严重性)。由于类似原因,季节性施用本发明的组合物特别适合于治疗ncfb。
[0056]
受试者可以表现出copd和ncfb,其共同发病。实际上,ncfb与copd的更晚期阶段相关[2]。因此,在另一个实施方案中,本发明的组合物特别适合于预防或治疗患有copd和ncfb的受试者的急性加重。
[0057]
低igg水平
[0058]
本发明的受试者可以是免疫球蛋白g(igg)水平低于健康成年人的正常范围的受试者。这些受试者罹患copd的风险增加,copd的严重程度增加,和/或copd急性加重的风险增加。ncfb也是具有免疫缺陷,包括低水平的igg的受试者的常见表现。
[0059]
呼吸道,尤其是肺中的igg来自两个来源:位于支气管粘膜中的浆细胞局部产生,以及通过漏出从血浆中产生。因此,本发明的受试者在呼吸道中可能具有低水平的igg,例如由于低系统水平的igg和/或igg的低局部产生。
[0060]
在一个实施方案中,所述受试者具有低血浆水平的igg。如参考文献[13]中所述,健康成年人中总血浆igg的正常范围为639
‑
1,349mg/dl,平均值为994mg/dl。成人血浆igg的低水平可以为低于700mg/dl的水平。成年人较低总血浆igg水平可分为类轻度
‑
中度(300
‑
600mg/dl)、显著(100
‑
300mg/dl)或大幅降低(低于约100mg/dl)。在一个特定的实施方案中,受试者具有低于约700mg/dl、低于约600mg/dl、低于约300mg/dl或低于约100mg/dl的血浆igg水平。在一些实施方案中,受试者具有约100至约600mg/dl范围内的血浆igg水平,(包括在约300至约600mg/dl或约100至约300mg/dl的范围内)。
[0061]
用于测定总血浆igg的不同方法为本领域中已知的,例如速率散射比浊法和/或径向免疫扩散[14]。还可以通过elisa,例如根据用于如下实施本发明的方式中所述的方案,定量血清igg。
[0062]
本发明预防或治疗的急性加重在呼吸道中出现,因此呼吸道中igg的局部浓度是确定呼吸道感染的风险的重要因素,因此也是确定急性加重的风险的重要因素。与健康成
人相比呼吸道igg水平更低的受试者发生呼吸道感染和急性加重的风险更大。因此,在一个实施方案中,本发明的受试者具有比健康成年人更低的呼吸道中的igg水平。
[0063]
可以通过分析来自受试者的痰液来测量呼吸道中igg的水平。痰液是由呼吸道,典型地作为感染或其他疾病,例如copd或ncfb的结果而咳出的唾液和粘液的混合物。通常在显微镜下检查痰液以帮助医学诊断。还可以分析痰液的生物分子,包括免疫球蛋白(例如igg、iga和/或igm)和细胞因子(例如il
‑
1β、il
‑
6和/或il
‑
8)的含量。确定痰中免疫球蛋白浓度的各种方法在本领域是已知的,例如速率散射比浊法和/或径向免疫扩散[15]。痰免疫球蛋白也可以通过elisa,例如,根据以下实施本发明的方式中描述的方案进行定量。
[0064]
本发明的治疗效果
[0065]
呼吸道感染的预防和/或治疗
[0066]
呼吸道感染可以为急性加重的一个原因,因此预防或治疗呼吸道感染特别适用于预防或治疗急性加重。在一个实施方案中,本发明的组合物适用于预防急性加重,其中多克隆免疫球蛋白导致对呼吸道中的一种或多种潜在致病性微生物(例如细菌和/或病毒)的免疫排斥。多克隆免疫球蛋白可以通过结合呼吸道中的潜在致病性微生物导致免疫排斥,例如,多克隆免疫球蛋白结合潜在致病性微生物,并且防止它们粘附至呼吸道的粘膜上皮。
[0067]
在另一个实施方案中,本发明的组合物用于预防或治疗急性加重,其中多克隆免疫球蛋白导致呼吸道中的一种或多种潜在致病性微生物(例如细菌和/或病毒)聚集。微生物的聚集也称作凝集。
[0068]
在另一个实施方案中,本发明的组合物用于预防或治疗急性加重,其中多克隆免疫球蛋白募集免疫细胞以杀伤微生物,例如在称作抗体依赖性细胞的细胞毒性(adcc)的方法中。
[0069]
呼吸道感染导致的损伤的预防和/或减轻
[0070]
受试者呼吸道中微生物的活性可能具有致病作用。因此,在一个实施方案中,本发明的组合物用于预防或治疗急性加重,其中多克隆免疫球蛋白减少病原体(例如细菌和/或病毒)对呼吸道的损害。例如,多克隆免疫球蛋白可以抑制胞外酶的活性。此类胞外酶是例如细菌分泌到粘膜中的酶,且包括例如具有组织降解活性的酶,例如蛋白酶。阻断此类胞外酶的活性可以保护受试者的呼吸道上皮免于受损。在一个具体实施方案中,本发明的组合物防止上皮屏障完整性的丧失,并防止病原体通过上皮。在一个具体实施方案中,病原体是病毒,且多克隆免疫球蛋白与该病毒结合并阻止该病毒与受试者呼吸道中的宿主细胞直接结合。因此,免疫球蛋白阻止了病毒在受试者的呼吸道中进入、复制和脱落。
[0071]
炎症减轻
[0072]
慢性炎症导致小气道的结构变化和狭窄,其促成copd的体征,以及导致ncfb中支气管的不可逆扩张的气道损伤和重塑。增加的炎症和所造成的损害可能会增加急性加重的风险。本发明的组合物可减轻受试者的炎症,因此特别适用于预防或治疗急性加重,典型地在患有copd或ncfb的受试者中。
[0073]
在一个实施方案中,本发明的组合物减轻受试者的炎症,典型地局部炎症,例如呼吸道炎症。特别地,该组合物减少了病原体引起的炎症,特别是受试者呼吸道中的病原体引起的炎症。
[0074]
炎症的特征在于一种或多种促炎细胞因子,例如il
‑
1β和/或il
‑
6和/或il
‑
8的水
平增加。因此,在一个具体实施方案中,本发明的组合物降低il
‑
1和/或il
‑
6和/或il
‑
8的水平,特别是在呼吸道的粘液层中。
[0075]
呼吸道粘液层中一种或多种细胞因子水平(例如il
‑
1β和/或il
‑
6和/或il
‑
8水平)可以通过分析受试者产生的痰中的水平来定量。痰中的细胞因子浓度可以根据标准方法,例如通过速率比浊法[14]或elisa(例如按照下述本发明的方式)定量。
[0076]
多克隆免疫球蛋白
[0077]
本发明涉及多克隆免疫球蛋白在预防或治疗患有慢性肺病的受试者的急性加重中的用途。这类多克隆免疫球蛋白已经成功地用于治疗感染性疾病,作为患有原发性免疫缺陷障碍的受试者中的替代疗法,并且用于预防和治疗各种炎症和自身免疫疾病,以及某些神经障碍。
[0078]
这些多克隆免疫球蛋白制剂被开发用于系统施用,且主要包含igg。目前,这些制剂来源于数以千计的健康供体(1,000
‑
60,000个供体)的汇集的血浆,并且包含特异性和天然的抗体,从而反映出供体群的累积抗原经历。该广谱特异性和天然的抗体可以识别广泛的抗原(例如病原体、外来抗原和自身/自体抗原)。
[0079]
通常,通过静脉内或皮下施用多克隆免疫球蛋白。几种可商购的制剂可利用于这些施用途径。
[0080]
本发明的组合物包含多克隆免疫球蛋白,其也被称为ig。典型地,多克隆免疫球蛋白得自人供体的血浆。优选地,汇集来自多个供体的血浆,以使靶抗原特异性的多样性最大化,例如来自100个以上供体,优选来自500个以上供体,甚至更优选来自1,000个以上供体。
[0081]
典型地,使血浆汇集物经历乙醇分级分离,然后进行几次纯化步骤,例如进一步的沉淀步骤和/或柱色谱步骤,以及使其他病原体失活和去除,例如纳滤或溶剂/洗涤剂处理,例如参考文献16中所示的方法。
[0082]
或者,多克隆免疫球蛋白可以通过例如从包含人免疫组库的文库中重组产生。
[0083]
典型地,多克隆免疫球蛋白为多克隆igg、多克隆单体iga、多克隆二聚化iga、多克隆igm或其组合。在具体实施方案中,所述的组合物包含多克隆igg。多克隆免疫球蛋白还可以包含含有iga和/或igm的j
‑
链,如wo2013/132052中所述的,其与分泌成分合并。
[0084]
igg
[0085]
本发明涉及包含多克隆免疫球蛋白的组合物,其用于预防或治疗患有慢性肺病,典型地copd和/或ncfb的受试者的急性加重。令人惊奇地,本发明人发现了在igg与铜绿假单胞菌之间形成大免疫复合物。免疫球蛋白的抗原结合主要依赖于靶抗原结合(fab)结构域。当igg相对于fab结构域仅为二价时,这类铜绿假单胞菌与igg之间的聚集体(免疫复合物)是令人意外的。因此,在一个实施方案中,本发明的组合物包含多克隆人血浆来源的igg。多克隆免疫球蛋白为至少95%igg,优选为至少98%igg。多克隆igg通过治疗和/或预防一种或多种呼吸道感染特别适用于预防或治疗患有慢性肺病,典型地copd和/或ncfb的受试者的急性加重。
[0086]
igg和铜绿假单胞菌的免疫复合物的令人意外形成的一种解释在于,igg可能通过其糖另外与fab区外部的铜绿假单胞菌结合。因此,igg可能在向免疫系统传导铜绿假单胞菌信号方面令人意外地比所预期的更有效。因此,在一个具体实施方案中,包含igg的本发明的组合物用于预防或治疗患有慢性肺病,典型地copd和/或ncfb的受试者的急性加重,其
中该受试者患有并发的铜绿假单胞菌感染。在另一个实施方案中,将包含igg的本发明的组合物施用于受试者以预防铜绿假单胞菌的呼吸道感染。因此,在一个优选的实施方案中,将包含igg的本发明的组合物用于预防急性加重,其中该组合物作为维持疗法施用。该组合物对于患有慢性肺疾病,典型地为copd和/或ncfb的受试者的维持疗法特别有用,因为铜绿假单胞菌是机会病原体,其可以影响具有肺防御能力受损的受试者,例如患有copd或ncfb的患者。特别地,将其描述为是copd患者中以及copd急性加重过程中发现的最有害的细菌之一[7]。
[0087]
可以得到具有至少95%igg纯度的正常人igg,这意味着95%的多克隆ig为igg。因此,在一个实施方案中,本发明的组合物中包含的igg通常具有至少95%igg,优选至少96%igg,更优选至少98%igg,例如至少99%igg的纯度。
[0088]
向患有选择性iga缺乏症的受试者施用包含iga的组合物可导致受试者的过敏反应。过敏反应是一种严重的过敏反应,其通常迅速开始并可能导致受试者死亡。因此,在一些实施方案中,本发明的组合物仅包含少量的iga,例如小于200μg/ml的iga,优选小于25μg/ml的iga。这些组合物特别适合于向受试者施用,其中该受试者具有选择性的iga缺乏症。此外,选择性的iga缺乏症没有严重的症状,因此本发明的受试者可能不知晓其具有选择性的iga缺乏症。因此,这些组合物特别适用于向不知道是否具有选择性iga缺乏症的受试者施用。
[0089]
因此,在一个优选的实施方案中,本发明的组合物包含为至少98%igg的多克隆免疫球蛋白,并且包含低于25μg/ml的iga。
[0090]
在一个具体实施方案中,用于本发明的组合物为privigen
tm
。根据本发明还可以使用的商购免疫球蛋白制剂包括:bivigam
tm
、clairyg
tm
、flebogam
tm 5%、flebogamma
tm dif 5%、gammagard
tm
液体10%、gammaplex
tm
、gamunex
tm 10%、ig vena
tm n、intratect
tm
、kiovig
tm
、nanogam
tm
、octagam
tm
、octagam
tm 10%、polyglobin
tm n10%、sandoglobulin
tm nf液体、vigam
tm
和iqymune
tm
。
[0091]
特异性抗体富集的多克隆免疫球蛋白
[0092]
本发明涉及用于预防和/或治疗患有慢性肺病,典型地copd和/或ncfb的受试者的急性加重的组合物。如上所述,急性加重可以因受试者的呼吸道感染导致。在一个实施方案中,本发明的组合物富集一种或多种对一种或多种特定病原体(例如细菌和/或病毒)或潜在致病性微生物(例如细菌和/或病毒)具有特异性的抗体。这类组合物特别有用,因为它具有增加免疫球蛋白的有效剂量的作用,免疫球蛋白对微生物或病原体具有活性,其因此具有显著的治疗效果,或在施用较低总剂量的组合物时可以实现等效的治疗作用。在一个实施方案中,本发明的组合物通过对组合物补充对病原体具有特异性的单克隆抗体而富集对病原体具有特异性的抗体。
[0093]
在一个实施方案中,本发明的组合物富集对鼻病毒、a型流感、人类偏肺病毒rsv、冠状病毒、b型流感、腺病毒、铜绿假单胞菌、流感嗜血杆菌、肺炎链球菌、卡他莫拉菌、副流感嗜血杆菌和/或金黄色葡萄球菌的一种或多种具有特异性的抗体。这类组合物可能特别有用,因为这些病原体是患有慢性阻塞性呼吸系统疾病,典型地为copd和/或ncfb的受试者的急性加重的最常见原因。优选地,本发明的组合物富集对铜绿假单胞菌具有特异性的抗体,已经将其描述为患有copd的受试者中和copd加重过程中发现的最有害的细菌之一[7]。
优选地,本发明的组合物富集对人鼻病毒具有特异性的抗体,而人鼻病毒为导致copd的急性加重的最常见病毒感染。
[0094]
在一个实施方案中,可以通过用单克隆abs或两种或更多种单克隆抗体的混合物补充包含多克隆免疫球蛋白的组合物,得到富集对特定病原体具有特异性的抗体的本发明的组合物,其对选自如下的一种或多种病原体具有特异性:鼻病毒、a型流感、人类偏肺病毒、rsv、冠状病毒、b型流感、腺病毒、铜绿假单胞菌、流感嗜血杆菌、肺炎链球菌、卡他莫拉菌、副流感嗜血杆菌和/或金黄色葡萄球菌。
[0095]
在一个实施方案中,可以通过用从被工程改造以在免疫接种特定病原体后表达人免疫球蛋白的转基因动物中获得的多克隆免疫球蛋白补充包含多克隆免疫球蛋白的组合物,得到富集对特定病原体具有特异性的抗体的本发明的组合物。
[0096]
在一个实施方案中,可以通过用从使用特定病原体或来源于特定病原体的抗原筛选人抗原结合位点文库并且重组产生具有这些抗原结合位点的病原体特异性免疫球蛋白获得的几种特异性免疫球蛋白补充包含多克隆免疫球蛋白的组合物,得到富集对特定病原体具有特异性的抗体的本发明的组合物。
[0097]
iga和igm
[0098]
在一个实施方案中,本发明的组合物包含iga和/或igm。在一个具体实施方案中,至少95%重量的多克隆免疫球蛋白为iga和/或igm。可以通过与重组分泌成分组合将iga和/或igm组装成分泌抗体。在一个具体实施方案中,所述的组合物包含iga和igm,两者的质量比为约2:1。
[0099]
优选地,例如,如wo 2013/132053中详细描述的,由血浆制备iga和/或igm。
[0100]
可以如wo2013/132052中所详细描述,制备优选地用于本发明的组合物。优选地,在体外将包含iga和/或igm的血浆来源的制备物与sc合并,无需在先纯化包含iga/igm的二聚化/聚合j
‑
链。这类材料称作分泌样iga或分泌样igm,或缩写为sciga或scigm。然而,该材料与体内产生的分泌性iga(通常缩写为siga)和体内产生的分泌性igm(通常缩写为sigm)行为极为类似。
[0101]
在一个实施方案中,所述的组合物包含多克隆人血浆来源的聚合iga和igm。在一个优选的实施方案中,通过与重组分泌成分(sc)组合将iga和igm组装成分泌抗体。优选地,该组合物包含iga和igm,两者的质量比为2:1。
[0102]
在另一个具体实施方案中,所述的组合物包含iga,其纯度为至少90%,优选至少92%,更优选至少94%,甚至更优选至少96%,最优选至少98%。优选地,iga纯化自人血浆;然而,也可以使用iga的另外的来源,例如牛奶、唾液或其他包含iga的体液。在另一个具体实施方案中,iga为单体iga。在另一个具体实施方案中,iga富含二聚化iga,其也包含j
‑
链;优选地,至少20%的iga为二聚化形式,更优选至少30%,甚至更优选至少40%,最优选至少50%。任选地,iga组合物还可以包含分泌成分(sc),优选以重组方式产生的分泌成分。例如,可以使用如wo2013/132052中公开的组合物,通过引用将该文献的全部内容并入本说明书。
[0103]
在还另一个具体实施方案中,所述的组合物包含igm。在一个实施方案中,所述的组合物包含igm和iga。在一个优选的实施方案中,所述的组合物包含igm和二聚化iga,其也包含j
‑
链。任选地,该组合物还可以包含分泌成分,优选以重组方式产生的分泌成分。在另
一个实施方案中,所述的组合物包含igm、iga和igg。在一个具体实施方案中,这类组合物可以包含76%igg、12%iga和12%igm。
[0104]
由人血浆制备iga和/或igm。优选地,将iga和/或igm在体外与分泌成分(sc)合并。更优选地,sc为人分泌成分。甚至更优选地,sc为重组sc,其在哺乳动物细胞系中表达。
[0105]
优选地,组合物中至少10%的蛋白质为sciga(与sc合并的iga),更优选组合物中至少15%、18%、20%或25%,甚至更优选至少30%、40%或50%的蛋白质为sciga。优选地,组合物中至少10%的蛋白质为scigm(igm与sc合并),更优选组合物中至少15%、18%、20%或25%,甚至更优选至少30%、40%或50%的蛋白质为scigm。
[0106]
优选地,组合物中至少10%的蛋白质为sciga,且组合物中至少10%的蛋白质为scigm,更优选至少15%为sciga,且至少15%为scigm,甚至更优选至少20%为sciga,且至少20%为scigm。
[0107]
气雾剂
[0108]
本发明涉及包含多克隆免疫球蛋白的组合物,其用于治疗或预防患有慢性肺病,特别是copd和/或ncfb的患者的急性加重,其中将该组合物施用于受试者的呼吸道。典型地,将本发明的组合物作为气雾剂施用于受试者的呼吸道。可以通过雾化包含多克隆免疫球蛋白的液体含水组合物生成气雾剂。或者,该气雾剂可以为干粉气雾剂,例如作为干粉吸入系统产生[17]。或者,可以使用软雾吸入器、水滴吸入器或加压定量吸入器,或适合于将免疫球蛋白递送至患者呼吸道的任何其他装置。
[0109]
液体含水组合物
[0110]
液体含水组合物特别适合于雾化以形成气雾剂以施用于受试者的呼吸道。因此,本发明的组合物通常为水性液体形式。液体含水组合物为液体系统,其中液体载体或溶剂主要或完全由水组成。在特定情况下,液体载体可以包含小部分的一种或多种与水至少部分混溶的液体。
[0111]
本发明涉及将本发明的组合物施用于受试者的呼吸道。对于这样的呼吸道施用,优选使用高浓度的多克隆免疫球蛋白。通常,高剂量的多克隆免疫球蛋白可用于提高药效,但是,在通过雾化器进行施用时,另外有用的是尽可能地缩短雾化时间,同时也要尽可能地将施用体积减小至最低限度。保持雾化时间尽可能短对维持受试者依从性特别有用。因此,在一个实施方案中,本发明的组合物具有多克隆免疫球蛋白的高浓度,例如约20至约200mg/ml。多克隆免疫球蛋白的浓度可以为20
‑
190mg/ml、20
‑
180mg/ml、20
‑
170mg/ml、20
‑
160mg/ml、20
‑
150mg/ml、30
‑
200mg/ml、30
‑
190mg/ml、30
‑
180mg/ml、30
‑
170mg/ml、30
‑
160mg/ml、30
‑
150mg/ml、40
‑
200mg/ml、40
‑
190mg/ml、40
‑
180mg/ml、40
‑
170mg/ml、40
‑
160mg/ml、40
‑
150mg/ml。适合于本发明的组合物的多克隆免疫球蛋白浓度为20
‑
140mg/ml、20
‑
130mg/ml、20
‑
120mg/ml、30
‑
140mg/ml、30
‑
130mg/ml、30
‑
120mg/ml、40
‑
140mg/ml、40
‑
130mg/ml、40
‑
120mg/ml、50
‑
140mg/ml、50
‑
130mg/ml或50
‑
120mg/ml;特别地,多克隆免疫球蛋白浓度为约50mg/ml、约60mg/ml、约70mg/ml、约80mg/ml、约90mg/ml、约100mg/ml、约110mg/ml或约120mg/ml。
[0112]
相对较高的浓度对于确保低填充量和较短的雾化时间并因此确保治疗的治疗效率很重要。在一个特定的优选实施方案中,所述组合物包含浓度约50mg/ml至约100mg/ml的多克隆igg。最优选地,该组合物包含浓度为约100mg/ml的多克隆igg。
[0113]
典型地,本发明的液体含水组合物包含一种或多种稳定剂。配制液体免疫球蛋白制剂时经常遇到的一个问题在于,如果用适当的添加剂不能充分稳定,则免疫球蛋白倾向于聚集并形成沉淀。因此,在一个实施方案中,本发明的组合物包含稳定剂,例如氨基酸,脯氨酸、甘氨酸和组氨酸,或糖,或糖醇,或蛋白质,例如白蛋白,或其组合。已知这些添加剂中的每一种都能在液体水性制剂中稳定免疫球蛋白,并且可以用于本发明的液体含水组合物中。在一个具体实施方案中,本发明的组合物包含稳定剂,其中该稳定剂是脯氨酸、甘氨酸或组氨酸,优选脯氨酸。
[0114]
液体含水组合物中免疫球蛋白浓度的增加导致粘度的非线性增加。为了避免由高粘度引起的雾化问题,已经发现脯氨酸特别适合用作稳定剂,因为即使多克隆免疫球蛋白的浓度较高,也可以实现本发明的组合物的相对低粘度。如wo2011/095543中公开的。脯氨酸一方面在液体含水组合物中提供了期望的多克隆免疫球蛋白稳定性,而另一方面降低了组合物的粘度,从而以高多克隆免疫球蛋白浓度雾化了小液体体积,这导致通过雾化进行快速有效的治疗。因此,在一个具体实施方案中,特别是当本发明的组合物为液体水溶液形式时,本发明的组合物包含脯氨酸。
[0115]
l
‑
脯氨酸特别适用于本发明的组合物,因为它通常存在于人体中并具有非常有利的毒性特性。l
‑
脯氨酸的安全性已在重复剂量毒性研究、生殖毒性研究、诱变性研究和安全药理学研究中进行了研究,但未注意到不良反应。因此,在一个优选的实施方案中,本发明的组合物包含l
‑
脯氨酸。通常,本发明的组合物包含脯氨酸,优选l
‑
脯氨酸,其在约10至约1000mmol/l,例如约100至约500mmol/l的范围内,特别是约250mmol/l。
[0116]
在一个优选的实施方案中,本发明的组合物包含约210
‑
290mmol/l的l
‑
脯氨酸,特别是250mmol/l的l
‑
脯氨酸。在一个具体实施方案中,所述的组合物包含多克隆igg和约250mmol/l的l
‑
脯氨酸。
[0117]
在一个实施方案中,包含多克隆免疫球蛋白和脯氨酸的本发明液体含水组合物的粘度在1mpa
‑
s和17mpa
‑
s之间(在20.0℃+/
‑
0.1℃温度下)。在一个具体实施方案中,包含100mg/ml多克隆igg和250mmol/l的l
‑
脯氨酸的组合物粘度在20.0℃+/
‑
0.1℃温度下为约3mpa
‑
s。
[0118]
典型地,包含多克隆igg和包含脯氨酸的本发明的组合物具有4.2
‑
5.4,优选4.6
‑
5.0,最优选约4.8的ph,这进一步促成了制剂的高度稳定性。
[0119]
脯氨酸的应用允许制备组合物,其中该制剂的稳定性增加,且该组合物的粘度通过使用一种单一试剂得到降低。这产生特别用于使用筛网雾化器生成气雾剂的方法中的组合物。
[0120]
除多克隆免疫球蛋白外,本发明的组合物通常还包括成分,例如它典型地包括一种或多种另外的药用载体和/或赋形剂。这类成分的讨论在参考文献18中得到。
[0121]
在一个实施方案中,本发明的组合物还包含可药用赋形剂,其用于优化组合物的特性和/或气雾剂的特性。这种赋形剂的实例为用于调节或缓冲ph的赋形剂,用于调节重量摩尔渗透压浓度的赋形剂,抗氧化剂,表面活性剂,用于持续释放或延长的局部保留的赋形剂,掩味剂,甜味剂和矫味剂。这些赋形剂用于获得最佳的ph值,重量摩尔渗透压浓度,粘度,表面张力和味道,从而支持制剂的稳定性,雾化性,吸入时制剂的的耐受性和/或功效。
[0122]
本发明的液体含水组合物典型地具有约60至75mlm/m,优选约64至71mlm/m的表面
张力。可以将表面活性剂加入到本发明的组合物中。这些可以有助于控制多克隆免疫球蛋白在组合物中(即在储存期间和储库中)和雾化期间(即在通过雾化器筛网期间和之后)的聚集速率,由此对气雾剂中多克隆免疫球蛋白的活性产生影响。因此,在一个实施方案中,本发明的组合物为包含表面活性剂例如聚山梨酯,例如聚山梨酯80的液体含水组合物。
[0123]
雾化
[0124]
本发明涉及将所述组合物施用于受试者的呼吸道。本发明的组合物可以作为使用雾化器雾化本发明的液体含水组合物生成的气雾剂施用于受试者的呼吸道。
[0125]
雾化器是一种能够将液体材料雾化成分散液相的装置。气雾剂是一种系统,其包含连续的气相以及分散在其中的固体或液体颗粒(典型地为当通过液体含水组合物的雾化而产生时的液体颗粒)的不连续或分散相。
[0126]
本发明的液体含水组合物可以通过筛网雾化器或超声雾化器或喷射雾化器或任何其他能够喷雾本发明的组合物的装置雾化。在一个实施方案中,筛网雾化器可用于产生气雾剂以施用于受试者。例如,可以使用wo 2015/150510中公开的筛网雾化器和产生的气雾剂,通过引用将该文献的全部内容并入本说明书。
[0127]
分散的液相(气雾剂)主要由液滴组成。分散相的液滴在液体环境中包含多克隆ig,例如igg、iga、igm或其组合。液体环境主要是水相,有或没有如下文进一步所述的其他赋形剂。本领域技术人员将理解,如本文所公开的,关于液体组合物的特征和偏好也可以应用于由其产生的气雾剂的分散相,且反之亦然。
[0128]
可以通过实验测定两个值,且这两个值可用于描述生成的气雾剂的粒径或液滴尺寸:质量中位数直径(mmd)和质量中位数空气动力学直径(mmad)。这两个值之间的差异在于,mmad是针对水的密度(等效空气动力学)校准的。
[0129]
mmad可以通过例如anderson级联冲击器(aci)或下一代冲击器(ngi)这样的冲击器来测量。或者,可以使用激光衍射法,例如malvern mastersizer x
tm
来测量mmd。
[0130]
通过本发明的方法产生的气雾剂的分散相典型地表现出粒径,例如优选地mmd小于10μm,优选约1至约6μm,更优选约1.5至约5μm,且甚至更优选地约2至约4.5μm。或者,粒径的优选地可以具有小于10μm,优选约1至约6μm,更优选约1.5至约5μm,甚至更优选地约2至约4.5μm的mmad。描述气雾剂分散相的另一个参数是雾化液体颗粒或液滴的粒径分布。几何标准偏差(gsd)是用于生成的气雾剂颗粒或液滴的颗粒或液滴尺寸分布的宽度的常用度量。
[0131]
在上述范围内选择精确的mmd应当考虑到目标区域或组织,以沉积气雾剂。例如,最佳液滴直径将取决于是否预期口服、经鼻或气管吸入,以及是否向上和/或向下呼吸道递送(例如,向口咽,咽喉,气管,支气管,肺泡,肺,鼻,和/或鼻旁窦施用)。另外,与年龄相关的解剖学几何形状(例如鼻,口腔或呼吸道的几何形状)以及受试者的呼吸系统疾病和状况以及他们的呼吸模式属于确定将药物递送至下呼吸道或上呼吸道的最佳粒径(例如mmd和gsd)的重要因素。
[0132]
通常,由小于2mm的内径定义的小气道几乎占肺容积的99%,因此在肺功能中起重要作用。肺泡是深肺中氧气和二氧化碳与血液交换的部位。一些病毒或细菌在肺泡中诱导的炎症导致原位流体分泌,并直接影响肺部对氧气的吸收。气雾剂对深肺气道的治疗目标要求具有低于5.0μm,优选低于4.0μm,更优选低于3.5μm,甚至更优选,低于3.0μm的mmd。因
此,设想将这样的mmd值用于本发明。
[0133]
为了将气雾剂递送至呼吸道,该气雾剂具有低于10.0μm,优选低于5.0μm,更优选低于3.3μm,甚至更多优选低于2.0μm的mmd。优选地,mmd(液滴尺寸为)在约1.0至约5.0μm的范围内,且尺寸分布具有小于2.2,优选小于2.0,更优选小于1.8乃至优选小于1.6的gsd。相对于雾化的药物量,这样的粒径和粒径分布参数对于在包括支气管和细支气管的人的呼吸道(例如肺)中实现高局部药物浓度特别有用。在这种情况下,必须考虑到深部肺部沉积需要mmd比在成人和儿童以及婴儿和幼儿的中央气道中的沉积量少,甚至更小的液滴尺寸(mmd)在约1.0至约3.3μm的范围内是更优选的,并且小于2.0μm的范围甚至是更优选的。因此,在气雾疗法中,通常评估小于5μm(代表成人可呼吸的部分)且小于3.3μm(代表儿童可呼吸的或沉积在成人肺的较深处的部分)的液滴部分。另外,通常评估小于2μm的液滴部分,因为它代表了可以最佳地到达成人和儿童的末端细支气管和肺泡并且可以透过婴幼儿肺部的气雾剂比例。
[0134]
在本发明中,具有小于5μm的粒径的液滴的部分优选大于65%,更优选大于70%且甚至更优选大于80%。具有粒径小于3.3μm的液滴比例优选地大于25%,更优选大于30%,甚至更优选大于35%,仍然优选地大于40%。具有粒径小于2μm的液滴比例优选地大于4%,更优选地大于6%,且甚至更优选地大于8%。
[0135]
气雾剂还可以通过在呼吸模拟实验中确定的递送剂量(dd)来表征。例如,基于通过激光衍射(例如malvern mastersizer x
tm
)或使用冲击器(例如anderson级联冲击器
–
aci,或下一代冲击器
‑
ngi)测量的合适呼吸部分(rf),递送的剂量可用于计算可吸入剂量(rd)。当将本发明的方法应用于具有成人呼吸型(正弦式流,500ml潮气量,15次呼气/min)的呼吸模拟实验(例如使用来自copley的呼吸模拟器,如brs3000,或来自pari的compass ii
tm
)并且将2ml组合物(例如200mg ig,200mg igg,200mg iga,200mg igm或其组合)填充入筛网雾化器时,递送剂量(dd)优选地高于40%(80mg ig,例如igg、iga、igm或其组合),更优选高于45%(90mg ig,例如igg、iga、igm或其组合),甚至更优选高于50%(100mg ig,例如igg、iga、igm或其组合).
[0136]
为了治疗上呼吸道,特别是鼻部、鼻和/或鼻窦粘膜、骨肉复合体和鼻旁腔,mmd低于约5.0μm,或低于约4.5μm,或低于约4.0μm,或低于约3.3或低于3.0μm是特别适合的。
[0137]
所产生的气雾剂适用于上呼吸道的适合性可以在鼻吸入模型中评估,例如在wo2009/027095中所述的人鼻铸型模型中。为了将气雾递送至鼻,例如存在来自pari的sinus
tm
装置(喷射雾化器)以及另外的筛网雾化器(vibrent
tm
技术的原型)。
[0138]
本发明中使用的雾化器可以是筛网雾化器。优选地,筛网雾化器是振动膜雾化器。后一种类型的雾化器包含储器,其中用于雾化的液体被填充在该储器中。当操作雾化器时,液体被输送至使之摆动,即振动的网孔(例如,借助于压电元件)。因此,存在于振动筛网一侧的液体通过振动筛网中的开口(也称作为“开口”或“孔”)传输,并在振动筛网的另一侧呈气雾剂形式(例如来自pari的eflow rapid和erapid,来自health and life的hl100以及来自aerogen的aeronebgo和aeronebsolo)。这样的雾化器可以称作“活动性膜雾化器”。
[0139]
在其他有用的筛网雾化器中,可以通过振动液体而不是膜来雾化组合物。这种振动流体筛网雾化器包含储器,其中待雾化的液体填充在该储器中。当操作雾化器时,液体通过液体使其震动的供给系统被供给至膜(即,例如通过压电元件振动)。该液体进料系统可
以是储器罐的振动后壁(例如aerovectrx
tm technology,pfeifer technology),也可以是振动液体递送滑块(例如,来自respironics的i
‑
neb
tm
装置,或来自omron的u22
tm
装置)。这些雾化器可以称作“被动式筛网雾化器”。
[0140]
不同的膜类型可用于使用筛网雾化器雾化液体。这些膜的特征在于不同的孔径,这些孔径会产生具有不同液滴尺寸(mmd和gsd)的气雾剂。根据组合物的特性和期望的气雾剂特性的不同,可以使用不同的膜类型(即,不同的改进的筛网雾化器或气雾剂发生器)。在本发明中,优选使用产生mmd在2.0μm
‑
5.0μm,优选3.0μm
‑
4.9μm且更优选3.4μm
‑
4.5μm的范围内的气雾剂的膜类型。在本发明的另一个实施方案中,优选使用内置在产生气雾剂的气雾剂发生器装置中的膜类型,例如等渗盐水(nacl 0.9%),其具有的mmd在2.8μm
‑
5.5μm,优选3.3μm
‑
5.0μm,且更优选3.3μm
‑
4.4μm的范围内。在本发明的另一个实施方案中,优选使用内置在气雾发生器装置中的膜类型,其产生气雾剂,例如等渗盐水,其具有的mmd在2.8μm
‑
5.5μm,优选2.9μm
‑
5.0μm,且更优选3.8μm
‑
5.0μm的范围内。
[0141]
如果想将所述的治疗靶向下呼吸道,例如支气管或深肺,则特别优选选择压电多孔筛网型雾化器以产生气雾剂。适合的雾化器的实例包括被动筛网雾化器,例如l
‑
neb
tm
,u22
tm
,u1
tm
,micro air
tm
,超声波雾化器,例如multisonic
tm
和/或主动筛网雾化器,例如hl100
tm
、respimate
tm
、eflow
tm technology雾化器、aeroneb
tm
、aeroneb pro
tm
、aeronebgo
tm
和aerodose
tm
装置家族以及原型pfeifer、chrysalis(philip morris)或aerovectrx
tm
装置。特别优选的用于使药物靶向至下呼吸道的雾化器为振动穿孔式膜雾化器或所谓的主动式筛网雾化器,例如eflow
tm
雾化器(电子振动膜雾化器,购自pari,德国)。或者,可以使用被动式筛网雾化器,例如来自omron的u22
tm
或u1
tm
或基于telemaq.fr技术或ing.erich pfeiffer gmbh技术的雾化器。
[0142]
用于靶向上呼吸道的优选的筛网雾化器是通过穿孔的振动膜原理产生气雾剂的雾化器,例如使用eflow
tm
技术的改进的研究性膜雾化器,但是它还能够发射出脉动的气流,从而产生的气雾剂在期望的位置或在将气雾剂云输送至期望的位置(例如鼻窦或鼻旁窦)期间云脉动(即承受压力波动)。这种类型的雾化器具有一个鼻梁,其用于引导将气雾剂云递送至鼻的气流。与以连续(非脉冲)模式递送气雾剂相比,通过这种改进的电子雾化器递送的气雾剂可以更好地到达鼻腔或鼻旁腔。脉动的压力波实现了鼻窦的更强的通气,使得伴随施加的气雾剂可以更好地分布并沉积在这些腔体内。
[0143]
更具体地,用于靶向受试者的上呼吸道的优选雾化器是适于以小于约5升/分钟的有效流速产生气雾剂并且适于同时操作用于以在约10hz至约90hz的范围内的频率实现气雾剂的压力脉动的装置的雾化器,其中有效流速是气雾剂进入受试者的呼吸系统时的流速。在wo2009/027095中公开了这种电子雾化装置的实例。
[0144]
在本发明的一个优选实施方案中,用于靶向上呼吸道的雾化器是这样一种雾化器,该雾化器使用当雾状云到达期望位置时可以中断的递送流,然后以交替的模式开始雾状云的脉动。在wo2010/097119和wo2011/134940中描述了细节。
[0145]
无论是适合肺部递送还是鼻窦递送,优选地均应选择雾化器或使其适合于能够以优选的输出速率雾化单位剂量的雾化器。本文将单位剂量定义为包含有效量的活性化合物即ig、igg、iga、igm或其组合的液体含水组合物的体积,其指定在单次施用期间施用。优选地,雾化器可以以至少0.1ml/min的速率或假设组合物的相对密度通常在1附近,以至少
100mg/min的速率递送这种单位剂量。更优选地,雾化器能够分别产生至少0.4ml/min或400mg/min的输出速率。在进一步的实施方案中,雾化器或气雾剂发生器的液体输出速率为至少0.50ml/min,优选至少0.55ml/min,更优选至少0.60ml/min,甚至更优选至少0.65ml/min,并且最优选至少0.7ml/min,这类装置称作具有高输出量或高输出速率的烟雾发生器。优选地,液体输出速率范围在约0.35至约1.0ml/min或约350至约1000mg/min;优选地,液体输出速率在约0.5至约0.90ml/min或约500至约800mg/min。液体输出速率是指每时间单位雾化的液体组合物的量。液体可以包含活性化合物,药物,ig,igg,iga,igm或其组合和/或替代物例如0.9%的氯化钠。
[0146]
雾化器的输出速率应典型地选择以实现液体组合物的短雾化时间。显然,雾化时间将取决于将被雾化的组合物的体积以及输出速率。优选地,雾化器应被选择或调整为能够在不超过20分钟的时间内雾化一定体积的包含有效剂量的多克隆ig例如igg、iga、igm或其组合的液体组合物。更优选地,单位剂量的雾化时间不超过15分钟。在另一个实施方案中,选择或调整雾化器以使每单位剂量的雾化时间不超过10分钟,并且优选地,不超过6分钟,甚至优选地,不超过3分钟。目前,最优选的雾化时间为0.5至5分钟。
[0147]
根据本发明雾化的组合物的体积优选较低,以允许较短的雾化时间。体积,也称作剂量的体积,或剂量单位体积,或单位剂量体积,应理解为旨在用于一次单次施用或雾化器治疗过程的体积。具体地,该体积可以在0.3ml至6.0ml,优选0.5ml至4.0ml或以上,或更优选地,为1.0ml至约3.0ml,乃至更优选地,约2.0ml。如果残留量为期望的或有帮助,则该残留量应小于1.0ml,更优选小于0.5ml,最优选小于0.3ml。然后,有效雾化的体积优选在0.2至3.0ml或0.5至2.5ml,或更优选地,在0.75至2.5ml或1.0至2.5ml。
[0148]
优选地,雾化器适合于产生气雾剂,其中大部分负载剂量的液体组合物作为气雾剂递送,即具有高输出量。更具体地,雾化器适于产生在组合物中包含至少50%剂量的ig,例如igg、iga、igm或其组合的剂量的气雾剂,或者换句话说,其释放至少50%的ig,例如igg、iga、igm或其组合,或换句话说,其发射填充在储器中的至少50%的液体组合物。特别是与单克隆抗体相比,其中由于其特异性,剂量不需要很高,因此选择能产生如此高输出量的多克隆ig,例如igg、iga、igm或其组合的雾化器非常重要。发现作为本发明的方法中使用的筛网雾化器能够产生具有特别高的输出量的多克隆ig,例如igg、iga、igm或其组合的气雾剂。
[0149]
干粉吸入
[0150]
本发明的组合物还可以为干粉。干粉吸入器的不同形式为可得到的,例如胶囊或多剂量干粉吸入器,单剂量形式,例如旋转吸入器,多剂量,例如accuhaler和圆盘吸入器。干粉吸入器通过提供适合更频繁使用的易于使用的快速的吸入系统而可能是有利的。
[0151]
给药
[0152]
本发明的组合物用于预防或治疗急性加重。
[0153]
在一个实施方案中,本发明的组合物用于预防患有慢性肺病(典型地为copd或ncfb)的受试者的急性加重,其中将该组合物作为维持疗法使用。维持疗法是指一旦疗法启动,则受试者持续使用该疗法延长的时间期限。例如,该疗法持续至少6个月。典型地,该疗法持续至少1年。
[0154]
将本发明的组合物施用于受试者的呼吸道,典型地作为气雾剂。特别地,可以使用
雾化器由液体含水组合物生成气雾剂。适合的液体含水组合物如上所述。在一个优选的实施方案中,液体含水组合物具有约50mg/ml至约150mg/ml,例如约100mg/ml的多克隆免疫球蛋白(例如igg、iga,igm或其组合)。
[0155]
为了对本发明受试者的呼吸道施用,可以将用于生成气雾剂的液体含水组合物以2
‑
10ml的体积施用。
[0156]
为了用于治疗或预防急性加重(典型地为预防),例如copd或ncfb的急性加重,可以将该组合物在疗法期间每隔48小时施用1次,每隔24小时施用1次,或每隔12小时施用1次。在一个具体实施方案中,将本发明的组合物每隔12小时施用1次。在一个具体实施方案中,将本发明的组合物每隔24小时施用1次。在一个具体实施方案中,将本发明的组合物每隔48小时施用1次。
[0157]
为了用于预防或治疗急性加重(典型地为预防),例如copd或ncfb的急性加重,使用约0.01g至约1.5g多克隆免疫球蛋白的剂量。本发明的组合物的特定剂量在约0.1g至约1.5g的多克隆免疫球蛋白,例如约0.2g至约1g的剂量,特别地,该剂量为约0.2g。在一个具体实施方案中,每日1次施用约0.2g的剂量。
[0158]
可以根据可能增加急性加重风险,例如呼吸道感染风险的因素的不同来调整此类剂量。举例来说,根据本发明的施用剂量和/或频率可以在秋季和冬季月份,特别是在冬季月份期间增加。
[0159]
在另一个实施方案中,可以使用干粉吸入器由干组合物产生气雾剂。典型地,在一次施用中递送的剂量可能相对较低,例如约0.5mg,但受试者可以天使用多次吸入,例如一天期间吸入一次至约二十次,优选两次至约十五次。
[0160]
季节性施用
[0161]
本发明的疗法(预防或治疗)在较寒冷的天气中特别有用,这与患有慢性肺病,典型地为copd和/或ncfb的受试者的呼吸道感染和急性加重的比率增加有关。在一个实施方案中,所述的组合物在秋季和/或冬季月份施用。特别地,该组合物在冬季期间施用。copd急性加重的发生率呈季节变化,其中秋季和冬季月份发病率较高[19]。这种急性加重的增加可能是由于呼吸道感染(例如鼻病毒感染)增加导致。因此,在秋季和冬季月份内施用该组合物在风险增加的期间内提供了针对这种感染的防护。
[0162]
这种季节性变化被认为影响所有患有copd的受试者,因此,例如在秋季和冬季月份,尤其是冬季月份,这种季节性施用对于任何以本文为特征的copd受试者都是有用的。可以预期,copd和ncfb之间的相似性,特别是可能由呼吸道感染引起的急性加重启示这种季节性变化对患有ncfb的受试者有用。
[0163]
如本说明书中所用,术语“秋季月份”是指通常被认为是在秋或秋季发生的那些月份。在北半球,这些月份包括9月,10月和11月。在南半球,这些月份包括三月,四月和五月。
[0164]
如本说明书中所用,术语“冬季月份”是指通常认为是在冬季发生的那几个月。在北半球,这些月份包括10月,11月,12月,1月和2月。在南半球,这些月份包括4月,5月,6月,7月和8月。
[0165]
与抗生素的联合疗法
[0166]
本发明的多克隆免疫球蛋白特别适合于与抗生素联合使用,例如用于预防或治疗患有慢性肺病典型地为copd和/或ncfb的受试者的细菌性呼吸道感染。
[0167]
在一个实施方案中,在细菌感染的急性期期间将本发明的组合物与抗生素一起施用,而受试者正在接受抗生素疗法,即除施用标准抗生素疗法外,在前2天期间还施用该组合物,特别是在前3天期间,在前4天期间,或在感染的前5天期间。
[0168]
一般描述
[0169]
术语“包含”涵盖“包括”以及“由
…
组成”,例如“包含”x的组合物可以仅由x组成,或可以包括一些额外的成分,例如x+y。
[0170]
措词“基本上”不排除“完全”,例如“基本上不”含y的组合物可以完全不含y。如果必要,则措词“基本上”可以从本发明的定义中省略。
[0171]
与数值x相关的术语“约”为任选的并且是指例如x
±
10%。
[0172]
本发明的组合物为包含多克隆免疫球蛋白的组合物。除非另有说明,否则归因于该组合物的效果由多克隆免疫球蛋白而不是未指定的另外的成分介导。
[0173]
除非特别说明,否则包含混合两种或更多种成分的步骤的方法不需要任何特定的混合顺序。因此,成分可以以任何顺序混合。如果存在三种成分,则可以将两种成分彼此组合,然后可以将该组合与第三种成分合并等。
[0174]
附图简述
[0175]
现在将在下列非限制性实施例中并参照如下附图举例说明本发明:
[0176]
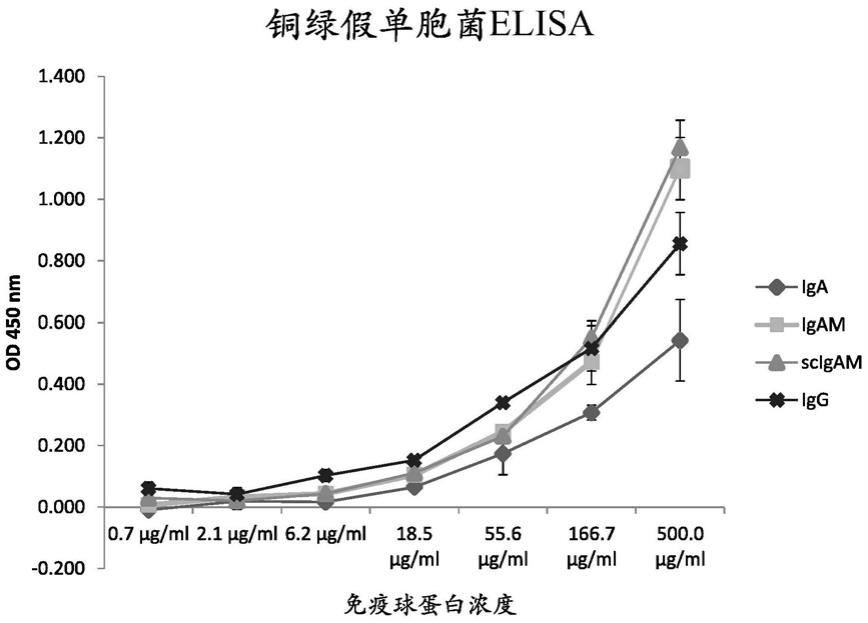
图1.血浆来源的ab制剂与铜绿假单胞菌(pa)相互作用。如通过elisa测定的浓度增加的血浆来源的abs或分泌型iga/m与包被的pa的结合。
[0177]
图2.血浆来源的igg制剂与pa结合促进凝集。与血浆来源的igg相关的pa免疫复合物的激光共聚焦显微镜检查。用cfse标记细菌并且用cy3染料标记igg。图像为得自来自两个独立的载玻片的5
‑
10次观察的一个观察视野的代表。
[0178]
图3.血浆来源的免疫球蛋白制剂pa
‑
诱导的ldh组织释放。通过测量mucilair
tm
在基底外侧培养基中ldh的释放来评估组织损伤。未感染的transwell只接受介质或作为对照的血浆来源的免疫球蛋白制剂。pa感染的transwell作为阳性对照。数据为3个独立实验的代表。
[0179]
图4.血浆来源的igg制剂以剂量依赖性方式预防经上皮电阻缺失。通过测量经上皮电阻来评估组织完整性。未感染和经脯氨酸处理的transwell作为阴性对照,而pa感染的transwell作为组织损伤的阳性对照。数据为3个独立实验的代表。
[0180]
图5.血浆来源的igg制剂以剂量依赖性方式预防pa
‑
诱导的组织损伤。获得石蜡固定的mucilair
tm
切片的激光扫描共焦显微镜检查图像,并分析细胞角蛋白和β
‑
微管蛋白的表达。仅接受介质或igg制剂的未感染transwell作为对照。用介质处理的pa感染的transwell用作阳性对照。数据为3个独立实验代表的。
[0181]
图6.血浆来源的免疫球蛋白制剂减少上皮细胞的pa
‑
诱导的il
‑
8释放。测量了在mucilair
tm
的基底外侧培养基中的il
‑
8。未感染的transwell只接受介质或免疫球蛋白制剂作为对照。用脯氨酸处理过的pa感染的transwell作为阳性对照。数据为3个独立实验的代表。
[0182]
图7.血浆来源的igg制剂以剂量依赖性方式减少pa
‑
水平细胞的诱导的il
‑
8释放。关于当与10cfu pa暴露24h时由mucilair
tm
分泌的il
‑
8,计算了相对的il
‑
8分泌浓度。未感染的transwell只接受介质或免疫球蛋白制剂作为对照。用脯氨酸处理过的pa感染的
transwell作为阳性对照。数据为每种条件下使用来自3个不同供体的mucilair
tm
进行的一项实验的代表。
[0183]
图8.血浆来源的ab制剂减少上皮细胞的pa
‑
诱导的il
‑
6释放。测量了在mucilair
tm
的基底外侧培养基中的il
‑
6。未感染的transwell只接受介质或免疫球蛋白制剂作为对照。用介质处理的pa感染的transwell用作阳性对照。数据为3个独立实验的代表。
[0184]
图9.血浆来源的ab制剂与人鼻病毒c15相互作用。如通过elisa测定的浓度增加的血浆来源的abs或分泌型igam与包被的hrv c15结合。
[0185]
图10.血浆来源的abs减少hrv脱落.使用q
‑
pcr测量在顶端洗涤液中hrv
‑
c15基因组的拷贝数。用脯氨酸处理的hrv感染的transwell作为感染的阳性对照。为了进行功效测量,用芦平曲韦处理的transwell作为阳性对照。
[0186]
图11.血浆来源的abs减轻hrv
‑
诱导的组织损伤。通过测量经上皮电阻来评估组织完整性。用脯氨酸处理的未感染的transwell作为阴性对照。用脯氨酸处理的hrv感染的transwell作为感染的阳性对照。为了进行功效测量,用芦平曲韦处理的transwell作为阳性对照。
[0187]
图12.血浆来源的abs预防hrv
‑
诱导的粘膜纤毛清除减少。粘膜纤毛清除率通过测量30μm直径的聚苯乙烯微珠添加到mucilair
tm
顶端表面上的速度来评估。用脯氨酸处理的未感染的transwell作为阴性对照。用脯氨酸处理的hrv感染的transwell作为感染的阳性对照。为了进行功效测量,用芦平曲韦处理的transwell作为阳性对照。
[0188]
图13.血浆来源的免疫球蛋白制剂以剂量依赖性方式抑制hrv增殖。在用4μg/孔,20μg/孔,100μg/孔和500μg/孔的不同免疫球蛋白制剂处理后,使用q
‑
pcr测量在顶端洗涤液中hrv
‑
c15基因组的拷贝数。用脯氨酸处理的hrv感染的transwell作为感染的阳性对照。为了进行功效测量,用芦平曲韦处理的transwell作为阳性对照。
[0189]
图14.血浆来源的免疫球蛋白制剂以剂量依赖性方式抑制流感病毒的增殖。在用4μg/孔,20μg/孔,100μg/孔和500μg/孔的不同免疫球蛋白制剂处理后,使用q
‑
pcr测量在顶端洗涤液中流感病毒基因组的拷贝数。用脯氨酸处理的流感病毒感染的transwell作为感染的阳性对照。为了进行功效测量,使用奥司他韦处理的transwell作为阳性对照。
[0190]
实施本发明的方式
[0191]
下列非限制性实施例用于举例说明本发明。
[0192]
下列实施例中包括的研究表明,递送至气道组织上的免疫球蛋白可以具有联合的抗微生物(免疫排斥)和抗炎作用,因此是有效治疗或预防患有慢性肺病,例如copd和ncfb的受试者中的急性加重(尤其是与感染相关的加重)的有吸引力的选择。特别地,其适合于患有这些疾病的受试者中的维持疗法,以防止长期感染和急性加重。
[0193]
通过组成性、非特异性物质(粘液、溶菌酶和防卫素)的组合,并且还通过特异性免疫机制包括在体液水平上分泌igs(sigs),提供防止粘膜表面不受微生物移生和可能进入和侵入[20;21]。在体内,对感染的实验性和临床抵抗力可能与在粘膜表面起免疫屏障作用的特异性分泌型iga(siga)抗体(abs)相关[22;23]。认为siga的多价性有利于病原体在粘膜表面的聚集、固定和中和[24;25]。在缺乏iga的个体中,sigm作为siga的替代品显然通过类似的保护机制发挥作用[26]。
[0194]
对于几种病原体,例如脊髓灰质炎病毒、沙门菌属或流感,可以通过许可疫苗的主
动粘膜免疫接种来诱导针对粘膜感染的保护。但是,对于大多数粘膜病原体,没有活性粘膜疫苗可以利用。或者,abs的保护水平可以通过被动免疫直接传递到粘膜表面。实际上,这是通过将母体抗体通过牛奶转移到其后代中而在许多哺乳动物物种中以生理学方式发生的[27]。使用被动粘膜免疫的人和动物研究表明,通过口服,鼻内,子宫内或肺部滴注施用的piga和siga抗体分子可以预防、减少或治愈细菌和病毒感染[28]。然而,很少使用天然存在于粘膜表面的分泌形式的iga,迄今为止尚不可能大规模生产siga。利用生物技术方法构建siga具有挑战性,但此类分子可能具有重要的临床应用[29]。同样适用于含有分泌成分的igm。
[0195]
血浆来源的免疫球蛋白已经数十年用于预防患者因潜在致死性感染导致的免疫缺陷[30]。血浆来源的免疫球蛋白通常对igg具有高纯度。然而,几乎没有在其制剂(例如pentaglobin
tm
)中富含igm的igg产品。血浆来源的免疫球蛋白的递送是静脉内或皮下进行的,从而确保了免疫球蛋白在体内的系统分布。尽管已显示ig替代疗法可降低免疫缺陷患者的肺炎发生率,但显然它们对上呼吸道感染和支气管感染的影响有限。局部施用血浆来源的免疫球蛋白可以在粘膜表面支持更高的ig含量,而不必增加系统性ig的递送。
[0196]
选择hrv和pa来检测血浆来源的免疫球蛋白预防上皮组织感染的功效,因为它们在copd和ncfb急性加重作中起主要作用。为了更好地模拟在人体中的情况,使用基于人类原代细胞的气道模型mucilair
tm
(epithelix s
à
rl,geneva)。mucilair
tm
是在体外重构的人呼吸道上皮细胞模型。mucilair
tm
‑
pool由分别从14种不同或独特的供体中分离出的鼻腔或支气管细胞的混合物制成。在气
‑
液界面上培养,该模型显示出高的经上皮电阻,纤毛跳动以及粘液产生,这证明了上皮组织的全部功能,就像它在体内存在一样。可以在感染期间检测到细胞因子释放(例如il
‑
8和il
‑
6)以及乳酸脱氢酶(ldh)释放,反映出如何感染与该模型中的炎症和组织损伤相关。
[0197]
材料和方法
[0198]
气道感染始于致病菌和病毒在气道上皮顶端的沉积。为了到达组织,病毒会感染上皮细胞,而细菌则倾向于通过外毒素的分泌来损伤细胞。使用铜绿假单胞菌感染模型测试血浆来源的免疫球蛋白预防组织损伤的功效。
[0199]
菌株
[0200]
用于该模型的铜绿假单胞菌(pa)为得自感染性疾病研究所(institute of infectious disease)(波恩大学,瑞士)的临床分离物。pa为人体中导致疾病的致病生物并且是肺部感染的原因。将pa在血琼脂平皿上培养。筛选菌落并且将其在脑心浸液(bhi)培养基中在37℃和400转/分钟(rpm)培养24h。第二天,用新鲜bhi培养基以1:10稀释,并且在37℃和400rpm再放置1小时。然后测量od并且根据od/细菌载量曲线估计细菌数量,所述od/细菌载量曲线在实验前使用多个培养物生成。在给药前采集等分部分用于进一步稀释,且采集第二个等分部分用于进一步在血琼脂板上铺板以精确验证细菌载量。
[0201]
病毒株
[0202]
鼻病毒c15为得自日内瓦医院(hospital of geneva)的临床分离物(名称s07
‑
09
‑
08
‑
u)。用mucilair
tm
培养基生产病毒储备溶液并且在培养基中稀释,对它们既不未进行纯化,也未浓缩。
[0203]
为了进行剂量
‑
效应研究,如[31]中所述,直接用来自临床样本的mucilair
tm
分离
鼻病毒c15(2009)和a型流感/switzerland/7717739/2013(h1n1)。用mucilair
tm
生产用于实验的病毒储备溶液,用培养基采集顶端洗涤液。汇集几天的产量并且通过qpcr定量,等分并且储存在
‑
80℃下。
[0204]
组织
[0205]
mucilair
tm
(epithelix s
à
rl,日内瓦)用于模拟人支气管组织。对于每个研究组,使用3个mucilair
tm transwell,其中每个transwell来源于一个不同供体或用于剂量响应研究的14个供体的混合物。在气
‑
液界面上进行mucilair
tm
培养。用于底外侧的培养基为mucilair
tm
培养基(epithelix s
à
rl,日内瓦),其包含生长因子和酚红。它不含血清。
[0206]
铜绿假单胞菌感染模型和治疗
[0207]
使用pa的感染模型基于在10μl的体积下在一个10μl的mucilair
tm transwell顶侧可沉积低至10个pa菌落形成单位(cfu)。在24h内,pa将增长达到>109cfu/transwell。感染导致乳酸脱氢酶(ldh)(与组织损伤有关)和促炎分子例如il
‑
8和il
‑
6释放。组织中的孔的出现和经上皮电阻的损耗也证明了组织的损伤。
[0208]
在某些实验中,免疫球蛋白在细菌前10分钟或同时沉积。将免疫球蛋白以10μl最终体积施用。将免疫球蛋白的作用与介质溶液(25mm脯氨酸)进行比较。
[0209]
人鼻病毒c15和流感h1n1感染模型和治疗
[0210]
在t=0时,在剂量依赖性研究中(图13&14),对于hrv和流感h1n1,在34℃和5%co2下,将概念验证实验中的15μl 3.8x107基因组拷贝/ml hrv c15(临床菌株:s07
‑
09
‑
08
‑
u)储备溶液(图10)和10μl 1.0x108基因组拷贝数/ml施用在mucilair
tm
的顶侧3h。与病毒5μl同时将免疫球蛋白施用在mucilair
tm
顶侧,并且在3.5和24小时时更新。将免疫球蛋白的作用与介质溶液(25mm脯氨酸)比较。接种后3小时,用pbs(具有ca2+/mg2+)洗涤上皮以清洁接种物。
[0211]
在接种后3.5小时,然后在24、48小时时采集具有200μl mucilair
tm
培养基的不含细胞的顶端洗涤液(20分钟),并且储存在
‑
80℃。
[0212]
免疫球蛋白
[0213]
人血浆来源的igg制剂(igpro10,privigen)按报道制备[32]。从用于由人血浆大规模制备igg的离子交换层析侧级分中得到包含iga和igm的制剂。浓缩含有iga和igm的洗脱级分,并通过切向流过(tff;pellicon xl biomax 30,merck millipore)将其在pbs中重新缓冲至50g/l蛋白质。通过体外合并iga/m与重组人sc,进一步处理所得iga/m溶液(包含质量比为2:1的iga和igm)得到sciga/m[33]。
[0214]
elisa
[0215]
在感染后24h收集的基底外侧培养基的等分试样中测量感染时人支气管组织的促炎细胞因子释放。特别地,评估了il
‑
8(rnd systems;dy208)和il
‑
6(rnd systems;dy206)。根据用户手册进行测量。
[0216]
对于pa elisa,将pa在bbl托
‑
休二氏培养基中在37℃下培养过夜。通过离心(3220g)10分钟使pa沉淀。除去上清液,并将沉淀用0.1m碳酸盐缓冲液(ph 9.6)洗涤2次。将沉淀重悬于碳酸盐缓冲液中,并将50μl/孔(4x 106个细菌)加入到聚山梨酯板上。在2
‑
8℃下包被过夜。第二天,将孔用pbs/吐温(0.05%)洗涤3次,并在室温下用pbs/fcs(2,5%)封闭1.5h。然后将孔用pbs/吐温(0,05%)洗涤3次。在室温下,将ig制剂(0.7μg/ml
‑
500μg/ml)
加入孔中2小时。用pbs/吐温(0,05%),涤2次后,将二抗山羊抗人igg/a/m
‑
hrp(1mg/ml,在封闭缓冲液中为1:2'000)于室温下在样品上温育2h。在使用过氧化物酶的tmb底物之前,用pbs/吐温(0,05%)进行最终洗涤3次。蓝色沉淀形成与每个孔中酶的量成线性比例。用50μl/孔hcl 1m终止酶促反应。在450nm(参比波长620nm)处读取吸光度。从细菌包被的吸光度中减去每个一式三份的平均空白吸光度。
[0217]
对于鼻病毒elisa,将maxisorp板(nunc)在0.1m碳酸盐缓冲液中用纯化的鼻病毒c储备液(3x 106/ml;临床名称:s07
‑
09
‑
09
‑
u)(2
‑
4℃)包被过夜。第二块maxisorp板在0.1m碳酸盐缓冲液中的5%bsa包被,并用作“空白”板。第二天,将孔用pbs/吐温(0,05%)洗涤3次,并在室温下用pbs/fcs(2,5%)封闭1.5h。然后将孔用pbs/吐温(0,05%)洗涤3次。在室温下,将ig制剂(0.7μg/ml
‑
500μg/ml)加入孔中2h。用pbs/吐温(0,05%)洗涤2次后,将二抗山羊抗人igg/a/m
‑
hrp(1mg/ml,在封闭缓冲液中为1:2'000)于室温下在样品上温育2h。在使用过氧化物酶的tmb底物之前,用pbs/吐温(0,05%)进行最终洗涤3次。蓝色沉淀形成与每个孔中酶的量成线性比例。用50μl/孔hcl 1m终止酶促反应。在450nm(参比波长620nm)处读取吸光度。从病毒包被的吸光度中减去每个一式三份的平均空白吸光度。
[0218]
免疫组织学
[0219]
使用激光扫描共焦显微镜检查评价组织损伤。如下制备组织。用pbs将mucilair
tm transwell洗涤一次,并在4℃在4%的多聚甲醛中固定过夜。第二天,将transwell用pbs洗涤3次,并用冰冷的甲醇在
‑
20℃下透化组织30分钟。然后将组织用pbs洗涤3次,并使用3%山羊血清在pbs中于4℃过夜进行封闭步骤。再用pbs洗涤(3次)步骤后,在4℃下用抗
‑
细胞角蛋白抗体(abcam;ab192643)(1/200)、抗
‑
β微管蛋白(abcam;ab11309)(1/200)和dapi(sigma d9542)(1/2000)对组织进行染色48h
‑
72h,均在pbs中稀释。然后将组织用pbs洗涤3次,并从组织中分离出transwell。然后将组织固定在载玻片上,并用固定介质和盖玻片覆盖。将载玻片在室温下放置24h,以使其干燥,然后再在zeiss lsm800共焦显微镜上成像。
[0220]
经上皮电阻(teer)
[0221]
teer是一个动态参数,其反映了上皮细胞的状态。然而,它可能会受到几个因素的影响。例如,如果存在孔或失去紧密的细胞连接,则teer值将达到低于100ω.cm2。相反,当上皮健康时,teer值典型地为200ω.cm2以上。
[0222]
未处理的样品以及用不含病毒或细菌的介质处理的样品用作阴性对照,而10%triton x
‑
100用作阳性对照。
[0223]
为了测量teer值,将200μl mucilair
tm
培养基添加到mucilair
tm
培养物的顶端隔室中,并针对每种情况用evomx伏特
‑
欧姆表(world precision instruments uk,stevenage)测量电阻。使用以下公式将电阻值(ω)转换为teer(ω.cm2):
[0224]
teer(ω.cm2)=(电阻值(ω)
‑
100(ω))x0.33(cm2)
[0225]
其中100ω为膜电阻,且0.33cm2为上皮细胞的总表面积。
[0226]
乳酸脱氢酶(ldh)测定
[0227]
乳酸脱氢酶为质膜破裂时快速释放入培养基中的稳定的胞质酶。在每个时间点采集100μl底外侧培养基并且与细胞毒性检测试剂盒plus、按照制造商的说明(sigma,roche,11644793001)的反应混合物一起温育。然后通过在490nm用微量滴定板读出器测量每一样品的吸光度来对释放的ldh的量进行定量。未处理和介质(无病毒或细菌)用作阴性对照,并
且相当于ldh的生理释放(≤5%)。10%triton x
‑
100用作阴性对照且相当于大量ldh释放(等于100%细胞毒性)。为了测定细胞毒性百分比,使用如下等式(a=吸光度值):
[0228]
细胞毒性(%)=(a(预期值)
‑
a(低对照)/a(高对照)
‑
a(低对照))*100
[0229]
病毒脱落
[0230]
在本研究的每个时间点,使用200μl mucilair
tm
培养基进行顶端洗涤。再用20μl用于病毒rna提取(病毒rna试剂盒(qiagen)),得到60μl rna洗脱体积。通过定量rt
‑
pcr(quantitect探针rt
‑
pcr,qiagen)、使用5μl病毒rna对病毒rna进行定量。还使用两个细小rna病毒科特异性泛
‑
细小rna病毒科引物和细小rna病毒科以及a型流感特异性引物和具有fam
‑
tamra报道分子
‑
淬灭剂染料的探针。
[0231]
包括4种已知浓度的hrv
‑
a16或h3n2 rna稀释液以及用于rt
‑
pcr的对照,并将平板在来自applied biosystems的taqman abi 7000或bio
‑
rad的chromo4 pcr detection system上运行。将ct数据报告到标准曲线,用稀释因子校正,并在示意图上以每ml的基因组拷贝数表示。
[0232]
粘膜纤毛清除
[0233]
使用连接到具有5倍物镜的olympus bx51显微镜的sony xcd
‑
u100cr照相机监控粘膜纤毛清除。将直径为30μm的聚苯乙烯微珠(sigma,84135)添加到mucilair
tm
的顶端表面上。在室温下以每秒2帧的速度对微珠运动进行视频跟踪,以获取30张图像。每个插图拍摄了3个影像。使用imageproplus 6.0软件计算平均珠粒运动速度(μm/sec)。数据表示为平均值+sem(n=3个插图)。
[0234]
实施例1:血浆来源的免疫球蛋白与铜绿假单胞菌相互作用
[0235]
pa与呼吸道的许多感染有关,例如在患有囊性纤维化或严重copd的受试者中。存在许多不同的菌株。临床分离物用于与临床设置的相关性。商购的血浆来源的免疫球蛋白主要由高度纯化的igg组成,该igg是从数千名健康成人供体收集的血浆库中分分级离得到的。由于其多供体来源,分离的免疫球蛋白不仅提供多价和多克隆性,而且作为接种疫苗的结果提供对某些病原体的更高滴度。可以从废物级分中分离出单体iga和五聚化igm与单体/二聚化iga的混合物。本发明人先前已经确定,与重组分泌成分(sc)组合时,可以将多反应性、血清来源的聚合iga、igm和两种同种型的混合物(iga/m)组装成分泌性abs[34]。为了支持它们用于局部被动免疫接种,这些分子在暴露于富含蛋白酶的肠洗液后显示出高度的体外稳定性[35]。
[0236]
图1显示了elisa测定法中血浆来源的免疫球蛋白与pa的结合。重要的是,在此测定法(参见材料和方法部分)中所有血浆来源的免疫球蛋白均能够结合pa临床分离物。与pa的结合是剂量依赖性的,免疫球蛋白的量在0.7μg/ml到500μg/ml变化。免疫球蛋白制剂之间的比较显示pa的结合能力的差异。例如,与sc结合或不与sc结合的iga和igm的混合物显示出对pa的最高亲和力,接着是igg和iga。
[0237]
实施例2:血浆来源的免疫球蛋白igg与pa形成大聚集体
[0238]
免疫球蛋白可能在粘膜表面起多种作用。它们可以用作调理素,导致增强的吞噬识别或促进补体的沉积和随后的裂解。它们可以结合并因此标记受感染细胞,以通过称作抗体依赖性细胞介导的细胞毒性(adcc)的机制进行破坏。免疫球蛋白可以通过结合病原体的表面抗原并抑制其生长来中和病原体。它还可以包被病原体并阻止其粘附于粘膜上皮,
这种机制称作免疫排斥。最后,免疫球蛋白由于具有二价或多价结合特性,可以将微生物凝集成更大的簇,从而使免疫系统更有效地识别和宿主机械清除[36]。存在于粘膜部位的分泌型iga和igm分别具有4价和10至12价。相反,igg仅显示2价。iga和igm比igg更倾向于导致微生物凝集[37;38]。
[0239]
图2显示了通过共聚焦显微镜检查对igg与pa之间形成的免疫复合物的分析。使用cfse标记的pa和cy3标记的血浆来源的igg,令人惊讶地检测到igg
‑
pa的大免疫复合物。免疫球蛋白的抗原结合在很大程度上取决于其抗原结合(fab)片段。由于igg仅是二价的,因此预计不会观察到此类聚集物。该结果可以指出,igg可以潜在地通过其糖另外结合fab区外部的pa。因此,如所预期的igg可能更有效将pa信号传导至免疫系统。
[0240]
实施例3:血浆来源的免疫球蛋白预防由pa诱导的组织损伤
[0241]
pa是一种致病性生物,因其参与生物膜形成及其对许多抗生素耐药而闻名[39]。pa呈现许多毒力因子。其中一些是胞外酶,例如弹性蛋白酶a和b,蛋白酶iv,外毒素a,胞外酶s或溶血素。胞外酶在保护pa抵抗免疫系统的成分以及参与其毒性和相关组织损伤方面发挥作用。
[0242]
为了评估在我们的感染模型中pa引起多大组织损伤,我们测量了乳酸脱氢酶(ldh)的释放,其与质膜破裂有关。实验在我们的原代3d细胞培养系统中进行,且在感染后24h采集的样品中测定了ldh。测试了所有的免疫球蛋白制剂(例如igg,iga,igam和sigam)脯氨酸(介质)。图3表明pa感染正在诱导ldh释放,释放水平高于稳态培养基中发现的正常ldh水平。重要的是,当将免疫球蛋白与pa一起给予时,显示所有免疫球蛋白制剂均能够防止ldh释放,因此防止组织损伤。
[0243]
评估组织损伤的另一种方式示在体外测量组织的经上皮电阻(teer)。实际上,该参数反映了上皮单层或多层的细胞培养模型中紧密连接动力学的完整性[40]。作为结果,当组织完整性受到影响时,teer降低。为了解pa感染如何影响代表主要上皮组织的屏障,测定了感染前teer和感染后24h的teer。图4显示了感染如何影响组织的完整性,以及igg如何在预防该影响中发挥作用。当transwell的顶侧不存在细菌时,最大剂量的igg和脯氨酸不会影响teer。pa感染时,如图3中所见不仅观察到释放了ldh,而且teer也降低(脯氨酸样品)。该结果表明当添加pa时,mucilair
tm
的组织完整性丧失。为了评估这方面igg的活性,使用了与pa(剂量范围为5至500μg)组合的增加剂量的igg。尽管最低的igg剂量并未显示出对组织损伤的良好保护作用,但增加剂量(50至500μg)则显示出对组织的良好保护作用,最高的2种剂量具有最佳效果。
[0244]
除了ldh释放和teer测量外,还使用显微镜观察mucilair
tm
组织,以评估pa感染期间发生的损伤。由于mucilair
tm
是多层上皮组织,因此使用了共焦显微镜检查术。使用与图4相同的设置。感染后24h,将组织固定并切成切片进行染色和分析。图5显示了igg在预防pa诱导的组织损伤中的功效。健康组织(对照)由下排最右侧显示的部分表示。pa感染时,组织中会出现大孔(用脯氨酸处理的transwell;上排,左)。将增加剂量的igg与pa(剂量范围为5至500μg)一起施用。观察到igg在预防组织损伤中的剂量依赖性作用。最低的igg剂量不能防止组织损伤,但似乎具有作用,因为存在具有较小表面的孔。增加igg剂量与无孔相关。然而,对于50至250μg的剂量,仍然可以观察到组织损伤。500μg igg得到了最佳效果,组织看起来和对照孔中一样好。
[0245]
总之,所有血浆来源的免疫球蛋白制剂均能够防止ldh释放。使用igg详细说明了该结果背后的作用机理,已经证实免疫球蛋白可以防止组织完整性的丧失以及组织损伤。
[0246]
实施例4:血浆来源的免疫球蛋白预防铜绿假单胞菌诱导的促炎细胞因子的组织释放
[0247]
粘膜环境中的上皮组织充当外界的屏障,以便从物理上阻止微生物进入组织。然而,一旦受到破坏,则微生物便可以自由进入。因此,为了在可能存在这些屏障的潜在感染和破坏时发出信号,上皮组织通过“危险”信号或细胞因子的分泌与免疫系统相互作用,以提醒免疫系统的细胞成分迁移至组织并提供第二层防御。
[0248]
il
‑
6和il
‑
8为促炎细胞因子,其受到损伤时可被上皮组织分泌。在下一组实验中,评估了血浆来源的免疫球蛋白在预防pa感染引起的促炎细胞因子释放中的作用。图6显示了pa感染后24h mucilair
tm
释放的il
‑
8。测试了所有的免疫球蛋白制剂(例如igg,iga,igam和sigam)以及脯氨酸(介质)。图6表明在pa感染期间il
‑
8分泌高度增加,达到几乎3倍增加。在稳态下,所述免疫球蛋白制剂无一对组织的il
‑
8释放产生显著影响。然而,当与pa一起施用时,所有免疫球蛋白制剂均可以预防pa诱导的il
‑
8分泌。
[0249]
为了描述igg在预防pa诱导的il
‑
8释放中的作用,测试了与pa组合的增加剂量的igg(剂量范围为5至500μg)。图7详细说明了il
‑
8分泌对igg的剂量响应。实验在从3个不同的供体产生的mucilair
tm
上进行。为了解释供体间的差异,将感染后的il
‑
8分泌与脯氨酸联合设定为100%释放条件。计算了相对于100%释放的附加条件。如图7所示,最大剂量的igg和脯氨酸不影响il
‑
8的释放。有意义地的是,igg以剂量依赖性方式明显降低了pa
‑
诱导的il
‑
8分泌,最大剂量(500μg)得到了最佳效果。
[0250]
以相同的方式,研究了pa后感染il
‑
6的分泌。图8显示了pa感染后24h mucilair
tm
释放的il
‑
6。测试了所有的免疫球蛋白制剂(例如igg,iga,igam和sigam)以及脯氨酸(介质)。图8表明pa使il
‑
6分泌高度增加,达到几乎6倍增加。在稳态下,所述免疫球蛋白制剂中没有一种对组织的il
‑
6释放有显著影响。然而,当与pa一施用用时,所有的免疫球蛋白制剂均可以预防pa诱导的il
‑
6分泌。
[0251]
总之,该数据集证明,所有免疫球蛋白制剂均能防止促炎细胞因子例如il
‑
6和il
‑
8的释放,并将潜在地减少接受局部施用的免疫球蛋白作为预防的pa感染受试者的局部炎症。pa感染时预防il
‑
8和il
‑
6分泌实际上可以通过局部施用针对pa的免疫球蛋白翻译组织损伤的预防。血浆来源的免疫球蛋白可能通过针对pa的免疫排斥以及抑制胞外酶活性发挥作用。
[0252]
实施例5:血浆来源的免疫球蛋白与人鼻病毒相互作用
[0253]
已知hrv可导致一半以上的感冒类疾病[41]。然而,也涉及慢性阻塞性肺病(copd)以及哮喘的加重。存在超过100种血清型。为了评估雾化的血浆来源的免疫球蛋白是否可以保护个体免受hrv感染,测试了不同血浆来源的免疫球蛋白与来自hrv临床分离物的结合。图9显示,所有免疫球蛋白制剂均能够以剂量依赖性方式在elisa测定法(参见材料和方法部分)中以0.7μg/ml至500μg/ml的剂量范围结合hrv。然而,在每种免疫球蛋白制剂之间结合是不同的。igg是效力较低的结合剂,而igam和iga显示出良好结合。将sc添加到igam中似乎降低了igam结合hrv的效力。可以指出某些结合不是fab依赖性的。
[0254]
实施例6:血浆来源的免疫球蛋白预防脱落和人鼻病毒诱导的组织损伤
[0255]
像其他病毒一样,hrv正在感染能够复制的细胞。在接下来的步骤中,然后在通过细胞裂解进行细胞输出/脱落之前,将病毒体组装并包装。图10证实了血浆来源的免疫球蛋白防止mucilair
tm
感染后hrv脱落的作用。当使用介质对照(脯氨酸)时,在mucilair
tm
的顶侧检测到pa的高脱落(~109hrv c15基因组拷贝数/ml)。使用抗人鼻病毒的鼻病毒3c蛋白酶抑制剂芦平曲韦作为阳性对照。正如所观察到的,芦平曲韦的施用有效减少了3个对数的hrv脱落。出人意料地,在感染时施用血浆来源的免疫球蛋白将hrv脱落完全降低到用我们的检测方法无法检测到的水平。除igam以外的所有免疫球蛋白制剂均可显示出这种减少。然而,重要的是,igam仍可使hrv脱落减少至少4个对数。
[0256]
因此,血浆来源的免疫球蛋白能够防止hrv进入上皮因此防止随后的复制和扩散。
[0257]
复制时,hrv可导致细胞裂解。在上皮的情况下,我们评估了血浆来源的免疫球蛋白是否能够保护上皮细胞免受hrv诱导的组织损伤。为了对此进行评估,使用teer参数作为评估hrv感染后组织完整性的平均值(图11)。在稳态(无感染)下,用介质处理后(阴性对照)的teer值为约260ohm.cm2。在hrv感染并将介质施加到组织上(阳性对照)时,teer降低了近5倍,表明感染后组织完整性丧失。如图11所示,芦平曲韦通过预防hrv诱导的组织损伤具有积极作用。当与hrv一起给予时,所有血浆来源的制剂都能防止组织完整性的丧失。血浆来源的免疫球蛋白对hrv的免疫排斥证明足以保护肺组织免受pa侵袭以及pa诱导的细胞损伤。
[0258]
实施例7:血浆来源的免疫球蛋白减少人鼻病毒诱导的粘膜纤毛清除减少
[0259]
粘膜纤毛清除是支气管组织的关键功能。被俘获在粘液中的病原体从肺部排出并被咳痰,以防止病原体停滞在肺部组织上并复制。粘膜纤毛清除可能受不同机制的影响,其中之一是组织损伤。
[0260]
由于hrv感染与组织损伤有关,因此评估了hrv感染后48h血浆来源的免疫球蛋白对粘膜纤毛清除的作用(图12)。在稳定状态(无感染)下,用介质处理(阴性对照)后粘液纤毛清除率为~40mm/s。在hrv感染和将介质施加到组织上(阳性对照)后,粘膜纤毛清除率降低了2
‑
倍。如图12所示,芦平曲韦可通过防止hrv
‑
诱导的粘膜纤毛清除率降低而发挥积极作用。所有血浆来源的制剂均能够防止粘膜纤毛清除率降低,iga和igm得到的效果最佳,对它们未观察到粘膜纤毛清除丧失。
[0261]
实施例8:人血浆来源的免疫球蛋白制剂对人鼻病毒感染的影响的剂量依赖性
[0262]
接下来,研究了所观察到的效果是否剂量依赖。分别以4、20、100和500微克/孔添加免疫球蛋白制剂,并通过测量hrv基因组拷贝数来评估其对hrv扩展的影响。图13表明血浆来源的人免疫球蛋白制剂能够以剂量依赖性方式抑制hrv的扩展。
[0263]
如上所述,还研究了对teer的影响。免疫球蛋白制剂以4微克/孔和20微克/孔、100微克/孔使hrv
‑
诱导的teer降低。在500微克/孔时,完全可以避免这种下降。
[0264]
此外,使用与上述指定相同的剂量,评估了不同剂量的免疫球蛋白制剂对纤毛跳动频率和粘膜纤毛清除率的影响。此外,在测试所有免疫球蛋白制剂的情况下,观察到了对纤毛跳动频率和粘液纤毛清除率的剂量依赖性作用。
[0265]
血浆来源的免疫球蛋白制剂也可抑制感染后第2天hrv
‑
诱导的il
‑
8分泌;甚至在4微克/孔时,igam和sigam仍能得到完全抑制;igg和iga在4微克/孔可实现非常显著的降低,并且所有免疫球蛋白制剂在较高剂量下均可以实现完全抑制。hrv
‑
诱导的rantes产生也被
所用最低剂量的免疫球蛋白(4μg/ml)显著抑制,并在第2天被更高剂量的所有免疫球蛋白制剂完全抑制。
[0266]
总之,血浆来源的免疫球蛋白能够保护体外肺组织免受hrv感染及其相关的组织损伤。预防性地将血浆来源的免疫球蛋白局部施用于处于肺部感染风险中的受试者的肺中将给予他们对抗病毒或细菌来源的微生物的保护作用。
[0267]
实施例9:人血浆来源的免疫球蛋白制剂对流感病毒感染的影响
[0268]
使用mucilair
tm
培养物的鼻病毒感染相同的实验方案,应用流感株h1n1进行了本实验。以10微克/孔的奥司他韦用作阳性对照。结果表明,免疫球蛋白制剂均以剂量依赖的方式减少了流感的扩散,如图14所示。
[0269]
流感病毒对teer的破坏也减少了4微克/孔和20微克/孔的每种免疫球蛋白制剂,并以100μg/ml和500微克/孔完全防止。
[0270]
在感染后第4天观察到了由流感病毒
‑
诱导的纤毛跳动频率的降低。igg对纤毛跳动的频率显示出最佳的挽救效果,已经以4微克/孔的速度完全恢复。iga、igam和sigam制剂也能够挽救纤毛的跳动频率,尽管仅以20微克/孔和更高的浓度。ig制剂还能够恢复粘膜纤毛清除,减少流感
‑
诱导的il
‑
8分泌和流感
‑
诱导的rantes分泌。
[0271]
实施例10:使用雾化的血浆来源的免疫球蛋白预防患有慢性阻塞性肺病(copd)和/或非囊性纤维化支气管扩张(ncfb)的受试者中的呼吸道感染驱动的加重
[0272]
患有copd和/或ncfb的受试者会经历慢性呼吸道感染,这可能会加剧他们的疾病。这些感染的长期性正在驱动其组织的重塑,从而增加了疾病的严重程度。
[0273]
如以上实施例所示,局部施用的血浆来源的免疫球蛋白可防止细菌和病毒在体外粘附和侵袭人类初级呼吸道组织。这些微生物的免疫排斥可预防组织损伤,并间接预防促炎性细胞因子的释放以及粘膜纤毛清除的丧失。
[0274]
为了打断这些感染的长期性,用雾化血浆来源的免疫球蛋白将患有ncfb或轻度至重度copd、潜在地与ncfb相关的受试者每日治疗1次或次。使用主动式振动筛网雾化器雾化配制成50mg/ml至150mg/ml的溶液的血浆来源的免疫球蛋白。以每日为基础在早晨和/或晚间施用2
‑
10ml的血浆来源的免疫球蛋白制剂。
[0275]
减少感染驱动的恶化将减轻copd和ncfb受试者的局部炎症,并将延缓所述疾病的进展。
[0276]
应当理解,仅通过举例描述了本发明,并且可以在保留本发明范围和精神内同时进行改变。
[0277]
参考文献
[0278]
[1]vestbo et al.(2013)am j respir crit care med 187(4):347
‑
65.
[0279]
[2]flume et al.(2018)lancet 392(10150):880
‑
90.
[0280]
[3]chalmers et al.(2018)am j respir crit care med 197(11):1410
‑
20.
[0281]
[4]global strategy for the diagnosis,management,and prevention of chronic obstructive pulmonary disease,2018 report;global initiative for chronic obstructive lung disease(gold).
[0282]
[5]mohan a et al.(2010)respirology 15(3):536
‑
42.
[0283]
[6]molyneaux et al.(2013)am j respir crit care med 188(10):1224
‑
31.
[0284]
[7]hassett et al.(2014)j microbiol 52(3):21 1
‑
26.
[0285]
[8]miravitlles et al.(2017)respiratory research 18:198.
[0286]
[9]singanayagam et al.(2018)nature communications 9(1):2229.
[0287]
[10]british thoracic society:guideline for non
‑
cf bronchiectasis(2010)thorax vol.65,supp.1.
[0288]
[11]spirometry for health care providers(june 2010).published by the global initiative for chronic obstructive lung disease(gold).
[0289]
[12]published by the association for respiratory technology and physiology(www.artp.org.uk).
[0290]
[13]agarwal and cunningham
‑
rundles(2007)ann allergy asthma immunol.99(3):281
‑
3.
[0291]
[14]normansell(1982)crc critical reviews in clinical laboratory sciences 17(2):103
‑
66.
[0292]
[15]hill et al.(1998)thorax 53:463
‑
8.
[0293]
[16]stucki et al.(2008)biologicals 36(4):239
‑
47.
[0294]
[17]wo/2012/030664.
[0295]
[18]gennaro(2000)remington:the science and practice of pharmacy.20th edition,isbn:0683306472.
[0296]
[19]donaldson and wedzicha(2014)int j of copd 9:1 101
ꢀ‑
10.
[0297]
[20]chairatana and nolan(2016)crit.rev.biochem.mol.biol.113:1
‑
12.
[0298]
[21]mantis et al.(2011)mucosal immunol.4:603
‑
11.
[0299]
[22]corthesy(2013)autoimmun.rev.12:661
‑
5.
[0300]
[23]strugnell and wijburg(2011)nat.rev.microbiol.8:656
‑
67.
[0301]
[24]mathias et al.(2013)infect.immun.81:3027
‑
34.
[0302]
[25]levinson et al.(2015)infect.immun.83:1674
‑
83.
[0303]
[26]brandtzaeg(2009)scand.j.immunol.70:505
‑
15.
[0304]
[27]brandtzaeg(2003)vaccine 21:3382
‑
88.
[0305]
[28]corthesy(2003)curr.pharm.biotechnol.4:51
‑
67.
[0306]
[29]corthesy(2002)trends biotechnol.20:65
‑
71.
[0307]
[30]lucas et al.(2010)j allergy clin immunol.125(6):1354
‑
60.
[0308]
[31]essaidi
‑
laziosi et al.(2018)j.allergy clin immunol.141(6):2074
‑
2084
[0309]
[32]cramer et al.(2009)vox sang.96:219
‑
25.
[0310]
[33]phalipon et al.(2002)immunity 17:107
‑
15.
[0311]
[34]longet et al.(2013)j.biol.chem.288:4085
‑
94.
[0312]
[35]crottet and corthesy(1998)j.immunol.161:5445
‑
53.
[0313]
[36]roche et al.(2015)mucosal immunology 8(1):176
‑
85.
[0314]
[37]bioley et al.(2017)front immunol.8:1043.
[0315]
[38]longet et al.(2014)jbc 289(31):21617
‑
26.
[0316]
[39]azham et al.(2018)drug discov today s1359
‑
6446(18):30235
‑
6.
[0317]
[40]srinivasan et al.(2015)j lab autom 20(2):107
‑
26.
[0318]
[41]jacobs et al.(2013)clinical microbiology reviews 26(1):135
‑
62.
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1