水溶性含硅颗粒的制作方法
本发明涉及一种含有生物可利用形式的硅化合物的制剂及其制备方法和用途。
背景技术:
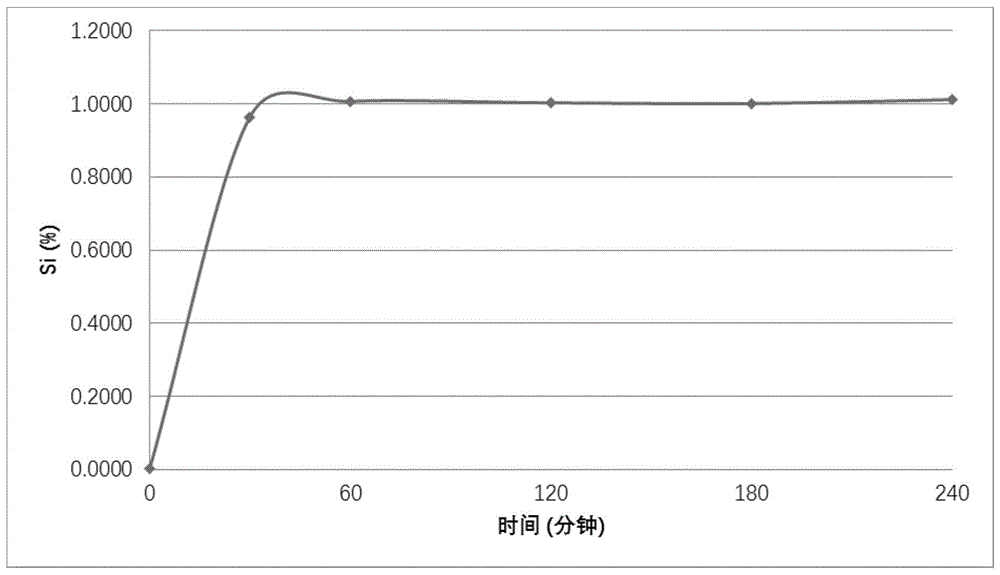
:矿物硅的生物可利用形式是原硅酸(osa),它在稀释浓度即<10-3m下是化学稳定的(iler1979)。在较高的浓度下,osa发生缩聚反应,从而导致低聚物和聚合物的形成。单体的这些缩聚形式不会被人类吸收(jugdaohsingh等人,2000年),但应该被胃酸转化为osa,以便在胃肠道中吸收。为了抑制所述缩聚,可以使用稳定剂。结果是生物可利用形式的硅酸,也称为生物可利用硅化合物。单烷基三硅醇(monoalkyltrisilanol)化合物如单甲基三硅醇(monomethyltrisilanol)也已被提议作为生物可利用硅化合物。本申请人已经发明了稳定的硅酸的液体和固体制剂,并已开发成可商购的产品。ep0743922中公开了液体制剂,ep1551763中公开了通过挤出滚圆技术制备的固体制剂。固体制剂为粒度在800-1200μm之间的珠粒形式,用于填充硬胶囊。这些产品已在各种临床试验中进行了测试,其中在骨骼、软骨、头发、指甲和皮肤上均发现了有益的结果。已经发现,在口服摄入稳定的硅酸之后,所摄取的硅化合物主要被发现是血液和尿液中的原硅酸。希望提供一种适用于食品、饲料和药物应用的生物可利用的硅酸固体制剂,其中剂量是预先确定的,能够很容易地用液体或饮品溶解成易于饮用的低粘度制剂。当患者正在旅行时,这样的制剂将有助于患者的依从性,便于其使用。固体制剂还可以与其他营养成分、香精和/或甜味剂共混,而不会出现分离的风险,并且还可以替代采用挤出滚圆技术制成的珠粒。技术实现要素:第一个目的是提供这种包含生物可利用硅化合物的改进的固体制剂。因此,本发明的第一个目的是提供一种生物可利用硅化合物的改进的固体制剂的制造方法。本发明的另一个目的是提供一种能够溶解在液体中的剂型,其中有效剂量是预先确定的。本发明的又一个目的是提供作为食品或饲料补充剂的用途。本发明的另一个目的是提供用作药物的制剂。第一个目的是以水溶性含硅颗粒实现的,该颗粒包含:(1)式yxsi(oh)4-x的硅化合物或其低聚物,其中y为可选取代的(c1-c4)-烷基、(c2-c5)-烯基、(c1-c4)-烷氧基、氨基,其中x为0-2;以及(2)冷水可溶性淀粉材料。第二个目的是以提供本发明的水溶性含硅颗粒的方法实现的,该方法包括以下步骤:-提供式yxsi(oh)4-x的硅化合物或其低聚物的液体制剂,其中y为可选取代的(c1-c4)烷基、(c2-c5)-烯基、(c1-c4)-烷氧基、氨基,其中x为0-2,优选x=0;-提供冷水可溶性淀粉材料;以及-将液体制剂与冷水可溶性淀粉材料混合,使硅化合物吸附在淀粉材料上,形成含硅颗粒。第一个目的也以通过本发明的方法可获得的颗粒得以实现。其他目的通过以下形式实现:盖仑组合物或营养组合物,例如,包含本发明颗粒的剂型或包装;盖仑组合物或营养组合物作为食品补充剂或饲料补充剂的用途;以及用于预防、抑制和/或治疗骨质流失和软骨退化相关疾病、头发指甲质量下降、脱发和皮肤老化疾病的颗粒。此外,在预防、抑制和/或治疗骨质流失和软骨退化相关疾病、头发指甲质量下降、脱发和皮肤老化疾病的方法中实现了进一步的目的,包括使用本发明的水溶性含硅颗粒,和/或包含所述颗粒的任何剂型或包装。在一个优选的实施方式中,在向顾客或患者口服给药之前,将颗粒或与其一起的固体剂型溶解或分散到饮品中。本发明的发明人已经发现,可以通过将硅化合物的液体制剂与冷水可溶性淀粉材料混合来制备含有硅化合物(例如原硅酸或其低聚物)的水溶性颗粒。这是一种实用的方法,它避免了对进入造粒工艺的固体部分使用单独的粘结剂溶液。除此之外,颗粒是与其他营养素和/或固体食品结合的合适形式。此外,所得颗粒被证明是非常有利的,因为顾客或患者可以在使用前将颗粒溶解到饮品中。在此,硅化合物的味道受到饮品味道的抑制。并且令发明人惊讶的是,颗粒中的硅酸不会进一步聚合成不能再被胃肠道吸收的形式。术语“冷水可溶性淀粉”在淀粉领域本身是已知的,涉及这样的淀粉材料,即,当在环境温度下被加入水中时,表现出颗粒结构完全破坏以及形成胶体分散体或甚至溶液或透明溶液。改性处理的非限制性例子有:酯化,可能与成盐相结合;醇-碱处理,例如m.j.jivanetal,j.foodsciencetechnology(march2014),51(3),601-605中所公开的;在高温高压下将淀粉与含水醇混合;使用氢氧化钠和尿素的混合物作为水解剂的淀粉水解;糊精化。合适地,改性淀粉材料在室温(25℃)下具有至少50wt%,更优选至少60wt%,或甚至至少70wt%的溶解度百分比。溶解度百分比是基于通过使用旋转振荡器在室温下以1000rpm混合45分钟而产生的改性淀粉的1wt%水性悬浮液测量的。使用离心处理(1200g速率,15分钟)将上清液与悬浮液分离,随后将上清液干燥(6小时,105℃)。溶解度百分比计算为上清液中固体质量与样品质量的比值乘以100%。优选的载体材料包括一种或多种化学改性淀粉材料,例如糊精、酸处理淀粉、碱改性淀粉、漂白淀粉、氧化淀粉、酶处理淀粉。一类优选的改性淀粉材料为酯化淀粉,例如,单淀粉磷酸酯,二淀粉甘油酯,三偏磷酸钠酯化的二淀粉磷酸酯,磷酸化二淀粉磷酸酯,乙酰化二淀粉磷酸酯,醋酸酐酯化的淀粉醋酸酯,醋酸乙烯酯化的淀粉醋酸酯,乙酰化己二酸双淀粉酯,乙酰化二淀粉甘油酯,辛烯基琥珀酸淀粉钠和/或其组合。羟丙基淀粉、羟丙基二淀粉磷酸酯、羟丙基二淀粉甘油酯也可以是合适的。改性淀和酯化的淀粉可以进一步以盐的形式使用,例如钠盐。更优选地,使用第一改性淀粉材料和第二改性淀粉材料的组合,其中例如第一改性淀粉材料具有比第二淀粉材料更高的分子量。由此获得了良好的实验结果。最合适地,两种改性淀粉材料都是所谓的冷水可溶性淀粉。实验发现,可以在形成颗粒(其至少80wt%、优选至少90wt%具有100-600μm的尺寸)期间,加入第二淀粉,特别是减少小于100μm的颗粒的量。优选组合是酯化淀粉和糊精或麦芽糖糊精的组合。酯化淀粉更优选为盐。最优选的组合是辛烯基琥珀酸淀粉钠和糊精的组合。认为优选的是,第一改性淀粉的质量比为50%-75%,第二改性淀粉的质量比为25wt%-50wt%。更优选地,第一改性淀粉与第二改性淀粉的相互重量比在1.5和2.5之间,例如1.8-2.2。淀粉材料可以具有任何期望来源,包括例如小麦淀粉、玉蜀黍淀粉、玉米淀粉、马铃薯淀粉、木薯淀粉、树薯淀粉。在使用第一改性淀粉和第二改性淀粉的情况下,不需要两者都源自相同的淀粉来源。优选地,硅化合物与抑制硅化合物聚合的稳定剂组合使用。该抑制尤其防止形成水不溶性且不再可水解的硅聚合物。这种硅聚合物不是生物可利用的,即其消耗不允许身体吸收准备被吸收的形式的硅,特别是硅酸单体原硅酸、其低聚物和可能的某些变体,例如硅醇和硅酸盐。可通过使用以下物质来获得稳定化:氨基酸,其他有机酸如水杨酸,山梨糖醇酸,抗坏血酸,乳酸和己酸,肽,肉碱,酚类或多酚类化合物如香兰素(4-羟基-3-甲氧基苯甲醛),季铵化合物,例如甜菜碱和胆碱及其衍生物。胆碱化合物是优选的,例如选自氯化胆碱、酒石酸氢胆碱、氢氧化胆碱、柠檬酸二氢胆碱、2-4-二氯苯氧基乙酸胆碱(2,4-d胆碱盐)、乙酸胆碱、碳酸胆碱、柠檬酸胆碱、酒石酸胆碱、乳酸胆碱、二丁基磷酸胆碱;o,o'-二乙基二硫代磷酸胆碱、磷酸二氢胆碱;磷酸胆碱。已发现使用氯化胆碱具有良好的结果。当稳定剂为季铵化合物如氯化胆碱时,液体制剂的特点是味道不好、气味难闻,可谓鱼腥味和苦味,对产品的依从性具有负面影响。使用载体如微晶纤维素来获得固体丸状制剂或液体填充的多糖胶囊克服了这个问题。然而,这两种固体剂量制剂都不是水溶性的。使用本发明的固体制剂克服了该缺点。在最优选的实施方式中,硅酸化合物是称为原硅酸的硅酸单体和/或其低聚物。这对应于式(i)中的值x=0。原硅酸的生物利用度已在多项科学研究中得到直接证明,这也得到了欧洲食品安全局(efsa)的认可。此外,与单甲基三硅醇(monomethyltrisilanol)相比,它是一种天然成分,单甲基三硅醇并不存在于自然界,而是一种人造合成化合物。优选地,在本发明中,硅酸基本上包含原硅酸的低聚物和/或单体。例如,低聚物是每分子包含少于1000个单体、优选少于100个单体的低聚物。更优选地,低聚物是在本文中硅原子的至少80%并且优选至少90%经由硅-氧-硅桥键合至至多3个其他硅原子的低聚物。在本文中术语“基本上”合适地是指至少95wt%,优选至少98wt%,更优选至少99wt%。仅聚合到在胃肠道中水解成单体、二聚体和三聚体是可行的程度的硅酸制剂被称为生物可利用硅。这种制剂的硅酸能够被人体吸收。在替代实施方式中,使用三硅醇化合物例如单甲基三硅醇作为硅化合物。这对应于式i中的x=1的选项。三硅醇化合物可以进一步用于根据式(i)的硅化合物的共混物中,其中x=0-2,优选地,x=0,1。一个优选的侧基y为c1-c4烷基,例如甲基。作为进一步优选,固体制剂为微粒,其中至少80wt%的粒子具有100-800μm范围内的尺寸,如通过筛分分析测量的。优选例的筛分分析表明可以达到这样的分布,即90%的颗粒小于600μm。可选地,可以应用筛分来选择具有特定窄粒度分布的粒子部分,或去除尺寸>600μm的粒子。更优选地,粒度分布为使得具有小于100μm的粒子的部分占粒子的至多15wt%,更优选地占粒子的至多10wt%或甚至粒子的至多5wt%。在另一个实施方式中,干燥颗粒的硅浓度在0.002wt%至2.0wt%的范围内。优选地,硅浓度为至少0.01wt%,更优选至少0.1wt%,以限制颗粒体积,以达到临床研究已知的日剂量。最优选地,硅浓度高于0.5%w/w。后者可以通过将硅化合物与稳定剂例如胆碱化合物组合来实现。在一个有利的实施方式中,颗粒中的至少0.5%w/w的高硅浓度是通过使用原硅酸和/或其低聚物作为硅化合物来实现的。在优选实施方式中,所产生的颗粒在它们形成之后被干燥到预定含水率。该含水率例如为至多5wt%,但是也可以替代地选择至多4wt%或至多3wt%的水分水平。根据一个重要的实施方式,该颗粒为流化颗粒。更具体地,该颗粒可通过包括以下步骤的方法获得:(1)提供硅化合物的液体制剂;(2)将包含淀粉材料的粒子载体引入流化床造粒机;以及(3)在流化床造粒机的运行过程中将所述液体制剂喷入其中,其中载体粒子与作为粘结剂的液体制剂附聚成颗粒。流化床造粒工艺通过载体材料确保了液体硅制剂的均匀分布。此外,已发现粒度分布良好,流化工艺产生具有相对低密度和孔隙率的颗粒,这被认为有利于溶解(包括胶体溶液的产生,其形式上为稀释的悬浮液)。该实施方式与以下方式组合是特别重要的:使用原硅酸和/或低聚物作为硅化合物,存在用于硅化合物的稳定剂,更特别地,胆碱化合物作为稳定剂。事实证明,对于这种特定的硅化合物及其稳定剂,利用其他湿法造粒方法制造具有均匀颗粒尺寸的颗粒更加困难。在优选实施方式中,本发明的颗粒的密度范围为0.25-0.60g/cm3,更优选为0.30-0.55g/mol,例如为0.33-0.36g/cm3或0.40-0.53g/mol。该密度明显低于通过挤出滚圆获得的密度,因为挤出滚圆通常导致密度高于0.75g/cm3。在优选实施方式中,干燥步骤发生在产生颗粒的流化床造粒机中。喷射、造粒和干燥这3个不同的步骤可以通过流化床造粒进行,在一个实施方式中,在单个造粒机单元中进行。这种流化床造粒单元本身是已知的,例如来自glatt,具有用于不同工艺步骤的多种配件。流化床造粒单元通常包括可调节位置和喷射速率的喷嘴。优选地,使用所谓的顶部喷嘴。合适的喷射速率在500-2000g/min的范围内。在另一个实施方式中,所获得的颗粒可以设有包衣,优选通过流化床造粒施加包衣。如果需要,这种包衣可以在单个单元中以相同的流化床造粒工艺施加。包衣可用于改变风味或香气,防止氧化,改变视觉外观或用于肠溶衣。包衣的例子有薄膜包衣、肠溶衣、迟释包衣、热熔包衣。在又一个实施方式中,用载气(优选用空气)进行流化床造粒,载气加热至室温以上。载气的优选温度为至少50℃至高达120℃,优选在70-100℃的范围内。加热的载气进一步使得材料干燥。在优选实施方式中,将25-40wt%稳定的硅酸喷在60-75wt%载体材料上,例如改性淀粉,例如酯化淀粉。可以组合几种类型的改性淀粉来改变所得颗粒的粒度分布。液体稳定的硅酸制剂与载体材料之间的比例优选为1:2。在又一个实施方式中,将颗粒添加并混合在饮品和液体食品中。因此,在一个实施方式中,将本发明的颗粒与营养素、植物基提取物、蛋白质和多种生物活性分子中的至少一种共混,然后进行包装。这种共混物也被称为“超级食品”。优选地,使用具有这样粒度分布的颗粒,即,使得至少90wt%,优选至少95wt%或甚至100%的粒子具有至多600μm的直径。这种特定的粒度分布使得能够获得完美的共混。不存在大粒子(>600μm)使共混组分的分离风险降到最低。顾客可以在食用前通过将共混物和/或颗粒与水、乳制品(例如牛奶的液体和例如酸奶的半液体)、果汁、蛋白质饮料或其他饮品混合来制备营养组合物。或者,可以将颗粒包装在小袋或条状包装或其他类型的单剂量包装中,将内容物与饮品和/或(半)液体食品混合并立即食用。单剂量包装方便顾客在旅行时随身携带产品。在另一个应用中,颗粒用作制造诸如片剂、咀嚼片、泡腾片和硬明胶或蔬菜胶囊的其他固体剂量盖仑剂型的原材料。在另一个实施方式中,任何这种剂型或包装可包括另外的常规添加剂和营养素,例如甜味剂;香精;赋形剂如抗结剂;微量元素,例如镁、硼、钙、硒、锌中的至少一种;维生素,例如维生素c、维生素d、维生素k中的至少一种。为完整起见,可以看到任何上述实施方式都被认为与根据本发明的任何方面相关。附图说明参考实施例和附图,将进一步阐明本发明的这些方面和其他方面,其中:图1a示出了通过gfaas(元素硅)测量的溶解介质的硅浓度。使用500ml溶解介质,在37℃和1000rpm混合速率下,在溶解装置中培养500mg稳定的硅酸颗粒(loti-160713)。240分钟后的硅浓度为1.01%(gfaas)w/v;图1b示出了通过钼蓝比色法(专用于单体硅酸)测量的溶解介质的硅浓度。使用500ml溶解介质,在37℃和1000rpm混合速率下,在溶解装置中培养500mg稳定的硅酸颗粒(loti-160713)。240分钟后的硅浓度为0.95%(比色法)w/v。具体实施方式在所有实施例中,除非另有说明,百分比是指重量百分比。实施例1用无水盐酸处理氯化胆碱。将四氯化硅(iv)添加到形成的胆碱溶液中(sicl4与氯化胆碱之比为1摩尔:1至5摩尔)。通过在-10℃至-30℃的温度范围内冷却的同时添加水(冰/冰水)来水解所得溶液。通过添加氢氧化钠并保持温度低于0℃来中和溶液。最终ph在1-1.5之间。用商购自stratos的ph分析仪(型号msa405,knick)来测量ph,该ph分析仪配备有具有ag/agcl2参比体系的memosensph电极和液态kcl电解质。用活性炭纯化后,通过与活性炭一起过滤来除去沉淀物。通过在真空下蒸馏来降低水浓度,直到获得含有按体积计2.0%-4%的硅、按重量计60%-80%的氯化胆碱和按重量计15%-30%的水的制剂。通过过滤除去蒸馏过程中形成的沉淀。将65.67%辛烯基琥珀酸淀粉钠(emarustaa1,松谷化学工业株式会社,日本)和1%磷酸三钙的混合物添加到流涂机flo-120(freundbldg,日本)流化床系统中。流化床造粒工艺是通过以下步骤开始的:将进气温度设置为85℃,在产品达到50℃的温度时将33.33%液态胆碱稳定的硅酸喷射在改性淀粉上。喷射后,flo-120单元中的流化颗粒在50℃的产品温度下自动开始干燥,直到颗粒中的水含量低于3%。表1中给出了通过筛分分析测量的粒度分布的例子,说明有96%的粒子具有小于595μm(30目)的尺寸。密度介于0.408g/ml与0.525g/ml之间。如通过石墨炉原子吸收光谱法(gfaas)所测量,干燥的颗粒具有介于0.75%(w/w)与1.5%(w/w)之间的元素硅浓度。表1:仅含有辛烯基琥珀酸淀粉钠作为载体的胆碱稳定的硅酸颗粒的筛分分析。如通过石墨炉原子吸收光谱法(gfaas)所测量,干燥的颗粒具有介于0.75%(w/w)与1.5%(w/w)之间的元素硅浓度。令人惊讶的是,当利用gfaas或钼蓝比色法进行分析时,在500ml溶解介质中含有500mg颗粒的溶解介质的分析显示出相同的曲线(见图1)。后者仅对单体硅酸具有反应性。这表明造粒工艺不会导致稳定的硅酸的缩聚,稳定的硅酸在水性环境中从淀粉载体迅速释放。该颗粒表现出优异的稳定性,因为在40℃和75%相对湿度下在密封容器中培养6个月时,通过钼蓝比色法测量的硅浓度没有显著变化(见表2)。表2:在40℃和75rh下在密封容器中培养的胆碱稳定的硅酸颗粒的稳定性。实施例2使用以下配方,将根据实施例1制备的硅酸颗粒与甜味剂、盐和香精混合:该共混物具有优异的流动性,可轻松装入单剂量条状包装中(每条4克)。将填充的条状包装在40℃培养6个月,以测试调味颗粒的稳定性。如表3所示,发现具有优异的稳定性,稳定的硅酸与添加的化合物之间没有发生相互作用。表3:在40℃和75rh下在条状包装中培养的胆碱稳定的硅酸颗粒与甜味剂和香精的共混物的稳定性。实施例3用无水盐酸处理氯化胆碱。将四氯化硅(iv)添加到形成的胆碱溶液中(sicl4与氯化胆碱之比为1摩尔:1至5摩尔)。通过在-10℃至-30℃的温度范围内冷却的同时添加水(冰/冰水)来水解所得溶液。通过添加氢氧化钠并保持温度低于0℃来中和溶液。最终ph在1-1.5之间。用商购自stratos的ph分析仪(型号msa405,knick)来测量ph,该ph分析仪配备有具有ag/agcl2参比体系的memosensph电极和液态kcl电解质。用活性炭纯化后,通过与活性炭一起过滤来除去沉淀物。通过在真空下蒸馏来降低水浓度,直到获得含有按体积计2.0%-4%的硅、按重量计60%-80%的氯化胆碱和按重量计15%-30%的水的制剂。通过过滤除去蒸馏过程中形成的沉淀。改性淀粉即以capsulhs(ingredion)可商购获得的辛烯基琥珀酸淀粉、糊精(crystaltex626,ingredion)、及其组合在gpcg1.1型实验室规模的流化床设备(glatt)中用作液态胆碱稳定的硅酸(ch-osa)的载体。表4给出了配方。将干燥的淀粉和糊精在80-100℃的热进气流下流化,导致最高产品温度在60-70℃范围内。用顶部喷嘴将胆碱稳定的硅酸喷射在载体上,导致形成颗粒,将颗粒在同一设备中干燥,直至获得小于3.5%的干燥失重。根据该配方,干燥颗粒的密度介于330g/l与360g/l之间。筛分分析表明,有大于90%的粒子小于600μm(见表5)。使用糊精导致了更少的粉尘(即低于100μm的粒子),这改进了所得颗粒的可加工性和流动性。表4:在gpcg1.1型流化床设备(glatt)中制备的制剂配方。粒度a47-01a47-03a47-04%>800μm002%600-800μm002%400-600μm406%200-400μm141856%100-200μm487034<100μm34120表5:在gpcg1.1型流化床设备(glatt)中制备的制剂的筛分分析。实施例4在较大的中试规模gpcg15系统(glatt)中,使用8kgcapsulhs和4kgcrystaltex626的混合物重复实施例3,该混合物用作6kg胆碱稳定的硅酸的载体,但使用仅65℃的进气流,这导致最高产品温度为53℃。同样,在这些条件下,中试规模的流化床工艺产生了颗粒,其中大于90%的粒子具有小于600μm的尺寸(见表6)。由于在500-2000g/mol的范围内,实验a47-06中使用了比实验a47-05更高的喷射速率,因此颗粒变得更粗大并且消除了非常细的粒子(灰尘,<100μm)。粒度a47-05a47-06%>800μm13%600-800μm14%400-600μm516%200-400μm4849%100-200μm4228<100μm30表6:在gpcg15型中试规模的流化床设备(glatt)中制备的制剂的筛分分析。对于实验室规模和中试规模,所有制剂的硅浓度都在0.99%(w/w)与1.05%(w/w)之间。制剂的水含量在2%(w/w)与3%(w/w)之间。实施例5在工业水平上重复实施例4:在配备有顶部喷嘴的gpcg300流化床系统中,140.8kgcapsulhs和70.4kgcrystaltex626用作105.6kg胆碱稳定的硅酸的载体。使用65℃的进气温度将固体材料加热至53℃,然后以540-1800g/min的喷射速率和2bar压力将胆碱稳定的硅酸喷射到流化床中。为了干燥,使用了相似的进气温度,导致最终颗粒的水分含量为3%-4%。所得颗粒的堆积密度为0.356g/cm3,93%的粒子具有低于600μm的尺寸,94%的粒子具有至少125μm的尺寸。粒度分布如表7所示,表明工业规模的实验中得到的粒度分布与实验室规模的实验没有显著差异。该过程的总产量为293kg颗粒。随机抽取样品以检查均匀性。总结在表8中的结果表明形成了均匀的产品。这证实了工业造粒工艺不会导致稳定硅酸的缩聚,因为gfaas和钼分析显示硅浓度没有差异。粒度lot18g26%>1180μm0.61%600-1180μm6.3%400-600μm18.1%200-400μm62.3%125-200μm7.1<125μm5.5表7:使用gpcg300型流化床设备(glatt)以工业级制成的颗粒的筛分分析。表8:在gpcg300型流化床设备(glatt)中制备的颗粒的随机选择样品的化学分析。实施例6使用以下配方将实施例1中获得的颗粒压制成片剂:-200mg胆碱稳定的硅酸颗粒-90.01mg微晶纤维素-6mg硬脂酸钙-3.99mg磷酸三钙-3mg虫胶发现当该片剂包装在铝/铝箔中并在40℃和75%相对湿度下培养3个月时是稳定的,因为gfaas和钼分析显示硅浓度没有差异,随时间推移,崩解时间仍保持相似(表9)。表9:包装在密封铝/铝袋中并在40℃和75%相对湿度下培养的片剂的稳定性。实施例7使用以下配方将实施例1中获得的颗粒压制成咀嚼片:-500mg胆碱稳定的硅酸颗粒-1.25mg微晶纤维素-650mgadvantose-10mg三氯蔗糖-300mg麦芽糖糊精-100mg硬脂酸镁-30mg姜柠檬香精-30mg香蕉香精-45mg抗坏血酸发现当该片剂包装在铝/铝箔中并在40℃和75%相对湿度下培养3个月时是稳定的,因为gfaas和钼分析显示硅浓度没有差异,随时间推移也保持不变(表10)。表10:包装在密封铝/铝袋中并在40℃和75%相对湿度下培养的咀嚼片的稳定性。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1