一种提高射干药材苷元含量的方法及射干提取物的制备工艺与流程
本发明属于中草药技术领域,特别提供一种富含黄酮苷元的高效无毒的射干饮片的制备工艺。
背景技术:
射干药材及饮片收载于2015年版中国药典一部,具有清热解毒,消痰,利咽的功效。多用于热毒痰火郁结,咽喉肿痛,痰涎壅盛,咳嗽气喘。黄酮类化合物是射干的主要药效成分,具有广泛的生物活性。我们前期对射干进行了基于本草考证传统功效的药效学实验,明确了射干黄酮具有抗炎、止咳、解热、抗病毒、镇静等功效。目前,已报道的射干黄酮类成分有50余种,以黄酮苷及黄酮苷元的形式存在。
研究发现射干中黄酮苷元类成分的生物活性显著优于射干中苷类成分,这是因为黄酮类化合物在体内代谢时,仅有苷元型黄酮可以直接被吸收入血,而大部分糖苷型黄酮不能通过小肠壁进入血液中,黄酮苷被肠道菌群通过杂环裂解方式降解和代谢,生成苷元才能重新吸收进入血液。因此,黄酮糖苷在动物体内的生物利用率远远低于苷元型黄酮。我们前期对射干提取物的肠道菌群代谢试验进行了研究,明确了射干的黄酮苷及对应的苷元组分在人体内的转化关系,研究也提示了射干黄酮苷类成分在体内转化为相应苷元而发挥药理作用。射干药材中的黄酮苷类成分含量较高,相应的苷元含量较低。因此,改善射干黄酮的构型,增加入血浓度,提高吸收率是提高射干黄酮生物利用度的重要途径。目前,主要有两种方法能改变黄酮苷配糖体的构型,即化学转化法和生物转化法。化学法水解黄酮糖苷是通过对黄酮结构的醚化、酯化、酰基化等来改变黄酮苷的特性,但是反应过程会屏蔽黄酮化合物的主要功能团酚羟基,影响药效,且污染环境;现有技术(cn106620061a)公开了一种富含黄酮苷元的射干饮片及其提取物的制备工艺,采用生物转化法的酶技术提高射干苷元含量,但是生物转化法常用的酶技术,需要考察酶残留对中药材和制剂中有效成分降解、络合等反应,技术也存在一定的局限性。我们再次深入挖掘射干的古医籍,从射干药材古代炮制方法中寻求灵感,发现米泔水中及药材自身存在的酶类成分可能会对射干黄酮的存在形式产生影响。
米泔水,也称“米泔”,是指大米或糯米淘洗时第二次滤出的浑浊液,其中含有少量淀粉和维生素。《本草纲目》中记载:“其有清热,止烦渴、利小便、凉血、解毒等功效。”明代缪希雍在《炮炙大法》中写道:“米泔水,即淘米汁也。”《本草分经》中记载:“浸泡时间有长、短之分,从一天到七天不等”。米泔水制,是传统中药炮炙中的一种,在古代应用较为普遍,主要用来除去药物中多余的油脂,减弱药物的辛燥气味和滑肠作用。
《雷公炮炙论》记载“射干,凡使,先以米泔浸一宿,漉出,然后用堇竹叶煮,从午至亥,漉出,日干用之。”本发明思路来自于其中的米泔水炮制射干,但炮制目的不尽相同。传统米泔水制射干,是将射干药材在米泔水常温下浸一宿,晾干即可,炮制是为了降低射干药材的燥性和毒副作用。古法炮制后,射干异黄酮成分变化不大,苷元增加较少。但本发明首次利用转化条件,即利用米泔水酶特性与射干药材自身存在的酶特性,启动酶反应,通过控制关键的浸制温度及干燥温度,使射干药材中苷类转化成苷元成分,并控制在科学合理的范围内。射干味苦、性寒、微毒,研究中还发现未经米泔水处理的射干会使大鼠肝脏中的ast及alt转移酶显著升高,有一定的肝毒性,而米泔水制射干未见肝脏转氨酶升高。
因此,本发明拟研制一种提高射干药材苷元含量的制备方法,可以期待得到疗效高、无毒性的高质量射干药材。
技术实现要素:
针对现有技术的不足,本发明的目的在于提供一种提高射干药材苷元含量的处理方法及其提取物的制备工艺,该工艺可以显著提高射干饮片中的黄酮苷元的含量,并降低原药材的毒性。以此为原料,进行提取、分离、纯化并制成制剂,为药材的临床应用提供保证。
本发明思路来自于古医籍米泔水炮制射干,但炮制目的不尽相同。米泔水浸制药材后,射干黄酮苷元类成分提高,米中含有的酶类主要是淀粉酶,β-葡萄糖苷酶、纤维素酶及半纤维素酶等组成的混合酶。其中纤维素酶和半纤维素酶等可以水解或降解植物药材的细胞壁的组成成分、破坏细胞壁结构,降低其致密性,使得β-葡萄糖苷酶更易于与射干黄酮苷类成分相作用,多种酶相互作用达到提高射干药材苷元含量的目的。
本发明首次利用转化条件,即米泔中酶的特性,启动酶反应,并联合射干药材自身固有酶,通过控制关键的浸制温度及干燥温度,使射干药材中苷类转化成苷元成分,从而调节射干异黄酮苷元与苷的含量比,使其控制在科学合理的范围内。
为实现上述目的,本发明的技术方案具体如下:
一种提高射干药材苷元含量的方法,该方法通过在射干中加入米泔水浸制,浸制温度为40-60℃,保温6-72小时,滤过除去米泔水,射干药材于60-90℃烘干至含水量在10%以下,得到富含苷元的射干药材。
所述射干为射干原药材、原药材切制的饮片或破碎后的药材粉末,优选射干药材或饮片。
所述米泔水为淘米水或通过米粉冲水得到;其中,米为糯米、粳米、籼米或粟米。
所述米泔水通过米粉冲水制备时米与水的比例为0.5-20%。
所述米泔水为淘米水时米与水的比例为1:5-30。
所述射干与米泔水的体积比为1:2-10。
作为优选,射干为射干药材或饮片,在40-60℃的条件下,按每1kg加入2-10倍体积的浓度为1%-20%的米泔水,保温6-72小时,取出,沥干水分,在60-90℃干燥,筛去碎屑,制成高效低毒射干饮片。
本发明提供了一种射干提取物的制备方法,上述米泔水处理后富含苷元的射干药材提取液上于苯乙烯类大孔吸附树脂柱上,采用水除杂,除杂体积1-4bv,再用4~10倍量柱体积含醇量为20~40%的溶液洗脱除杂,续用4~10倍柱体积、体积分数为60~80%的乙醇洗脱,收集乙醇洗脱液,回收溶剂,浓缩干燥,即得射干提取物。已确定的黄酮苷元及它们的重量比为:(鸢尾黄素+野鸢尾黄素):(次野鸢尾黄素+白射干素)=(2-12):1。
本发明制备射干提取物所需原料为射干米泔水制备后的药材、或米泔水制备后破碎的药材粉末。
本发明制备得到的射干提取物应用于口服的制剂,所述口服的制剂为片剂、胶囊剂、颗粒剂或滴丸以及临床上适宜的其它剂型。所述制剂含有的添加剂,包括但不限于填充剂、润湿剂、粘合剂、崩解剂、润滑剂、ph调节剂、调味剂或着色剂。
所述药用辅料所占的总量百分比分别为:填充剂0-90%、润湿剂0-30%、粘合剂0-50%、崩解剂0-50%,而润滑剂、ph调节剂、调味剂、着色剂可根据剂型或工艺灵活添加。
所述填充剂,包括葡萄糖、乳糖、甘露醇、白糖、糊精、玉米淀粉、马铃薯淀粉、碳酸钙、磷酸钙、硫酸钙及结晶纤维素等。
所述崩解剂,包括淀粉、明胶粉、琼脂、碳酸钙、碳酸氢钠、海藻酸钠、结晶纤维素、羧甲基纤维素钠及羧甲基纤维素钙等。
所述粘结剂,包括淀粉、糖浆、明胶、黄芪胶、羟丙基纤维素、甲基纤维素、乙基纤维素、羧甲基纤维素、聚乙烯醇、聚乙烯醚及聚乙烯吡咯烷酮等。
所述润滑剂,包括硬脂酸镁、滑石、氢化植物油及聚乙二醇等。
所述着色剂可以使用允许添加到药物中的任意着色剂。
可以根据需要添加ph调节剂、缓冲剂、稳定化剂及增溶剂等。
此外,药品组合物可以制备成多种剂型,如口服制剂或非口服制剂。
与现有技术相比,本发明具有如下优点和效果:
1.本发明利用米泔水中存在的酶和射干药材自体酶,将射干黄酮苷通过酶转换为射干黄酮苷元,经过处理的射干药材及提取物中黄酮苷元含量显著高于普通射干药材,药效实验证明,米泔水处理后射干药材提取物有明显抗炎、止咳作用,效果优于普通射干饮片,且其肝毒性显著低于普通射干药材。
2.射干黄酮苷转化成黄酮苷元,相比常用生物转化法中的酶技术,避免了实验中需要考察酶残留对中药材和制剂中有效成分降解、络合等反应的技术局限性。
3.本发明干燥温度60-90的设定,有助于射干有效含量的增加。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
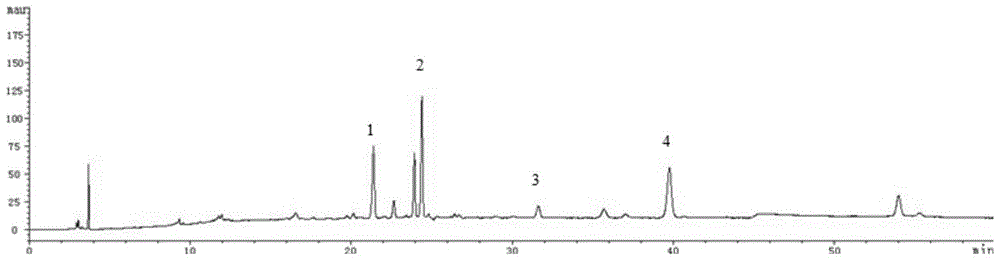
图1:生射干饮片hplc色谱图;
图2:古法炮制的射干饮片hplc色谱图;
图3:本发明制备的射干饮片hplc色谱图;
其中,1:鸢尾苷;2:野鸢尾苷;3:鸢尾黄素;4:野鸢尾黄素。
具体实施方式
为了更好的理解本发明的实质,下面结合具体实施例和附图对本发明进一步的阐述。
实施例1
一、射干药材制备工艺研究
1.仪器与材料
仪器:watersuplc(pdadetector),色谱柱(watersacquityuplcbehc181.7μm,2.1×50mm),phs-25cph计(上海唐仪仪器有限公司),kq-250db数控超声波清洗器(昆山市超声波仪器有限公司)。
试药:射干饮片(产地为湖北黄冈射干种植基地,购自湖北卫尔康现代中药有限公司,批号:20170619);籼米(辽宁省盘锦鹤乡佳缘米业有限公司,批号:20170203);粳米(辽宁省盘锦鹤乡佳缘米业有限公司,批号:20170205;江米(黑龙江省五常,批号:20170501);粟米(内蒙古阿鲁科尔沁旗先锋乡浩源米业有限公司,批号:20170406)。
2、实验方法
选择对总苷元增加率有极显著影响的浸制温度、浸制时间、米的种类、米粉水浓度四个因素,每个因素设定三个水平。同时考虑浸制温度与浸制时间、浸制温度与米种类、浸制时间与米种类的交互作用,因此用l18(37)正交表进行正交试验,确定其最佳工艺。米泔水用量为药材的4倍量。
表1射干转化研究正交试验因素水平表
射干饮片购自湖北卫尔康现代中药有限公司,经辽宁省中医药研究院尤献民研究员鉴定为鸢尾科植物射干belamcandachinensis(l.)dc.干燥根茎的加工品,筛选、除杂后,以四分法取样,平均分成24份,每份100g,供正交试验及验证试验使用。
随机抽取上述正交试验饮片1份置1000ml烧杯中,按正交试验安排表安排实验,实验完成之后取出,沥干水分,置于80℃的烘箱内烘干。
各试验号射干饮片,粉碎,取粉末各0.5g,精密称定,置100ml具塞三角烧瓶中,分别精密加入70%乙醇25ml,密塞,称定重量。超声(250w,50khz)提取60min,冷却,称重,用70%乙醇补足减失的重量,摇匀,滤过,用0.22um微孔滤膜过滤,供hplc分析。
表2正交实验安排表
正交试验直观分析结果:
从直观分析可知,最佳工艺为a2b1c1d3,即药材饮片加入4倍量的1%的大米米泔水,在40℃的条件下浸泡48小时。
正交试验方差分析结果:
由于d因素、a×c交互的离均差小于空白列,因此与空白列一起作为误差项。正交实验方差分析结果详见表3。
表3正交试验方差分析表
(f0.05(2,12)=3.89、f0.01(2,12)=6.93,f0.05(4,12)=3.26、f0.01(4,12)=5.41)
从方差分析表可以看出,a因素(浸制温度)、b因素(浸制时间)及a与b的交互对米泔水制备工艺具有极显著性意义;而c因素(米种类)及b与c的交互对制备工艺影响无显著性意义。
交互作用分析:
由于a与b的交互作用对制备工艺具有极显著性影响,因此分析a因素与b因素的最优搭配,从搭配结果可以看出,最优搭配为a2与b1,见表4。
表4因素a与因素b的交互搭配结果
综上所述,射干药材米泔水制备最佳工艺为:药材饮片加入4倍量的1%的大米米泔水,在40℃的条件下浸泡48小时。
3.上述最佳工艺与古法米泔水制射干有效成分对比
古法:取射干饮片,加入米泔水,室温放置12h,备用。
最佳工艺法:取射干饮片,按前述最佳工艺条件制备,备用。
结果:如图1、图2和图3所示,与生射干药材比较,古法制备后射干黄酮苷类成分略微降低,黄酮苷元类成分升高,但整体变化不大;而按照最佳制备工艺,控制米泔水浸制温度和时间后,所测黄酮苷类成分明显减少,黄酮苷元显著增加。上述结果表明,古法米泔水炮制射干并不能对射干黄酮的存在形式产生影响,起到增效的目的。而我们的发明创新性的利用米泔水中酶的性质,并保留了其降低药材燥性的优点,开发了米泔水解毒增效的用途。有效成分变化详细结果见表5。
表5射干饮片制备前后有效成分平均含量(n=10)
二、药理学研究
实验动物分组与方法:将大鼠适应性饲养一周后,按体重随机分为7组,每组10只。分别为空白组、模型组、阳性药组、射干药材高剂量组、射干药材低剂量组、最佳制备工艺射干高剂量组、最佳制备工艺射干低剂量组。
1.各组药物对琼脂肉芽肿亚急性炎症的影响实验
除空白组外,将各组大鼠用水合氯醛溶液进行麻醉,每只大鼠均沿背部中线注射2ml浓度为2%的琼脂溶液,次日起灌胃给药,连续给药14天,模型组及空白组均给等体积的蒸馏水。实验于末次给药30分钟后进行大鼠腹主动脉取血,收集于血浆分离采血管,并剪开肉芽部位皮肤,剥离肉芽肿琼脂块,称取肉芽湿重,计算大鼠肉芽肿抑制率。
实验结果显示,与模型组比较,射干低剂量组、最佳制备工艺高剂量组、最佳制备工艺低剂量组对大鼠肉芽肿均有显著抑制作用,平均抑制率分别为23.6%、21.3%、22.8%。
实验结果见下表6
表6大鼠肉芽肿统计结果表
注:与模型组比较,★p<0.05,有显著性差异
与射干高剂量组比,☆p<0.05,有显著性差异
由实验结果分析表可见,与模型组比较,阳性药组有显著抑制作用,平均抑制率为48.8%,本次实验模型复制成功;与模型组比较,射干低剂量组、最佳制备工艺高剂量组、最佳制备工艺低剂量组对大鼠肉芽肿均有显著抑制作用,平均抑制率分别为23.6%、21.3%、22.8%。
2.各组药物对琼脂肉芽肿亚急性炎症大鼠肝肾功能指标的影响实验
取上述大鼠血以3000r/min离心10分钟,吸取血浆,分装到ep管中进行肝肾功能指标测定。
结果显示,测定并记录肉芽肿亚急性炎症模型大鼠血浆ast、alt、ggt、tbil、bun、gre,实验结果采用x±s形式表示,组间比较采用成组t检验,数据分析结果如下所示
表7ast、alt实验结果表
注:★表示与模型组比较,有显著性差异,p<0.05
☆表示与射干药材组比较,有显著性差异,p<0.05
表8ggt、tbil实验结果表
注:★表示与模型组比较,有显著性差异,p<0.05
☆表示与射干药材组比较,有显著性差异,p<0.05
实验结果提示:与空白组比较,模型组各项测定指标值均无显著性差异,表明琼脂致大鼠肉芽肿引起的炎症不会引起肝肾损伤。ast、ast测定结果显示:射干长期给药可使大鼠血浆ast、alt含量显著增加,表明长期服用生品射干药材对大鼠肝脏存在损伤,而最佳制备工艺组射干给药后,大鼠血浆中ast、alt含量均未显著增加,表明米泔水处理射干后无肝脏损伤的作用。但各组大鼠血浆中ggt、ibil均无显著性差异。
表9bun、cre实验结果表
注:★表示与模型组比较,有显著性差异,p<0.05
☆表示与射干药材组比较,有显著性差异,p<0.05
实验结果显示,射干药材给药组及最佳制备工艺组均未使大鼠体内bun、cre含量显著上升,表明长期服用两种药物均未对大鼠肾脏造成损伤。
实验结论
本发明利用米泔水可显著促进射干饮片中黄酮苷类成分转化为黄酮苷元,从而使产品和射干饮片相比,在动物急性炎症和亚急性炎症模型中产生显著差异,起到减毒增效的作用。
实施例2
射干提取物的制备工艺
1.树脂选择
(1)静态吸附
选择了d101、nka-9、x-5、ab-8、s-8、hpd450、hpd400、hpd300、hp20、hpd500、hpd600的苯乙烯类大孔吸附树脂,进行静态吸附考查。
大孔树脂预处理:取树脂40g,置于具塞三角烧瓶,分别加95%乙醇60ml浸泡12h以上,装填于内径为3cm的树脂柱中,用95%乙醇洗至流出液无色、溶液澄清,再用蒸馏水洗至无醇味,流出液澄清。
上样液制备:取米泔水处理后的射干饮片,按照提取工艺提取,回收乙醇至无醇味,加乙醇和蒸馏水调节,使含生药量为0.3g/ml,含醇量为30%。
静态吸附能力考察:精密称取已处理好的各种树脂,淋尽水,各称取35g,分别置于具塞三角烧瓶中,各加入上样溶液200ml,轻轻振摇1分钟,每隔30分钟振摇1分钟,持续6小时,室温放置24小时后,摇匀。同时测定吸附后溶液中各成分含量s1,吸附前溶液中各成分的含量s,静态吸附量q=(s-s1)v/w。
(2)静态解吸
取静态吸附后的树脂,分别淋尽上样液,用蒸馏水少量多次洗涤树脂至洗液无色,淋尽水后,精密加入95%乙醇50ml,轻轻振摇1分钟,每隔20分钟轻轻振摇10秒,持续2小时后,测定解吸液中各成分含量s2,静态解吸率d(%)=s2/q*100%,根据静态吸附率和解析率综合考虑,确定一种或几种树脂作为后续研究用。结果表明,静态吸附量结果ab8、hpd-450和nka-9较好,解吸能力适中。
(3)动态吸附
根据静态吸附、解吸结果,选择ab-8进行动态吸附量实验。取选择的大孔树脂装柱(柱内径3cm,装柱高度20cm,记录树脂重量),以0.3g/ml生药的上样液上样500ml,流速2ml/min,每0.5b为1份收集流出液,测定流出液中苷元含量,当流出液中可以检测到有效成分时,确定为动态最大上样量。结果:4bv开始可以检测出有效成分;
2.分离纯化
(1)称取米泔水处理后射干饮片1000g,粉碎,用6、4、4倍体积的70%乙醇回流提取2次,每次2h,合并滤液减压蒸馏回收乙醇,调节醇浓度至30%,静置12~24小时,离心除去少量不溶物,得到每1ml含0.2~0.5g药材的吸附液。
(2)将2bv的上述吸附液通过装有ab-8的大孔吸附树脂的树脂柱(柱内径10cm,柱长150cm,装有6000ml湿树脂),吸附速度为1.0bv/h;
(3)吸附完成后,用2bv的30%乙醇水溶液将树脂上吸附能力较弱的杂质洗脱下来速度为1.0bv/h;
(4)用5bv的80%乙醇水溶液作解吸剂,解吸速度为1.0bv/h,收集解吸液;
(5)将上述解吸液经减压蒸馏并回收乙醇,然后经浓缩、真空干燥,得到总苷元提取物28.32g。
(6)经hplc分析测定,提取物中总苷元含量为52.7%(w%),且通过molish检测为阴性,该提取物中不含苷。
实施例3
剂型的制备
1.颗粒剂的制备
1)射干提取物450g,糊精550g,混合均匀,用70%乙醇制粒,70℃干燥,整粒,即得。
2)射干提取物450g,糊精500g,混合均匀,用70%乙醇制粒,70℃干燥,整粒,即得。
3)射干提取物420g,糊精580g,混合均匀,用70%乙醇制粒,70℃干燥,整粒,即得。
2.胶囊剂的制备
1)射干提取物150g,淀粉150g,混合均匀,用70%乙醇制粒,70℃干燥,整粒,装胶囊,即得。
2)射干提取物150g,淀粉150g,混合均匀,用70%乙醇制粒,70℃干燥,整粒,装胶囊,即得。
3)射干提取物140g,淀粉160g,混合均匀,用70%乙醇制粒,70℃干燥,整粒,装胶囊,即得。
3.片剂的制备
1)射干提取物150g,微晶纤维素100g,交联聚维酮50g,混合均匀,用1%聚维酮的70%乙醇溶液制粒,70℃干燥,整粒,加羧甲基淀粉钠3g,硬脂酸镁1.5g,混匀,压片,即得。
2)射干提取物150g,微晶纤维素100g,交联聚维酮50g,混合均匀,用1%聚维酮的70%乙醇溶液制粒,70℃干燥,整粒,加羧甲基淀粉钠3g,硬脂酸镁1.5g,混匀,压片,即得。
3)射干提取物140g,微晶纤维素110g,交联聚维酮50g,混合均匀,用1%聚维酮的70%乙醇溶液制粒,70℃干燥,整粒,加羧甲基淀粉钠3g,硬脂酸镁1.5g,混匀,压片,即得。
4.滴丸剂的制备
1)取500g聚乙二醇6000,于水浴中加热熔融后,加入射干提取物150g,全部熔融后搅拌混匀,60目筛滤过,保持60℃滴入已经冷却至10℃以下的液体石蜡中,成丸,即得。
2)取500g聚乙二醇6000,于水浴中加热熔融后,加入射干射干提取物150g,全部熔融后搅拌混匀,60目筛滤过,保持60℃滴入已经冷却至10℃以下的液体石蜡中,成丸,即得。
3)取510g聚乙二醇6000,于水浴中加热熔融后,加入射干提取物140g,全部熔融后搅拌混匀,60目筛滤过,保持60℃滴入已经冷却至10℃以下的液体石蜡中,成丸,即得。
5.软胶囊剂的制备
1)取大豆油300g,大豆磷脂50g,蜂蜡50g,加热熔融,混合均匀,放冷,加入射干提取物150g,研匀,压制软胶囊,即得。
2)取大豆油300g,大豆磷脂50g,蜂蜡50g,加热熔融,混合均匀,放冷,加入射干提取物150g,研匀,压制软胶囊,即得。
3)取大豆油310g,大豆磷脂50g,蜂蜡50g,加热熔融,混合均匀,放冷,加入射干提取物140g,研匀,压制软胶囊,即得。
6.微丸剂的制备
1)取100g聚乙二醇6000、50g泊洛沙姆、100g丙烯酸树脂于水浴中加热熔融后,加入射干提取物150g,全部熔融后搅拌混匀,熔融挤出发制微丸。
2)取100g聚乙二醇6000、50g泊洛沙姆、100g丙烯酸树脂于水浴中加热熔融后,加入射干提取物150g,全部熔融后搅拌混匀,熔融挤出发制微丸。
3)取110g聚乙二醇6000、50g泊洛沙姆、100g丙烯酸树脂于水浴中加热熔融后,加入射干提取物140g,全部熔融后搅拌混匀,熔融挤出发制微丸。
- 还没有人留言评论。精彩留言会获得点赞!