一种高效穿过血脑屏障的寡聚核苷酸/原子精细纳米团簇复合物及其制备方法以及应用与流程
本发明属于纳米生物材料领域,具体涉及一种高效穿过血脑屏障的寡聚核苷酸/原子精细纳米团簇复合物及其制备方法以及应用。
背景技术:
血脑屏障(blood-brainbarrier,简称bbb)是治疗脑部疾病所面临的一道国际难题。因为它的存在,使100%的大分子药物及98%以上的小分子药物均无法穿过并到达脑组织,极大限制了药物对脑部疾病的疗效。因此,发明一种能有效穿透血脑屏障的生物材料或者药物载体一直以来备受期待。
血脑屏障主要由大脑毛细血管内皮细胞、星形胶质细胞粘性末端及周皮细胞紧密连接形成的特殊结构。在正常生理条件下,血脑屏障仅允许气体及相对分子质量小于600da的脂溶性小分子通过。外界物质穿越血脑屏障有两种途径,即自由扩散和受体介导的主动转运。自由扩散仅限于小分子量、非极性、亲脂性物质,而大多数药物分子穿越血脑屏障主要借助于脑内皮细胞上的受体转运系统。mirkin开发的球形核酸作为穿越血脑屏障的工具即可实现1%左右的血脑屏障穿越效率,同时其他高分子聚合物例如脂质体,plga小球等也可以实现1%左右的血脑屏障穿越效率。开发新型的纳米材料提升血脑屏障穿越效率对于脑部疾病的治疗和诊断监测有着重要的意义。因此,设计可穿越血脑屏障药物的关键是开发可以高效的进行细胞内化以及转运的材料,可以极高的效率进行血脑屏障的穿越,实现治疗成像等功能。
技术实现要素:
本发明的目的是提供一种高效穿过血脑屏障的寡聚核苷酸/原子精细纳米团簇复合物及其制备方法以及应用,从而解决现有技术中缺少高效的穿越血脑屏障材料的问题。
为了解决上述技术问题,本发明采用以下技术方案:
根据本发明的第一方面,提供一种高效穿过血脑屏障的寡聚核苷酸/原子精细纳米团簇复合物,所述寡聚核苷酸/原子精细纳米团簇复合物由寡聚核苷酸和疏水性原子精细纳米团簇组成,是一种具有亲水性寡聚核苷酸外壳,同时具有疏水性原子精细纳米团簇内核的类病毒颗粒,其中,所述寡聚核苷酸为通过腺嘌呤、鸟嘌呤、胞嘧啶、胸腺嘧啶中的至少一种按照任意组合排列而成的寡聚核苷酸单链,所述疏水性原子精细纳米团簇为具有原子精细结构的疏水性金属原子的团簇。
所述金属原子可选自:金、银、铜、铂中的任意一种或其任意组合。
所述寡聚核苷酸单链的长度为10~100个碱基。
所述疏水性原子精细纳米团簇中金属原子的数目为5~100个。
所述寡聚核苷酸/原子精细纳米团簇复合物具有聚集诱导发光性质及在近红外光区发射荧光信号的性质。
所述的寡聚核苷酸单链的序列可以为腺嘌呤(a)、鸟嘌呤(g)、胞嘧啶(c)、胸腺嘧啶(t)中的至少一种按照任意的组成组合,可以是腺嘌呤(a)、鸟嘌呤(g)、胞嘧啶(c)、胸腺嘧啶(t)中的任意一种组成的序列,也可以是腺嘌呤(a)、鸟嘌呤(g)、胞嘧啶(c)、胸腺嘧啶(t)中的至少两种组成的序列,比如,a20,c20,g20,t20,a10,a20,a40,a100,a10c20g20t30,a20c30,a30g50等等。
本发明中所述的原子精细纳米团簇为具有一定原子数目以及原子空间分布的精细纳米团簇。
本发明仅限于疏水性的原子精细纳米团簇,本发明所述的寡聚核苷酸/原子精细纳米团簇复合物需要疏水的组分,在纳米团簇提供疏水组分的同时,寡聚核苷酸与纳米团簇共同组成的复合结构可以实现一系列的功能,包括荧光成像,光热等效应,可以应用于脑部疾病的治疗和诊断。寡聚核苷酸起到保护整个复合结构的作用,同时可以使整个结构分散在水相中,实现高效穿越血脑屏障的功能。
根据本发明的第二方面,还提供一种如上面所述的高效穿过血脑屏障的寡聚核苷酸/原子精细纳米团簇复合物的制备方法,包括以下步骤:s1:将原子精细纳米团簇溶解于有机溶剂中获得原子精细纳米团簇溶液;s2:将寡聚核苷酸溶解于去离子水中获得寡聚核苷酸溶液;以及s3:将步骤s1中获得的原子精细纳米团簇溶液加入步骤s2获得的寡聚核苷酸溶液中,并加入能与水互溶的有机溶剂,室温下震荡,采用超滤或透析即可获得溶解于水相的寡聚核苷酸/原子精细纳米团簇复合物。
步骤s1中,原子精细纳米团簇在有机溶剂中的浓度为10~200μm,优选为50-150μm。
步骤s2中,寡聚核苷酸在去离子水中的浓度为10~200μm,优选为50-150μm。
步骤s3中,原子精细纳米团簇溶液,寡聚核苷酸溶液与有机溶剂的体积比为(1~5):1:(2~10),优选为2:1:10。
步骤s1中,所述有机溶剂为可以溶解原子级精细纳米团簇的有机溶剂包括:乙腈、二甲基甲酰胺(dmf)、二甲基亚砜(dmso)、四氢呋喃中任意一种,优选为乙腈。
步骤s3中,可以与水互溶的有机溶剂包括乙腈,二甲基甲酰胺,二甲基亚砜,四氢呋喃中任意一种。优选为二甲基甲酰胺。
所述的室温为20~28℃,优选为25℃。
所述的震荡过程为混匀仪震荡,转速为300~700rpm,优选为500rpm。
所述的震荡时间为8~18h,优选为12h。
根据本发明的一个优选方案,所述的超滤过程为,使用10k超滤管,10000~15000rpm的转速,10~20min,利用去离子水置换溶剂,超滤三次,将有机溶剂置换为去离子水,除去多余的寡聚核苷酸以及金纳米团簇。
根据本发明的第三方面,还提供一种高效穿过血脑屏障的寡聚核苷酸/原子精细纳米团簇复合物在老鼠体内进行血脑屏障穿越的应用。
根据本发明的一个优选方案,通过尾静脉向老鼠体内注射,该复合物可以穿越血脑屏障进入脑实质。
根据本发明的第四方面,还提供一种高效穿过血脑屏障的寡聚核苷酸/原子精细纳米团簇复合物的应用,通过改变金纳米团簇的种类可实现脑荧光成像,脑肿瘤靶向,以及基因药物载送。
根据本发明提供的一种高效穿越血脑屏障寡聚核苷酸/原子精细纳米团簇复合物,相对于现有的穿越血脑屏障技术,利用寡核苷酸链通过疏水相互作用形成的复合物进行血脑屏障穿越,构建了一种具有亲水的dna外壳,同时具有疏水性内核的类病毒颗粒,利用此前没有过的人工纳米复合物仿病毒入侵模式,实现了血脑屏障的高效穿越。充分利用了原子精细的纳米团簇的疏水性,提高了血脑屏障穿越效率。相比于其他穿越血脑屏障的纳米粒子有了明显的提高。
根据本发明,提供了一种全新的dna保护原子精细金纳米团簇的方法,使之可以在生理环境中长时间稳定存在,同时,可以在血脑屏障穿越中,发挥疏水作用在穿越血脑屏障中的优势,这在之前是很难做到的,同时具有原子精细纳米团簇本身的性质。其可以应用于脑荧光成像,脑肿瘤靶向,基因药物载送应用。所述寡聚核苷酸保护的金纳米团簇可以穿越生物体的血脑屏障,转运到大脑。并且,采用活体监控技术,可以监控该材料在生物体内的实时分布情况。取得了良好的生物学效果。该纳米材料性质稳定,可以跨越血脑屏障,在短时间内到达生物体脑部,并进入大脑深部组织。
综上所述,本发明提供了一种可以高效穿越血脑屏障的寡聚核苷酸/原子精细纳米团簇复合物,为脑近红外成像及脑肿瘤或者神经退行性疾病的成像及治疗提供一种有效的药物载体。
附图说明
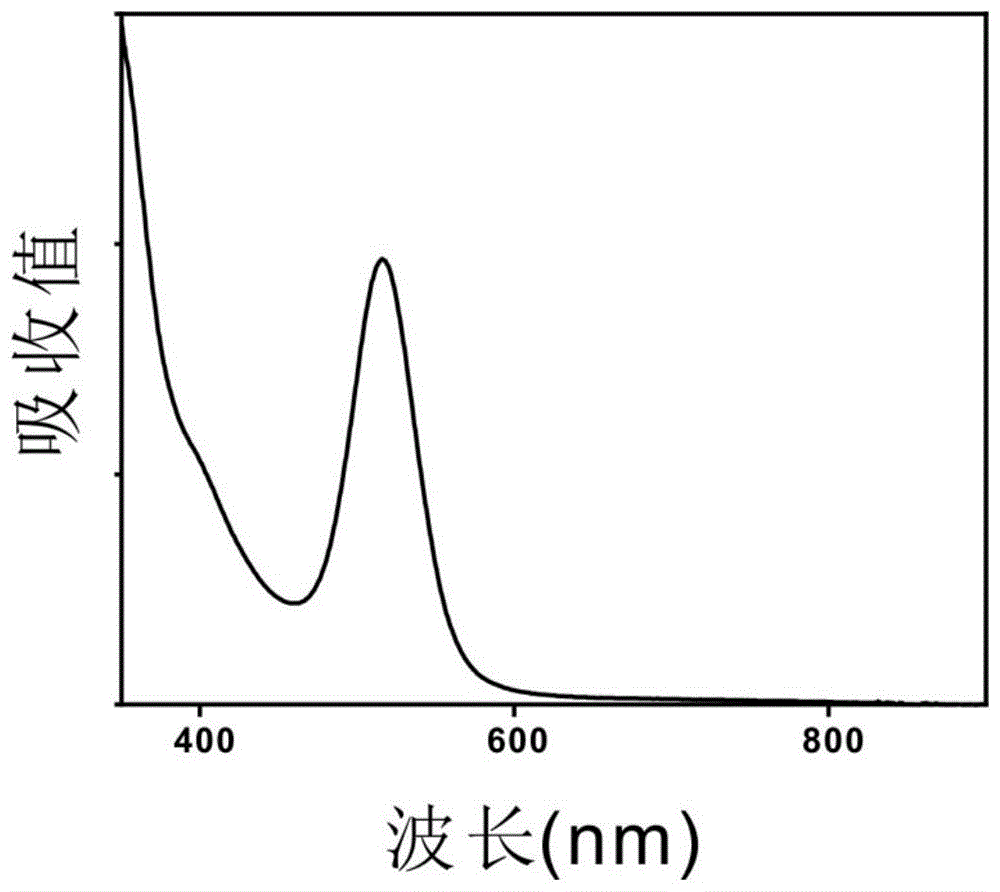
图1是实施例1中制备的寡聚核苷酸保护的原子精细的金纳米团簇水溶液的紫外吸收光谱;
图2是实施例1中制备的寡聚核苷酸保护的原子精细的金纳米团簇水溶液的荧光光谱;
图3是实施例1中制备的寡聚核苷酸保护的原子精细的金纳米团簇水溶液的电子显微镜下观察到的形貌;
图4是实施例2中寡聚核苷酸保护的原子精细的金纳米团簇被注射进入小鼠体内不同时间下在小鼠脑部的荧光;
图5是实施例2中寡聚核苷酸保护的原子精细的金纳米团簇在小鼠脑部荧光共聚焦显微镜图;
图6是实施例2中寡聚核苷酸保护的原子精细的金纳米团簇在小鼠体内不同部位的分布情况;
图7是实施例3中寡聚核苷酸保护的原子精细的金纳米团簇被脑内皮细胞摄取的共聚焦荧光显微镜图;
图8是实施例4中寡聚核苷酸保护的原子精细的金纳米团簇的共聚焦荧光显微镜图;
图9是实施例5中寡聚核苷酸保护的原子精细的金纳米团簇的稳定性试验结果图;
图10和图11是实施例6中使用不同寡聚核苷酸单链实现相同效果的紫外吸收光谱;
图12和图13是实施例6中使用不同原子团簇实现相同效果的紫外吸收光谱;
图14是实施例6中使用不同寡聚核苷酸单链构成的复合物在小鼠脑部的分布情况。
具体实施方式
下面结合实施例对本发明进行具体地描述,但本发明的保护范围不限于以下实施例。
实施例1
本实施例中寡聚核苷酸保护的原子精细的金纳米团簇包括具有特定结构的au8团簇,含有40个胸腺嘧啶(t40)寡聚核苷酸单链,以及可以与水互溶的有机溶剂二甲基甲酰胺。
该寡聚核苷酸保护的原子精细金纳米团簇的制备方法如下:
1)将au8溶解于乙腈里,终浓度为100μm;
2)将t40单链寡聚核苷酸溶解于去离子水里,终浓度为100μm;
3)取200μlau8溶液,加入100μlt40单链寡聚核苷酸溶液,加入100μl可以与水互溶的二甲基甲酰胺,混匀,室温25℃,400rpm震荡过夜12h。
4)向步骤3)中获得的混合溶液中加入3ml去离子水,使用k超滤管,12000rpm,15min超滤三次,回收超滤管截留的液体,获得寡聚核苷酸保护的原子精细的金纳米团簇水溶液。
5)本实施例步骤4)中获得的寡聚核苷酸保护的原子精细的金纳米团簇水溶液紫外吸收光谱如图1所示;荧光光谱如图2所示。
6)本实施例步骤4)中获得的寡聚核苷酸保护的原子精细的金纳米团簇在电子显微镜下表征为20nm左右的颗粒,如图3所示。
实施例2
寡聚核苷酸保护的原子精细的金纳米团簇在小鼠体内的血脑屏障穿越应用如下:
1)将实施例1中获得的寡聚核苷酸保护的原子精细的金纳米团簇水溶液与10xpbs以9:1的比例混合,超声30min。
2)使用1ml注射器通过尾静脉注射进入小鼠体内,利用小动物活体成像仪观察下小鼠脑部的荧光(1h,6h,12h,36h),结果如图4所示。
3)在施用12h后,解剖小鼠,取小鼠脑组织,进行冰冻切片观察,切片厚度为10μm,利用dapi染小鼠脑组织的细胞核,荧光共聚焦显微镜观察,可以看到脑部的红色荧光为本发明中的寡聚核苷酸保护的原子精细的金纳米团簇,如图5所示。说明寡聚核苷酸保护的原子精细的金纳米团簇可以有效的穿越小鼠血脑屏障。
4)收集5min,1h,4h,12h,24h的小鼠器官,包括心,肝,脾,肺,肾,脑。用盐酸和硝酸以3:1的比例消解器官,用icp-mass定量器官中的金含量,得出寡聚核苷酸保护的原子精细的金纳米团簇的小鼠体内分布,发现金团簇主要集中分布在肝脏和脑部,其他脏器中分布较少,分布在脑中的金团簇占注射量的3.2%,如图6所示。
实施例3
1)培养人血脑屏障脑内皮细胞bend.3至1×105左右(100×20mm培养皿,corning,usa)。培养条件为:含有生长因子、dmem培养基(gibcolifetechnologiesinc.,uk),加入10%(v/v)的胎牛血清及青霉素和链霉素(100u/ml,sigma-aldrich)及链霉素(100μg/ml,sigma-aldrich),37℃,5%co2条件下培养。
2)将实施例1中获得的寡聚核苷酸保护的原子精细的金纳米团簇与培养基混合,金团簇终浓度为2μm。37℃,与细胞孵育30min后,共聚焦荧光显微镜观察,可以看到寡聚核苷酸保护的原子精细的金纳米团簇可以有效的被脑内皮细胞摄取。如图7所示。
实施例4
1)取实施例2中剖出的脑组织,用冰冻切片机切片,切片厚度为100μm。切片4℃放置过夜。
2)将切片用pbs缓冲液清洗三次,每次10min。
3)用4%的多聚甲醛固定15分钟,pbs缓冲液清洗三次,每次10min。
4)用1.2%双氧水作用30min,除去非特异性染色,pbs缓冲液清洗三次,每次10min。
5)0.3%的triton-x100作用30min,pbs缓冲液清洗三次,每次10min。
6)用6%的bsa封闭1h,pbs清洗之后用1%的bsa的脑内皮细胞一抗稀释液孵育切片,4℃过夜。
7)洗掉一抗,pbs清洗三次,每次10min,孵育稀释后的荧光二抗,室温下2小时,洗掉荧光二抗,pbs清洗三次,封片。
8)荧光共聚焦显微镜下观察,成像,获得切片的3d图片。imaris软件处理图片,重构血脑屏障,观察金团簇可以有效的穿过血脑屏障,统计发现大约80%进入脑区的金团簇成功穿过了血脑屏障进入了脑实质中,如图8所示。
实施例5
将实施例1中获得的寡聚核苷酸保护的原子精细的金纳米团簇与未灭活的小鼠血清混合,孵育不同时间(0h,1h,4h,12h,24h),收集样品,利用dls测量与血清孵育不同时间的粒径大小,以及进行琼脂糖凝胶电泳(120v,30min)证明材料的稳定性,发现材料在与血清孵育24h后仍然具有很好的稳定性。如图9所示。
实施例6
本实施例中验证寡聚核苷酸/原子精细的纳米团簇组装的普适性。
1)使用不同的寡聚核苷酸单链,包括a20,c20,g20,t20,a10,a20,a40,a100进行复合物的组装,实现了相同效果,如图10,图11所示。
2)选择不同的原子团簇,包括:au20(pp3)4cl4,au20(tpe)8(tpp)6(bf4)2,经验证可以进行同样的组装,如图12,图13所示。
3)按照实施例2的方法注射进入老鼠体内,取老鼠脑部进行切片,可以观察到脑部有着明显的金团簇分布,说明本发明具有普适性,如图14所示。
- 还没有人留言评论。精彩留言会获得点赞!