一种用于皮肤表面的仿生胶原溶液及其制备方法和使用方法与流程
[0001]
本发明涉及一种生物材料的制备及其使用方法,具体涉及一种用于皮肤表面的仿生胶原溶液,及其制备方法和使用方法.
背景技术:
[0002]
皮肤组织中,胶原蛋白是真皮的支撑结构组成成份之一,其网状架构为皮肤提供了保护和弹性,在纤维之间则分布着大量的水分、细胞外基质和功能性细胞,是皮肤重要的生化反应场所,为表皮层提供水分和营养.然而,当胶原分子接触皮肤表面角质层时,由于角质层的屏障作用,分子的扩散系数与分子量的平方根或立方根成反比,分子量愈大,分子体积愈大,扩散系数愈小,相对分子质量从约2kd至300kd不等的胶原分子因此很难通过角质层扩散进入真皮层,被皮肤组织吸收发挥其修复再生功效.
[0003]
一般而言,胶原分子只能通过毛囊、皮脂腺和汗腺等皮肤附属器官吸收,然而毛囊、汗腺和皮脂腺总面积小于皮肤总表面积的1%,吸收量也很小,况且皮肤是一个以排泄为主的器官,靠被动扩散效率显然不会太高.
[0004]
为了提高胶原在皮肤表面(尤其在真皮层)的吸收进而修复皮肤损伤(如皱纹),常规的方法是降低胶原分子的分子量,使用小分子量的胶原蛋白肽,然而胶原蛋白肽是由胶原或明胶经蛋白酶降解处理后制成的,生物活性差,而且由于分子量较小,胶原蛋白肽在体内很容易降解,也很容易被皮肤组织消化吸收,因此皮肤修复效果有限.
[0005]
另外,也可以借助导入仪器(电导、超声波导入、射频导入以及微晶、微针导入等)的功能达到促进胶原吸收的效果,然而仪器长期无序使用会对皮肤会造成一定的伤害,而操作的复杂性也不利于大规模的推广和使用.
[0006]
针对以上胶原分子经皮肤吸收的问题,本发明从仿生的角度开发用于皮肤表面的仿生胶原溶液:(1)胶原原材料选用皮肤组织特有的i型、iii型或v型胶原;(2)添加模拟体液成份,调控溶液ph值,模拟皮肤组织的微环境;(3)添加连接分子,促进胶原分子在皮肤组织中(特别是真皮层)的吸收.所开发的低浓度仿生胶原溶液经由涂抹、喷涂或浸没的方式在皮肤表面使用.
技术实现要素:
[0007]
本发明提供一种用于皮肤表面的仿生胶原溶液,及其制备方法和使用方法.
[0008]
一种用于皮肤表面的仿生胶原溶液制备方法,其中,依次包括如下步骤:
[0009]
(1)将固体胶原材料置入水中,搅拌过程中添加酸性溶液溶解胶原形成均质溶液,胶原溶液的浓度为大于等于0.0001wt.%但小于等于0.1wt.%;
[0010]
(2)低温条件下,将步骤(1)所得胶原溶液在搅拌过程中缓慢加入模拟体液成份,充分溶解;
[0011]
(3)低温条件下,通过碱性溶液或酸性溶液调节步骤(2)所得胶原溶液ph 值至大于等于4但小于等于10,形成均质溶液;
[0012]
(4)低温条件下,在步骤(3)所得胶原溶液中加入连接分子溶液搅拌均匀后制备完成,制备完成后,在低温条件下保存.
[0013]
本发明一种用于皮肤表面的仿生胶原溶液制备方法,其中,低温条件的范围为大于等于0℃但小于等于10℃;所述固体胶原材料选自i型、iii型、v型胶原中的一种或两种以上的组合;所述步骤(3)中,通过碱性溶液或酸性溶液调节胶原溶液ph值至大于等于6但小于等于8.
[0014]
本发明一种用于皮肤表面的仿生胶原溶液制备方法,其中,i型、iii型或v 型胶原是皮肤组织特有的胶原类型,制备过程中尽可能按照皮肤组织中不同类型胶原的含量制备胶原溶液,但为了利于胶原分子的流动,胶原溶液最终为稀溶液,所有类型胶原的总浓度为大于等于0.0001wt.%但小于等于0.1wt.%
[0015]
本发明一种用于皮肤表面的仿生胶原溶液制备方法,其中,所述步骤(1) 和所述步骤(3)中的酸生溶液包括盐酸、硝酸、硫酸、磷酸、酒石酸、柠檬酸、草酸、乙酸和甲酸中的至少一种;所述步骤(3)中的碱性溶液包括三乙胺、四甲基乙二胺、吡啶、哌啶、氢氧化钠、氢氧化钾、氢氧化钙、氢氧化镁、氨水、磷酸氢二钠和碳酸氢钠中的至少一种;所述酸性溶液、碱性溶液的浓度为大于等于0.01m但小于10m.
[0016]
本发明一种用于皮肤表面的仿生胶原溶液制备方法,其中,所述步骤(1) 中的酸性溶液是为了充分溶解固体胶原材料添加的,为微量添加,不显著改变其中胶原溶液浓度,以溶解胶原形成均质溶液为准.
[0017]
本发明一种用于皮肤表面的仿生胶原溶液制备方法,其中,所述步骤(3) 中添加碱性溶液或酸性溶液是为了调节胶原溶液的ph值,为微量添加,不显著改变其中胶原溶液浓度,以溶液达到预设ph值且形成均质溶液为准.
[0018]
本发明一种用于皮肤表面的仿生胶原溶液制备方法,其中,模拟体液成份包括na
+
、k
+
、mg
2+
、ca
2+
、cl-、hco
3-、hpo
42-、so
42-、co
32-、po
43-、h2po
4-中的一种或两种以上的组合.添加模拟体液成份是为了使胶原溶液的离子环境与皮肤组织内的微环境相适应,为微量添加,不显著改变其中胶原溶液浓度.在用于皮肤表面的仿生胶原溶液中各离子的最终离子浓度范围为0.1-500mm,最终总离子浓度范围为0.1-1000mm.
[0019]
本发明一种用于皮肤表面的仿生胶原溶液制备方法,其中,连接分子为异硫氰酸酯、异氰酸酯、酰基叠氮化物、nhs酯、磺酰氯、醛、环氧化物、芳基卤化物、酰亚胺酯、碳二亚胺、酸酐、氟苯基酯、原花青素、京尼平中的一种或两种以上的混合物.添加连接分子是为了增强胶原分子在皮肤组织中的吸收,连接分子溶液的添加不显著改变其中胶原溶液浓度,所述连接分子在用于皮肤表面的仿生胶原溶液中的最终浓度为大于等于0.0001wt.%但小于等于10wt.%.
[0020]
本发明一种用于皮肤表面的仿生胶原溶液制备方法,其中,所述连接分子在用于皮肤表面的仿生胶原溶液中的最终浓度为大于等于0.0001wt.%但小于等于 1wt.%.
[0021]
本发明一种用于皮肤表面的仿生胶原溶液制备方法,其中,所述连接分子在用于皮肤表面的仿生胶原溶液中的最终浓度为大于等于0.0001wt.%但小于等于 0.1wt.%.
[0022]
本发明一种用于皮肤表面的仿生胶原溶液制备方法,其中,所述连接分子在用于皮肤表面的仿生胶原溶液中的最终浓度为大于等于0.001wt.%但小于等于 0.01wt.%.
[0023]
使用本发明任意一种用于皮肤表面的仿生胶原溶液制备方法所制备的用于皮肤
表面的仿生胶原溶液.
[0024]
使用本发明用于皮肤表面的仿生胶原溶液的方法,其中,采用自涂抹、喷涂、浸没中的一种或两种以上的组合将胶原溶液应用于皮肤表面.
[0025]
本发明是针对胶原分子经皮肤吸收困难的问题从仿生角度提出的解决方案. 为了提高胶原溶液的生物相容性,增强胶原分子在皮肤组织中(特别在真皮层) 的吸收,本发明主要进行如下优化:(1)按照皮肤组织中所含胶原分子的类型,选用i型、iii型或v型胶原,按照皮肤组织中不同类型胶原的含量制备胶原溶液,在溶液组成上尽可能与皮肤组织相匹配;(2)按照体液中离子的成份和含量以及ph环境,在溶液中添加模拟体液成份,通过调控离子成份和离子强度,并进一步调控ph值,使胶原溶液与皮肤组织的微环境相匹配;(3)相较于常规通过胶原分子直接与皮肤组织结合实现胶原分子吸收的方法,本发明在胶原溶液中添加了连接分子成份,连接分子可以与胶原溶液中的胶原分子和皮肤组织中的胶原成份同时发生反应,从而将胶原分子结合在皮肤组织中,连接分子的高效反应可以提高胶原分子在皮肤组织中的吸收率.
[0026]
本发明一种用于皮肤表面的仿生胶原溶液制备方法,其中,由于添加了连接分子,在胶原溶液未使用在皮肤表面前,有可能会发生胶原分子与连接分子发生反应的情况,从而影响溶液中胶原分子的流动性,进而影响其在皮肤组织中的吸收.因此,制备方法中,添加连接分子后胶原溶液的保存时间为大于等于0min 但小于等于60min,以不影响其使用效果.
[0027]
本发明一种用于皮肤表面的仿生胶原溶液制备方法,其中,胶原溶液的浓度为大于等于0.0001wt.%但小于等于0.1wt.%,选用低浓度胶原溶液有利于胶原分子的流动传输,利于胶原分子在皮肤组织中的吸收.
[0028]
本发明的仿生胶原溶液中溶液环境与皮肤组织的微环境更接近,其生物相容性比常规胶原溶液更好,更利于胶原分子进入皮肤组织中(特别在真皮层)吸收;由于连接分子在皮肤组织中的作用,可以延缓胶原分子的降解性,发挥其生物活性,促进皮肤组织修复再生.
附图说明
[0029]
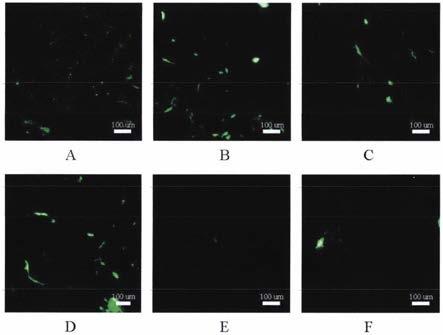
图1 fitc荧光染色标记的胶原分子在大鼠皮下的吸收情况效果图(图1a是实施例1样品,图1b是实施例2样品,图1c是实施例3样品,图1d是实施例4样品,图1e是对比例1样品,图1f是对比例2样品)
[0030]
图2胶原溶液中活/死细胞染色情况效果图(图2a是实施例1样品,图2b是实施例2样品,图2c是实施例3样品,图2d是实施例4样品,图2e是对比例1样品,图2f是对比例2样品)
[0031]
图3胶原溶液植入大鼠体内的he染色情况效果图(图3a是实施例1样品,图3b是实施例2样品,图3c是实施例3样品,图3d是实施例4样品,图3e是对比例1样品,图3f是对比例2样品)
具体实施方式
[0032]
实施例1
[0033]
一种用于皮肤表面的仿生胶原溶液制备方法,其中,依次包括如下步骤:
[0034]
(1)将0.1g iii型胶原材料置入5000g去离子水中,搅拌过程中添加0.1m乙酸溶液溶解胶原形成均质溶液;
[0035]
(2)在2℃下,将步骤(1)所得胶原溶液在搅拌过程中缓慢加入1g nah2po4和0.5g khco3,充分溶解;
[0036]
(3)在5℃下,通过0.01m naoh溶液或0.01m乙酸溶液调节步骤(2)所得胶原溶液ph值至7.2,形成均质溶液;
[0037]
(4)在0℃下,在步骤(3)所得胶原溶液中加入0.01wt.%原花青素溶液,搅拌均匀.
[0038]
仿生胶原溶液配制10min后,将其均匀涂抹于预修复皮肤表面,2h后清洗皮肤表面.
[0039]
实施例2
[0040]
一种用于皮肤表面的仿生胶原溶液制备方法,其中,依次包括如下步骤:
[0041]
(1)将1g i型胶原材料和0.1g iii型胶原材料置入10000g去离子水中,搅拌过程中添加0.03m盐酸溶液溶解胶原形成均质溶液;
[0042]
(2)在10℃下,将步骤(1)所得胶原溶液在搅拌过程中缓慢加入2g nacl 和5g na2co3,充分溶解;
[0043]
(3)在2℃下,通过0.2m koh溶液或0.1m氨水溶液调节步骤(2)所得胶原溶液ph值至10,形成均质溶液;
[0044]
(4)在2℃下,在步骤(3)所得胶原溶液中加入2wt.%碳二亚胺溶液,搅拌均匀.
[0045]
仿生胶原溶液配制60min后,将其均匀喷涂于预修复皮肤表面,1h后清洗皮肤表面.
[0046]
实施例3
[0047]
一种用于皮肤表面的仿生胶原溶液制备方法,其中,依次包括如下步骤:
[0048]
(1)将1g v型胶原材料置入1000000g去离子水中,搅拌过程中添加10m 草酸溶液溶解胶原形成均质溶液;
[0049]
(2)在0℃下,将步骤(1)所得胶原溶液在搅拌过程中缓慢加入2g na3po4和4g nahco3,充分溶解;
[0050]
(3)在5℃下,通过1m甲酸溶液或0.2m磷酸溶液调节步骤(2)所得胶原溶液ph值至4,形成均质溶液;
[0051]
(4)在8℃下,在步骤(3)所得胶原溶液中加入10wt.%nhs酯溶液和1wt.%京尼平溶液,搅拌均匀.
[0052]
仿生胶原溶液配制0min后,将预修复皮肤表面浸没在溶液中,3h后清洗皮肤表面.
[0053]
实施例4
[0054]
一种用于皮肤表面的仿生胶原溶液制备方法,依次包括如下步骤:
[0055]
(1)将2g i型、0.5g iii型和0.1g v型胶原材料置入200000g去离子水中,搅拌过程中添加1m硝酸溶液溶解胶原形成均质溶液;
[0056]
(2)在3℃下,将步骤(1)所得胶原溶液在搅拌过程中缓慢加入10g k2so4和20g na2hpo4,充分溶解;
[0057]
(3)在7℃下,通过0.01m吡啶溶液或2m酒石酸溶液调节步骤(2)所得胶原溶液ph值至6,形成均质溶液;
[0058]
(4)在0℃下,在步骤(3)所得胶原溶液中加入0.001wt.%酰基叠氮化物溶液,搅拌均匀.
[0059]
仿生胶原溶液配制30min后,将其先均匀喷涂再涂抹于预修复皮肤表面,2 h后清洗皮肤表面.
[0060]
实施例5
[0061]
用于皮肤表面的仿生胶原溶液效果比较试验
[0062]
一、对比胶原水溶液的制备
[0063]
对比例1:一种用于皮肤表面的胶原溶液制备方法,依次包括如下步骤:
[0064]
将2g i型胶原材料置入100g去离子水中,搅拌过程中添加0.5m乙酸溶液溶解胶原形成均质溶液;
[0065]
将胶原溶液通过喷涂的方式应用于皮肤表面.
[0066]
对比例2:一种用于皮肤表面的胶原溶液制备方法,其中,依次包括如下步骤:
[0067]
将1g i型胶原材料置入10000g去离子水中,搅拌过程中添加1m盐酸溶液溶解胶原形成均质溶液;
[0068]
将胶原溶液通过涂抹的方式应用于皮肤表面.
[0069]
二、效果试验对比
[0070]
(1)胶原分子在皮肤组织中吸收情况对比:实施例1-4以及对比例1-2中的胶原原材料经fitc荧光染料标记后分别制备对应的胶原溶液,经过对应的方式应用于大鼠皮肤表面,24h后处死实验大鼠,剪取对应皮肤切片,在a1激光共聚焦显微镜上观察(nikon),绿色激发光波长为488nm,比较皮肤中胶原分子的吸收情况,结果见图1.由图1可知,由于实施例中的胶原溶液含有模拟体液成份及ph环境,能够更好的与皮肤微环境相适应,而且连接分子在胶原分子进入皮肤组织的传输过程中可以促进其与周围组织的结合,在皮肤切片中吸收了大量的胶原分子.由于测试胶原分子已标记绿色荧光标记分子fitc,在实施例样品图1a-1d中可以发现大量绿色荧光信号.而对比例中胶原溶液不能模拟皮肤微环境,也没有连接分子,胶原分子进入皮肤组织的传输效率很低,仅能吸收极少的胶原分子,在对比例样品图1e-1f中只发现很少绿色荧光信号.因此,实施例中模拟体液成份的添加、ph值的调控以及连接分子的添加可以促进胶原分子在皮肤组织中的吸收.
[0071]
(2)三维细胞培养情况比较:制备实施例1-4以及对比例1-2中的胶原溶液,分别取1ml与6
×
105大鼠皮肤成纤维细胞(中国科学院上海细胞库)混合,在37℃条件下形成胶原水凝胶包裹细胞进行三维培养实验.培养基为高糖 dmem(hyclone)培养基,含10%(v/v%)的胎牛血清,1%的链霉素和青霉素,培养基每天更换一次.培养箱(steri 371,thermo electron corporation)温度设定为37℃,含有5%(v/v%)co2的湿空气.培养10d后,水凝胶中的细胞经活/ 死细胞染色处理,染色液为2mmol/l的calcein-am(sigma)溶液(染活细胞,发绿色荧光)和2mmol/l的ethd-1(sigma)溶液(染死细胞,发红色荧光),样品在a1激光共聚焦显微镜上观察(nikon),绿色激发光波长为488nm,红色激发光波长为562nm.胶原水凝胶中活/死细胞染色情况见图2.由图2可知,由于实施例中的胶原溶液与皮肤组织微环境更接近,其形成的胶原水凝胶更适宜皮肤细胞的生长,在实施例样品图2a-2d中代表活细胞的绿色荧光信号更强,说明细胞在本发明制备的仿生胶原溶液中可以正常生长,材料的生物相容性好.然而,在对比例中,胶原水凝胶不适宜皮肤细胞生长,在对比例样品图2e-2f中
代表死细胞的红色荧光信号更强,细胞无法在对比例中制备的胶原溶液中正常生长,材料的生物相容性很差.因此,实施例中模拟体液成份的添加和ph值的调控更利于细胞生长,胶原溶液也表现出更好的生物相容性.
[0072]
(3)组织相容性比较:在大鼠肌肉分别植入实施例1-4以及对比例1-2制备的胶原溶液,经1个月后处死实验大鼠,取出植入材料,用4wt.%多聚甲醛固定液固定,进行he染色.
[0073]
具体步骤如下:
[0074]
(1)将样品放在石蜡包埋机里进行包埋,然后用切片机进行切片,将切好的片子放入60℃的水浴锅里,用载玻片小心插入靠近切片的水里,将漂浮的石蜡切片转移到载玻片上,若有水泡,用针头挑出.
[0075]
(2)二甲苯脱水5min,两次,100%酒精、95%酒精、85%酒精、70%酒精、50%酒精依次冲洗,自来水冲洗,苏木精染色5min,自来水冲洗使颜色变蓝.
[0076]
(3)放入1%盐酸乙醇溶液褪色2-10s,颜色变红并较浅,自来水冲洗恢复蓝色.
[0077]
(4)再放入50%酒精、70%酒精、80%酒精各5min,0.5%伊红酒精溶液对比染色1-3min.
[0078]
(5)将切片放入95%酒精中洗去多余红色,然后放入100%酒精中3-5min,吸水纸吸取多余酒精,将切片放入二甲苯i、ii各3-5min.
[0079]
(6)用中性树胶封存,固定.
[0080]
不同样品的he染色结果见图3,由图3可知,由于实施例1-4中(图3a-3d) 的胶原溶液与大鼠体内组织的微环境更接近,材料植入体内后能很快与周围组织融合,只发现少量炎症细胞,而对比例1-2中(图3e-3f)则发现大量炎症细胞,材料的组织相容性很差.因此,实施例1-4中模拟体液成份的添加和ph值的调控可以明显提高胶原溶液在体内的组织相容性.
[0081]
结合效果试验可知,实施例1-4与对比例1-2比较,对比例中胶原溶液为强酸性溶液,不利于胶原溶液在皮肤表面的使用,实施例中胶原溶液偏中性,且可根据不同皮肤的进行调控,更适宜皮肤表面的微环境;实施例中添加了与体液相似的离子成份,使胶原溶液的离子强度,渗透性等性能与皮肤的微环境更接近,利于胶原分子传输;实施例中添加了连接分子,可以在胶原分子进入真皮层的过程中实现胶原分子与真皮层中胶原成份的结合,利于溶液中胶原分子在真皮层的富集和吸收;实施例中胶原溶液更利于细胞生长以及与体内组织的融合.
[0082]
以上所述的实施例仅仅是对本发明的优选实施方式进行描述,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1