靶向氧化石墨烯复合物用于治疗耐药骨肉瘤的实验方法与流程
本发明涉及耐药骨肉瘤治疗技术领域,具体是靶向氧化石墨烯复合物用于治疗耐药骨肉瘤的实验方法。
背景技术:
骨肉瘤(osteosarcoma,os)是最常见的侵袭性原发性恶性骨肿瘤,多发生于儿童和青年人。目前,治疗骨肉瘤的金标准为:首先使用综合化疗,然后进行肿瘤的根治性切除(如果情况允许也可切除转移瘤),然后再次进行综合化疗。非转移性骨肉瘤患者的5年生存率为70%,而转移性或复发性骨肉瘤患者的5年生存率仅约为20%。然而,这种综合治疗策略在骨肉瘤患者中的有效比例仍不超过60%。尽管有不同的治疗策略,骨肉瘤的预后在过去的几十年中并没有得到明显的改善。目前治疗效果有限的主要原因是由于对化疗药物的耐药。肿瘤耐药的产生的原因包括:肿瘤细胞过表达atp结合盒式转运蛋白,如p-糖蛋白(p-gp),这是一种细胞膜上三磷酸腺苷(atp)依赖的单向外排泵,可将抗癌药物排出胞外;长期的化疗药物选择之后出现了对相应化疗药物产生耐受能力的细胞克隆。因此,迫切需要针对新的治疗靶点研发新的疗法,以逆转肿瘤的耐药性。
近年来,线粒体作为有效的肿瘤治疗靶点受到了广泛关注。线粒体是细胞的能量工厂,是一种不可或缺的亚细胞器,每个细胞有数百到数千个,在细胞的各种生理过程中起着至关重要的作用,包括启动内源性凋亡途径。线粒体功能改变是肿瘤发生、发展,血管生成及化疗药物耐药的重要标志。通过诱导线粒体凋亡,可释放细胞色素c,进而激活caspase级联。因此,通过线粒体靶向诱导肿瘤细胞凋亡在治疗恶性肿瘤方面具有巨大的潜力。
以光动力疗法(pdt)联合光热疗法(ptt)为代表的协同光疗可用于治疗耐药肿瘤,由于作用机制的不同,其治疗效果优于化疗。协同光疗是一种无创、高选择性、低全身毒性的肿瘤治疗方法。在光疗中,光照被光敏剂(ps)或光热剂吸收,并转化为活性氧(ros)或局部高热,进而导致肿瘤细胞死亡。利用其光诱发性,通过合理的联合pdt及ptt,可协同促进肿瘤治疗。然而,如果pdt及ptt的激发光谱不匹配,照射过程中可能需要连续两次照射,因此增加了治疗的时间及复杂性。此外,一些固有的缺陷,如ros的寿命较短(10ns–320ns)和扩散半径较局限(10nm–55nm)会降低pdt的治疗效果。因此,使用单剂照射,在某些对ros敏感的细胞器中诱导产生ros,可能是一种有前途的治疗策略。
报道表明,在所有细胞器中,线粒体对ros和高温介导的损伤最为敏感,可迅速扰乱线粒体功能,改变线粒体膜电位,减少atp生成,最终诱导肿瘤细胞凋亡。因此,通过光疗选择性在线粒体产生ros和高热可以显著提高它们的治疗效果。此外,热疗结合ros介导线粒体功能障碍,同时抑制atp生成应是克服肿瘤耐药性的一种有效策略。因此,线粒体靶向协同光疗可作为耐药骨肉瘤治疗的替代策略。
因此,选择性、高效性促进光敏剂及光热剂在线粒体聚集,将光束精确聚焦于肿瘤区域,通过单剂近红外光同时激发,将光能充分地转化为热能并生成ros至关重要。因此,在光疗过程中,需要实时勾勒出肿瘤边缘,将其与正常组织区分开来,从而使光束能准确聚焦在肿瘤区域。研究表明,在700nm–900nm波长范围内的近红外(nir)区域的荧光(fl)成像可用于实时监测光敏剂和光热剂在体内的动态分布,以及检测肿瘤及其边缘。此外,为了提高治疗效率,减少操作步骤和治疗所需时间,并充分利用pdt和ptt的协同作用,光敏剂和光热剂须以复合结构的形式同时递送到线粒体,并使用单剂nir进行激发。因此,协同光疗有赖于光敏剂和光热剂的吸收光谱相重叠。然而,这种特殊的要求和复杂的合成工艺有可能限制其进一步的应用。因此,开发一种简单、高效的纳米复合物协同进行pdt和ptt,具有重大需求。
吲哚菁绿(icg)是美国fda批准的近红外造影剂,不仅可以用于近红外荧光成像,还可以将光能转换为热能并生成ros,实现协同光疗。因此,icg被认为是肿瘤治疗的理想药物之一。然而,icg在肿瘤治疗中的应用存在以下几个缺点:i)体内半衰期短;ii)由于其亲水性强,细胞摄取能力差;iii)可能被p-gp单向排出;iv)缺乏肿瘤特异性聚集;v)肿瘤光疗效率较低,需与其他治疗策略结合以改善治疗结果。
技术实现要素:
本发明的目的在于提供靶向氧化石墨烯复合物用于治疗耐药骨肉瘤的实验方法,以解决上述背景技术中提出的问题。
为实现上述目的,本发明提供如下技术方案:
靶向氧化石墨烯复合物用于治疗耐药骨肉瘤的实验方法,线粒体靶向氧化石墨烯纳米复合物用于荧光成像引导下的协同光疗治疗耐药骨肉瘤,包括如下步骤:(1)、实验细胞、动物及肿瘤异种移植,将mg63/dox细胞植于小鼠背部皮下,然后用荷瘤小鼠进行活体成像和光疗,(2)、ppg、tpp-ppg和tpp-ppg@icg制备,(3)、表征,对tpp-ppg、icg和tpp-ppg@icg的光学特性采用紫外可见近红外分光光度计进行表征,(4)、单线态氧检测,用单线态氧绿色荧光探针检测单线态氧的生成,(5)、光热转换实验,用近红外光进行照射,使用红外线温度计记录温度变化,(6)、细胞摄取和细胞内定位,将mg63/dox细胞培养孵育后,用pbs洗涤后在培养基中重悬,流式细胞仪检测样品的平均荧光强度,将mg63/dox细胞与tpp-ppg@icg共同培养,pbs洗涤细胞后加入线粒体荧光探针孵育,对线粒体进行标记,pbs再次洗涤细胞后用激光扫描共聚焦显微镜扫描获取图像,(7)、体外实验,将mg63/dox细胞悬液培养加入不同浓度的icg、tpp-ppg和ppg@icg溶液,对非照射组pbs洗涤后再次培养,照射组使用808nmnir照射后再次培养,检测细胞活力同时进行活细胞/死细胞双染,将mg63/dox细胞加入pbs、tpp-ppg@icg、icg、tpp-ppg、ppg@icg及tpp-ppg@icg培养,加入双染试剂盒孵育,使用近红外荧光光谱进行观察,(8)、细胞凋亡和胞内ros检测,mg63/dox细胞培养nir照射后低速离心收集细胞,在缓冲液中重新悬浮避光染色后,低速离心收集细胞,pbs洗涤并用结合缓冲液稀释后进行流式细胞分析,用dcfh-da试剂盒检测细胞内ros的产生,(9)、线粒体膜电位检测,用jc-1记录线粒体膜电位的变化,用激光共聚焦显微镜采集图像,(10)线粒体超氧化物检测,使用线粒体超氧化物荧光探针检测线粒体超氧化物的产生,(11)、atp检测,使用atp检测试剂盒绘制atp浓度标准曲线,(12)、近红外荧光及热学成像,对mg63/dox荷瘤裸鼠尾静脉注射tpp-ppg@icg,采用近红外成像系统进行体外近红外成像,使用nri进行照射时使用红外热成像相机对小鼠肿瘤组织温度变化进行实时成像,(13)、体内pdt/ptt联合治疗,将荷瘤小鼠随机分为6组,pbs非照射组(对照组)、tpp-ppg@icg非照射组、icg照射组、tpp-ppg照射组、ppg@icg照射组和tpp-ppg@icg照射组,静脉注射icg,照射组在肿瘤部位使用808nmnir进行照射,持续15天,收集肿瘤和主要器官,获取的内脏进行苏木精-伊红染色,并进行显微镜观察。
作为本发明进一步的方案:所述步骤(1)中mg63/dox细胞混于100μl基质凝胶中进行移植,肿瘤体积达到60mm3时,进行活体成像和光疗。
作为本发明进一步的方案:所述步骤(5)中近红外光采用808nm近红外光。
作为本发明进一步的方案:所述步骤(8)中mg63/dox细胞接种在6孔板中过夜,然后加入等效剂量的pbs(-)、tpp-ppg@icg(-)、icg(+)、tpp-ppg(+)、ppg@icg(+)及tpp-ppg@icg(+)共培养24h。
作为本发明进一步的方案:所述步骤(8)中dcfh-da试剂盒检测细胞内ros的产生,要先将mg63/dox细胞接种在24孔板中过夜,加入等效剂量的pbs(-)、tpp-ppg@icg(-)、icg(+)、tpp-ppg(+)、ppg@icg(+)及tpp-ppg@icg(+)共培养24h。
作为本发明进一步的方案:所述步骤(9)中要先将mg63/dox细胞与等效剂量的pbs(-)、tpp-ppg@icg(-)、icg(+)、tpp-ppg(+)、ppg@icg(+)及tpp-ppg@icg(+)共培养24h,nir照射后再孵育24h,未照射组在相同条件下孵育48h,然后用pbs洗涤细胞,并在37℃下加入5mm的jc-1共培养30分钟,再用pbs洗涤细胞并使用clsm进行观察。
作为本发明进一步的方案:所述步骤(10)中要先将mg63/dox细胞接种在35毫米玻璃培养皿中过夜,然后加入等效剂量的pbs(-)、tpp-ppg@icg(-)、icg(+)、tpp-ppg(+)、ppg@icg(+)及tpp-ppg@icg(+)共培养24h,处理后用pbs洗涤细胞两次,加入5μm线粒体超氧化物荧光探针孵育10分钟,再用pbs洗涤两次并用clsm观察采集图片。
作为本发明进一步的方案:所述步骤(11)中要先将mg63/dox细胞接种在96孔板中,加入100μldmem培养24小时,然后加入等效剂量的pbs(-)、tpp-ppg@icg(-)、icg(+)、tpp-ppg(+)、ppg@icg(+)及tpp-ppg@icg(+)共培养24h,去除培养基并加入细胞裂解液,然后加入atp检测试剂盒,检测荧光值,计算atp浓度,每个实验重复三次,计算平均值。
作为本发明进一步的方案:所述步骤(13)中需要每3天监测一次肿瘤体积和小鼠体重的变化,持续15天,以评估治疗效果。
与现有技术相比,本发明的有益效果是:本发明将线粒体靶向tpp和icg与peg及bpei修饰的ngo结合,用于pdt/ptt协同治疗,材料的epr效应使tpp-ppg@icg聚集于肿瘤组织,icg的近红外成像特性可用于近红外成像,引导光束聚焦于肿瘤组织,可最大限度地减少光疗的副作用;使用peg及bpei对ngo进行修饰,可促进了icg的分散和细胞摄取,而线粒体靶向tpp增强了肿瘤的pdt/ptt协同治疗效应;在单次近红外光照射下,tpp-ppg@icg可迅速扰乱线粒体功能,改变线粒体膜电位,减少atp生成,最终诱导肿瘤细胞凋亡,该策略可有效抑制耐药骨肿瘤。
附图说明
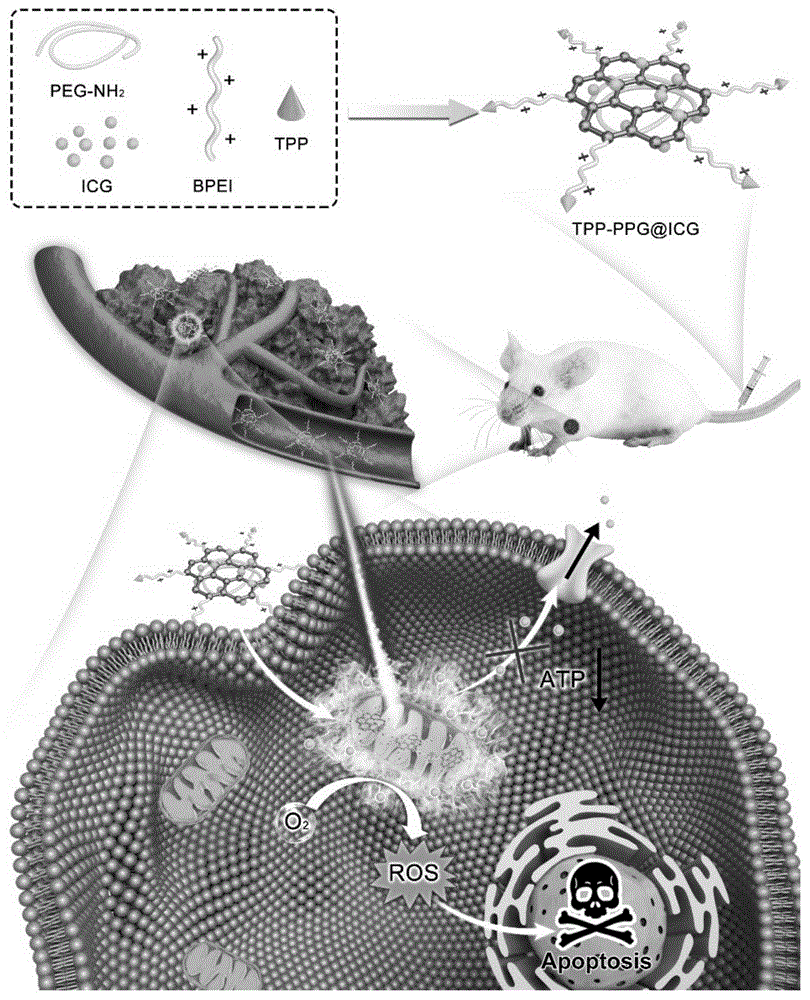
图1为tpp-ppg@icg靶向线粒体进行协同光疗示意图。
图2为tpp-ppg@icg表征及生化特征。
图3为细胞摄入及亚细胞定位。
图4为tpp-ppg@icg对mg63/dox细胞的体外协同光疗。
图5为tpp-ppg@icg协同光疗效应的细胞机制。
图6为tpp-ppg@icg协同光疗对线粒体功能的影响。
图7为nir照射或非照射细胞内atp的相对浓度测定。
图8为tpp-ppg@icg体内协同光疗治疗mg63/dox荷瘤小鼠。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
请参阅图1,本发明实施例中,靶向氧化石墨烯复合物用于治疗耐药骨肉瘤的实验方法,线粒体靶向氧化石墨烯纳米复合物用于荧光成像引导下的协同光疗治疗耐药骨肉瘤,包括如下步骤:(1)、实验细胞、动物及肿瘤异种移植。人骨肉瘤细胞系mg63及抗阿霉素骨肉瘤细胞系mg63/dox,用含10%fbs及1%青霉素/链霉素双抗的rpmi-1640培养基进行培养(37℃,5%co2)。裸鼠(6周龄,体重18g–22g)于spf环境下进行饲养,将mg63/dox细胞(约1×107)混于100μl基质凝胶中,植于小鼠背部皮下。当肿瘤体积达到60mm3时,用荷瘤小鼠进行活体成像和光疗。
(2)、ppg、tpp-ppg和tpp-ppg@icg制备,ngo根据改良hummer法制备,首先进行石墨片层氧化,然后进行超声波处理,再制备pg和ppg。tpp与ppg的嫁接:将5mgtpp溶解在4ml水中,并在室温下用edc·hcl(15mg)和nhs(15mg)活化15min。随后,向反应混合物中添加4mlppg(1.0mg/ml)溶液,并在室温下磁力搅拌24h。最后,通过10kda透析超滤管过滤去除多余tpp,并用双蒸馏水反复洗涤,以获得ppg-tpp(等同ngo-peg浓度0.5mg/ml)。合成tpp-ppg@icg:将icg(7.74mg)溶解于1ml无水二甲基亚砜中,作为储备液(10mm),供进一步使用。将200μlicg(10mm)和1.8mltpp-ppg(0.5mg/ml)混合并在室温下搅拌24小时。然后,整个系统在蒸馏水中透析24h(截留分子量:10kda)。将最终产品(tpp-ppg@icg)冷冻干燥,并在4℃以下储存备用。通过标准曲线及781nm处的吸光度峰测定装载于tpp-ppg上的icg浓度。
请参阅图2,靶向氧化石墨烯复合物用于治疗耐药骨肉瘤的实验方法,(3)、表征。获取tpp-ppg@icg红外光谱,确认icg成功装载于纳米氧化石墨烯。原子力显微镜检测tpp-ppg@icg纳米材料的大小和厚度。tpp-ppg、icg和tpp-ppg@icg光学特性采用紫外可见近红外分光光度计进行表征。纳米材料稳定性测试如下:tpp-ppg或tpp-ppg@icg与pbs、细胞培养基(rpmi-1640培养基)或血清一起孵育,检测混合物中是否产生沉淀。在37℃和43℃的酸性(ph=5.0)和弱碱性(ph=7.4)磷酸盐缓冲液(pbs)中分别加入tpp-ppg@icg的icg进行释放研究,一定时间后离心后收集pbs,用紫外-可见光谱对tpp-ppg释放的icg量进行检测。随后加入相同体积的pbs,继续进行释放检测。
(4)、单线态氧检测。用单线态氧绿色荧光探针(sosg)检测单线态氧(1o2)的生成。将sosg溶解于2%甲醇水溶液中,使其终浓度为1mm,加入icg、tpp-ppg和tpp-ppg@icg(icg浓度=10μm)溶液与之混合。然后,立即用808nm近红外光照射混合溶液5min(能量密度:0.8w/cm2)。随后用494nm光源激发,检测530nmsosg发射峰,进而计算单线态氧的生成。
(5)、光热转换实验。将1mlpbs、icg、tpp-ppg和tpp-ppg@icg溶液置于石英比色皿,以2.5min的时间间隔用808nm近红外光进行照射(能量密度:0.8w/cm2)10min。使用红外线温度计记录温度变化。
请参阅图3,靶向氧化石墨烯复合物用于治疗耐药骨肉瘤的实验方法,(6)、细胞摄取和细胞内定位。将mg63/dox细胞以1×105个细胞/孔的密度接种在6孔板中。隔夜培养后,加入10μmtpp-ppg@icg。孵育1h、4h、8h、12h和24h后,用pbs洗涤细胞三次后胰蛋白酶消化,在培养基中重悬。流式细胞仪检测每个样品的平均荧光强度。亚细胞定位:将mg63/dox细胞与tpp-ppg@icg(icg浓度=10μm)于35mm培养皿中共培养24h。pbs洗涤细胞三次,加入线粒体荧光探针孵育10min,对线粒体进行标记。pbs再次洗涤细胞三次,激光扫描共聚焦显微镜扫描获取图像。
请参阅图4,靶向氧化石墨烯复合物用于治疗耐药骨肉瘤的实验方法,(7)、体外实验。将100μlmg63/dox细胞悬液(5×103个细胞/孔)接种于96孔板中培养24h,然后加入不同浓度的icg、tpp-ppg和ppg@icg溶液。非照射组,pbs洗涤后再次培养24h。照射组使用808nmnir(能量密度:0.8w/cm2)照射5min后再次培养24h。cck-8法检测细胞活力。同时,进行活细胞/死细胞双染用于评估tpp-ppg@icg协同光疗效应。将mg63/dox细胞(1×105个细胞/孔)接种在6孔板中并培养过夜。然后,加入等效剂量的pbs(-),tpp-ppg@icg(-),icg(+),tpp-ppg(+),ppg@icg(+),及tpp-ppg@icg(+)(ngo20μg/ml;icg15μm)共培养24h(-:无光照,+:0.8w/cm2nir照射5min)。再培养24h后,加入calceinam/pi双染试剂盒在37℃下孵育20min,使用近红外荧光光谱进行观察。
请参阅图5,靶向氧化石墨烯复合物用于治疗耐药骨肉瘤的实验方法,(8)、细胞凋亡和胞内ros检测。将mg63/dox细胞接种在6孔板(2×105个细胞/孔)中过夜,然后加入等效剂量的pbs(-),tpp-ppg@icg(-),icg(+),tpp-ppg(+),ppg@icg(+)及tpp-ppg@icg(+)(ngo20μg/ml;icg15μm)共培养24h(-:无光照,+:0.8w/cm2nir照射5min)共培养24h。nir照射6h后,胰蛋白酶消化,低速离心收集细胞,然后用pbs洗涤两次。将收集的细胞在100μl缓冲液中重新悬浮,避光加入2μlannexinv-fitc和2μlpi染色15min。染色后,通过低速离心收集细胞,用pbs洗涤两次,并用400μl的结合缓冲液稀释后进行流式细胞分析。dcfh-da试剂盒检测细胞内ros的产生。将mg63/dox细胞接种在24孔板(1×105个细胞/孔)中过夜,加入等效剂量的pbs(-),tpp-ppg@icg(-),icg(+),tpp-ppg(+),ppg@icg(+)及tpp-ppg@icg(+)(ngo20μg/ml;icg15μm)共培养24h(-:无光照,+:0.8w/cm2nir照射5min)共培养24h。照射后立即用pbs冲洗细胞,37℃孵育30min,用dmlrb倒置显微镜观察ros荧光信号。
请参阅图6,靶向氧化石墨烯复合物用于治疗耐药骨肉瘤的实验方法,(9)、线粒体膜电位检测。用jc-1记录线粒体膜电位的变化,用激光共聚焦显微镜(clsm)采集图像。mg63/dox细胞(1×105个细胞/孔)与等效剂量的pbs(-),tpp-ppg@icg(-),icg(+),tpp-ppg(+),ppg@icg(+)及tpp-ppg@icg(+)(ngo20μg/ml;icg15μm)共培养24h(-:无光照,+:0.8w/cm2nir照射5min)共培养24h。nir照射后再孵育24h,未照射组在相同条件下孵育48h。然后,立即用pbs洗涤细胞,并在37℃下加入5mm的jc-1共培养30分钟。再次用pbs洗涤细胞并使用clsm进行观察。
(10)、线粒体超氧化物检测。使用线粒体超氧化物荧光探针检测线粒体超氧化物的产生。将mg63/dox细胞接种在35毫米玻璃培养皿中过夜,然后加入等效剂量的pbs(-),tpp-ppg@icg(-),icg(+),tpp-ppg(+),ppg@icg(+)及tpp-ppg@icg(+)(ngo20μg/ml;icg15μm)共培养24h(-:无光照,+:0.8w/cm2nir照射5min)。处理后,用pbs洗涤细胞两次,加入5μm线粒体超氧化物荧光探针孵育10分钟,pbs洗涤两次,并用clsm观察采集图片。
请参阅图7,靶向氧化石墨烯复合物用于治疗耐药骨肉瘤的实验方法,(11)、atp检测。使用atp检测试剂盒绘制atp浓度标准曲线。将mg63/dox细胞接种在96孔板(1×104个细胞/孔)中,加入100μldmem培养24小时。然后加入等效剂量的pbs(-),tpp-ppg@icg(-),icg(+),tpp-ppg(+),ppg@icg(+)及tpp-ppg@icg(+)(ngo20μg/ml;icg15μm)共培养24h(-:无光照,+:0.8w/cm2nir照射5min)。6小时后,去除培养基并加入细胞裂解液。然后,加入atp检测试剂盒,检测荧光值,计算atp浓度。每个实验重复三次,计算平均值。
请参阅图8,靶向氧化石墨烯复合物用于治疗耐药骨肉瘤的实验方法,(12)、近红外荧光及热学成像。以mg63/dox荷瘤裸鼠为实验动物评价材料的肿瘤靶向性,按0.5mg/kg的剂量通过尾静脉注射tpp-ppg@icg。采用近红外成像系统(kodak)进行体外近红外成像。所有的设置及成像条件按文献报道进行。注射tpp-ppg@icg24h后,处死小鼠并获取其内脏器官。为了评估在体ptt特性,当使用nri进行照射时使用红外热成像相机对小鼠肿瘤组织温度变化进行实时成像。
(13)、体内pdt/ptt联合治疗。当肿瘤体积达到60mm3时,将荷瘤小鼠随机分为6组,每组5只:pbs非照射组(对照组)、tpp-ppg@icg非照射组、icg照射组、tpp-ppg照射组、ppg@icg照射组和tpp-ppg@icg照射组。静脉注射等效剂量的药物(icg750μm)。照射组在肿瘤部位使用808nm(0.8w/cm2,5min)nir进行照射。每3天监测一次肿瘤体积和小鼠体重的变化,持续15天,以评估治疗效果。第15天,动物被安乐死。收集肿瘤和主要器官(心、肝、脾脏、肺和肾脏)。获取的内脏进行苏木精-伊红染色,并进行显微镜观察。
尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!