一种利鲁唑缓释片及其制备方法与流程
1.本发明属于医药技术领域,提供了一种利鲁唑缓释片及其制备方法。
背景技术:
2.利鲁唑片由赛诺菲安万特公司研制开发,于1996年获fda批准上市,规格为50mg。利鲁唑,即2-氨基-6-三氟甲氧基苯并噻唑,适用于延长肌萎缩侧索硬化(als)患者的生命或延长其发展至需要机械通气支持的时间。利鲁唑的作用机制尚不清楚,其作用可能与抑制谷氨酸释放、稳定电压依赖性钠通道的失活状态、干扰神经递质与兴奋性氨基酸受体结合后细胞内事件有关。
3.利鲁唑在水中几乎不溶,在甲醇或乙醇中易溶。每天需服用2次(50mg每12小时一次),每日定时口服,血药浓度波动大,峰浓度高,不良反应严重。
4.缓释制剂是指在规定介质中,按要求缓慢的非恒速释放药物,与相应的普通制剂比较,给药频率减少一半或有所减少,且能显著增加患者依从性的制剂。其特点在于活性药物释放缓慢,吸收入血后可维持较长时间的有效治疗血药浓度。
5.申请号为201910043880.3,发明名称为一种利鲁唑缓释口服混悬液的发明专利中公开了一种利鲁唑缓释口服混悬液,解决了老年儿童等吞咽困难人群给药顺应性问题。
技术实现要素:
6.本发明的目的在于提供一种利鲁唑缓释片及其制备方法,本发明的缓释片是骨架型和膜控型结合的缓释制剂,释药徐缓,使血药浓度平稳,避免峰谷现象,并且能长时间维持有效血药浓度,发挥最佳治疗效果。由于减少了峰谷现象,故有利于降低药物的毒副作用,减少耐药性的发生。
7.本发明具体技术方案如下:
8.本发明所述的利鲁唑缓释片主要由85%~95%含药片芯及5%~15%的缓释包衣层组成。其中,所述含药片芯主要由利鲁唑、填充剂、崩解剂、助流剂、润滑剂、缓释骨架材料组成;所述缓释包衣层主要由eudragit rl 30d、eudragit rs 30d、柠檬酸三乙酯、二甲基硅油、滑石粉组成。
9.优选的,上述利鲁唑缓释片由90%含药片芯、10%的缓释包衣层组成。
10.进一步优选的,上述含药片芯由以下组分组成:
[0011][0012]
更优选的,所述的含药片芯由以下组分组成:
[0013][0014]
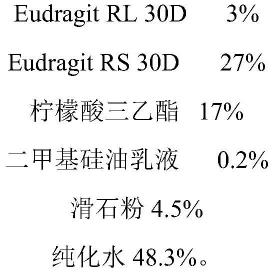
进一步优选的,上述缓释包衣层由以下组分组成:
[0015]
eudragit rl 30d
ꢀꢀ
2%~7%
[0016]
eudragit rs 30d
ꢀꢀ
24%~30%
[0017]
柠檬酸三乙酯 15%~20%
[0018]
二甲基硅油乳液
ꢀꢀ
0.1%~0.3%
[0019]
滑石粉
ꢀꢀ
3%~5%
[0020]
纯化水
ꢀꢀ
45%~50%。
[0021]
更优选的,所述的缓释包衣层由以下组分组成:
[0022]
eudragit rl 30d
ꢀꢀ
3%
[0023]
eudragit rs 30d
ꢀꢀ
27%
[0024]
柠檬酸三乙酯 17%
[0025]
二甲基硅油乳液
ꢀꢀ
0.2%
[0026]
滑石粉
ꢀꢀ
4.5%
[0027]
纯化水
ꢀꢀ
48.3%
[0028]
上述缓释骨架材料为羟乙基纤维素、羟丙甲纤维素、卡波姆树脂、羧甲基纤维素钠、海藻酸钠中的一种或多种;优选的,所述的缓释骨架材料为羟乙基纤维素。
[0029]
上述填充剂为微晶纤维素、乳糖、淀粉、无水磷酸氢钙、预胶化淀粉、甘露醇中的一种或多种混合。
[0030]
优选的,所述填充剂为微晶纤维素、乳糖;
[0031]
进一步优选的,微晶纤维素、乳糖的比例为16:5-15;
[0032]
更优选的,微晶纤维素、乳糖的比例为16:9。
[0033]
上述崩解剂为低取代羟丙基纤维素、干淀粉、羧甲基淀粉钠、交联pvp中的一种或
多种混合。
[0034]
优选的,所述的崩解剂为低取代羟丙基纤维素。
[0035]
优选的,上述助流剂为微粉硅胶、二氧化硅的一种或两种混合。
[0036]
优选的,上述润滑剂为硬脂酸镁、微粉硅胶、氢化植物油、硬脂富马酸钠中的一种或多种混合;
[0037]
进一步优选的,所述的润滑剂为硬脂酸镁。
[0038]
本发明的目的还在于提供上述利鲁唑缓释片的制备方法,所述制备方法主要包括以下步骤:
[0039]
a:取处方量利鲁唑、填充剂、崩解剂、缓释骨架材料、助流剂混合,压片,得素片备用;
[0040]
b:取处方量的缓释包衣层成分,制作包衣液,备用;
[0041]
c:将步骤a中所得素片用步骤b中所得包衣液进行包衣,即得利鲁唑缓释片;
[0042]
优选的,所述制备方法包括以下步骤:
[0043]
a:取处方量利鲁唑与微晶纤维素、乳糖混合,加入处方量低取代羟丙纤维素、羟乙纤维素和微粉硅胶混合,加入处方量硬脂酸镁混合,压片,得素片备用;
[0044]
b:取处方量的缓释包衣层成分,制作包衣液,备用;
[0045]
c:将步骤a中所得素片用步骤b中所得包衣液进行包衣,即得利鲁唑缓释片。
[0046]
与现有技术相比,本发明具有以下技术效果:
[0047]
本发明所制备的利鲁唑缓释片,是一种骨架型与膜控型结合的缓释制剂。在消化液中释药徐缓,胃肠道转运时间相对恒定,避免剂量突释现象,保证临床用药安全性。同时在胃肠道分布面积大,药物的生物利用度高;且制备工艺简单,技术难度低,批次间的差异小,释放曲线重现性好,利于工业化的大规模生产。
附图说明
[0048]
图1为实施例1、2、3、4、5、6、7,对比实施例1、2所得利鲁唑缓释片的体外累积释放曲线图
具体实施例
[0049]
实施例1:
[0050]
含药片芯:
[0051]
利鲁唑 320g
[0052]
微晶纤维素 256g
[0053]
乳糖
ꢀꢀ
144g
[0054]
低取代羟丙基纤维素
ꢀꢀ
24g
[0055]
二氧化硅
ꢀꢀ
8g
[0056]
硬脂酸镁
ꢀꢀ
8g
[0057]
羟乙基纤维素
ꢀꢀ
240g;
[0058]
缓释包衣层:
[0059]
eudragit rl 30d
ꢀꢀ
30g
[0060]
eudragit rs 30d
ꢀꢀ
270g
[0061]
柠檬酸三乙酯
ꢀꢀ
170g
[0062]
二甲基硅油乳液
ꢀꢀ
2g
[0063]
滑石粉 45g
[0064]
纯化水 483g;
[0065]
取处方量的利鲁唑、微晶纤维素、乳糖混合均匀,再加入处方量的低取代羟丙纤维素、羟乙纤维素、微粉硅胶混合均匀,最后加入处方量的硬脂酸镁混合均匀,压片机制得素片,备用。
[0066]
取处方量的eudragit rl 30d、eudragit rs 30d、滑石粉、柠檬酸三乙酯加入水中,匀浆机匀化,过滤,加入处方量二甲基硅油消泡,得包衣液,备用。
[0067]
将上述所得素片在包衣锅中以上述所得包衣液进行包衣(包衣增重为10%),即得利鲁唑缓释片。
[0068]
实施例2
[0069]
含药片芯:
[0070]
利鲁唑 320g
[0071]
微晶纤维素 305g
[0072]
乳糖
ꢀꢀ
95g
[0073]
低取代羟丙基纤维素
ꢀꢀ
24g
[0074]
二氧化硅
ꢀꢀ
8g
[0075]
硬脂酸镁
ꢀꢀ
8g
[0076]
羟乙基纤维素
ꢀꢀ
240g;
[0077]
缓释包衣层:
[0078]
eudragit rl 30d
ꢀꢀ
30g
[0079]
eudragit rs 30d
ꢀꢀ
270g
[0080]
柠檬酸三乙酯
ꢀꢀ
170g
[0081]
二甲基硅油乳液
ꢀꢀ
2g
[0082]
滑石粉 45g
[0083]
纯化水 483g;
[0084]
制备方法参考实施例1,其中包衣增重为10%。
[0085]
实施例3
[0086]
含药片芯:
[0087]
利鲁唑 320g
[0088]
微晶纤维素 206g
[0089]
乳糖
ꢀꢀ
194g
[0090]
低取代羟丙基纤维素
ꢀꢀ
24g
[0091]
二氧化硅
ꢀꢀ
8g
[0092]
硬脂酸镁
ꢀꢀ
8g
[0093]
羟乙基纤维素
ꢀꢀ
240g;
[0094]
缓释包衣层:
[0095]
eudragit rl 30d
ꢀꢀ
30g
[0096]
eudragit rs 30d
ꢀꢀ
270g
[0097]
柠檬酸三乙酯
ꢀꢀ
170g
[0098]
二甲基硅油乳液
ꢀꢀ
2g
[0099]
滑石粉 45g
[0100]
纯化水 483g;
[0101]
制备方法参考实施例1,其中包衣增重为10%。
[0102]
实施例4
[0103]
含药片芯:
[0104]
利鲁唑 200g
[0105]
淀粉
ꢀꢀ
350g
[0106]
交联pvp
ꢀꢀ
50g
[0107]
微粉硅胶
ꢀꢀ
5g
[0108]
氢化植物油
ꢀꢀ
10g
[0109]
羟丙甲纤维素 385g;
[0110]
缓释包衣层:
[0111]
eudragit rl 30d
ꢀꢀ
70g
[0112]
eudragit rs 30d
ꢀꢀ
240g
[0113]
柠檬酸三乙酯
ꢀꢀ
150g
[0114]
二甲基硅油乳液
ꢀꢀ
3g
[0115]
滑石粉 50g
[0116]
纯化水 487;
[0117]
制备方法参考实施例1,其中包衣增重为5%。
[0118]
实施例5
[0119]
含药片芯:
[0120]
利鲁唑 400g
[0121]
甘露醇 415g
[0122]
干淀粉 20g
[0123]
微粉硅胶 10g
[0124]
硬脂富马酸钠 5g
[0125]
卡波姆树脂
ꢀꢀ
150g;
[0126]
缓释包衣层:
[0127]
eudragit rl 30d
ꢀꢀ
20g
[0128]
eudragit rs 30d
ꢀꢀ
300g
[0129]
柠檬酸三乙酯
ꢀꢀ
198g
[0130]
二甲基硅油乳液
ꢀꢀ
2g
[0131]
滑石粉 30g
[0132]
纯化水 450g;
[0133]
制备方法参考实施例1,其中包衣增重为10%。
[0134]
实施例6
[0135]
含药片芯:
[0136]
利鲁唑 214g
[0137]
预胶化淀粉
ꢀꢀ
350g
[0138]
羧甲基淀粉钠
ꢀꢀ
20g
[0139]
二氧化硅
ꢀꢀ
8g
[0140]
微粉硅胶
ꢀꢀ
8g
[0141]
羧甲基纤维素钠
ꢀꢀ
400g;
[0142]
缓释包衣层:
[0143]
eudragit rl 30d
ꢀꢀ
53g
[0144]
eudragit rs 30d
ꢀꢀ
200g
[0145]
柠檬酸三乙酯
ꢀꢀ
200g
[0146]
二甲基硅油乳液
ꢀꢀ
2g
[0147]
滑石粉 45g
[0148]
纯化水 500g;
[0149]
制备方法参考实施例1,其中包衣增重为15%。
[0150]
实施例7
[0151]
含药片芯:
[0152]
利鲁唑 310.00g
[0153]
无水磷酸氢钙 500.00g
[0154]
低取代羟丙基纤维素
ꢀꢀ
24.00g
[0155]
二氧化硅
ꢀꢀ
8.00g
[0156]
硬脂酸镁
ꢀꢀ
8.00g
[0157]
海藻酸钠
ꢀꢀ
150.00g;
[0158]
缓释包衣层:
[0159]
eudragit rl 30d
ꢀꢀ
30g
[0160]
eudragit rs 30d
ꢀꢀ
270g
[0161]
柠檬酸三乙酯
ꢀꢀ
170g
[0162]
二甲基硅油乳液
ꢀꢀ
2g
[0163]
滑石粉 45g
[0164]
纯化水 483g;
[0165]
制备方法参考实施例1,其中包衣增重为10%。
[0166]
对比实施例1
[0167]
利鲁唑 320g
[0168]
微晶纤维素 256g
[0169]
乳糖
ꢀꢀ
144g
[0170]
低取代羟丙基纤维素
ꢀꢀ
24g
[0171]
二氧化硅
ꢀꢀ
8g
[0172]
硬脂酸镁
ꢀꢀ
8g
[0173]
羟乙基纤维素
ꢀꢀ
240g;
[0174]
取处方量的利鲁唑、微晶纤维素、乳糖混合均匀,再加入处方量的低取代羟丙纤维素、羟乙纤维素、微粉硅胶混合均匀,最后加入处方量的硬脂酸镁混合均匀,压片,即得利鲁唑缓释片。
[0175]
对比实施例2
[0176]
利鲁唑 320g
[0177]
微晶纤维素 256g
[0178]
乳糖
ꢀꢀ
144g
[0179]
低取代羟丙基纤维素
ꢀꢀ
24g
[0180]
二氧化硅
ꢀꢀ
8g
[0181]
硬脂酸镁
ꢀꢀ
8g;
[0182]
缓释包衣层:
[0183]
eudragit rl 30d
ꢀꢀ
30g
[0184]
eudragit rs 30d
ꢀꢀ
270g
[0185]
柠檬酸三乙酯
ꢀꢀ
170g
[0186]
二甲基硅油乳液
ꢀꢀ
2g
[0187]
滑石粉 45g
[0188]
纯化水 483g;
[0189]
取处方量的利鲁唑、微晶纤维素、乳糖混合均匀,再加入处方量的低取代羟丙纤维素、微粉硅胶混合均匀,最后加入处方量的硬脂酸镁混合均匀,压片机制得素片,备用;
[0190]
取处方量的eudragit rl 30d、eudragit rs 30d、滑石粉、柠檬酸三乙酯加入水中,匀浆机匀化,过滤,加入处方量二甲基硅油消泡,得包衣液,备用。
[0191]
将上述所得素片在包衣锅中以上述所得包衣液进行包衣(包衣增重为10%),即得利鲁唑缓释片。
[0192]
释放度检测
[0193]
释放度照溶出度与释放度测定法(中国药典2015年版四部通则0931第二法)测定。
[0194]
将实施例1-7、对比实施例1-2所得利鲁唑缓释片分别以0.1mol/l的盐酸溶液900ml为溶出介质,转速每分钟50转,依法操作,经1小时、2小时、4小时、6小时、8小时、10小时、12小时时分别取样10ml。滤过,并及时在操作容器中补充相同温度的溶出介质10ml,精密量取续滤液5ml,置100ml量瓶中,用0.1mol/l的盐酸溶液稀释至刻度,分别作为供试品溶液;取利鲁唑对照品适量,精密称定,加0.1mol/l盐酸溶液溶解并定量稀释制成每1ml中约含10μg的溶液,作为对照品溶液。分别取供试品溶液和对照品溶液,照紫外-可见分光光度法(中国药典2015年版四部通则0401),在254nm的波长处分别测定吸收度,计算每片在不同时间的释放量。测试结果如表1所示。
[0195]
由实验结果可知,本发明所制备的利鲁唑缓释片在14h内平稳释放,可有效避免突释现象。
[0196]
表1利鲁唑缓释片体外累积释放度(%)
[0197]
时间(h)12468101214实施例12634435264748796
实施例22936466069818896实施例32329394862718593实施例43547556580869297实施例53350596780869095实施例63645536576859198实施例73948566678839095对比实施例15672869595959595对比实施例24960728394949494
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1