一种改善氧化微环境的ROS响应性仿生纳米粒及制备方法
一种改善氧化微环境的ros响应性仿生纳米粒及制备方法
技术领域
1.本发明涉及一种改善氧化微环境的ros响应性仿生纳米粒及制备方法,属于生物医学、纳米医学领域。
背景技术:
2.活性氧(ros)调节细胞内稳态,并作为细胞功能障碍的主要调节剂参与疾病的病理生理学。与炎症信号和代谢功能障碍相关的疾病,如动脉粥样硬化、缺血性疾病、糖尿病、炎症性疾病,与氧化还原平衡改变有关。ros作为炎症信号的中枢调节器,特别是在nf
‑
κb活化和炎症体信号传导方面有调节作用。典型的nf
‑
κb信号转导与胰岛素抵抗、肥胖和动脉粥样硬化有关。
3.动物研究明确表明ros是心血管疾病治疗干预的一个可行靶点。然而,临床试验的结果并不理想。大多数抗氧化剂试验都是用各种维生素(a、c和e)进行的。现有技术存在抗氧化剂ros响应性灵敏度低的局限性,也无法通过组织抗氧化有效清除ros。
4.普罗布考、他汀类等药物,具有降血脂、抗氧化和抗炎作用。但这些药物很难被吸收,生物利用度小于10%。因此,无法产生明显的疗效,其临床应用也非常有限。
技术实现要素:
5.本发明的目的是克服现有技术的不足,提供一种改善氧化微环境的ros响应性仿生纳米粒。
6.本发明的第二个目的是提供一种改善氧化微环境的ros响应性仿生纳米粒的制备方法。
7.本发明的技术方案概述如下:
8.一种改善氧化微环境的ros响应性仿生纳米粒的制备方法,包括如下步骤:
9.(1)将细胞浸于低渗溶液中10
‑
60min,离心,用低渗溶液洗涤3
‑
6次,去除细胞内容物,冰浴条件下10%
‑
30%剪切率超声探头超声5
‑
30min,冻干,得到纳米级细胞膜;
10.(2)按比例,将5
‑
50mg药物溶于0.1
‑
0.5ml第一种溶剂中,得到溶液一,将50
‑
300mg ros响应性的聚合物材料溶于1
‑
5ml第二种溶剂中,得到溶液二,在冰浴条件下10%
‑
30%剪切率超声探头超声3
‑
10min;在超声的同时,将溶液一滴加到溶液二中;
11.(3)按比例,在容器中加入10
‑
30ml质量浓度为0.1%
‑
5%的乳化剂水溶液,再加入5
‑
30mg步骤(1)获得的纳米级细胞膜,在冰浴条件下10%
‑
30%剪切率超声探头超声10
‑
20min;在超声的同时,滴入步骤(2)获得的液体;
12.(4)挥发溶剂,在15000
‑
30000rpm条件下,离心15
‑
40min,蒸馏水洗涤3
‑
6次并冷冻干燥,得到一种改善氧化微环境的ros响应性仿生纳米粒。
13.细胞优选红细胞、血小板、巨噬细胞、中性粒细胞、t细胞、b细胞或内皮细胞。
14.低渗溶液优选0.25
×
生理盐水或0.25
×
0.01m、ph=7.4的pbs。
15.药物优选普罗布考、阿托伐他汀、阿司匹林、二甲双胍或吲哚美辛,还可以选用其
它的与炎症信号和代谢功能障碍相关的疾病的治疗药物。
16.第一种溶剂为二氯甲烷、丙酮、二甲基亚砜、乙酸乙酯、水、乙醇和甲醇中至少一种。
17.第二种溶剂为二氯甲烷、丙酮、二甲基甲酰胺、二甲基亚砜、四氢呋喃和乙酸乙酯中至少一种。
18.乳化剂为聚乙烯醇、聚氧乙烯醚、聚氧丙烯醚、环氧乙烷和环氧丙烷嵌段共聚物、十二烷基硫酸钠、十二烷基苯磺酸钠或磷酸钠。
19.上述制备方法制备的改善氧化微环境的ros响应性仿生纳米粒。
20.本发明的优点:
21.本发明一种改善氧化微环境的ros响应性仿生纳米粒的制备方法简单,成本低。与现有技术比它可以提高ros响应灵敏度,降低ros水平,抑制炎症反应,从而改善病理微环境。相比游离药物,本发明的纳米粒能被巨噬细胞更多地吞噬,且减少细胞内过量的ros及炎症因子表达。一种改善氧化微环境的ros响应性仿生纳米粒还提高了药物的生物利用度。同时在动物实验水平证明了纳米粒相比游离药物有更好的疾病治疗效果,显示了其增效作用。
附图说明
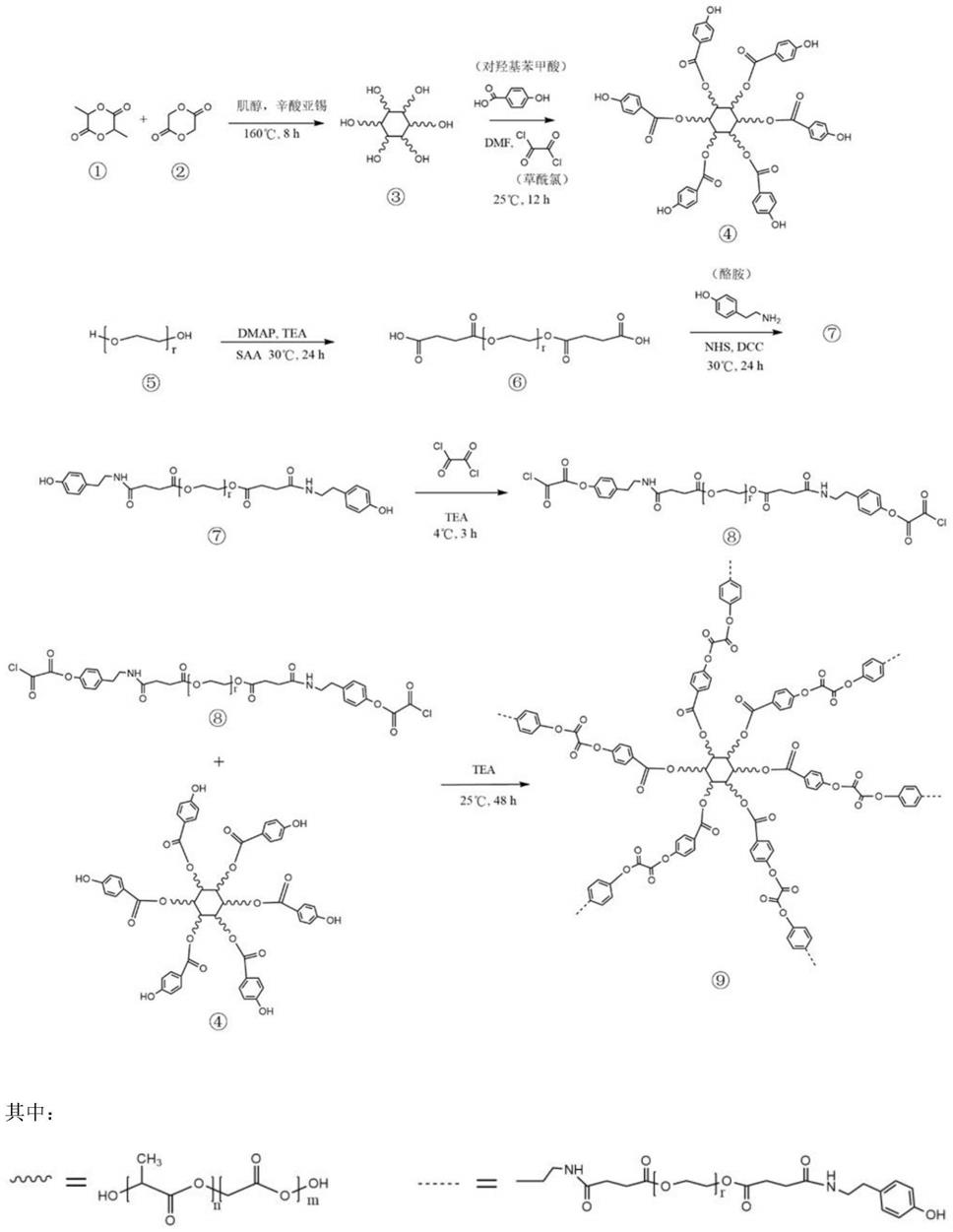
22.图1为ros响应性的聚合物材料合成路线图。
23.图2a为6s
‑
plga红外光谱图;图2b是6s
‑
plga
‑
ph
‑
po
‑
ph
‑
peg红外光谱图。
24.图3为ros响应性的聚合物材料核磁共振光谱表征图。图3a为6s
‑
plga氢谱图;图3b为6s
‑
plga
‑
ph
‑
po
‑
ph
‑
peg氢谱图;图3c为图3b的不同化学位移的放大图。
25.图4为ros响应性的聚合物材料dsc结果图。
26.图5为一种改善氧化微环境的ros响应性仿生纳米粒粒理化性质表征图。其中图5a为纳米粒14天多分散系数变化;图5b为纳米粒14天粒径变化;图5c为纳米粒14天电位变化;
27.图6为一种改善氧化微环境的ros响应性仿生纳米粒过氧化氢响应实验结果图。其中图6a为纳米粒的透射电镜图(左图为在pbs溶液(ph7.4,0.01m)中纳米粒形态;右图为在10μm过氧化氢溶液中纳米粒形态);图6b为2h纳米粒对10μm过氧化氢溶液的清除作用;图6c为纳米粒在pbs(ph7.4,0.01m)及10μm过氧化氢溶液中释放的释放曲线;
28.图7为一种改善氧化微环境的ros响应性仿生纳米粒对细胞的ros清除作用。其中图7a为纳米粒对细胞的ros清除作用共聚焦代表图片;图7b为纳米粒对细胞的ros清除作用的定量图;
29.图8为一种改善氧化微环境的ros响应性仿生纳米粒在巨噬细胞中的吞噬图。其中图8a为纳米粒在细胞吞噬的共聚焦代表图片;图8b为纳米粒在细胞吞噬的的定量图;
30.图9为一种改善氧化微环境的ros响应性仿生纳米粒细胞抗炎作用图。图中图9a为纳米粒对il
‑
1β作用图;图9b为纳米粒对il
‑
6作用图;图9c为纳米粒对tnf
‑
α作用图;
31.图10为一种改善氧化微环境的ros响应性仿生纳米粒对apoe
‑
/
‑
小鼠治疗12周后,血脂水平评价。图中图10a为纳米粒对hdl水平变化的作用图;图10b为纳米粒对ldl水平变化的作用图;图10c为纳米粒对tc水平变化的作用图;图10d为纳米粒对tg水平变化的作用图;
32.图11为一种改善氧化微环境的ros响应性仿生纳米粒对apoe
‑
/
‑
小鼠治疗12周后,腹主动脉油红o染色图。其中图11a为腹主动脉油红o染色代表性血管图;图11b为腹主动脉油红o染色定量图;
33.各图中control代表阴性对照组;peg代表聚乙二醇4000;plga
‑
peg代表ros响应性的聚合物材料空白纳米粒;rpp代表空白ros响应性仿生纳米粒;pu代表游离普罗布考;rpp
‑
pu代表一种改善氧化微环境的ros响应性仿生纳米粒(其中包载的药物为普罗布考)
34.h2o2代表10μm过氧化氢溶液,溶剂为ph=7.4,0.01m pbs;lps代表脂多糖;cou
‑
6代表香豆素6;rpp
‑
cou
‑
6代表包载cou
‑
6的ros响应性仿生纳米粒(制备方法同实施例5)
具体实施方式
35.细胞的获得:细胞来源于灵长类动物、猪、大小鼠、豚鼠、狗、兔等哺乳动物。
36.下面通过具体实施例对本发明作进一步的说明。
37.一种ros响应性的聚合物材料的制备方法,包括如下步骤:
38.(1)聚酯类单体在引发剂和催化剂的作用下,通过聚合得到平均分子量8000
‑
100000的聚酯;
39.(2)以步骤(1)获得的聚酯为原料制备聚酯
‑
ar
‑
oh;用平均分子量2000
‑
6000的peg合成peg
‑
ar
‑
oh,
40.(3)通过peg
‑
ar
‑
oh与过量草酰氯反应得到peg
‑
ar
‑
ocococl;
41.(4)过量的peg
‑
ar
‑
ocococl与聚酯
‑
ar
‑
oh反应,得到ros响应性的聚合物材料;
42.所述ar为苯环(ph)或通过酯键连接的双苯环(ph
‑
coo
‑
ph)。
43.所述聚酯类单体、引发剂和催化剂的摩尔比为(6000
‑
100000):(50
‑
200):1。
44.聚酯类单体为乙交酯、丙交酯、羟基乙酸、羟基丙酸、羟基丁酸、丁二酸、丁二醇、戊内酯和己内酯中至少一种。
45.引发剂为乙二醇,丙二醇,丁二醇,三羟甲基乙烷,丙三醇,季戊四醇,丁四醇,戊五醇,环戊五醇或肌醇。
46.催化剂为辛酸亚锡,异辛酸亚锡,氢氧化铝,异丙醇铝,醋酸锌。
47.上述方法制备的一种ros响应性的聚合物材料。
48.实施例1
49.一种ros响应性的聚合物材料的制备方法(见图1),包括如下步骤:
50.(1)将聚酯类单体(摩尔比为3:1的丙交酯
①
和乙交酯
②
)、引发剂肌醇和催化剂辛酸亚锡,混合于聚合管,重复抽真空将聚合管密封后,先用加热套加热至250℃使肌醇熔化,然后置于160℃烘箱中聚合反应8h,得到平均分子量8000的聚乳酸聚乙醇酸(6s
‑
plga
③
),对粗产物进行纯化、重沉淀3次,真空干燥至恒重;
51.上述聚酯类单体、引发剂和催化剂的摩尔比为6000:50:1;
52.(2)以步骤(1)获得的6s
‑
plga为原料制备6s
‑
plga
‑
ph
‑
oh
④
;用平均分子量4000的peg
⑤
合成peg
‑
ph
‑
oh
⑦
。
53.将2mmol对羟基苯甲酸和2mmol n,n
‑
二甲基甲酰胺(dmf)溶解在10ml四氢呋喃(thf)中,得到溶液一;将2mmol草酰氯溶解于10mlthf中,滴入溶液一中;加入0.2mmol 6s
‑
plga
③
和1mmol三乙胺(tea),室温搅拌12h;对粗产物进行纯化、重沉淀3次后真空干燥至恒
重;得到6s
‑
plga
‑
ph
‑
oh
④
;
54.将5mmol平均分子量4000peg
⑤
加入到20ml二氧六环中溶解,得到溶液二;将12.5mmol 4
‑
二甲基氨基吡啶(dmap)和12.5mmol tea溶解于20ml二氧六环中,逐滴加入到溶液二中得到溶液三,反应15min后,将溶有12.5mmol丁二酸酐(ssa)的二氧六环溶液20ml滴加到溶液三中,30℃反应24h;反应结束后重沉淀3次,于真空烘箱中室温干燥至恒重,得到peg
‑
cooh
⑥
;将3.75mmol peg
‑
cooh在30℃下溶解于20ml thf中,然后添加10mmol二环己基碳二亚胺(dcc)和10mmol n
‑
羟基琥珀酰亚胺(nhs)反应30min,最后添加10mmol酪胺(ta)反应24h,经过反复沉淀3次后真空干燥至恒重,得到peg
‑
ph
‑
oh
⑦
;
55.(3)通过peg
‑
ph
‑
oh与过量草酰氯反应得到peg
‑
ph
‑
ocococl
⑧
:
56.量取20ml ch2cl2,加入8mmol草酰氯搅拌,得草酰氯溶液,将1mmol peg
‑
ph
‑
oh和1mmol tea溶解于20mlch2cl2中,滴加到草酰氯溶液中,4℃搅拌3h,反应完成后,通过旋转蒸发除去杂质,干燥后留下固体物质,即peg
‑
ph
‑
ocococl。
57.(4)过量的peg
‑
ph
‑
ocococl与6s
‑
plga
‑
ph
‑
oh反应制备ros响应性的聚合物材料6s
‑
plga
‑
ph
‑
po
‑
ph
‑
peg:(其中po为
‑
ococoo
‑
)
58.将1mmol peg
‑
ph
‑
ocococl溶解于20ml ch2cl2与1mmol tea均匀混合,得到溶液四;
59.将0.1mmol 6s
‑
plga
‑
ph
‑
oh溶于20mlch2cl2中,滴入溶液四中,室温搅拌反应48h,纯化重沉淀3次,真空干燥至恒重得到6s
‑
plga
‑
ph
‑
po
‑
ph
‑
peg
⑨
。
60.图1结构分子式中m=5,n=15,r=90;
61.本实施例采用红外光谱法测定了6s
‑
plga
‑
ph
‑
po
‑
ph
‑
peg主要官能团(图2b),并与6s
‑
plga(图2a)进行了比较。2998cm
‑1和2948cm
‑1处的峰为饱和ch键的特征峰,1756cm
‑1处的峰对应c=o官能团。peg改性后,peg中亚甲基的拉伸振动吸收峰出现在2884cm
‑1处。苯环c=c的伸缩振动吸收峰出现在1561cm
‑1处。表明苯环连接成功。以上结果表明,peg
‑
ph
‑
oh与6s
‑
plga
‑
ph
‑
oh成功结合。
62.核磁共振氢谱法(1h
‑
nmr)核磁测定了材料组成。如图3a所示a峰对应于plga段的ch3基团,其比例与相应氢原子的比例相同。ch2和ch分别表示为b峰和c峰。如图3b所示,d峰表明peg中ch2基团。如图3c所示,e、f、g、h峰结果表明酰胺和苯环的存在。peg与聚酯类聚合物连接成功。
63.用差示扫描量热法(dsc)测定了6s
‑
plga和6s
‑
plga
‑
ph
‑
po
‑
ph
‑
peg玻璃化转变温度。dsc曲线如图4所示,随着peg链的加入,plga共聚物的结构变得更加复杂。
64.实施例2
65.一种ros响应性的聚合物材料的制备方法,包括如下步骤:
66.(1)将聚酯类单体羟基乙酸、引发剂乙二醇和催化剂异辛酸亚锡,混合于聚合管,重复抽真空将聚合管密封后,置于150℃烘箱中反应6h,得到平均分子量20000的聚羟基乙酸(pga),对粗产物进行纯化、重沉淀3次,真空干燥至恒重;
67.聚酯类单体、引发剂和催化剂的摩尔比为34500:100:1;
68.(2)以步骤(1)获得的pga为原料制备pga
‑
ph
‑
coo
‑
ph
‑
oh;用平均分子量2000的peg合成peg
‑
ph
‑
oh。
69.将8mmol对羟基苯甲酸和8mmol dmf溶解在20mlthf中,得到溶液一;将8mmol草酰氯溶解于20mlthf中,滴入溶液一中;加入0.8mmol pga和2mmol三乙胺,室温搅拌8h;对粗产
物进行纯化、重沉淀3次后真空干燥至恒重;得到pga
‑
ph
‑
oh;再将8mmol草酰氯溶解于20ml thf中,滴入新制备的溶液一中;加入0.6mmol pga
‑
ph
‑
oh和2mmol三乙胺,室温搅拌8h;对粗产物进行纯化、重沉淀3次后真空干燥至恒重,得到pga
‑
ph
‑
coo
‑
ph
‑
oh;
70.将8mmol平均分子量2000peg加入到30ml二氧六环中溶解,得到溶液二;将30mmol dmap和30mmol tea溶解于30ml二氧六环中,逐滴加入到溶液二中得到溶液三,反应30min后,将溶有30mmol丁二酸酐的二氧六环溶液30ml滴加到溶液三中,30℃反应24h;反应结束后重沉淀3次,于真空烘箱中室温干燥至恒重,得到peg
‑
cooh;将6mmol peg
‑
cooh在30℃下溶解于30ml thf中;然后添加20mmol dcc和20mmol nhs反应30min;最后添加20mmol酪胺反应24h,经过反复沉淀3次后真空干燥至恒重,得到peg
‑
ph
‑
oh;
71.(3)通过peg
‑
ph
‑
oh与过量草酰氯反应得到peg
‑
ph
‑
ocococl:
72.量取20ml ch2cl2,加入20mmol草酰氯搅拌,得草酰氯溶液;将5mmol peg
‑
ph
‑
oh和5mmol tea溶解于20ml ch2cl2中,滴加到草酰氯溶液中,4℃持续搅拌5h;反应完成后,通过旋转蒸发除去杂质,干燥后留下固体物质,即peg
‑
ph
‑
ocococl。
73.(4)过量的peg
‑
ph
‑
ocococl与pga
‑
ph
‑
coo
‑
ph
‑
oh反应制备ros响应性的聚合物材料pga
‑
ph
‑
coo
‑
ph
‑
po
‑
ph
‑
peg:(其中po为
‑
ococoo
‑
)
74.将4mmol peg
‑
ph
‑
ocococl溶解于20ml ch2cl2与4mmol tea均匀混合,得到溶液四;
75.将0.4mmol pga
‑
ph
‑
coo
‑
ph
‑
oh溶于20mlch2cl2中,滴入溶液四中,室温搅拌反应48h,纯化重沉淀3次,真空干燥至恒重得到pga
‑
ph
‑
coo
‑
ph
‑
po
‑
ph
‑
peg。
76.实施例3
77.一种ros响应性的聚合物材料的制备方法,包括如下步骤:
78.(1)将聚酯类单体(摩尔比为1:1的丁二酸和丁二醇)、引发剂丙三醇和催化剂氢氧化铝,混合于聚合管,重复抽真空将聚合管密封后,置于200℃烘箱中反应12h,得到平均分子量50000的聚丁二酸丁二醇酯(3s
‑
pbs);对粗产物进行纯化、重沉淀3次,真空干燥至恒重;
79.聚酯类单体、引发剂和催化剂的摩尔比为63000:200:1;
80.(2)以步骤(1)获得的3s
‑
pbs为原料制备3s
‑
pbs
‑
ph
‑
oh;用平均分子量5000的peg合成peg
‑
ph
‑
coo
‑
ph
‑
oh。
81.将30mmol对羟基苯甲酸和30mmol dmf溶解在50ml thf中,得到溶液一;将30mmol草酰氯溶解于50ml thf中,滴入溶液一中;加入4mmol 3s
‑
pbs和8mmol三乙胺,室温搅拌24h;对粗产物进行纯化、重沉淀3次后真空干燥至恒重;得到3s
‑
pbs
‑
ph
‑
oh。
82.将40mmol平均分子量5000peg加入到50ml二氧六环中溶解,得到溶液二;将100mmol dmap和100mmol tea溶解于50ml二氧六环中,逐滴加入到溶液二中得到溶液三,反应1h后,将溶有100mmol丁二酸酐的二氧六环溶液50ml滴加到溶液三中,30℃反应24h;反应结束后重沉淀3次,于真空烘箱中室温干燥至恒重,得到peg
‑
cooh;将30mmol peg
‑
cooh在30℃下溶解于50ml thf中;然后添加80mmol dcc和80mmol nhs反应30min;最后添加80mmol酪胺(ta)反应48h;经过反复沉淀3次后真空干燥至恒重,得到peg
‑
ph
‑
oh。
83.将80mmol对羟基苯甲酸和80mmol dmf溶解在50ml thf中,得到溶液一;将80mmol草酰氯溶解于50ml thf中,滴入溶液一中;加入25mmol peg
‑
ph
‑
oh和40mmol三乙胺,室温搅拌24h;对粗产物进行纯化、重沉淀3次后真空干燥至恒重;得到peg
‑
ph
‑
coo
‑
ph
‑
oh。
84.(3)通过peg
‑
ph
‑
coo
‑
ph
‑
oh与过量草酰氯反应得到peg
‑
ph
‑
coo
‑
ph
‑
ocococl:
85.量取50ml ch2cl2,加入80mmol草酰氯搅拌,将25mmol peg
‑
ph
‑
coo
‑
ph
‑
oh和25mmol tea溶解于50ml ch2cl2中,滴加到草酰氯溶液中,4℃持续搅拌12h。反应完成后,通过旋转蒸发除去杂质,干燥后留下固体物质,即peg
‑
ph
‑
coo
‑
ph
‑
ocococl。
86.(4)过量的peg
‑
ph
‑
coo
‑
ph
‑
ocococl与3s
‑
pbs
‑
ph
‑
oh反应制备ros响应性的聚合物材料3s
‑
pbs
‑
ph
‑
po
‑
ph
‑
coo
‑
ph
‑
peg:(其中po为
‑
ococoo
‑
)
87.将20mmol peg
‑
ph
‑
coo
‑
ph
‑
ocococl溶解于50ml ch2cl2与tea均匀混合,得到溶液四;
88.2mmol 3s
‑
pbs
‑
ph
‑
oh溶于20mlch2cl2中,滴入溶液四中,室温搅拌反应72h,纯化重沉淀3次,真空干燥至恒重得到3s
‑
pbs
‑
ph
‑
po
‑
ph
‑
coo
‑
ph
‑
peg。
89.实施例4
90.一种ros响应性的聚合物材料的制备方法,包括如下步骤:
91.(1)将聚酯类单体己内酯、引发剂丁四醇和催化剂醋酸锌,混合于聚合管,重复抽真空将聚合管密封后,置于220℃烘箱中反应16h,得到平均分子量100000的聚己内酯(4s
‑
pcl),对粗产物进行纯化、重沉淀3次,真空干燥至恒重;
92.聚酯类单体、引发剂和催化剂的摩尔比为100000:120:1;
93.(2)以步骤(1)获得的4s
‑
pcl为原料制备4s
‑
pcl
‑
ph
‑
coo
‑
ph
‑
oh;用平均分子量6000的peg合成peg
‑
ph
‑
coo
‑
ph
‑
oh。
94.将60mmol对羟基苯甲酸和60mmol dmf溶解在100ml thf中,得到溶液一;将60mmol草酰氯溶解于100ml thf中,滴入溶液一中;加入8mmol 4s
‑
pcl和20mmol三乙胺,室温搅拌36h;对粗产物进行纯化、重沉淀3次后真空干燥至恒重,得到4s
‑
pcl
‑
ph
‑
oh;再将60mmol草酰氯溶解于100ml thf中,滴入新制备的溶液一中;加入6mmol 4s
‑
pcl
‑
ph
‑
oh和12mmol三乙胺,室温搅拌12h;对粗产物进行纯化、重沉淀3次后真空干燥至恒重;得到4s
‑
pcl
‑
ph
‑
coo
‑
ph
‑
oh;
95.将80mmol平均分子量6000peg加入到100ml二氧六环中溶解,得到溶液二;将200mmol dmap和200mmol tea溶解于100ml二氧六环中,逐滴加入到溶液二中得到溶液三,反应2h后,将溶有200mmol丁二酸酐的二氧六环溶液100ml滴加到溶液三中,30℃反应24h;反应结束后重沉淀3次,于真空烘箱中室温干燥至恒重,得到peg
‑
cooh。将60mmol peg
‑
cooh在30℃下溶解于100ml thf中。然后添加200mmol dcc和200mmol nhs反应30min;最后添加150mmol酪胺(ta)反应48h。经过反复沉淀3次后真空干燥至恒重,得到peg
‑
ph
‑
oh。
96.将100mmol对羟基苯甲酸和100mmol dmf溶解在100ml thf中,得到溶液一;将100mmol草酰氯溶解于100ml thf中,滴入溶液一中;加入55mmol peg
‑
ph
‑
oh和70mmol三乙胺,室温搅拌24h;对粗产物进行纯化、重沉淀3次后真空干燥至恒重;得到peg
‑
ph
‑
coo
‑
ph
‑
oh。
97.(3)通过peg
‑
ph
‑
coo
‑
ph
‑
oh与过量草酰氯反应得到peg
‑
ph
‑
coo
‑
ph
‑
ocococl:
98.量取100ml ch2cl2,加入160mmol草酰氯搅拌,得草酰氯溶液;将50mmol peg
‑
ph
‑
coo
‑
ph
‑
oh和50mmol tea溶解于100ml ch2cl2中,滴加到草酰氯溶液中,4℃搅拌24h。反应完成后,通过旋转蒸发除去杂质,干燥后留下固体物质,即peg
‑
ph
‑
coo
‑
ph
‑
ocococl。
99.(4)过量的peg
‑
ph
‑
coo
‑
ph
‑
ocococl与4s
‑
pcl
‑
ph
‑
coo
‑
ph
‑
oh反应制备ros响应性
的聚合物材料4s
‑
pcl
‑
ph
‑
coo
‑
ph
‑
po
‑
ph
‑
coo
‑
ph
‑
peg:
100.将40mmol peg
‑
ph
‑
coo
‑
ph
‑
ocococl溶解于80ml ch2cl2与40mmol tea均匀混合,得到溶液四;
101.4mmol 4s
‑
pcl
‑
ph
‑
coo
‑
ph
‑
oh溶于40mlch2cl2中,滴入溶液四中,搅拌反应100h,纯化重沉淀3次,真空干燥至恒重得到4s
‑
pcl
‑
ph
‑
coo
‑
ph
‑
po
‑
ph
‑
coo
‑
ph
‑
peg。
102.用羟基丙酸、羟基丁酸、或戊内酯替代本实施例中的己内酯,其它同本实施例,分别制备出相应的ros响应性的聚合物材料。
103.用丙二醇,丁二醇,三羟甲基乙烷,季戊四醇,戊五醇或环戊五醇替代本实施例的丁四醇,其它同本实施例,分别制备出相应的ros响应性的聚合物材料。
104.用异丙醇铝替代本实施例的醋酸锌,其它同本实施例,制备出相应的ros响应性的聚合物材料。
105.实施例5
106.一种改善氧化微环境的ros响应性仿生纳米粒的制备方法,包括如下步骤:
107.(1)将c57bl/6j(6周)小鼠眼球取血,血液离心得到红细胞,浸于低渗溶液(0.25
×
0.01m、ph=7.4的pbs)中30min,离心,用低渗溶液洗涤3次,去除细胞内容物,冰浴条件下20%剪切率超声探头超声20min,冻干,得到纳米级红细胞膜;
108.(2)将30mg普罗布考溶于0.3ml第一种溶剂(二氯甲烷)中,得到溶液一,将100mg ros响应性的聚合物材料(实施例1制备)溶于2ml第二种溶剂(体积比为3:1的二氯甲烷和丙酮的混合溶剂)中,得到溶液二,在冰浴条件下20%剪切率超声探头超声5min;在超声的同时,将溶液一滴加到溶液二中;
109.(3)在容器中加入20ml质量浓度为0.5%的乳化剂水溶液(乳化剂为:平均分子量30000
‑
70000聚乙烯醇),再加入20mg步骤(1)获得的纳米级红细胞膜,在冰浴条件下20%剪切率超声探头超声10min;在超声的同时,滴入步骤(2)获得的液体;
110.(4)挥发溶剂,在23000rpm条件下,离心30min,蒸馏水洗涤4次并冷冻干燥,得到一种改善氧化微环境的ros响应性仿生纳米粒。
111.本实施例制备的改善氧化微环境的ros响应性仿生纳米粒,简称rpp
‑
pu。
112.采用动态光散射法(dls)测定了改善氧化微环境的ros响应性仿生纳米粒的平均粒径和分布。rpp
‑
pu的平均粒径为100nm
‑
300nm,rpp
‑
pu的多分散系数(pdi)为0.1
‑
0.3。rpp
‑
pu的表面电荷为(
‑
10)mv
‑
(
‑
15)mv。
113.稳定性试验通过将2mg rpp
‑
pu溶解在2ml无菌水中并储存在4℃下进行。14天内rpp
‑
pu的粒径和分布没有明显变化(图5)。表面电荷数的少量减少可能会提高纳米粒子的稳定性,多分散系数(pdi)有降低的趋势。结果表明,rpp
‑
pu具有很强的稳定性。
114.采用高效液相色谱法(hplc)测定rpp
‑
pu中普罗布考的浓度。计算rpp
‑
pu的包封率和载药量。rpp
‑
pu的包封率高达97.9
±
0.15%。rpp
‑
pu的载药量为29.8
±
0.59%。
115.实施例6
116.一种改善氧化微环境的ros响应性仿生纳米粒的制备方法,包括如下步骤:
117.(1)将家兔(10周)的巨噬细胞浸于低渗溶液(0.25
×
0.01m、ph=7.4的pbs)中20min,离心,用低渗溶液洗涤6次,去除细胞内容物,冰浴条件下30%剪切率超声探头超声5min,冻干,得到纳米级细胞膜;
118.(2)将5mg阿托伐他汀溶于0.1ml第一种溶剂(甲醇)中,得到溶液一,将50mg ros响应性的聚合物材料(实施例2制备的)溶于1ml第二种溶剂(四氢呋喃)中,得到溶液二,在冰浴条件下10%剪切率超声探头超声10min;在超声的同时,将溶液一滴加到溶液二中;
119.(3)在容器中加入10ml质量浓度为0.1%的乳化剂(乳化剂为:平均分子量10000
‑
30000聚氧乙烯醚)水溶液,再加入5mg步骤(1)获得的纳米级细胞膜,在冰浴条件下10%剪切率超声探头超声20min;在超声的同时,滴入步骤(2)获得的液体;
120.(4)挥发溶剂,在15000rpm条件下,离心40min,蒸馏水洗涤3次并冷冻干燥,得到一种改善氧化微环境的ros响应性仿生纳米粒。
121.实施例7
122.一种改善氧化微环境的ros响应性仿生纳米粒的制备方法,包括如下步骤:
123.(1)将c57bl/6j(6周)小鼠眼球取血,分离得到血小板,浸于低渗溶液(0.25
×
生理盐水)中10min,离心,用低渗溶液洗涤3次,去除细胞内容物,冰浴条件下10%剪切率超声探头超声30min,冻干,得到纳米级细胞膜;
124.(2)将50mg阿司匹林溶于0.5ml第一种溶剂(乙醇)中,得到溶液一,将300mg ros响应性的聚合物材料(实施例3制备)溶于5ml第二种溶剂(二甲基甲酰胺)中,得到溶液二,在冰浴条件下30%剪切率超声探头超声3min;在超声的同时,将溶液一滴加到溶液二中;
125.(3)在容器中加入30ml质量浓度为5%的乳化剂(乳化剂为:平均分子量30000
‑
50000环氧乙烷和环氧丙烷嵌段共聚物)水溶液,再加入30mg步骤(1)获得的纳米级细胞膜,在冰浴条件下30%剪切率超声探头超声10min;在超声的同时,滴入步骤(2)获得的液体;
126.(4)挥发溶剂,在30000rpm条件下,离心15min,蒸馏水洗涤6次并冷冻干燥,得到一种改善氧化微环境的ros响应性仿生纳米粒。
127.实施例8
128.一种改善氧化微环境的ros响应性仿生纳米粒的制备方法,包括如下步骤:
129.(1)从新生比格犬的脐静脉获得内皮细胞,浸于低渗溶液(0.25
×
生理盐水)中60min,离心,用低渗溶液洗涤4次,去除细胞内容物,冰浴条件下20%剪切率超声探头超声20min,冻干,得到纳米级细胞膜;
130.(2)将30mg二甲双胍溶于0.3ml第一种溶剂(水)中,得到溶液一,将100mgros响应性的聚合物材料(实施例4制备)溶于3ml第二种溶剂(乙酸乙酯)中,得到溶液二,在冰浴条件下20%剪切率超声探头超声5min;在超声的同时,将溶液一滴加到溶液二中;
131.(3)在容器中加入20ml质量浓度为3%的乳化剂(乳化剂为:十二烷基硫酸钠)水溶液,再加入10mg步骤(1)获得的纳米级细胞膜,在冰浴条件下20%剪切率超声探头超声15min;在超声的同时,滴入步骤(2)获得的液体;
132.(4)挥发溶剂,在20000rpm条件下,离心20min,蒸馏水洗涤4次并冷冻干燥,得到一种改善氧化微环境的ros响应性仿生纳米粒。
133.实施例9
134.一种改善氧化微环境的ros响应性仿生纳米粒的制备方法,包括如下步骤:
135.用sd大鼠(8周)的中性粒细胞替代实施例8的内皮细胞、用吲哚美辛替代二甲双胍、用丙酮替代第一种溶剂水;用丙酮替代第二种溶剂乙酸乙酯;用平均分子量10000
‑
30000的聚氧丙烯醚替代十二烷基硫酸钠;其它同实施例8,制备出一种改善氧化微环境的
ros响应性仿生纳米粒。
136.实施例10
137.一种改善氧化微环境的ros响应性仿生纳米粒的制备方法,包括如下步骤:
138.用豚鼠(6周)的t细胞替代实施例8的内皮细胞、用普罗布考替代二甲双胍、用二甲基亚砜替代第一种溶剂水;用二甲基亚砜替代第二种溶剂乙酸乙酯;用十二烷基苯磺酸钠替代十二烷基硫酸钠;其它同实施例8,制备出一种改善氧化微环境的ros响应性仿生纳米粒。
139.实施例11
140.一种改善氧化微环境的ros响应性仿生纳米粒的制备方法,包括如下步骤:
141.用恒河猴(3岁)的b细胞替代实施例8的内皮细胞、用普罗布考替代二甲双胍、用体积比为1:1的二氯甲烷和乙酸乙酯的混合溶剂替代第一种溶剂水;用四氢呋喃替代第二种溶剂乙酸乙酯;用磷酸钠替代十二烷基硫酸钠,其它同实施例8,制备出一种改善氧化微环境的ros响应性仿生纳米粒。
142.实施例5
‑
11制备的一种改善氧化微环境的ros响应性仿生纳米粒的平均粒径、多分散系数和表面电荷与实施例5相似。
143.实施例12:一种改善氧化微环境的ros响应性仿生纳米粒(实施例5)过氧化氢清除作用及细胞实验(本实施例中所涉及的pbs,均为pbs(ph=7.4,0.01m);本实施例中所涉及的过氧化氢溶液的溶剂为pbs(ph=7.4,0.01m))
144.(1)改善氧化微环境的ros响应性仿生纳米粒(实施例5制备,简称rpp
‑
pu)体外过氧化氢清除作用
145.通过透射电镜(tem)观察pbs及10μm的过氧化氢溶液下rpp
‑
pu的形态。tem结果显示rpp
‑
pu粒径约为100
‑
300nm。可观察到rpp
‑
pu的红细胞膜包被的双层膜结构。rpp
‑
pu在pbs下呈球形,具有良好的分散性(图6a左)。在h2o2下,rpp
‑
pu的形态变得不规则,纳米粒的聚集是由于h2o2中过氧草酸酯键的断裂引起的(图6a右)。
146.rpp
‑
pu对于过氧化氢的响应能力测试主要通过amplex red过氧化氢检测试剂盒来测试过氧化氢的清除。首先,用浓度10μm的过氧化氢溶液悬浮rpp
‑
pu,制备浓度为2mg/ml的rpp
‑
pu悬浮体。在摇床中孵育2h后,检测过氧化氢的相对浓度。
147.rpp为空白ros响应性仿生纳米粒(制备方法同实施例5,不添加药物)。如图6b所示,peg溶液中的h2o2没有被消除。与peg相比,rpp和rpp
‑
pu具有更显著的h2o2去除能力。在rpp快速崩解的情况下,h2o2的去除率在前2h可达到70%以上。因此,我们验证了rpp对h2o2的响应性。
148.pbs及过氧化氢对纳米粒的影响体外释放实验测试步骤如下:
149.在两个离心管中分别放入24mg的rpp
‑
pu,再用4mlpbs混悬,放于37℃摇床中培养。于1h,3h,6h,10h,1d,2d,3d,5d,7d,9d,11d,15d,20d,25d,35d将离心管取出,离心后取出上清溶液2ml,然后加入2ml新鲜的pbs。在10h之后,将其中一组rpp
‑
pu所加入的pbs换为浓度为10μm的过氧化氢溶液,后续时间点都换入10μm的过氧化氢溶液,其他条件保持不变。rpp
‑
pu的累积药物释放曲线如图6c所示。第一天观察到超过15%的普罗布考释放,随后在pbs中缓慢且持续释放35天。结果表明,rpp
‑
pu在h2o2中的释放比pbs中的释放更快,这表明rpp
‑
pu对h2o2具有良好的响应性。
150.(2)改善氧化微环境的ros响应性仿生纳米粒对细胞过氧化氢清除作用
151.1μg lps刺激巨噬细胞30min产生ros,作为阳性对照。用细胞共培养法观察rpp及rpp
‑
pu对ros的影响,用2'7'
‑
二氯荧光素二乙酸(dcfh
‑
da)荧光探针检测细胞中ros含量。采用共聚焦激光扫描显微镜观察ros的定位和强度。结果表明,rpp和rpp
‑
pu培养后细胞的ros水平明显低于阳性对照组(图7)。
152.(3)改善氧化微环境的ros响应性仿生纳米粒在细胞中的吞噬作用
153.用香豆素
‑
6(cou
‑
6)替代实施例5的普罗布考,其它同实施例5,制备出ros响应性仿生纳米粒(rpp
‑
cou
‑
6)。
154.将巨噬细胞传代培养。在共聚焦培养皿中分别加入用dmem培养基稀释的cou
‑
6和rpp
‑
cou
‑
6。培养2h后,激光共聚焦显微镜观察纳米粒在细胞内的分布。如图8所示,与对照组相比,rpp
‑
cou6的香豆素摄取量增加了约6倍,表明纳米粒可以提高药物的生物利用度。
155.(4)改善氧化微环境的ros响应性仿生纳米粒的对细胞炎症因子表达的作用
156.巨噬细胞传代培养,调整细胞密度为5
×
104个/ml,以每孔100μl细胞悬浮液接种于96孔板,继续于细胞培养箱中培养24h。向孔板中分别加入每孔100μl用dmem培养基稀释的纳米粒rbc、rpp(rbc,实施例5步骤(1)获得)以及加入1μg的lps为阳性对照组,继续培养24h。上清液利用elisa方法测试il
‑
1β、il
‑
6及tnf
‑
α的表达。结果表明,相对于阳性对照组来说,rbc组及rpp组炎症因子的表达量很低,具有抗炎的作用(图9)。
157.实施例13:一种改善氧化微环境的ros响应性仿生纳米粒(实施例5制备的)对于apoe
‑
/
‑
动脉粥样硬化模型小鼠体内治疗评价
158.选用c57bl/6j雄性载脂蛋白e基因敲除(apoe
‑
/
‑
)鼠,高脂饲养12周,同时给药干预,剂量0.2ml(实施例5制备20mg/ml)一周腹腔注射三次。共注射12周,在13周,动物处死前采血,分离血清,冻存。检测以下指标:血清胆固醇(tc)、甘油三酯(tg)、低密度脂蛋白(ldl)、高密度脂蛋白(hdl)。检测结果,rpp
‑
pu可显著降低tc、tg、ldl水平,hdl与其它各组没有显著性差异(图10)。与游离普罗布考相比,rpp
‑
pu能更有效地降低血脂水平。且rpp不含药物的纳米粒也比对照组有降低脂质的趋势,可见材料本身也有对动脉粥样硬化改善的作用。
159.小鼠腹主动脉进行大体油红染色。定量分析结果显示,与对照组和游离普罗布考组相比,rpp
‑
pu组脂肪斑块面积较低,有显著性差异,有效地减少斑块面积(图11)。
160.实验证明:
161.实施例6
‑
11制备的改善氧化微环境的ros响应性仿生纳米粒在过氧化氢清除实验、细胞吞噬实验和细胞抗炎实验的效果与实施例5制备的改善氧化微环境的ros响应性仿生纳米粒的效果相似。
162.综上所述,本发明的一种改善氧化微环境的ros响应性仿生纳米粒在稳定性、消除ros作用、细胞吞噬作用和提高生物利用度方面都是令人满意的。改善氧化微环境的ros响应性仿生纳米粒相比于游离药物血脂明显降低,粥样硬化斑块面积减少,炎症水平降低。这种多功能仿生纳米粒为动脉粥样硬化、缺血性疾病、糖尿病、炎症性疾病的治疗提供了新的选择。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1