用于治疗炎性肠病的治疗性组合和组合物
用于治疗炎性肠病的治疗性组合和组合物
1.本发明涉及至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药与核黄素的药物组合,用于治疗患有炎性肠病(inflammatory bowel disease,ibd)或其他炎症(诸如,类风湿性关节炎、强直性脊柱炎、银屑病、红斑狼疮以及多发性硬化症)的患者。本发明还涉及至少一种硫嘌呤和核黄素的添加剂和/或组合。
2.本发明还涉及一种用于治疗或预防ibd的方法,所述方法包括施用治疗有效量的硫嘌呤和核黄素。
3.硫嘌呤药物是广泛用于治疗炎性肠病(ibd)的嘌呤抗代谢物。
4.硫嘌呤(thiopurine)涵盖一系列各种活性化合物,诸如:
[0005]6‑
巯基嘌呤(6
‑
mp),也称为巯基嘌呤,以purinethol等商品名出售。它是口服药。
[0006]
硫唑嘌呤(aza),以imuran等商品名出售。它可以口服或注射到静脉中。
[0007]
硫鸟嘌呤,也称为巯基鸟嘌或6
‑
硫鸟嘌呤(6
‑
tg),以lanvis等商品名出售。它是口服药。
[0008]
核黄素,也称为维生素b2,是一种微量营养素,在维持人类和其他哺乳动物的健康方面起着关键作用。它是辅助因子fad和fmn的核心成分,因此是所有黄素蛋白所必需的。因此,核黄素是多种细胞过程所必需的。它在能量代谢以及脂肪、酮体、碳水化合物以及蛋白质的代谢中起着关键作用。此外,核黄素还具有抗炎和抗氧化作用。核黄素天然存在于芦笋、爆米花、香蕉、柿子、秋葵、甜菜、奶酪、牛奶、酸奶、肉类、蛋类、鱼、以及青豆中。其他来源为,例如,奶酪、绿叶蔬菜、肝脏、肾脏、豆科作物、西红柿、酵母、蘑菇、以及杏仁。
[0009]
炎性肠病(ibd)是一种慢性且使人衰弱的疾病。它的特点是慢性肠道炎症,通常表现为间歇性病程,伴有急性发作,然后是缓解期。急性发作时的临床症状包括腹泻、出血、腹痛、发烧、关节痛、以及体重减轻。这些症状的范围可以从轻微到严重,并且可能从最初的轻微不适逐渐潜移默化地发展,或者可能突然以完全形式出现。ibd可以以多种形式表现出来,其中最常见的是克罗恩病(crohn’s disease)和溃疡性结肠炎。这两种疾病的炎症模式在胃肠道中分布不同,但在临床症状方面是相似的。克罗恩病是肠道的慢性透壁炎症,影响整个胃肠道,通常呈不连续模式。cd(克罗恩病)的初始位置最常见于回肠下部。炎症从这里通常向小肠的近端部分蔓延。然而,结肠也经常受到影响。
[0010]
溃疡性结肠炎是一种慢性炎性肠病,仅累及结肠,并在胃肠黏膜中连续分布。在大多数患者中,炎症的焦点位于结肠和直肠的远端。炎症由此经常向近端蔓延。在最严重的情况下,整个结肠都会受到影响,称为“全结肠炎”。大约30%的患者患有这种严重的uc(溃疡性结肠炎)。
[0011]
本发明涉及一种药物组合(pc),其包括:
[0012]
(i)至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药,和
[0013]
(ii)核黄素。
[0014]
本发明涉及一种药物组合(pc’),其包括:
[0015]
(i)至少一种硫嘌呤,和
[0016]
(ii)核黄素。
[0017]
本发明涉及一种药物组合(pc”),其包括:
[0018]
(i)硫嘌呤的至少一种药学上可接受的盐,和
[0019]
(ii)核黄素。
[0020]
本发明涉及一种药物组合(pc
’”
),其包括:
[0021]
(i)硫嘌呤的至少一种前药,和
[0022]
(ii)核黄素。
[0023]
本发明还涉及一种药物组合(pc
””
),其为满足以下条件的药物组合(pc)、(pc’)、(pc”)或(pc
’”
),其中硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药选自6
‑
巯基嘌呤、硫唑嘌呤以及硫鸟嘌呤。
[0024]
本发明涉及一种药物组合(pc1),其由以下成分组成:
[0025]
(i)至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药,和
[0026]
(ii)核黄素。
[0027]
本发明涉及一种药物组合(pc1’),其由以下成分组成:
[0028]
(i)至少一种硫嘌呤,和
[0029]
(ii)核黄素。
[0030]
本发明涉及一种药物组合(pc1”),其由以下成分组成:
[0031]
(i)硫嘌呤的至少一种药学上可接受的盐,和
[0032]
(ii)核黄素。
[0033]
本发明涉及一种药物组合(pc1
”’
),其由以下成分组成:
[0034]
(i)硫嘌呤的至少一种前药,和
[0035]
(ii)核黄素。
[0036]
本发明还涉及一种药物组合(pc1
””
),其为满足以下条件的药物组合(pc1)、(pc1’)、(pc1”)或(pc1
”’
),其中硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药选自6
‑
巯基嘌呤、硫唑嘌呤以及硫鸟嘌呤。
[0037]
本发明涉及一种制剂(f),其包括以下药物的组合:
[0038]
(i)至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药,和
[0039]
(ii)核黄素。
[0040]
本发明涉及一种制剂(f’),其包括以下药物的组合:
[0041]
(i)至少一种硫嘌呤,和
[0042]
(ii)核黄素。
[0043]
本发明涉及一种制剂(f”),其包括以下药物的组合:
[0044]
(i)硫嘌呤的至少一种药学上可接受的盐,和
[0045]
(ii)核黄素。
[0046]
本发明涉及一种制剂(f
”’
),其包括以下药物的组合:
[0047]
(i)硫嘌呤的至少一种前药,和
[0048]
(ii)核黄素。
[0049]
本发明还涉及一种制剂(f
””
),其为满足以下条件的制剂(f)、(f’)、(f”)或(f
”’
),其中硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药选自6
‑
巯基嘌呤、硫唑嘌呤以及硫鸟嘌呤。
[0050]
本发明还涉及一种用于治疗或预防ibd或其他炎症的方法(m),所述方法包括施用治疗有效量的:
[0051]
(i)至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药,和
[0052]
(ii)核黄素。
[0053]
本发明还涉及一种用于治疗或预防ibd或其他炎症的方法(m’),所述方法包括施用治疗有效量的:
[0054]
(i)至少一种硫嘌呤,和
[0055]
(ii)核黄素。
[0056]
本发明还涉及一种用于治疗或预防ibd或其他炎症的方法(m”),所述方法包括施用治疗有效量的:
[0057]
(i)硫嘌呤的至少一种药学上可接受的盐,和
[0058]
(ii)核黄素。
[0059]
本发明还涉及一种用于治疗或预防ibd或其他炎症的方法(m
’”
),所述方法包括施用治疗有效量的:
[0060]
(i)硫嘌呤的至少一种前药,和
[0061]
(ii)核黄素。
[0062]
本发明还涉及一种方法(m
””
),其为满足以下条件的方法(m)、(m’)、(m”)或(m
’”
),其中硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药选自6
‑
巯基嘌呤、硫唑嘌呤以及硫鸟嘌呤。
[0063]
本发明还涉及一种用于治疗ibd或其他炎症的方法(m1),所述方法包括施用治疗有效量的:
[0064]
(i)至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药,和
[0065]
(ii)核黄素。
[0066]
本发明还涉及一种用于治疗ibd或其他炎症的方法(m1’),所述方法包括施用治疗有效量的:
[0067]
(i)至少一种硫嘌呤,和
[0068]
(ii)核黄素。
[0069]
本发明还涉及一种用于治疗ibd或其他炎症的方法(m1”),所述方法包括施用治疗有效量的:
[0070]
(i)硫嘌呤的至少一种药学上可接受的盐,和
[0071]
(ii)核黄素。
[0072]
本发明还涉及一种用于治疗ibd或其他炎症的方法(m1
’”
),所述方法包括施用治疗有效量的:
[0073]
(i)硫嘌呤的至少一种前药,和
[0074]
(ii)核黄素。
[0075]
本发明还涉及一种方法(m1
””
),其为满足以下条件的方法(m1)、(m1’)、(m1”)或(m1
’”
),其中硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药选自6
‑
巯基嘌呤、硫唑嘌呤以及硫鸟嘌呤。
[0076]
本发明的另一个实施方式是一种治疗或减轻炎性肠病或其他炎症的症状的方法,包括向有需要的人施用有效量的至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药和核黄素。
[0077]
因此,本发明还涉及一种治疗或减轻炎性肠病或其他炎症的症状的方法(m2),包括向有需要的人施用有效量的:
[0078]
(i)至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药,和
[0079]
(ii)核黄素。
[0080]
因此,本发明还涉及一种治疗或减轻炎性肠病或其他炎症的症状的方法(m2’),包括向有需要的人施用有效量的:
[0081]
(i)至少一种硫嘌呤,和
[0082]
(ii)核黄素。
[0083]
因此,本发明还涉及一种治疗或减轻炎性肠病或其他炎症的症状的方法(m2”),包括向有需要的人施用有效量的:
[0084]
(i)硫嘌呤的至少一种药学上可接受的盐,和
[0085]
(ii)核黄素。
[0086]
因此,本发明还涉及一种治疗或减轻炎性肠病或其他炎症的症状的方法(m2
’”
),包括向有需要的人施用有效量的:
[0087]
(i)硫嘌呤的至少一种前药,和
[0088]
(ii)核黄素。
[0089]
本发明还涉及一种方法(m2
””
),其为满足以下条件的方法(m2)、(m2’)、(m2”)或(m2
’”
),其中硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药选自6
‑
巯基嘌呤、硫唑嘌呤以及硫鸟嘌呤。
[0090]
本发明的另一个实施方式是至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药与核黄素的组合在治疗或减轻ibd或其他炎症的症状中的用途。
[0091]
因此,本发明还涉及以下组合在治疗或减轻ibd或其他炎症的症状中的用途(u):
[0092]
(i)至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药,和
[0093]
(ii)核黄素。
[0094]
因此,本发明还涉及以下组合在治疗或减轻ibd或其他炎症的症状中的用途(u’):
[0095]
(i)至少一种硫嘌呤,和
[0096]
(ii)核黄素。
[0097]
因此,本发明还涉及以下组合在治疗或减轻ibd或其他炎症的症状中的用途(u”):
[0098]
(i)硫嘌呤的至少一种药学上可接受的盐,和
[0099]
(ii)核黄素。
[0100]
因此,本发明还涉及以下组合在治疗或减轻ibd或其他炎症的症状中的用途(u
”’
):
[0101]
(i)硫嘌呤的至少一种前药,和
[0102]
(ii)核黄素。
[0103]
本发明还涉及一种方法(u
””
),其为满足以下条件的用途(u)、(u’)、(u”)或(u
”’
),其中硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药选自6
‑
巯基嘌呤、硫唑嘌呤以及硫鸟嘌呤。
[0104]
本发明的另一个实施方式是核黄素和至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药的组合在制备用于治疗或减轻ibd症状的药物中的用途。
[0105]
因此,本发明还涉及以下成分的组合在制备用于治疗或减轻ibd或其他炎症的症状的药物中的用途(u1):
[0106]
(i)至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药,和
[0107]
(ii)核黄素。
[0108]
因此,本发明还涉及以下成分的组合在制备用于治疗或减轻ibd或其他炎症的症状的药物中的用途(u1’):
[0109]
(i)至少一种硫嘌呤,和
[0110]
(ii)核黄素。
[0111]
因此,本发明还涉及以下成分的组合在制备用于治疗或减轻ibd或其他炎症的症状的药物中的用途(u1”):
[0112]
(i)硫嘌呤的至少一种药学上可接受的盐,和
[0113]
(ii)核黄素。
[0114]
因此,本发明还涉及以下成分的组合在制备用于治疗或减轻ibd或其他炎症的症状的药物中的用途(u1
’”
):
[0115]
(i)硫嘌呤的至少一种前药,和
[0116]
(ii)核黄素。
[0117]
本发明还涉及一种方法(u1
””
),其为满足以下条件的用途(u1)、(u1’)、(u1”)或(u1
’”
),其中硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药选自6
‑
巯基嘌呤、硫唑嘌呤以及硫鸟嘌呤。
[0118]
此外,本发明还涉及用作药剂的药物组合(pc)、(pc’)、(pc”)、(pc
’”
)或(pc
””
)。
[0119]
此外,本发明还涉及用作药剂的药物组合(pc1)、(pc1’)、(pc1”)、(pc1
’”
)或(pc1
””
)。
[0120]
此外,本发明还涉及用作药剂的制剂(f)、(f’)、(f”)、(f
’”
)或(f
””
)。
[0121]
此外,本发明还涉及用于治疗ibd或其他炎症(尤其是克罗恩病)的药物组合(pc)、(pc’)、(pc”)、(pc
’”
)或(pc
””
)。
[0122]
此外,本发明还涉及用于治疗ibd或其他炎症(尤其是克罗恩病)的药物组合(pc1)、(pc1’)、(pc1”)、(pc1
’”
)或(pc1
””
)。
[0123]
此外,本发明还涉及用于治疗ibd或其他炎症(尤其是克罗恩病)的制剂(f)、(f’)、(f”)、(f
’”
)或(f
””
)。
[0124]
至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药与核黄素的组合产生协同作用。
[0125]
或者,也可以由于这两种化合物的作用而降低至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药的量。由于已知硫嘌呤有副作用(诸如,流感样症状、关节痛、胃肠道不适、皮疹、胰腺炎、肝毒性、以及骨髓毒性),因此,这是一种非常棒且令人惊讶的效果。
[0126]
因此,本发明涉及通过将至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药与核黄素的组合施用于患者来预防和/或减轻硫嘌呤的副作用。
[0127]
当使用如上公开的用于治疗或预防ibd或其他炎症的方法时,施用硫嘌呤(和/或其至少一种药学上可接受的盐和/或其至少一种前药)和核黄素的顺序可以变化。可以先施用硫嘌呤,然后施用核黄素(反之亦然)。也可以将它们一起施用(诸如,如果可能的话,在一种盖仑制剂中)。顺序还可以是硫嘌呤、核黄素、硫嘌呤等。这意味着施用顺序可以变化。
[0128]
还考虑到在两种化合物不同时施用的情况下施用的时间段。这意味着施用硫嘌呤和施用核黄素之间可以存在时间间隔(反之亦然)。
[0129]
优选地,硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药和核黄素是制剂中仅有的活性成分。这意味着制剂中可能存在此特定制剂所需的其他(辅助)成分。通常添加这些(辅助)成分是为了获得合适且稳定的制剂。
[0130]
因此,本发明还涉及一种制剂(f1),其为满足以下条件的制剂(f)、(f’)、(f”)、(f
’”
)或(f
””
),其中至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药和核黄素是制剂中仅有的活性成分。
[0131]
因此,本发明涉及包括由以下活性成分组成的药物组合的制剂(f2):
[0132]
(i)至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药,和
[0133]
(ii)核黄素。
[0134]
因此,本发明涉及包括由以下活性成分组成的药物组合的制剂(f2’):
[0135]
(i)至少一种硫嘌呤,和
[0136]
(ii)核黄素。
[0137]
因此,本发明涉及包括由以下活性成分组成的药物组合的制剂(f2”):
[0138]
(i)硫嘌呤的至少一种药学上可接受的盐,和
[0139]
(ii)核黄素。
[0140]
因此,本发明涉及包括由以下活性成分组成的药物组合的制剂(f2
’”
):
[0141]
(i)硫嘌呤的至少一种前药,和
[0142]
(ii)核黄素。
[0143]
优选地,硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药选自6
‑
巯基嘌呤、硫唑嘌呤以及硫鸟嘌呤。
[0144]
因此,本发明还涉及一种制剂(f3),其为满足以下条件的制剂(f2)、(f2’)、(f2”)或(f2
’”
),其中硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药选自6
‑
巯基嘌呤、硫唑嘌呤以及硫鸟嘌呤。
[0145]
因此,本发明还涉及一种制剂(f3’),其为满足以下条件的制剂(f2)、(f2’)、(f2”)
或(f2
’”
),其包括由以下活性成分组成的药物组合:
[0146]
(i)6
‑
巯基嘌呤和/或其药学上可接受的盐和/或其至少一种前药,和
[0147]
(ii)核黄素。
[0148]
因此,本发明还涉及一种制剂(f3”),其为满足以下条件的制剂(f2)、(f2’)、(f2”)或(f2
’”
),其包括由以下活性成分组成的药物组合:
[0149]
(i)硫唑嘌呤和/或其药学上可接受的盐和/或其至少一种前药,和
[0150]
(ii)核黄素。
[0151]
因此,本发明还涉及一种制剂(f3
’”
),其为满足以下条件的制剂(f2)、(f2’)、(f2”)或(f2
’”
),其包括由以下活性成分组成的药物组合:
[0152]
(i)硫鸟嘌呤和/或其药学上可接受的盐和/或其至少一种前药,和
[0153]
(ii)核黄素。
[0154]
本发明的另一个实施方式是制备制剂(f)、(f’)、(f”)、(f
’”
)、(f
””
)、(f1)、(f2)、(f2’)、(f2”)、(f2
’”
)、(f3)、(f3’)、(f3”),和/或(f3
’”
)。
[0155]
这些药物组合和/或制剂可以原样使用,也可以作为预混物使用,或处于任何合适的盖仑制剂中。
[0156]
因此,本发明还涉及包括制剂(f)、(f’)、(f”)、(f
’”
)、(f
””
)、(f1)、(f2)、(f2’)、(f2”)、(f2
’”
)、(f3)、(f3’)、(f3”),和/或(f3
’”
)的盖仑制剂(gf)。
[0157]
本发明的另一个实施方式是通过施用制剂(f)、(f’)、(f”)、(f
’”
)、(f
””
)、(f1)、(f2)、(f2’)、(f2”)、(f2
’”
)、(f3)、(f3’)、(f3”),和/或(f3
’”
)来治疗或减轻ibd或其他炎症。。
[0158]
本发明的另一个实施方式是通过施用盖仑制剂(gf)来治疗ibd或其他炎症。
[0159]
如上所述,本发明还涉及一种用于治疗或预防ibd或其他炎症的方法(m),所述方法包括施用治疗有效量的:
[0160]
(i)至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药,和
[0161]
(ii)核黄素。
[0162]
使用硫唑嘌呤时,硫唑嘌呤也可以是盖仑剂型,待注射到静脉中。在这种情况下,核黄素可以添加到这种盖仑剂型中,或者核黄素可以口服施用。
[0163]
然而,根据本发明的方法不排除两种化合物必须以相同方式施用(即都为口服)。
[0164]
还可以分开施用至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药和核黄素,其中至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药和核黄素的施用应在适当的时间段内发生。当通过将至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药与核黄素分开施用进行施用时,施用顺序并不重要,这意味着可以首先施用至少一种硫嘌呤和/或其至少一种药学上可接受的盐和/或其至少一种前药,然后施用核黄素,反之亦然。
[0165]
硫嘌呤可以以每天约0.2mg/kg体重至约2.5mg/kg体重的剂量范围使用,而核黄素可以以每天1mg至500mg(优选为30mg
‑
300mg)的合适剂量范围使用,可以以一天一次或一天数次施用。
[0166]
针对各种硫嘌呤,剂量有所不同。
[0167]6‑
巯基嘌呤的剂量范围为每天约1mg/kg体重至约1.5mg/kg体重,硫唑嘌呤的剂量范围为每天约2.0mg/kg体重至约2.5mg/kg体重,而硫鸟嘌呤的剂量范围为每天约0.2mg/kg体重至约0.3mg/kg体重。
[0168]
因此,本发明涉及包括0.2mg/kg体重至2.5mg/kg体重的硫嘌呤和1mg至500mg(优选为30mg至300mg)核黄素的日剂量单位(ddu)。
[0169]
日剂量单位是指活性成分(硫嘌呤和核黄素)的量可以每天服用一次或每天服用一次以上。
[0170]
硫嘌呤可以以每天约0.2mg/kg体重至约2.5mg/kg体重的剂量范围使用,而核黄素可以以每天1mg至500mg(优选为30mg
‑
300mg)的合适剂量范围使用,可以以一天一次或一天数次施用。
[0171]
针对各种硫嘌呤,剂量有所不同。
[0172]6‑
巯基嘌呤的剂量范围为每天约1mg/kg体重至约1.5mg/kg体重,硫唑嘌呤的剂量范围为每天约2.0mg/kg体重至约2.5mg/kg体重,而硫鸟嘌呤的剂量范围为每天约0.2mg/kg体重至约0.3mg/kg体重。
[0173]
因此,本发明涉及包括2mg/kg体重至2.5mg/kg体重的硫唑嘌呤和1mg至500mg(优选为30mg
‑
300mg)的核黄素的日剂量单位(ddu1)。
[0174]
因此,本发明涉及包括1mg/kg体重至1.5mg/kg体重的6
‑
巯基嘌呤和1mg至500mg(优选为30mg
‑
300mg)的核黄素的日剂量单位(ddu2)。
[0175]
因此,本发明涉及包括0.2mg/kg体重至0.3mg/kg体重的硫鸟嘌呤和1mg至500mg(优选为30mg
‑
300mg)的核黄素的日剂量单位(ddu3)。
[0176]
这些剂量单位通常是如下所述的盖仑制剂形式。
[0177]
一天一次是指在24小时内仅服用一次的剂型,通过此剂型可以在体内保持一整天的药物浓度。
[0178]
一天数次是指在24小时内服用数次的剂型。
[0179]
也可以具有用于2天、3天、4天、5天、6天或每周剂量单位的剂量单位。
[0180]
盖仑制剂可以包括形成此盖仑制剂所必需、需要或期望的任何药学上可接受的辅助剂。盖仑制剂可以是适合患者的任何形式。最常见的是固体形式(诸如,片剂、颗粒、球剂、粉末等)。
[0181]“药学上可接受的”是指在生物学上或其他方面不是不合需要的材料。
[0182]
药学上可接受的赋形剂包括但不限于粘合剂、稀释剂、润滑剂、助流剂以及表面活性剂。
[0183]
当将硫嘌呤和核黄素整合成合适的施用形式时,使用此类药学上可接受的赋形剂。
[0184]
所用添加剂的量将取决于要使用多少活性剂。一种赋形剂可以执行多于一种功能。
[0185]
粘合剂包括但不限于淀粉,诸如,马铃薯淀粉、小麦淀粉、玉米淀粉;微晶纤维素;纤维素,诸如,羟丙基纤维素、羟乙基纤维素、羟丙基甲基纤维素(hpmc)、乙基纤维素、羧甲基纤维素钠;天然树胶,如阿拉伯胶、海藻酸、瓜尔胶;液体葡萄糖、糊精、聚维酮、糖浆、聚环氧乙烷、聚乙烯吡咯烷酮等,及其混合物。
[0186]
可以使用的填充剂或稀释剂包括但不限于糖果粉、可压缩糖、葡萄糖结合剂(dextrate)、糊精、葡萄糖、果糖、乳糖醇、甘露醇、蔗糖、淀粉、乳糖、木糖醇、山梨糖醇、滑石、微晶纤维素、碳酸钙、磷酸二氢钙或磷酸钙、硫酸钙等。
[0187]
润滑剂可选自但不限于本领域常规已知的那些,诸如,镁、铝或钙或锌的硬脂酸盐、聚乙二醇、山嵛酸甘油酯、矿物油、硬脂富马酸钠、硬脂酸、氢化植物油以及滑石。
[0188]
助流剂包括但不限于二氧化硅;三硅酸镁、粉状纤维素、淀粉、滑石粉和磷酸三钙、硅酸钙、硅酸镁、胶体二氧化硅、硅水凝胶以及本领域普通技术人员已知的其他材料。
[0189]
根据本发明的药物制剂(为口服剂型)包括但不限于悬浮片剂(单层片剂、多层片剂、mups、微型片剂、生物粘附片剂、囊片、基质片剂、片内片剂、粘膜粘附片剂、调释片剂、脉冲释放片剂、定时释放片剂)、丸剂、珠粒、颗粒、缓释制剂、胶囊、微胶囊、胶囊和微球中的片剂、基质制剂、微胶囊和粉末/丸剂/颗粒。
[0190]
本发明的盖仑制剂可任选地具有一种或多种包衣,诸如,薄膜包衣、糖衣、肠溶包衣、生物粘附包衣以及本领域已知的其他包衣。这些包衣有助于药物制剂在所需的作用部位释放药物。在一个实施例中,附加的包衣防止剂量接触口腔或食道。在另一个实施例中,附加的包衣在到达小肠和/或大肠之前保持完整(例如,肠溶包衣)。生物粘附层的过早暴露或药物剂型在口腔中的溶解可以通过亲水性聚合物(诸如,hpmc或明胶)的涂层或包衣来防止。任选地,可以将eudragit fs 3od或其他合适的聚合物掺入包衣组合物中,以延迟药物的释放,从而确保药物在结肠中释放。
[0191]
这些包衣层包括选自包衣剂、遮光剂、掩味剂、填充剂、抛光剂、着色剂、抗粘剂等的一种或多种赋形剂。
[0192]
本发明的盖仑制剂可以通过多种方法进行包衣。合适的方法包括压缩包衣、在流化床或锅中包衣以及热熔(挤出)包衣。此类方法是本领域技术人员公知的。
[0193]
不溶性聚合物(例如,醋酸纤维素、乙基纤维素)的非渗透性包衣可以用作延迟释放/修饰释放(dr/mr)的肠溶包衣,方法是在包衣中加入可溶性成孔剂,例如,peg、pva、糖、盐、洗涤剂、柠檬酸三乙酯、甘油三乙酸酯等。
[0194]
此外,易受结肠细菌酶裂解影响的聚合物包衣是另一种确保释放至远端回肠和升结肠的方法。果胶酸钙等材料可用作剂型和多颗粒的包衣,并在下胃肠道中因细菌作用而崩解。还可提供用于封装生物粘附性多颗粒的果胶酸钙胶囊。
[0195]
本发明的药物组合物可任选地包括一种或多种增溶剂,即用于增加药物活性成分或其他组合物组分在固体载体中的溶解度的添加剂。用于本发明组合物的合适的增溶剂包括:醇和多元醇,诸如,乙醇、异丙醇、丁醇、苯甲醇、乙二醇、丙二醇、丁二醇及其异构体、甘油、季戊四醇、山梨糖醇、甘露醇、卡必醇、二甲基异山梨醇、聚乙二醇、聚丙二醇、聚乙烯醇、羟丙基甲基纤维素等纤维素衍生物、环糊精和环糊精衍生物;平均分子量为约200至约6000的聚乙二醇醚,诸如,四氢糠醇peg醚(四甘醇,可从basf(巴斯夫)以商品名tetraglycol购得)或甲氧基peg(union carbide(联合碳化物));酰胺,诸如,2
‑
吡咯烷酮、2
‑
哌啶酮、ε
‑
己内酰胺、n
‑
烷基吡咯烷酮、n
‑
羟烷基吡咯烷酮、n
‑
烷基哌啶酮、n
‑
烷基己内酰胺、二甲基乙酰胺、以及聚乙烯吡咯烷酮;酯,诸如,丙酸乙酯、柠檬酸三丁酯、乙酰柠檬酸三乙酯、乙酰柠檬酸三丁酯、柠檬酸三乙酯、油酸乙酯、辛酸乙酯、丁酸乙酯、甘油三乙酸酯、丙二醇单乙酸酯、丙二醇二乙酸酯、ε
‑
己内酯及其异构体、δ
‑
戊内酯及其异构体、β
‑
丁内酯及其异构体;以及
本领域已知的其他增溶剂,诸如,二甲基乙酰胺、二甲基异山梨醇(arlasolve dmi(ici))、n
‑
甲基吡咯烷酮(pharmasolve(isp))、单辛精(monooctanoin)、二乙二醇单乙醚(可从gattefosse(盖提佛斯)以商品名trans
‑
cutol购得)、以及水。
[0196]
优选的增溶剂包括甘油三乙酸酯、柠檬酸三乙酯、油酸乙酯、辛酸乙酯、二甲基乙酰胺、n
‑
甲基吡咯烷酮、n
‑
羟乙基吡咯烷酮、聚乙烯吡咯烷酮、羟丙基甲基纤维素、羟丙基环糊精、乙醇、聚乙二醇200
‑
600、四甘醇(glycofurol)、卡必醇(transcutol)、丙二醇、以及二甲基异山梨醇。特别优选的增溶剂包括山梨糖醇、甘油、甘油三乙酸酯、乙醇、sls、聚乙二醇四甘醇以及丙二醇、环糊精多氧聚合物(cyclodextrins poly
‑
oxomers)、表面活性剂等。
[0197]
非常合适的药学上可接受的赋形剂是(预胶化的)淀粉(玉米、马铃薯)、乳糖(一水合物)、硬脂酸、硬脂酸镁、甲氧基羟丙基纤维素、聚乙二醇(诸如,聚乙二醇400)、阿拉伯胶以及(纯化的)水。
[0198]
因此,本发明涉及一种盖仑制剂(gf),其包括制剂(f)、(f’)、(f”)、(f
’”
)、(f
””
)、(f1)、(f2)、(f2’)、(f2”)、(f2
’”
)、(f3)、(f3’)、(f3”),和/或(f3
’”
)的片剂、颗粒、球剂或粉末形式,包括至少一种药学上可接受的赋形剂,所述赋形剂选自(预胶化的)淀粉(玉米、马铃薯)、乳糖(一水合物)、硬脂酸、硬脂酸镁、甲氧基羟丙基纤维素、聚乙二醇(诸如,聚乙二醇400)、阿拉伯胶以及(纯化的)水。
[0199]
上文描述和公开的所有制剂以及盖仑制剂都可以通过使用众所周知的方法和工艺来制造。
实施例
[0200]
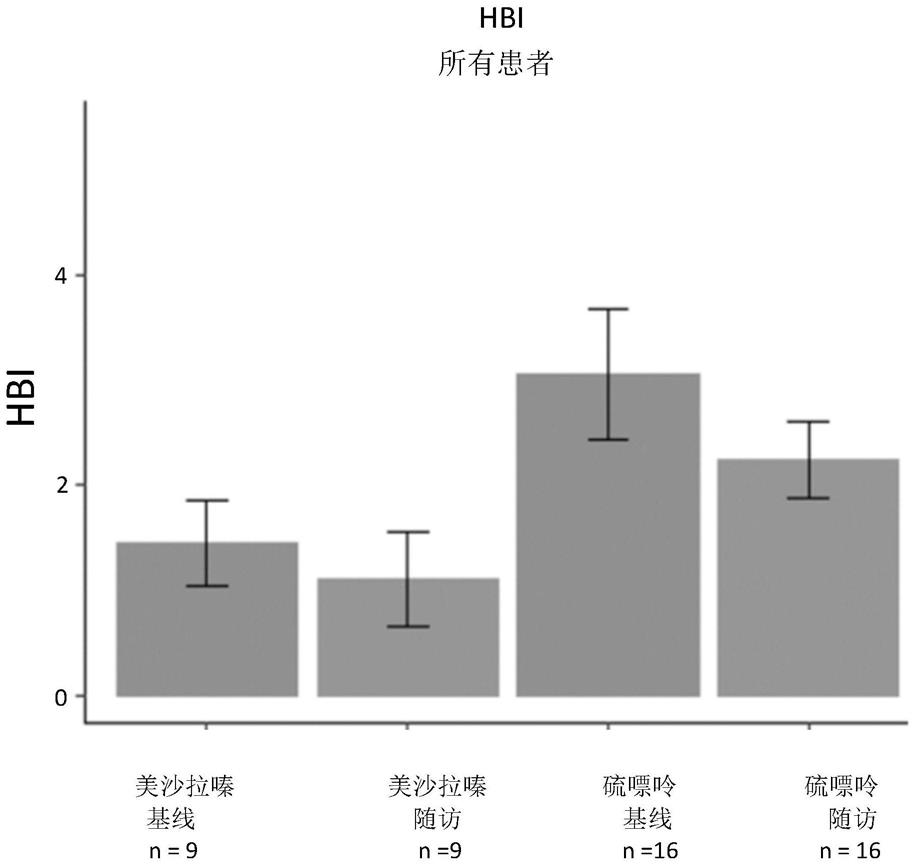
在一项前瞻性临床干预研究中,70名cd患者被纳入研究并分为两组,有(活跃)和无(静息态)粘膜炎症迹象(由粪便钙卫蛋白(fc)截断值限定:200μg/g)。患者每天接受100mg核黄素,持续3周。在核黄素干预前后分析了临床疾病活动度(harvey
‑
bradshaw指数:hbi)、炎性生物标志物(包括白介素2)以及粪便微生物组成(包括致病性肠杆菌科,包括大肠杆菌)。
[0201]
令人惊讶的是,我们发现补充核黄素进一步降低了接受硫嘌呤治疗的患者(尤其是处于静息状态的患者)的临床疾病活动度(hbi),然而,接受美沙拉嗪治疗的患者并非如此(没有那么明显)(如图1和图2所示)。
[0202]
与接受美沙拉嗪治疗的患者相比,这些作用伴随着促炎细胞因子il2以及包括大肠杆菌在内的肠杆菌科细菌在接受硫嘌呤治疗的患者中进一步减少(如图3和图4所示)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1