注射装置的制作方法
1.本发明涉及用于将至少一种材料注射到角质材料(例如人类皮肤和粘膜)中的装置
背景技术:
2.us 8167852和us 8834423公开了包括由支撑物承载的微植入物(也称为“微针”)阵列的装置。
3.这种装置可用于将美容材料、药物或疫苗输送到皮肤中。一个优点是它们可以穿透角质层、表皮或真皮而没有传统针引起的疼痛,并且可以自己给药。
4.固体微针阵列的生产已在各种申请中进行了描述,例如wo2008/139786、wo2009/040548、wo2015/147040和wo2016/076442。
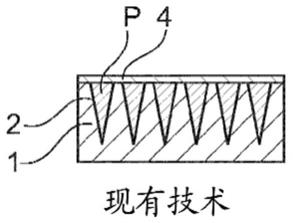
5.因此,可以使用如图1所示的模具1制造微植入物装置,该模具1设有空腔2,空腔2具有要赋予微植入物的形状。产品p被倒入模具1中并且背板4被压靠在存在于空腔开口处的产品上。当微植入物5脱模时,如图2a所示,它们仍然附着在背板4上。
6.然后需要将微植入物包装在合适的无菌包装(未示出)中直至使用。包装应该保护微植入物免受机械损坏并且应该是坚硬的。这增加了成本和浪费。
7.使用时,如图2b所示,将装置压入皮肤,微植入物穿透角质层、表皮或真皮。由于皮肤的柔软性,因此难以均匀地按压微植入物,并且微植入物的厚度e可能会保留一部分未插入角质层、表皮或真皮中。当背板4被移除时,如图2c所示,微植入物的某些部分6可能保留在背板4上,因而造成损失。
8.此外,由于皮肤运动和在装置上按压之后恢复其初始形状的能力,微植入物可能不会保持插入角质材料中。反压力将背板排出,从而将微植入物从皮肤中抽出。背板的刚性是微植入物在皮肤运动期间被排斥的一个原因。微植入物的未插入部分无法在角质材料中溶解或分解,因而造成损失。因此,输送到皮肤中的材料的量可能相对较低,并且处理效果比预期的要弱。
技术实现要素:
9.需要改进用于将材料注射到角质材料中并克服现有技术装置的至少一些缺点的进一步装置。改进输送和减少浪费将是有益的。
10.本发明的示例性实施方式涉及一种用于将至少一种材料注射到人类角质材料中的注射系统,包括:
11.○
至少一个处理单元,其限定至少一个空腔和由所述至少一种材料制成的至少一个微植入物,所述至少一个微植入物容纳在所述空腔中并具有与相应空腔形状相同的至少一个部分;
12.○
注射装置,其被配置为用于向所述至少一个微植入物施加压力以将所述至少一个微植入物从所述处理单元排出到所述角质材料中。
13.由于本发明,至少部分地限定至少一个空腔的单元的芯可用于模制微植入物,并且芯可用作用于保护和保持微植入物直至使用的包装。这可以使微植入物的包装更便宜和/或更简单,因为可能不再需要坚硬的包装。所述单元可以更好地保护微植入物免受压力、湿度或其他环境因素的影响,直到使用。可以降低包装的成本。
14.此外,本发明使得将整个微植入物注射到体内变得更容易,而不会损失材料。减少了浪费且增加了输送。
15.没有传统的背板有助于微植入物穿透到角质层、真皮或表皮中,并促使更好地输送待注射的材料,即使在高度柔软的皮肤区域也是如此。
16.本发明使得能够使用具有无法脱模的形状(诸如具有截顶部的形状)的微植入物。本发明还实现了在传统的出模过程期间将阻碍的形状。本发明能够使用不同材料的组合来制作微植入物,从而使该微植入物难以脱模。
17.本发明还有助于将不同材料的微植入物关联在同一处理单元中。
18.所述单元可以在注射之前被压靠在身体上。为此,该单元可以具有用于当所述至少一个微植入物被排出所述单元时接触角质材料的施加表面。
19.所述至少一个微植入物优选地至少部分地接触容纳其的相应空腔的内表面。
20.单元
21.该单元可以限定多个空腔,多个微植入物分别被容纳在该单元的相应空腔中并且分别具有与相应空腔形状相同的至少一个部分。微植入物可以分别至少部分地接触容纳其的相应空腔的内表面。所述单元可以包括空腔阵列。该阵列可以包括沿彼此垂直的两个方向规则地或随机地间隔开的空腔。空腔的形状可以正好对应于整个微植入物的形状。因此,空腔的高度可以正好对应于微植入物的高度。所有空腔的纵向轴线可彼此平行。在变型中,空腔的纵向轴线可以不平行。具有非平行轴线的空腔可以允许芯更好地符合身体突起的某些部分。
22.该芯优选是聚合物的,例如是弹性体的,该芯包括例如硅弹性体。在这种情况下,芯可以在微植入物的注射期间以可逆的方式变形。芯可以在注射期间被挤压。所述芯还可以在注射期间被微植入物撕开或刺穿一定程度。所述芯可在注射期间变形,使得至少两个空腔的纵向轴线一个相对于另一个而取向。
23.在变型中,芯是非弹性体的。芯可以包括至少一种选自pmma(聚甲基丙烯酸甲酯)、pdms(聚二甲基硅氧烷)或其他聚合物的材料。在这种情况下,芯可以在注射期间被微植入物穿孔和/或破坏。
24.芯可以是可溶于液体的,所述液体例如水或另一种溶剂或组合物。芯在溶解时可以部分地与微植入物一起被注射。芯的溶解性可用于易于从芯中取出微植入物,因为它例如可以使芯脆弱。
25.芯优选地是生物相容性的。芯优选是生物可吸收性的。
26.芯可以是液体或气体可渗透的。
27.当使用气体排出微植入物时,注射系统可以以一些气体穿透皮肤的方式配置。使芯可渗透气体可以帮助气体穿透皮肤。已穿透皮肤的气体可以协助使皮肤局部膨胀,这在一些寻求使皮肤丰盈(如减少皱纹)的应用中可能是有益的。
28.由于使用了弹性体材料或由于空隙和/或微空间或通道的存在,该芯可以是可挤
压的,这些空隙和/或微空间或通道可以在为排出微植入物而施加的压力下塌陷。芯可以具有实心结构或可通过将片材成形以形成空腔而制成。芯可以具有复合结构,该复合结构具有限定空心的实心主体和至少存在于所述空心中以限定微植入物所位于的空腔的边界的内衬。这使得可以使用低机械强度和高孔隙率的主体,而内衬的存在允许以精确形状和表面状态模制微植入物。
29.所述单元可以包括至少一个可刺穿区域,至少一个微植入物通过该可刺穿区域被排出。可刺穿区域的存在在微植入物的远端提供了保护屏障,并可以有助于保持微植入物的无菌条件。
30.所述单元可以包括至少一个可刺穿密封膜,至少一个微植入物通过该密封膜被排出。密封膜可以包括金属(优选铝)和/或聚合物(例如聚丙烯)。在注射之前密封膜可以被移除或不被移除。当密封膜不被移除时,它优选地是生物相容性的和/或生物可吸收性的。
31.所述单元可以包括在至少一个微植入物的近端侧固定到芯上的保护盖。在使用所述系统之前,保护盖可以从芯上拆下。
32.所述单元每平方厘米(cm2)可以包括1到5000个微植入物。具有微植入物的区域的轮廓可以限定为直径范围为3mm至80mm、更好为5mm至50mm的圆。
33.两个相邻微植入物的阵列内的间距在平面的x方向和y方向上的范围都可以为50μm至50mm。
34.所述单元的厚度范围可以为例如25μm至30mm,优选为25μm至10mm,例如为大约3mm。
35.微植入物在其基部可以具有不大于1500μm的最大横向尺寸,例如最大横向尺寸的范围为1μm至1500μm。微植入物的截面优选为圆形,在这种情况下微植入物的最大直径的范围可以为1μm至1000μm,优选在200μm和400μm之间。
36.微植入物的长度的范围可以为100μm至1500μm,更好地为200μm至800μm,甚至更好地为400μm至600μm。
37.微植入物可以包括具有恒定截面的圆柱形近端部分和具有朝向微植入物的尖端变窄的截面的远端部分,例如锥形远端部分。微植入物的近端部分和远端部分可以具有基本相同的长度,例如l
p
*0.8<l
d
<l
p
*1.2,其中l
p
是近端部分的长度,l
d
是远端部分的长度。近端部分的长度的范围可以为200μm至400μm,远端部分的长度的范围也可以为200μm至400μm。当然,其他范围也是可以的。
38.微植入物还可具有截头的远端部分、或倒角的远端部分、或斜面的远端部分。
39.微植入物可以至少部分地对气体或液体是能渗透的。
40.所述芯可以包括空腔,每个空腔包含由轴向叠加的多个微植入物形成的柱。每次注射时,该柱中的微植入物的数量可以减少一个微植入物。用于将位于该柱远端的微植入物推入皮肤中的力可以施加在位于该柱相对端的微植入物上。当所述单元包含至少一个由多个微植入物形成的柱时,该柱中所有的微植入物可以相同或不同。例如,一种化合物的浓度可以随着该柱的微植入物逐渐变化,或者两个连续的微植入物可以包含不同的化合物。
41.所述单元可以在第一次使用后或在所有微植入物已从其排出后丢弃。该单元可重复使用以生成新的微植入物。芯为空时可用于模制新的微植入物。芯的材料可以重新成形以形成新的模制空腔。
42.所有的微植入物可以由相同的材料制成。在变型中,一些微植入物由第一材料制成,而另外一些微植入物由至少一种不同于第一材料的第二材料制成。
43.所述至少一个微植入物可以由不同的材料制成;例如,微植入物的近端部分由第一材料制成,而微植入物的远端部分由与第一材料不同的第二材料制成。微植入物可以包括具有不同硬度的至少两个部分。微植入物可以包括硬度大于近端部分的硬度的远端部分。具有更大硬度的远端部分可以有助于刺透皮肤。
44.所述至少一个微植入物可以包括至少一个用于将微植入物锚定到角质材料中的锚定突起。所述至少一个微植入物可以包括锯齿状头部或鱼叉状头部中的至少一者。本发明允许在微植入物中形成截顶部。
45.所述至少一个微植入物可以包括至少一种选自可植入物质的材料,例如可植入类别的透明质酸(ha)、pvp(聚乙烯吡咯烷酮)、peg(聚乙二醇)或木糖醇。微植入物的材料可以是纯ha或可以基于ha和木糖醇。
46.所述至少一个微植入物可以携带活性物质,这些活性物质可以是美容活性物质、或药物或疫苗。微植入物可以由可再吸收的材料制成,优选由可溶于水或可溶于任何体液的材料制成。
47.所述至少一个微植入物可以包括至少两种处于干燥状态的材料,它们被选择以在与体液接触时发生反应。该反应可以导致产生气体。这种气体可以导致皮肤局部膨胀,这可以用于减少皱纹。
48.微植入物的材料可以具有高膨胀能力和高粘弹性。
49.所述单元可以具有圆盘形状。该单元可以具有其他形状,例如具有非圆形轮廓(例如多边形轮廓)的丸粒形状、或者带状或缎带状。
50.所述单元可以包括具有不同材料、体积、长度和/或形状的至少两种微植入物。不同材料、体积、长度和/或形状的微植入物可以位于所述单元的各个不同区域中或者可以均匀地分布在阵列内。
51.所述微植入物或每个所述微植入物的背面可以是自由的并且不附接到背层。
52.所述单元可以包括与所述至少一个微植入物接触的液体。该液体可以在所述单元的包装中与(一个或多个)微植入物接触,或者该液体可以仅在使用前或使用时由于使用者的动作而与微植入物接触。例如,当微植入物被排出时或就在喷出之前,液体被封装并释放。
53.如上所述,微植入物可以包括至少一个防止其脱模的截顶部。这可以有助于微植入物抵抗由其被注射到的组织施加的反压力。这可以有助于减少材料损失。
54.微植入物的尖端可以位于同一平面中。所述单元的用于接触皮肤的面可以是平面的。在变型中,微植入物的尖端不位于同一平面中,并且所述单元的用于接触皮肤的面可以不是平面的。例如,该面的形状与待处理区域的皮肤形状相匹配。例如,该面具有向外凸出的形状,并且所述尖端沿着平行于该面的表面定位。由于微植入物不需要被脱模,因此非平面形状不会引起脱模问题。
55.本发明的另一个目的是一种适合于在如上所述的系统中使用的处理单元,该处理单元包括:
56.‑
至少部分地限定至少一个空腔的芯,
57.‑
至少一个微植入物,所述至少一个微植入物由所述至少一种材料制成并容纳在所述芯的所述空腔中且具有与所述空腔形状相同的至少一个部分。
58.这种单元可以在使用前要打开或不打开的包装中提供给使用者。
59.这种包装可以是袋,并且不需要是刚性的,因为芯为微植入物提供了某些保护。这种包装可以是每端具有一个或两个盖的管。
60.注射装置
61.注射装置可以包括冲击构件,该冲击构件被配置为用于接触至少一个微植入物的近端以将所述至少一个微植入物排出所述单元。
62.冲击构件可由任何合适的手段驱动,例如机电致动器、弹簧、气动或液压装置、烟火装置、或手动施加在表面上并传递到微植入物的压力。
63.手动压力可以直接施加在所述单元或冲击构件上以将微植入物推入皮肤。
64.冲击构件可以具有接触表面,该接触表面被配置为用于同时接触多个微植入物的近端。该表面可以是平坦的或例如如果所述单元的接触皮肤的面不是平面而是凸面则该表面可以具有任何其他合适的形状。
65.所述单元可以包括可挤压的芯以允许冲击构件沿着足够长的距离推动微植入物以使其离开芯。冲击构件可以具有多个单独的突出部,每个突出部用于接触相应微植入物的近端。可以是杆的突出部(也称为“反向针”)的存在可以使得能够使用刚性芯,因为该芯不需要为了将微植入物推出芯而塌陷。突出部可以进入空腔以将微植入物从其中推出。
66.冲击构件可以同时或按顺序冲击多个微植入物。在后一种情况下,冲击构件可以在冲击位置和升高位置之间振荡,并且在两次连续冲击之间移动以在升高位置时定位为与下一个要冲击的微植入物成一直线。
67.所述系统可以包括用于容纳所述单元的至少一个腔室。
68.所述系统可以被配置为用于选择性地排出微植入物。注射装置和所述单元可以相对于彼此移动以选择要排出的至少一个微植入物。例如,注射装置和所述单元可以一个相对于另一个旋转以选择要排出的至少一个微植入物。
69.所述系统可以包括能量发生器,例如电动机或弹簧,以用于使注射装置相对于所述单元移位,反之亦然。
70.所述系统可以被配置为用于使液体与所述至少一个微植入物接触。使接触可以在排出所述至少一个微植入物之前发生。
71.使接触可以在至少一个微植入物已经被注射到角质材料中之后发生。
72.所述系统可以包括用于储存所述液体的储液器。
73.可以选择液体和微植入物的材料,使得液体溶解所述材料或反应以产生另一种材料。该液体也可以导致微植入物的材料膨胀。
74.所述系统可以被配置为用于临时使所述液体与微植入物接触。
75.所述系统可以包括图像传感器和处理器,以用于自动检测角质材料的目标区域,并用于当系统相对于目标区域正确定位时在排出所述至少一个微植入物之前向使用者发出信号和/或用于当系统相对于目标区域正确定位时自动触发所述至少一个微植入物的注射。图像传感器可以是诸如照相机的光学传感器或诸如电容式传感器的非光学传感器。
76.所述系统可以通过无线连接或通过电缆连接到终端,例如智能手机或诊断装置。
无线连接可以是wi
‑
fi或蓝牙。
77.目标区域可以包括皱纹和/或任何皮肤凹陷或其他皮肤缺陷,例如色素缺乏。
78.当图像传感器相对于微植入物偏心时,系统被配置为用于检测注射系统沿皮肤的位移以在触发注射之前补偿这种偏心。可以光学地检测该位移。
79.所述系统可以包括用于振动所述单元和/或注射装置的机电致动器。这可以有助于产生抵抗疼痛和/或提高材料在角质层、表皮或真皮内的扩散的按摩动作。
80.所述系统可以包括用于在注射之前、期间或之后降低所述单元和/或角质材料的温度的冷源。这可以有助于减少炎症副作用、疼痛和/或使真皮或表皮更坚固。
81.所述系统可以包括用于在注射之前、期间或之后升高所述单元和/或角质材料的温度的热源。这可以降低芯的材料的刚度并有助于从其中排出微植入物。
82.所述系统可以包括用于将光投射到待注射所述至少一个微植入物的目标区域上的光源。这可以有助于使用者将系统定位在待处理区域和/或促进皱纹或待用该系统处理的其他元素的检测。
83.所述系统可以包括至少一个电极,其用于使待注射所述至少一个微植入物的目标区域经受微电流。微电流可以有助于微植入物的材料更深地穿透组织,例如通过用离子电渗疗法将一些活性物质推入皮肤来实现。微电流还可以产生活性物质或增强一些内部反应。
84.注射装置可在注射后立即移除或留在原位预定量的时间。
85.所述系统可以包括用于存储多个处理单元的存储隔室。这种存储隔室可以是其中存在一组单元的筒。使用者可以将筒插入注射装置中,并在筒中的所有单元都被使用后更换新筒。
86.注射装置可以被配置为用于保持多于一个的筒,这些筒可以包含具有不同体积、材料和/或长度或形状的微植入物的单元。
87.所述系统可以包括供给机构,该供给机构被配置为用于用来自存储隔室的新单元自动更换存在的使用过的单元。
88.所述系统可以被配置为用于自动识别单元。取决于已识别的单元,注射装置可在不同条件下操作。
89.所述系统可以允许其在任何方向上操作,例如头朝上或朝下。
90.微植入物
91.本发明的另一个目的是一种微植入物,其具有至少一个防止其脱模的截顶部,所述截顶部例如为箭头形状。
92.另一个目的是一种具有至少两种不同的材料的复合结构的微植入物。
93.另一个目的是存在于所述单元的空腔中的微植入物的柱。
94.这些微植入物中的任何一者都可以具有以上详述的任何特征。
95.制造方法
96.本发明的另一个目的是一种制造在如上所述的系统中使用的单元的方法,包括在该单元的相应空腔中模制所述至少一个微植入物。
97.所述方法可以包括将微植入物的材料的可倾倒前体注入到所述空腔中并且使所述前体在所述空腔中硬化。微植入物的材料可以在空腔中干燥。
98.选择能够在角质层、表皮或真皮中形成开口的微植入物的材料。优选地,当在所述单元上施加力以将微植入物排出到皮肤中时,微植入物不会破裂。
99.所述方法可以包括对所述单元进行消毒,例如使用伽马或贝塔射线、高压灭菌器或化学消毒来实现。
100.用于模制微植入物材料的芯可以接受一些机械处理。例如,在芯上制造孔或狭缝,以促进在排出微植入物时芯的变形。这些孔或狭缝可以用激光来制造。例如,芯可以接受表面处理以降低或增强其亲水性或疏水性。
101.所述方法可以包括在芯的空腔中模制单元的柱。该柱可以包括促进微植入物的分离的脆弱区域。可以在芯中一个接一个地模制该柱中的微植入物。该柱中的两个连续的微植入物可以通过促进在注射过程期间将该柱中的一个微植入物和与之连续的微植入物分离的材料分离。
102.所述方法可以包括在被切割以形成单元的细长芯中模制所述柱。切割线可以垂直于芯的细长轴线,或者在变型中切割线可以倾斜以形成具有斜面端部的微植入物。
103.非治疗性方法
104.本发明的另一个目的是一种用于处理角质材料的非治疗性方法,包括使用如上所述的系统将至少一个微植入物注射到角质材料中。优选地,所述至少一个微植入物在注射期间从所述单元整体排出。
105.可以执行所述方法来处理皱纹。
106.芯如果可弹性变形并且没有被注射损坏,则可以在制造另一个单元时重新使用。否则,芯可以被丢弃。
107.优选地,当微植入物被排出时,芯不穿透皮肤。然而,在变型中,芯的某一部分可以与微植入物一起穿透皮肤。在后一种情况下,芯的材料优选是生物相容性的和/或生物可吸收性的,并且可以被选择为在皮肤中溶解或分解。芯可以是水溶性的。
附图说明
108.考虑到以下非限制性实施方式的描述并考虑到附图,将更好地理解本发明,附图中:
109.图1是根据现有技术的用于制造微植入物的模具示意图,
110.图2a至图2c示出了根据现有技术的微植入物的脱模和使用,
111.图3是根据本发明的示例性实施方式的注射系统的纵向截面的局部示意图,
112.图4是图3的装置的透视图,
113.图5单独示出了一个微植入物,
114.图6示出了根据变型实施方式的包括微植入物的处理单元,
115.图7a示出了微植入物从图6的单元中喷出,
116.图7b示出了图6的单元的微植入物注射在真皮或表皮中,
117.图7c示出了微植入物喷出后的图6的单元,
118.图8和图9示出了处理单元的变型实施方式,
119.图10是根据本发明的装置的变型实施方式的局部示意图,
120.图11和图12是与图10的变型实施方式相似的视图,
121.图13示出了一组处理单元,
122.图14示出了单元的变型实施方式,
123.图15是注射装置的变型的示意性框图,
124.图16示出了复合微植入物,
125.图17示出了微植入物的变型实施方式的正视图,
126.图18示出了单元的变型,
127.图19示出了单元的另一变型,
128.图20是注射装置的变型的示意图,以及
129.图21示出了包括微植入物的柱的单元。
具体实施方式
130.图3和图4所示的注射系统10包括处理单元20和作用在单元20上的注射装置30。
131.单元20包括芯21和容纳在芯中的微植入物40。
132.图5示出了一个微植入物40。如图所示,微植入物40可以包括长度为l
p
且直径为c的圆柱形部分41和锥形头部42。微植入物的总长度e的范围可以为25μm至2000μm。直径c的范围可以为100μm至3mm。近端部分的长度l
p
的范围可以为50μm至50mm。直径c例如等于350μm。长度e例如等于500μm。长度l
p
例如等于250μm。
133.微植入物40将被整体注射到角质层、表皮或真皮中,并且由根据所需作用选择的一种或多种材料制成。
134.例如,微植入物40由透明质酸或其衍生物制成。
135.芯21用作用于使微植入物40成形的模具并且用于在使用前保护微植入物40。
136.取决于微植入物40被推出芯21的方式,各种材料可用于芯21。
137.在图3和图4的实施方式中,选择芯21的材料以允许当注射装置30的冲击构件在微植入物40的上端43上施加指向微植入物40的尖端44的力时取出微植入物40。
138.在该实施方式中,该力通过由在圆柱形引导件33中移动的板32保持的相应杆31施加。板32可以通过其与杆31相对的面附接到阀杆34,阀杆34连接到驱动机构(未示出),该驱动机构被配置为用于当微植入物40要被推入皮肤时向前移动阀杆。
139.驱动机构可以包括机电装置,例如电动机或弹簧。
140.本发明不限于用于驱动杆31的特定装置,并且杆31可以基于例如烟火装置、气动或液压装置等、或者手动力而以各种方式被驱动。
141.当杆31被压靠在微植入物40上时,微植入物40被从单元20中排出并穿透真皮或表皮。芯21可以弹性变形以允许微植入物离开它们在芯21内的相应空腔。芯21可以包括被微植入物40穿孔或撕开或以其他方式损坏的部分。
142.杆31优选地具有与微植入物40直径相同的圆柱形形状并且相对于微植入物40定心。这样杆31可以穿透到空腔中以推动微植入物。
143.杆31的长度优选地大于e,从而不需要用板32压缩芯21来将微植入物40排出芯21。
144.杆31的端面优选地具有与将被杆冲击的微植入物的端部的形状互补的形状。
145.如图所示,杆31的端面可以是平坦的并且垂直于引导件33的纵向轴线。微植入物40的近端43优选地具有相应的平坦表面,使得杆和微植入物之间的接触面积最大。这有助
于降低微植入物在被推出模具时破裂的风险。
146.要使用图3和图4中所示的系统,使用者将单元20放置在注射装置30的相应腔室中,然后定位系统10,使得单元20紧靠应注射微植入物的区域定位。
147.然后,使用者触发驱动机构,使杆31撞击微植入物并将它们排出芯21。
148.一旦微植入物进入角质层、表皮和/或真皮内,使用者就可以撤回注射系统10并继续用新的处理单元更换处理单元。
149.通常,微植入物被整体排出到角质层、表皮或真皮中,并且不应该还有微植入物40的被困在芯21内的任何未注射部分。
150.现在将参考图6描述处理单元20的变型实施方式。
151.在该实施方式中,单元20包括限定空腔26的芯21以及分别覆盖芯21的近端面和远端面的保护膜28和29,其中,空腔26具有与包含在其中的微植入物40相同的形状。
152.空腔26的底部与芯21的远端面相距非零距离,使得空腔在其底端被芯21的材料封闭。
153.空腔26在其相对端被膜28封闭,膜28接触微植入物40的一端。
154.膜28和29构成屏障,该屏障有助于保持微植入物40的无菌条件。
155.当使用所述单元时,膜28和29可以保留在芯21上。在变型中,在将单元放置在注射装置中之前移除膜28和/或29。
156.当在注射装置的使用期间膜28和/或29存在于注射装置中时,膜可在注射过程期间被穿孔。
157.芯21可以由能够在注射阶段期间被压缩的材料制成,该注射阶段可以由于包括作为冲击构件的压力板38的注射装置而执行,如图7a所示。
158.压力板38可具有旨在接触膜28的平面表面。压力被传递至微植入物40的近端。膜29可以位于微植入物40将被注射的区域上。芯21可以在板38施加的压力下塌陷,从而允许微植入物被向前推动穿过膜29而进入真皮或表皮d,如图7b所示。
159.一旦压缩停止,芯21不能恢复其初始形状和厚度,如图7c所示。
160.为了制造处理单元20,芯21用作微植入物或其前体的材料的模具。在形成微植入物40之后,膜28和29可以附接到芯21。在变型中,膜29可以在用于制作微植入物的材料被倾倒入芯21的空腔中之前附接到芯21。膜28可以在制作微植入物的材料硬化之前或之后附接到芯21。如果在材料硬化之前带上膜28,则可以有助于膜28粘附到单元20的其余部分。
161.处理单元20可以包括完全相同的微植入物40或者不同尺寸和/或材料的微植入物。注射装置30可以被配置用于选择性注射这些微植入物中的一种或多种,这取决于各种标准,例如待处理区域的大小和/或性质和/或待执行处理的性质。
162.在图8所示的示例中,单元20形成密封包装,其中通过芯的材料和/或通过微植入物近端侧上的密封膜将微植入物与环境空气隔离。
163.图9示出了包括由不同材料制成和/或包括不同形状的各组微植入物40a、40b、40c和40d的单元20的变型。每个组可以存在于单元的特定区域中,例如存在于如图所示的特定角扇区中。
164.该单元可以包括各种高度和/或大小的微植入物。
165.注射装置可以包括存储器,其中存储了单元20的每个微植入物40的特征和位置。
可以基于单元的标识符来访问该信息。例如,单元和/或单元的包装带有由注射系统读取的条形码。基于读取的信息和/或使用者在诸如键盘或触觉屏的hmi上输入的可能的额外信息,注射系统自动确定应该将哪些微植入物排出并注射到皮肤中。
166.注射系统可以基于例如要注射的每种材料的剂量来自动选择注射所需的微植入物。
167.注射装置可以包括可独立于其他杆被控制的单独杆。杆可以具有不同的长度、直径和形状。杆可以上下移动。这些杆的数量可以与微植入物的数量一样多。注射装置可以被配置为记住已经从单元中排出的微植入物的位置。这样,注射装置可以确定在每次使用后应该致动哪些杆以排出剩余的微植入物。
168.注射装置还可以包含比微植入物少的杆,并且注射系统被配置为用于一旦单元的给定区域的所有微植入物已经被排出,则允许单元相对于注射装置移位。该移位可以是单元20和/或杆31和板32的旋转,如图10所示。
169.该系统还可以包括一个或多个致动杆,这些致动杆由可在x方向和y方向上相对于该单元移动的托架承载。
170.注射系统10可以包括至少一个压力传感器并且被配置为仅当在皮肤上超过阈值压力时才允许注射。这有助于减小皮肤的柔软性并改善微植入物穿透皮肤。
171.图11示出了注射系统,其中注射装置30配备有示意性表示的传感器52,该传感器可以是压力传感器。该传感器提供注射系统10对皮肤的压力的指示。注射装置30可以包括控制用于移动杆31的驱动机构或用于排出微植入物40的其他压力装置的处理器。该处理器接收来自压力传感器的信号并且可以仅在达到给定压力时触发注射。
172.注射装置中压力传感器的存在可以有助于根据皮肤机械特性为微植入物插入产生正确的压力。
173.如图11所示,注射系统10还可以包括识别传感器55以识别所使用的单元20。例如,基于该识别,注射装置可以根据特定程序操作。
174.可以由于在单元上存在特定标记、例如如上所述的条形码而执行识别。
175.芯21可由可溶于特定溶剂(例如水)的材料制成。在微植入物被排出之前,可以使单元20与该溶剂接触。溶剂可以改变芯21的刚度并促进芯的变形,这是允许微植入物离开芯所必需的。
176.注射也可以在液体存在下进行,该液体被选择以提高微植入物的材料在真皮或表皮或微植入物被注射到的其他介质中的溶解度。
177.该液体l可以存在于单元20上方,如图12所示。注射装置30可以首先驱动微植入物从芯21中排出,然后迫使一些液体跟随微植入物进入真皮或表皮。
178.如图13所示,多个单元20可以包装在同一个筒50中。这种筒可以是管状的。
179.注射装置30然后可以被配置为从筒中一次取出一个单元20。当单元已经被使用后,它会从系统中喷出,并从筒中抽取新的单元。
180.微植入物40可以被赋予各种形状,包括具有将防止微植入物从芯21脱模的底切的形状。
181.作为示例,图14示出了包括具有箭头形状的微植入物40的处理单元20。这种形状允许将微植入物更好地锚定在其已被注射到的组织中。微植入物包括至少一个截顶部
(cutback)60以防止它们脱模。
182.注射装置可设有用于识别给定区域以自动对其进行处理的目标传感器。例如,目标传感器检测皱纹并且注射装置被配置为仅在皱纹区域注射微植入物。
183.注射装置可以包括如图15所示的图像传感器110和处理器111,以用于自动检测角质材料的目标区域,并用于当系统相对于目标区域正确定位时在排出所述至少一个微植入物之前向使用者发出信号和/或用于当系统相对于目标区域正确定位时自动触发所述至少一个微植入物的注射。
184.注射装置可以包括界面112和用于致动冲击构件以排出微植入物的致动器113。界面112可以包括触觉屏和/或一些按钮以选择操作参数。
185.图16示出了微植入物40具有复合性质的可能性,例如其远端部分40b由硬度高于近端部分40a的材料制成。
186.微植入物的远端可以具有各种形状。它不一定是圆锥形的。它可以是平坦的、圆形的或斜面的,如图17所示。
187.如图19所示,芯21可以具有细长形状并且可以通过切割细长芯的连续部分来形成各个单元。通过改变切割线之间的间距,可以改变微植入物40的长度。切割线可以相对于芯21的纵向轴线倾斜,以便形成微植入物的斜面远端。
188.如图19所示,芯21可以是柔性的并且变形以采取身体部分s的形状,所述单元在注射微植入物之前贴靠在身体部分s上。
189.在图20所示的变型实施方式中,注射装置包括外壳110,外壳110具有被配置为用于放置在皮肤上的开口。真空泵在外壳内部的空间100中产生真空,从而使皮肤s朝向所述单元变形。通过改变真空的强度,可以使皮肤朝向所述单元更大或更小地变形。这样,微植入物和皮肤之间的距离可以改变,并且微植入物穿透皮肤的深度也随之改变。真空也有助于在注射前使皮肤特性均匀。
190.在图21所示的另一实施方式中,微植入物被轴向叠加成柱,并一个接一个地输送到皮肤。由于施加在位于该柱顶部的微植入物上的压力,位于该柱底部的微植入物被迫使进入皮肤。这些微植入物可以完全相同或由不同材料制成或具有不同浓度的活性成分。例如,浓度从底部到顶部变化,以考虑到需要适时改变处理的强度。第一次注射输送浓度较小的微植入物,随着后续注射浓度逐渐增加。在变型中,第一次注射具有最高浓度,然后随着后续注射浓度降低。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1