生物体对药物的吸收性优异且化学稳定性也优异的医药组合物的制作方法
1.本发明涉及一种含有东莨菪碱的盐以及/或其水合物作为有效成分的医药组合物。
背景技术:
2.东莨菪碱作为抗胆碱能药物而广为人知,是具有抑制口腔内、呼吸道内分泌、预防有害的副交感神经反射等效果的药物。迄今为止,已开发出含有东莨菪碱作为有效成分的医药品,例如,在日本国内制造销售含有东莨菪碱的盐即东莨菪碱氢溴酸盐水合物作为有效成分的注射剂的“hysco(
ハイスコ
)(注册商标)皮下注射,杏林制药”,在海外制造销售含有东莨菪碱游离碱作为有效成分的贴剂“transdermscop(注册商标),novartis”。
3.众所周知,在细胞的周围存在脂双层(lipid bilayer),起到限制细胞内外的物质的透过性的屏障的作用,当然,水溶性的物质难以透过脂双层,脂溶性的物质容易透过脂双层。因此,除了能够避免带有脂双层的粘膜、表皮这样的生物体的屏障功能的注射剂以外,一般来说,就药物而言,脂溶性高的药物比水溶性高的药物更容易被吸收至细胞内并转移到血液中。作为东莨菪碱的盐的东莨菪碱氢溴酸盐水合物的水溶性高,为了转移至细胞内,必须作为脂溶性高的游离碱。然而,通常,药物从处理、化学稳定性方面考虑,优选为盐的状态。此外,在本说明书中,化学稳定性一词表示与化合物的分解相关的稳定性,物理稳定性一词表示与化合物的结晶析出相关的稳定性。
4.本发明的发明人发现,在尝试含有东莨菪碱的盐即东莨菪碱氢溴酸盐水合物的医药组合物的制造时,得到化学稳定性优异但生物体的吸收性低的医药组合物,另一方面,在尝试在制造中或医药组合物中将东莨菪碱氢溴酸盐水合物作为游离碱的医药组合物的制造时,得到生物体的吸收性优异但化学稳定性低的医药组合物。进而,本发明的发明人反复研究的结果表明,在医药组合物中的东莨菪碱的分解中,东莨菪碱的光学异构体以及阿朴东莨菪碱(aposcopolamine)是主要的分解生成物。
5.对于与生物体对东莨菪碱的吸收性、化学稳定性相关的技术,例如,在专利文献1中示出有如下的方法,即,针对含有产生以酸为触媒的分解反应的化合物的组合物,通过使用酸以外的吸收促进剂,在不使化学稳定性恶化的情况下提高生物体的吸收性。然而,并没有描述解决由酸以外的因素导致的化学稳定性恶化的方法。
6.在专利文献2中,示出有通过作为不含乙酸乙烯酯以及极性成分的组合物,在不使东莨菪碱的化学稳定性以及物理稳定性恶化的情况下提高生物体的吸收性的方法,但对于解决含有极性成分的组合物中的化学稳定性的恶化的方法没有任何描述。在从处理、化学稳定性的方面出发而使用东莨菪碱的盐的情况下,为了得到生物体对东莨菪碱的吸收性优异的医药组合物,需要在制造中或医药组合物中以使东莨菪碱的盐成为东莨菪碱游离碱为目的而含有作为极性成分的碱,因此不能适用该专利的方法。
7.在专利文献3、专利文献4以及专利文献5中,示出了提高东莨菪碱的物理稳定性来
维持或改善生物体的吸收性的方法,但关于提高化学稳定性的方法没有任何启示。
8.现有技术文献
9.专利文献
10.专利文献1:日本专利第4081139号
11.专利文献2:日本特表2009
‑
528357
12.专利文献3:美国专利第4832953号
13.专利文献4:日本专利第4466977号
14.专利文献5:日本专利第5695562号
技术实现要素:
15.发明要解决的问题
16.本发明是鉴于上述课题而完成的,其课题在于,提供一种医药组合物,含有具有高的生物体对东莨菪碱的吸收性且东莨菪碱的化学稳定性也优异的东莨菪碱的盐以及/或其水合物。
17.用于解决问题的手段
18.本发明的发明人为了解决上述课题而反复研究的结果表明,通过使在制造中或医药组合物中使东莨菪碱的盐以及/或其水合物成为游离碱的医药组合物中含有聚乙烯吡咯烷酮,维持高的生物体对东莨菪碱的吸收性,并提高化学稳定性。如所述专利文献5所记载的那样,聚乙烯吡咯烷酮使东莨菪碱的物理稳定性提高。一般来说,溶解状态以及非晶状态与结晶状态相比是化学性并不稳定的状态。因此,使医药组合物中含有聚乙烯吡咯烷酮在东莨菪碱的化学稳定性方面被认为是不利的。实际上,对于所述专利文献5所记载的、已知与聚乙烯吡咯烷酮同样地使东莨菪碱的物理稳定性提高的羟丙基纤维素而言,在医药组合物中含有该物质并没有提高东莨菪碱的化学稳定性的效果,相反,东莨菪碱的化学稳定性降低。然而,出人意料的是,在医药组合物中含有聚乙烯吡咯烷酮的情况下,东莨菪碱的化学稳定性提高,并抑制了作为主要分解物的东莨菪碱的光学异构体以及阿朴东莨菪碱两者的生成。进而,本发明的发明人明确了通过使用胺化合物作为在制造中或医药组合物中用于使东莨菪碱的盐以及/或其水合物成为游离碱的碱,可进一步提高东莨菪碱的化学稳定性。即,发现通过在含有东莨菪碱的盐以及/或其水合物的组合物中含有聚乙烯吡咯烷酮以及使用胺化合物作为用于使东莨菪碱的盐以及/或其水合物成为游离碱的碱,能够得到具有高的生物体对东莨菪碱的吸收性且提高了东莨菪碱的化学稳定性的医药组合物,从而完成本发明。
19.发明的效果
20.本发明的医药组合物(以下称为“本发明组合物”)具有高的生物体对东莨菪碱的吸收性且有效地抑制东莨菪碱的分解,因此能够有效且持续地利用东莨菪碱的药理效果。
具体实施方式
21.本发明组合物是含有作为有效成分的东莨菪碱((
‑
)
‑
(s)
‑3‑
羟基
‑2‑
苯基丙酸(1r,2r,4s,7s,9s)
‑9‑
甲基
‑3‑
氧杂
‑9‑
氮杂三环[3.3.1.0
2,4
]壬烷
‑7‑
基酯)的盐以及/或其水合物、聚乙烯吡咯烷酮以及碱的医药组合物。
[0022]
作为本发明组合物所使用的东莨菪碱的盐,例如,可列举与无机酸或有机酸的酸加成盐(acid addition salt),具体来说,可列举盐酸盐、氢溴酸盐、硝酸盐、磷酸盐、硫酸盐、乙酸盐、抗坏血酸盐、安息香酸盐、桂皮酸盐、柠檬酸盐、甲酸盐、富马酸盐、谷氨酸盐、乳酸盐、马来酸盐、苹果酸盐、丙二酸盐、扁桃酸盐、甲磺酸盐(甲磺酸酯)、邻苯二甲酸盐、水杨酸盐、硬脂酸盐、琥珀酸盐、酒石酸盐、丙酸盐、丁酸盐、帕莫酸盐(pamoate)、对甲苯磺酸盐(甲苯磺酸酯)等,但并不限定于此。在本发明组合物中,优选使用东莨菪碱氢溴酸盐以及/或东莨菪碱氢溴酸盐水合物。
[0023]
本发明组合物含有有效治疗量的东莨菪碱的盐以及/或其水合物即可,其状态没有特别限定,但从生物体的吸收性的观点出发,优选溶解状态、非晶状态。为了向患者施用对治疗有效的量的有效成分,在组合物中含有某一定量的有效成分是很重要的。本发明组合物中东莨菪碱的盐以及/或其水合物的含量相对于组合物整体为0.5~10质量%,优选为1~8质量%,更优选为3~6质量%。在不足0.5质量%的情况下,治疗效果可能会不充分,另一方面,在超过10质量%的量的情况下,存在经济性不利的情况。
[0024]
本发明组合物为了提高东莨菪碱的化学稳定性而含有聚乙烯吡咯烷酮。一般所使用的聚乙烯吡咯烷酮的重量平均分子量存在数千至数百万,但本发明组合物中所使用的聚乙烯吡咯烷酮的重量平均分子量没有特别限定。这些聚乙烯吡咯烷酮能够使用一种以上。
[0025]
本发明组合物中聚乙烯吡咯烷酮的含量相对于组合物整体为0.3~12质量%,优选为0.5~10质量%,更优选为1~8质量%的范围。在不足0.3质量%的情况下,有可能无法得到充分的化学稳定性提高效果,另一方面,在超过12质量%的量的情况下,有可能对组合物的物理特性造成恶劣影响,因而不优选。另外,聚乙烯吡咯烷酮相对于东莨菪碱的盐以及/或其水合物的质量比为2以上的情况下,有可能对组合物的均匀性造成恶劣影响,所以优选聚乙烯吡咯烷酮相对于东莨菪碱的盐以及/或其水合物的质量比不足2。
[0026]
本发明组合物含有用于使东莨菪碱的盐以及/或其水合物成为游离碱的碱。碱的种类没有特别限定,例如,可列举胺化合物、氨、碱金属的氢氧化物等。在这些碱中,就化学稳定性的方面而言,也优选胺化合物。
[0027]
胺化合物可以是伯胺、仲胺、叔胺中的任一种,作为伯胺,可以列举甲胺、乙胺、十二胺等,作为仲胺,可以列举二甲胺、二乙胺、n
‑
甲基乙胺等,作为叔胺,可以列举n,n
‑
二乙基甲胺、三丁胺、n,n
‑
二甲基
‑
对甲苯胺、n,n
‑
二乙基
‑
对甲苯胺、甲基丙烯酸甲酯
‑
甲基丙烯酸丁酯
‑
甲基丙烯酸二甲氨基乙酯共聚物等,但并不限定于此。这些胺化合物能够使用至少一种。另外,在这些胺化合物中,优选甲基丙烯酸甲酯
‑
甲基丙烯酸丁酯
‑
甲基丙烯酸二甲氨基乙酯共聚物。另外,作为碱金属的氢氧化物,可以列举氢氧化钠、氢氧化钾等,但并不限定于此。
[0028]
本发明组合物中碱的含量相对于组合物整体为0.3~10质量%,优选为0.5~8.5质量%,更优选为0.9~7.5质量%的范围。在不足0.3质量%的情况下,有可能无法得到充分的生物体的吸收性,另一方面,在超过10质量%的情况下,有可能对化学稳定性造成恶劣影响。
[0029]
本发明组合物的制造方法没有特别限定,例如,将上述必需成分搅拌混合即可。另外,也可以根据需要而添加乙酸乙酯、甲醇等溶剂。
[0030]
以上说明的本发明组合物能够代替以往的医药组合物的有效成分等来进行调配。
作为本发明组合物的剂型,可以列举口服剂、注射剂、外用剂等,但并不限定于此。在这些剂型中,优选易于施用的外用剂。
[0031]
作为外用剂,可以列举撒布粉剂、洗剂、软膏剂、乳膏剂、喷雾剂、液剂、贴剂、气雾剂、肛门栓剂、滴耳剂、滴眼剂、滴鼻剂、吸入剂等,但并不限定于此。在它们当中,由于不需要进行擦拭、调节施用量等复杂的操作,由于能够稳定地保持有效成分的血中浓度,因而效果时间长,在发现有害事象时通过剥离就可以简单地进行施用的中断,因此优选贴剂。
[0032]
作为贴剂,可列举基质型、储库型(reservoir type)。本发明组合物可以是基质型或储库型中的任一种,但由于制剂设计容易且能够降低制造时的成本,因而优选基质型。
[0033]
基质型的贴剂由支撑体、含药物粘合剂层、剥离衬垫构成(以下,将其称为“本发明贴剂”)。
[0034]
含药物粘合剂层含有本发明组合物即可,但优选进一步含有基剂成分。该含药物粘合剂层所使用的基剂成分没有特别地限定,但优选橡胶类粘接成分、丙烯酸类粘接成分、硅酮类粘接成分等一般情况下用于贴剂的粘接成分,特别优选丙烯酸类粘接成分,更优选非极性型的丙烯酸类粘接成分以及含羟基型的丙烯酸类粘接成分。这些基剂成分能够使用至少一种。
[0035]
丙烯酸类粘接成分是含有至少一种(甲基)丙烯酸酯的聚合物或共聚物。
[0036]
非极性型丙烯酸类粘接成分在单体构成单元中的侧链不具有官能团,例如可以列举(甲基)丙烯酸烷基酯聚合物或共聚物、(甲基)丙烯酸烷基酯
‑
乙酸乙烯酯共聚物等,具体来说,可以列举丙烯酸
‑2‑
乙基己酯
‑
甲基丙烯酸
‑2‑
乙基己酯
‑
甲基丙烯酸十二烷基酯共聚物、丙烯酸
‑2‑
乙基己酯
‑
乙酸乙烯酯共聚物、甲基丙烯酸甲酯
‑
甲基丙烯酸丁酯
‑
甲基丙烯酸二甲氨基乙酯共聚物等,但并不限定于此。
[0037]
含羟基型丙烯酸类粘接成分是将在单体构成单元中的侧链中含有游离羟基的(甲基)丙烯酸酯的至少一种作为构成单元的聚合物或共聚物,例如,可以列举含有(甲基)丙烯酸羟烷基酯的共聚物等,具体来说,丙烯酸
‑2‑
乙基己酯
‑
丙烯酸羟基乙酯
‑
乙酸乙烯酯共聚物、丙烯酸
‑2‑
乙基己酯、乙烯吡咯烷酮
‑
丙烯酸羟基乙酯
‑
乙酸乙烯酯共聚物、丙烯酸
‑2‑
乙基己酯
‑
丙烯酸羟基乙酯
‑
乙酸乙烯酯共聚物、丙烯酸
‑2‑
乙基己酯
‑
丙烯酸羟基乙酯
‑
丙烯酸缩水甘油
‑
乙酸乙烯酯共聚物、丙烯酸
‑2‑
乙基己酯
‑
乙酸乙烯酯
‑
丙烯酸
‑2‑
羟基乙酯共聚物、丙烯酸
‑2‑
乙基己酯
‑
乙酸乙烯酯
‑
丙烯酸
‑2‑
羟基乙酯
‑
甲基丙烯酸缩水甘油共聚物等,但并不限定于此。
[0038]
考虑到含药物粘合剂层的形成以及充分的药物释放性,含药物粘合剂层中的基剂成分的含量相对于含药物粘合剂层整体为60~98.9质量%,优选为63~98质量%,更优选为66~96质量%。在不足60质量%的情况下,锚定性等贴剂的物理特性降低,另外,在超过98.9%的量的情况下,则不能充分调配有效成分以及其他的添加剂,有时不优选。
[0039]
在含药物粘合剂层中,也可以根据需要而含有吸收促进剂。作为吸收促进剂,可以是任一种以往经皮施用时被认为具有吸收促进作用的化合物,例如可以列举月桂酸、油酸、异硬脂酸、肉豆蔻酸异丙酯、肉豆蔻酸辛基十二烷基酯、甘油油酸单酯、异硬脂酸己基葵基酯等脂肪酸以及其酯类、油醇、丙二醇、聚乙二醇单油酸酯等醇及其酯类或醚类、失水山梨糖醇倍半油酸酯,聚氧乙烯失水山梨糖醇单油酸酯、失水山梨糖醇单月桂酸酯、失水山梨糖醇单油酸酯等失水山梨糖醇酯类或醚类、聚氧乙烯壬基苯基醚、聚氧乙烯辛基苯基醚等酚
醚类、蓖麻油或硬化蓖麻油、油酰肌氨酸、月桂精二甲氨基乙酸甜菜碱(laurindimethylamino acetatebetaine)、月桂基硫酸钠等离子性表面活性剂、聚氧乙烯油基醚、聚氧乙烯月桂基醚等非离子性表面活性剂、二甲基亚砜、葵基甲基亚砜(decylmethyl sulfoxide)等烷基甲基亚砜、1
‑
十二烷基氮杂环庚烷
‑2‑
酮(1
‑
dodecylazacyclo heptan
‑2‑
one)、1
‑
香叶基氮杂环庚烷
‑2‑
酮等氮杂环烷烃类、除聚乙烯吡咯烷酮以外的吡咯烷酮等。
[0040]
本发明贴剂所使用的支撑体没有特别限定,例如能够使用药物不透过性且伸缩性或非伸缩性的支撑体。作为支撑体,例如可以列举聚乙烯、聚丙烯、聚丁二烯、乙烯乙酸乙烯酯共聚物、聚氯乙烯、聚酯(聚对苯二甲酸乙二醇酯等)、尼龙、聚氨酯等合成树脂膜或片或它们的层叠体、多孔质体、发泡体、纸、纺布、无纺布等。
[0041]
本发明贴剂所使用的剥离衬垫没有特别限定,例如能够使用药物不透过性的剥离衬垫。作为剥离衬垫,例如可以列举聚乙烯、聚丙烯、聚酯等高分子材料所制作的膜、在膜上蒸镀了铝的膜、在纸上涂布了硅油等的纸。其中,从有效成分无法透过、加工性、低成本等方面出发,优选聚酯膜,特别优选聚对苯二甲酸乙二醇酯(pet)膜。进而,剥离衬垫也可以使用将多个材料贴合而成的层压膜等。
[0042]
本发明贴剂在使用之前保存于包装材料中。本发明贴剂所使用的包装材料没有特别限定,可以列举塑料膜、金属(铝等)层叠塑料膜、金属蒸镀塑料膜、陶瓷(氧化硅等)蒸镀塑料膜、铝箔等金属箔、不锈钢等金属、玻璃等。其中,从制造成本等方面出发,优选使用金属层叠塑料膜、金属蒸镀塑料膜等。
[0043]
在本发明贴剂中,为了控制有效成分的经皮吸收,还可以根据需要而在含药物粘合剂层的皮肤粘贴侧追加释放控制膜、用于向皮肤粘贴的粘接层。
[0044]
以上说明的本发明贴剂由支撑体、含药物粘合剂层以及剥离衬垫构成,但是就厚度而言,支撑体为1~1000μm,优选为10~700μm,含药物粘合剂层为10~200μm,优选为30~150μm,剥离衬垫为1~500μm,优选为10~200μm。
[0045]
本发明贴剂能够按照公知的贴剂的制造方法来制造。作为本发明贴剂的优选制造方法,例如可以列举以下的方法。
[0046]
<方法1>
[0047]
使作为有效成分的东莨菪碱的盐以及/或其水合物、碱、聚乙烯吡咯烷酮、基剂成分、根据需要而进一步添加的吸收促进剂等溶解于例如乙酸乙酯、甲醇等有机溶剂或它们的混合溶剂中,将得到的溶解物在剥离衬垫或支撑体上展延,使溶解物中的有机溶剂蒸发而形成含药物粘合剂层后,通过贴合支撑体或剥离衬垫而得到贴剂。
[0048]
<方法2>
[0049]
使作为有效成分的东莨菪碱的盐以及/或其水合物、碱、聚乙烯吡咯烷酮、基剂成分、根据需要而进一步添加的吸收促进剂等加热溶解,将该溶融物在剥离衬垫或支撑体上展延,在形成含药物粘合剂层后,通过贴合支撑体或剥离衬垫而得到贴剂。
[0050]
实施例
[0051]
以下,将示出制造例等进一步地对本发明进行具体地说明,但本发明并不限定于这些制造例等,在不超出本发明的技术思想的范围内能够进行多种变更。
[0052]
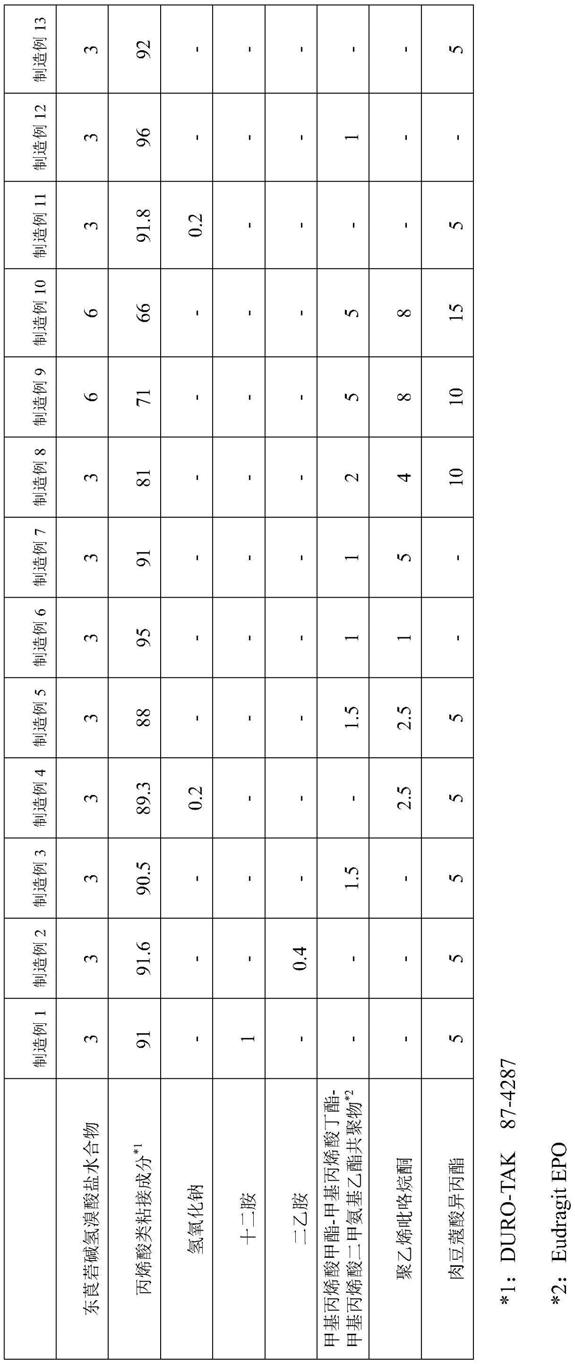
制造例1
[0053]
按照表1所记载的调配比,使东莨菪碱氢溴酸盐水合物、肉豆蔻酸异丙酯、十二胺溶解于乙酸乙酯/甲醇混合液中,添加丙烯酸类粘接成分(商品名:duro
‑
tak87
‑
4287,汉高(henkel)生产)并混合搅拌,得到均匀的溶解物。接下来,将该溶解物使用刮刀涂布机以干燥后的厚度成为100μm的方式延展成剥离膜,干燥并形成含药物粘合剂层后,贴合支撑体。之后,裁剪成所希望的大小而得到贴剂。
[0054]
制造例2
[0055]
按照表1所记载的调配比,除了以使东莨菪碱游离碱的量与制造例1等量的方式调配二乙胺代替十二胺之外,与制造例1同样地得到贴剂。
[0056]
制造例3
[0057]
按照表1所记载的调配比,除了以使东莨菪碱游离碱的量与制造例1等量的方式调配甲基丙烯酸甲酯
‑
甲基丙烯酸丁酯
‑
甲基丙烯酸二甲氨基乙酯共聚物(商品名:eudragit epo,赢创(evonik)生产)代替十二胺之外,与制造例1同样地得到贴剂。
[0058]
制造例4
[0059]
按照表1所记载的调配比,除了以使东莨菪碱游离碱的量与制造例1等量的方式调配氢氧化钠代替十二胺,再调配聚乙烯吡咯烷酮(商品名:kollidon30,basfse生产)之外,与制造例1同样地得到贴剂。
[0060]
制造例5
[0061]
按照表1所记载的调配比,除了以使东莨菪碱游离碱的量与制造例1等量的方式调配eudragit epo代替十二胺,再调配聚乙烯吡咯烷酮之外,与制造例1同样地得到贴剂。
[0062]
制造例6
[0063]
按照表1所记载的调配比,使东莨菪碱氢溴酸盐水合物、eudragit epo、聚乙烯吡咯烷酮溶解于乙酸乙酯/甲醇混合液中,添加duro
‑
tak87
‑
4287并混合搅拌,得到均匀的溶解物。接下来,将该溶解物使用刮刀涂布机以干燥后的厚度成为100μm的方式延展成剥离膜,干燥并形成含药物粘合剂层后,贴合支撑体。之后,裁剪成所希望的大小而得到贴剂。
[0064]
制造例7
[0065]
按照表1所记载的调配比,除了增加聚乙烯吡咯烷酮的调配量之外,与制造例6同样地得到贴剂。
[0066]
制造例8
[0067]
按照表1所记载的调配比,使东莨菪碱氢溴酸盐水合物、肉豆蔻酸异丙酯、eudragit epo、聚乙烯吡咯烷酮溶解于乙酸乙酯/甲醇混和液中,添加duro
‑
tak87
‑
4287并混合搅拌,得到均匀的溶解物。接下来,将该溶解物使用刮刀涂布机以干燥后的厚度成为100μm的方式延展成剥离膜,在干燥而形成含药物粘合剂层后,贴合支撑体。之后,裁剪成所希望的大小而得到贴剂。
[0068]
制造例9
[0069]
按照表1所记载的调配比,使东莨菪碱氢溴酸盐水合物、肉豆蔻酸异丙酯、eudragit epo、聚乙烯吡咯烷酮溶解于乙酸乙酯/甲醇混合液中,添加duro
‑
tak87
‑
4287并混合搅拌,得到均匀的溶解物。接下来,将该溶解物使用刮刀涂布机以干燥后的厚度成为50μm的方式延展成剥离膜,在干燥而形成含药物粘合剂层后,贴合支撑体。之后,裁剪成所希望的大小而得到贴剂。
[0070]
制造例10
[0071]
按照表1所记载的调配比,除了增加肉豆蔻酸异丙酯的调配量之外,与制造例9同样地得到贴剂。
[0072]
制造例11
[0073]
按照表1所记载的调配比,除了以使东莨菪碱游离碱的量与制造例1等量的方式调配氢氧化钠代替十二胺外,与制造例1同样地得到贴剂。
[0074]
制造例12
[0075]
按照表1所记载的调配比,除了未调配聚乙烯吡咯烷酮之外,与制造例6同样地得到贴剂。
[0076]
制造例13
[0077]
按照表1所记载的调配比,除了未调配十二胺之外,与制造例1同样地得到贴剂。
[0078]
[表1]
pax生产)的袋中,利用恒温恒湿器(温度:60℃,csh
‑
110,tabai espec生产)保存3天或28天,测定作为主要的分解物的光学异构体的量。对于3块各贴剂,除去衬垫,取至10ml离心沉淀管中,加入四氢呋喃1ml以及甲醇0.5ml,振动10分钟,使膏体完全溶解。向该液体中加入水1ml,振动10分钟,使粘接基剂成分完全凝聚、沉淀。将该上清液作为试样溶液,利用高效液相色谱法(测定波长:210nm)进行定量。将利用该方法测定出的保存后的光学异构体的量示于表2以及表3中。
[0082]
试验例2(化学稳定性试验2)
[0083]
将由制造例1~13得到的各贴剂充填至复合膜(最内层热封pet的铝层压膜、meiwa pax生产)的袋中,利用恒温恒湿器(温度:60℃,csh
‑
110,tabai espec生产)保存3天或28天,测定作为主要的分解物的阿朴东莨菪碱的量。对于3块各贴剂,除去衬垫,取至10ml离心沉淀管中,加入四氢呋喃1ml以及甲醇0.5ml,振动10分钟,使膏体完全溶解。向该液体中加入水1ml,振动10分钟,使粘接基剂成分完全凝聚、沉淀。将该上清液作为试样溶液,利用高效液相色谱法(测定波长:220nm)进行定量。将利用该方法测定出的保存后的阿朴东莨菪碱的量示于表2以及表3中。
[0084]
试验例3(释放试验)
[0085]
针对由制造例5、制造例8、制造例9、制造例10以及制造例13得到的各贴剂,测定来自贴剂的东莨菪碱的释放率。将各贴剂以直径15mm的皮冲头(leather punch)进行裁剪,粘贴在滤纸上,在其上贴上覆盖用胶带,以使试验片成为中心的方式使用直径23mm的皮冲头进行裁剪,使用经皮吸收试验装置(trans view c 12,cosmed制药生产)实施释放试验。经皮吸收试验装置的操作如下:在扩散池内放入搅拌器,将试验片和扩散池孔对齐地设置,从其上方安装套环和盖,向扩散池的接收槽中注入保温为32℃的试验液(在水1000ml中溶解磷酸二氢钾3.40g以及无水磷酸氢二钠3.55g),将扩散池放入加热块恒温槽(温度:32
±
2℃),对24小时后的试样溶液采样,利用高效液相色谱(测定波长:210nm)进行定量。将利用该方法测定的各贴剂中的东莨菪碱的24小时后的释放率示于表4中。
[0086]
试验例4(调配试验)
[0087]
调制以使东莨菪碱游离碱与聚乙烯吡咯烷酮的调配比为1:0、2:1、1:1、1:2的方式而调配的药物溶液(制造例14~17)。针对得到的各药物溶液,取至10ml离心沉淀管中,利用热风干燥器(温度:70℃,lc
‑
110,tabai espec生产)保存1天,利用高效液相色谱(测定波长:210nm以及220nm)对保存后的光学异构体以及阿朴东莨菪碱的量进行定量。将利用该方法测定的保存后的光学异构体以及阿朴东莨菪碱的量示于表5中。
[0088]
[表2]
[0089][0090]
[表3]
[0091][0092]
[表4]
[0093] 释放率(%、24小时后)制造例133.4制造例554.8制造例638.6制造例735.7制造例882.0制造例980.0制造例1082.2
[0094]
[表5]
[0095][0096]
与制造例11(使用氢氧化钠进行游离碱化)相比,在使用胺化合物作为用于使东莨菪碱成为游离碱的碱的制造例1(使用十二胺进行游离碱化)、制造例2(使用二乙胺进行游离碱化)、制造例3(使用eudragit epo进行游离碱化)中,光学异构体以及阿朴东莨菪碱的量少。根据以上结果可以看出,使用胺化合物作为用于使东莨菪碱的盐以及/或其水合物成为游离碱的碱,对于提高东莨菪碱的化学稳定性是有效的。
[0097]
在调配试验中,通过调配聚乙烯吡咯烷酮(制造例15~17),与不调配聚乙烯吡咯烷酮的情况(制造例14)相比,光学异构体以及阿朴东莨菪碱的量减少。另外,随着聚乙烯吡咯烷酮相对于东莨菪碱游离碱的调配比增加,光学异构体以及阿朴东莨菪碱的量减少。根据以上结果可以看出,聚乙烯吡咯烷酮的调配对于提高东莨菪碱的化学稳定性是有效的。
[0098]
与制造例11相比,在调配了聚乙烯吡咯烷酮的制造例4中,光学异构体以及阿朴东莨菪碱的量少。另外,与制造例3相比,在调配了聚乙烯吡咯烷酮的制造例5中,光学异构体以及阿朴东莨菪碱的量少。进而,与制造例12相比,在调配了聚乙烯吡咯烷酮的制造例6以及制造例7中,光学异构体以及阿朴东莨菪碱的量少。根据以上结果可以看出,即使在选择贴剂作为剂型的情况下,聚乙烯吡咯烷酮的调配对于提高东莨菪碱的化学稳定性也是有效的。
[0099]
制造例8是以东莨菪碱游离碱的量成为制造例12的2倍的方式增加eudragit epo
的量且化学稳定性的条件比制造例12更严苛的处方。另外,制造例9以及制造例10是以东莨菪碱游离碱的量成为制造例12的4.7倍的方式增加东莨菪碱氢溴酸盐水合物以及eudragit epo的量且化学稳定性的条件比制造例12更严苛的处方。在该条件下,与制造例12相比,聚乙烯吡咯烷酮的调配不能抑制光学异构体的量的增加,但阿朴东莨菪碱的量减少,分解物的量的合计也减少。根据上述结果可以看出,聚乙烯吡咯烷酮的调配即使在化学稳定性过于严苛的条件下对于提高东莨菪碱的化学稳定性也是有效的。
[0100]
与制造例13相比,在制造例5、制造例6、制造例7、制造例8、制造例9以及制造例10中,24小时后的释放率高。根据以上结果可以看出,使用胺化合物作为碱来使东莨菪碱氢溴酸盐成为游离碱对于提高生物体的吸收性是有效的。
[0101]
产业上的可利用性
[0102]
如上所述,本发明组合物是通过使含有东莨菪碱的盐以及/或其水合物的组合物中含有聚乙烯吡咯烷酮以及碱而制造的医药组合物,是具有高的生物体的吸收性且东莨菪碱的化学稳定性优异的新型医药组合物。本发明组合物能够有效且持续地利用东莨菪碱的药理效果。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1