结合BCMA的抗原结合蛋白的制作方法
结合bcma的抗原结合蛋白
1.对相关申请的交叉引用
2.本技术要求根据35u.s.c.
§
119对2019年2月26日提交的美国临时申请第62/810,771号和2019年2月27日提交的美国临时申请第62/811,431号享有优先权。所有上述申请的公开内容以全文引用的方式并入。
3.在整个本技术中,引用了各种出版物、专利和/或专利申请。所述出版物、专利和/或专利申请的公开内容在此以全文引用的方式并入本技术中,以便更全面地描述本公开所涉及的目前先进技术。
技术领域
4.本公开提供了与b细胞成熟抗原(bcma)特异性结合的抗原结合蛋白和编码所述抗原结合蛋白的核酸、包含所述核酸的载体、携带所述载体的宿主细胞及其使用方法。
背景技术:
5.b细胞成熟抗原(bcma),也称为tnfrsf17和cd269(uniprot q02223),是肿瘤坏死受体超家族的成员。bcma是一种在分化的浆细胞上表达的非糖基化iii型跨膜蛋白(laabi等人,1992 the embo journal 11(11):3897
‑
3904;laabi等人,1994nucleic acids research 22(7):1147
‑
1154;madry等人,1998international immunology 10(11):1693
‑
1702),并且是一种参与b细胞发育和存活的细胞表面受体。
6.bcma是tnf超家族的两个配体april(增殖诱导配体,a proliferation
‑
inducing ligand)和baff的细胞表面受体。april和baff分别是bcma的高亲和力和低亲和力配体。april是增殖诱导配体,baff是b淋巴细胞刺激因子。taci是结合april和baff的负调控因子。april和baff与bcma和/或taci的协同结合诱导因子nf
‑
κb的转录,增加促存活bcl
‑
2家族成员的表达,并下调促凋亡因子的表达,从而促进存活并抑制凋亡。这种复杂的相互作用促进b细胞的分化、增殖、存活和抗体产生(rickert 2011 immunology review 244(1):115
‑
133)。已知bcma支持恶性人b细胞的生长和存活,且据报道,bcma和taci在包括多发性骨髓瘤(mm)细胞的恶性人b细胞中的表达上调(参见mackay等人在“baff和april:b细胞存活教程(baff and april:a tutorial on b cell survival)”中的综述,2004 annual review immunology 21:231
‑
264)。此外,据报道,bcma、april和baff信号传导在b细胞肿瘤和多发性骨髓瘤中激活nfκb。
7.多发性骨髓瘤是一种克隆性b细胞淋巴瘤,其在骨髓的多个部位出现,然后通过循环扩散。与正常组织相比,bcma在多发性骨髓瘤细胞中的表达水平显著较高,这使得bcma成为免疫疗法的良好靶抗原。因此,bcma是一种有吸引力的抗体靶向抗原。本公开提供了特异性结合bcma的bcma结合蛋白,特别是抗bcma抗体或其抗原结合部分,及其用途。
技术实现要素:
8.本公开提供了一种全人抗bcma抗体或其抗原结合片段,其包含重链和轻链,其中
no:91的氨基酸序列的λ轻链cdr3。
9.本公开提供了一种全人抗bcma抗体或其抗原结合片段,其包含重链和轻链,所述重链包含与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性的重链可变区;并且所述轻链包含与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性的轻链可变区。
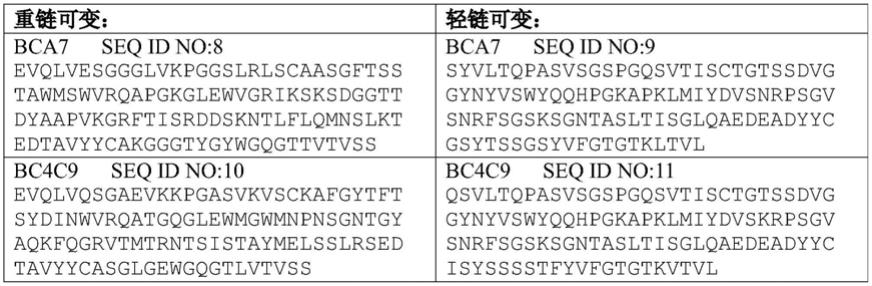
10.本公开提供了一种全人抗bcma抗体或其抗原结合片段,其包含重链可变区和轻链可变区,其中所述重链可变区和所述轻链可变区包含seq id no:8和9(例如,本文称为bca7);seq id no:10和11(例如,本文称为bc4c9);seq id no:12和13(例如,本文称为cd5c4);seq id no:14和15(例如,本文称为bc6g8);seq id no:8和16(例如,本文称为bca7
‑
2c5);seq id no:8和17(例如,本文称为bca7
‑
2e1);seq id no:8和18(例如,本文称为bca7
‑
2d11);seq id no:8和19(例如,本文称为bca7
‑
2g2);seq id no:8和20(例如,本文称为bca7
‑
2d8);seq id no:8和21(例如,本文称为bca7
‑
2e8);或seq id no:22和23(例如,本文称为具有λ轻链的bca7
‑
2c5)的氨基酸序列。
11.本公开提供了一种全人抗bcma抗体或其抗原结合片段,其中所述抗原结合片段是fab片段,其包含来自重链的可变域区和来自轻链的可变域区,其中(a)所述来自重链的可变域区包含:具有seq id no:29的氨基酸序列的重链互补决定区1(cdr1)、具有seq id no:30的氨基酸序列的重链cdr2、具有seq id no:31的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:32的氨基酸序列的轻链cdr1、具有seq id no:33的氨基酸序列的轻链cdr2和具有seq id no:34的氨基酸序列的轻链cdr3;其中(b)所述来自重链的可变域区包含:具有seq id no:35的氨基酸序列的重链cdr1、具有seq id no:36的氨基酸序列的重链cdr2、具有seq id no:37的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:38的氨基酸序列的轻链cdr1、具有seq id no:39的氨基酸序列的轻链cdr2和具有seq id no:40的氨基酸序列的轻链cdr3;其中(c)所述来自重链的可变域区包含:具有seq id no:41的氨基酸序列的重链cdr1、具有seq id no:42的氨基酸序列的重链cdr2、具有seq id no:43的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:44的氨基酸序列的轻链cdr1、具有seq id no:45的氨基酸序列的轻链cdr2和具有seq id no:46的氨基酸序列的轻链cdr3;其中(d)所述来自重链的可变域区包含:具有seq id no:47的氨基酸序列的重链cdr1、具有seq id no:48的氨基酸序列的重链cdr2、具有seq id no:49的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:50的氨基酸序列的轻链cdr1、具有seq id no:51的氨基酸序列的轻链cdr2和具有seq id no:52的氨基酸序列的轻链cdr3;其中(e)所述来自重链的可变域区包含:具有seq id no:53的氨基酸序列的重链cdr1、具有seq id no:54的氨基酸序列的重链cdr2、具有seq id no:55的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:56的氨基酸序列的轻链cdr1、具有seq id no:57的氨基酸序列的轻链cdr2和具有seq id no:58的氨基酸序列的轻链cdr3;其中(f)所述来自重链的可变域区包含:具有seq id no:59的氨基酸序列的重链cdr1、具有seq id no:60的氨基酸序列的重链cdr2、具有seq id no:61的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:62的氨基酸序列的轻链cdr1、具有seq id no:63的氨基酸序列的轻链cdr2和具有seq id no:64的氨基酸序列的轻链cdr3;其中(g)所述来自重链的可变域区包含:具有
seq id no:65的氨基酸序列的重链cdr1、具有seq id no:66的氨基酸序列的重链cdr2、具有seq id no:67的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:68的氨基酸序列的轻链cdr1、具有seq id no:69的氨基酸序列的轻链cdr2和具有seq id no:70的氨基酸序列的轻链cdr3;其中(h)所述来自重链的可变域区包含:具有seq id no:71的氨基酸序列的重链cdr1、具有seq id no:72的氨基酸序列的重链cdr2、具有seq id no:73的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:74的氨基酸序列的轻链cdr1、具有seq id no:75的氨基酸序列的轻链cdr2和具有seq id no:76的氨基酸序列的轻链cdr3;其中(i)所述来自重链的可变域区包含:具有seq id no:77的氨基酸序列的重链cdr1、具有seq id no:78的氨基酸序列的重链cdr2、具有seq id no:79的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:80的氨基酸序列的轻链cdr1、具有seq id no:81的氨基酸序列的轻链cdr2和具有seq id no:82的氨基酸序列的轻链cdr3;其中(j)所述来自重链的可变域区包含:具有seq id no:83的氨基酸序列的重链cdr1、具有seq id no:84的氨基酸序列的重链cdr2、具有seq id no:85的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:86的氨基酸序列的轻链cdr1、具有seq id no:87的氨基酸序列的轻链cdr2和具有seq id no:88的氨基酸序列的轻链cdr3;或其中(k)所述来自重链的可变域区包含:具有seq id no:53的氨基酸序列的重链cdr1、具有seq id no:54的氨基酸序列的重链cdr2、具有seq id no:55的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:89的氨基酸序列的λ轻链cdr1、具有seq id no:90的氨基酸序列的λ轻链cdr2和具有seq id no:91的氨基酸序列的λ轻链cdr3。
12.本公开提供了一种全人抗bcma抗体或其抗原结合片段,其中所述抗原结合片段是fab片段,其包含来自重链的可变域区和来自轻链的可变域区,其中所述来自重链的可变域区包含与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性的序列,并且其中所述来自轻链的可变域区包含与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性的序列。
13.本公开提供了一种全人抗bcma抗体或其抗原结合片段,其中所述抗原结合片段是fab片段,其包含来自重链的可变域区和来自轻链的可变域区,其中所述来自重链的可变域区和所述来自轻链的可变域区是seq id no:8和9(例如,本文称为bca7);seq id no:10和11(例如,本文称为bc4c9);seq id no:12和13(例如,本文称为cd5c4);seq id no:14和15(例如,本文称为bc6g8);seq id no:8和16(例如,本文称为bca7
‑
2c5);seq id no:8和17(例如,本文称为bca7
‑
2e1);seq id no:8和18(例如,本文称为bca7
‑
2d11);seq id no:8和19(例如,本文称为bca7
‑
2g2);seq id no:8和20(例如,本文称为bca7
‑
2d8);seq id no:8和21(例如,本文称为bca7
‑
2e8);或seq id no:22和23(例如,本文称为具有λ轻链的bca7
‑
2c5)。
14.本公开提供了一种全人抗bcma抗体或其抗原结合片段,其中所述抗原结合片段是单链抗体,其包含通过肽接头连接在一起的来自重链的可变域区和来自轻链的可变域区,其中(a)所述来自重链的可变域区包含:具有seq id no:29的氨基酸序列的重链互补决定区1(cdr1)、具有seq id no:30的氨基酸序列的重链cdr2、具有seq id no:31的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:32的氨基酸序列的轻链
cdr1、具有seq id no:33的氨基酸序列的轻链cdr2和具有seq id no:34的氨基酸序列的轻链cdr3;其中(b)所述来自重链的可变域区包含:具有seq id no:35的氨基酸序列的重链cdr1、具有seq id no:36的氨基酸序列的重链cdr2、具有seq id no:37的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:38的氨基酸序列的轻链cdr1、具有seq id no:39的氨基酸序列的轻链cdr2和具有seq id no:40的氨基酸序列的轻链cdr3;其中(c)所述来自重链的可变域区包含:具有seq id no:41的氨基酸序列的重链cdr1、具有seq id no:42的氨基酸序列的重链cdr2、具有seq id no:43的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:44的氨基酸序列的轻链cdr1、具有seq id no:45的氨基酸序列的轻链cdr2和具有seq id no:46的氨基酸序列的轻链cdr3;其中(d)所述来自重链的可变域区包含:具有seq id no:47的氨基酸序列的重链cdr1、具有seq id no:48的氨基酸序列的重链cdr2、具有seq id no:49的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:50的氨基酸序列的轻链cdr1、具有seq id no:51的氨基酸序列的轻链cdr2和具有seq id no:52的氨基酸序列的轻链cdr3;其中(e)所述来自重链的可变域区包含:具有seq id no:53的氨基酸序列的重链cdr1、具有seq id no:54的氨基酸序列的重链cdr2、具有seq id no:55的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:56的氨基酸序列的轻链cdr1、具有seq id no:57的氨基酸序列的轻链cdr2和具有seq id no:58的氨基酸序列的轻链cdr3;其中(f)所述来自重链的可变域区包含:具有seq id no:59的氨基酸序列的重链cdr1、具有seq id no:60的氨基酸序列的重链cdr2、具有seq id no:61的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:62的氨基酸序列的轻链cdr1、具有seq id no:63的氨基酸序列的轻链cdr2和具有seq id no:64的氨基酸序列的轻链cdr3;其中(g)所述来自重链的可变域区包含:具有seq id no:65的氨基酸序列的重链cdr1、具有seq id no:66的氨基酸序列的重链cdr2、具有seq id no:67的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:68的氨基酸序列的轻链cdr1、具有seq id no:69的氨基酸序列的轻链cdr2和具有seq id no:70的氨基酸序列的轻链cdr3;其中(h)所述来自重链的可变域区包含:具有seq id no:71的氨基酸序列的重链cdr1、具有seq id no:72的氨基酸序列的重链cdr2、具有seq id no:73的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:74的氨基酸序列的轻链cdr1、具有seq id no:75的氨基酸序列的轻链cdr2和具有seq id no:76的氨基酸序列的轻链cdr3;其中(i)所述来自重链的可变域区包含:具有seq id no:77的氨基酸序列的重链cdr1、具有seq id no:78的氨基酸序列的重链cdr2、具有seq id no:79的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:80的氨基酸序列的轻链cdr1、具有seq id no:81的氨基酸序列的轻链cdr2和具有seq id no:82的氨基酸序列的轻链cdr3;其中(j)所述来自重链的可变域区包含:具有seq id no:83的氨基酸序列的重链cdr1、具有seq id no:84的氨基酸序列的重链cdr2、具有seq id no:85的氨基酸序列的重链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:86的氨基酸序列的轻链cdr1、具有seq id no:87的氨基酸序列的轻链cdr2和具有seq id no:88的氨基酸序列的轻链cdr3;或其中(k)所述来自重链的可变域区包含:具有seq id no:53的氨基酸序列的重链cdr1、具有seq id no:54的氨基酸序列的重链cdr2、具有seq id no:55的氨基酸序列的重
链cdr3;并且所述来自轻链的可变域区包含:具有seq id no:89的氨基酸序列的λ轻链cdr1、具有seq id no:90的氨基酸序列的λ轻链cdr2和具有seq id no:91的氨基酸序列的λ轻链cdr3。
15.本公开提供了一种全人抗bcma抗体或其抗原结合片段,其中所述抗原结合片段是单链抗体,其包含通过肽接头连接在一起的来自重链的可变域区和来自轻链的可变域区,其中所述来自重链的可变域区包含与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性的序列,并且其中所述来自轻链的可变域区包含与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性的序列。
16.本公开提供了一种全人抗bcma抗体或其抗原结合片段,其中所述抗原结合片段是单链抗体,其包含通过肽接头连接在一起的来自重链的可变域区和来自轻链的可变域区,其中所述来自重链的可变域区和所述来自轻链的可变域区是seq id no:8和9(例如,本文称为bca7);seq id no:10和11(例如,本文称为bc4c9);seq id no:12和13(例如,本文称为cd5c4);seq id no:14和15(例如,本文称为bc6g8);seq id no:8和16(例如,本文称为bca7
‑
2c5);seq id no:8和17(例如,本文称为bca7
‑
2e1);seq id no:8和18(例如,本文称为bca7
‑
2d11);seq id no:8和19(例如,本文称为bca7
‑
2g2);seq id no:8和20(例如,本文称为bca7
‑
2d8);seq id no:8和21(例如,本文称为bca7
‑
2e8);或seq id no:22和23(例如,本文称为具有λ轻链的bca7
‑
2c5)。
17.在一个实施方式中,本文公开的任何全人抗bcma抗体或其任何抗原结合片段包含igg1、igg2、igg3或igg4抗体。
18.在一个实施方式中,本文公开的任何全人抗bcma抗体或其任何抗原结合片段包含igg1或igg4同型抗体。
19.在一个实施方式中,本文公开的任何全人抗bcma抗体或其任何抗原结合片段可阻断人april(增殖诱导配体;也称为tnf13和cd256)蛋白与人bcma蛋白的结合。
20.在一个实施方式中,本文公开的任何全人抗bcma抗体或其任何抗原结合片段与人bcma蛋白结合并与小鼠和食蟹猕猴的bcma蛋白交叉反应。
21.在一个实施方式中,本文公开的任何全人抗bcma抗体或其任何抗原结合片段与人bcma蛋白结合并且不与小鼠或食蟹猕猴的bcma蛋白交叉反应。
22.在一个实施方式中,本文公开的任何全人抗bcma抗体或其任何抗原结合片段结合人bcma蛋白的k
d
为10
‑8m或更小。
23.在一个实施方式中,本文公开的任何全人抗bcma抗体或其任何抗原结合片段结合食蟹猕猴bcma蛋白的k
d
为10
‑7m或更小。
24.在一个实施方式中,本文公开的任何全人抗bcma抗体或其任何抗原结合片段结合小鼠bcma蛋白的k
d
为10
‑5m或更小。
25.在一个实施方式中,本文公开的任何全人抗bcma抗体或其任何抗原结合片段与表达bcma蛋白的细胞结合,包括例如与表达bcma蛋白的人骨髓瘤细胞结合。
26.本公开提供了一种药物组合物,其包含所公开的人抗bcma抗体中的任一种或其任何抗原结合片段和药学上可接受的赋形剂。
27.本公开提供了一种试剂盒,其包含所公开的人抗bcma抗体中的任一种或其任何抗原结合片段。
28.本公开提供了一种编码包含抗体重链可变区的第一多肽的第一核酸,所述抗体重链可变区具有所公开的人抗bcma抗体中的任一种的重链互补决定区(cdr),其包括(a)具有seq id no:29的氨基酸序列的重链cdr1、具有seq id no:30的氨基酸序列的重链cdr2和具有seq id no:31的氨基酸序列的重链cdr3;或(b)具有seq id no:35的氨基酸序列的重链cdr1、具有seq id no:36的氨基酸序列的重链cdr2和具有seq id no:37的氨基酸序列的重链cdr3;或(c)具有seq id no:41的氨基酸序列的重链cdr1、具有seq id no:42的氨基酸序列的重链cdr2和具有seq id no:43的氨基酸序列的重链cdr3;或(d)具有seq id no:47的氨基酸序列的重链cdr1、具有seq id no:48的氨基酸序列的重链cdr2和具有seq id no:49的氨基酸序列的重链cdr3;或(e)具有seq id no:53的氨基酸序列的重链cdr1、具有seq id no:54的氨基酸序列的重链cdr2和具有seq id no:55的氨基酸序列的重链cdr3;或(f)具有seq id no:59的氨基酸序列的重链cdr1、具有seq id no:60的氨基酸序列的重链cdr2和具有seq id no:61的氨基酸序列的重链cdr3;或(g)具有seq id no:65的氨基酸序列的重链cdr1、具有seq id no:66的氨基酸序列的重链cdr2和具有seq id no:67的氨基酸序列的重链cdr3;或(h)具有seq id no:71的氨基酸序列的重链cdr1、具有seq id no:72的氨基酸序列的重链cdr2和具有seq id no:73的氨基酸序列的重链cdr3;或(i)具有seq id no:77的氨基酸序列的重链cdr1、具有seq id no:78的氨基酸序列的重链cdr2和具有seq id no:79的氨基酸序列的重链cdr3;或(j)具有seq id no:83的氨基酸序列的重链cdr1、具有seq id no:84的氨基酸序列的重链cdr2和具有seq id no:85的氨基酸序列的重链cdr3。
29.本公开提供了与第一核酸可操作地连接的第一载体,所述第一核酸编码包含抗体重链可变区的第一多肽,所述抗体重链可变区具有本文公开的人抗bcma抗体中的任一种的cdr 1、2和3。
30.本公开提供了一种第一宿主细胞,其携带与第一核酸可操作地连接的第一载体,所述第一核酸编码包含抗体重链可变区的第一多肽,所述抗体重链可变区具有本文公开的人抗bcma抗体中的任一种的cdr 1、2和3。在一个实施方式中,第一载体包括第一表达载体。在一个实施方式中,第一宿主细胞表达包含抗体重链可变区的第一多肽,所述抗体重链可变区具有本文公开的人抗bcma抗体中的任一种的cdr 1、2和3。
31.本公开提供了一种用于制备具有包含cdr 1、2和3的抗体重链可变区的第一多肽的方法,所述方法包括:在适合表达具有包含cdr 1、2和3的抗体重链可变区的第一多肽的条件下,培养携带第一表达载体的第一宿主细胞的群体(例如多个)。在一个实施方式中,所述方法进一步包括:从第一宿主细胞的群体回收具有包含cdr 1、2和3的抗体重链可变区的表达的第一多肽。
32.本公开提供了一种编码包含抗体重链可变区的第一多肽的第一核酸,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性。
33.本公开提供了一种与第一核酸可操作地连接的第一载体,所述第一核酸编码包含抗体重链可变区的第一多肽,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性。
34.本发明提供了一种第一宿主细胞,其携带与第一核酸可操作地连接的第一载体,所述第一核酸编码包含抗体重链可变区的第一多肽,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性。在一个实施方式中,第一载体包括
第一表达载体。在一个实施方式中,第一宿主细胞表达包含抗体重链可变区的第一多肽,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性。
35.本公开提供了一种用于制备具有抗体重链可变区的第一多肽的方法,所述方法包括:在适合表达具有抗体重链可变区的第一多肽的条件下,培养携带第一表达载体的第一宿主细胞的群体(例如多个),所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性。在一个实施方式中,所述方法进一步包括:从第一宿主细胞的群体回收与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性的表达的第一多肽。
36.本公开提供了一种编码包含抗体轻链可变区的多肽的第二核酸,所述抗体轻链可变区具有所公开的人抗bcma抗体中的任一种的轻链互补决定区(cdr),其包括(a)具有seq id no:32的氨基酸序列的轻链cdr1、具有seq id no:33的氨基酸序列的轻链cdr2和具有seq id no:34的氨基酸序列的轻链cdr3;或(b)具有seq id no:38的氨基酸序列的轻链cdr1、具有seq id no:39的氨基酸序列的轻链cdr2和具有seq id no:40的氨基酸序列的轻链cdr3;或(c)具有seq id no:44的氨基酸序列的轻链cdr1、具有seq id no:45的氨基酸序列的轻链cdr2和具有seq id no:46的氨基酸序列的轻链cdr3;或(d)具有seq id no:50的氨基酸序列的轻链cdr1、具有seq id no:51的氨基酸序列的轻链cdr2和具有seq id no:52的氨基酸序列的轻链cdr3;或(e)具有seq id no:56的氨基酸序列的轻链cdr1、具有seq id no:57的氨基酸序列的轻链cdr2和具有seq id no:58的氨基酸序列的轻链cdr3;或(f)具有seq id no:62的氨基酸序列的轻链cdr1、具有seq id no:63的氨基酸序列的轻链cdr2和具有seq id no:64的氨基酸序列的轻链cdr3;或(g)具有seq id no:68的氨基酸序列的轻链cdr1、具有seq id no:69的氨基酸序列的轻链cdr2和具有seq id no:70的氨基酸序列的轻链cdr3;或(h)具有seq id no:74的氨基酸序列的轻链cdr1、具有seq id no:75的氨基酸序列的轻链cdr2和具有seq id no:76的氨基酸序列的轻链cdr3;或(i)具有seq id no:80的氨基酸序列的轻链cdr1、具有seq id no:81的氨基酸序列的轻链cdr2和具有seq id no:82的氨基酸序列的轻链cdr3;或(j)具有seq id no:86的氨基酸序列的轻链cdr1、具有seq id no:87的氨基酸序列的轻链cdr2和具有seq id no:88的氨基酸序列的轻链cdr3;或(k)具有seq id no:89的氨基酸序列的λ轻链cdr1、具有seq id no:90的氨基酸序列的λ轻链cdr2和具有seq id no:91的氨基酸序列的λ轻链cdr3。
37.本公开提供了与第二核酸可操作地连接的第二载体,所述第二核酸编码包含抗体轻链可变区的第二多肽,所述抗体轻链可变区具有本文公开的人抗bcma抗体中的任一种的cdr 1、2和3。
38.本公开提供了一种第二宿主细胞,其携带与第二核酸可操作地连接的第二载体,所述第二核酸编码包含抗体轻链可变区的第二多肽,所述抗体轻链可变区具有本文公开的人抗bcma抗体中的任一种的cdr 1、2和3。在一个实施方式中,第二载体包括第二表达载体。在一个实施方式中,第二宿主细胞表达包含抗体轻链可变区的第二多肽,所述抗体轻链可变区具有本文公开的人抗bcma抗体中的任一种的cdr 1、2和3。
39.本公开提供了一种用于制备具有包含cdr 1、2和3的抗体轻链可变区的第二多肽的方法,所述方法包括:在适合表达具有包含cdr 1、2和3的抗体轻链可变区的第二多肽的条件下,培养携带第二表达载体的第二宿主细胞的群体(例如多个)。在一个实施方式中,所
述方法进一步包括:从第二宿主细胞的群体回收具有包含cdr 1、2和3的抗体轻链可变区的表达的第二多肽。
40.本公开提供了一种编码包含抗体轻链可变区的第二多肽的第二核酸,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。
41.本公开提供了一种与第二核酸可操作地连接的第二载体,所述第二核酸编码包含抗体轻链可变区的第二多肽,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。
42.本发明提供一种第二宿主细胞,其携带与第二核酸可操作地连接的第二载体,所述第二核酸编码包含抗体轻链可变区的第二多肽,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。在一个实施方式中,第二载体包括第二表达载体。在一个实施方式中,第二宿主细胞表达包含抗体轻链可变区的第二多肽,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。
43.本公开提供了一种用于制备具有抗体轻链可变区的第二多肽的方法,所述方法包括:在适合表达具有抗体轻链可变区的第二多肽的条件下,培养携带第二表达载体的第二宿主细胞的群体(例如多个),所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。在一个实施方式中,所述方法进一步包括:从第二宿主细胞的群体回收与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性的表达的第二多肽。
44.本公开提供了编码包含抗体重链可变区的第一多肽的第一核酸和编码包含抗体轻链可变区的第二多肽的第二核酸,所述抗体重链可变区具有所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3),所述抗体轻链可变区具有所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3),其中(a)重链cdr 1、2和3区分别包含seq id no:29、30和31的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:32、33和34的氨基酸序列;或(b)重链cdr 1、2和3区分别包含seq id no:35、36和37的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:38、39和40的氨基酸序列;或(c)重链cdr 1、2和3区分别包含seq id no:41、42和43的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:44、45和46的氨基酸序列;或(d)重链cdr 1、2和3区分别包含seq id no:47、48和49的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:50、51和52的氨基酸序列;或(e)重链cdr 1、2和3区分别包含seq id no:53、54和55的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:56、57和58的氨基酸序列;或(f)重链cdr 1、2和3区分别包含seq id no:59、60和61的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:62、63和64的氨基酸序列;或(g)重链cdr 1、2和3区分别包含seq id no:65、66和67的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:68、69和70的氨基酸序列;或(h)重链cdr1、2和3区分别包含seq id no:71、72和73的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:74、75和76的氨基酸序列;或(i)重链cdr 1、2和3区分别包含seq id no:77、78和79的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:80、81和82的氨基酸序列;或(j)重链cdr 1、2和3区分别包含seq id no:83、84和85的氨基酸序列,并且轻链cdr 1、2和3区分别
包含seq id no:86、87和88的氨基酸序列;或(k)重链cdr 1、2和3区分别包含seq id no:53、54和55的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:89、90和91的氨基酸序列。
45.本公开提供了一种与编码第一多肽的第一核酸可操作地连接的载体,所述第一多肽包含具有所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3)的抗体重链可变区,并且所述载体与编码第二多肽的第二核酸可操作地连接,所述第二多肽包含具有所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3)的抗体轻链可变区。
46.本公开提供了一种携带载体的宿主细胞,所述载体与编码第一多肽的第一核酸和编码第二多肽的第二核酸可操作地连接,所述第一多肽包含所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3),所述第二多肽包含所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3)。在一个实施方式中,载体包括表达载体。在一个实施方式中,宿主细胞表达包含所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3)的第一多肽和包含所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3)的第二多肽。
47.本公开提供了一种用于制备第一和第二多肽的方法,所述方法包括:在适合表达第一多肽和第二多肽的条件下,培养携带表达载体的宿主细胞的群体(例如多个),所述第一多肽包含所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3),所述第二多肽包含所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3)。在一个实施方式中,所述方法进一步包括:从宿主细胞的群体回收表达的第一和第二多肽。
48.本公开提供了编码包含抗体重链可变区的第一多肽的第一核酸和编码包含抗体轻链可变区的第二多肽的第二核酸,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。
49.本公开提供了一种与编码包含抗体重链可变区的第一多肽的第一核酸可操作地连接的载体,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,并且所述载体与编码包含抗体轻链可变区的第二多肽的第二核酸可操作地连接,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。
50.本发明提供了一种宿主细胞,其携带与编码包含抗体重链可变区的第一多肽的第一核酸可操作地连接的载体,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,并且所述载体与编码包含抗体轻链可变区的第二多肽的第二核酸可操作地连接,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。在一个实施方式中,载体包括表达载体。在一个实施方式中,宿主细胞表达包含抗体重链可变区的第一多肽,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,并且宿主细胞表达包含抗体轻链可变区的第二多肽,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。
51.本公开提供了一种用于制备具有抗体重链可变区的第一多肽和具有抗体轻链可
变区的第二多肽的方法,所述方法包括:在适合表达包含抗体重链可变区的第一多肽和表达具有抗体轻链可变区的第二多肽的条件下,培养携带表达载体的宿主细胞的群体(例如多个),所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。在一个实施方式中,所述方法进一步包括:从宿主细胞的群体回收包含抗体重链可变区的表达的第一多肽和表达的第二多肽,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,所述第二多肽与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性。
52.本公开提供了编码包含抗体重链可变区的第一多肽的第一核酸和编码包含抗体轻链可变区的第二多肽的第二核酸,所述抗体重链可变区具有所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3),所述抗体轻链可变区具有所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3),其中(a)重链cdr 1、2和3区分别包含seq id no:29、30和31的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:32、33和34的氨基酸序列;或(b)重链cdr 1、2和3区分别包含seq id no:35、36和37的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:38、39和40的氨基酸序列;或(c)重链cdr 1、2和3区分别包含seq id no:41、42和43的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:44、45和46的氨基酸序列;或(d)重链cdr 1、2和3区分别包含seq id no:47、48和49的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:50、51和52的氨基酸序列;或(e)重链cdr 1、2和3区分别包含seq id no:53、54和55的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:56、57和58的氨基酸序列;或(f)重链cdr 1、2和3区分别包含seq id no:59、60和61的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:62、63和64的氨基酸序列;或(g)重链cdr 1、2和3区分别包含seq id no:65、66和67的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:68、69和70的氨基酸序列;或(h)重链cdr1、2和3区分别包含seq id no:71、72和73的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:74、75和76的氨基酸序列;或(i)重链cdr 1、2和3区分别包含seq id no:77、78和79的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:80、81和82的氨基酸序列;或(j)重链cdr 1、2和3区分别包含seq id no:83、84和85的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:86、87和88的氨基酸序列;或(k)重链cdr 1、2和3区分别包含seq id no:53、54和55的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:89、90和91的氨基酸序列。
53.本公开提供了与编码第一多肽的第一核酸可操作地连接的第一载体和与编码第二多肽的第二核酸可操作地连接的第二载体,所述第一多肽包含具有所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3)的抗体重链可变区,所述第二多肽包含具有所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3)的抗体轻链可变区。
54.本公开提供了一种携带第一载体的宿主细胞,所述第一载体与编码第一多肽的第一核酸可操作地连接,所述第一多肽包含所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3),并且所述宿主细胞携带第二载体,其与编码第二多肽的第二核酸可操作地连接,所述第二多肽包含所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3)。在一个实施方式中,第一和第二载体分别是第一和第二表达载体。在一个实施方式中,宿主细胞表达包含所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3)的第一多肽,并且宿主细胞表达包含所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3)的第二多肽。
55.本公开提供了一种用于制备第一和第二多肽的方法,所述方法包括:在适合表达第一多肽和第二多肽的条件下,培养携带第一和第二表达载体的宿主细胞的群体(例如多个),所述第一多肽包含所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3),所述第二多肽包含所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3)。在一个实施方式中,所述方法进一步包括:从宿主细胞的群体回收表达的第一和第二多肽。
56.本公开提供了编码包含抗体重链可变区的第一多肽的第一核酸和编码包含抗体轻链可变区的第二多肽的第二核酸,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。
57.本公开提供了与编码包含抗体重链可变区的第一多肽的第一核酸可操作地连接的第一载体,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,并且第二载体与编码包含抗体轻链可变区的第二多肽的第二核酸可操作地连接,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。
58.本发明提供了一种宿主细胞,其携带与编码包含抗体重链可变区的第一多肽的第一核酸可操作地连接的第一载体,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,并且所述宿主细胞携带第二载体,其与编码包含抗体轻链可变区的第二多肽的第二核酸可操作地连接,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。在一个实施方式中,第一和第二载体分别包括第一和第二表达载体。在一个实施方式中,宿主细胞表达包含抗体重链可变区的第一多肽,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,并且宿主细胞表达包含抗体轻链可变区的第二多肽,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。
59.本公开提供了一种用于制备具有抗体重链可变区的第一多肽和具有抗体轻链可变区的第二多肽的方法,所述方法包括:在适合表达包含抗体重链可变区的第一多肽和表达具有抗体轻链可变区的第二多肽的条件下,培养携带第一和第二表达载体的宿主细胞的群体(例如多个),所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。在一个实施方式中,所述方法进一步包括:从宿主细胞的群体回收包含抗体重链可变区的表达的第一多肽和表达的第二多肽,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,所述第二多肽与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性。
60.本公开提供了一种编码包含抗体重链可变区和抗体轻链可变区的多肽(例如,包
括scfv的单链抗体)的核酸,所述抗体重链可变区具有所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3),所述抗体轻链可变区具有所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3),其中(a)重链cdr 1、2和3区分别包含seq id no:29、30和31的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:32、33和34的氨基酸序列;或(b)重链cdr 1、2和3区分别包含seq id no:35、36和37的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:38、39和40的氨基酸序列;或(c)重链cdr 1、2和3区分别包含seq id no:41、42和43的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:44、45和46的氨基酸序列;或(d)重链cdr 1、2和3区分别包含seq id no:47、48和49的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:50、51和52的氨基酸序列;或(e)重链cdr 1、2和3区分别包含seq id no:53、54和55的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:56、57和58的氨基酸序列;或(f)重链cdr 1、2和3区分别包含seq id no:59、60和61的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:62、63和64的氨基酸序列;或(g)重链cdr 1、2和3区分别包含seq id no:65、66和67的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:68、69和70的氨基酸序列;或(h)重链cdr1、2和3区分别包含seq id no:71、72和73的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:74、75和76的氨基酸序列;或(i)重链cdr 1、2和3区分别包含seq id no:77、78和79的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:80、81和82的氨基酸序列;或(j)重链cdr 1、2和3区分别包含seq id no:83、84和85的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:86、87和88的氨基酸序列;或(k)重链cdr 1、2和3区分别包含seq id no:53、54和55的氨基酸序列,并且轻链cdr 1、2和3区分别包含seq id no:89、90和91的氨基酸序列。
61.本公开提供了一种与编码包含抗体重链可变区和抗体轻链可变区的多肽(例如,包括scfv的单链抗体)的核酸可操作地连接的载体,所述抗体重链可变区具有所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3),所述抗体轻链可变区具有所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3)。
62.本公开提供了一种携带载体的宿主细胞,所述载体与编码包含抗体重链可变区和抗体轻链可变区的多肽(例如,包括scfv的单链抗体)的核酸可操作地连接,所述抗体重链可变区具有所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3),所述抗体轻链可变区具有所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3)。在一个实施方式中,载体包括表达载体。在一个实施方式中,宿主细胞表达包含抗体重链可变区和抗体轻链可变区的多肽,所述抗体重链可变区具有所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3),所述抗体轻链可变区具有所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3)。
63.本公开提供了一种用于制备多肽的方法,所述方法包括:在适合表达包含抗体重链可变区和抗体轻链可变区的多肽的条件下,培养携带表达载体的宿主细胞的群体(例如多个),所述抗体重链可变区具有所公开的人抗bcma抗体中的任一种的重链互补决定区(hc
‑
cdr 1、2和3),所述抗体轻链可变区具有所公开的人抗bcma抗体中的任一种的轻链互补决定区(lc
‑
cdr 1、2和3)。在一个实施方式中,所述方法进一步包括:从宿主细胞的群体回收表达的多肽。
64.本公开提供了一种编码包含抗体重链可变区和抗体轻链可变区的多肽(例如,包
括scfv的单链抗体)的核酸,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。
65.本公开提供了一种与编码包含抗体重链可变区和抗体轻链可变区的多肽(例如,包括scfv的单链抗体)的核酸可操作地连接的载体,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。
66.本发明提供了一种宿主细胞,其携带与编码包含抗体重链可变区和抗体轻链可变区的多肽(例如,包括scfv的单链抗体)的核酸可操作地连接的载体,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。在一个实施方式中,载体包括表达载体。在一个实施方式中,宿主细胞表达包含抗体重链可变区和抗体轻链可变区的多肽(例如,包括scfv的单链抗体),所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。
67.本公开提供了一种用于制备多肽(例如,包括scfv的单链抗体)的方法,所述方法包括:在适合表达多肽(例如,包括scfv的单链抗体)的条件下,培养携带表达载体的宿主细胞的群体(例如多个),所述多肽包含抗体重链可变区和抗体轻链可变区,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。在一个实施方式中,所述方法进一步包括:从宿主细胞的群体回收表达的多肽(例如,包括scfv的单链抗体),所述多肽包含抗体重链可变区和抗体轻链可变区,所述抗体重链可变区与seq id no:8、10、12、14或22的氨基酸序列具有至少95%序列同一性,所述抗体轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23的氨基酸序列具有至少95%序列同一性。
68.本公开提供了一种用于抑制表达bcma的细胞的生长或增殖的方法(例如体外方法),其包括:在适合抑制表达bcma的细胞的生长或增殖的条件下,使(i)效应细胞的群体(例如多个)与(ii)表达bcma的靶细胞的群体(例如多个)(iii)在本文所述的人抗bcma抗体中的任一种或2
‑
3种的任何组合存在下接触。在一个实施方式中,效应细胞的群体包括pbmc或nk细胞。在一个实施方式中,靶细胞的群体包括表达bcma的多发性骨髓瘤(mm)细胞或表达bcma的转基因细胞。在一个实施方式中,效应细胞与靶细胞的比例为1:1、2:1、3:1、4:1或5:1。在一个实施方式中,效应细胞与靶细胞的比例为5
‑
10:1、10
‑
20:1或20
‑
30:1。
69.本公开提供了一种用于杀死表达bcma的细胞的方法(例如体外方法),其包括:在适合杀死表达bcma的细胞的条件下,使(i)效应细胞的群体(例如多个)与(ii)表达bcma的靶细胞的群体(例如多个)(iii)在本文所述的人抗bcma抗体中的任一种或2
‑
3种的任何组合存在下接触。在一个实施方式中,效应细胞的群体包括pbmc或nk细胞。在一个实施方式中,靶细胞的群体包括表达bcma的多发性骨髓瘤(mm)细胞或表达bcma的转基因细胞。在一个实施方式中,效应细胞与靶细胞的比例为1:1、2:1、3:1、4:1或5:1。在一个实施方式中,效
应细胞与靶细胞的比例为5
‑
10:1、10
‑
20:1或20
‑
30:1。
70.本公开提供了一种用于治疗患有与bcma过度表达相关的疾病的受试者的方法,所述方法包括:向所述受试者施用有效量的治疗组合物,所述治疗组合物包含本文所述的人抗bcma抗体中的任一种或2
‑
3种的任何组合。在一个实施方式中,与bcma过度表达相关的疾病包括:b细胞白血病、b细胞淋巴瘤或b细胞骨髓瘤。在一个实施方式中,与bcma过度表达相关的疾病选自由以下组成的组:多发性骨髓瘤(mm)、包括伯基特氏淋巴瘤(burkitt's lymphoma,bl)的非霍奇金氏淋巴瘤(non
‑
hodgkin's lymphoma,nhl)、b慢性淋巴细胞性白血病(b
‑
cll)、全身性红斑狼疮(sle)、b和t急性淋巴细胞性白血病(all)、急性骨髓性白血病(aml)、慢性淋巴细胞性白血病(cll)、弥漫性大b细胞淋巴瘤、慢性骨髓性白血病(cml)、毛细胞白血病(hcl)、滤泡性淋巴瘤、瓦尔登斯特伦氏巨球蛋白血症(waldenstrom's macroglobulinemia)、套细胞淋巴瘤、霍奇金氏淋巴瘤(hodgkin's lymphoma,hl)、浆细胞骨髓瘤、前体b细胞淋巴母细胞性白血病/淋巴瘤、浆细胞瘤、巨细胞骨髓瘤、浆细胞骨髓瘤、重链骨髓瘤、轻链或本周氏骨髓瘤(bence
‑
jones myeloma)、淋巴瘤样肉芽肿病、移植后淋巴增生性病症、免疫调节病症、类风湿性关节炎、重症肌无力、特发性血小板减少性紫癜、抗磷脂综合征、恰加斯氏病(chagas'disease)、格雷夫氏病(grave's disease)、韦格纳氏肉牙肿病(wegener's granulomatosis)、结节性多动脉炎、休格连氏综合征(sjogren's syndrome)、寻常型天疱疮、硬皮病、多发性硬化症、抗磷脂综合征、anca相关血管炎、古德帕斯彻氏病(goodpasture's disease)、川崎病(kawasaki disease)、自身免疫性溶血性贫血和急进性肾小球肾炎、重链病、原发性或免疫细胞相关淀粉样变性和意义未明的单克隆丙种球蛋白病。
附图说明
71.图1显示了bca7抗体的结合动力学的spr传感图。
72.图2显示了gsk j6m0抗体的结合动力学的spr传感图。
73.图3显示了bc4c9抗体的结合动力学的spr传感图。
74.图4显示了bc5c5抗体的结合动力学的spr传感图。
75.图5显示了bca7
‑
2c5抗体的结合动力学的spr传感图。
76.图6显示了bca7
‑
2d11抗体的结合动力学的spr传感图。
77.图7显示了bca7
‑
2g2抗体的结合动力学的spr传感图。
78.图8显示了bca7
‑
2e1抗体的结合动力学的spr传感图。
79.图9显示了bca7
‑
2d8抗体的结合动力学的spr传感图。
80.图10显示了bca7
‑
2e81抗体的结合动力学的spr传感图。
81.图11a显示了bca7
‑
2c5抗体与人bcma蛋白的结合动力学的spr传感图。
82.图11b显示了bca7
‑
2e1抗体与人bcma蛋白的结合动力学的spr传感图。
83.图12a显示了bca7
‑
2c5抗体与食蟹猕猴bcma蛋白的结合动力学的spr传感图。
84.图12b显示了bca7
‑
2e1抗体与食蟹猕猴bcma蛋白的结合动力学的spr传感图。
85.图13a显示了bca7
‑
2c5抗体与小鼠bcma蛋白的结合动力学的spr传感图。
86.图13b显示了bca7
‑
2e1抗体与小鼠bcma蛋白的结合动力学的spr传感图。
87.图14是显示各种抗bcma抗体与小鼠、食蟹猕猴或人bcma蛋白的交叉反应性的
elisa分析结果的条形图。纵轴显示吸光度。
88.图15是显示通过流式细胞术将各种抗bcma抗体与mm1r细胞系结合的结果的图。
89.图16是显示使用夹心elisa程序的表位作图分析的结果的条形图。纵轴显示吸光度。
90.图17显示了bcma蛋白呈现的带状图。
91.图18是显示使用生物层干涉测量法进行的蛋白质
‑
蛋白质结合分析的结果的图。
92.图19是显示使用生物层干涉测量法进行的蛋白质
‑
蛋白质结合分析的结果的图。
93.图20是显示使用生物层干涉测量法的表位作图分析的结果的条形图。
94.图21显示了使用生物层干涉测量法的蛋白质结合阻断分析的结果。
95.图22显示了使用生物层干涉测量法进行的抗体
‑
蛋白质结合分析的结果。
具体实施方式
96.定义:
97.除非另外定义,否则本文使用的技术和科学术语具有本领域普通技术人员通常理解的含义。一般来说,与本文所述的细胞和组织培养、分子生物学、免疫学、微生物学、遗传学、转基因细胞生产、蛋白质化学和核酸化学以及杂交技术有关的术语是本领域中众所周知和常用的。除非另外指明,否则本文提供的方法和技术通常是根据本领域众所周知以及本文所引用和讨论的各种一般和更具体的参考文献中所描述的常规程序进行。参见例如sambrook等人分子克隆:实验室手册(molecular cloning:alaboratory manual),第2版,cold spring harbor laboratory press,cold spring harbor,n.y.(1989)和ausubel等人,分子生物学的现行协议(current protocols in molecular biology),greene publishing associates(1992)。许多基本文本描述了标准抗体生产过程,包括borrebaeck(编)抗体工程(antibody engineering),第2版freeman and company,ny,1995;mccafferty等人抗体工程,实用方法(antibody engineering,a practical approach)irl at oxford press,oxford,england,1996;和paul(1995)抗体工程方案(antibody engineering protocols)humana press,towata,n.j.,1995;paul(编),基础免疫学(fundamental immunology),raven press,n.y,1993;coligan(1991)免疫学的现行协议(current protocols in immunology)wiley/greene,ny;harlow和lane(1989)抗体:实验室手册(antibodies:a laboratory manual)cold spring harbor press,ny;stites等人(编)基础与临床免疫学(basic and clinical immunology)(第4版)lange medical publications,los altos,calif.和其中引用的参考文献;编码单克隆抗体:原理与实践(coding monoclonal antibodies:principles and practice)(第2版)academic press,new york,n.y.,1986以及kohler和milstein nature 256:495
‑
497,1975。本文引用的所有参考文献均以全文引用的方式并入本文中。酶促反应和富集/纯化技术也是众所周知的,并根据制造商的说明书进行,如本领域通常完成的或如本文所述。与本文所述的分析化学、合成有机化学以及药物和制药化学有关的术语以及实验室程序和技术都是本领域中众所周知和常用的。标准技术可用于化学合成、化学分析、药物制备、配制和递送以及对患者的治疗。
98.本文提供的标题不是对本公开的各个方面的限制,这些方面可以通过参考整个说
明书来理解。
99.除非上下文另有要求,否则单数术语应包括复数,且复数术语应包括单数。单数形式“一(a/an)”和“所述(the)”以及任何词语的单数使用均包括复数指示物,除非明确无误地限制在一个指示物。
100.应理解,本文使用的替代词(例如“或”)意指替代物中的一个或两个或其任何组合。
101.本文使用的术语“和/或”意指对每个特定特征或组件的具体公开,无论是否具有其它特征或组件。例如,在本文如“a和/或b”的短语中使用的术语“和/或”旨在包括“a和b”、“a或b”、“a”(单独)和“b”(单独)。同样,在如“a、b和/或c”的短语中使用的术语“和/或”旨在涵盖以下各个方面:a、b和c;a、b或c;a或c;a或b;b或c;a和c;a和b;b和c;a(单独);b(单独);以及c(单独)。
102.如本文所用,术语“包含”、“包括”、“具有”和“含有”以及它们的语法变体旨在为非限制性的,使得列表中的一个项目或多个项目并不排除可以被替换或添加到所列项目中的其它项目。应理解,凡是本文用“包括”语言描述的方面,也提供按照“由
……
组成”和/或“基本上由
……
组成”描述的其它类似方面。
103.如本文所用,术语“约”是指在本领域普通技术人员确定的特定值或组成的可接受误差范围内的值或组成,这将部分取决于如何测量或确定该值或组成,即测量系统的限制。例如,“约”或“基本上包括”可以意指按照本领域的实践在一个或多于一个标准偏差内。替代地,“约”或“基本上包括”可以意指至多10%(即
±
10%)或更多的范围,取决于测量系统的限制。例如,约5mg可以包括4.5mg与5.5mg之间的任何数字。此外,特别是就生物系统或过程而言,所述术语可以意指至多一个数量级或至多5倍的值。当本公开中提供特定值或组成时,除非另有说明,否则“约”或“基本上包括”的含义应假定为在该特定值或组成的可接受误差范围内。
104.术语“肽”、“多肽”和“蛋白质”以及本文使用的其它相关术语可互换使用,是指氨基酸的聚合物并且不限于任何特定长度。多肽可以包含天然和非天然氨基酸。多肽包括重组形式或化学合成形式。这些术语涵盖原生和人工蛋白质、蛋白质片段和蛋白质序列的多肽类似物(如突变蛋白、变异体、嵌合蛋白和融合蛋白)以及翻译后或以其它方式共价或非共价修饰的蛋白质。本文描述了包含使用重组程序制备的结合bcma的结合蛋白的氨基酸序列的多肽(例如,抗bcma抗体或其抗原结合部分)。
105.术语“核酸”、“多核苷酸”和“寡核苷酸”以及本文使用的其它相关术语可互换使用,是指核苷酸的聚合物并且不限于任何特定长度。核酸包括重组形式和化学合成形式。核酸包括dna分子(cdna或基因组dna)、rna分子(例如mrna)、使用核苷酸类似物生成的dna或rna的类似物(例如肽核酸和非天然存在的核苷酸类似物)及其杂交物。核酸分子可以是单链的或双链的。在一个实施方式中,本公开的核酸分子包括编码抗体或其片段或scfv、衍生物、突变蛋白或变异体的连续开放阅读框。在一个实施方式中,核酸包括一种类型的多核苷酸或两种或更多种不同类型的多核苷酸的混合物。本文描述了编码抗bcma抗体或其抗原结合部分的核酸。
106.术语“回收(recover/recovery/recovering)”和其它相关术语是指从宿主细胞培养基或从宿主细胞裂解物或从宿主细胞膜中获得蛋白质(例如,抗体或其抗原结合部分)。
在一个实施方式中,蛋白质由宿主细胞表达为与分泌信号肽序列融合的重组蛋白,分泌信号肽序列介导所表达的蛋白质的分泌。分泌的蛋白可以从宿主细胞培养基中回收。在一个实施方式中,蛋白质由宿主细胞表达为缺乏分泌信号肽序列的重组蛋白,其可从宿主细胞裂解物中回收。在一个实施方式中,蛋白质由宿主细胞表达为膜结合蛋白,其可以使用清洁剂从宿主细胞膜释放表达的蛋白质来进行回收。在一个实施方式中,无论使用何种方法回收蛋白质,都可以对蛋白质进行从回收的蛋白质中去除细胞碎片的程序。例如,回收的蛋白质可以进行色谱、凝胶电泳和/或透析。在一个实施方式中,色谱包括任何一种或任何组合或两种或更多种程序,包括亲和色谱、羟基磷灰石色谱、离子交换色谱、反相色谱和/或硅胶色谱。在一个实施方式中,亲和色谱包括蛋白a或g(来自金黄色葡萄球菌(staphylococcus aureus)的细胞壁组分)。
107.术语“分离的”是指基本上不含其它细胞物质的蛋白质(例如,抗体或其抗原结合部分)或多核苷酸。蛋白质可以通过使用本领域众所周知的蛋白质纯化技术进行分离,使其基本上不含天然相关成分(或与细胞表达系统或用于生产抗体的化学合成方法相关的组分)。术语分离的在一些实施方式中还指基本上不含同一物种的其它分子的蛋白质或多核苷酸,例如分别具有不同氨基酸或核苷酸序列的其它蛋白质或多核苷酸。所需分子的纯度均一性可以使用本领域众所周知的技术进行分析,包括低分辨率方法如凝胶电泳和高分辨率方法如hplc或质谱法。在一个实施方式中,分离任何抗bcma抗体或其抗原结合蛋白。
108.本文所用的“抗原结合蛋白”和相关术语是指包含与抗原结合的部分和支架或框架部分的蛋白质,任选地,所述支架或框架部分允许抗原结合部分采用促进抗原结合蛋白与抗原结合的构象。抗原结合蛋白的实例包括抗体、抗体片段(例如,抗体的抗原结合部分)、抗体衍生物和抗体类似物。抗原结合蛋白可包含例如具有移植cdr或cdr衍生物的替代蛋白质支架或人工支架。此类支架包括但不限于抗体衍生的支架,其包含引入以例如稳定抗原结合蛋白的三维结构的突变;以及完全合成的支架,其包含例如生物相容性聚合物。参见例如korndorfer等人,2003,蛋白质:结构、功能和生物信息学(proteins:structure,function,and bioinformatics),第53卷,第1期:121
‑
129;roque等人,2004,biotechnol.prog.20:639
‑
654。此外,还可以使用肽抗体模拟物(“pam”),以及基于利用纤维连接组分作为支架的抗体模拟物的支架。本文描述了结合bcma的抗原结合蛋白。
109.抗原结合蛋白可以具有例如免疫球蛋白的结构。在一个实施方式中,“免疫球蛋白”是指由两对相同的多肽链构成的四聚体分子,每一对具有一条“轻”链(约25kda)和一条“重”链(约50
‑
70kda)。每条链的氨基末端部分包括约100至110个或更多个氨基酸的可变区,主要负责抗原识别。每条链的羧基末端部分定义了主要负责效应功能的恒定区。将人轻链分类为κ或λ轻链。将重链分类为μ、δ、γ、α或ε,并将抗体的同型分别定义为igm、igd、igg、iga和ige。在轻链和重链内,可变区和恒定区由约12个或更多个氨基酸的“j”区连接,重链还包括约10多个氨基酸的“d”区。一般参见基础免疫学(fundamental immunology)第7章(paul,w.编,第2版raven press,n.y.(1989))(出于所有目的以全文引用的方式并入)。每个轻/重链对的可变区形成抗体结合位点,使得完整的免疫球蛋白具有两个抗原结合位点。在一个实施方式中,抗原结合蛋白可以是一种合成分子,其结构与四聚体免疫球蛋白分子不同,但仍能结合靶抗原或结合两个或更多个靶抗原。例如,合成抗原结合蛋白可以包括抗体片段、1
‑
6条或更多条多肽链、多肽的不对称组合体或其它合成分子。本文描述了具有与
bcma特异性结合的免疫球蛋白样特性的抗原结合蛋白。
110.免疫球蛋白链的可变区表现出相同的一般结构,即相对保守的框架区(fr)由三个高变区,也称为互补决定区或cdr连接。从n端到c端,轻链和重链两者都包含域fr1、cdr1、fr2、cdr2、fr3、cdr3和fr4。
111.一个或多个cdr可以共价或非共价地并入分子中,使其成为抗原结合蛋白。抗原结合蛋白可以将cdr作为较大多肽链的一部分并入,可以将cdr与另一条多肽链共价连接,或可以非共价地并入cdr。cdr允许抗原结合蛋白与相关特定抗原特异性结合。
112.每个域的氨基酸分配符合kabat等人在具有免疫学意义的蛋白质序列(sequences of proteins of immunological interest),第5版,美国卫生和公众服务部,phs,nih,nih出版物编号91
‑
3242,1991中的定义。免疫球蛋白链中氨基酸的其它编号系统包括imgt.rtm.(国际免疫遗传学信息系统;lefranc等人,dev.comp.immunol.29:185
‑
203;2005)和aho(honegger和pluckthun,j.mol.biol.309(3):657
‑
670;2001);chothia(al
‑
lazikani等人,1997journal of molecular biology 273:927
‑
948;contact(maccallum等人,1996 journal of molecular biology 262:732
‑
745和aho(honegger和pluckthun 2001 journal of molecular biology 309:657
‑
670。
113.本文所用的“抗体(antibody/antibodies)”和相关术语是指与抗原特异性结合的完整免疫球蛋白或其抗原结合部分(或其抗原结合片段)。抗原结合部分(或抗原结合片段)可以通过重组dna技术或通过完整抗体的酶促或化学裂解产生。抗原结合部分(或抗原结合片段)尤其包括fab、fab'、f(ab')2、fv、域抗体(dab)和互补决定区(cdr)片段、单链抗体(scfv)、嵌合抗体、双功能抗体、三功能抗体、四功能抗体和含有免疫球蛋白的至少一部分的多肽,所述免疫球蛋白的至少一部分足以赋予多肽特异性的抗原结合。
114.抗体包括重组产生的抗体和抗原结合部分。抗体包括非人抗体、嵌合抗体、人源化抗体和全人抗体。抗体包括单特异性、多特异性(例如双特异性、三特异性和高阶特异性)。抗体包括四聚抗体、轻链单体、重链单体、轻链二聚体、重链二聚体。抗体包括f(ab')2片段、fab'片段和fab片段。抗体包括单域抗体、单价抗体、单链抗体、单链可变片段(scfv)、骆驼化抗体、亲和抗体、二硫键连接的fv(sdfv)、抗独特型抗体(抗id)、微型抗体。抗体包括单克隆和多克隆群体。本文描述了抗bcma抗体。
115.本文所用的“抗原结合域”、“抗原结合区”或“抗原结合位点”和其它相关术语是指抗原结合蛋白的一部分,其含有与抗原相互作用并且有助于抗原结合蛋白对抗原的特异性和亲和力的氨基酸残基(或其它部分)。对于与其抗原特异性结合的抗体,这将包括其至少一个cdr域的至少一部分。本文描述了抗bcma抗体的抗原结合域。
116.如本文在抗体或抗原结合蛋白或抗体片段的上下文中所用,术语“特异性结合(specific binding/specifically binds/specifically binding)”和其它相关术语是指相对于其它分子或部分,与抗原的非共价或共价优先结合(例如,相对于其它可用的抗原,抗体与特定抗原特异性结合)。在一个实施方式中,如果抗体与抗原结合的解离常数k
d
为10
‑5m或更小,或10
‑6m或更小,或10
‑7m或更小,或10
‑8m或更小,或10
‑9m或更小,或10
‑
10
m或更小,则抗体与靶抗原特异性结合。本文描述了特异性结合bcma的抗bcma抗体。
117.在一个实施方式中,解离常数(k
d
)可以使用biacore表面等离子体共振(spr)分析来测量。表面等离子体共振是指一种光学现象,可以通过检测生物传感器基质内蛋白质浓
度的变化来分析实时相互作用,例如使用biacore系统(biacore life sciences division of ge healthcare,piscataway,nj)。
118.如本文所用,“表位”和相关术语是指由抗原结合蛋白(例如,由抗体或其抗原结合部分)结合的抗原的部分。表位可以包含由抗原结合蛋白结合的两个或更多个抗原的部分。表位可以包含一个抗原或两个或更多个抗原的非连续部分(例如,在抗原的一级序列中不连续的氨基酸残基,但在抗原的三级和四级结构的情况下,它们彼此接近,足以由抗原结合蛋白所结合)。一般来说,抗体的可变区,特别是cdr,与表位相互作用。本文描述了结合bcma多肽的表位的抗bcma抗体及其抗原结合蛋白。
119.本文所用的“抗体片段”、“抗体部分”、“抗体的抗原结合片段”或“抗体的抗原结合部分”和其它相关术语是指除完整抗体之外的分子,其包含完整抗体的一部分,所述部分与完整抗体所结合的抗原结合。抗体片段的实例包括但不限于fv、fab、fab'、fab'
‑
sh、f(ab')2;fd;和fv片段,以及dab;双功能抗体;线性抗体;单链抗体分子(例如scfv);含有抗体的至少一部分的多肽,其足以赋予多肽特异性的抗原结合。抗体的抗原结合部分可以通过重组dna技术或通过完整抗体的酶促或化学裂解产生。抗原结合部分尤其包括fab、fab'、f(ab')2、fv、域抗体(dab)和互补决定区(cdr)片段、嵌合抗体、双功能抗体、三功能抗体、四功能抗体和含有至少免疫球蛋白的足以赋予抗体片段抗原结合特性的部分的多肽。本文描述了抗bcma抗体的抗原结合片段。
120.术语“fab”、“fab片段”和其它相关术语是指包含可变轻链区(v
l
)、恒定轻链区(c
l
)、可变重链区(v
h
)和第一恒定区(c
h1
)的单价片段。fab能够结合抗原。f(ab')2片段是包含两个在铰链区由二硫键连接的fab片段的二价片段。f(ab')2具有抗原结合能力。fd片段包含v
h
和c
h1
区。fv片段包含v
l
和v
h
区。fv可以结合抗原。dab片段具有v
h
域、v
l
域或v
h
或vl域的抗原结合片段(美国专利6,846,634和6,696,245;美国公开申请号2002/02512、2004/0202995、2004/0038291、2004/0009507、2003/0039958;和ward等人,nature 341:544
‑
546,1989)。本文描述了包含抗bcma抗体的抗原结合部分的fab片段。
121.单链抗体(scfv)是v
l
和v
h
区通过接头(例如,氨基酸残基的合成序列)连接以形成连续蛋白质链的抗体。优选地,接头足够长以允许蛋白质链自身折回并形成单价抗原结合位点(参见例如bird等人,1988,science 242:423
‑
26和huston等人,1988,proc.natl.acad.sci.usa 85:5879
‑
83)。本文描述了包含抗bcma抗体的抗原结合部分的单链抗体。
122.双链抗体(“diabody”)是包含两条多肽链的二价抗体,其中每条多肽链包含通过接头连接的v
h
和v
l
域,所述接头太短以致无法在同一链上的两个域之间配对,因此允许每个域与另一条多肽链上的互补域配对(参见例如holliger等人,1993,proc.natl.acad.sci.usa 90:6444
‑
48和poljak等人,1994,structure 2:1121
‑
23)。如果双链抗体的两条多肽链相同,则由它们配对产生的双链抗体将具有两个相同的抗原结合位点。具有不同序列的多肽链可用于制造具有两个不同抗原结合位点的双链抗体。类似地,三链抗体和四链抗体是分别包含三条和四条多肽链并分别形成三个和四个抗原结合位点的抗体,所述抗原结合位点可以相同或不同。双链抗体、三链抗体和四链抗体构建体可以使用本文所述的任何抗bcma抗体的抗原结合部分来制备。
123.术语“人抗体”是指具有一个或多个源自人免疫球蛋白序列的可变区和恒定区的
抗体。在一个实施方式中,所有可变域和恒定域都源自人免疫球蛋白序列(例如全人抗体)。这些抗体可以通过多种方式制备,其实例如下所述,包括通过重组方法或通过用小鼠的感兴趣的抗原进行免疫,所述小鼠经基因修饰以表达源自人重链和/或轻链编码基因的抗体。本文描述了全人抗bcma抗体及其抗原结合蛋白。
[0124]“人源化”抗体是指序列通过一个或多个氨基酸取代、缺失和/或添加而与源自非人物种的抗体的序列不同的抗体,从而使人源化抗体与非人物种抗体相比,在施用于人类受试者时,不太可能诱发免疫反应,和/或诱发较不严重的免疫反应。在一个实施方式中,非人物种抗体的重链和/或轻链的框架和恒定域中的某些氨基酸突变以产生人源化抗体。在另一个实施方式中,人抗体的恒定域与非人物种的可变域融合。在另一个实施方式中,改变非人抗体的一个或多个cdr序列中的一个或多个氨基酸残基以降低非人抗体施用于人类受试者时可能的免疫原性,其中改变的氨基酸残基对于抗体与其抗原的免疫特异性结合不是关键性的,或者对氨基酸序列所做的改变是保守的改变,使得人源化抗体与抗原的结合不会比非人抗体与抗原的结合明显更差。如何制造人源化抗体的的实例可以在美国专利第6,054,297号、第5,886,152号和第5,877,293号中找到。
[0125]
本文所用的术语“嵌合抗体”和相关术语是指含有来自第一抗体的一个或多个区和来自一个或多个其它抗体的一个或多个区的抗体。在一个实施方式中,一个或多个cdr源自人抗体。在另一个实施方式中,所有cdr都源自人抗体。在另一个实施方式中,来自一个以上人抗体的cdr在嵌合抗体中混合和匹配。例如,嵌合抗体可以包含来自第一人抗体轻链的cdr1、来自第二人抗体轻链的cdr2和cdr3以及来自第三抗体重链的cdr。在另一个实例中,cdr来源于不同的物种,如人和小鼠,或人和兔,或人和山羊。本领域技术人员将理解,其它组合也是可能的。
[0126]
此外,框架区可源自相同抗体之一、源自一种或多种不同抗体,如人抗体,或源自人源化抗体。在嵌合抗体的一个实例中,重链和/或轻链的一部分与来自特定物种或属于特定抗体类别或亚类的抗体相同、同源或源自所述抗体,而链的其余部分与来自另一物种或属于另一抗体类别或亚类的抗体相同、同源或源自所述抗体。还包括此类抗体的片段,它们表现出所需的生物活性(即,特异性结合靶抗原的能力)。嵌合抗体可以由本文所述的任何抗bcma抗体的部分制备。
[0127]
如本文所用,术语“变异”多肽和多肽的“变异体”是指包含相对于参考多肽序列具有一个或多个氨基酸残基插入氨基酸序列中、从氨基酸序列中缺失和/或取代到氨基酸序列中的氨基酸序列的多肽。多肽变异体包括融合蛋白。同样地,变异多核苷酸包含相对于另一个多核苷酸序列具有一个或多个核苷酸插入核苷酸序列中、从核苷酸序列中缺失和/或取代到核苷酸序列中的核苷酸序列。多核苷酸变异体包括融合多核苷酸。
[0128]
如本文所用,术语多肽的“衍生物”是已经过化学修饰的多肽(例如抗体),例如通过与另一化学部分如聚乙二醇、白蛋白(例如人血清白蛋白)的缀合、磷酸化和糖基化。除非另外指明,否则术语“抗体”除了包含两条全长重链和两条全长轻链的抗体外,还包括其衍生物、变异体、片段和突变蛋白,其实例如下所述。
[0129]
如本文所用,术语“fc”或“fc区”是指在铰链区中或之后开始并在重链的c端结束的抗体重链恒定区的部分。fc区包含ch和ch3区的至少一部分并且可以包括或可以不包括铰链区的一部分。两条各自携带半个fc区的多肽链可以二聚化形成完整的fc域。fc域可以
结合fc细胞表面受体和免疫补体系统的一些蛋白质。fc域表现出效应功能,包括两种或更多种活性的任何一种或任何组合,包括补体依赖性细胞毒性(cdc)、抗体依赖性细胞介导的细胞毒性(adcc)、抗体依赖性吞噬作用(adp)、调理作用和/或细胞结合。fc域可以结合fc受体,包括fcγri(例如cd64)、fcγrii(例如cd32)和/或fcγriii(例如cd16a)。
[0130]
如本文所用的术语“标记抗体”或相关术语是指未标记或连接至可检测的标记或部分用于检测的抗体及其抗原结合部分,其中可检测的标记或部分是放射性的、比色的、抗原性的、酶促的、可检测的珠粒(如磁性或电子致密(如金)珠粒)、生物素、链霉亲和素或蛋白a。可以采用多种标记,包括但不限于放射性核素、荧光剂、酶、酶底物、酶辅因子、酶抑制剂和配体(例如生物素、半抗原)。本文所述的任何抗bcma抗体可以是未标记的或可以连接到可检测的标记或部分。
[0131]
本文所用的“同一性百分比”或“同源性百分比”和相关术语是指对两个多肽之间或两个多核苷酸序列之间的相似性的定量测量。两个多肽序列之间的同一性百分比是两个多肽序列之间在对齐位置共享的相同氨基酸数量的函数,考虑到间隙的数量以及每个间隙的长度,这可能需要引入以优化两个多肽序列的对齐。以类似的方式,两个多核苷酸序列之间的同一性百分比是两个多核苷酸序列之间在对齐位置共享的相同核苷酸数量的函数,考虑到间隙的数量和每个间隙的长度,这可能需要引入以优化两个多核苷酸序列的对齐。序列的比较和两个多肽序列之间或两个多核苷酸序列之间的同一性百分比的确定可以使用数学算法实现。例如,两个多肽或两个多核苷酸序列的“同一性百分比”或“同源性百分比”可以通过使用gap计算机程序(gcg wisconsin package的一部分,版本10.3(accelrys,san diego,calif.))使用其默认参数比较序列来确定。
[0132]
在一个实施方式中,测试抗体的氨基酸序列可以与构成本文所述的任何抗bcma抗体或其抗原结合蛋白的多肽的任何氨基酸序列相似但不相同。测试抗体与多肽之间的相似性可以是与构成本文所述的任何抗bcma抗体或其抗原结合蛋白的任何多肽至少95%、或至少96%相同、或至少97%相同、或至少98%相同、或至少99%相同。在一个实施方式中,类似的多肽可以含有重链和/或轻链内的氨基酸取代。在一个实施方式中,氨基酸取代包括一个或多个保守氨基酸取代。“保守氨基酸取代”是一个氨基酸残基被另一个具有类似化学特性(例如电荷或疏水性)的侧链(r基团)的氨基酸残基取代。一般来说,保守氨基酸取代基本上不会改变蛋白质的功能特性。在两个或更多个氨基酸序列因保守取代而彼此不同的情况下,可以向上调整序列同一性百分比或相似程度以校正取代的保守性质。进行这种调整的手段是本领域技术人员所熟知的。参见例如pearson(1994)methods mol.biol.24:307
‑
331,其以全文引用的方式并入本文中。具有类似化学特性的侧链的氨基酸组的实例包括(1)脂肪族侧链:甘氨酸、丙氨酸、缬氨酸、亮氨酸和异亮氨酸;(2)脂肪族羟基侧链:丝氨酸与苏氨酸;(3)含酰胺的侧链:天冬酰胺和谷氨酰胺;(4)芳香族侧链:苯丙氨酸、酪氨酸和色氨酸;(5)碱性侧链:赖氨酸、精氨酸和组氨酸;(6)酸性侧链:天冬氨酸和谷氨酸,以及(7)含硫侧链:半胱氨酸和甲硫氨酸。
[0133]
抗体可以从含有不同抗原特异性的免疫球蛋白的血清或血浆等来源获得。如果对此类抗体进行亲和纯化,它们可以富集特定的抗原特异性。此类富集的抗体制剂通常由少于约10%的对特定抗原具有特异性结合活性的抗体制成。对这些制剂进行几轮亲和纯化可以增加对抗原具有特异性结合活性的抗体的比例。以这种方式制备的抗体通常被称为“单
特异性”。单特异性抗体制剂可以由约10%、20%、30%、40%、50%、60%、70%、75%、80%、85%、90%、95%、97%、99%或99.9%的对特定抗原具有特异性结合活性的抗体构成。抗体可以使用如下所述的重组核酸技术产生。
[0134]
本文所用的“载体”和相关术语是指可与外来遗传物质(例如核酸转基因)可操作地连接的核酸分子(例如dna或rna)。载体可以用作将外来遗传物质引入细胞(例如宿主细胞)中的运载工具。载体可以包括至少一个限制性核酸内切酶识别序列,用于将转基因插入载体中。载体可以包括至少一个赋予抗生素抗性或可选择的特征的基因序列,以帮助选择携带载体
‑
转基因构建体的宿主细胞。载体可以是单链或双链核酸分子。载体可以是线性或环状核酸分子。一种类型的载体是“质粒”,它是指线性或环形的双链染色体外dna分子,它可以与转基因连接,并能够在宿主细胞中复制,以及转录和/或翻译转基因。病毒载体通常含有可与转基因连接的病毒rna或dna骨架序列。病毒骨架序列可以经修饰以使感染失效,但保留病毒骨架和共同连接的转基因插入宿主细胞基因组中。病毒载体的实例包括逆转录病毒、慢病毒、腺病毒、腺相关病毒、杆状病毒、乳多空病毒、疫苗病毒、单纯疱疹病毒和爱泼斯坦巴尔病毒载体。某些载体能够在其被引入的宿主细胞中自主复制(例如,包含细菌复制起点的细菌载体和附加型哺乳动物载体)。其它载体(例如,非附加型哺乳动物载体)在引入宿主细胞后整合到宿主细胞的基因组中,从而与宿主基因组一起复制。
[0135]“表达载体”是一种可以含有一个或多个调控序列如诱导型和/或组成型启动子和增强子的载体类型。表达载体可以包括核糖体结合位点和/或多腺苷酸化位点。调控序列指导与转导到宿主细胞中的表达载体相连的转基因的转录或转录和翻译。调控序列可以控制转基因的表达水平、时间和/或位置。例如,调控序列可以直接或通过一种或多种其它分子(例如,与调控序列和/或核酸结合的多肽)的作用对转基因施加其影响。调控序列可以是载体的一部分。调控序列的其它实例描述于例如goeddel,1990,基因表达技术:酶学中的方法185(gene expression technology:methods in enzymology 185),academic press,san diego,calif.和baron等人,1995,nucleic acids res.23:3605
‑
3606中。表达载体可以包含本文所述的任何抗bcma抗体的至少一部分。
[0136]
当转基因与载体之间存在联系以允许载体中包含的转基因序列发挥功能或表达时,转基因与载体“可操作地连接”。在一个实施方式中,当调控序列影响到转基因的表达(例如表达的水平、时间或位置)时,转基因与调控序列“可操作地连接”。
[0137]
本文所用的术语“转染”或“转化”或“转导”或其它相关术语是指将外源核酸(例如转基因)转移或引入宿主细胞的过程。“转染的”或“转化的”或“转导的”宿主细胞是已经用外源核酸(转基因)转染、转化或转导的宿主细胞。宿主细胞包括原代受试者细胞及其后代。编码本文所述的任何抗bcma抗体的至少一部分的外源核酸可以被引入宿主细胞。包含本文所述的任何抗bcma抗体的至少一部分的表达载体可以被引入宿主细胞,并且宿主细胞可以表达包含至少一部分抗bcma抗体的多肽。
[0138]
如本文所用的术语“宿主细胞”或“或宿主细胞的群体”或相关术语是指已引入外来(外源或转基因)核酸的细胞(或其群体或多个宿主细胞)。外来核酸可以包括与转基因可操作地连接的表达载体,并且宿主细胞可用于表达外来核酸(转基因)所编码的核酸和/或多肽。宿主细胞(或其群体)可以是培养的细胞或可以从受试者提取。宿主细胞(或其群体)包括原代受试者细胞及其后代,而不考虑传代次数。与母体细胞相比,后代细胞可能含有或
可能不含有相同的遗传物质。宿主细胞涵盖后代细胞。在一个实施方式中,宿主细胞描述了以任何方式被修饰、转染、转导、转化和/或操纵以表达如本文所公开的抗体的任何细胞(包括其后代)。在一个实例中,宿主细胞(或其群体)可以引入与编码本文所述的所需抗体或其抗原结合部分的核酸可操作地连接的表达载体。宿主细胞及其群体可以携带稳定整合到宿主基因组的表达载体或可以携带染色体外表达载体。在一个实施方式中,宿主细胞及其群体可以携带染色体外载体,所述载体在几次细胞分裂后存在,或暂时存在并在几次细胞分裂后消失。
[0139]
宿主细胞可以是原核生物,例如大肠杆菌,或者可以是真核生物,例如单细胞真核生物(例如酵母或其它真菌)、植物细胞(例如烟草或番茄植物细胞)、哺乳动物细胞(例如人细胞、猴细胞、仓鼠细胞、大鼠细胞、小鼠细胞或昆虫细胞)或杂交瘤。在一个实施方式中,宿主细胞可以引入与编码所需抗体的核酸可操作地连接的表达载体,从而产生转染/转化的宿主细胞,其在适合转染/转化的宿主细胞表达抗体的条件下进行培养,并可任选地从转染/转化的宿主细胞中回收抗体(例如,从宿主细胞裂解物中回收)或从培养基中回收。在一个实施方式中,宿主细胞包括非人细胞,包括cho、bhk、ns0、sp2/0和yb2/0。在一个实施方式中,宿主细胞包括人细胞,包括hek293、ht
‑
1080、huh
‑
7和per.c6。宿主细胞的实例包括猴肾细胞的cos
‑
7系(atcc crl 1651)(参见gluzman等人,1981,cell 23:175)、l细胞、c127细胞、3t3细胞(atcc ccl 163)、中国仓鼠卵巢(cho)细胞或其衍生物,如veggie cho和在无血清培养基中生长的相关细胞系(参见rasmussen等人,1998,cytotechnology 28:31)或缺乏dhfr的cho菌株dx
‑
b 11(参见urlaub等人,1980,proc.natl.acad.sci.usa 77:4216
‑
20)、hela细胞、bhk(atcc crl 10)细胞系、源自非洲绿猴肾细胞系cv1(atcc ccl 70)的cv1/ebna细胞系(参见mcmahan等人,1991,embo j.10:2821)、人胚胎肾细胞如293、293ebna或msr 293、人表皮a431细胞、人colo 205细胞、其它转化的灵长类细胞系、正常二倍体细胞、从原生组织体外培养得到的细胞品系、原生外植体、hl
‑
60、u937、hak或jurkat细胞。在一个实施方式中,宿主细胞包括淋巴细胞,如y0、ns0或sp20。在一个实施方式中,宿主细胞是哺乳动物宿主细胞,但不是人类宿主细胞。通常,宿主细胞是可以用编码多肽的核酸转化或转染的培养细胞,所述核酸然后可以在宿主细胞中表达。短语“转基因宿主细胞”或“重组宿主细胞”可用于表示已用待表达的核酸转化或转染的宿主细胞。宿主细胞也可以是包含核酸但不以期望的水平表达核酸的细胞,除非将调控序列引入宿主细胞,使其与核酸可操作地连接。应理解,术语“宿主细胞”不仅指特定的受试者细胞,而且还指此类细胞的后代或潜在后代。因为某些修饰可能会由于例如突变或环境影响而在后续世代中发生,因此这样的后代事实上可能不会与母体细胞相同,但仍包括在本文所用术语的范围内。
[0140]
本公开的多肽(例如抗体和抗原结合蛋白)可以使用本领域已知的任何方法产生。在一个实施例中,多肽是通过重组核酸方法,通过将编码多肽的核酸序列(例如dna)插入重组表达载体中,将重组表达载体引入宿主细胞并由宿主细胞在促进表达的条件下表达而产生。
[0141]
重组核酸操作的一般技术描述于例如sambrook等人,分子克隆:实验室手册(molecular cloning:a laboratory manual),第1
‑
3卷,cold spring harbor laboratory press,第2版,1989或f.ausubel等人,分子生物学中的现行协议(current protocols in molecular biology)(green publishing and wiley
‑
interscience:new york,1987)和定
期更新中,它们以全文引用的方式并入本文中。编码多肽的核酸(例如dna)与携带一种或多种源自哺乳动物、病毒或昆虫基因的合适的转录或翻译调控元件的表达载体可操作地连接。此类调控元件包括转录启动子、控制转录的任选操纵子序列、编码合适的mrna核糖体结合位点的序列以及控制转录和翻译终止的序列。表达载体可以包括赋予在宿主细胞中的复制能力的起点或复制。表达载体可以包括赋予选择以促进转基因宿主细胞(例如转化体)识别的基因。
[0142]
重组dna还可以编码任何类型的蛋白质标签序列,这可能对纯化蛋白质有用。蛋白质标签的实例包括但不限于组氨酸标签、flag标签、myc标签、ha标签或gst标签。用于细菌、真菌、酵母和哺乳动物细胞宿主的适当克隆和表达载体可见于克隆载体:实验室手册(cloning vectors:a laboratory manual),(elsevier,n.y.,1985)。
[0143]
表达载体构建体可以使用适合于宿主细胞的方法引入宿主细胞中。将核酸引入宿主细胞的各种方法是本领域已知的,包括但不限于电穿孔;采用氯化钙、氯化铷、磷酸钙、deae
‑
葡聚糖或其它物质的转染;病毒转染;非病毒转染;微弹轰击;脂转染;以及感染(例如,当载体是感染物时)。合适的宿主细胞包括原核生物、酵母、哺乳动物细胞或细菌细胞。
[0144]
合适的细菌包括革兰氏阴性或革兰氏阳性生物,例如大肠杆菌或芽孢杆菌属。酵母,优选来自酵母属,如酿酒酵母(s.cerevisiae),也可用于生产多肽。各种哺乳动物或昆虫细胞培养系统也可用于表达重组蛋白。luckow和summers,(bio/technology,6:47,1988)综述了用于在昆虫细胞中产生异源蛋白的杆状病毒系统。合适的哺乳动物宿主细胞系的实例包括内皮细胞、cos
‑
7猴肾细胞、cv
‑
1、l细胞、c127、3t3、中国仓鼠卵巢(cho)、人胚胎肾细胞、hela、293、293t和bhk细胞系。通过培养合适的宿主/载体系统以表达重组蛋白来制备纯化的多肽。对于许多应用,本文公开的许多多肽的小尺寸将使在大肠杆菌中表达成为优选的表达方法。然后从培养基或细胞提取物纯化蛋白质。任何抗bcma抗体或其抗原结合蛋白均可以由转基因宿主细胞表达。
[0145]
本文公开的抗体和抗原结合蛋白也可以使用细胞翻译系统产生。出于此类目的,编码多肽的核酸必须经修饰以允许体外转录产生mrna,并允许mrna在所利用的特定无细胞系统(真核生物,如哺乳动物或酵母无细胞翻译系统或原核生物,如细菌无细胞翻译系统)中进行无细胞翻译。
[0146]
编码本文公开的各种多肽中的任一种的核酸可以化学合成。可以选择密码子使用以改善在细胞中的表达。这种密码子使用将取决于所选的细胞类型。已经为大肠杆菌和其它细菌以及哺乳动物细胞、植物细胞、酵母细胞和昆虫细胞开发了专门的密码子使用模式。参见例如:mayfield等人,proc.natl.acad.sci.usa.2003 100(2):438
‑
42;sinclair等人protein expr.purif.2002(1):96
‑
105;connell n d.curr.opin.biotechnol.2001 12(5):446
‑
9;makrides等人microbiol.rev.1996 60(3):512
‑
38;和sharp等人yeast.1991 7(7):657
‑
78。
[0147]
本文所述的抗体和抗原结合蛋白也可以通过化学合成(例如,通过固相多肽合成(solid phase peptide synthesis),第2版,1984,the pierce chemical co.,rockford,ill.中描述的方法)来生产。对蛋白质的修饰也可以通过化学合成产生。
[0148]
本文所述的抗体和抗原结合蛋白可以通过蛋白质化学领域普遍已知的蛋白质的分离/纯化方法进行纯化。非限制性实例包括萃取、重结晶、盐析(例如用硫酸铵或硫酸钠)、
离心、透析、超滤、吸附色谱、离子交换色谱、疏水色谱、正相色谱、反相色谱、凝胶过滤、凝胶渗透色谱、亲和色谱、电泳、逆流分布或这些的任何组合。纯化后,多肽可以交换到不同的缓冲液中和/或通过本领域已知的多种方法中的任一种进行浓缩,包括但不限于过滤和透析。
[0149]
本文所述的纯化的抗体和抗原结合蛋白优选为至少65%纯、至少75%纯、至少85%纯、更优选至少95%纯并且最优选至少98%纯。无论纯度的确切数值如何,多肽对于用作医药产品来说是足够纯的。本文所述的任何抗bcma抗体或其抗原结合蛋白可以由转基因宿主细胞表达,然后使用任何本领域已知的方法纯化至约65
‑
98%的纯度或高水平纯度。
[0150]
在某些实施方式中,本文的抗体和抗原结合蛋白还可以包含翻译后修饰。示例性的翻译后蛋白质修饰包括磷酸化、乙酰化、甲基化、adp
‑
核糖基化、泛素化、糖基化、羰基化、苏素化、生物素化或添加多肽侧链或疏水基团。因此,修饰的多肽可能含有非氨基酸元素,如脂质、多糖或单糖和磷酸盐。糖基化的优选形式是唾液酸化,其将一个或多个唾液酸部分与多肽缀合。唾液酸部分改善了溶解度和血清半衰期,同时也降低了蛋白质的可能免疫原性。参见raju等人biochemistry.2001 31;40(30):8868
‑
76。
[0151]
在一个实施方式中,本文所述的抗体和抗原结合蛋白可以被修饰成可溶性多肽,这包括将抗体和抗原结合蛋白与非蛋白质聚合物连接。在一个实施方式中,非蛋白质聚合物包括聚乙二醇(“peg”)、聚丙二醇或聚氧化烯,其方式如美国专利第4,640,835号;第4,496,689号;第4,301,144号;第4,670,417号;第4,791,192号或第4,179,337号中所述。
[0152]
peg是一种水溶性聚合物,其可商购或可以根据本领域众所周知的方法通过乙二醇的开环聚合来制备(sandler和karo,polymer synthesis,academic press,new york,第3卷,第138
‑
161页)。术语“peg”广泛用于涵盖任何聚乙二醇分子,不考虑大小或peg末端的修饰,并且可以由下式表示:x
‑
o(ch2ch2o)
n
‑
ch2ch2oh(1),其中n为20至2300并且x为h或末端修饰,例如c1‑4烷基。在一个实施方式中,peg在一端以羟基或甲氧基终止,即x是h或ch3(“甲氧基peg”)。peg可以含有结合反应所必需的其它化学基团;由分子的化学合成产生;或者是分子各部分最佳距离的间隔物。此外,这种peg可以由一个或多个peg侧链组成,这些侧链连接在一起。具有一个以上peg链的peg被称为多臂或支链peg。例如,支链peg可以通过将聚环氧乙烷加入各种多元醇,包括甘油、季戊四醇和山梨糖醇来制备。例如,四臂支链peg可以由季戊四醇和环氧乙烷制备。支链peg描述于例如ep
‑
a 0 473 084和美国专利第5,932,462号中。peg的一种形式包括通过赖氨酸的伯氨基连接的两个peg侧链(peg2)(monfardini等人,bioconjugate chem.6(1995)62
‑
69)。
[0153]
peg修饰的多肽的血清清除率相对于未修饰的抗体和抗原结合蛋白结合多肽的清除率可被调节(例如增加或减少)约10%、20%、30%、40%、50%、60%、70%、80%或甚至90%。peg修饰的抗体和抗原结合蛋白可具有相对于未修饰多肽的半衰期增加的半衰期(t
1/2
)。peg修饰的多肽的半衰期相对于未修饰的抗体和抗原结合蛋白的半衰期可增加至少10%、20%、30%、40%、50%、60%、70%、80%、90%、100%、125%、150%、175%、200%、250%、300%、400%或500%,或甚至1000%。在一些实施方式中,蛋白质半衰期是在体外测定的,如在缓冲盐水溶液中或在血清中。在其它实施方式中,蛋白质半衰期是体内半衰期,如蛋白质在动物血清或其它体液中的半衰期。
[0154]
本公开提供包含本文所述的任何抗bcma抗体或其抗原结合蛋白和药学上可接受的赋形剂的治疗组合物。赋形剂涵盖载剂、稳定剂和赋形剂。药学上可接受的赋形剂的赋形
剂包括例如惰性稀释剂或填充剂(例如蔗糖和山梨糖醇)、润滑剂、助滑剂和抗粘剂(例如硬脂酸镁、硬脂酸锌、硬脂酸、二氧化硅、氢化植物油或滑石)。其他的实例包括缓冲剂、稳定剂、防腐剂、非离子型清洁剂、抗氧化剂和等渗剂。
[0155]
治疗组合物及其制备方法是本领域众所周知的,并且可见于例如“雷明顿:药学的科学与实践(remington:the science and practice of pharmacy)”(第20版,a.r.gennaro a r.编,2000,lippincott williams&wilkins,philadelphia,pa.)。治疗组合物可以配制用于肠胃外施用,并且可以例如含有赋形剂、无菌水、生理盐水、聚烷二醇如聚乙二醇、植物来源的油或氢化萘。生物相容性、可生物降解的丙交酯聚合物、丙交酯/乙交酯共聚物或聚氧乙烯
‑
聚氧丙烯共聚物可用于控制本文所述的抗体(或其抗原结合蛋白)的释放。纳米颗粒配制品(例如,可生物降解的纳米颗粒、固体脂质纳米颗粒、脂质体)可用于控制抗体(或其抗原结合蛋白)的生物分布。其它可能有用的肠胃外递送系统包括乙烯
‑
乙酸乙烯酯共聚物颗粒、渗透泵、可植入输注系统和脂质体。配制品中抗体(或其抗原结合蛋白)的浓度取决于多种因素而变化,包括待施用的药物剂量和施用途径。
[0156]
任何抗bcma抗体(或其抗原结合部分)可以任选地以药学上可接受的盐形式施用,如制药业中常用的无毒酸加成盐或金属络合物。酸加成盐的实例包括有机酸,如乙酸、乳酸、双羟萘酸、马来酸、柠檬酸、苹果酸、抗坏血酸、琥珀酸、苯甲酸、棕榈酸、辛二酸、水杨酸、酒石酸、甲磺酸、甲苯磺酸或三氟乙酸等;聚合酸,如单宁酸、羧甲基纤维素等;和无机酸,如盐酸、氢溴酸、硫酸、磷酸等。金属络合物包括锌、铁等。在一个实例中,抗体(或其抗原结合部分)在乙酸钠存在下配制以增加热稳定性。
[0157]
任何抗bcma抗体(或其抗原结合部分)可配制成口服使用,包括含有活性成分与无毒药学上可接受的赋形剂的混合物的片剂。用于口服使用的配制品也可提供为咀嚼片,或硬明胶胶囊,其中活性成分与惰性固体稀释剂混合,或软明胶胶囊,其中活性成分与水或油介质混合。
[0158]
如本文所用,术语“受试者”是指人和非人动物,包括脊椎动物、哺乳动物和非哺乳动物。在一个实施方式中,受试者可以是人、非人灵长类动物、猿猴、猿、鼠(例如小鼠和大鼠)、牛、猪、马、犬、猫、山羊、狼、蛙或鱼。
[0159]
术语“施用(administering/administered)”和语法变体是指使用本领域技术人员已知的各种方法和递送系统中的任一种将药剂物理引入受试者体内。本文公开的配制品的示例性施用途径包括静脉内、肌肉内、皮下、腹膜内、脊髓或其它肠胃外施用途径,例如通过注射或输注。如本文所用,短语“肠胃外施用”是指除肠内和局部施用以外的施用方式,通常通过注射,包括但不限于静脉内、肌肉内、动脉内、鞘内、淋巴管内、病灶内、囊内、眶内、心内、皮内、腹膜内、经气管、皮下、关节内、囊下、蛛网膜下、椎管内、硬膜外和胸骨内注射和输注,以及体内电穿孔。在一些实施方式中,配制品通过非肠胃外途径施用,例如口服。其它非肠胃外途径包括局部、表皮或粘膜施用途径,例如鼻内、经阴道、经直肠、舌下或局部。施用也可以例如进行一次、多次和/或经过一个或多个延长的时期。本文所述的任何抗bcma抗体(或其抗原结合蛋白)可以使用本领域已知的方法和递送途径施用于受试者。
[0160]
术语“有效量”、“治疗有效量”或“有效剂量”或相关术语可以互换使用,指的是抗体或抗原结合蛋白(例如,本文所述的任何抗bcma抗体或其抗原结合蛋白)的量,当施用于受试者时,足以实现与肿瘤或癌症抗原表达相关的疾病或病症的可测量的改善或预防。本
文提供的抗体在单独或组合使用时的治疗有效量将取决于抗体和组合的相对活性(例如,在抑制细胞生长方面),并取决于所治疗的受试者和治疗的疾病状况、受试者的体重、年龄和性别、受试者的疾病状况的严重程度、施用方式等,这些都可以由本领域的普通技术人员容易地确定。
[0161]
在一个实施方式中,治疗有效量将取决于待治疗的受试者和待治疗的病症的某些方面,并且可由本领域的技术人员使用已知技术确定。一般来说,多肽以每天约0.01g/kg至约50mg/kg,优选每天0.01mg/kg至约30mg/kg,最优选每天0.1mg/kg至约20mg/kg施用。多肽可以每天(例如,每天一次、两次、三次或四次)或优选地以较低频率(例如,每周、每两周、每三周、每月或每季度)施用。此外,如本领域已知,可能需要根据年龄以及体重、一般健康状况、性别、饮食、施用时间、药物相互作用和疾病的严重程度进行调整。
[0162]
本公开提供了用于治疗患有与bcma表达相关的疾病的受试者的方法。所述疾病包括表达肿瘤相关抗原的癌症或肿瘤细胞。在一个实施方式中,癌症或肿瘤包括前列腺癌、乳腺癌、卵巢癌、头颈癌、膀胱癌、皮肤癌、结肠直肠癌、肛门癌、直肠癌、胰腺癌、肺癌(包括非小细胞肺癌和小细胞肺癌)、平滑肌瘤、脑癌、神经胶质瘤、神经胶质母细胞瘤、食道癌、肝癌、肾癌、胃癌、结肠癌、子宫颈癌、子宫癌、子宫内膜癌、外阴癌、喉癌、阴道癌、骨癌、鼻腔癌、副鼻窦癌、鼻咽癌、口腔癌、口咽癌、喉癌、下喉癌、唾液腺癌、输尿管癌、尿道癌、阴茎癌和睾丸癌。
[0163]
在一个实施方式中,癌症包括血液癌症,包括白血病、淋巴瘤、骨髓瘤和b细胞淋巴瘤。血液癌症包括多发性骨髓瘤(mm)、包括伯基特氏淋巴瘤(bl)的非霍奇金氏淋巴瘤(nhl)、b慢性淋巴细胞性白血病(b
‑
cll)、全身性红斑狼疮(sle)、b和t急性淋巴细胞性白血病(all)、急性骨髓性白血病(aml)、慢性淋巴细胞性白血病(cll)、弥漫性大b细胞淋巴瘤、慢性骨髓性白血病(cml)、毛细胞白血病(hcl)、滤泡性淋巴瘤、瓦尔登斯特伦氏巨球蛋白血症、套细胞淋巴瘤、霍奇金氏淋巴瘤(hl)、浆细胞骨髓瘤、前体b细胞淋巴母细胞性白血病/淋巴瘤、浆细胞瘤、巨细胞骨髓瘤、浆细胞骨髓瘤、重链骨髓瘤、轻链或本周氏骨髓瘤、淋巴瘤样肉芽肿病、移植后淋巴增生性病症、免疫调节病症、类风湿性关节炎、重症肌无力、特发性血小板减少性紫癜、抗磷脂综合征、恰加斯氏病、格雷夫氏病、韦格纳氏肉牙肿病、结节性多动脉炎、休格连氏综合征、寻常型天疱疮、硬皮病、多发性硬化症、抗磷脂综合征、anca相关血管炎、古德帕斯彻氏病、川崎病、自身免疫性溶血性贫血和急进性肾小球肾炎、重链病、原发性或免疫细胞相关淀粉样变性和意义未明的单克隆丙种球蛋白病。
[0164]
本公开提供了特异性结合bcma的bcma结合蛋白,特别是抗bcma抗体或其抗原结合部分,以及其用途。在一个实施方式中,bcma结合蛋白结合bcma(b细胞成熟抗原(bcma)的表位。bcma也称为tnfrsf17和cd269(例如uniprot q02223))。抗bcma抗体的各个方面涉及抗体片段、单链抗体、药物组合物、核酸、重组表达载体、宿主细胞以及制备和使用此类抗bcma抗体的方法。使用抗bcma抗体的方法包括结合bcma、检测bcma和治疗与bcma表达相关的疾病的体外和体内方法。
[0165]
本公开提供了与bcma多肽(例如抗原靶)或bcma多肽的片段特异性结合的抗原结合蛋白。在一个实施方式中,bcma靶抗原包括具有野生型或多态性或突变型氨基酸序列的天然存在的多肽(例如uniprot登录号q02223
‑
1)。bcma靶抗原可以通过重组方法制备或可以化学合成。bcma靶抗原可以呈可溶形式或膜结合形式(例如,由细胞或噬菌体表达)。在一
个实施方式中,bcma靶抗原由细胞表达,例如天然表达bcma或被工程化以表达bcma的癌症或非癌症细胞系,如u2392、ejm、mmur、u266、opm2、h929、jjn
‑
3、rpmi
‑
8226、k562、ncih929、anbl
‑
6、dp
‑
6、kas
‑
6/1、kp6或jmw。不表达bcma的细胞系预计不会与抗bcma抗体结合,如k562、a549和tc71细胞系。bcma靶抗原可以是融合蛋白或与例如可检测部分如荧光团缀合。bcma靶抗原可以结合april和/或baff。bcma靶抗原可以呈突变形式,增加或减少与april和/或baff的结合。在一个实施方式中,人bcma靶抗原包含seq id no:1(例如,来自lifespan biosciences的重组人bcma,目录号ls
‑
g5771)或seq id no:2(例如,来自acrobiosystems的带有his标签的重组人bcma,目录号bca
‑
h522y
‑
100ug)的氨基酸序列。在一个实施方式中,bcma靶抗原是包含seq id no:3或4的氨基酸序列的突变多肽。在一个实施方式中,野生型和/或突变型人bcma抗原可用于比较本文所述的任何抗bcma抗体与对照抗bcma抗体的结合能力的分析,和/或用于比较本文所述的任何抗bcma抗体与对照抗bcma抗体的结合能力的表位作图分析。
[0166]
本公开提供了与bcma多肽结合的igg类的全人抗体。在一个实施方式中,抗bcma抗体包含与seq id no:8、10、12、14或22或其组合的氨基酸序列具有至少95%序列同一性、或至少96%序列同一性、或至少97%序列同一性、或至少98%序列同一性、或至少99%序列同一性的重链可变区;和/或抗bcma抗体包含与seq id no:9、11、13、15、16、17、18、19、20、21或23或其组合的氨基酸序列具有95%序列同一性、或至少96%序列同一性、或至少97%序列同一性、或至少98%序列同一性、或至少99%序列同一性的轻链可变区。在一个实施方式中,抗bcma抗体包括igg1、igg2、igg3或igg4类抗体。在一个实施方式中,抗bcma抗体包括igg1或igg4类抗体。
[0167]
在一个实施方式中,抗bcma抗体或其片段包含抗原结合部分,其结合bcma靶抗原的表位的结合亲和力(k
d
)为10
‑6m或更小、10
‑7m或更小、10
‑8m或更小、10
‑9m或更小、或10
‑
10
m或更小(参见图3
‑
10和表2和3)。在一个实施方式中,bcma抗原包括细胞表面bcma抗原或可溶性bcma抗原。在一个实施方式中,bcma抗原包含细胞表面bcma抗原的胞外部分。在一个实施方式中,bcma抗原包括人或非人bcma抗原。在一个实施方式中,bcma抗原由人或非人细胞表达。在一个实施方式中,抗bcma抗体结合由人b细胞表达或由人多发性骨髓瘤细胞表达的人bcma。在一个实施方式中,可以使用表面等离子体共振、流式细胞术和/或elisa检测和测量抗bcma抗体或其片段之间的结合。
[0168]
在一个实施方式中,抗bcma抗体或抗原结合片段包含结合人bcma表位并阻断人april和/或人baff与人bcma表位的结合(例如抑制结合)的抗原结合部分。在一个实施方式中,april是指人增殖诱导配体(也称为tnf13、cd256),其可从r&d systems(目录号5860
‑
ap
‑
010/cf)或ibi scientific(目录号#rph
‑
151)商购获得。在一个实施方式中,baff是指人baff(例如uniprot登录号q9y275)。在一个实施方式中,抗bcma抗体或抗原结合片段阻断人april和/或人baff与人bcma表位的结合,使结合水平降低约5
‑
25%,或约25
‑
45%,或约45
‑
65%,或约65
‑
85%,或约85
‑
95%或更高的结合水平降低。
[0169]
在一个实施方式中,抗bcma抗体使april依赖性或baff依赖性nf
‑
κb激活减少约1
‑
5%(或小于约1%),约5
‑
25%,或约25
‑
45%,或约45
‑
65%,或约65
‑
85%,或约85
‑
95%或更高的结合水平降低。
[0170]
本公开提供了一种抗bcma抗体或抗原结合片段,其结合来自人的bcma表位,或可
以与来自非人动物如小鼠、大鼠、山羊、兔子、仓鼠和/或猴子(例如食蟹猕猴)中的任何一种或任何组合的bcma(例如同源抗原)表位结合(例如交叉反应)。在一个实施方式中,抗bcma抗体或抗原结合片段结合小鼠bcma的结合亲和力k
d
为10
‑5m或更小,或10
‑6m或更小,或10
‑7m或更小,或10
‑8m或更小,或10
‑9m或更小,或10
‑
10
m或更小。在一个实施方式中,抗bcma抗体或抗原结合片段结合食蟹猕猴bcam的结合亲和力k
d
为10
‑5m或更小,或10
‑6m或更小,或10
‑7m或更小,或10
‑8m或更小,或10
‑9m或更小,或10
‑
10
m或更小。在一个实施方式中,食蟹猕猴bcma可从acrobiosystems(目录号bca
‑
c52h7)商购获得。在一个实施方式中,小鼠bcma可从acrobiosystems(目录号bca
‑
m52h3)商购获得。
[0171]
本公开提供了一种抗bcma抗体或抗原结合片段,其结合来自人的april和/或baff的表位,或可以与来自非人动物如小鼠、大鼠、山羊、兔子、仓鼠和/或猴子(例如食蟹猕猴)中的任何一种或任何组合的april和/或baff(例如同源抗原)的表位结合(例如交叉反应)。在一个实施方式中,人april蛋白可从r&d systems(目录号5860
‑
ap
‑
010/cf)或ibi scientific(目录号rph
‑
151)商购获得。
[0172]
本公开提供了一种包含重链和轻链的全人抗体,其中重/轻链可变区氨基酸序列与以下任何一个氨基酸序列组具有至少95%序列同一性,或至少96%序列同一性,或至少97%序列同一性,或至少98%序列同一性,或至少99%序列同一性:seq id no:8和9(本文称为bca7)、seq id no:10和11(本文称为bc4c9)、seq id no:12和13(本文称为cd5c4)、seq id no:14和15(本文称为bc6g8)、seq id no:8和16(本文称为bca7
‑
2c5)、seq id no:8和17(本文称为bca7
‑
2e1)、seq id no:8和18(本文称为bca7
‑
2d11)、seq id no:8和19(本文称为bca7
‑
2g2)、seq id no:8和20(本文称为bca7
‑
2d8)、seq id no:8和21(本文称为bca7
‑
2e8)或seq id no:22和23(本文称为bca7
‑
2c5全长)。
[0173]
本公开提供了一种fab全人抗体片段,其包含来自重链的重链可变区和来自轻链的可变区,其中来自重链的可变区的序列与seq id no:8、10、12、14或22或其组合的氨基酸序列至少95%相同,或至少96%相同,或至少97%相同,或至少98%相同,或至少99%相同。来自轻链的可变区的序列与seq id no:9、11、13、15、16、17、18、19、20、21或23或其组合的氨基酸序列至少95%相同,或至少96%相同,或至少97%相同,或至少98%相同,或至少99%相同。
[0174]
本公开提供了一种fab全人抗体片段,其包含重链可变区和轻链可变区,其中重/轻链可变区氨基酸序列与以下任何一个氨基酸序列组至少95%相同,或至少96%相同,或至少97%相同,或至少98%相同,或至少99%相同:seq id no:8和9(本文称为bca7)、seq id no:10和11(本文称为bc4c9)、seq id no:12和13(本文称为cd5c4)、seq id no:14和15(本文称为bc6g8)、seq id no:8和16(本文称为bca7
‑
2c5)、seq id no:8和17(本文称为bca7
‑
2e1)、seq id no:8和18(本文称为bca7
‑
2d11)、seq id no:8和19(本文称为bca7
‑
2g2)、seq id no:8和20(本文称为bca7
‑
2d8)、seq id no:8和21(本文称为bca7
‑
2e8)或seq id no:22和23(本文称为bca7
‑
2c5全长)。
[0175]
本公开提供了一种单链全人抗体,其包含具有来自全人重链的可变区和来自全人轻链的可变区的多肽链,以及任选地连接重链可变区和轻链可变区的接头,其中重链可变区与seq id no:8、10、12、14或22或其组合的氨基酸序列包含至少95%序列同一性,或至少96%序列同一性,或至少97%序列同一性,或至少98%序列同一性,或至少99%序列同一
性。轻链可变区与seq id no:9、11、13、15、16、17、18、19、20、21或23或其组合的氨基酸序列包含至少95%序列同一性,或至少96%序列同一性,或至少97%序列同一性,或至少98%序列同一性,或至少99%序列同一性。
[0176]
本公开提供了一种单链全人抗体,其包含具有重链可变区和轻链可变区的多肽链,其中重/轻链可变区氨基酸序列组与以下任何一个氨基酸序列组至少95%相同,或至少96%相同,或至少97%相同,或至少98%相同,或至少99%相同:seq id no:8和9(本文称为bca7)、seq id no:10和11(本文称为bc4c9)、seq id no:12和13(本文称为cd5c4)、seq id no:14和15(本文称为bc6g8)、seq id no:8和16(本文称为bca7
‑
2c5)、seq id no:8和17(本文称为bca7
‑
2e1)、seq id no:8和18(本文称为bca7
‑
2d11)、seq id no:8和19(本文称为bca7
‑
2g2)、seq id no:8和20(本文称为bca7
‑
2d8)、seq id no:8和21(本文称为bca7
‑
2e8)或seq id no:22和23(本文称为bca7
‑
2c5全长)。
[0177]
本公开提供了包含本文所述的任何抗bcma抗体或抗原结合片段和药学上可接受的赋形剂的药物组合物。赋形剂涵盖载剂和稳定剂。在一个实施方式中,药物组合物包含抗bcma抗体或其抗原结合片段,其包含重链可变区和轻链可变区,其中重/轻链可变区氨基酸序列与以下任何一个氨基酸序列组至少95%相同,或至少96%相同,或至少97%相同,或至少98%相同,或至少99%相同:seq id no:8和9(本文称为bca7)、seq id no:10和11(本文称为bc4c9)、seq id no:12和13(本文称为cd5c4)、seq id no:14和15(本文称为bc6g8)、seq id no:8和16(本文称为bca7
‑
2c5)、seq id no:8和17(本文称为bca7
‑
2e1)、seq id no:8和18(本文称为bca7
‑
2d11)、seq id no:8和19(本文称为bca7
‑
2g2)、seq id no:8和20(本文称为bca7
‑
2d8)、seq id no:8和21(本文称为bca7
‑
2e8)或seq id no:22和23(本文称为bca7
‑
2c5全长)。
[0178]
本公开提供了一种试剂盒,其包含本文所述的抗bcma抗体或其抗原结合片段中的任何一种或两种或更多种的任何组合。在一个实施方式中,试剂盒包含两种或更多种抗bcma抗体或其抗原结合片段中的任何一种或任何组合,所述抗体或其抗原结合片段包含重链可变区和轻链可变区,其中重/轻链可变区氨基酸序列与以下任何一个氨基酸序列组至少95%相同,或至少96%相同,或至少97%相同,或至少98%相同,或至少99%相同:seq id no:8和9(本文称为bca7)、seq id no:10和11(本文称为bc4c9)、seq id no:12和13(本文称为cd5c4)、seq id no:14和15(本文称为bc6g8)、seq id no:8和16(本文称为bca7
‑
2c5)、seq id no:8和17(本文称为bca7
‑
2e1)、seq id no:8和18(本文称为bca7
‑
2d11)、seq id no:8和19(本文称为bca7
‑
2g2)、seq id no:8和20(本文称为bca7
‑
2d8)、seq id no:8和21(本文称为bca7
‑
2e8)或seq id no:22和23(本文称为bca7
‑
2c5全长)。试剂盒可用于检测例如生物样品中bcma抗原的存在或不存在。试剂盒可用于进行体外反应,如eliza、流式细胞术或等离子体表面共振形式的抗原结合分析;体外细胞激活分析,包括nf
‑
κb激活分析;荧光素酶报告基因分析;蛋白质印迹和检测;以及其它此类体外分析。试剂盒可用于治疗患有bcma相关疾病或病症如多发性骨髓瘤的受试者。
[0179]
本公开提供了用于抑制靶细胞生长或增殖的方法,或用于杀死靶细胞的方法,所述方法包括:在适合杀死靶细胞的条件下,使效应细胞的群体与靶细胞(例如表达bcma的靶细胞)的群体在本文所述的抗bcma抗体(或其抗体片段)存在下接触。在一个实施方式中,效应细胞的群体包含外周血单核细胞(pbmc)或自然杀伤(nk)细胞。pbmc可以包括淋巴细胞,
包括t细胞、b细胞和/或nk细胞。在一个实施方式中,靶细胞的群体包含天然表达bcma的细胞,包括b细胞、多发性骨髓瘤(mm)细胞或来自患有与bcma表达相关的疾病的受试者的任何类型的b细胞。在一个实施方式中,靶细胞的群体是经工程化以表达bcma的任何类型的转基因细胞。在一个实施方式中,效应细胞与靶细胞的比例可以是约1:1,或约2:1,或约3:1,或约4:1,或约5:1,或约5
‑
10:1,或约10
‑
20:1,或约20
‑
30:1。
[0180]
本公开提供了用于治疗患有与bcma过度表达相关的疾病或bcma阳性癌症的受试者的方法,所述方法包括:向受试者施用有效量的治疗组合物,所述治疗组合物包含本文所述的抗bcma抗体或其抗原结合片段,例如其选自由以下组成的组:本文所述的任何全人抗bcma抗体、本文所述的任何fab全人抗bcma抗体和本文所述的任何单链人抗bcma抗体。在一个实施方式中,bcma阳性癌症包括:b细胞白血病、b细胞淋巴瘤或b细胞骨髓瘤。还提供了用于治疗患有与bcma表达相关的疾病的受试者的方法,其中与bcma表达相关的疾病选自由以下组成的组:多发性骨髓瘤(mm)、包括伯基特氏淋巴瘤(bl)的非霍奇金氏淋巴瘤(nhl)、b慢性淋巴细胞性白血病(b
‑
cll)、全身性红斑狼疮(sle)、b和t急性淋巴细胞性白血病(all)、急性骨髓性白血病(aml)、慢性淋巴细胞性白血病(cll)、弥漫性大b细胞淋巴瘤、慢性骨髓性白血病(cml)、毛细胞白血病(hcl)、滤泡性淋巴瘤、瓦尔登斯特伦氏巨球蛋白血症、套细胞淋巴瘤、霍奇金氏淋巴瘤(hl)、浆细胞骨髓瘤、前体b细胞淋巴母细胞性白血病/淋巴瘤、浆细胞瘤、巨细胞骨髓瘤、浆细胞骨髓瘤、重链骨髓瘤、轻链或本周氏骨髓瘤、淋巴瘤样肉芽肿病、移植后淋巴增生性病症、免疫调节病症、类风湿性关节炎、重症肌无力、特发性血小板减少性紫癜、抗磷脂综合征、恰加斯氏病、格雷夫氏病、韦格纳氏肉牙肿病、结节性多动脉炎、休格连氏综合征、寻常型天疱疮、硬皮病、多发性硬化症、抗磷脂综合征、anca相关血管炎、古德帕斯彻氏病、川崎病、自身免疫性溶血性贫血和急进性肾小球肾炎、重链病、原发性或免疫细胞相关淀粉样变性和意义未明的单克隆丙种球蛋白病,所述方法包括:向受试者施用有效量的包含本文所述的抗体或其抗原结合片段的治疗组合物。
[0181]
序列表:
[0182]
野生型人bcma蛋白(5
‑
54)seq id no:1:
[0183]
agqcsqneyfdsllhacipcqlrcssntppltcqrycnasvtnsvkgtna.
[0184]
野生型人bcma蛋白(1
‑
54)seq id no:2:
[0185]
mlqmagqcsqneyfdsllhacipcqlrcssntppltcqrycnasvtnsvkgtna.
[0186]
野生型人bcma蛋白(uniprot q02223
‑
1)seq id no:92
[0187]
mlqmagqcsqneyfdsllhacipcqlrcssntppltcqrycnasvtnsvkgtnailwtclglsliislavfvlmfllrkinseplkdefkntgsgllgmanidleksrtgdeiilprgleytveectcedcikskpkvdsdhcfplpameegatilvttktndyckslpaalsateieksisar.
[0188]
突变体
‑
1人bcma蛋白seq id no:3:
[0189]
mlqmagqcsqneyfdsgghacipcqlrcssntppltcqrycnasvtnsvkgtna.
[0190]
突变体
‑
2人bcma蛋白seq id no:4:
[0191]
mlqmagqcsqneyfdsllhacipcqlrcssnppgtcqrycnasvtnsvkgtna.
[0192]
野生型人bcma蛋白
‑
小鼠fc seq id no:5:
[0193]
mlqmagqcsqneyfdsllhacipcqlrcssntppltcqrycnasvtnsvkgtnaglgglvdykddddkthtcppckcpapnllggpsvfifppkikdvlmislspivtcvvvdvseddpdvqiswfvnnvevhtaqtqthredy
nstlrvvsalpiqhqdwmsgkefkckvnnkdlpapiertiskpkgsvrapqvyvlpppeeemtkkqvtltcmvtdfmpediyvewtnngktelnykntepvldsdgsyfmysklrvekknwvernsyscsvvheglhnhhttksfsrtpgk.
[0194]
突变体
‑
1人bcma蛋白
‑
小鼠fc seq id no:6:
[0195]
mlqmagqcsqneyfdsgghacipcqlrcssntppltcqrycnasvtnsvkgtnaglgglvdykddddkthtcppckcpapnllggpsvfifppkikdvlmislspivtcvvvdvseddpdvqiswfvnnvevhtaqtqthredynstlrvvsalpiqhqdwmsgkefkckvnnkdlpapiertiskpkgsvrapqvyvlpppeeemtkkqvtltcmvtdfmpediyvewtnngktelnykntepvldsdgsyfmysklrvekknwvernsyscsvvheglhnhhttksfsrtpgk.
[0196]
突变体
‑
2人bcma蛋白
‑
小鼠fc seq id no:7:
[0197]
mlqmagqcsqneyfdsllhacipcqlrcssnppgtcqrycnasvtnsvkgtnaglgglvdykddddkthtcppckcpapnllggpsvfifppkikdvlmislspivtcvvvdvseddpdvqiswfvnnvevhtaqtqthredynstlrvvsalpiqhqdwmsgkefkckvnnkdlpapiertiskpkgsvrapqvyvlpppeeemtkkqvtltcmvtdfmpediyvewtnngktelnykntepvldsdgsyfmysklrvekknwvernsyscsvvheglhnhhttksfsrtpgk.
[0198]
表1:
[0199]
[0200]
[0201][0202]
表2:
[0203]
[0204]
[0205][0206]
实施例
[0207]
以下实施例旨在为说明性的,可用于进一步理解本公开的实施方式,并且不应被解释为以任何方式限制本教示的范围。
[0208]
实施例1:产生抗bcma抗体.
[0209]
单克隆噬菌体elisa用于从全人抗体库中选择抗体。采用标准淘选程序来选择结合bcma蛋白和表达bcma的rpmi8226细胞系的抗体。使用标准分子生物学技术,将scfv克隆到sti
‑
fc载体中,或将重链和轻链可变区克隆到含有各自恒定区的sti重链和λ轻链载体中。含有经验证的插入序列的质粒用于在cho
‑
s细胞中瞬时表达,并使用蛋白a树脂纯化抗体。选择的抗bcma抗体包括bca7、bc4c9、bc5c4和bc6g8。
[0210]
使用软随机噬菌体库对bca7抗体克隆进行亲和力成熟。bca8噬菌粒dna用作pcr模板。六个简并寡核苷酸用作pcr引物以将突变引入六个cdr区。pcr片段用限制酶消化并连接到线性化的噬菌粒载体pcgmt3中,并电穿孔到大肠杆菌ss320细胞中。使用人bcma蛋白和表达bcma的prmi8226细胞系进行淘选。选择的抗bcma抗体包括bca7
‑
2c5、bca7
‑
2e1、bca7
‑
2d11、bca7
‑
2g2、bca7
‑
2d8和bca7
‑
2e8。
[0211]
实施例2:使用表面等离子体共振测量结合亲和力.
[0212]
使用表面等离子体共振(spr)测量抗bcma抗体与带有his标签的人bcma蛋白(acrobiosystems,目录号bca
‑
h522y
‑
100ug,uniprot q02223
‑
1,seq id no:92)的结合动力学。使用biacore t200表面等离子体共振(ge healthcare)在25℃下测量抗体与带有his标签的bcma蛋白之间的动力学相互作用。使用标准n
‑
羟基琥珀酰亚胺/n
‑
乙基
‑
n
′‑
(3
‑
二甲氨基丙基)碳化二亚胺盐酸盐(nhs/edc)偶联方法,将抗人片段可结晶区(fc区)抗体固定在cm5传感器芯片上以达到约8000个共振单位(ru)。抗bcma抗体(2μg/ml)以10μl/min的流速捕获60秒。带有his标签的bcma蛋白在0.01m hepes ph 7.4、0.15m nacl、3mm edta、0.05%v/v surfactant p20(hbs
‑
ep+)的运行缓冲液中,以3.12、6.25、12.5、25、50、100和200nm的六个不同稀释度运行。测量25nm bcma蛋白运行两次。所有测量均在hbs
‑
ep+缓冲液中进行,流速为30μl/min。使用1:1(langmuir)结合模型来拟合数据。抗bcma抗体bca7、gsk j6m0、
bc4c9和bc5c4的spr传感图分别显示于图1、2、3和4中,其相应的结合动力学列于表3。
[0213]
表3:
[0214] ka(1/ms)kd(1/s)k
d
(m)χ2(ru2)模型bc4c92.08e+045.67e
‑
042.73e
‑
080.1461:1结合bc5c43.56e+063.30e
‑
029.27e
‑
090.2811:1结合bca71.03e+031.80e
‑
021.75e
‑
050.08471:1结合gsk
‑
j6m01.97e+054.96e
‑
042.52e
‑
090.0221:1结合
[0215]
以上述方式分析了优化的抗bcma抗体bca7
‑
2c5、bca7
‑
2d11、bca7
‑
2g2、bca7
‑
2e1、bca7
‑
2d8和bca7
‑
2e8与带有his标签的人bcma蛋白(acrobiosystems,目录号bca
‑
h522y
‑
100ug)的结合动力学。传感图分别显示于图5
‑
10中,其相应的结合动力学列于表4。优化的抗bcma抗体表现出与bcma蛋白的结合明显改善。
[0216]
表4:
[0217] ka1(1/ms)kd1(1/s)ka2(1/s)kd2(1/s)k
d
(m)χ2(ru2)bca7785.90.034930.0046350.012043.21e
‑
050.08412c51.37e+060.042168.47e
‑
040.001451.94e
‑
080.05312e12.51e+060.15060.0017979.29e
‑
042.04e
‑
080.02452d111.87e+060.26080.0038157.10e
‑
042.19e
‑
080.01312g23.21e+040.0037610.0014320.0012095.37e
‑
081.322d82.43e+061.0920.011320.0025988.38e
‑
080.06822e84.87e+040.020230.011890.0070741.55e
‑
071.42
[0218]
实施例3:使用表面等离子体共振测量结合亲和力.
[0219]
通过spr以上述方式分析两种抗bcma抗体bca7
‑
2c5和bca7
‑
2e1与带有his标签的人、食蟹猕猴或小鼠bcma蛋白的交叉反应性。所有三种带有his标签的bcma蛋白均从acrobiosystems获得:带有his标签的人bcma蛋白(目录号bca
‑
h522y
‑
100ug)、带有his标签的食蟹猕猴bcma蛋白(目录号bca
‑
c52h7)和带有his标签的小鼠bcma蛋白(目录号bca
‑
m52h3)。传感图显示于:具有kd值的图11a和b(2c5和2e1抗体分别与人bcma蛋白结合);具有kd值的图12a和b(2c5和2e1抗体分别与食蟹猕猴bcma蛋白结合);以及具有kc值的图13a和b(2c5和2e1分别与小鼠bcma蛋白结合)。
[0220]
实施例4:elisa交叉反应性.
[0221]
通过elisa分析法分析抗bcma抗体与来自人、食蟹猕猴或小鼠的带有his标签的bcma蛋白的交叉反应性。ni
‑
nta板涂布有2μg/ml带有his标签的bcma蛋白(列于上述实施例2中),然后与20μg/ml抗bcma抗体反应,并与1:2500稀释的抗人fc hrp(kpl scientific,目录号5220
‑
0279)反应。图14显示了8组,从左到右分别是抗bcma抗体2c5、2e1、4c9、5c4、bluebird c11d5(bb c11d5)、gsk j6m0、同型对照抗体和杜尔贝科氏磷酸盐缓冲盐水。每组包括5个测试抗原或缓冲液,从左到右分别是:阴性对照抗原、带有his标签的小鼠bcma蛋白、带有his标签的食蟹猕猴bcma蛋白、带有his标签的人bcma蛋白和杜尔贝科氏磷酸盐缓冲盐水。图14显示,gsk和bluebird抗体结合人和食蟹猕猴bcma蛋白,但不结合小鼠bcma蛋白;2c5和2e1抗体结合人、食蟹猕猴和小鼠bcma蛋白;4c9和5c4抗体仅结合人bcma蛋白。
[0222]
实施例5:流式细胞术分析.
id no:6)或突变体
‑
2人bcma
‑
小鼠fc(突变del32
‑
35g;seq id no:7)。图20显示:抗体2c5、2e1和4c9结合野生型和突变体
‑
2bcma蛋白并且表现出与突变体
‑
1bcma蛋白的结合降低;bluebird c11d5抗体结合野生型和两种突变型的bcma蛋白;gsk j6m0抗体结合野生型和突变体
‑
1bcma蛋白并且表现出与突变体
‑
2bcma蛋白的结合降低。抗体6g8表现出与此分析中使用的所有形式的bcma蛋白的结合均显著降低。这一数据表明,抗体2c5、2e1和4c9结合的人bcma蛋白的表位与bluebird和gsk抗体结合的表位不同。
[0234]
实施例10:用于测量april阻断活性的生物层干涉测量法.
[0235]
生物层干涉测量法用于评估各种抗bcma抗体结合人bcma表位和阻断人april与人bcma表位结合的能力。将人april蛋白(r&d systems,目录号5860
‑
ap
‑
010/cf)加载到ar2g传感器上(2μg/ml),并与预先混合的人bcma蛋白(2μg/ml)与各种抗bcma抗体之一或同型对照(25μg/ml)反应1小时。图21中的结果显示,各种抗bcma抗体(2c5、2e1、4c9、5c4、bluebird c11d5和gsk j6m0)阻断bcma蛋白与april蛋白的结合。
[0236]
实施例11:测量交叉反应的生物层干涉测量法.
[0237]
生物层干涉测量法用于测量(1)两种不同的抗bcma抗体(bca7
‑
2c5或bb c11d5)或对照同型与(2)包括taci和baffr的各种人类抗原之间的交叉结合。
[0238]
抗体的固定化是通过标准edc催化的酰胺键形成来实现,以在蛋白质上的反应性胺与羧基封端的生物传感器表面之间形成共价键。简而言之,ar2g传感器(来自fortebio的octetred96e)被edc
‑
nhs激活6分钟,然后在10mm乙酸盐缓冲液ph 5.0中加载5μg/ml抗体(bca7
‑
2c5抗体、bluebird c11d5嵌合抗体或人igg同型抗体)6分钟,然后用1m乙醇胺ph 8.5淬灭6分钟。3分钟的基线步骤从生物传感器中去除任何未结合的抗体,然后缔合三种分析蛋白taci(人taci/tnfrsf13b(cd267)his标签,来自sino biological,1μg/ml的pbs溶液)、baffr(人baffr/tnfrsf13c(cd268)fc标签),来自sino biological,2μg/ml的pbs溶液)和人bcma蛋白(用小鼠fc内部制备,2μg/ml的pbs溶液)各1.5分钟。分析步骤概述于下表4中:
[0239]
表4:
[0240]
步骤编号步骤名称步骤时间(秒)步骤类型名称1基线1240基线2激活360激活3加载360加载4淬灭360淬灭5基线2180基线6缔合90缔合7缔合90缔合8缔合90缔合9解离180解离
[0241]
图22中的结果显示,抗bcma抗体(bca7
‑
2c5和bb c11d5)与bcma蛋白结合,但不与taci或baffr蛋白结合。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1