用于治疗肝脏病症的方法和组合物与流程
用于治疗肝脏病症的方法和组合物
1.交叉引用
2.本技术要求于2019年5月21日提交的美国临时专利申请号62/850,773的优先权,所述申请通过引用整体并入本文。
背景技术:
3.可以几乎没有争议地说,除了物理损伤外,对人的生命力、健康最重要的输入来自三个方面:(1)人体的结构构成,其通过人基因组模板化,并通过所述基因组的复制、表达和转录成构成人体组织的生物结构来构建;(2)对人体结构的输入,包括环境输入和摄取输入,例如食物;以及(3)人体结构处理那些输入的过程或界面,包括处理那些输入的组织的整体生理特性,以及涉及人体结构表面和内部的总体微生物群的共生过程,并且在那些输入的处理过程中充当中介和/或界面,以转移至或保护身体的生理结构。
4.大量研究已深入探究了人类健康的遗传和物理方面,并且得到了许多在诊断和治疗多种健康障碍以及提出健康生活习惯的建议方面提供显著健康益处的发现。同样,已经对环境和营养输入对于人类健康的影响进行了细致研究,从而更深入地了解我们的环境和饮食如何影响我们的健康。
5.虽然研究人员通过用于分析生命系统的技术的进步继续推进对人类健康和疾病的了解,但健康和疾病的许多方面仍然是一个谜,导致无法鉴定大量人类疾病的原因和/或治疗。这种无力性尤其体现在过去一个世纪中流行的大量复杂疾病上。
6.例如,对于复杂的退行性疾病,如阿尔茨海默病、帕金森病、肌萎缩侧索硬化(als)、自闭症和许多其他发生率上升的神经系统病症,研究人员试图但未能明确鉴定潜在的遗传或其他原因。因此,鉴定这些疾病的潜在治疗的尝试经常失败。类似地,尽管早期相信遗传或营养根本原因,但是一大类代谢障碍的原因和潜在治疗也同样难以找到其根本原因,并且因此难以进行其潜在治疗。这些包括诸如以下的病症:糖尿病(1型和2型)、血脂异常、胰岛素抵抗、炎症性肠病、肠易激综合征、肥胖症和相关肝病,诸如非酒精性脂肪肝(nafld),包括从非酒精性脂肪性肝炎(nash)进展到肝纤维化和肝硬化。
7.鉴于许多这些代谢障碍与潜在的遗传或环境原因之间没有明确关系,研究人员已经开始探索肠道微生物组在这些病症的病因学中的作用。虽然这项研究提供了关于这些病症的进展中的微生物组组分的诱人线索,但迄今为止,尚未鉴定出在这种疾病进展中存在或缺乏的微生物组功能的任何关键组分,以及另外,用于补救或减轻所述进展的任何潜在策略。本公开解决了这些和许多其他需要。
技术实现要素:
8.提供了用于治疗、减轻、管理、减少或预防肝脏病症的症状、体征或指标以及所述病症本身的发作的组合物和方法。所述组合物和方法包括微生物组合物,所述微生物组合物经选择以改善它们所施用的所述受试者的肠道功能,以便带来肝脏病症和/或那些病症的体征、症状和指标的治疗。
reuteri)、鼠李糖乳杆菌(lactobacillus rhamnosus)、吉氏颤螺菌(oscillospira guilliermondii)、盲肠罗斯氏菌(roseburia cecicola)、食葡糖罗斯氏菌(roseburia inulinivorans)、生黄瘤胃球菌(ruminococcus flavefaciens)、活泼瘤胃球菌(ruminococcus gnavus)、卵形瘤胃球菌(ruminococcus obeum)、乳脂链球菌(streptococcus cremoris)、屎链球菌(streptococcus faecium)、婴儿链球菌(streptococcus infantis)、变异链球菌(streptococcus mutans)、嗜热链球菌(streptococcus thermophilus)、粪厌氧棒形菌(anaerofustis stercorihominis)、产丁酸盐菌(anaerostipes hadrus)、人结肠厌氧棍状菌(anaerotruncus colihominis)、生孢梭菌(clostridium sporogenes)、破伤风梭菌(clostridium tetani)、粪球菌属(coprococcus)、规则粪球菌(coprococcus eutactus)、柱状真杆菌(eubacterium cylindroides)、细长真杆菌(eubacterium dolichum)、凸腹真杆菌(eubacterium ventriosum)、粪便罗斯氏菌(roseburia faeccis)、人罗斯氏菌(roseburia hominis)、肠道罗斯氏菌(roseburia intestinalis)以及其任何组合。在一些实施方案中,聚生体包含2种或更多种选自由以下组成的组的微生物种群:嗜粘蛋白阿克曼菌、青春双歧杆菌、婴儿双歧杆菌、长双歧杆菌、拜氏梭菌、丁酸梭菌、吲哚梭菌、霍氏真杆菌以及普拉梭菌。在一些实施方案中,施用使受试者的天冬氨酸转氨酶(ast)和丙氨酰转氨酶(alt)中的一种或多种的血清水平与施用分离并纯化的微生物物种的聚生体之前受试者的alt和/或ast水平相比降低至少10iu/l。在一些实施方案中,施用使受试者的天冬氨酸转氨酶(ast)和丙氨酰转氨酶(alt)中的一种或多种的血清水平与施用分离并纯化的微生物物种的聚生体之前受试者的alt和/或ast水平相比降低至少20iu/l。在一些实施方案中,施用使受试者的天冬氨酸转氨酶(ast)和丙氨酰转氨酶(alt)中的一种或多种的血清水平与施用分离并纯化的微生物物种的聚生体之前受试者的alt和/或ast水平相比降低至少50iu/l。在一些实施方案中,施用使受试者的天冬氨酸转氨酶(ast)和丙氨酰转氨酶(alt)中的一种或多种的血清水平与施用分离并纯化的微生物物种的聚生体之前受试者的alt和/或ast水平相比降低至少100iu/l。
11.在一些方面,本公开提供了一种降低受试者的一种或多种升高的肝损伤或肝病指标的方法,其包括向具有一种或多种升高的肝损伤指标的受试者施用有效量的包含一种或多种纯化的活微生物种群的组合物,其中一种或多种纯化的活微生物种群能够在受试者的肠道中产生丁酸盐,这样的有效量导致受试者的一种或多种肝病指标降低。
12.在一些实施方案中,一种或多种肝损伤指标选自由以下组成的组:ast、alt、ast:alt比率、纤维化评分(“nfs”)、fib-4指数、天冬氨酸转氨酶(“ast”)、血小板比率指数(“apri”)、增强肝纤维化(“elf”)分组(enhanced liver fibrosis(“elf”)panel)、瞬时弹性成像(“te”)、磁共振(“mr”)弹性成像、声辐射力脉冲成像以及超声剪切波弹性成像。
13.在一些方面,本公开提供了一种降低患有肝脏病症或有患肝脏病症风险的受试者的alt和ast血清水平中的一种或多种的方法,其包括向受试者施用有效量的分离并纯化的微生物物种的聚生体,以降低受试者的一种或多种alt和ast血清水平。
14.在一些实施方案中,受试者患有2型糖尿病。在一些实施方案中,受试者已被诊断为患有肝脏病症。在一些实施方案中,肝脏病症是nafld、nash、肝纤维化、肝硬化或dili。在一些实施方案中,受试者被同时施用具有已知肝毒性的药物。
15.在一些方面,本公开提供了一种降低一种或多种已知具有肝毒性的药物化合物的肝毒性的方法,其包括:与一种或多种药物化合物共同施用有效量的包含有效量的分离并纯化的微生物物种的聚生体的组合物以降低一种或多种肝损伤指标。
16.在一些方面,本公开提供了一种治疗有需要的受试者的肝脏病症的方法,其包括:向受试者施用有效量的分离并纯化的微生物物种的聚生体以减轻肝脏病症。
附图说明
17.图1示出人消化途径的实例,并且肠道微生物组在其中介导丁酸盐的产生。
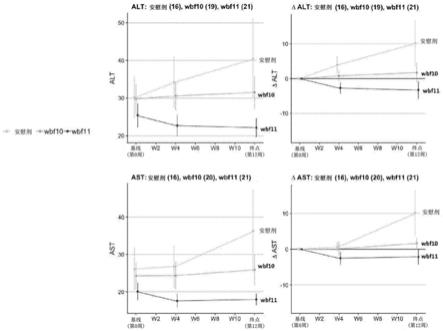
18.图2示出在用如本文所述的微生物种群治疗后受试者的肝病的肝酶生物标志物的临床减少。
具体实施方式
19.i.综述
20.微生物组干预先前已被描述用于治疗代谢障碍,如2型糖尿病、肥胖症和相关疾病。具体地,已显示包含共生微生物种群的组合物的口服施用显著降低2型糖尿病患者的餐后葡萄糖水平和hba1c水平(参见于2019年2月6日提交的共同未决的美国专利申请号62/801,983和于2019年9月24日提交的共同未决的pct申请号pct/us19/52694,所述申请中的每一个出于所有目的通过引用整体并入本文)。然而,如本文所述,作为微生物组干预施用微生物组合物还可提供用于治疗或减轻另外病症的方法,所述病症诸如与药物或其他毒性相关的肝脏病症,和/或与代谢障碍相关的那些,诸如nafld和nash,以及其他肝脏病症。
21.在一些情况下,本文所述的组合物的施用可导致肝脏相关病症诸如nash、nafld以及此类病症的进展诸如肝纤维化和肝硬化的治疗或减轻。在某些情况下,这些病症或此类病症的增加的风险发生在这样的患者或受试者中:其中它们与此类患者的其他代谢障碍相关或同时发生,诸如1型糖尿病、2型糖尿病、胰岛素抵抗、肥胖症等,并且因此,治疗方法可应用于这些患者组,以治疗与这些病状相关的肝脏病症或延迟其发作(视情况而定)。在其他情况下,本文所述的组合物的施用可导致其他肝脏病症的治疗或减轻,诸如与药物毒性、过量饮酒等相关的肝损伤。为了便于讨论,上述肝脏病症和/或损伤在本文统称为肝脏病症。
22.ii.组合物
23.本文所述的组合物包括可用于治疗或以其他方式减轻肝脏病症的症状的微生物组合物。具体地,在一些情况下,提供了减轻症状、治疗或管理肝脏病症的方法,其通过向患有此类病症的受试者施用有效量的微生物组合物(如本文进一步描述的)以实现这种减轻、治疗或管理来实现。
24.这些微生物组合物可包括天然存在的微生物菌株,其在患有此类肝脏病症的受试者中可能富集不足(underrepresented)或未充分富集。在一些情况下,相对于其在健康受试者的肠道中的富集水平,微生物菌株在患有肝脏病症或损伤的受试者的肠道中可能富集不足,并且因此微生物组合物的施用可旨在恢复此类微生物在肠道中的健康水平,以便减轻肝脏病症的症状、治疗或管理所述肝脏病症。在其他情况下,可能期望使患有这种病症或损伤的受试者的肠道中微生物物种的富集增加超过在健康受试者的肠道中通常发现的水
平,并且因此微生物组合物的施用可旨在实现这种过度富集(over-representation),以便减轻症状或以其他方式治疗或管理此类肝脏病症。
25.微生物组合物可包括多种不同的微生物种群中的任一种。如本文所用,微生物种群通常是指基本上由单一菌株、物种或属组成的微生物种群,当从此类菌株、物种或属的分离并纯化的亚群培养所述种群时可能出现这种情况。因此,相对于给定的微生物种群,如果从分离的微生物物种或菌株培养,则所述种群在本文中将称为纯化的或基本上纯的。所得种群关于所述微生物物种或菌株通常可具有至少80%的纯度,相对于所述特定种群内的其他微生物物种或菌株可具有至少90%的纯度、至少95%的纯度、至少98%的纯度、至少99%的纯度、至少99.5%的纯度或至少99.9%的纯度。相反,任何特定的期望微生物种群中非期望菌株的水平将少于20%、少于10%、少于5%、少于2%、少于1%、少于0.5%或少于0.1%。在包含多种微生物种群的聚生体的组合物的情况下,各种群在掺入组合物之前,或在关于聚生体总体测量时,都可具有上述纯度。例如,纯化种群的聚生体中的杂质(例如,其他非期望的微生物菌株或物种)水平可按比例处于或低于上文针对各期望种群所陈述的水平。
26.不受任何特定操作理论的束缚,据信本文所述的微生物组合物在人肠道中的膳食碳水化合物的代谢和能量生成中起重要作用。因此,已显示出肠道中这些生物体的种群的增强改善代谢障碍诸如2型糖尿病的症状。令人惊讶的是,如本文其他地方所述,此类增强还已展示出改善在一些情况下可与这些代谢障碍(诸如肝脏病症或损伤)相关的其他病症的症状和指征的能力。具体地,参与短链脂肪酸的产生和吸收的微生物被认为在代谢过程中特别有用,可以帮助治疗或以其他方式减轻肝病或肝损伤的症状。这些微生物的实例包括,例如,嗜粘蛋白阿克曼菌、粪厌氧棒杆菌、青春双歧杆菌、两歧双歧杆菌、婴儿双歧杆菌、长双歧杆菌、溶纤维丁酸弧菌、丙酮丁醇梭菌、嗜氨基梭菌、拜氏梭菌、丁酸梭菌、大肠梭状芽胞杆菌、吲哚梭菌、解黄酮梭菌、屎肠球菌、霍氏真杆菌、直肠真杆菌、普拉梭菌、产琥珀酸丝状杆菌、嗜酸乳杆菌、短乳杆菌、保加利亚乳杆菌、干酪乳杆菌、高加索乳杆菌、发酵乳杆菌、瑞士乳杆菌、乳酸乳杆菌、植物乳杆菌、罗伊氏乳杆菌、鼠李糖乳杆菌、吉氏颤螺菌、盲肠罗斯氏菌、食葡糖罗斯氏菌、生黄瘤胃球菌、活泼瘤胃球菌、卵形瘤胃球菌、乳脂链球菌、屎链球菌、婴儿链球菌、变异链球菌、嗜热链球菌、粪厌氧棒形菌、产丁酸盐菌、人结肠厌氧棍状菌、生孢梭菌、破伤风梭菌、粪球菌属、规则粪球菌、柱状真杆菌、细长真杆菌、凸腹真杆菌、粪便罗斯氏菌、人罗斯氏菌、肠道罗斯氏菌以及其任何组合。
27.在一些情况下,可选择微生物种群以在肠道内提供增强的代谢功能,这可尤其有助于减轻或治疗肝脏病症或损伤的症状。举例来说,丁酸盐是可以影响肠道通透性的抗炎因子。某些丁酸盐产生菌(例如梭菌簇xiva和iv)的较低水平以及乳酸盐产生菌(例如青春双歧杆菌)的水平降低已与某些代谢障碍关联,诸如ii型糖尿病(t2d)、肥胖症和其他类似的代谢障碍。已经显示患有代谢障碍的受试者与肝脏病症的发生之间存在强关联(参见,例如chalassani等人,hepatology第67卷,第1期(2018)328-357)。
28.图1描绘了可影响代谢相关健康状况的消化途径。同样,不受任何具体操作理论的束缚,据信使用本发明的微生物组合物改变该途径可以纠正受试者的所述途径的缺陷,这继而可导致肝脏病症或损伤的减轻或治疗。如图所示,在结肠中,膳食纤维可以被产丁酸盐的微生物加工产生丁酸盐(即丁酸酯),其为短链脂肪酸(scfa)。继而,丁酸盐可以启动g蛋白偶联受体(gpcr)信号传导,从而导致胰高血糖素样肽1(glp-1)分泌,这可导致胰岛素分
泌增加、胰岛素敏感性增加和/或食欲下降。通过改变受试者中的产丁酸盐的微生物组,例如患有t2dm或胰岛素不敏感的受试者,可以刺激该途径。在一些患者中,胰岛素分泌可以得到改善,并且在一些情况下,可利用微生物组合物增加和/或恢复至糖尿病前期水平。
29.如本文所述,旨在确定包括这些微生物亚群的微生物组合物对t2d患者的影响的临床试验(参见美国临时专利申请号62/801,983,其先前出于所有目的通过引用整体并入本文)也证明了与肝脏病症和肝损伤相关的生物标志物的显著改善(参见以下实施例1和图2)。
30.因此,并且不受任何具体操作理论的束缚,在本发明的一些方面,可通过鉴定在导致glp-1产生的功能途径中起作用的细菌超集(superset)的方式来选择目标菌株(例如,具有丁酸激酶、丁酸辅酶a(coa)和/或丁酸coa转移酶基因的细菌)。丁酸激酶是可属于转移酶家族的酶,例如转移含磷基团的那些(例如,磷酸转移酶),其中羧基作为受体。该酶类的系统名称可以是atp:丁酸酯1-磷酸转移酶(atp:butanoate 1-phosphotransferase)。丁酸激酶可以参与丁酸盐代谢。丁酸激酶可以催化以下反应:adp+丁酰磷酸atp+丁酸盐,丁酸辅酶a,也称为丁酰辅酶a,可以是丁酸的辅酶a活化形式。它可以被丁酰coa脱氢酶作用,并且可以是丙酮-丁醇-乙醇发酵的中间化合物。丁酸辅酶a可以参与丁酸盐代谢。
31.丁酸辅酶a转移酶,也称为丁酸-乙酰乙酸coa转移酶,可以属于转移酶家族,例如coa转移酶。该酶类的系统名称可以是丁酰基coa:乙酰乙酸coa转移酶。其他常用名称可以包括丁酰辅酶a-乙酰乙酸辅酶a转移酶和丁酰coa-乙酰乙酸coa转移酶。丁酸辅酶a转移酶可以催化以下化学反应:丁酰基coa+乙酰乙酸丁酸酯+乙酰乙酰coa。
32.丁酰coa脱氢酶可以属于氧化还原酶家族,例如,与其他受体一起作用于供体的ch
‑‑
ch基团的那些。该酶类的系统名称可以是丁酰基coa:受体2,3-氧化还原酶。其他常用名称可以包括丁酰脱氢酶、不饱和酰基coa还原酶、乙烯还原酶、烯酰辅酶a还原酶、不饱和酰基辅酶a还原酶、丁酰辅酶a脱氢酶、短链酰基coa脱氢酶、短链酰基辅酶a脱氢酶、3-羟酰coa还原酶以及丁酰基coa:(受体)2,3-氧化还原酶。丁酰coa脱氢酶可以参与的代谢途径的非限制性实例包括:脂肪酸代谢;缬氨酸、亮氨酸和异亮氨酸降解;以及丁酸酯代谢。丁酰coa脱氢酶可以采用一种辅因子fad。丁酰coa脱氢酶可以催化以下反应:丁酰coa+受体2-丁烯酰coa+还原受体。
33.β-羟基丁酰coa脱氢酶或3-羟基丁酰coa脱氢酶可以属于氧化还原酶家族,例如与作为受体的nad+或nadp+一起作用于供体的ch
‑‑
oh基团的那些。该酶类的系统名称可以是(s)-3-羟基丁酰基coa:nadp+氧化还原酶。其他常用名称可以包括β-羟基丁酰辅酶a脱氢酶、l(+)-3-羟基丁酰coa脱氢酶、bhbd、脱氢酶、l-3-羟基丁酰辅酶a(烟酰胺腺嘌呤、磷酸二核苷酸)、l-(+)-3-羟基丁酰coa脱氢酶以及3-羟基丁酰coa脱氢酶。β-羟基丁酰coa脱氢酶可以通过coa连接参与苯甲酸酯降解。β-羟基丁酰coa脱氢酶可以参与丁酸酯代谢。β-羟基丁酰coa脱氢酶可以催化以下反应:(s)-3-羟基丁酰基coa+nadp.
+
3-乙酰乙酰coa+nadph+h
+
。
34.巴豆酸酶可以包括具有例如脱卤酶、水合酶、异构酶活性的酶。巴豆酸酶可以与硫酯的碳-碳键形成、裂解和水解有关。巴豆酸酶超家族中的酶可以包括,例如,烯酰coa水合酶,其可以催化2-反式-烯酰coa水合为3-羟酰coa;3-2反式-烯酰coa异构酶或十二碳烯酰coa异构酶(例如,ec 5.3.3.8),其可以将不饱和脂肪酸氧化的中间体的3-双键转变为2-反
式位置;3-羟基丁酰coa脱水酶(例如,巴豆酸酶;ec 4.2.1.55),其可以参与丁酸盐/丁醇产生途径;4-氯苯甲酰coa脱卤酶(例如,ec 3.8.1.6),其可以催化4-氯苯甲酸coa转化为4-羟基苯甲酸coa;二烯酰coa异构酶,其可以催化3-反式,5-顺式-二烯酰coa异构化为2-反式,4-反式-二烯酰coa;萘甲酸合酶(例如,menb或dhna合成酶;ec 4.1.3.36),其可以参与甲基萘醌(例如,维生素k2)的生物合成;肉毒碱消旋酶(例如,基因caid),其可以在大肠杆菌中催化巴豆甜菜碱向左旋肉毒碱的可逆转化;甲基丙二酰coa脱羧酶(例如,mmcd;ec 4.1.1.41);羧甲基脯氨酸合酶(例如,carb),其可以参与碳青霉烯生物合成;6-氧代樟脑水解酶,其可以催化二环β-二酮去对称化为旋光酮酸;脂肪酸氧化复合物的α亚基,一种多酶复合物,其可以催化脂肪酸β-氧化循环中的最后三个反应;以及auh蛋白,其可以是烯酰coa水合酶的双功能rna结合同系物。
35.硫解酶,也称为乙酰辅酶a乙酰转移酶(acat),可以将两个单位的乙酰coa转化为乙酰乙酰coa,例如,在甲羟戊酸途径中。硫解酶可以包括,例如,分解硫解酶(例如,ec 2.3.1.16)和生物合成硫解酶(例如,ec 2.3.1.9)。3-酮酰coa硫解酶,也称为硫解酶i,可以参与诸如脂肪酸β-氧化等降解途径。乙酰乙酰coa硫解酶,也称为硫解酶ii,对于乙酰乙酰coa的硫解可以具有特异性,并且可以参与诸如聚β-羟基丁酸合成或类固醇生物合成的生物合成途径。
36.如图1所示,丁酸盐的产生可以涉及两个主要阶段或微生物,例如初级发酵菌和二级发酵菌。当给定能量源(例如纤维)时,初级发酵菌可以产生中间体分子(例如乳酸盐、乙酸盐)。二级发酵菌可以将初级发酵菌产生的中间体分子转化为丁酸盐。许多这些初级和二级发酵菌将表达参与该丁酸盐途径的酶,诸如以下非限制性酶实例:丁酰coa脱氢酶、β-羟基丁酰coa脱氢酶或3-羟基丁酰coa脱氢酶、巴豆酸酶、电子转移蛋白a、电子转移蛋白b以及硫解酶。
37.初级发酵菌的非限制性实例可包括诸如嗜粘蛋白阿克曼菌、青春双歧杆菌、婴儿双歧杆菌和长双歧杆菌的微生物。二级发酵菌的非限制性实例可包括诸如拜氏梭菌、丁酸梭菌、吲哚梭菌、霍氏真杆菌和普拉梭菌的微生物。
38.关于这些示例性微生物物种,嗜粘蛋白阿克曼菌是可以在粘蛋白降解中发挥作用的革兰氏阴性的严格厌氧菌。嗜粘蛋白阿克曼菌的水平在患有代谢障碍(例如,肥胖症和t2dm)的受试者中可降低。嗜粘蛋白阿克曼菌可预防代谢障碍,例如,通过增加控制炎症、肠道屏障和肠肽分泌的内源性大麻素的水平。嗜粘蛋白阿克曼菌可以用作初级发酵菌,并且在一些情况下,可以与本文所述的二级发酵菌中的任何一种或多种组合。青春双歧杆菌可以是从婴儿期就可以在健康的人肠道中发现的革兰氏阳性厌氧菌。青春双歧杆菌可以合成b维生素。青春双歧杆菌可以用作初级发酵菌,并且在一些情况下,可以与本文所述的二级发酵菌中的任何一种或多种组合。婴儿双歧杆菌可以是革兰氏阳性的、过氧化氢酶阴性的微耐氧厌氧菌。婴儿双歧杆菌可以用作初级发酵菌,并且在一些情况下,可以与本文所述的二级发酵菌中的任何一种或多种组合。长双歧杆菌可以是革兰氏阳性的、过氧化氢酶阴性的微耐氧厌氧菌。长双歧杆菌可以用作初级发酵菌,并且在一些情况下,可以与本文所述的二级发酵菌中的任何一种或多种组合。拜氏梭菌可以是革兰氏阳性的严格厌氧菌,其属于梭菌簇i。拜氏梭菌可以用作二级发酵菌,并且在一些情况下,可以与本文所述的初级发酵菌中的任何一种或多种组合。丁酸梭菌可以是革兰氏阳性的严格厌氧菌,其可以用作二级
发酵菌,并且在一些情况下,可以与本文所述的初级发酵菌中的任何一种或多种组合。吲哚梭菌可以是革兰氏阳性的严格厌氧菌,其属于梭菌簇xiva。吲哚梭菌可以用作二级发酵菌,并且在一些情况下,可以与本文所述的初级发酵菌中的任何一种或多种组合。霍氏真杆菌可以是革兰氏阳性厌氧菌,其属于排列a(arrangement a)梭菌簇xiva。霍氏真杆菌可以用作二级发酵菌,并且在一些情况下,可以与本文所述的初级发酵菌中的任何一种或多种组合。普拉梭菌可以是属于梭菌簇iv的革兰氏阳性厌氧菌。普拉梭菌可以是最常见的肠道细菌之一并且也是最大的丁酸产生菌。普拉梭菌可以用作二级发酵菌,并且在一些情况下,可以与本文所述的初级发酵菌中的任何一种或多种组合。
39.在一些实施方案中,微生物组合物包含嗜粘蛋白阿克曼菌、青春双歧杆菌、婴儿双歧杆菌、长双歧杆菌、拜氏梭菌、丁酸梭菌、吲哚梭菌、霍氏真杆菌或其组合。
40.在一些实施方案中,微生物组合物包含嗜粘蛋白阿克曼菌和霍氏真杆菌。在一些实施方案中,微生物组合物包含婴儿双歧杆菌、拜氏梭菌和丁酸梭菌。在一些实施方案中,微生物组合物包含嗜粘蛋白阿克曼菌、婴儿双歧杆菌、拜氏梭菌、丁酸梭菌和霍氏真杆菌。
41.在一些实施方案中,微生物组合物包含嗜粘蛋白阿克曼菌、霍氏真杆菌,以及一种或多种婴儿双歧杆菌、拜氏梭菌或丁酸梭菌。
42.在一些实施方案中,微生物种群包含与嗜粘蛋白阿克曼菌、青春双歧杆菌、婴儿双歧杆菌、长双歧杆菌、拜氏梭菌、丁酸梭菌、吲哚梭菌或霍氏真杆菌的rrna序列包含至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的rrna序列。
43.在一些实施方案中,组合物基本上不含动物产品。在一些实施方案中,组合物基本上不含乳源性组分。在一些实施方案中,组合物完全不含动物来源的任何产品或任何乳源性组分。
44.在一些实施方案中,微生物组合物包含至少一种冻干的物种。在一些实施方案中,微生物组合物包含至少一种没有活力的物种。
45.初级和二级发酵菌的组合可以用于在受试者中产生丁酸盐,不受任何具体操作理论或作用机制的束缚,据信其减轻代谢障碍,并且因此可治疗或以其他方式减轻肝脏病症的症状。包含至少一种初级发酵菌和至少一种二级发酵菌的制剂的子集可以用于治疗和/或减轻包括肝脏病症或肝损伤在内的代谢健康病状的进展。制剂可以另外包含益生元。
46.因此,在一些情况下,本文所述的组合物可包括一种或多种分离并纯化的微生物种群。在一些情况下,组合物可包括两种或更多种分离并纯化的微生物种群。在其他情况下,三种或更多种分离并纯化的微生物种群可存在于本文所述的组合物中。在其他情况下,4种或更多种分离并纯化的微生物种群、5种或更多种分离并纯化的微生物种群,或6种或更多种分离并纯化的微生物种群可包括在组合物中。
47.在一些情况下,在存在的微生物种群中,组合物可包含至少一种初级发酵菌和至少一种二级发酵菌。在一些情况下,组合物可包括至少一种初级发酵菌,其选自下组:嗜粘蛋白阿克曼菌、青春双歧杆菌、婴儿双歧杆菌和长双歧杆菌。类似地,在一些情况下,组合物可包含至少一种二级发酵菌,其选自下组:拜氏梭菌、丁酸梭菌、吲哚梭菌、霍氏真杆菌和普拉梭菌。在一些实施方案中,治疗组合物包含至少一种初级发酵菌、至少一种二级发酵菌和至少一种益生元。
48.在一些情况下,组合物可包含降解或调节粘蛋白的微生物。降解或调节粘蛋白的
微生物的实例包括,例如,嗜粘蛋白阿克曼菌、脆弱拟杆菌(bacterioides fragilis)、多形拟杆菌(bacterioides thetaiotaomicron)、普通拟杆菌(bacterioides vulgatus)、双歧杆菌属物种,诸如两歧双歧杆菌等。
49.在一些情况下,组合物可包含微生物的聚生体,所述微生物的聚生体在组合物内包括至少2种不同的微生物种群。在其他情况下,组合物可包含至少3种不同的微生物种群、至少4种不同的微生物种群、至少5种不同的微生物种群、至少6种不同的微生物种群,并且在一些情况下超过6种不同的微生物种群。
50.iii.治疗方法
51.本文提供治疗多种肝脏病症中的一种或多种的方法。如本文所用,本文所述的方法可用于治疗患有一种或多种肝脏病症或肝损伤的受试者,以便减少、补救、减轻或减慢患有这些病症的那些受试者中此类损伤或病症的进展和/或此类病症的症状、体征和/或指标。另外或可替代地,本文所述的方法可用于治疗可处于发展这些损伤或病症和/或其症状的较高风险下的受试者,以便预防或延迟此类损伤或病症和/或其体征或症状的发作。为便于讨论,这些干预措施(治疗、减轻、缓解、预防、管理、补救等)统称为“治疗(treat、treating和/或treatment)”。
52.如本文所述,上述方法可包括使用本文所述的组合物治疗一种或多种不同的肝脏病症和/或其体征、症状和/或指标,和/或预防或延迟。具体地,在一些情况下,本文描述的方法可用于治疗患有诸如非酒精性脂肪性肝炎(nash)、非酒精性脂肪肝(nafld)、肝纤维化、肝硬化、药物性肝损伤(dili)、酒精性肝病,例如酒精性肝炎等肝脏相关病症(或症状)和损伤或有此风险的受试者,以便减少和/或延迟这些病症的体征和/或症状的发作。
53.这些肝脏病症的治疗通常包括向需要这种治疗的受试者施用有效量的包含本文所述的微生物组合物的组合物,所述受试者包括患有此类病症的受试者和可需要预防或减轻此类病症的发作的受试者。具体地,本文所述的治疗方法可旨在是治疗性的,例如用于治疗、减轻或管理已经在患者或受试者体内表现和/或诊断的肝脏病症。
54.在其他情况下,所述方法可以是预防性的,例如用于治疗可能处于增加的肝脏病症风险但可能尚未表现出该病症的体征或症状的受试者,例如可能尚未显露出肝病的明显体征但否则此类疾病的风险升高的受试者。此类受试者的实例包括,例如,患有其他代谢障碍诸如糖尿病(1型和/或2型)、肥胖症、胰岛素抵抗等的受试者。同样,肝损伤或肝脏病症的风险增加的受试者可包括正在使用具有已知或预期的肝毒性问题的药物进行治疗的受试者,或以其他方式暴露于具有已知的肝毒性问题的环境和/或物质的受试者,例如酒精中毒受试者等。
55.在一些情况下,预防性治疗可包括与具有提高的肝毒性风险的其他治疗剂共同施用。例如,在一些情况下,本文所述的微生物组合物可与已知或怀疑具有肝毒性问题的其他药物联合预防性施用,以便预防肝损伤或减少肝毒性(诸如由共同施用的药物引起的肝毒性)的发作和/或症状。例如,许多经批准的药物,包括非处方药物,如对乙酰氨基酚,在按照批准剂量服用时或在以高于推荐的剂量施用时,可具有导致肝损伤的可能性。通过将这些药物与本文所述的组合物共同施用,可减轻毒性对肝脏的影响,从而允许继续施用特定药物,或甚至提高此类药物的剂量。
56.此外,在许多情况下,潜在的候选药物可能不被批准,或可能在临床测试期间被放
弃,这是由于感知的、潜在的或实际的肝毒性问题超过或可能超过此类潜在药物的潜在治疗效果。通过将本文所述的组合物与此类预期药物共同施用,可减轻肝毒性问题并可能利用此类药物可以其他方式提供的益处。
57.有效量的本文所述的组合物通常可包含产生期望治疗效果的量的此类组合物,所述期望治疗效果例如,疾病症状的减少、与疾病关联的生物标志物的水平的变化、处于此类疾病的增高风险下的受试者的疾病体征或症状的延迟发作、对肝毒性药物或物质的耐受性更高等。如将认识到的,有效量将根据所治疗的病症的性质、效果的期望程度,以及患者的特征,例如身高、体重等而变化。
58.肝脏病症的治疗可集中于所讨论的病症的一种或多种症状的减少或改善。在一些情况下,这些症状可以是病症的物理表现,例如黄疸、纤维化进展、高甘油三酯血症和腹水。在此类情况下,治疗可包括以相对于类似情况的未治疗受试者而言有效减少此类物理表现的症状,例如减少黄疸,或减慢此类症状的进展,例如减慢纤维化进展的量施用本文所述的组合物。
59.在一些情况下,治疗可导致与肝病的进展相关或关联的一种或多种指标的有利变化,包括与病状相关的生物标志物或指标的变化。多个诊断指标已被用于鉴定和表征肝脏病症的发作和进展(参见,例如,chalassani等人,hepatology第67卷,第1期(2018)328-357)。例如,用于评估肝脏病症的常用非侵入性工具包括nafld纤维化评分(“nfs”)、fib-4指数、天冬氨酸转氨酶(“ast”)血小板比率指数(“apri”)以及其他血清生物标志物,诸如增强肝纤维化(“elf”)分组,以及成像技术,包括瞬时弹性成像(“te”)和磁共振(“mr”)弹性成像,以及超声方法,诸如声辐射力脉冲成像和超声剪切波弹性成像。
60.许多这些诊断工具依赖于一系列受试者特征,包括,例如,身体质量指数、高血糖和多种生物标志物,诸如血小板计数、天冬氨酸氨基转移酶(“ast”)以及丙氨酸氨基转移酶(“alt”)水平或比率。例如,肝脏中脂肪沉积的增加已被证明诱发炎症反应,包括增大水平的转氨酶ast和alt的分泌。因此,ast和alt是与肝毒性(药物性肝损伤-dili)相关的肝损伤、nafld(非酒精性脂肪肝;从nafl到nash、纤维化和肝硬化)、酒精性肝炎以及其他类似或有关的肝脏病症的常用生物标志物,其单独、与如上文所述的总体评分和诊断工具一起或作为其一部分使用。肝病已被鉴定为血清中转氨酶活性增加的主要原因。已显示在疾病过程影响肝细胞完整性时,天冬氨酸转氨酶(ast)和丙氨酸转氨酶(alt)的血清活性升高。在这两者之间,alt是肝损伤的更专一的酶,因为ast也可来源于骨骼肌和心肌组织。alt活性的改变比ast活性持续的时间更长。这两种酶的活性在肝病中可达到高达参考上限的100倍(参见,例如,kim wr、flamm sl、di bisceglie am等人serum activity of alanine aminotransferase(alt)as an indicator of health and disease.hepatology.2008;47:1363-1370)。大于1的ast/alt比率已被用作肝硬化的预测,并且已分别显示出81.3%和55.3%的敏感性和特异性。在慢性肝炎的一些病因学中,该比率可小于或等于1,而大于2的比率可表明酒精性肝炎(参见,例如,giannini e、risso d、botta f等人validity and clinical utility of the aspartate aminotransferase-alanine aminotransferase ratio in assessing disease severity and prognosis in patients with hepatitis c related chronic liver disease.arch.intern.med.2003;163:218
–
224)。
61.在一些情况下,本文所述的治疗方法可导致肝损伤的上述指标、体征或症状中的
一种或多种的减少或其他改善,包括,例如,综合诊断评分,例如,fib-4和/或nfs、apri、elf分组等,以及成像和/或声学评估工具,诸如te、mr和超声波方法。此类减少可包括这些诊断工具的一个或多个输入参数的减少和/或由其引起,诸如肝酶(alt和/或ast)或基质转换蛋白(透明质酸、金属蛋白酶1和n末端原胶原iii肽的组织抑制剂、bmi、高血糖指标、血小板计数,或一种或多种成像或弹性成像测量。
62.例如,alt、ast和ast:alt比率已全部在诊断筛选中用作肝病或肝损伤的指标。具体地,ast的正常参考值通常在8至40iu/l的范围内(在男性中为~10-40,在女性中为~9-32),而成人alt的正常参考范围为7至55iu/l。相比之下,在一些情况下,在患有肝病或肝损伤的患者中,这些水平可显著增加,例如为正常水平的2倍、5倍、10倍,或甚至20倍或更多。在临床诊断环境中,对于男性患者,高于30的alt水平,或高于18的女性水平通常被视为指示nash/nafld的风险增加。
63.在一些情况下,根据本文所述的方法治疗的受试者可具有至少15iu/l、至少20iu/l、至少25iu/l、至少30iu/l、至少35iu/l、至少40iu/l、至少45iu/l、至少50iu/l、至少55iu/l、至少60iu/l、至少65iu/l、至少70iu/l、至少75iu/l、至少80iu/l、至少85iu/l、至少90iu/l、至少95iu/l、至少100iu/l、至少110iu/l、至少120iu/l、至少130iu/l、至少140iu/l、至少150iu/l、至少160iu/l、至少170iu/l、至少180iu/l、至少190iu/l、至少200iu/l或更多的起始ast水平(治疗前)。
64.在一些情况下,根据本文所述的方法治疗的受试者可具有至少10iu/l、至少15iu/l、至少20iu/l、至少25iu/l、至少30iu/l、至少35iu/l、至少40iu/l、至少45iu/l、至少50iu/l、至少55iu/l、至少60iu/l、至少65iu/l、至少70iu/l、至少75iu/l、至少80iu/l、至少85iu/l、至少90iu/l、至少95iu/l、至少100iu/l、至少110iu/l、至少120iu/l、至少130iu/l、至少140iu/l、至少150iu/l、至少160iu/l、至少170iu/l、至少180iu/l、至少190iu/l、至少200iu/l或更多的起始alt水平(治疗前)。
65.在一些情况下,如上文所述,施用有效量的本文所述的组合物将减少肝脏病症的症状,或延迟其发作,和/或将导致与肝病或其进展相关或关联的生物标志物的水平的有利变化。在一些情况下,上述治疗以有效量施用以降低患有肝病或肝损伤的受试者或有患此类疾病或损伤风险的那些受试者的ast和/或alt水平,例如在表现出升高的ast和/或alt水平的那些受试者中。具体地,在一些情况下,使用上述组合物进行治疗可使受试者的ast和/或alt水平中的一者或两者降低至少5iu/l,在一些情况下,至少10iu/l,在一些情况下,至少20iu/l,在一些情况下至少40iu/l,在一些情况下至少50iu/l,在一些情况下至少60iu/l,在一些情况下至少70iu/l,在一些情况下至少80iu/l,在一些情况下至少90iu/l,并且在一些情况下,至少100iu/l、200iu/l、300iu/l、400iu/l、500iu/l或更多。在一些情况下,待治疗的受试者将具有超过1、超过1.1、超过1.2、超过1.3、超过1.4、超过1.5、超过2、超过5、超过10、超过20、超过30、超过40、超过50、超过60、超过70、超过80、超过90、超过100或更多的起始ast/alt比率。在一些情况下,在如本文其他地方阐述的治疗之后,这些比率可降低至接近1的比率,或比起始比率更接近1的比率,包括降低至少10%、至少20%、至少30%、至少40%、至少50%,并且在足够高的起始比率的情况下,至少60%、至少70%、至少80%、至少90%或更多。
66.微生物组合物的有效量可根据病症的严重程度、受试者的身高和体重,以及受试
者的肠道微生物组的相对状况而变化,例如,无论目标是过度富集肠道中的微生物种群,还是在种群不足的肠道中补充微生物种群。无论如何,相对于任何个别微生物种群而言,针对本文所述的治疗施用的微生物组合物的有效量可关于施用给受试者的活微生物以“菌落形成单位”或“cfu”描述。
67.在一些情况下,有效量可包括以每次施用介于约1x107与1x10
15
cfu之间的活微生物种群的总量向受试者施用一种或多种活微生物种群。在一些情况下,施用将为每次施用至少1x107cfu的微生物、每次施用至少1x108cfu、每次施用至少1x109cfu、每次施用至少1x10
10
cfu、每次施用至少1x10
11
cfu、每次施用至少1x10
12
cfu、每次施用至少1x10
13
cfu、每次施用至少1x10
14
cfu或更多。
68.当组合物中存在多种微生物种群时,各种群将构成以上总微生物负载的任何部分。具体地,各微生物种群可以组合物中存在的微生物种群的1%或更少至99%或更多或其间的任何整数存在。所述分数可以基于各微生物种群的cfu数量计算。在一些情况下,任何一种微生物种群可以每次施用约1x107和1x10
15
cfu、每次施用至少1x107cfu的微生物、每次施用至少1x108cfu、每次施用至少1x109cfu、每次施用至少1x10
10
cfu、每次施用至少1x10
11
cfu、每次施用至少1x10
12
cfu、每次施用至少1x10
13
cfu、每次施用至少1x10
14
cfu或更多的水平存在于组合物或剂量中。
69.在一些情况下,可以每周一次、每周两次、每周三次、每隔一天、每周4次、每周五次、每周六次、每天、每天两次、每天三次、每天四次或更多地向受试者给予以上量的活微生物。
70.这些施用可持续一天、两天、一周、两周、四周、六周、八周、十二周、十八周、二十六周、7个月、8个月、9个月、10个月、11个月、一年、一年与两年之间、两年、两年与三年之间、三年、三年与四年之间或更长的过程。
71.在一些情况下,有效量可以单次剂量或多次剂量施用,和/或以单次施用,或随时间推移给予的多次施用进行施用。单独的剂量可包括在单独的可施用形式中,例如单丸剂、片剂、咀嚼剂、袋剂(sachet)、棒剂、栓剂等,或其可包括在2、3、4、5、6、7、8、9、10种或更多种单独的可施用形式中。
72.关于包含在给定剂量中的一种或多种微生物种群中的任一种,微生物组合物的单独剂量可包括每剂量约1x107与1x10
15
cfu之间。在一些情况下,施用将是每剂量至少1x107cfu的微生物、每剂量至少1x108cfu、每剂量至少1x109cfu、每剂量至少1x10
10
cfu、每剂量至少1x10
11
cfu、每剂量至少1x10
12
cfu、每剂量至少1x10
13
cfu、每剂量至少1x10
14
cfu或更多。举例来说,对于包含多种不同微生物菌株,即2种或更多种不同微生物种群的组合物,各种群可以每剂量上述活微生物负载的适当分数存在于单剂量中。
73.在一些情况下,在组合物、剂量或施用中,不同的微生物种群可比其他微生物种群在更大程度上富集。例如,在一些情况下,可希望在组合物中提供较大比例的初级和二级发酵菌生物体以及相对较小比例的粘蛋白降解微生物。在其他情况下,可能期望相反的情况。因此,在给定组合物中存在微生物种群的聚生体的情况下,所述种群聚生体中的任一微生物种群可占组合物的总微生物负载的1%至99%,并且在一些情况下,将占组合物中总微生物负载的5%或更少、5%至10%、最多并包括15%、最多并包括20%、最多并包括25%、最多并包括30%、最多并包括35%、最多并包括40%、最多并包括45%、最多并包括50%、最多并
包括55%、最多并包括60%、最多并包括65%、最多并包括70%、最多并包括75%、最多并包括80%、最多并包括85%、最多并包括90%,或最多并包括95%或更多。
74.在一些情况下,肝脏病症的治疗可包括在一段时间内施用多次剂量。在一些情况下,施用可包括在一天的时间段内施用1、2、3、4、5、6或更多次剂量。在一些情况下,这样的每日施用可以在一周内发生1天、2天、3天、4天、5天、6天或7天。在一些情况下,这样的每周施用可在1周、2周、3周、4周、6周、10周、12周或更长时间的过程中发生。在一些情况下,这样的长期施用可在1个月、2个月、3个月、4个月、5个月、6个月、7个月、8个月、9个月、10个月、11个月、12个月或更长时间的过程中发生。在一些情况下,施用可持续进行,以便维持这种治疗的效果,例如,其中上述施用在1年、2年、3年、4年、5年、6年、7年、8年、9年、10年或更长时间的过程中发生。
75.在许多情况下,本文所述的组合物的施用将通过口服/肠内施用实现。在此类情况下,组合物可配制成多种经口可摄取组合物类型中的任一种,包括例如,胶囊、片剂、混悬剂或乳剂,或食物类产品,诸如咀嚼剂、软糖、棒剂、薄片剂(wafer)、饼干或包括本文所述的微生物组合物的其他可食用形式。在一些情况下,组合物可通过其他方式施用,包括例如作为栓剂、灌肠剂或植入物直接施用到肠道中,例如通过结肠施用。
76.在一些情况下,当配制用于口服施用时,微生物组合物可包含在耐酸性基质中,诸如肠溶包衣、胶囊或微胶囊,以确保具有最大活力的微生物能够在胃的酸性条件下存活,并到达肠道,例如回肠、盲肠等。可获得多种耐酸性材料以用于递送治疗和/或生物活性成分通过胃,包括例如,羟丙基甲基纤维素(hpmc)和hpmc邻苯二甲酸酯封装材料。这些材料通常可作为片剂的包衣或作为微胶囊的基质,或作为其中可包装微生物组合物的预制胶囊商购获得。在一些情况下,胶囊和/或包衣以及赋形剂和其他辅料将不含动物源性产品,诸如奶、乳蛋白、动物源性明胶或其他动物源性蛋白质。
77.在一些情况下,本文所述的组合物的施用可与进餐同时、可在进餐之前,或可在进餐之后,以便为将组合物通过胃过渡到肠道中的一种或多种提供最佳条件。
78.可以将如本文所公开的微生物组合物配制成补充剂,例如膳食补充剂(例如,营养补充剂)或每日补充剂。膳食补充剂可以是含有用于补充饮食的膳食成分的口服产品。膳食补充剂可旨在提供否则可能无法足量摄入的营养素;例如,维生素、矿物质、蛋白质、氨基酸或其他营养物质。在一些实施方案中,膳食补充剂不旨在治疗、诊断、治愈或缓解疾病或病状的影响。膳食补充剂可以是本文公开的任何形式。
79.如本文所公开的微生物组合物可以配制成医疗食品。如本文所公开的微生物组合物可以被标记为医疗食品。医疗食品可以是被配制成在医师的监督下食用或经肠施用并且旨在用于疾病或病状(例如,本文公开的疾病或病状)的特定膳食管理的食品,所述疾病或病状的基于公认的科学原理的独特营养需求通过医学评估确定。在一些实施方案中,医疗食品可以例如,通过医疗食品旨在满足疾病或病状的独特营养需求的要求与用于特殊膳食用途的更广泛类别的食品区分开来,旨在在医疗监督下使用,并且旨在用于疾病或病状的特定膳食管理。医师的监督可以指由已经确定医疗食品对于受试者的整体医疗护理是必要的医师进行的持续的医疗监督(例如,在健康护理机构中或作为门诊病人)。受试者通常可以尤其为了作为给定疾病或病状的膳食管理的一部分的医疗食品的使用说明而反复就医。
80.在一些实施方案中,医疗食品不是由医师简单推荐作为整体饮食的一部分以管理
症状或降低疾病或病状的风险的那些。相反,在一些实施方案中,医疗食品可以是为需要使用该产品(例如,作为疾病或病状的特定膳食管理的主要组分)的受试者特别配制和加工的食品(与在自然状态下使用的天然存在的食物相反)。在一些实施方案中,医疗食品不作为药物进行监管,并且不需要处方。医疗食品可以是本文公开的任何形式。
81.在一些实施方案中,本公开的组合物是仅在医疗监督下使用的医疗食品。在一些实施方案中,本公开的医疗食品用于管理如本文所公开的肝脏病症。
82.iii.实施例
83.将包括初级和二级发酵菌的微生物物种的活聚生体配制成干粉并掺入延迟释放胶囊中,所述胶囊经选择以在摄取后离开受试者的胃之后释放其内容物。
84.一项双盲、安慰剂对照的临床试验在两个测试组中各招募了23至37名患者,并且在安慰剂组中招募了26名患者。两个测试组接受包含与益生元纤维源和赋形剂组合的不同微生物菌株亚群的两种封装制剂中的一种,而安慰剂组接受仅包含益生元纤维源和赋形剂的封装制剂。第一测试组每天施用多次剂量的测试制剂wbf-010,其包括三种不同的微生物菌株:两种二级发酵菌,即丁酸梭菌(每天3.3x109cfu)和拜氏梭菌(每天1.2x10
10
cfu),以及一种初级发酵菌,即婴儿双歧杆菌(每天2x109cfu)。
85.第二测试组另外包括粘蛋白降解微生物-嗜粘蛋白阿克曼菌(每天1.2x109cfu)和另一种二级发酵菌,即霍氏真杆菌(每天0.9x109cfu)。两种测试制剂还包括一定量的益生元纤维,并用惰性赋形剂构成剩余质量。安慰剂组施用相同质量和颜色以及益生元纤维的胶囊,但用惰性赋形剂取代微生物菌株粉末。
86.在12周的过程中,受试者每天施用6粒胶囊(早上3粒,晚上3粒),并在开始治疗后的0、2和4周验血,并且在第12周的日期测试alt和ast,以及与正在测试的代谢障碍相关的其他标志物。
87.图2示出每个患者组(安慰剂、wb-010和wb-011)中的ast和alt水平以及从时间0开始的ast和alt水平的变化的图。如图所示,接受安慰剂的那些受试者显示出alt和ast水平均从其初始水平增加到研究完成时的那些水平。相反,接受包括微生物聚生体的测试组合物中的一种的那些受试者显示出较低的ast和alt水平,并且接受wbf-010制剂的那些受试者显示出水平相对于其起始点适度降低,而wbf-011制剂表现出随时间推移的最大减少,并且比安慰剂组有临床上显著的减少。
88.虽然出于清楚和理解的目的已经对上述发明进行了一些详细的描述,但本领域技术人员通过阅读本公开将清楚,可以在不脱离本发明的真实范围的情况下对形式和细节作出各种改变。例如,上述所有技术和设备可以各种组合使用。本技术中引用的所有出版物、专利、专利申请和/或其他文件出于所有目的通过引用整体并入,其程度如同每个单独的出版物、专利、专利申请和/或其他文件被各自且单独地指出出于所有目的通过引用并入一样。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1