变体IGF2构建体的制作方法
变体igf2构建体
相关申请的交叉引用
1.本技术要求于2019年10月10日提交的美国临时申请62/913,677和于2019年10月31日提交的美国临时申请62/929,054的优先权权益,每个临时申请皆通过引用以其全文并入本文。
背景技术:
2.遗传障碍是经由在基因组的基因编码区中发生的可遗传突变或新生(de novo)突变引起的。在一些情况下,通过施用替代由患有遗传障碍的个体中突变的基因编码的蛋白质的蛋白质或通过施用编码这种蛋白质的基因疗法载体来治疗此类遗传障碍。然而,这样的治疗具有挑战,因为施用的蛋白质或由基因疗法载体编码的蛋白质并不总使蛋白质到达需要它的器官、细胞或细胞器。需要具有改善的细胞内靶向(例如,针对溶酶体)的蛋白质,以及编码它们的基因疗法载体。
技术实现要素:
3.在某些方面,提供了核酸构建体,这些核酸构建体包含:(a)编码治疗性蛋白质的核酸序列,和(b)编码变体igf2(vigf2)肽的核酸序列。在一些实施例中,该vigf2肽具有与表3的igf2变体肽有至少90%、95%、96%、97%、98%或99%同一性的氨基酸序列。在一些实施例中,该vigf2肽包含与选自由表3的seq id no:90-123组成的组的igf2变体肽有至少90%、95%、96%、97%、98%或99%同一性的氨基酸序列。在一些实施例中,该vigf2肽进一步包含接头,该接头具有与选自由seq id no:181-188组成的组的序列有至少90%、95%、96%、97%、98%或99%同一性的序列。在一些实施例中,与原生igf2肽相比,该vigf2肽对胰岛素受体和igfr1具有降低的亲和力或没有亲和力。在一些实施例中,与原生igf2肽相比,该vigf2肽对ci-mpr的亲和力增加。在一些实施例中,与原生igf2肽相比,该vigf2肽赋予融合蛋白改善的表达和/或分泌。在一些实施例中,该vigf2肽能够促进该治疗性蛋白质摄取到细胞中的溶酶体中。在一些实施例中,该治疗性蛋白质能够替代患有遗传障碍的受试者中与遗传障碍相关的有缺陷的或缺乏的蛋白质。在一些实施例中,遗传障碍是溶酶体贮积症。在一些实施例中,遗传障碍选自由以下组成的组:天冬氨酰葡糖胺尿症、cln1病、cln2病、胱氨酸病、法布里病(fabry disease)、i型戈谢病(gaucher disease)、ii型戈谢病、iii型戈谢病、庞贝病(pompe disease)、泰-萨克斯病(tay sachs disease)、桑德霍夫病(sandhoff disease)、异染性脑白质营养不良、i型黏脂贮积病、ii型黏脂贮积病、iii型黏脂贮积病、iv型黏脂贮积病、贺勒病(hurler disease)、亨特病(hunter disease)、a型圣菲利波病(sanfilippo disease)、b型圣菲利波病、c型圣菲利波病、d型圣菲利波病、a型莫基奥病(morquio disease)、b型莫基奥病、马罗托-拉米病(maroteau-lamy disease)、斯莱病(sly disease)、a型尼曼-皮克病(niemann-pick disease)、b型尼曼-皮克病、c1型尼曼-皮克病、c2型尼曼-皮克病、i型辛德勒病(schindler disease)、ii型辛德勒病、腺苷脱氨酶重症联合免疫缺陷(ada-scid)、慢性肉芽肿病(cgd)以及神经元蜡样质脂褐质沉积症。在一
些实施例中,遗传障碍是庞贝病。在一些实施例中,遗传障碍是神经元蜡样质脂褐质沉积症。在一些实施例中,该治疗性蛋白质包含选自由以下组成的组的酶:α-半乳糖苷酶(a或b)、β-半乳糖苷酶、β-己糖胺酶(a或b)、半乳糖神经酰胺酶、芳基硫酸酯酶(a或b)、β-葡萄糖脑苷脂酶、葡萄糖脑苷脂酶、溶酶体酸性脂肪酶、溶酶体酶酸性鞘磷脂酶、甲酰甘氨酸生成酶、艾杜糖醛酸酶(例如,α-l)、乙酰辅酶a:α-氨基葡糖苷n-乙酰转移酶、糖胺聚糖α-l-艾杜糖醛酸水解酶、乙酰肝素n-硫酸酯酶、n-乙酰基-α-d-氨基葡糖苷酶(naglu)、艾杜糖醛酸-2-硫酸酯酶、半乳糖胺-6-硫酸硫酸酯酶、n-乙酰半乳糖胺-6-硫酸酯酶、n-磺基葡糖胺磺基水解酶、糖胺聚糖n-乙酰半乳糖胺4-硫酸酯酶、β-葡糖醛酸糖苷酶、透明质酸酶、α-n-乙酰神经氨酸酶(唾液酸酶)、神经节苷脂唾液酸酶、磷酸转移酶、α-葡糖苷酶、α-d-甘露糖苷酶、β-d-甘露糖苷酶、天冬氨酰氨基葡糖苷酶、α-l-岩藻糖苷酶、巴滕素(battenin)、棕榈酰蛋白硫酯酶和其他巴滕病(batten)相关蛋白(例如,蜡样质脂褐质沉积症神经元蛋白6),或其酶活性片段。在一些实施例中,该治疗性蛋白质是α-葡糖苷酶,或其酶活性片段。在一些实施例中,该治疗性蛋白质是棕榈酰蛋白硫酯酶1(ppt1)。在一些实施例中,该治疗性蛋白质是三肽基肽酶1(tpp1)。在一些实施例中,该治疗性蛋白质是天冬氨酰氨基葡糖苷酶。在一些实施例中,该治疗性蛋白质是naglu(seq id no:54)。在一些实施例中,该治疗性蛋白质是naglu的成熟肽,对应于去除原生信号肽(seq id no:180)后保留的seq id no:54的氨基酸24-743。在一些实施例中,该核酸构建体进一步包含翻译起始序列。在一些实施例中,该翻译起始序列包含kozak序列。在一些实施例中,编码vigf2的核酸序列在编码治疗性蛋白质的核酸序列的5’端。在一些实施例中,编码vigf2的核酸序列在编码治疗性蛋白质的核酸序列的3’端。在一些实施例中,该核酸构建体进一步包含接头序列,该接头序列编码在vigf2核苷酸序列和编码治疗性蛋白质的核酸序列之间的接头肽。在一些实施例中,该接头肽包含seq id no:181-188。在一些实施例中,该核酸构建体是病毒载体。在一些实施例中,病毒载体是腺病毒载体、腺相关病毒(aav)载体、逆转录病毒载体、慢病毒载体、痘病毒载体、牛痘病毒载体、腺病毒载体或疱疹病毒载体。
4.在另外的方面,提供了药物组合物,其包含治疗有效量的本文提供的任何一种核酸构建体、药学上可接受的载剂或赋形剂。在一些实施例中,赋形剂包括非离子型低渗透性化合物、缓冲剂、聚合物、盐或其组合。
5.在进一步的方面,提供了用于治疗遗传障碍的方法,这些方法包括向有需要的受试者施用本文提供的任何一种核酸构建体或本文提供的任何一种药物组合物。在一些实施例中,遗传障碍是溶酶体贮积症。在一些实施例中,遗传障碍选自由以下组成的组:天冬氨酰葡糖胺尿症、巴滕病、胱氨酸病、法布里病、i型戈谢病、ii型戈谢病、iii型戈谢病、庞贝病、泰-萨克斯病、桑德霍夫病、异染性脑白质营养不良、i型黏脂贮积病、ii型黏脂贮积病、iii型黏脂贮积病、iv型黏脂贮积病、贺勒病、亨特病、a型圣菲利波病、b型圣菲利波病、c型圣菲利波病、d型圣菲利波病、a型莫基奥病、b型莫基奥病、马罗托-拉米病、斯莱病、a型尼曼-皮克病、b型尼曼-皮克病、c1型尼曼-皮克病、c2型尼曼-皮克病、i型辛德勒病、ii型辛德勒病、腺苷脱氨酶重症联合免疫缺陷(ada-scid)、慢性肉芽肿病(cgd)和神经元蜡样质脂褐质沉积症(巴滕病)。在一些实施例中,遗传障碍是庞贝病。在一些实施例中,遗传障碍是神经元蜡样质脂褐质沉积症。在一些实施例中,遗传障碍是天冬氨酰葡糖胺尿症。在一些实施例中,施用是通过鞘内、眼内、玻璃体内、视网膜、静脉内、肌内、心室内、大脑内、小脑内、脑
室内、实质内、皮下或其组合来进行。在一些实施例中,进行鞘内施用。
6.在另外的方面,提供了药物组合物以用于治疗遗传障碍,这些药物组合物包含本文提供的任何一种基因疗法载体和药学上可接受的载剂或赋形剂。在进一步的方面,提供了药物组合物以用于制备用于治疗遗传障碍的药剂,这些药物组合物包含本文提供的任何一种核酸构建体和药学上可接受的载剂或赋形剂。在一些实施例中,遗传障碍是溶酶体贮积症。在一些实施例中,遗传障碍选自由以下组成的组:天冬氨酰葡糖胺尿症、巴滕病、胱氨酸病、法布里病、i型戈谢病、ii型戈谢病、iii型戈谢病、庞贝病、泰-萨克斯病、桑德霍夫病、异染性脑白质营养不良、i型黏脂贮积病、ii型黏脂贮积病、iii型黏脂贮积病、iv型黏脂贮积病、贺勒病、亨特病、a型圣菲利波病、b型圣菲利波病、c型圣菲利波病、d型圣菲利波病、a型莫基奥病、b型莫基奥病、马罗托-拉米病、斯莱病、a型尼曼-皮克病、b型尼曼-皮克病、c1型尼曼-皮克病、c2型尼曼-皮克病、i型辛德勒病、ii型辛德勒病、腺苷脱氨酶重症联合免疫缺陷(ada-scid)、慢性肉芽肿病(cgd)和神经元蜡样质脂褐质沉积症。在一些实施例中,遗传障碍是庞贝病。在一些实施例中,遗传障碍是神经元蜡样质脂褐质沉积症。在一些实施例中,遗传障碍是天冬氨酰葡糖胺尿症。在一些实施例中,将组合物配制为鞘内、眼内、玻璃体内、视网膜、静脉内、肌内、心室内、大脑内、小脑内或皮下施用。在一些实施例中,将组合物配制为鞘内施用。
7.在另外的方面,提供了编码融合蛋白的核酸,该融合蛋白具有与选自由seq id no:47-53组成的组的序列有至少90%、95%、96%、97%、98%或99%同一性的氨基酸序列。在一些实施例中,该核酸与选自由seq id no:60-67组成的组的序列有至少85%、90%、95%、96%、97%、98%或99%同一性。
8.在进一步的方面,提供了药物组合物,其包含任何一种上述核酸和药学上可接受的载剂或赋形剂。在一些实施例中,赋形剂包括非离子型低渗透性化合物、缓冲剂、聚合物、盐或其组合。
9.在进一步的方面,药物组合物包含融合蛋白和药学上可接受的载剂或赋形剂,该融合蛋白具有与选自由seq id no:47-53和seq id no:60-67组成的组的序列有至少90%、95%、96%、97%、98%或99%同一性的氨基酸序列。在一些实施例中,赋形剂包括非离子型低渗透性化合物、缓冲剂、聚合物、盐或其组合。
10.在另外的方面,提供了基因疗法载体,其包含编码与选自由seq id no:47-53和seq id no:60-67组成的组的序列有至少90%、95%、96%、97%、98%或99%同一性的氨基酸序列的核酸;和编码与选自由seq id no:106、109、111、119、120和121组成的组的序列有至少90%、95%、96%、97%、98%或99%同一性的氨基酸序列的核酸。在一些实施例中,基因疗法载体是病毒载体。在一些实施例中,病毒载体是腺病毒载体、腺相关病毒(aav)载体、逆转录病毒载体、慢病毒载体、痘病毒载体、牛痘病毒载体、腺病毒载体或疱疹病毒载体,和药学上可接受的载剂或赋形剂。在一些实施例中,赋形剂包括非离子型低渗透性化合物、缓冲剂、聚合物、盐或其组合。
11.在另外的方面,提供了治疗cln1/ppt1病或cln2/tpp1病的方法,其包括向有需要的受试者施用治疗有效量的本文的任何一种核酸、本文的任何一种融合蛋白、本文的任何一种基因疗法载体,或本文的任何一种药物组合物。在一些实施例中,施用是通过鞘内、眼内、玻璃体内、视网膜、静脉内、肌内、心室内、大脑内、小脑内、脑室内、实质内、皮下或其组
合来进行。
12.在一些实施例中,该核酸具有与选自由seq id no:189-250组成的组的序列有至少85%、90%、95%、96%、97%、98%或99%同一性的核酸序列。
13.在另外的方面,提供了药物组合物,其包含本文的任何一种核酸、药学上可接受的载剂或赋形剂。在一些实施例中,赋形剂包括非离子型低渗透性化合物、缓冲剂、聚合物、盐或其组合。
14.在一些实施例中,提供了与选自由seq id no:90-103组成的组的序列有至少95%、96%、97%、98%或99%同一性的变体igf2(vigf2)肽。
15.在一些实施例中,该变体igf2(vigf2)肽与选自seq id no:106、109、111、119、120、121的至少一个序列有至少98%同一性。在一些实施例中,该vigf2肽与seq id no:120或121有至少95%、96%、97%、98%或99%同一性。
16.在一些实施例中,提供了包含变体vigf2肽和治疗性蛋白质的融合蛋白,该治疗性蛋白质具有与选自由以下组成的组的序列有至少95%、96%、97%、98%或99%同一性的氨基酸序列:seq id no:4、seq id no:4的氨基酸残基21-306、seq id no:4的氨基酸残基28-306、seq id no:8、seq id no:46和seq id no:54。
17.在一些实施例中,该融合蛋白具有与选自由seq id no:60-67、seq id no:47-53和seq id no:54-59组成的组的序列有至少95%、96%、97%、98%或99%同一性的氨基酸序列。在一些实施例中,该融合蛋白进一步包含溶酶体切割肽。在一些实施例中,该溶酶体切割肽具有seq id no:188。在一些实施例中,该vigf2肽在治疗性蛋白质的n末端。在一些实施例中,该vigf2肽在治疗性蛋白质的c末端。
18.在一些实施例中,该融合蛋白包含信号序列。在一些实施例中,该信号序列具有与选自由seq id no:169-180组成的组的序列有至少95%、96%、97%、98%或99%同一性的氨基酸序列。
19.在一些实施例中,该治疗性蛋白质是ppt1或其酶活性片段、tpp1或其酶活性片段、或naglu或其酶活性片段。
20.在一些实施例中,该融合蛋白比缺少vigf2肽的相应蛋白更有效地被靶细胞摄取。在一些实施例中,该融合蛋白被脑中的细胞摄取。在一些实施例中,该融合蛋白被神经元细胞摄取。在一些实施例中,该融合蛋白被神经胶质细胞摄取。
21.本文还提供了药物组合物,其包含具有vigf2肽和治疗性蛋白质的融合蛋白,以及药学上可接受的载剂或赋形剂。本文还提供了治疗溶酶体贮积症的方法,其包括向有需要的受试者施用此类药物组合物。在一些实施例中,溶酶体贮积症选自由cln1/ppt1病、cln2/tpp1病和b型圣菲利波病组成的组。在一些实施例中,该融合蛋白或包含该融合蛋白的药物组合物通过鞘内、眼内、玻璃体内、视网膜、静脉内、肌内、心室内、大脑内、小脑内、脑室内、实质内、皮下或其组合施用。
22.在一些实施例中,施用该药物组合物防止/减少或逆转自发荧光贮积物质(asm)在脑中的积聚。在一些实施例中,施用该药物组合物防止/减少或逆转胶质原纤维酸性蛋白(gfap)在脑中的升高。在一些实施例中,施用该药物组合物防止/减少或逆转自发荧光贮积物质(asm)在皮质或丘脑中的积聚。在一些实施例中,施用该药物组合物防止/减少或逆转胶质原纤维酸性蛋白(gfap)在脑皮质或丘脑中的升高。
23.本文进一步提供了编码包含vigf2和治疗性蛋白的融合蛋白的核酸,其中该核酸与选自由seq id no:189-250组成的组的序列有至少85%、90%、95%、96%、97%、98%或99%同一性。
24.在另外的方面,提供了包含本文的任何一种融合蛋白和药学上可接受的载剂或赋形剂的药物组合物。在一些实施例中,赋形剂包括非离子型低渗透性化合物、缓冲剂、聚合物、盐或其组合。
25.在进一步的方面,提供了基因疗法载体,其包含编码与seq id no:51有至少90%同一性的氨基酸序列的核酸。在一些实施例中,基因疗法载体是病毒载体。在一些实施例中,病毒载体是腺病毒载体、腺相关病毒(aav)载体、逆转录病毒载体、慢病毒载体、痘病毒载体、牛痘病毒载体、腺病毒载体或疱疹病毒载体。
26.在另外的方面,提供了包含本文提供的任何一种基因疗法载体和药学上可接受的载剂或赋形剂的药物组合物。在一些实施例中,赋形剂包括非离子型低渗透性化合物、缓冲剂、聚合物、盐或其组合。
27.在另一个方面,提供了核酸构建体,其包含:(a)编码治疗性蛋白质的核酸序列,和(b)编码变体igf2(vigf2)肽的核酸序列,该igf2肽与选自seq id no:90-103的至少一个序列有至少95%、96%、97%、98%或99%同一性。在一些方面,该vigf2肽具有与选自seq id no:106、109、111、119、120、121的igf2变体肽有至少95%、96%、97%、98%或99%同一性的氨基酸序列。在一些实施例中,该vigf2肽包含与选自由seq id no:120和seq id no:121组成的组的igf2变体肽有至少95%、96%、97%、98%或99%同一性的氨基酸序列。
28.在一些方面,该核酸进一步包含编码接头的序列,该接头具有与选自由seq id no:181-188组成的组的序列有至少95%、96%、97%、98%或99%同一性的序列。在一些实施例中,与具有seq id no:80的氨基酸序列的vigf2肽相比,该vigf2肽能够增加治疗性蛋白质的表达和/或分泌。在一些实施例中,与具有seq id no:80的氨基酸序列的vigf2肽相比,该vigf2肽对ci-mpr具有增加的亲和力。在一些实施例中,该vigf2肽能够提高靶细胞(例如人脑细胞)对治疗性蛋白质的摄取。在一些实施例中,人脑细胞是神经元细胞或神经胶质细胞。
29.在某些方面,该治疗性蛋白质能够替代患有遗传障碍的受试者中与遗传障碍相关的有缺陷的或缺乏的蛋白质。在一些实施例中,遗传障碍是溶酶体贮积症。在一些实施例中,遗传障碍选自由以下组成的组:天冬氨酰葡糖胺尿症、神经元蜡样质脂褐质沉积症、cln1/ppt1病、cln2/ppt1病、胱氨酸病、法布里病、i型戈谢病、ii型戈谢病、iii型戈谢病、庞贝病、泰-萨克斯病、桑德霍夫病、异染性脑白质营养不良、i型黏脂贮积病、ii型黏脂贮积病、iii型黏脂贮积病、iv型黏脂贮积病、贺勒病、亨特病、a型圣菲利波病、b型圣菲利波病、c型圣菲利波病、d型圣菲利波病、a型莫基奥病、b型莫基奥病、马罗托-拉米病、斯莱病、a型尼曼-皮克病、b型尼曼-皮克病、c1型尼曼-皮克病、c2型尼曼-皮克病、i型辛德勒病、ii型辛德勒病、腺苷脱氨酶重症联合免疫缺陷(ada-scid)和神经元蜡样质脂褐质沉积症。在一些实施例中,遗传障碍选自由cln1/ppt1病、cln2/ppt1病、庞贝病和mps iiib病组成的组。在一些方面,遗传障碍是cln1/ppt1病或cln2/ppt1病。
30.在一些方面,该治疗性蛋白质包含选自由以下组成的组的人酶:α-半乳糖苷酶(a或b)、β-半乳糖苷酶、β-己糖胺酶(a或b)、半乳糖神经酰胺酶、芳基硫酸酯酶(a或b)、β-葡萄
糖脑苷脂酶、葡萄糖脑苷脂酶、溶酶体酸性脂肪酶、溶酶体酶酸性鞘磷脂酶、甲酰甘氨酸生成酶、艾杜糖醛酸酶(例如,α-l)、乙酰辅酶a:α-氨基葡糖苷n-乙酰转移酶、糖胺聚糖α-l-艾杜糖醛酸水解酶、乙酰肝素n-硫酸酯酶、n-乙酰基-α-d-氨基葡糖苷酶(naglu)、艾杜糖醛酸-2-硫酸酯酶、半乳糖胺-6-硫酸硫酸酯酶、n-乙酰半乳糖胺-6-硫酸酯酶、n-磺基葡糖胺磺基水解酶、糖胺聚糖n-乙酰半乳糖胺4-硫酸酯酶、β-葡糖醛酸糖苷酶、透明质酸酶、α-n-乙酰神经氨酸酶(唾液酸酶)、神经节苷脂唾液酸酶、磷酸转移酶、α-葡糖苷酶、α-d-甘露糖苷酶、β-d-甘露糖苷酶、天冬氨酰氨基葡糖苷酶、α-l-岩藻糖苷酶、巴滕素、ppt1、tpp1和其他巴滕病相关蛋白(例如,蜡样质脂褐质沉积症神经元蛋白6),或其酶活性片段。在一些实施例中,治疗性蛋白质是人溶酶体酶或其酶活性片段。在一些实施例中,人溶酶体酶是α-葡糖苷酶、ppt1、tpp1或naglu。
31.在一些方面,核酸构建体进一步包含编码信号肽的序列。在一些实施例中,信号肽是选自由seq id no:169-180组成的组的序列。在一些实施例中,编码vigf2的核酸序列在编码治疗性蛋白质的核酸序列的5’端。在其他实施例中,编码vigf2的核酸序列在编码治疗性蛋白质的核酸序列的3’端。
32.进一步提供了包含本文所述的核酸的基因疗法载体。在一些实施例中,基因疗法载体是病毒载体。在一些实施例中,病毒载体是腺病毒载体、腺相关病毒(aav)载体、逆转录病毒载体、慢病毒载体、痘病毒载体、牛痘病毒载体、腺病毒载体或疱疹病毒载体。
33.在一些方面,本文的核酸构建体在质粒或细菌人工染色体中。在一些实施例中,本文所述的核酸构建体在宿主细胞中。
34.进一步提供了药物组合物,其包含治疗有效量的本文所述核酸构建体,或包含本文所述核酸构建体的基因疗法载体,以及药学上可接受的载剂或赋形剂。在一些实施例中,赋形剂包括非离子型低渗透性化合物、缓冲剂、聚合物、盐或其组合。
35.本文进一步提供了用于治疗遗传障碍的方法,其包括向有需要的受试者施用本文所述的核酸构建体、基因疗法载体和/或药物组合物。在一些实施例中,遗传障碍是溶酶体贮积症。在一些实施例中,遗传障碍选自由以下组成的组:天冬氨酰葡糖胺尿症、神经元蜡样质脂褐质沉积症、cln1/ppt1病、cln2/ppt1病、胱氨酸病、法布里病、i型戈谢病、ii型戈谢病、iii型戈谢病、庞贝病、泰-萨克斯病、桑德霍夫病、异染性脑白质营养不良、i型黏脂贮积病、ii型黏脂贮积病、iii型黏脂贮积病、iv型黏脂贮积病、贺勒病、亨特病、a型圣菲利波病、b型圣菲利波病、c型圣菲利波病、d型圣菲利波病、a型莫基奥病、b型莫基奥病、马罗托-拉米病、斯莱病、a型尼曼-皮克病、b型尼曼-皮克病、c1型尼曼-皮克病、c2型尼曼-皮克病、i型辛德勒病、ii型辛德勒病、腺苷脱氨酶重症联合免疫缺陷(ada-scid)和慢性肉芽肿病(cgd)。在一些实施例中,遗传障碍是巴滕病,例如cln1/ppt1病或cln2/tpp1病。在一些实施例中,遗传障碍是庞贝病或b型圣菲利波病。
36.在一些实施例中,施用是通过鞘内、眼内、玻璃体内、视网膜、静脉内、肌内、心室内、大脑内、小脑内、脑室内、实质内、皮下或其组合来进行。
37.在一些方面,施用该核酸、基因疗法载体、融合蛋白或药物组合物防止/减少或逆转自发荧光贮积物质(asm)在脑中的积聚。在一些实施例中,施用该核酸、基因疗法载体、融合蛋白或药物组合物防止/减少或逆转胶质原纤维酸性蛋白(gfap)在脑中的升高。在一些实施例中,施用该核酸、基因疗法载体、融合蛋白或药物组合物防止/减少或逆转自发荧光
贮积物质(asm)在皮质或丘脑中的积聚。在一些方面,施用该核酸、基因疗法载体、融合蛋白或药物组合物防止/减少或逆转胶质原纤维酸性蛋白(gfap)在脑皮质或丘脑中的升高。
38.在一些方面,核酸编码融合蛋白,该融合蛋白具有与选自由seq id no:60-67组成的组的序列有至少95%、96%、97%、98%或99%同一性的序列。在一些实施例中,该核酸编码融合蛋白,该融合蛋白具有与选自由seq id no:47-53组成的组的序列有至少98%同一性的序列。
39.在一些方面,该核酸编码融合蛋白,该融合蛋白包含:(a)与选自由seq id no:106、109、111、119、120和121组成的组的序列有至少95%、96%、97%、98%或99%同一性的氨基酸序列;和(b)与选自由以下组成的组的序列有至少95%、96%、97%、98%或99%同一性的氨基酸序列:seq id no:4、seq id no:4的残基21-306、seq id no:4的残基28-306、seq id no:8和seq id no:46。在一些实施例中,该核酸编码与seq id no:120和121有至少95%、96%、97%、98%或99%同一性的vigf2。在一些实施例中,该核酸编码融合蛋白,该融合蛋白包含:(a)seq id no:106、109、111、119、120或121中的至少一个;和(b)seq id no:4、seq id no:4的残基21-306、seq id no:4的残基28-306、seq id no:8和seq id no:46、seq id no:4的残基28-306、seq id no:8和seq id no:46中的至少一个。
40.在一些实施例中,该核酸进一步编码溶酶体切割肽。
41.在一些方面,该融合蛋白具有与seq id no:60-67和seq id no:47-53中的至少一个有至少95%、96%、97%、98%或99%同一性的序列。在一些实施例中,该融合蛋白包含seq id no:60-67和seq id no:47-53中的至少一个。在一些实施例中,该融合蛋白由或基本上由seq id no:60-67和seq id no:47-53组成。
42.在另外的方面,提供了治疗溶酶体贮积病的方法,其包括向有需要的受试者施用治疗有效量的本文的任何一种核酸、本文的任何一种融合蛋白、本文的任何一种基因疗法载体或本文的任何一种药物组合物。在一些实施例中,施用是通过鞘内、眼内、玻璃体内、视网膜、静脉内、肌内、心室内、大脑内、小脑内、脑室内、实质内、皮下或其组合来进行。
43.在进一步的方面,提供了治疗巴滕病(包括cln1/ppt1病和cln2/tpp1病)的方法,其包括向有需要的受试者施用治疗有效量的本文的任何一种核酸、本文的任何一种融合蛋白、本文的任何一种基因疗法载体或本文的任何一种药物组合物。在一些实施例中,施用是通过鞘内、眼内、玻璃体内、视网膜、静脉内、肌内、心室内、大脑内、小脑内、脑室内、实质内、皮下或其组合来进行。
44.在另外的方面,提供了药物组合物,其包含本文提供的任何一种核酸和药学上可接受的载剂或赋形剂。在一些实施例中,赋形剂包括非离子型低渗透性化合物、缓冲剂、聚合物、盐或其组合。
45.在另外的方面,提供了包含本文提供的任何一种基因疗法载体和药学上可接受的载剂或赋形剂的药物组合物。
46.在另外的方面,提供了融合蛋白,其包含:(a)溶酶体酶,和(b)变体igf2(vigf2)肽,其中该vigf2肽包含与表3的igf2变体肽有至少95%、96%、97%、98%或99%同一性的氨基酸序列。在一些实施例中,该vigf2肽包含与选自由seq id no:69-131组成的组的igf2变体肽有至少95%、96%、97%、98%或99%同一性的氨基酸序列。在一些实施例中,该vigf2肽包含与选自由seq id no:90-123组成的组的igf2变体肽有至少95%、96%、97%、
98%或99%同一性的氨基酸序列。在一些实施例中,该vigf2已被修饰为用四个甘氨酸残基替换野生型igf2的残基31-38(δ31-38gggg)。在一些实施例中,该vigf2由v43l突变进一步修饰。在一些实施例中,该vigf2已被进一步修饰为用酸性残基(天冬氨酸或谷氨酸)替换50位丝氨酸。在一些方面,该vigf2具有seq id no:120或121的序列。
47.在一些实施例中,该vigf2肽进一步包含接头,该接头具有与选自由seq id no:181-188组成的组的序列有至少95%、96%、97%、98%或99%同一性的序列。在一些实施例中,该接头是可切割的。在一些实施例中,与原生igf2肽相比,该vigf2肽对胰岛素受体和igfr1具有降低的亲和力或没有亲和力。在一些实施例中,与原生igf2肽相比,该vigf2肽对ci-mpr的亲和力增加。在一些实施例中,该vigf2肽能够促进溶酶体酶摄取到细胞中的溶酶体中。在一些实施例中,该溶酶体酶能够替代与溶酶体贮积症相关的有缺陷的或缺乏的蛋白质。在一些实施例中,溶酶体贮积症选自由以下组成的组:天冬氨酰葡糖胺尿症、巴滕病、胱氨酸病、法布里病、i型戈谢病、ii型戈谢病、iii型戈谢病、庞贝病、泰-萨克斯病、桑德霍夫病、异染性脑白质营养不良、i型黏脂贮积病、ii型黏脂贮积病、iii型黏脂贮积病、iv型黏脂贮积病、贺勒病、亨特病、a型圣菲利波病、b型圣菲利波病、c型圣菲利波病、d型圣菲利波病、a型莫基奥病、b型莫基奥病、马罗托-拉米病、斯莱病、a型尼曼-皮克病、b型尼曼-皮克病、c1型尼曼-皮克病、c2型尼曼-皮克病、i型辛德勒病、ii型辛德勒病、腺苷脱氨酶重症联合免疫缺陷(ada-scid)、慢性肉芽肿病(cgd)和神经元蜡样质脂褐质沉积症。在一些实施例中,溶酶体贮积症是庞贝病。在一些实施例中,溶酶体贮积症是神经元蜡样质脂褐质沉积症。在一些实施例中,溶酶体酶包含选自由以下组成的组的酶:α-半乳糖苷酶(a或b)、β-半乳糖苷酶、β-己糖胺酶(a或b)、半乳糖神经酰胺酶、芳基硫酸酯酶(a或b)、β-葡萄糖脑苷脂酶、葡萄糖脑苷脂酶、溶酶体酸性脂肪酶、溶酶体酶酸性鞘磷脂酶、甲酰甘氨酸生成酶、艾杜糖醛酸酶(例如,α-l)、乙酰辅酶a:α-氨基葡糖苷n-乙酰转移酶、糖胺聚糖α-l-艾杜糖醛酸水解酶、乙酰肝素n-硫酸酯酶、n-乙酰基-α-d-氨基葡糖苷酶(naglu)、艾杜糖醛酸-2-硫酸酯酶、半乳糖胺-6-硫酸硫酸酯酶、n-磺基葡糖胺磺基水解酶、n-乙酰半乳糖胺-6-硫酸酯酶、糖胺聚糖n-乙酰半乳糖胺4-硫酸酯酶、β-葡糖醛酸糖苷酶、透明质酸酶、α-n-乙酰神经氨酸酶(唾液酸酶)、神经节苷脂唾液酸酶、磷酸转移酶、α-葡糖苷酶、α-d-甘露糖苷酶、β-d-甘露糖苷酶、天冬氨酰氨基葡糖苷酶、α-l-岩藻糖苷酶、巴滕素、棕榈酰蛋白硫酯酶和其他巴滕病相关蛋白(例如,蜡样质脂褐质沉积症神经元蛋白6),或其酶活性片段。在一些实施例中,溶酶体酶是α-葡糖苷酶,或其酶活性片段。在一些实施例中,溶酶体酶是棕榈酰蛋白硫酯酶。在一些实施例中,溶酶体酶是三肽基肽酶1。在一些实施例中,溶酶体酶是天冬氨酰氨基葡糖苷酶。
48.此外,本文提供了药物组合物,其包含治疗有效量的本文提供的任何一种融合蛋白和药学上可接受的载剂或赋形剂。通过引用并入
49.本说明书中所提到的所有出版物、专利和专利申请都通过引用并入本文,并入程度如同指示每个单独出版物、专利或专利申请明确且单独地通过引用并入一般。
附图说明
50.本专利申请文件含有至少一张彩色附图。在请求并支付必要的费用后,官方将会
提供带有一幅或多幅彩色附图的本专利申请的副本。将通过参考阐述了利用本披露内容原理的说明性实施例的以下具体实施方式和附图获得对本披露内容的特征和优点的理解,在所述附图中:
51.图1显示了利用使用固定化ci-mpr的亲和色谱法来确定能够通过磷酸化寡糖与ci-mpr相互作用的gaa的比例。第一个峰是流过色谱柱的物质,表明它没有磷酸化聚糖。后面的峰是能够结合固定化ci-mpr的物质。它是以递增的m6p梯度进行洗脱。m6p揭示了gaa含有含m6p的部分和缺少m6p的部分。由于结合ci-mpr是受体介导的内吞作用的强制性第一步,因此只有结合ci-mpr的rhgaa部分才能有效地被细胞摄取。
52.图2显示了ci-mpr的结构,包括针对igf2以及针对单磷酸化寡糖和双磷酸化寡糖的不同结合结构域。
53.图3显示了成熟人igf2肽的序列和结构。提出了影响与其他受体和血清蛋白的结合的位点特异性氨基酸取代。
54.图4显示了通过表面等离子共振测量的野生型igf2(wtigf2)肽与ci-mpr的结合。
55.图5显示了通过表面等离子共振测量的变体igf2(vigf2)肽与ci-mpr的结合。
56.图6显示了向阿糖苷酶α添加vigf2对于增加与igf2/ci-mpr的结合的益处。
57.图7显示了向重组人n-乙酰基-α-d-氨基葡糖苷酶(rhnaglu)添加vigf2对于增加与igf2/ci-mpr的结合的益处。
58.图8显示了野生型人igf2与胰岛素受体的结合。
59.图9显示了没有可检测到的vigf2与胰岛素受体的结合。
60.图10显示了野生型igf2与胰岛素样生长因子1受体的结合。
61.图11显示了与野生型igf2相比,vigf2肽与胰岛素样生长因子1受体的结合降低。
62.图12显示了编码天然hgaa和工程化hgaa的基因疗法表达盒的两个实例。天然hgaa的磷酸化程度很低,且无法有效结合ci-mpr。工程化hgaa添加了用于改善cimpr结合的元件(vigf2),并加入2gs接头以允许vigf2-gaa蛋白与ci-mpr的更强相互作用,并添加了bip信号肽以改善分泌。
63.图13显示了来自表达以下的细胞的棕榈酰蛋白硫酯酶1(ppt1)的蛋白质印迹:重组人ppt1(ppt1-1)、具有vigf2靶向结构域的重组人ppt1(ppt1-2)和具有vigf2靶向结构域和bip信号序列的重组人ppt1(ppt1-29)。蛋白质表达会受到所用igf变体的影响。
64.图14显示了ppt1构建体与ci-mpr的结合。
65.图15显示了在表达工程化或天然hgaa的cho细胞的条件培养基中的gaa活性。
66.图16显示了在gaa敲除小鼠中的4周基因疗法小鼠研究的研究设计。
67.图17显示了如所指示未经处理的野生型(“正常”)小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠中的gaa血浆活性。
68.图18显示了如所指示在未经处理的野生型(“正常”)小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠中测量的gaa水平。
69.图19显示了如所指示获得自经处理小鼠的血浆样品中rhgaa的细胞表面受体ci-mpr结合。
70.图20显示了如所指示未经处理的野生型(“正常”)小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的胫骨前肌的gaa活性和糖原组织病理学评分。
71.图21显示了如所指示来自未经处理的野生型小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的胫骨前肌的糖原pas。
72.图22显示了如所指示来自未经处理的野生型小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的胫骨前肌的hgaa免疫组织化学。
73.图23显示了如所指示来自未经处理的野生型(“正常”)小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的脑和脊髓的脑gaa活性、脑糖原和脊髓糖原组织病理学评分。
74.图24显示了如所指示来自未经处理的野生型小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的脑的糖原pas。
75.图25显示了如所指示来自未经处理的野生型(“正常”)小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的脑干和脉络丛的hgaa免疫组织化学。
76.图26显示了如所指示来自未经处理的野生型小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的脊髓的糖原pas。
77.图27显示了如所指示来自未经处理的野生型小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的脊髓的hgaa免疫组织化学。
78.图28显示了如所指示来自未经处理的野生型(“正常”)小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的股四头肌gaa活性和糖原组织病理学评分。
79.图29显示了如所指示来自未经处理的野生型小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的股四头肌的糖原luxol/pas。
80.图30显示了如所指示来自未经处理的野生型小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的股四头肌的hgaa免疫组织化学。
81.图31显示了如所指示未经处理的野生型(“正常”)小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的肱三头肌gaa活性和组织病理学评分。
82.图32显示了如所指示来自未经处理的野生型小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的肱三头肌的糖原luxol/pas。
83.图33显示了如所指示来自未经处理的野生型小鼠或用基因疗法载体或媒介物处理的gaa敲除小鼠的肱三头肌的hgaa免疫组织化学。
84.图34显示了工程化和野生型ppt1与cimpr的结合。
85.图35显示了工程化和野生型tpp1与cimpr的结合。
86.图36显示了工程化和野生型aga与cimpr的结合。
87.图37显示了工程化和野生型gla与cimpr的结合。
88.图38显示了来自条件培养基中表达各种突变vigf2-gaa构建体的细胞的gaa的蛋白质印迹。
89.图39显示了新的igf2-gaa变体相对于来自图38的蛋白质印迹的vigf2-gaa构建体的分泌。
90.图40显示了各种vigf2-gaa构建体的ci-mpr结合。
91.图41显示了各种vigf2-gaa构建体的cimpr结合的bmax和kd值。
92.图42显示了各种vigf2-gaa构建体的ci-mpr结合。
93.图43显示了各种vigf2-gaa构建体的cimpr结合的bmax和kd值。
94.图44显示了各种vigf2-gaa构建体的ci-mpr结合。
95.图45显示了各种vigf2-gaa构建体的cimpr结合的bmax和kd值。
96.图46显示了各种vigf2-gaa构建体的细胞摄取。
97.图47显示了各种vigf2-gaa构建体的细胞摄取。
98.图48显示了与ci-mpr或igf2r结合的各种vigf2肽。
99.图49显示了通过蛋白质印迹定量的条件培养基中的ppt1。
100.图50显示了通过蛋白质印迹定量的条件培养基中的ppt1。
101.图51显示了通过活性定量的条件培养基中的ppt1。
102.图52显示了ppt1蛋白质印迹定量与活性定量之间的相关性。
103.图53显示了ppt1构建体与ci-mpr的结合。
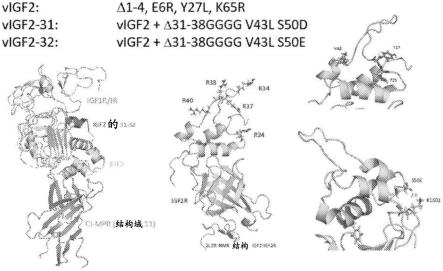
104.图54显示了所选ppt1构建体的结构图。
105.图55显示了分泌到条件培养基中的ppt1的蛋白质印迹。
106.图56显示了通过蛋白质印迹的细胞内的ppt1加工。
107.图57显示了通过蛋白质印迹定量的条件培养基中的ppt1。
108.图58显示了相对ppt1活性。
109.图59显示了ppt1构建体与ci-mpr的结合。
110.图60显示了ppt1构建体与ci-mpr的结合。
111.图61显示了igf2-gaa变体的比对(1:vigf2;2:vigf2-17;3:igf2-20;和4:igf2-22)。
112.图62显示了另外的ppt1构建体。
113.图63(a)显示了ppt1构建体的表达,通过蛋白质印迹上的条带强度测量并相对于野生型、未标记的ppt1(构建体100)而归一化。显示了每个样品的四次重复转染的平均强度,并带有标准偏差误差线。(b)显示了培养基中的ppt1表达/ppt1分泌,通过蛋白质印迹上的条带强度测量并相对于野生型而归一化。
114.图64显示了通过免疫荧光测量的大鼠皮质神经元对ppt1构建体的摄取。(a)显示了纯化的ppt1-101和ppt1-104的神经元摄取。(b)显示了ppt-1构建体从培养基(未纯化)中的神经元摄取。
115.图65显示了另外的naglu构建体。
116.图67(a)显示了naglu构建体的表达,通过蛋白质印迹上的条带强度测量并相对于野生型、未标记的ppt1(构建体100)而归一化。显示了每个样品的四次重复转染的平均强度,并带有标准偏差误差线。(b)显示了培养基中的ppt1表达/ppt1分泌,通过蛋白质印迹上的条带强度测量并相对于野生型而归一化。
117.图68显示了tpp1构建体的表达,通过蛋白质印迹上的条带强度测量并相对于野生型、未标记的tpp1而归一化。
118.图69显示了tpp1构建体的cimpr结合。
119.图70显示了如通过rt-qpcr检测的人cln1转基因表达。
120.图71-72显示了脑自发荧光贮积物质(asm)积聚,其为溶酶体功能障碍的相关因素。
121.图73显示了胶质原纤维酸性蛋白(gfap),其为星形胶质细胞增生和神经炎症的相关因素。
具体实施方式
122.本文提供了新型工程化igf2肽,其具有增强的特性,包括增强的表达、分泌和cimpr结合。本文进一步提供了融合蛋白和编码融合蛋白的核酸,这些融合蛋白包含新型igf2肽和溶酶体酶,具有增强的特性,例如增加的cimpr结合和改善的表达和分泌。本文提供的融合蛋白和核酸构建体可用于酶替代疗法和基因疗法两者来治疗溶酶体贮积症。
123.单基因遗传障碍的基因疗法为疾病和障碍提供了潜在的一次性治疗,其中一些疾病和障碍具有破坏性症状,这些症状可能在生命早期出现并且有时会导致终身残疾。遗传障碍(例如神经障碍或溶酶体贮积症)通常用酶替代疗法治疗,酶替代疗法向患者施用治疗性蛋白质,该治疗性蛋白质是处于疾病或障碍状态下有缺陷的或缺乏的蛋白质的活性形式。然而,当前疗法存在挑战,包括频繁的治疗,产生对治疗性蛋白质的免疫应答,以及难以将治疗性蛋白质靶向受影响的组织、细胞或亚细胞区室。基因疗法的优势包括减少治疗次数和持久疗效。
124.本文提供了用于作为酶替代疗法施用或由基因疗法载体编码的融合蛋白,其提供对酶替代疗法或基因疗法的改善,例如在需要时提供更多的治疗性蛋白质,从而提高治疗功效。在本文中通过改善治疗性蛋白质的表达和细胞摄取或递送以及细胞内或亚细胞靶向解决了此类挑战。本文提供的特定工具或组分包括但不限于用于增加分泌的信号肽(例如,免疫球蛋白结合蛋白(bip)和gaussia信号肽)和增加治疗性蛋白质内吞作用的肽(例如,以高亲和力结合ci-mpr以增加细胞摄取和溶酶体递送的肽)。此类肽与由基因疗法载体编码的治疗性蛋白质融合。在一些实施例中,肽是igf2(胰岛素样生长因子2)肽或其变体。在一些实施例中,本文提供的基因疗法载体预期包含编码治疗性蛋白质的核酸,该治疗性蛋白质与以高亲和力结合ci-mpr的肽融合以优化基因疗法的功效。
125.设计了用于酶替代基因疗法的基因疗法构建体。翻译起始序列,包括但不限于kozak序列或ires序列(例如crpv ires),位于构建体的5’端,其后是编码信号肽的核酸,该信号肽选自下列中的一者或多者:gaa信号肽、编码抗胰蛋白酶抑制剂的核酸和编码bip序列的核酸。随后是编码细胞靶向结构域的核酸,该结构域可以是vigf-2、hirmab或tfrmab或其他细胞靶向肽或蛋白质。该基因疗法构建体进一步包含编码接头的核酸和编码校正酶或其酶活性片段的核酸,其中接头将细胞靶向结构域连接至校正酶或其酶活性片段。合适的校正酶包括但不限于α-葡糖苷酶(gaa)、α-半乳糖苷酶(gla)、艾杜糖苷酶(idua)、艾杜糖苷酸-2-硫酸酯酶(ids)、ppt1、tpp1、naglu或其酶活性片段,以及发现在个体中缺乏的其他酶。治疗性蛋白质的细胞内靶向
126.大多数溶酶体蛋白的n连接碳水化合物经过修饰而含有称为6-磷酸甘露糖(m6p)的特殊碳水化合物结构。m6p是一种生物信号,其能够通过膜结合的m6p受体将溶酶体蛋白转运至溶酶体。溶酶体贮积症的酶替代疗法利用m6p受体来摄取治疗性蛋白质并递送至溶酶体。某些治疗剂不利用m6p受体,包括和其他形式的重组人gcase,而是利用能够结合蛋白聚糖末端甘露糖并递送至溶酶体的甘露糖受体。某些酶替代治疗剂面临的问题是酶治疗剂中存在少量的m6p,这需要更高的剂量来达到治疗效果。这导致输注时间实质上更长,对治疗剂产生免疫应答的可能性更高,以及更高的药物需求,需要增加蛋白质制造,从而导致成本增加。
127.ci-mpr从循环中捕获含有m6p的溶酶体酶。该受体具有针对m6p和胰岛素样生长因子的不同结合结构域(结构域1-3和7-9,参见图2),且因此也称为igf2/甘露糖-6-磷酸受体或igf2/ci-mpr。可利用该受体靶向含有m6p或igf2或igf2变体的酶替代治疗剂。该受体对这些配体(包括胰岛素样生长因子)的结合亲和力在表1中提供。值得注意的是,igf2肽对ci-mpr具有高于单磷酸化寡糖或双磷酸化寡糖的结合亲和力。
128.因此,在一些实施例中,需要设计改善的变体igf2(vigf2)肽用于制备具有增加的稳定性、ci-mpr结合、细胞摄取和溶酶体定位的治疗性融合蛋白,例如在治疗诸如溶酶体贮积症等疾病中。
129.在一些实施例中,该变体vigf2具有改善的与ci-mpr的结合,ci-mpr负责细胞摄取igf2并将其递送至溶酶体以降解。一些变体igf2肽对胰岛素样生长因子受体1(igf1r)具有降低的亲和力。在一些实施例中,igf2对整合素的亲和力降低或没有亲和力。在一些实施例中,igf2还对至少一种胰岛素样生长因子结合蛋白(igfbp1-6)具有降低的亲和力或没有亲和力。在一些实施例中,igf2变体对肝素具有降低的结合或没有结合。在一些实施例中,igf2变体
130.设计vigf2肽的目标是改善vigf2的生物物理特性并增强与ci-mpr的结合/细胞摄取和溶酶体递送,同时最大限度地减少其他功能。因此,vigf2肽可以(1)提高vigf2的稳定性/溶解度;(2)减弱对ir/igf1r/整合素的结合亲和力;以及(3)提高对ci-mpr的结合亲和力。在一些实施例中,使用结构指导的理性设计来设计vigf2肽,识别关键残基与可有可无的残基、点突变和截短。在一些实施例中,使用包括系统突变研究的计算机计算的实验设计vigf2肽,以确定给定突变是否影响对各种结合配偶体的稳定性和亲和力、丙氨酸扫描诱变(namd)和/或改善igf2溶解度、生物利用度和/或降低免疫原性。在一些实施例中,通过基于分裂-gfp测定的定向进化设计vigf2肽。在一些实施例中,通过基于噬菌体展示的定向进化设计vigf2肽。
131.在一些实施例中,使用包括系统突变研究的计算机计算的实验设计vigf2肽,以确定给定突变是否影响igf2肽的稳定性。在一些实施例中,具有突变的肽的稳定性与野生型igf2相比相同或增加。
132.在一些实施例中,设计vigf2肽以减少与整合素的结合。在一些实施例中,与整合素结合减少的vigf2肽包含突变r24e/r34e、r24e/r37e/r38e、r34e/r37e/r38e、r24e/r37e、r24e/r38e或r24e/r34e/r37e/r38e。在一些实施例中,vigf2肽与整合素和肝素具有降低的结合,例如残基r37、r38或r40的突变。
133.在一些实施例中,突变t16i、t16v、t16l、t16f、t16y或t16w增加vigf2与ci-mpr的结合。在一些实施例中,突变t16v或t16y增加vigf2与ci-mpr的结合。在一些实施例中,d23
38gggg),并且这些vigf2肽中的一些进一步含有v43l和s50e或s50d突变。(seq id no:120-121)。在一些实施例中,与seq id no:120-121有至少95%同一性的vigf2肽增强治疗性蛋白质的表达和/或分泌。在一些实施例中,治疗性蛋白质是ppt1或tpp1或其酶活性片段。用于基因疗法的治疗性融合蛋白
140.本文提供了由基因疗法载体产生的治疗性融合蛋白。在一些实施例中,该融合蛋白由用编码融合蛋白的基因疗法载体转导的细胞分泌。在一些实施例中,这些转导的细胞在组织或器官(例如,肝脏)内。一旦从细胞中分泌出来,该融合蛋白就会通过患者的血管系统转运并到达目标组织。在一些实施例中,该治疗性融合蛋白经过工程化以具有改善的分泌。在一些实施例中,与相应的治疗性蛋白质或包含仅具有原生信号肽的治疗性蛋白质的融合蛋白相比,该融合蛋白包含用于提高分泌水平的信号肽。
141.在一些实施例中,所提供的基因疗法载体经过工程化以改善治疗性蛋白质的递送。例如,在某些情况下,如果将不足量的治疗性蛋白质递送到需要治疗性蛋白质的细胞中(例如,由于物理和/或生物屏障阻碍治疗性蛋白质分布到需要的部位),仅通过在患者体内产生足够量的治疗性蛋白质,基因疗法可能无法实现预期的治疗。因此,即使基因疗法能够用高浓度的治疗性蛋白质将血液或组织充斥到饱和点,基因疗法也可能不足以治疗。此外,非生产性清除途径可能会去除绝大多数治疗性蛋白质。即使治疗性蛋白质从脉管系统转运到组织(例如肌纤维)内的间质空间,也不能保证足够的治疗效果。为了有效治疗溶酶体贮积症,治疗有效量的治疗性蛋白质必须经历细胞内吞作用和溶酶体递送以产生有意义的功效。本披露内容通过提供编码融合蛋白的基因疗法载体解决了这些问题,这些融合蛋白包含能够使治疗性蛋白质内吞到靶细胞中用于治疗的肽,从而产生有效的治疗。在一些实施例中,能够进行内吞作用的肽是结合ci-mpr的肽。在一些实施例中,结合ci-mpr的肽是vigf2肽。已知重组表达的gla充分磷酸化并因此与cimpr结合,但令人惊讶的是,在小鼠中表达的gla磷酸化不足并且与cimpr结合不佳。因此,用于基因疗法的gla出人意料地需要另外的工程化来增强cimpr结合(例如igf2标签)。
142.本文提供了编码融合蛋白的基因疗法载体,这些融合蛋白包含能够使治疗性蛋白质内吞到靶细胞中用于治疗的肽。在一些实施例中,基因疗法载体编码包含治疗性蛋白质和结合ci-mpr的肽的融合蛋白。当从基因疗法载体表达时,此类融合蛋白将治疗性蛋白质(例如酶替代治疗剂)靶向到需要它们的细胞,增加此类细胞的递送或细胞摄取并将治疗性蛋白质靶向亚细胞位置(例如,溶酶体)。在一些实施例中,该肽是igf2肽或其变体,其可以将治疗性蛋白质靶向溶酶体。在一些实施例中,本文的融合蛋白还进一步包含增加分泌的信号肽,例如bip信号肽或gaussia信号肽。在一些实施例中,融合蛋白包含接头序列。在一些实施例中,编码本文融合蛋白的核酸包含内部核糖体进入序列。用于酶替代疗法的治疗性融合蛋白
143.本文提供了为酶替代疗法产生的治疗性融合蛋白。在一些实施例中,所提供的融合蛋白经过工程化以改善治疗性蛋白质的递送。例如,在某些情况下,如果将不足量的治疗性融合蛋白递送到需要治疗性蛋白质的细胞中(例如,由于物理和/或生物屏障阻碍治疗性蛋白质分布到需要的部位),则融合蛋白可能无法实现预期的治疗。即使治疗性蛋白质从脉管系统转运到组织(例如肌纤维)内的间质空间,也不能保证足够的治疗效果。为了有效治疗溶酶体贮积症,治疗有效量的治疗性蛋白质必须经历细胞内吞作用和溶酶体递送以产生
有意义的功效。本披露内容通过提供融合蛋白来解决这些问题,这些融合蛋白包含能够使治疗性蛋白质内吞到靶细胞中用于治疗的肽,从而产生有效的治疗。在一些实施例中,能够进行内吞作用的肽是结合ci-mpr的肽。在一些实施例中,结合ci-mpr的肽是vigf2肽。
144.本文提供了包含能够使治疗性蛋白质内吞到靶细胞中用于治疗的肽的融合蛋白。在一些实施例中,融合蛋白包含结合ci-mpr的肽。此类融合蛋白用作酶替代治疗剂,具有增加的递送到需要此类蛋白质的细胞中或被细胞摄取的能力,并将治疗性蛋白质靶向亚细胞位置(例如,溶酶体)。在一些实施例中,该肽是igf2肽或其变体,其可以将治疗性蛋白质靶向溶酶体。
145.本文提供了包含vigf2肽的用于酶替代疗法或基因疗法的治疗性蛋白质。示例性蛋白质在下表2中提供。
146.本文提供的融合蛋白的组分在下文进一步描述。结合ci-mpr的肽(例如,vigf2肽)
147.本文提供了结合ci-mpr的肽。包含此类肽和治疗性蛋白质的融合蛋白当从基因疗法载体表达时将治疗性蛋白质靶向至需要的细胞,增加此类细胞的细胞摄取并将治疗性蛋
白质靶向至亚细胞位置(例如,溶酶体)。在一些实施例中,该肽融合到治疗性肽的n末端。在一些实施例中,该肽融合到治疗性肽的c末端。在一些实施例中,该肽是vigf2肽。一些vigf2肽保持与ci-mpr的高亲和力结合,而它们对igf1受体、胰岛素受体和igf结合蛋白(igfbp)的亲和力降低或消除。一些vigf2肽增加与ci-mpr结合的亲和力。因此,与wt igf2相比,一些变体igf2肽实质上更具选择性并且具有降低的安全风险。本文的vigf2肽包括具有seq id no:31、120和121的氨基酸序列的那些肽。变体igf2肽进一步包括与wt igf2(seq id no:68)相比在位置6、26、27、31-38、43、48、49、50、54、55或65处具有变体氨基酸的那些肽。在一些实施例中,该vigf2肽具有如下序列,该序列具有来自由e6r、f26s、y27l、v43l、f48t、r49s、s50e、s50i、a54r、l55r和k65r组成的组的一个或多个取代。在一些实施例中,该vigf2肽具有如下序列,该序列具有e6r取代。在一些实施例中,该vigf2肽具有如下序列,该序列具有f26s取代。在一些实施例中,该vigf2肽具有如下序列,该序列具有y27l取代。在一些实施例中,该vigf2肽具有如下序列,该序列具有v43l取代。在一些实施例中,该vigf2肽具有如下序列,该序列具有f48t取代。在一些实施例中,该vigf2肽具有如下序列,该序列具有r49s取代。在一些实施例中,该vigf2肽具有如下序列,该序列具有s50i取代。在一些实施例中,该vigf2肽具有如下序列,该序列具有s50e取代。在一些实施例中,序列具有s50e取代的vigf2肽与ci-mpr的结合增加。在一些实施例中,该vigf2肽具有如下序列,该序列具有a54r取代。在一些实施例中,该vigf2肽具有如下序列,该序列具有l55r取代。在一些实施例中,该vigf2肽具有如下序列,该序列具有k65r取代。在一些实施例中,该vigf2肽具有如下序列,该序列具有e6r、f26s、y27l、v43l、f48t、r49s、s50i、a54r和l55r取代。在一些实施例中,该vigf2肽具有n末端缺失。在一些实施例中,该vigf2肽具有一个氨基酸的n末端缺失。在一些实施例中,该vigf2肽具有两个氨基酸的n末端缺失。在一些实施例中,该vigf2肽具有三个氨基酸的n末端缺失。在一些实施例中,该vigf2肽具有四个氨基酸的n末端缺失。在一些实施例中,该vigf2肽具有四个氨基酸的n末端缺失以及e6r、y27l和k65r取代。在一些实施例中,该vigf2肽具有四个氨基酸的n末端缺失以及e6r和y27l取代。在一些实施例中,该vigf2肽具有五个氨基酸的n末端缺失。在一些实施例中,该vigf2肽具有六个氨基酸的n末端缺失。在一些实施例中,该vigf2肽具有七个氨基酸的n末端缺失。在一些实施例中,该vigf2肽具有七个氨基酸的n末端缺失以及y27l和k65r取代。在一些实施例中,与seq id no:80相比,seq id no:83提高了cimpr结合的bmax。
内部核糖体进入序列
148.本文提供了可用于治疗障碍的基因疗法构建体,其进一步包含内部核糖体进入序列(ires),用于通过绕过翻译起始的瓶颈来增加基因表达。供基因疗法用于优化表达的合适的内部核糖体进入序列包括但不限于蟋蟀麻痹病毒(crpv)ires、小核糖核酸病毒ires、口蹄疫病毒ires、卡波西肉瘤(kaposi’s sarcoma)相关疱疹病毒ires、甲型肝炎ires、丙型肝炎ires、瘟病毒属(pestivirus)ires、蟋蟀麻痹病毒属(cripavirus)ires、禾谷缢管蚜(rhopalosiphum padi)病毒ires、默克病(merek’s disease)病毒ires以及其他合适的ires序列。在一些实施例中,基因疗法构建体包含crpv ires。在一些实施例中,crpv ires具有aaaaatgtgatcttgcttgtaaatacaattttgagaggttaataaattacaagtagtgctatttttgtatttaggttagctatttagctttacgttccaggatgcctagtggcagccccacaatatccaggaagccctctctgcggtttttcagattaggtagtcgaaaaacctaagaaatttacctgct的核酸序列(seq id no:191)。在一些实施例中,crpv ires序列与seq id no:191有至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%同一性。信号肽
149.在一些实施例中,本文提供的基因疗法构建体进一步包含信号肽,其改善治疗性蛋白质从用基因疗法构建体转导的细胞中的分泌。在一些实施例中,信号肽改善治疗性蛋
白质的蛋白质加工并且促进初生多肽-核糖体复合物向er易位,并且确保正确的共翻译和翻译后修饰。在一些实施例中,信号肽位于(i)翻译起始序列和治疗性蛋白质之间或(ii)治疗性蛋白质的下游位置。可用于基因疗法构建体的信号肽包括但不限于来自hsp70蛋白家族(例如,hspa5,热休克蛋白家族a成员5)的免疫球蛋白结合蛋白(bip)信号肽和gaussia信号肽、及其变体。这些信号肽对信号识别颗粒具有超高的亲和力。bip和gaussia氨基酸序列的实例提供于下表5中。在一些实施例中,信号肽具有与选自由seq id no:169-180组成的组的序列有至少90%、95%、96%、97%、98%或99%同一性的氨基酸序列。在一些实施例中,信号肽与选自由seq id no:169-180组成的组的序列相差5个或更少、4个或更少、3个或更少、2个或更少、或1个氨基酸。在一些实施例中,使用原生信号肽,在本文中可互换地称为溶酶体蛋白的“内源信号肽”。。
150.bip信号肽-信号识别粒子(srp)相互作用促进向er易位。图20中说明了这种相互作用。
151.gaussia信号肽来源于来自海洋桡脚类动物(gaussia princeps)的荧光素酶,并引导与该信号肽融合的治疗性蛋白质的蛋白质合成和分泌增加。在一些实施例中,gaussia信号肽具有与seq id no:174有至少90%、95%、96%、97%、98%或99%同一性的氨基酸序
列。在一些实施例中,信号肽与seq id no:174相差5个或更少、4个或更少、3个或更少、2个或更少、或1个氨基酸。接头
152.在一些实施例中,本文提供的基因疗法构建体包含靶向肽和治疗性蛋白质之间的接头。在一些实施例中,此类接头保持正确的间距并减轻vigf2肽和治疗性蛋白质之间的空间冲突。在一些实施例中,接头包含重复的甘氨酸残基、重复的甘氨酸-丝氨酸残基及其组合。在一些实施例中,接头由5-20个氨基酸、5-15个氨基酸、5-10个氨基酸、8-12个氨基酸或约5、6、7、8、9、10、11、12或13个氨基酸组成。用于本文的基因疗法和酶替代疗法构建体的合适接头包括但不限于下表6中提供的那些接头。翻译起始序列
153.本文提供的基因疗法构建体包含具有翻译起始序列(例如有助于mrna翻译起始的kozak序列)的核酸。本文考虑的kozak序列具有(gcc)rccatgg的共有序列,其中小写字母表示所述位置处最常见的碱基,并且所述碱基变化,大写字母指示仅变化很少的高度保守的碱基。r指示在所述位置处始终观测到嘌呤(腺嘌呤或鸟嘌呤)。括号中的序列(gcc)具有不确定的意义。在一些实施例中,kozak序列包含序列ax1x2atga,其中x1和x2中的每一个是任何核苷酸。在一些实施例中,x1包含a。在一些实施例中,x2包含g。在一些实施例中,kozak序列包含与aagatga有至少85%同一性的核酸序列。在一些实施例中,kozak序列与aagatga序列相差一个或两个核苷酸。在一些实施例中,本文提供的kozak序列具有aagatga序列。在一些实施例中,kozak序列包含与gcaagatg有至少85%同一性的核酸序列。在一些实施例中,kozak序列与gcaagatg序列相差一个或两个核苷酸。在一些实施例中,kozak序列包含gcaagatg。在一些实施例中,kozak序列包含与caccatg有至少85%同一性的核酸序列。在一些实施例中,kozak序列与caccatg序列相差一个或两个核苷酸。在一些实施例中,kozak序列包含caccatg。治疗性蛋白质
154.本文提供的基因疗法构建体包含编码治疗性蛋白质的核酸,该治疗性蛋白质用于治疗由于个体遗传缺陷导致的蛋白质缺失或缺陷而引起的遗传障碍。从基因疗法构建体表达的治疗性蛋白质替代缺失或有缺陷的蛋白质。因此,基于个体中需要治疗的遗传缺陷来选择治疗性蛋白质。在一些实施例中,该治疗性蛋白质是结构蛋白。在一些实施例中,该治
疗性蛋白质是酶。在一些实施例中,该治疗性蛋白质是调节蛋白。在一些实施例中,该治疗性蛋白质是受体。在一些实施例中,该治疗性蛋白质是肽激素。在一些实施例中,该治疗性蛋白质是细胞因子或趋化因子。
155.在一些实施例中,本文的基因疗法构建体编码酶,例如患有溶酶体贮积症的个体中具有遗传缺陷的酶。在一些实施例中,基因疗法构建体编码溶酶体酶,例如糖苷酶、蛋白酶或硫酸酯酶。在一些实施例中,由本文提供的基因疗法构建体编码的酶包括但不限于α-d-甘露糖苷酶;n-天冬氨酰-β-氨基葡糖苷酶;β-半乳糖苷酶;神经酰胺酶;岩藻糖苷酶;半乳糖脑苷脂酶;芳基硫酸酯酶a;n-乙酰氨基葡萄糖-1-磷酸转移酶;艾杜糖硫酸酯酶;n-乙酰氨基葡糖苷酶;乙酰辅酶a:α-氨基葡萄糖乙酰转移酶;n-乙酰氨基葡萄糖6-硫酸酯酶;β-葡糖醛酸糖苷酶;透明质酸酶;唾液酸酶;硫酸酯酶;鞘磷脂酶;酸性β-甘露糖苷酶;组织蛋白酶k;β-己糖胺酶a;β-己糖胺酶b;α-n-乙酰半乳糖胺酶;唾液素(sialin);己糖胺酶a;β-葡萄糖苷酶;α-艾杜糖苷酶;α-半乳糖苷酶a;β-葡萄糖脑苷脂酶;溶酶体酸性脂肪酶;糖胺聚糖α-l-艾杜糖醛酸水解酶;艾杜糖醛酸-2-硫酸酯酶;n-乙酰半乳糖胺-6-硫酸酯酶;糖胺聚糖n-乙酰半乳糖胺4-硫酸酯酶;α-葡萄糖苷酶;乙酰肝素磺胺酶;nadph氧化酶的gp-91亚基;腺苷脱氨酶;细胞周期蛋白依赖性激酶样5;和棕榈酰蛋白硫酯酶1。在一些实施例中,由本文提供的基因疗法构建体编码的酶包括α-葡糖苷酶。在一些实施例中,治疗性蛋白质与选自由以下组成的组的遗传障碍相关:囊性纤维化、α-和β-地中海贫血、镰状细胞性贫血、马方综合征(marfan syndrome)、脆性x综合征、亨廷顿病、血色素沉着病、先天性耳聋(非综合征型)、泰-萨克斯病、家族性高胆固醇血症、迪谢内肌营养不良(duchenne muscular dystrophy)、眼底黄色斑点症(stargardt disease)、厄舍综合征(usher syndrome)、无脉络膜、全色盲、x-连锁视网膜劈裂症(x-linked retinoschisis)、血友病、威斯科特-奥尔德里奇综合征(wiskott-aldrich syndrome)、x连锁慢性肉芽肿病、芳香族l-氨基酸脱羧酶缺乏症、隐性营养不良型大疱性表皮松解症、α1抗胰蛋白酶缺乏症、哈钦森-吉尔福德早衰综合征(hutchinson-gilford progeria syndrome,hgps)、努南综合征(noonan syndrome)、x连锁重症联合免疫缺陷(x-scid)。
156.基因疗法载体实例基因疗法载体和组合物
157.本文提供了基因疗法载体,其中核酸(例如dna)编码治疗性融合蛋白(例如vigf2融合物,任选地具有信号肽)。该基因疗法载体任选地包含内部核糖体进入序列。源自逆转录病毒(例如慢病毒)的载体是实现长期基因转移的合适工具,因为它们允许转基因的长期、稳定整合及其在子细胞中的繁殖。慢病毒和腺相关病毒载体与源自肿瘤逆转录病毒(例如鼠白血病病毒)的载体相比具有额外优势,因为它们能够转导非增殖细胞,例如肝细胞和神经元。它们还具有低免疫原性的额外优势。
158.本文的示例性基因疗法载体编码治疗性蛋白质和包含vigf2肽的治疗性融合蛋白。编码示例性融合蛋白氨基酸序列的核酸在下表7中提供。
159.在一些实施例中,本文提供的载体是腺相关病毒载体(a5/35),该载体包含编码所需治疗性融合蛋白(例如vigf2融合物或信号肽融合物,任选地具有内部核糖体进入序列)的核酸。
160.在一些实施例中,编码治疗性融合蛋白(例如vigf2融合物)的核酸任选地具有内部核糖体进入序列并且可以克隆到各种类型的载体中。例如,在一些实施例中,将核酸克隆到包括但不限于质粒、噬菌粒、噬菌体衍生物、动物病毒和黏粒的载体中。目标载体包括表达载体、复制载体、探针生成载体和测序载体。
161.此外,在一些实施例中,编码治疗性融合蛋白(例如vigf2融合物或信号肽融合物,任选地具有内部核糖体进入序列)的表达载体以病毒载体的形式提供给细胞。例如,在sambrook等人,2012,molecular cloning:a laboratory manual[分子克隆:实验室手册],第1-4卷,纽约冷泉港出版社,以及其他病毒学和分子生物学手册中描述了病毒载体技术。可用作载体的病毒包括但不限于逆转录病毒、腺病毒、腺相关病毒、疱疹病毒和慢病毒。一般而言,合适的载体含有在至少一种生物体中行使功能的复制起点、启动子序列、方便的限制性内切核酸酶位点以及一种或多种选择性标记(例如,wo 01/96584;wo 01/29058;和美国专利号6,326,193)。
[0162]
本文还提供了用于基因转移的组合物和系统。已经开发了许多基于病毒的系统,用于将基因转移到哺乳动物细胞中。例如,逆转录病毒为基因递送系统提供了方便的平台。在一些实施例中,将选定的基因插入载体中并使用合适的技术包装在逆转录病毒颗粒中。然后分离重组病毒,并且将其在体内或离体递送到受试者的细胞。许多逆转录病毒系统适用于基因疗法。在一些实施例中,使用腺病毒载体。许多腺病毒载体适用于基因疗法。在一些实施例中,使用腺相关病毒载体。许多腺相关病毒适用于基因疗法。在一个实施例中,使用慢病毒载体。
[0163]
本文提供的基因疗法构建体包含如下载体(或基因疗法表达载体),目标基因被克隆到其中,或以其他方式其以使得该载体的核苷酸序列允许目标基因表达(组成型或以其他方式以某种方式调控)的方式包括目标基因。本文提供的载体构建体包括任何合适的基因表达载体,其能够被递送到目标组织并且将提供目标基因在选定目标组织中的表达。
[0164]
在一些实施例中,该载体是腺相关病毒(aav)载体,因为aav载体有能力穿过血脑屏障并转导神经元组织。在本文提供的方法中,考虑了使用任何血清型的aav。在某些实施例中使用的病毒载体的血清型选自由以下组成的组:aav1载体、aav2载体、aav3载体、aav4
载体、aav5载体、aav6载体、aav7载体、aav8载体、aav9载体、aavrhs载体、aavrh10载体、aavrh33载体、aavrh34载体、aavrh74载体、aav anc80载体、aavphp.b载体、aavhu68载体、aav-dj载体以及适用于基因疗法的其他载体。
[0165]
aav载体是对哺乳动物无致病性的dna细小病毒。简而言之,基于aav的载体移除了占病毒基因组96%的rep和cap病毒基因,留下了用于启动病毒dna复制、包装和整合的两个145个碱基对的侧翼反向末端重复序列(itr)。
[0166]
进一步的实施例包括使用其他血清型衣壳来产生aav1载体、aav2载体、aav3载体、aav4载体、aav5载体、aav6载体、aav7载体、aav8载体、aav9载体、aavrhs载体、aavrh10载体、aavrh33载体、aavrh34载体、aavrh74载体、aav anc80载体、aavphp.b载体、aav-dj载体以及适用于基因疗法的其他载体。任选地,aav病毒衣壳是aav2/9、aav9、aavrhs、aavrh10、aavanc80或aav php.b。
[0167]
另外的启动子元件(例如,增强子)调控转录起始的频率。典型地,这些启动子元件位于起始位点上游30-110bp的区域中,尽管许多启动子已经被证明也含有起始位点下游的功能元件。启动子元件之间的间距通常是灵活的,因此当元件相对于彼此反向或移动时,启动子功能得以保留。在胸苷激酶(tk)启动子中,启动子元件之间的间距通常在活性开始下降之前增加到50bp。取决于启动子,单独元件似乎协同或独立地发挥作用以激活转录。
[0168]
能够使治疗性融合蛋白(例如vigf2融合物或信号肽融合物,任选地具有内部核糖体进入序列)在哺乳动物t细胞中转基因表达的启动子的实例是ef1a启动子。原生ef1a启动子驱动延伸因子-1复合物的α亚基的表达,该复合物负责将氨酰trna酶促递送到核糖体。ef1a启动子已经广泛用于哺乳动物表达质粒中,并且已经被证明可有效驱动克隆到慢病毒载体中的转基因的表达(参见例如,milone等人,mol.ther.[分子疗法]17(8):1453-1464(2009))。启动子的另一个实例是即刻早期巨细胞病毒(cmv)启动子序列。这种启动子序列是一种强组成型启动子序列,其能够驱动与其可操作连接的任何多核苷酸序列的高水平表达。然而,有时也使用其他组成型启动子序列,包括但不限于鸡β肌动蛋白启动子、p546启动子、猿猴病毒40(sv40)早期启动子、小鼠乳腺肿瘤病毒(mmtv)、人免疫缺陷病毒(hiv)长末端重复序列(ltr)启动子、momulv启动子、禽白血病病毒启动子、eb病毒(epstein-barr virus)即刻早期启动子、劳斯肉瘤(rous sarcoma)病毒启动子以及人基因启动子(例如但不限于肌动蛋白启动子、肌球蛋白启动子、延伸因子-1a启动子、血红蛋白启动子和肌酸激酶启动子)。此外,不考虑基因疗法载体仅限于使用组成型启动子。这里还考虑了诱导型启动子。诱导型启动子提供了一种分子开关,其能够在期望表达时开启与其可操作连接的多核苷酸序列的表达,并且在不期望表达时关闭表达。诱导型启动子的实例包括但不限于金属硫蛋白启动子、糖皮质激素启动子、孕酮启动子和四环素调控启动子。
[0169]
为了评估治疗性融合蛋白(例如vigf融合物或信号肽融合物,任选地具有内部核糖体进入序列)或其部分的表达,待引入细胞中的表达载体通常含有选择性标记基因或报告基因或两者,以便于从试图通过病毒载体转染或感染的细胞群中鉴定和选择表达细胞。在其他方面,选择性标记通常携带在单独的dna片段上,并且用于共转染程序。选择性标记和报告基因两者有时均侧接适当的调控序列,以使其能够在宿主细胞中表达。可用的选择性标记包括例如抗生素抗性基因,例如neo等。
[0170]
用于将基因引入细胞中并使其在细胞中表达的方法和组合物适用于本文的方法。
在表达载体的背景下,通过本领域的任何方法将载体容易地引入宿主细胞(例如,哺乳动物细胞、细菌细胞、酵母细胞或昆虫细胞)中。例如,通过物理、化学或生物学手段将表达载体转移到宿主细胞中。
[0171]
用于将多核苷酸引入宿主细胞中的物理方法和组合物包括磷酸钙沉淀、脂质转染、粒子轰击、显微注射、基因枪、电穿孔等。用于产生包含载体和/或外源核酸的细胞的方法适用于本文的方法(参见例如,sambrook等人,2012,molecular cloning:a laboratory manual[分子克隆:实验室手册],第1-4卷,纽约冷泉港出版社)。用于将多核苷酸引入宿主细胞中的一种方法是磷酸钙转染。
[0172]
用于将多核苷酸引入宿主细胞中的化学手段和组合物包括胶体分散系统,例如大分子复合物、纳米胶囊、微球、珠和基于脂质的系统(包括水包油乳剂、胶束、混合胶束、核酸-脂质颗粒和脂质体)。用作体外和体内递送媒介物的示例性胶体系统是脂质体(例如,人造膜囊)。现有技术的核酸靶向递送的其他方法是可用的,例如用靶向型纳米颗粒或其他合适的亚微米大小的递送系统递送多核苷酸。
[0173]
在利用非病毒递送系统的情况下,示例性递送媒介物是脂质体。考虑了使用脂质制剂将核酸引入宿主细胞中(体外、离体或体内)。在另一个方面,该核酸与脂质相关联。在一些实施例中,将与脂质相关联的核酸封装在脂质体的水性内部中、散布在脂质体的脂质双层内、经由与脂质体和寡核苷酸两者相关联的连接分子附着到脂质体、包裹在脂质体中、与脂质体复合、分散在含有脂质的溶液中、与脂质混合、与脂质组合、作为悬浮液包含在脂质中、用胶束包含或复合、或以其他方式与脂质相关联。脂质、脂质/dna或脂质/表达载体相关的组合物不限于溶液中的任何特定结构。例如,在一些实施例中,它们以双层结构、作为胶束或具有“塌缩”结构存在。可替代地,它们简单地散布在溶液中,可能形成大小或形状不均匀的聚集体。脂质是脂肪物质,在一些实施例中,其是天然存在的或合成的脂质。例如,脂质包括天然存在于细胞质中的脂肪滴以及含有长链脂族烃及其衍生物(例如脂肪酸、醇、胺、氨基醇和醛)的化合物类别。
[0174]
适合使用的脂质从商业来源获得。例如,在一些实施例中,二肉豆蔻酰磷脂酰胆碱(“dmpc”)从密苏里州圣路易斯的西格玛公司(sigma)获得;在一些实施例中,磷酸二鲸蜡酯(“dcp”)从k&k实验室(k&k laboratories)(纽约州普莱恩维尤)获得;在一些实施例中,胆固醇(“choi”)从卡尔生化-贝林公司(calbiochem-behring)获得;二肉豆蔻酰磷脂酰甘油(“dmpg”)和其他脂质通常从阿凡提极性脂质制品公司(avanti polar lipids,inc.)(阿拉巴马州伯明翰)获得。通常将脂质在氯仿或氯仿/甲醇中的储备溶液储存在约-20℃下。将氯仿用作唯一的溶剂,因为它比甲醇更容易蒸发。“脂质体”是通用术语,涵盖通过产生封闭的脂质双层或聚集体形成的各种单层和多层脂质媒介物。脂质体通常被表征为具有含有磷脂双层膜和内部水性介质的囊泡结构。多层脂质体具有由水性介质隔开的多个脂质层。当磷脂悬浮在过量的水性溶液中时,它们会自发形成。脂质组分在形成封闭结构之前经历自重排,并且捕获脂质双层之间的水和溶解的溶质(ghosh等人,1991glycobiology[糖生物学]5:505-10)。然而,还涵盖在溶液中具有与正常囊泡结构不同的结构的组合物。例如,在一些实施例中,脂质呈现胶束结构或仅作为脂质分子的不均匀聚集体存在。还考虑了脂转胺(lipofectamine)-核酸复合物。
[0175]
无论用于将外源核酸引入宿主细胞或以其他方式使细胞暴露于本文提供的治疗
性融合蛋白(例如,vigf2融合物或信号肽融合物,任选地具有内部核糖体进入序列)的方法如何,为了确认宿主细胞中存在重组dna序列,考虑进行多种测定。此类测定包括例如适用于本文方法的“分子生物学”测定,例如dna印迹法和rna印迹法、rt-pcr和pcr;“生物化学”测定,例如检测特定肽是否存在,例如通过免疫学手段(elisa和蛋白质印迹)或通过本文所述的测定来鉴定落入本文范围内的药剂。
[0176]
本披露内容进一步提供了载体,其包含编码治疗性融合蛋白(例如vigf2融合物或信号肽融合物,任选地具有内部核糖体进入序列)的核酸分子。在一个方面,该治疗性融合蛋白载体能够被直接转导到细胞中。在一个方面,载体是克隆载体或表达载体,例如包括但不限于一种或多种质粒(例如,表达质粒、克隆载体、微环、微载体、双微染色体)、逆转录病毒和慢病毒载体构建体的载体。在一个方面,载体可以用于在哺乳动物细胞中表达vigf2-治疗性融合蛋白构建体。在一个方面,哺乳动物细胞是人细胞。用途和治疗方法
[0177]
本文还提供了使用基因疗法治疗遗传障碍的方法,该方法包括向个体施用本文披露的核酸,其编码治疗性融合蛋白(例如vigf2融合物或信号肽融合物或信号肽-vigf2融合物),任选地具有内部核糖体进入序列。适合于使用本文方法治疗的遗传障碍包括个体中由基因组中的一个或多个突变引起的障碍,该一个或多个突变导致突变基因缺乏表达或表达功能障碍的蛋白质。
[0178]
本文进一步提供了药物组合物以用于制备用于治疗遗传障碍的药剂,这些药物组合物包含基因疗法载体(例如包含本文披露的核酸的基因疗法载体,该核酸编码治疗性融合蛋白(例如vigf2融合物或信号肽融合物或信号肽-vigf2融合物),任选地具有内部核糖体进入序列)和药学上可接受的载剂或赋形剂。
[0179]
在一些实施例中,适合使用本文提供的方法治疗的遗传障碍是溶酶体贮积症。在一些实施例中,在本文中使用基因疗法将缺失或有缺陷的酶递送至患者来治疗溶酶体贮积症。在一些实施例中,本文的方法将与vigf2融合或与信号肽融合的酶递送至患者,以便将酶递送至需要的细胞。在一些实施例中,溶酶体贮积症选自由以下组成的组:天冬氨酰葡糖胺尿症、巴滕病、胱氨酸病、法布里病、i型戈谢病、ii型戈谢病、iii型戈谢病、庞贝病、泰-萨克斯病、桑德霍夫病、异染性脑白质营养不良、i型黏脂贮积病、ii型黏脂贮积病、iii型黏脂贮积病、iv型黏脂贮积病、贺勒病、亨特病、a型圣菲利波病、b型圣菲利波病、c型圣菲利波病、d型圣菲利波病、a型莫基奥病、b型莫基奥病、马罗托-拉米病、斯莱病、a型尼曼-皮克病、b型尼曼-皮克病、c1型尼曼-皮克病、c2型尼曼-皮克病、i型辛德勒病和ii型辛德勒病。在一些实施例中,溶酶体贮积症选自由以下组成的组:激活剂缺乏症、gm2-神经节苷脂沉积症;ab变异型gm2-神经节苷脂沉积症;α-甘露糖苷沉积症(2型,中度形式;3型,新生儿期,重度);β-甘露糖苷沉积症;天冬氨酰葡糖胺尿症;溶酶体酸性脂肪酶缺乏症;胱氨酸病(迟发性青少年或青春期少年肾病型;婴儿肾病型);查纳林-多夫曼(chanarin-dorfman)综合征;伴有肌病的中性脂质贮积病;nlsdm;达农病(danon disease);法布里病;ii型法布里病,迟发性;法伯病(farber disease);法伯脂肪肉芽肿病;岩藻糖苷沉积症;半乳糖唾液酸沉积症(联合神经氨酸酶和β-半乳糖苷酶缺乏症);戈谢病;ii型戈谢病;iii型戈谢病;iiic型戈谢病;由于鞘脂激活蛋白c缺乏所致的非典型戈谢病;gm1-神经节苷脂沉积症(晚期婴儿型/青少年型gm1-神经节苷脂沉积症;成人型/慢性gm1-神经节苷脂沉积症);球形细胞脑白质
营养不良、克拉伯病(krabbe disease)(婴儿晚期发病型;青少年发病型;成人发病型);由于鞘脂激活蛋白a缺乏所致的非典型克拉伯病;异染性脑白质营养不良(青少年型;成人型);部分硫酸脑苷脂缺乏症;假芳基硫酸酯酶a缺乏症;由于鞘脂激活蛋白b缺乏引起的异染性脑白质营养不良;黏多糖贮积症:mps i,贺勒综合征;mps i,贺勒-谢伊综合征(hurler-scheie syndrome);mps i,谢伊综合征;mps ii,亨特综合征;mps ii,亨特综合征;a型圣菲利波综合征/mps iiia;b型圣菲利波综合征/mps iiib;c型圣菲利波综合征/mps iiic;d型圣菲利波综合征/mps iiid;a型莫基奥综合征/mps iva;b型莫基奥综合征/mps ivb;mps ix透明质酸酶缺乏症;mps vi马罗托-拉米综合征;mps vii斯莱综合征;i型黏脂贮积病,ii型唾液酸贮积症;包涵体细胞病(i-cell disease)、勒罗伊病(leroy disease)、ii型黏脂贮积病;假性贺勒多发性营养不良/iii型黏脂贮积病;iiic型黏脂贮积病/ml iiiγ;iv型黏脂贮积病;多种硫酸酯酶缺乏症;尼曼-皮克病(b型;c1型/慢性神经元病形式;c2型;d型/新斯科舍(nova scotian)型);神经元蜡样质脂褐质沉积症:cln6病-非典型晚期婴儿型,迟发变异型,早期青少年型;巴顿-斯皮尔迈耶-沃格特(batten-spielmeyer-vogt)/青少年型ncl/cln3病;芬兰变异型晚期婴儿型cln5;詹斯基-比尔朔夫斯基(jansky-bielschowsky)病/晚期婴儿型cln2/tpp1病;库夫斯(kufs)/成人发病型ncl/cln4病(b型);北方癫痫(northern epilepsy)/变异型晚期婴儿型cln8;桑塔沃里-哈尔蒂亚(santavuori-haltia)/婴儿型cln1/ppt病;庞贝病(ii型糖原贮积病);迟发性庞贝病;致密骨成骨不全;桑德霍夫病/gm2神经节苷脂沉积症;桑德霍夫病/gm2神经节苷脂沉积症;桑德霍夫病/gm2神经节苷脂沉积症;辛德勒病(iii型/中间型,可变);神崎病(kanzaki disease);萨拉病(salla disease);婴儿型游离唾液酸贮积病(issd);脊髓性肌萎缩伴进行性肌阵挛性癫痫(smapme);泰-萨克斯病/gm2神经节苷脂沉积症;青少年发病型泰-萨克斯病;迟发性泰-萨克斯病;克里斯蒂安森综合征(christianson syndrome);勒韦眼脑肾综合征(lowe oculocerebrorenal syndrome);4j型夏科-马里-图思病(charcot-marie-tooth)、cmt4j;尤尼斯-瓦隆综合征(yunis-varon syndrome);双侧颞枕多小脑回(btop);x连锁高钙尿性肾结石,1型登特病(dent-1);和2型登特病。在一些实施例中,该治疗性蛋白质与溶酶体贮积症相关,并且该治疗性蛋白质选自由以下组成的组:gm2-激活蛋白;α-甘露糖苷酶;man2b1;溶酶体β-甘露糖苷酶;糖基天冬酰胺酶;溶酶体酸性脂肪酶;胱氨酸转运蛋白(cystinosin);ctns;pnpla2;溶酶体相关膜蛋白-2;α-半乳糖苷酶a;gla;酸性神经酰胺酶;α-l-岩藻糖苷酶;保护性蛋白/组织蛋白酶a;酸性β-葡糖苷酶;gba;psap;β-半乳糖苷酶-1;glb1;半乳糖神经酰胺β-半乳糖苷酶;galc;psap;芳基硫酸酯酶a;arsa;α-l-艾杜糖苷酶;艾杜糖醛酸2-硫酸酯酶;乙酰肝素n-硫酸酯酶;n-α-乙酰氨基葡糖苷酶;乙酰肝素乙酰辅酶a:α-氨基葡萄糖乙酰转移酶;n-乙酰氨基葡萄糖6-硫酸酯酶;半乳糖胺-6
‑‑
硫酸硫酸酯酶;β-半乳糖苷酶;透明质酸酶;芳基硫酸酯酶b;β-葡糖醛酸糖苷酶;神经氨酸酶;neu1;n-乙酰氨基葡萄糖-1-磷酸转移酶的γ亚基;黏脂素-1;硫酸酯酶修饰因子-1;酸性鞘磷脂酶;smpd1;npc1;和npc2。
[0180]
在一些实施例中,经由本文方法进行的治疗将编码治疗性蛋白质的基因递送到需要该治疗性蛋白质的细胞。在一些实施例中,该治疗将基因递送到个体中的所有体细胞。在一些实施例中,该治疗替代靶向细胞中的有缺陷的基因。在一些实施例中,将经离体处理以表达治疗性蛋白质的细胞递送到个体。
[0181]
本文披露的用于障碍的基因疗法提供优于常规治疗方法(包括酶替代疗法)的治疗结果,因为它不需要长时间的输注治疗。定义
[0182]
如本文所用的“离体基因疗法”是指如下方法,在受试者体外对患者细胞进行基因修饰(例如)以表达治疗性基因。然后将具有新遗传信息的细胞回输到其源自的受试者。
[0183]
如本文所用的“体内基因疗法”是指将携带一个或多个治疗性基因的载体直接施用至受试者的方法。
[0184]
如本文所用的“融合蛋白”和“治疗性融合蛋白”在本文中可互换使用,并且是指连接有至少一种另外的蛋白质、肽或多肽的治疗性蛋白质。在一些情形中,融合蛋白是含有两个或更多个蛋白质或其片段的单个蛋白质分子,这些蛋白质或其片段在无化学接头下经由在其各自的肽链内的肽键共价连接。在一些实施例中,该融合蛋白包含治疗性蛋白质以及信号肽、增加该融合蛋白的内吞作用的肽或两者。在一些实施例中,增加内吞作用的肽是结合ci-mpr的肽。
[0185]
如本文所用的“载体”或“基因疗法载体”在本文中可互换使用,是指将治疗性基因递送到细胞的基因疗法递送媒介物或载剂。基因疗法载体是适于在基因疗法中使用的任何载体,例如适用于将核酸聚合物(编码多肽或其变体)治疗性递送到患者靶细胞(例如,感觉神经元)中的任何载体。在一些实施例中,基因疗法载体将编码治疗性蛋白质或治疗性融合蛋白的核酸递送到细胞,其中该治疗性蛋白质或融合蛋白从该细胞表达和分泌。该载体可以是任何类型的,例如它可以是质粒载体或微环dna。典型地,该载体是病毒载体。这些病毒载体包括遗传致残的病毒(例如腺病毒)载体和非病毒载体(例如脂质体)两者。病毒载体可以例如源自腺相关病毒(aav)、逆转录病毒、慢病毒、单纯疱疹病毒或腺病毒。aav源载体。该载体可以包含aav基因组或其衍生物。
[0186]
如本文所用的“构建体”是指核酸分子或序列,其编码治疗性蛋白质或融合蛋白,并且任选地包含另外的序列,例如翻译起始序列或ires序列。
[0187]
如本文所用的“质粒”是指在细胞内独立于染色体dna而复制的环状双链dna单元。
[0188]
如本文所用的“启动子”是指dna上与酶rna聚合酶结合并启动dna转录成rna的位点。
[0189]
如本文所用的“体细胞疗法”是指在细胞中操纵基因表达的方法,这些细胞将对患者进行纠正,但不会被下一代遗传。体细胞包括人体内所有的非生殖细胞
[0190]
如本文所用的“体细胞”是指除了生殖细胞之外的所有身体细胞。
[0191]
如本文所用的“趋向性”是指载体(例如病毒)对于某种细胞或组织类型的偏好。多种因素决定了载体感染特定细胞的能力。例如,病毒必须与特定的细胞表面受体结合才能进入细胞。如果病毒不表达必要的受体,则它们典型地不能感染细胞。
[0192]
术语“转导”用于指经由本披露内容的复制缺陷型raav在体内或体外向靶细胞施用/递送编码治疗性蛋白质的核酸,从而导致由受者细胞表达功能性多肽。用基因疗法载体(例如本披露内容的raav)转导细胞导致由raav编码的多肽或rna的持续表达。因此,本披露内容提供了通过鞘内、视网膜内、眼内、玻璃体内、脑室内、实质内或静脉内途径或其任何组合向受试者施用/递送基因疗法载体(例如编码治疗性蛋白质的raav)的方法。“鞘内”递送是指递送到脑或脊髓蛛网膜下的空间中。在一些实施例中,鞘内施用是经由脑池内施用。本
披露内容还提供了通过鞘内、视网膜内、眼内、玻璃体内、脑室内、实质内或静脉内途径或其任何组合施用/递送已经用基因疗法载体(例如编码治疗性蛋白质的raav载体)离体转导的细胞的方法。
[0193]
术语“受者”、“个体”、“受试者”、“宿主”和“患者”在本文中可互换使用并且在一些情况下,是指需要诊断、治疗或疗法的任何哺乳动物受试者,特别是人。出于治疗目的的“哺乳动物”是指被分类为哺乳动物的任何动物,包括人、家畜和农场动物、以及实验室、动物园、体育运动或宠物动物,例如狗、马、猫、乳牛、绵羊、山羊、猪、小鼠、大鼠、兔、豚鼠、猴等。在一些实施例中,哺乳动物是人。
[0194]
如本文所用,术语“治疗(treatment)”、“治疗(treating)”、“改善症状”等在一些情况下是指出于获得治疗效果的目的而施用药剂或实施程序,该治疗效果包括以统计学显著的方式或以临床显著的方式抑制、减弱、减轻、预防或改变障碍的至少一个方面或标记。术语“改善”或“治疗”并不陈述或暗示潜在病状的治愈。如本文所用的“治疗”或“改善”(等)可以包括治疗哺乳动物,特别是在人中,并且包括:(a)防止障碍或障碍的症状在可能易患障碍但尚未被诊断为患有障碍(例如,包括可能与原发障碍相关或由原发障碍引起的障碍)的受试者中发生;(b)抑制障碍,即遏制其发展;(c)缓解障碍,即引起障碍消退;以及(d)改善障碍的至少一种症状。治疗可以指治疗或改善或预防障碍的任何成功标志,包括任何客观或主观参数,例如消除;缓解;减轻症状或使障碍状况对患者为更可容忍的;减慢退化或衰退的速率;或者使退化的终点不那么虚弱。症状的治疗或改善是基于一个或多个客观或主观参数;包括医生的检查结果。因此,术语“治疗”包括施用本发明的化合物或药剂以预防或延迟、缓解或阻止或抑制与障碍相关的症状或病状的发展。术语“治疗效果”是指减轻、消除或预防受试者的障碍、障碍的症状或障碍的副作用。
[0195]
术语“亲和力”是指分子与其结合配偶体或受体之间的结合强度。
[0196]
如本文所用,短语“高亲和力”是指例如含有这种结合ci-mpr的肽的治疗性融合物,其对ci-mpr的亲和力是不含该肽的治疗性蛋白质的亲和力的约100至1,000倍或500至1,000倍。在一些实施例中,亲和力是没有该肽时的至少100倍、至少500倍或至少1000倍。例如,当治疗性蛋白质和ci-mpr以相对相等的浓度组合时,高亲和力的肽将与可用的ci-mpr结合,以便使平衡向高浓度的所得复合物转移。
[0197]
如本文所用的“分泌”是指蛋白质从细胞释放到(例如)血流中以被运送至目标组织或治疗性蛋白质的作用部位。当基因疗法产物分泌到器官的胞间隙中时,分泌可以允许对邻近细胞进行交叉校正。
[0198]
如本文所用的“递送”意指药物递送。在一些实施例中,递送过程意指将药物物质(例如,从用基因疗法载体转导的细胞产生的治疗性蛋白质或融合蛋白)从细胞外部(例如,血液、组织或胞间隙)运输到靶细胞中以获得药物物质的治疗活性。
[0199]
如这里所用的“工程化”或“蛋白质工程化”是指通过提供适当的编码蛋白质的核酸序列来操纵蛋白质的结构,以产生所期望的特性,或合成具有特定结构的蛋白质。
[0200]
在一些情况下,“治疗有效量”意指在施用至受试者用于治疗障碍时足以实现对该障碍的治疗的量。
[0201]
如本文所用,术语“约”某个数字是指从小于该数字10%到大于该数字10%的范围,并且包括该范围内的值,例如数字本身。
[0202]
如本文所用,术语“包含”技术方案的一个或多个要素是指包括那些要素,但不排除包括另外的一个或多个要素。实例
[0203]
给出以下实例是出于说明本发明的各种实施例的目的,并不意味着以任何方式限制本发明。本发明实例连同本文所述的方法目前代表优选的实施例,是示例性的,并且不意图作为对本发明范围的限制。本领域技术人员将会想到包含在如权利要求的范围所限定的本发明精神内的其中的变化和其他用途。实例1:变体igf2肽与ci-mpr受体的结合
[0204]
使用biacore进行表面等离子体共振(spr)实验以测量野生型igf2和变体igf2(vigf2)与ci-mpr受体的结合。野生型人成熟igf2肽(wt igf2)具有seq id no:68所示的序列。vigf2序列与wt igf2的不同之处在于它缺少残基1-4并含有以下突变:e6r、y27l和k65r。它具有如下氨基酸序列:srtlcggelvdtlqfvcgdrgflfsrpasrvsrrsrgiveeccfrscdlalletycatparse(seq id no:80)。vigf2还带有具有序列ggggsgggg(seq id no:181)的n末端接头。组合序列为ggggsggggsrtlcggelvdtlqfvcgdrgflfsrpasrvsrrsrgiveeccfrscdlalletycatparse。图4显示如预期的那样,野生型igf2肽以高亲和力(0.2nm)与ci-mpr受体结合。图5显示变体igf2肽(vigf2)也以高亲和力(0.5nm)与ci-mpr受体结合。这些数据表明,vigf2肽对预期的ci-mpr受体具有高亲和力,可将治疗剂靶向溶酶体。
[0205]
利用spr测量肽与胰岛素受体的结合,以评估潜在的副作用。胰岛素以高亲和力(约8nm;数据未显示)结合胰岛素受体。测试了野生型igf2和vigf2,其中vigf2具有序列srtlcggelvdtlqfvcgdrgflfsrpasrvsrrsrgiveeccfrscdlalletycatparse(seq id no:80),其带有具有序列ggggsgggg(seq id no:181)的n末端接头。图8显示野生型igf2也以相对高的亲和力(约100nm)结合胰岛素受体。来自拜玛林制药(biomarin)/齐斯特治疗公司(zystor)igf2-gaa融合蛋白(bmn-701)的igf2肽也以高亲和力结合胰岛素受体,并在临床试验中经证明可引起低血糖。图9显示没有可测量的vigf2肽与胰岛素受体的结合。这些数据显示,与wt igf2肽融合物相比,vigf2肽具有更高的安全性。
[0206]
使用相同的spr结合分析来表征vigf2肽与igf1受体的相互作用。图10显示野生型igf2肽以相对高的亲和力(约100nm)结合igf1受体。图11显示没有可测量的vigf2肽与igf1受体的结合,显示出与wt igf2相比改善的安全性。实例2:vigf2将低亲和力配体转化为用于ci-mpr的高亲和力ert
[0207]
将具有n末端接头(seq id no:181)的vigf2肽(seq id no:80)化学偶联至阿糖苷酶-α(在此命名为vigf2-阿糖苷酶-α)以确定vigf2肽是否可以提高对ci-mpr的亲和力。如图6所示,在用ci-mpr包被的96孔板中,使用ci-mpr板结合测定直接比较阿糖苷酶-α和vigf2-阿糖苷酶-α的结合亲和力。在测量结合酶活性之前将未结合的酶洗掉。在有或没有游离wt igf2肽的情况下使用不同浓度的两种酶制剂。vigf2实质上提高了对ci-mpr的亲和力。此外,vigf2-阿糖苷酶-α的结合被游离的wt igf2阻断,此指示结合是igf2依赖性的。
(数据未显示)。vigf2肽的偶联不损害gaa酶活性。
[0208]
将vigf2与重组人n-乙酰基-α-d-氨基葡糖苷酶(rhnaglu)偶联。rrhnaglu为一种缺少m6p的溶酶体酶,其用于确定肽是否可以将非配体转化为ci-mpr的高亲和力配体。在此实验中,利用ci-mpr包被的板,使用ci-mpr板结合测定直接比较rhnaglu和vigf2-rhnaglu。在测量结合酶活性之前将未结合的酶洗掉。在有或没有游离vigf2肽的情况下使用不同浓度的两种酶制剂。如图7所示,vigf2-rhnaglu对ci-mpr的亲和力明显高于缺少vigf2的rhnaglu。此外,vigf2-rhnaglu结合被游离的vigf2肽阻断,此指示受体结合对igf2肽具有特异性。这些结果显示,可利用vigf2肽来提高药物对溶酶体的靶向性。实例3:成肌细胞对vigf2-gaa融合蛋白的摄取
[0209]
施用vigf2-gaa融合蛋白(与实例1-2中相同的序列)并测量l6成肌细胞对酶的摄取。图6显示与rhgaa和m6p-gaa相比,vigf2-rhgaa的摄取更佳。因此,vigf2可有效地将gaa靶向到细胞。实例4:通过基因疗法递送的ert构建体
[0210]
图12中说明了两种不同的构建体。上图是编码“天然hgaa”(seq id no:189)的构建体,其含有kozak序列和编码具有原生信号肽的重组人gaa的核酸。中间图是编码“工程化hgaa”(seq id no:190)的构建体kozak-bip-vigf2-2gs-gaa。该构建体的特征在于kozak序列、编码bip信号肽的核酸、编码具有seq id no:80所示序列的vigf2肽的核酸、以及编码2gs接头(seq id no:181)的核酸,之后是编码重组人gaa(seq id no:1)的核酸,其中去除了n末端60个氨基酸以防止过早的加工和vigf2去除。“工程化hgaa”的氨基酸序列在seq id no:2中示出。实例5:基因疗法构建体的增强分泌
[0211]
工程化hgaa具有更多的分泌,并且能够与适合于细胞摄取和溶酶体靶向的细胞表面受体相互作用培养表达工程化hgaa(下文更详细描述)或天然hgaa的cho并收集条件培养基用于测量gaa活性。图15显示工程化hgaa和天然hgaa的相对活性,此显示工程化hgaa与天然hgaa相比具有增加的活性,表明工程化hgaa的更有效分泌。实例6:条件培养基中ppt1的分析
[0212]
ppt1构建体的克隆将ppt1构建体克隆到含有cmv启动子的pcdna3.1表达载体(赛默飞(thermofisher)目录号v79020)中。测试的构建体包括ppt1-1(wt-ppt1)(seq id no:4);ppt1-2(wt-vigf2-ppt1)(seq id no:5);ppt1-29(bip2aa-vigf2-ppt1)(seq id no:6)。ppt1分泌和结合
[0213]
使ppt1构建体在hek293t细胞中瞬时表达3天并且ppt1分泌到培养基中。通过蛋白质印迹定量分泌的ppt1,并使用已建立的方法测定ci-mpr结合。分泌的ppt1示于图13中。ci-mpr结合示于图14中。
[0214]
实例7:在庞贝病动物模型中测试基因疗法载体
[0215]
庞贝病基因疗法:临床前概念验证研究设计
[0216]
在gaa敲除(gaa ko)小鼠中使用高剂量进行了临床前研究以对构建体进行初步比较。构建体示于图12中。用媒介物或两种构建体(天然hgaa或工程化hgaa)中的一种处理小
鼠。给小鼠施用5e11 gc/小鼠(约2.5e13 gc/kg)。使用2月龄的gaa敲除小鼠。正常(野生型)小鼠用作对照。研究设计在图16中概述。
[0217]
庞贝病基因疗法:血浆
[0218]
如所指示从野生型(正常)小鼠或用媒介物或基因疗法载体处理的gaa ko小鼠收集血浆,并测量gaa活性和细胞表面结合。数据总结在图17、图27和图19中。在用基因疗法载体处理的小鼠中看到类似的高gaa水平(图17,图18)。然而,用工程化构建体观测到更高的细胞靶向受体结合(图19)。
[0219]
庞贝病基因疗法:股四头肌
[0220]
在正常(野生型)小鼠和经处理的gaa ko小鼠中评估gaa活性和糖原贮积/细胞质空泡化(图28)。股四头肌中的gaa活性比野生型高约20倍。还评估了糖原pas(图29)和免疫组织化学(图30)。免疫组织化学显示,与野生型相比,工程化hgaa的溶酶体靶向性更强。通过pas染色,工程化hgaa的糖原减少更一致。
[0221]
庞贝病基因疗法:肱三头肌
[0222]
在正常(野生型)小鼠和经处理的gaa ko小鼠中评估gaa活性和糖原贮积/细胞质空泡化(图31)。gaa活性比野生型高约10-15倍。还评估了免疫组织化学和糖原pas(图32和图33)。免疫组织化学说明,与野生型gaa相比,工程化hgaa的溶酶体靶向性更强。如通过pas染色所测量,工程化hgaa的糖原减少更一致。
[0223]
庞贝病基因疗法:胫骨前肌(ta)
[0224]
在正常(野生型)和经处理的gaa ko小鼠中评估gaa活性和糖原贮积/细胞质空泡化(图20)。ta中的gaa活性比野生型高约15-20倍。还评估了免疫组织化学和糖原pas(图21和图22)。免疫组织化学说明,与野生型gaa相比,工程化hgaa的溶酶体靶向性更强。糖原水平接近野生型水平。通过pas染色,工程化hgaa的糖原减少更一致。
[0225]
庞贝病基因疗法:脑和脊髓
[0226]
在正常(野生型)小鼠和经处理的gaa ko小鼠中评估gaa活性、糖原含量和糖原贮积/细胞质空泡化(图23)。脑中的gaa活性比野生型低约5倍。还评估了免疫组织化学和糖原pas(图24、图25、图26、图27)。免疫组织化学表明,某些细胞可能存在直接转导。然而,使用天然构建体几乎没有获得糖原清除。尽管活性仅为野生型的20%,但工程化构建体的糖原水平接近野生型水平。脊髓中的pas染色显示天然构建体几乎没有糖原清除。在包括运动神经元的腹角中观测到工程化构建体的糖原水平接近野生型。免疫组织化学证实脊髓神经元中的直接转导。由脉络丛和神经元细胞产生的工程化hgaa能够通过脊髓中的交叉校正来减少糖原,而天然hgaa几乎没有观测到糖原减少。
[0227]
结论
[0228]
总体而言,本实例中的数据证实,与常规治疗中使用的野生型gaa相比,工程化基因疗法构建体具有明显更好的组织摄取和糖原减少(包括在脑和脊髓中的效果)。实例8:动物研究方案
[0229]
aavhu68载体是由penn vector core按描述进行生产和滴定。(lock,alvira等人,2010年,“rapid,simple,and versatile manufacturing of recombinant adeno-associated viral vectors at scale.”[“快速、简单和多功能的大规模制造重组腺相关病毒载体”]hum gene ther[人类基因疗法]21(10):1259-1271)。
[0230]
c57bl/6/129背景首建鼠(founder)中的小家鼠(mus musculus)(gaa敲除的庞贝病小鼠)购自杰克逊实验室(jackson labs)(库存编号004154,也称为6neo小鼠)。
[0231]
在载体给药后第7天和第21天对经由侧尾静脉接受0.1ml的5
×
10
11
gc(大约2.5
×
10
13
gc/kg)aavhu68.cag.hgaa(包含天然hgaa(seq id no:189)或工程化hgaa(seq id no:190))的小鼠进行放血以进行血清分离,并且在注射后28天进行最终放血(用于血浆分离)并通过放血实施安乐死。从脑开始迅速地收集组织。gaa活性
[0232]
将血浆与5.6mm 4-mu-α-吡喃葡萄糖苷(ph 4.0)混合,并且在37℃下孵育三小时。用0.4m碳酸钠(ph 11.5)停止反应。使用victor3荧光计(激发在355nm处且发射在460nm处)来测量相对荧光单位(rfu)。通过从4-mu的标准曲线进行插值来计算活性(以nmol/ml/h为单位)。进一步将单独组织样品中的活性基于匀浆中的总蛋白质含量归一化。通过lc/ms得到的gaa特征肽
[0233]
将血浆在100%甲醇中沉淀并离心。弃去上清液。向沉淀中掺入hgaa独有的稳定的同位素标记的肽作为内标,并且用胰蛋白酶重新悬浮,并且在37℃下孵育一小时。用10%甲酸停止消化。通过c-18反相色谱法分离胰蛋白酶肽,并且通过esi-质谱法进行鉴定和定量。由特征肽浓度计算血浆中的总gaa浓度。细胞表面受体结合测定
[0234]
将96孔板用受体包被,洗涤,并且用bsa封闭。连续稀释来自aav处理的小鼠的28天血浆以产生一系列递减的浓度,并与偶联受体一起孵育。在孵育后,洗涤板以除去任何未结合的hgaa,并且添加4-mu-α-吡喃葡萄糖苷,在37℃下保持一小时。用1.0m甘氨酸(ph 10.5)停止反应,并且通过spectramax荧光计(激发370,发射460)读取rfu。将每个样品的rfu通过从4-mu的标准曲线进行插值转换为活性(nmol/ml/h)。使用graphpad prism完成非线性回归。组织学
[0235]
对组织进行福尔马林固定和石蜡包埋。肌肉载玻片用pas染色;cns载玻片用劳克坚牢蓝(luxol fast blue)/高碘酸希夫(periodic acid-schiff)(pas)染色。一位经过委员会认证的兽医病理学家(jh)盲审了组织学切片。在扫描的载玻片上对具有糖原贮积和细胞质空泡化的细胞的总百分比进行半定量估算。如下表中所描述归类为0到4分的评分。免疫组织化学(ihc)我们从使用抗人gaa抗体(西格玛hpa029126)免疫染色的载玻片来研究转基因表达和细胞定位。
[0236]
实例9:在庞贝病动物模型中的组织学-组织处理-方案和结果
[0237]
将所有组织固定在10%nbf(中性缓冲福尔马林)中。使用该领域中的常规测定
therapy of aspartylglucosaminuria.[用于天冬氨酰葡糖胺尿症的药理学伴侣疗法的小分子化合物的鉴定],sci rep[科学报告],2016。
[0249]
图34显示与野生型ppt1相比,工程化ppt1的结合增加。图35显示与野生型tpp1相比,工程化tpp1的结合增加。图36显示与野生型aga相比,工程化aga的结合增加。图37显示与野生型gla相比,工程化gla的结合增加。实例11:ppt1融合物的克隆
[0250]
使用来自宝生物(takara bio)的in-fusion克隆试剂盒将所有ppt1构建体组装到pcdna3.1表达载体中。
[0251]
将经线性化的pcdna3.1载体和每个ppt1基因片段通过infusion反应重组以产生含有所述ppt1构建体的最终pcdna3.1载体。实例12:克隆vigf2突变体
[0252]
使用来自宝生物(takara)的in-fusion克隆试剂盒将所有vigf2突变体交换到pcdna3.1-bip-vigf2-2gs-gaa表达载体中。
[0253]
通过infusion反应重组有序的vigf2片段和经线性化的pcdna3.1-gaa载体,得到最终的pcdna3.1-bip-vigf2*-2gs-gaa环状表达载体。实例13:vigf2-gaa构建体的表征
[0254]
用pcdna3.1-vigf2-gaa质粒瞬时转染hek293t细胞
[0255]
使用fugene hd转染试剂用1μg dna瞬时转染hek293t细胞。将培养物在37℃下(补充有5%co2)孵育另外的2-5天,之后收获条件培养基和细胞沉淀。
[0256]
条件培养基中vigf2-gaa的蛋白质印迹分析
[0257]
使用licor odyssey检测系统使用通用标准方法进行蛋白质印迹。用于vigf2-gaa检测的一抗是内部兔抗gaa抗体(fl059)。用于gaa的二抗是山羊抗兔dylight 800(赛默飞目录号sa5-35571)。
[0258]
gaa活性测定
[0259]
如上所述测量gaa活性。
[0260]
ci-mpr结合测定
[0261]
如上所述测量ci-mpr结合。
[0262]
细胞摄取测定
[0263]
创建30多个igf2-gaa构建体的结果如下。
[0264]
表现出不低于原始vigf2 80%的分泌/表达水平的vigf2-gaa构建体是vigf2-4、5、10、11、14、16、17、31和32(图38和图39)。
[0265]
表现出不低于原始vigf2 50%的分泌/表达水平的vigf2-gaa构建体是vigf2-4、5、6、9-14、16-23、25、27和29-34(图38和图39)。
[0266]
在观测到70/76kda成熟gaa肽片段的细胞内,所有vigf2-gaa构建体都显示为已正确加工(图38)。
[0267]
vigf2-17始终得到显著高于原始vigf2的ci-mpr结合bmax(图40、图41、图44和图45)。
[0268]
vigf2-24与ci-mpr的结合明显优于原始vigf2(图42和图43)。具有与原始vigf2相当或更好的pm25细胞摄取特性的vigf2-gaa构建体包括
vigf2-7、vigf2-10、vigf-17、vigf2-18、vigf2-20、vigf2-22和vigf2-23(图46和图47)。实例14:ppt1构建体的测试
[0269]
如本文别处所讨论来设计vigf2肽。基于增加的与ci-mpr的选择性结合和改善的蛋白质表达来选择变体。示例性肽及其结构在图48中提供。
[0270]
用pcdna3.1-ppt1质粒瞬时转染hek293t细胞
[0271]
使用fugene hd转染试剂用1μg dna瞬时转染hek293t细胞,这些细胞已经在12孔培养板中在补充有5%fbs的1ml optimem培养基中生长至约80%汇合。将培养物在37℃下(补充有5%co2)孵育另外的2-5天,之后收获条件培养基和细胞沉淀。
[0272]
条件培养基中ppt1的蛋白质印迹分析
[0273]
使用licor odyssey检测系统使用通用标准方法进行蛋白质印迹。用于ppt1检测的一抗是来自abcam的小鼠多克隆抗体(目录号ab89022)。用于ppt1的二抗是山羊抗小鼠dylight 800(赛默飞目录号sa5-35521)。
[0274]
ppt1表达的蛋白质印迹和显示条带强度的图示于图49中。显示通过蛋白质印迹定量的条件培养基中的ppt1的图示于图50中。
[0275]
ppt1活性测定
[0276]
所使用的ppt1活性测定基本上是由van diggelen等人(mol genet metab.[分子遗传学与代谢],66:240-244,1999)所描述的。简而言之,在典型的ppt1活性测定中,将10μl含有分泌的ppt1的条件培养基与90μl反应缓冲液在96孔黑色透明底板(康宁(corning)目录号3631)中混合,该反应缓冲液含有75um mu-6s-palm-βglc(4-甲基伞形酮基-6-硫代-棕榈酸酯-β-d-吡喃葡萄糖苷,开曼化学公司(cayman chemical);cas 229644-17-1)、2u/mlβ-葡糖苷酶(西格玛化学公司(sigma chemicals);cas 9001-22-3;g4511)、20mm柠檬酸盐(ph 4.0)、5mm dtt、0.02%triton x-100和50mm nacl。使用330nm的激发波长和450nm的发射波长,使用spectramax m2在25℃在1小时内以30秒的间隔监测荧光。通过用线性回归拟合时程荧光数据来提取ppt1反应的速率。
[0277]
显示通过活性定量的条件培养基中的ppt1的图示于图51中。发现活性与蛋白质印迹结果有很强的相关性。图52显示活性和蛋白质印迹定量之间的相关性。
[0278]
ppt1稳定性测定
[0279]
简而言之,在典型的稳定性测定中,将180μl含有ppt1的条件培养基用20μl 10x pbs(ph 7.4)稀释并在37℃下孵育。在不同的时间点,取出15μl的等分试样并在用干冰冷却的乙醇中快速冷冻。在时程实验结束时,将冷冻样品解冻并使用ppt1活性测定来测量ppt1活性。
[0280]
ci-mpr结合测定
[0281]
如前所述进行ci-mpr板结合测定,然后通过ppt1活性测定来确定结合量。
[0282]
下表中为在m6p存在下ppt1构建体与ci-mpr的结合。结合曲线示于图53中。
[0283]
表10:在m6p存在下ppt1构建体与ci-mpr的结合
[0284]
选择了六个ppt1构建体进行进一步分析。这六个构建体示于图54中。对这六个构建体确定了以下方面:分泌到培养基中的ppt1(图55)、细胞内的ppt1加工(图56)、ppt1的蛋白质印迹定量(图57)和活性(图58)。实例15外的ppt1 igf2融合构建体的工程化和测试
[0285]
如图62所示,设计和克隆了另外的ppt1构建体。这些构建体含有具有c6s突变的内源信号序列(seq id no:177)(任选地具有两个丙氨酸延伸以改善切割(seq id no:178)),或经修饰的bip信号肽bip-2(seq id no:171);包含野生型人ppt1(seq id no:4)的氨基酸残基21-306或28-306的ppt1序列,gs接头(seq id no:181-187)和变体igf2-31或变体igf2-32(seq id no:120或121),由溶酶体切割位点rpravptqa(seq id no:188)隔开。使所有ppt1构建体(图62)在freestyle 293悬浮细胞中瞬时表达。简而言之,使用聚乙烯亚胺(pei)作为转染试剂,用pcdna3.1主链中的每个ppt1构建体转染freestyle 293细胞。在freestyle 293表达培养基中表达四天后,收集来自每次转染的条件培养基并使用抗ppt1一抗进行蛋白质印迹。从这些蛋白质印迹上的条带密度定量培养基中的相对ppt1水平。图63显示测试的几种构建体具有比wt ppt1更高的分泌到培养基中的水平。条件培养基中较高的ppt1水平反映了良好表达和从细胞的有效分泌。尽管设计vigf2-31(seq id no:120)和vigf2-32(seq id no:32)用于改善cimpr结合,但与早期的igf2变体(seq id no:80)相比,ppt1的表达和分泌出人意料地增强了。用纯化的蛋白质构建体ppt1-101和ppt1-104进行的神经元摄取实验显示两种蛋白质的成功摄取,摄取的ppt1-104大约是ppt1-101的两倍(图64a)。对于该实验,将大鼠皮质神经元在neurocult培养基中培养并铺在包被有聚-l-赖氨酸的盖玻片上。用5μg/ml纯化的ppt1-101或ppt1-104(它们已用alexa fluor 680荧光染料标记)处理神经元。孵育一小时后,对细胞进行固定、透化并使用leica sp8共聚焦显微镜成像。如上所述,使用从freestyle 293细胞转染获得的条件培养基进行使用条件培养基的神经元摄取实验。首先通过蛋白质印迹利用了使用已知浓度的ppt1样品生成的标准曲线确定培养基中每种ppt1构建体蛋白的浓度。在处理神经元之前,浓缩每个条件培养基样品。将大鼠皮质神经元在原代神经元生长培养基中培养,并铺在包被有聚-l-赖氨酸的盖玻片上。用含以下浓度的ppt1蛋白的培养基处理神经元:孵育一小时后,对细胞进行固定、透化并使用leica sp8共聚焦显微镜成像。所有ppt1变体的摄取都高于wt ppt1;ppt1-104和ppt1-117显示出最高水平的摄取(图64b)。实例16naglu构建体的分析
[0286]
如图65所示,设计了包含插入在信号肽和naglu蛋白之间的n末端vigf2标签的重组人naglu蛋白的突变体融合蛋白。制备了几种变体,包括包含vigf2(seq id no:80)、vigf2-17(seq id no:106)、vigf2-31(seq id no:120)和vigf2-32(seq id no:121)的融合蛋白。在hek293f细胞中表达融合蛋白。显示了所测试的每种融合蛋白的裂解液和培养基部分中的naglu含量,如使用ab214671(r&d systems)通过蛋白质印迹测定。(图66a-b)通过4-mu测定来确定每种融合蛋白在条件培养基中的酶活性。(图66c)条件培养基中的蛋白质量未归一化/均衡化,并且活性数据代表构建体向条件培养基中的相对分泌,而不是等量蛋白质的相对比活性。如图66所见,与未标记的naglu相比,变体igf2的存在导致降低的表达和分泌。然而,与未标记的naglu相比,igf2标记的naglu的cimpr结合显著改善。(图67)值得注意的是,尽管用作结合测定的输入的igf2-标记的naglu相比于wt少约2.5倍,然而相比于wt更多标记的naglu结合到固定化受体。实例17tpp1构建体的分析
[0287]
设计了一系列用于表达与igf2变体连接的tpp1融合蛋白的核酸构建体,并测试了其表达、分泌和cimpr结合。融合蛋白包含信号肽(seq id no:179、变体igf2序列(seq id no:80、106、111、133、119-121)、gs接头(ggggsggggs,seq id no:186)、溶酶体切割位点(rpravptqa,seq id no:188)、tpp1前肽(seq id no:45)和tpp1成熟肽(seq id no:46)。生成并测试了n末端和c末端vigf2标记的构建体。设计和测试的ppt1融合蛋白的实例示于表11中。
[0288]
表11.tpp1融合构建体表11.tpp1融合构建体表达与分泌
[0289]
对于每个构建体,用9μl 1mg/ml pei和3μg dna转染freestyle 293细胞(1.5ml freestyle293培养基中的370万个细胞)并在摇动条件(37℃,5%co2,80%rh,250rpm)下在24孔深孔板中生长。转染后约24小时,将丙戊酸(终浓度2.2mm)和另外的1.5ml自由式培养基添加到转染物中。转染后3天收获培养物并离心以分离细胞和条件培养基。在sds-page凝胶上分离条件培养基中的蛋白质并转移到硝酸纤维素膜上。用5%牛奶封闭膜并用抗tpp1(abcam epr16537)和licor抗兔800cw(926-32213)探测。印迹成像并用licor odyssey clx
对条带进行定量,如图68所示。cimpr结合
[0290]
基本上如实例10中所述测量cimpr结合。结果示于图69中。rhtpp1(r&d system#2237-se-010,在小鼠骨髓瘤ns0细胞中表达)和wt tpp1(seq id no:8)作为对照包括在内。如图69所示,与rhtpp1相比,新型tpp1构建体都显示出改善的结合。实例18新型ppt1变体cln1小鼠模型的测试
[0291]
在cln1
r151x
小鼠模型中测试了ppt1-101(seq id no:60)和ppt1-104(seq id no:61)构建体。(miller,2014,human molecular genetics[人类分子遗传学],24(1)185-196)。制备了包含ppt1-101(seq id no:228)和ppt1-104(seq id no:235)的编码序列的基因疗法构建体。以5
×
10
10
、1
×
10
10
或1
×
109vg/动物的剂量向产后第1天(p1)小鼠脑室内注射病毒构建体(或pbs对照)。包括野生型ppt1(p546)作为对照。使用aav9载体引入转基因。在2月龄时评估结果。转基因表达
[0292]
通过rt-qpcr检测人cln1转基因表达。如图70所见,脑和脊髓提取物在各种构建体之间显示出相似的基因表达,在皮质中表达更高。自发荧光贮积物质的减少
[0293]
图71-72显示了每种构建体对脑自发荧光贮积物质(asm)积聚的影响,asm积聚为溶酶体功能障碍的相关因素。在皮质中5
×
10
10
和1
×
10
10
剂量下以及在丘脑中1
×
10
10
和1
×
109剂量下,与wt p546构建体相比,101和104构建体趋向于asm的更大程度地降少。胶质原纤维酸性蛋白(gfap)的减少
[0294]
图73显示了每种构建体对胶质原纤维酸性蛋白(gfap)的影响,gfap为星形胶质细胞增生和神经炎症的相关因素。在皮质中1
×
109剂量下,104构建体趋向于gfap的更大程度地减少。在丘脑中1
×
10
10
剂量下,101构建体趋向于gfap的更大程度地减少。gfap阳性细胞在形态上与反应性星形胶质细胞表型一致。
[0295]
因此,与cln1小鼠模型中的野生型ppt1相比,新型ppt1 101和104基因疗法构建体显示出改善的交叉校正,导致皮质和丘脑中asm和gfap的更大程度地减少。
[0296]
虽然在本文已经显示和描述了本发明的优选实施例,但对于本领域技术人员显而易见,此类实施例仅通过举例的方式来提供。在不背离本发明的情况下,本领域技术人员现在将想到许多变化、改变和替换。应当理解的是,可以采用本文所述的实施例的各种替代方案。意图在于,以下权利要求限定本发明的范围,并且由此覆盖这些权利要求及其等同物范围内的方法和结构。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1