一种光动力增强型聚合物纳米凝胶、制备方法及其应用
1.本发明涉及生物医用高分子材料技术领域,尤其涉及一种光动力增强型聚合物纳米凝胶、制备方法及其应用。
背景技术:
2.随着活性/受控自由基聚合和点击化学等先进聚合方法的出现,通过共价键连接的含卟啉的聚合物的合成得到了极大的发展。含卟啉的功能性聚合物具有明确的大分子结构、独特的自组装形态和特殊的光化学和光物理性质,在催化、太阳能电池、生物医学和环境科学等领域具有重要的应用。特别是,基于卟啉的光敏剂或缀合有卟啉的聚合物在光动力治疗(pdt)领域的应用。(angew.chem.int.ed.2018,57:16354
–
16358)
3.尽管fda已经批准了卟啉及衍生物作为二代光敏剂在临床光动力治疗中应用,但仍存在治疗深度较浅、肿瘤微环境乏氧、光敏副作用等问题。为解决这些问题,科研工作者设计了基于卟啉的聚合物纳米光疗体系,但这些体系的合成路线及工艺相对复杂,限制了它的大范围推广并且增加了治疗成本。如何设计合成简单却能解决上述问题的含卟啉的功能性聚合物是二代光敏剂末来发展的重中之重。另一方面,目前的卟啉基功能性聚合物的聚合物框架往往只作为载荷存在,聚合物自身可起到的功能非常有限,往往只起到组装包封或缀合小分子功能基团改善光敏剂水溶性和排布方式等作用。如何使聚合物参与到光动力能量转化过程中,提升单位光敏剂的光动力治疗效果是现在少之又少但非常值得探究的论题。
4.化学发光是一种能在室温下将化学反应能量转化成光能的反应过程。以草酸酯、过氧化氢和荧光剂为主要组成的过氧草酸酯类化学发光体系因其发光效率高和强度大等特点往往被认为是最有效的化学(非生物)发光体系之一。目前,虽然有过氧草酸酯类化学发光体系用来增强荧光分子体内成像的报道(acs nano 2020,14,3696
‑
3702),但利用肿瘤微环境高表达的过氧化氢或其他过氧化物提供光动力的额外活化能量转移位点的包含草酸酯和卟啉等荧光分子的聚合物凝胶却未见报道。
技术实现要素:
5.为了克服现有技术中存在的上述缺陷,本发明提供了一种光动力增强型聚合物纳米凝胶、制备方法及其应用,所述聚合物纳米凝胶具有合成路线简单且能使聚合物参与到光动力能量转化过程中提升单位光敏剂的光动力治疗效果的优势。
6.本发明通过如下技术方案实现:
7.一种光动力增强型聚合物纳米凝胶,具有式(ⅰ)或式(ⅱ)所示的结构,是由水溶性的聚乙二醇单甲醚衍生物、卟啉衍生物及草酰氯通过一步法制备得到;
[0008][0009]
其中,m为整数,且20≤m≤200;
[0010]
所述卟啉衍生物的结构式如下:
[0011][0012]
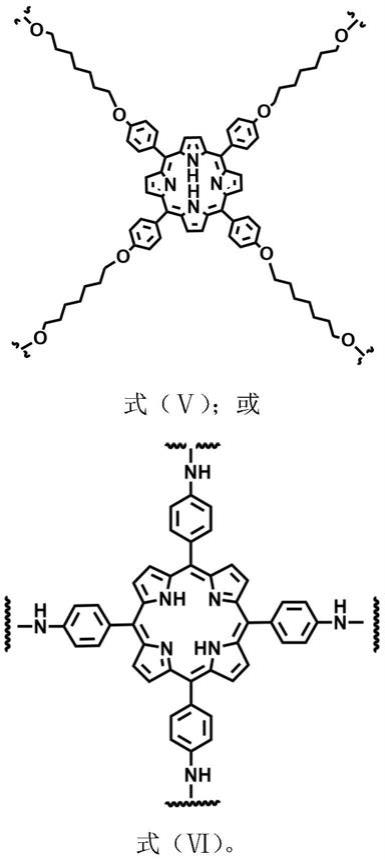
优选地,所述卟啉衍生物为四羟己基醚苯基卟啉或四氨基苯基卟啉。
[0013]
优选地,所述聚乙二醇单甲醚衍生物为聚乙二醇单甲醚或氨基化聚乙二醇单甲醚。
[0014]
本发明还提供了一种光动力增强型聚合物纳米凝胶的制备方法,包括以下步骤:
[0015]
在催化剂、缚酸剂和溶剂存在的条件下,将卟啉衍生物、聚乙二醇单甲醚衍生物及草酰氯进行亲核取代反应,一步法制备得到聚合物纳米凝胶。
[0016]
所述卟啉衍生物、聚乙二醇单甲醚衍生物、草酰氯的摩尔比为a:n:20~25*(n+a),其中,n=1~4*a。
[0017]
优选地,所述卟啉衍生物为四羟己基醚苯基卟啉或四氨基苯基卟啉;所述催化剂为4
‑
二甲氨基吡啶;所述聚乙二醇单甲醚衍生物为聚乙二醇单甲醚或氨基化聚乙二醇单甲醚;所述缚酸剂为碳酸钾或三乙胺;所述溶剂为无水二氯甲烷、无水二甲基亚砜或无水n,n
‑
二甲基甲酰胺;反应温度为0~10℃,反应时间为12~72h。
[0018]
优选地,所述四羟己基醚苯基卟啉由以下方法制得:
[0019]
在溶剂及催化剂存在的条件下,将四羟基苯基卟啉与6
‑
氯
‑1‑
己醇按照一定比例混合,将得到的反应产物依次用氢氧化钠溶液和去离子水洗涤,ph值调至7~8,将洗涤后的反应产物用布氏漏斗抽滤得到深紫色固体,并在真空干燥器中抽干得到四羟己基醚苯基卟
啉,反应方程式如下:
[0020][0021]
优选的,所述催化剂为碘化钠,所述溶剂为无水四氢呋喃、无水n,n
‑
二甲基甲酰胺或n
‑
甲基吡咯烷酮中的一种或几种。反应温度为120~160℃;反应时间为12~36h。
[0022]
优选的,所述四羟基苯基卟啉和6
‑
氯
‑1‑
己醇的摩尔比为1:1~10。
[0023]
所述四羟基苯基卟啉的结构式如式
ⅶ
所示;
[0024][0025]
本发明还提供了一种光动力增强型聚合物纳米凝胶在制备抗肿瘤药物中的应用。
[0026]
本发明的一种光动力增强型聚合物纳米凝胶的制备原理如下:
[0027]
在纳米凝胶中需要过草酸酯键或者过草酰胺键作为linker存在以满足实验设计理念,故而使卟啉衍生物和聚乙二醇单甲醚衍生物均带有羟基作为特征反应基团,以草酰氯的酰氯基团与之进行亲核取代缩合反应脱除氯化氢生成以过草酸酯键交联的具有式(ⅰ)结构的聚合物纳米凝胶;而以同样的理念设计使卟啉衍生物和聚乙二醇单甲醚衍生物均带有氨基作为特征反应基团,以草酰氯的酰氯基团与之进行亲核取代缩合反应脱除氯化氢生成过草酰胺键交联的具有式(ⅱ)结构的聚合物纳米凝胶。共同形成一系列交联位点可响应强氧化剂的光动力增强型聚合物纳米凝胶。反应方程式如下:
[0028][0029]
与现有技术相比,本发明的有益效果如下:
[0030]
本发明提供的一种光动力增强型聚合物纳米凝胶,能够在h2o2高表达的肿瘤微环境中,式(ⅰ)或式(ⅱ)结构中草酸酯或草酰胺的羰基受到h2o2的亲核进攻,生成能产生高能量的双氧基环状中间体二氧杂环丁二酮,中间体分解促使能量通过化学发光共振能量转移(cret)传递给受体荧光分子,提高单位光敏剂的光动力效率,更好地抑制肿瘤增长。这样的有益效果可以通过结合mtt细胞毒性试验对施加光照与否的各组别不同浓度梯度之间的细胞毒性予以验证,同时本发明通过流式细胞术验证了相同条件下这种纳米凝胶相对于原始光敏剂组和对照组来说更高的细胞内ros产生。另一方面,从合成过程本身来说,本发明提供的合成方法简单快捷,利用一步法制备纳米粒子避免了用于生物纳米粒子组装体的构建过程,在用于后续生产应用方面具有很大的优势。
附图说明
[0031]
图1为本发明实施例1制备得到的含长烷基链四臂苯基卟啉衍生物topp
‑
c6oh4的核磁共振氢谱图;
[0032]
图2为本发明实施例11制备得到的聚合物纳米凝胶tapp
‑
ngt在重水中的核磁共振氢谱图;
[0033]
图3为本发明实施例11制备得到的聚合物纳米凝胶tapp
‑
ngt在dmso
‑
d6中的核磁共振氢谱图;
[0034]
图4为本发明实施例3制备得到的聚合物纳米凝胶toppnps在重水中的核磁共振氢谱图;
[0035]
图5为本发明实施例3制备得到的聚合物纳米凝胶toppnps在dmso
‑
d6中的核磁共振氢谱图;
[0036]
图6为本发明实施例3制备得到的聚合物纳米凝胶toppnps的红外光谱图;
[0037]
图7为本发明实施例3制备得到的聚合物纳米凝胶toppnps的动态光散射图;
[0038]
图8为本发明实施例3制备得到的聚合物纳米凝胶toppnps的透射电子显微镜图;
[0039]
图9为本发明实施例3制备得到的聚合物纳米凝胶toppnps在pbs中培养30min七次取点的体外ros紫外谱图;
[0040]
图10为实施例11中b16
‑
f10鼠源黑色素瘤细胞随着tapp
‑
ngt所含光敏剂浓度的增加对应的细胞存活率;
[0041]
图11为实施例3中b16
‑
f10鼠源黑色素瘤细胞随着toppnps所含光敏剂浓度的增加对应的细胞存活率;
[0042]
图12为实施例11中b16
‑
f10鼠源黑色素瘤细胞内化4小时反映不同材料细胞内ros产生的流式细胞统计图。
具体实施方式
[0043]
下面将结合本发明实施例,对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0044]
一种光动力增强型聚合物纳米凝胶,具有式(ⅰ)或式(ⅱ)所示的结构,是由水溶性的聚乙二醇单甲醚、卟啉衍生物及草酰氯通过一步法制备得到;
[0045][0046]
其中,m为整数,且20≤m≤200;
[0047]
所述卟啉衍生物具有如下结构:
[0048][0049]
本发明还提供了一种聚合物纳米凝胶的制备方法,包括以下步骤:
[0050]
在催化剂、缚酸剂和溶剂存在情况下,将具有式(
ⅴ
)或式(
ⅵ
)结构的四羟己基醚
苯基卟啉或四氨基苯基卟啉搭配不同比例的聚乙二醇单甲醚或氨基化聚乙二醇单甲醚,及草酰氯通过一步法得到具有式(ⅰ)或式(ⅱ)结构的聚合物纳米凝胶。
[0051]
式(ⅰ)~式(
ⅵ
)所示结构中,所述波浪处对应的键为基团的连接键,与上述主体结构相连。
[0052]
在本发明的某些实施例中,20≤m≤200。
[0053]
在本发明的某些实施例中,n为a、2a、3a或4a;m为23、45或113。
[0054]
本发明提供的聚合物纳米凝胶经简单的一步法合成。该材料能够在h2o2高表达的肿瘤微环境中,草酸酯或草酰胺的羰基受到h2o2的亲核进攻,生成能产生高能量的双氧基环状中间体二氧杂环丁二酮,中间体分解促使能量通过化学发光共振能量转移(cret)传递给受体荧光分子,提高单位光敏剂的光动力效率,更好地抑制肿瘤增长。
[0055]
在本发明的某些实施例中,所述具有式(ⅰ)或式(ⅱ)结构的卟啉衍生物与聚乙二醇单甲醚衍生物物质的量的和,和草酰氯的物质的量比为1:20~25;
[0056]
在本发明的某些实施例中,所述溶剂包括无水二氯甲烷,无水二甲基亚砜或无水n,n
‑
二甲基甲酰胺;本发明对所述溶剂的用量并无特殊的限制,能够将卟啉衍生物、聚乙二醇单甲醚衍生物和草酰氯溶解即可。
[0057]
在本发明的某些实施例中,所述催化剂为dmap;所述缚酸剂为碳酸钾或三乙胺。
[0058]
在本发明的某些实施例中,所述反应的温度为0~10℃;所述反应的时间为12~72h。
[0059]
在本发明的某些实施例中,所述亲核取代反应在冰浴条件下进行,反应之前反应瓶需要真空烘干。
[0060]
在本发明的某些实施例中,具有式(ⅰ)或式(ⅱ)所示结构的聚合物在溶剂中缩合完成后,还包括:将反应后的产物进行透析和冻干。本发明对所述透析和冻干的方法并无特殊的限制,采用本领域技术人员熟知的透析和冻干的方法即可。
[0061]
在本发明的某些实施例中,所述具有式(
ⅴ
)结构的含长烷基链四臂苯基卟啉衍生物由以下方法制得:
[0062]
在催化剂的作用下,具有式(
ⅶ
)所示结构的四羟基苯基卟啉的酚羟基更易实现去质子化进而与6
‑
氯
‑1‑
己醇在溶剂中反应,得到具有式(
ⅴ
)结构的含长烷基链四臂苯基卟啉衍生物;所述催化剂为碘化钠;所述溶剂为无水四氢呋喃、无水n,n
‑
二甲基甲酰胺和n
‑
甲基吡咯烷酮中的一种或几种;
[0063]
[0064]
在本发明的某些实施例中,具有式(
ⅶ
)结构的四羟基苯基卟啉和6
‑
氯
‑1‑
己醇的摩尔比为1:1~10。
[0065]
在本发明的某些实施例中,所述反应的温度为120~160℃;所述反应的时间为12~36h。
[0066]
在本发明的某些实施例中,含长烷基链四臂苯基卟啉衍生物在溶剂中反应完成后,还包括:将得到的反应产物依次用氢氧化钠溶液和去离子水洗涤,ph值调至7~8。在本发明的某些实施例中,所述洗涤的次数大于等于3次。
[0067]
在本发明的某些实施例中,所述洗涤过程结束后,还包括:将洗涤后的反应产物用布氏漏斗抽滤得到深紫色固体,并在真空干燥器中抽干,得到具有式(
ⅴ
)所示结构的卟啉衍生物。
[0068]
本发明对上文采用的原料的来源并无特殊的限制,可以为一般市售。
[0069]
本发明还提供了一种上文所述的聚合物纳米凝胶或上文所述的制备方法制得的聚合物纳米凝胶在制备抗肿瘤药物中的应用。
[0070]
下面结合实施例对本发明做进一步详细的描述。
[0071]
实施例1
[0072]
具有式(
ⅴ
)结构的含长烷基链四臂苯基卟啉衍生物的合成:
[0073]
称取四羟基苯基卟啉0.678g(0.001mol)溶解于100ml dmf中,在冰浴条件下,加入5g nai(0.0035mol)进行活化。活化后,25℃下搅拌反应6h。随后将反应体系转入油浴锅,反应温度151℃,回流。用注射器向此密闭体系中滴加6
‑
氯
‑1‑
己醇1.4ml(0.01mol),继续回流反应12h。停止反应后,反应液倒入冷冻过的去离子水中,缓慢加氢氧化钠观察颜色变化。再用去离子水洗涤三次,用布氏漏斗抽滤得到暗紫色固体,在真空干燥器中抽干,得到四羟己基醚苯基卟啉topp
‑
c6oh4;反应方程式如下:
[0074][0075]
对上述得到的含长烷基链四臂苯基卟啉衍生物topp
‑
c6oh4进行结构表征,结果如图1所示。图1为本发明实施例1制备的含长烷基链四臂苯基卟啉衍生物topp
‑
c6oh4的核磁共振氢谱图。
[0076]
实施例2
[0077]
具有式(
ⅴ
)结构的含长烷基链四臂苯基卟啉衍生物的合成:
[0078]
称取四羟基苯基卟啉0.678g(0.001mol)溶解于100ml dmf中,冰浴,加入5g nai(0.0035mol)进行活化。活化后,25℃下搅拌反应6h。随后将反应体系转入油浴锅,反应温度151℃,回流。用注射器向此密闭体系中滴加6
‑
氯
‑1‑
己醇0.7ml(0.005mol),继续回流反应
24h。停止反应后,反应液倒入冷冻过的去离子水中,缓慢加氢氧化钠观察颜色变化。再用去离子水洗涤三次,用布氏漏斗抽滤得到暗紫色固体,在真空干燥器中抽干,得到四羟己基醚苯基卟啉。
[0079]
实施例3
[0080]
具有式(ⅰ)结构的过草酸酯交联的纳米凝胶的合成,式(ⅰ)结构中,n=a:
[0081]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg5000,分子量为5000)0.5g(0.0001mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅴ
)结构的四羟己基封端卟啉衍生物0.113g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯0.5ml(0.005mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶toppnps。反应方程式如下:
[0082][0083]
对上述得到的聚合物纳米凝胶toppnps进行表征,结果如图4和图5所示。图4为本发明实施例3制备得到的聚合物法纳米凝胶toppnps在重水中的核磁共振氢谱图。图5为本发明实施例3制备得到的聚合物纳米凝胶toppnps在dmso
‑
d6中的核磁共振氢谱图。从图4和图5可知,聚合物纳米凝胶toppnps已被成功合成并已构成纳米级组装体。图6的红外光谱图分析辅助了这一论点。
[0084]
图7为本发明实施例3制备得到的聚合物纳米凝胶toppnps的动态光散射图;图8为本发明实施例3制备得到的聚合物纳米凝胶toppnps的透射电子显微镜图。二者共同说明了纳米粒子稳定存在并且尺寸在120
‑
200nm之间。
[0085]
图9为本发明实施例3制备得到的聚合物纳米凝胶toppnps在pbs中培养30min七次取点的体外ros紫外谱图;证实了聚合物米凝胶toppnps能在光照下持续产生ros可作为光动力光疗体系使用。
[0086]
聚合物纳米凝胶toppnps的抗肿瘤活性通过细胞毒性试验来检测:
[0087]
将本发明实施例3制备得到的聚合物纳米凝胶toppnps和b16
‑
f10鼠源黑色素瘤细胞共培养,采用mtt实验进行评估:
[0088]
首先在96孔板中以7000个细胞/孔的密度(悬浮于200l dmem培养基)接种相应的细胞,在37℃下细胞培养箱中孵育24h。次日,用新鲜的dmem培养基溶解相应的聚合物纳米凝胶toppnps,并梯度稀释成不同的浓度,弃去前一天的培养基,加入含有不同浓度聚合物
纳米凝胶toppnps的dmem,继续在37℃下细胞培养箱中孵育24h。之后在每个孔中加入mtt溶液(最终浓度0.5mg/ml),继续在37℃下孵育4h。弃去孔板中的液体,并分别向每个孔中加入150l的dmso,溶解紫色甲瓒晶体。最后用酶标仪(tecan,switzerland)测定各个孔在492nm处的吸光度,用实验组的吸光度值和对照组相比即可计算出细胞的存活率。
[0089]
图11为实施例3中b16
‑
f10鼠源黑色素瘤细胞随着toppnps所含光敏剂浓度的增加对应的细胞存活率;可以看出非光照组几乎没有杀伤,光照组聚合物纳米凝胶toppnps相比于纯光敏剂治疗组肿瘤杀伤率在各个浓度梯度都有显著提升,印证了聚合物纳米凝胶toppnps导致单位光敏剂的光动力效率得到全面且显著的提升,起到更好的抗肿瘤效果的观点。
[0090]
实施例4
[0091]
具有式(ⅰ)结构的过草酸酯交联纳米凝胶的合成,式(ⅰ)结构中,n=2a:
[0092]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg5000,分子量为5000)1.0g(0.0002mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅴ
)结构的四羟己基封端卟啉衍生物0.113g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯0.7ml(0.0075mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶toppnps。
[0093]
实施例5
[0094]
具有式(ⅰ)结构的过草酸酯交联纳米凝胶的合成,式(ⅰ)结构中,n=3a:
[0095]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg5000,分子量为5000)1.5g(0.0003mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅴ
)结构的四羟己基封端卟啉衍生物0.113g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯0.9ml(0.01mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶toppnps。
[0096]
实施例6
[0097]
具有式(ⅰ)结构的过草酸酯交联纳米凝胶的合成,式(ⅰ)结构中,n=4a:
[0098]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg5000,分子量为5000)1.0g(0.0002mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅴ
)结构的四羟己基封端卟啉衍生物0.113g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯0.7ml(0.0075mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶toppnps。
[0099]
实施例7
[0100]
具有式(ⅰ)结构的过草酸酯交联纳米凝胶的合成,式(ⅰ)结构中,n=a:
[0101]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg2000,分子量为2000)0.2g(0.0001mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅴ
)结构的四羟己基封端卟啉衍生物0.113g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯0.5ml(0.005mol),
反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶toppnps。
[0102]
实施例8
[0103]
具有式(ⅰ)结构的过草酸酯交联纳米凝胶的合成,式(ⅰ)结构中,n=2a:
[0104]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg2000,分子量为2000)0.4g(0.0002mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅴ
)结构的四羟己基封端卟啉衍生物0.113g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯0.7ml(0.0075mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶toppnps。
[0105]
实施例9
[0106]
具有式(ⅰ)结构的过草酸酯交联纳米凝胶的合成,式(ⅰ)结构中,n=3a:
[0107]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg2000,分子量为2000)0.6g(0.0003mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅴ
)结构的四羟己基封端卟啉衍生物0.113g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯0.9ml(0.01mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶toppnps。
[0108]
实施例10
[0109]
具有式(ⅰ)结构的过草酸酯交联纳米凝胶的合成,式(ⅰ)结构中,n=4a:
[0110]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg2000,分子量为2000)0.8g(0.0004mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅴ
)结构的四羟己基封端卟啉衍生物0.113g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯1.1ml(0.0125mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶toppnps。
[0111]
实施例11
[0112]
具有式(ⅱ)结构的过草酰胺交联纳米凝胶的合成,式(ⅱ)结构中,n=a:
[0113]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg5000,分子量为5000)0.5g(0.0001mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅵ
)结构的四氨基苯基卟啉0.068g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯0.5ml(0.005mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶tapp
‑
ngt。反应方程式如下:
[0114][0115]
对上述得到的聚合物纳米凝胶tapp
‑
ngt进行表征,结果如图2和图3所示。图2为本发明实施例11制备得到的聚合物纳米凝胶tapp
‑
ngt在重水中的核磁共振氢谱图。图3为本发明实施例11制备得到的聚合物纳米凝胶tapp
‑
ngt在dmso
‑
d6中的核磁共振氢谱图。从图2和图3可知,聚合物纳米凝胶tapp
‑
ngt已被成功合成并已构成纳米级组装体。
[0116]
图10为实施例11中b16
‑
f10鼠源黑色素瘤细胞随着tapp
‑
ngt所含光敏剂浓度的增加对应的细胞存活率;可以看出非光照组几乎没有杀伤,光照组聚合物纳米凝胶tapp
‑
ngt相比于纯光敏剂治疗组肿瘤杀伤率在各个浓度梯度都有显著提升,印证了聚合物纳米凝胶tapp
‑
ngt导致单位光敏剂的光动力效率得到全面且显著的提升,起到更好的抗肿瘤效果的观点。
[0117]
图12为实施例11中b16
‑
f10鼠源黑色素瘤细胞内化4小时反映不同材料细胞内ros产生的流式细胞统计图。横坐标对应dcf
‑
dh探针荧光强度,本测试能反映细胞内ros产生量,结果显然聚合物纳米凝胶tapp
‑
ngt相比于纯光敏剂治疗组ros产生量有显著提升,印证了聚合物纳米凝胶tapp
‑
ngt导致单位光敏剂的光动力效率得到全面且显著的提升,起到更好的抗肿瘤效果的观点。
[0118]
实施例12
[0119]
具有式(ⅱ)结构的过草酰胺交联纳米凝胶的合成,式(ⅱ)结构中,n=2a:
[0120]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg5000,分子量为5000)1g(0.0002mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅵ
)结构的四氨基苯基卟啉0.068g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯0.7ml(0.0075mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶tapp
‑
ngt。
[0121]
实施例13
[0122]
具有式(ⅱ)结构的过草酰胺交联纳米凝胶的合成,式(ⅱ)结构中,n=3a:
[0123]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg5000,分子量为5000)1.5g(0.0003mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅵ
)结构的四氨基苯基卟啉0.068g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯0.9ml(0.01mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶tapp
‑
ngt。
[0124]
实施例14
[0125]
具有式(ⅱ)结构的过草酰胺交联纳米凝胶的合成,式(ⅱ)结构中,n=4a:
[0126]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg5000,分子量为5000)2g(0.0004mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷30ml充分溶解后,氮气保护下,加入具有式(
ⅵ
)结构的四氨基苯基卟啉0.068g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯1.1ml(0.0125mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶tapp
‑
ngt。
[0127]
实施例15
[0128]
具有式(ⅱ)结构的过草酰胺交联纳米凝胶的合成,式(ⅱ)结构中,n=a:
[0129]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg2000,分子量为2000)0.2g(0.0001mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅵ
)结构的四氨基苯基卟啉0.068g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯0.5ml(0.005mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶tapp
‑
ngt。
[0130]
实施例16
[0131]
具有式(ⅱ)结构的过草酰胺交联纳米凝胶的合成,式(ⅱ)结构中,n=2a:
[0132]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg2000,分子量为2000)0.4g(0.0002mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅵ
)结构的四氨基苯基卟啉0.068g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯0.7ml(0.0075mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶tapp
‑
ngt。
[0133]
实施例17
[0134]
具有式(ⅱ)结构的过草酰胺交联纳米凝胶的合成,式(ⅱ)结构中,n=3a:
[0135]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg2000,分子量为2000)0.6g(0.0003mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅵ
)结构的四氨基苯基卟啉0.068g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯0.9ml(0.01mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶tapp
‑
ngt。
[0136]
实施例18
[0137]
具有式(ⅱ)结构的过草酰胺交联纳米凝胶的合成,式(ⅱ)结构中,n=4a:
[0138]
反应装置无水无氧处理,称取聚乙二醇单甲醚(mpeg2000,分子量为2000)0.8g(0.0004mol),以甲苯做溶剂共沸回流4h除水。抽干甲苯溶剂,室温,加入无水二氯甲烷20ml充分溶解后,氮气保护下,加入具有式(
ⅵ
)结构的四氨基苯基卟啉0.068g(0.0001mol)和缚酸剂。冰浴,氮气保护,用注射器逐滴缓慢加入草酰氯1.1ml(0.0125mol),反应4h后,升温到25℃,搅拌,反应24h。反应结束后,用冷冻乙醚沉降,透析,冻干,得到聚合物纳米凝胶tapp
‑
ngt。
[0139]
由以上实施例可知,本发明提供了一种聚合物纳米凝胶、其制备方法及应用。所述
纳米凝胶具有式(ⅰ)或式(ⅱ)所示结构:其中,20≤m≤200。本发明提供的纳米凝胶经简单的一步法合成。该材料能够在h2o2高表达的肿瘤微环境中,草酸酯或草酰胺的羰基受到h2o2的亲核进攻,生成能产生高能量的双氧基环状中间体二氧杂环丁二酮,中间体分解促使能量通过化学发光共振能量转移(cret)传递给受体荧光分子,导致单位光敏剂的光动力效率得到全面且显著的提升,起到更好的抗肿瘤效果。
[0140]
以上实施例的说明只是用于帮助理解本发明的方法及其核心思想。对这些实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1