乳酸菌发酵溶胞物、制备方法、应用及含其的皮肤外用剂与流程
1.本发明属于发酵技术领域,尤其涉及一种乳酸菌发酵溶胞物、制备方法、应用及含其的皮肤外用剂。
背景技术:
2.随着生活水平的不断提高,人们对生活的需求不再是简单的温饱,逐渐的转向各个方面,比如精致完美的容貌,致使人们对功效化妆品的关注度越来越高,例如具有抗氧化、抗衰老或保湿等功效的化妆品。同时,功效化妆品的安全性也是化妆品领域关注的重要问题。因此,研发一种安全有效的化妆品原料是非常有必要的。
3.目前,对于乳酸菌发酵的研究主要集中在食品领域,虽然化妆品领域已经有利用乳酸菌发酵制备化妆品原料的相关报道,但功效普遍过于单一,或是使用安全性差。因此,本领域亟需开发一种使用安全高,且兼具多种功效的化妆品原料的制备方法。
技术实现要素:
4.本发明所要解决的技术问题是克服现有技术中利用乳酸菌发酵制得的化妆品原料功效单一或安全性差等缺陷,而提供一种乳酸菌发酵溶胞物、制备方法、应用及含其的皮肤外用剂。本发明制得的乳酸菌发酵溶胞物同时兼具抗氧化、保护和修复人皮肤成纤维细胞、提高胶原蛋白生成和保湿等功效,且安全性高,原料简单易得,制备成本低,可被广泛应用于皮肤外用剂领域。
5.本发明采用以下技术方案解决上述技术问题:
6.本发明提供一种乳酸菌发酵溶胞物的制备方法,具体包括如下步骤:乳酸菌接种到发酵底物中,经发酵培养、超声、灭菌,即可;其中,所述发酵底物包括原料乳。
7.本发明中,所述乳酸菌可为乳双歧杆菌。
8.其中,所述乳双歧杆菌可为danisco公司生产的产品编号为1261259的乳双岐杆菌和/或京川秀科技有限公司生产的双歧杆菌酸奶发酵菌粉。
9.本发明中,所述乳酸菌可按照本领域常规以乳酸菌菌液的形式添加,所述乳酸菌菌液中所述乳酸菌的浓度可为106‑
10
10
cfu/ml,较佳地为106‑
107cfu/ml。
10.其中,所述乳酸菌菌液与所述发酵底物的体积比可为本领域常规,较佳地为(2
‑
5):100。
11.其中,所述乳酸菌菌液的制备方法可为本领域常规,具体包括如下步骤:所述乳酸菌接种于ph值为7的mrs肉汤培养基中,在温度为40
‑
45℃条件下培养45
‑
50h,即可;较佳地为所述乳酸菌接种于ph值为7的mrs肉汤培养基中,在温度为43℃条件下培养48h,即可。
12.本发明中,所述原料乳可为本领域常规使用的原料乳,较佳地包括生鲜乳和/或复原乳。
13.其中,所述复原乳为本领域常规使用的复原乳,较佳地包括全脂乳粉和溶剂。其中,所述全脂乳粉可为新西兰全脂乳粉,例如,购于安徽轻工国际贸易股份有限公司的新西
兰全脂乳粉。其中,所述溶剂可为本领域常规使用的溶剂,较佳地为水,例如,去离子水。
14.本发明一较佳实施方案中,所述复原乳由所述全脂乳粉和所述溶剂组成。
15.当所述复原乳由所述全脂乳粉和所述溶剂组成时,所述全脂乳粉占所述复原乳的质量百分比可为本领域常规,一般可为2%
‑
12%,较佳地为3%
‑
8%,更佳地为5%~8%。
16.本发明中,所述发酵底物在使用前还可进一步包括灭菌的操作。所述灭菌的条件和方法可为本领域常规。
17.其中,所述灭菌的温度可为本领域该类操作常规的温度,较佳地为80
‑
100℃。
18.其中,所述灭菌的时间可为本领域该类操作常规的时间,较佳地为20
‑
30min。
19.本发明中,所述发酵培养的时间可为本领域该类操作常规的时间,较佳地为7
‑
15h,更佳地为8
‑
10h。
20.本发明中,所述发酵培养的温度可为本领域该类操作常规的温度,较佳地为40
‑
45℃,更佳地为43
‑
45℃。
21.本发明中,所述超声的条件和方法可为本领域常规,一般可使所述乳酸菌破碎即可。
22.本发明中,所述超声可按照本领域常规在超声波细胞破碎仪中进行。
23.本发明中,所述超声的时间可为本领域该类操作常规的时间,一般可为5
‑
20min,较佳地为10
‑
20min。
24.本发明中,所述超声的功率可为本领域该类操作常规的功率,一般可为10%
‑
25%,较佳地为20%
‑
25%。
25.本发明一较佳实施方案中,所述超声采用间歇超声的方法,每次超声的时间可为2
‑
10s,间歇时间可为10
‑
20s,所述超声时间和所述间歇时间的和为5
‑
20min;更佳地,所述超声采用间歇超声的方法,每次超声时间为2s,间歇时间为10s,所述超声时间和所述间歇时间的和为20min。按照本领域常规,所述间歇时间为相邻两次超声之间不进行超声的间隔时间。
26.本发明中,所述灭菌的条件和方法可为本领域常规。
27.本发明中,所述灭菌的温度可为本领域该类操作常规的温度,较佳地为85
‑
100℃,更佳地为90
‑
100℃。
28.本发明中,所述灭菌时间可为本领域该类操作常规的时间,较佳地为20
‑
30min。
29.本发明中,所述超声的操作后,还可进一步包括过滤的操作。
30.其中,所述过滤采用的滤膜的孔径可为本领域常规,一般可为0.45
‑
1μm。
31.本发明中,所述灭菌的操作后还可进一步包括与防腐剂混合的操作。
32.其中,所述混合的温度可为本领域该类操作常规的温度,较佳地为60
‑
75℃,更佳地为65℃。
33.其中,所述防腐剂可为本领域常规使用的防腐剂,较佳地包括对羟基苯乙酮和/或1,2
‑
己二醇。
34.当所述防腐剂包括对羟基苯乙酮和1,2
‑
己二醇时,所述对羟基苯乙酮占所述灭菌后制得物料的质量百分数可为0.3%
‑
0.5%,所述1,2
‑
己二醇占所述灭菌后制得物料的质量百分数可为0.5%
‑
1%;较佳地,所述对羟基苯乙酮占所述灭菌后制得物料的质量百分数为0.5%,所述1,2
‑
己二醇占所述灭菌后制得物料的质量百分数为0.5%。
35.本发明还提供一种乳酸菌发酵溶胞物,其由如上所述的乳酸菌发酵溶胞物的制备方法制得。
36.本发明中,所述乳酸菌发酵溶胞物的折光率可为1.330
‑
1.350,较佳地为1.335
‑
1.345,例如1.33418、1.340或1.342。
37.本发明还提供一种如上所述的乳酸菌发酵溶胞物在皮肤外用剂中的应用,所述乳酸菌发酵溶胞物可作为皮肤外用剂中的抗氧化活性成分、抗衰老活性成分和保湿活性成分中的任意一种或多种。
38.本发明中,所述抗氧化活性成分可为具有清除超氧阴离子自由基作用的抗氧化活性成分。
39.本发明中,所述抗衰老活性成分可为具有提高人皮肤成纤维细胞存活率和/或对受损人皮肤成纤维细胞具有修复作用的抗衰老活性成分。
40.其中,所述修复作用包括提高受损人皮肤成纤维细胞存活率、提高受损人皮肤成纤维细胞中gsh
‑
px的活力、sod活力、cat活力、总抗氧化能力和col
‑
1含量中一种或多种的作用。
41.本发明还提供一种皮肤外用剂,其包括如上所述的乳酸菌发酵溶胞物。
42.本发明中,所述皮肤外用剂可按照本领域常规包括且不限于面膜、精华或爽肤水。
43.本发明中,所述乳酸菌发酵溶胞物占所述皮肤外用剂的质量百分比可为10%
‑
100%。
44.本发明中,按照本领域常规,所述皮肤外用剂中还可进一步包括增稠剂和/或中和剂。
45.在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
46.本发明所用试剂和原料均市售可得。
47.本发明的积极进步效果在于:本发明通过选用合适的发酵底物原料乳和乳酸菌制得乳酸菌发酵溶胞物,其具有良好的抗氧化、保护和修复人皮肤成纤维细胞、提高胶原蛋白生成和保湿等功效,对人皮肤成纤维细胞无明显毒副作用,对皮肤无刺激性,且安全性高,原料简单易得,可被广泛应用于皮肤外用剂领域。
附图说明
48.本公开可以通过参考下文中结合附图所给出的描述而得到更好的理解。所述附图连同下面的详细说明一起包含在本说明书中并且形成本说明书的一部分,而且用来进一步举例说明本公开的优选实施例和解释本公开的原理和优点。其中:
49.图1为不同浓度的本发明实施例1
‑
2制得乳双歧杆菌发酵溶胞物对超氧阴离子自由基清除率的结果图;
50.图2为本发明实施例1
‑
2制得乳双歧杆菌发酵溶胞物对hsf细胞保护作用的结果图;
51.图3为本发明实施例1
‑
2制得乳双歧杆菌发酵溶胞物对hsf细胞保护作用测试过程中细胞存活率结果图;
52.图4为本发明实施例1制得的乳双歧杆菌发酵溶胞物对hsf细胞具有修复作用的证
明图;
53.图5为本发明实施例1制得的乳双歧杆菌发酵溶胞物对hsf细胞进行细胞修复后细胞内gsh
‑
px活力测试图;
54.图6为本发明实施例1制得的乳双歧杆菌发酵溶胞物对hsf细胞进行细胞修复后细胞内sod活力测试图;
55.图7为本发明实施例1制得的乳双歧杆菌发酵溶胞物对hsf细胞进行细胞修复后细胞内cat活力测试图;
56.图8为本发明实施例1制得的乳双歧杆菌发酵溶胞物对hsf细胞进行细胞修复后细胞内col
‑
1含量测试图;
57.图9为本发明实施例1制得的乳双歧杆菌发酵溶胞物处理皮肤后,皮肤含水量随时间变化趋势图;
58.图10为本发明实施例1和实施例3制得的乳双歧杆菌发酵溶胞物总抗氧化能力结果图。
具体实施方式
59.下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。
60.下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
61.下述实施例中全脂乳粉为购买于安徽轻工国际贸易股份有限公司的新西兰全脂乳。
62.下述实施例中,mrs肉汤液体培养基的配方为:肉汁10g,蛋白胨5g,酵母粉3g,d(+)
‑
葡萄糖5g,淀粉1g,nacl 5g,naac 3g,l
‑
半胱氨酸盐酸盐0.5g,蒸馏水1.0l;mrs肉汤液体培养基的配方中添加15g琼脂后,即得mrs肉汤固体培养基。
63.下述实施例1中使用的乳酸菌为danisco公司生产的产品编号为1261259的乳双岐杆菌,其对应的乳酸菌菌液1的制备方法包括如下步骤:
64.(1)菌种的活化:将乳双歧杆菌接种于mrs肉汤固体培养基中进行划线活化,于37℃培养箱中培养72h,获得单菌落;
65.(2)菌种的扩大培养:将步骤(1)获得的单菌落接种至100ml mrs肉汤液体培养基中,在43℃恒温培养箱中培养48h,得到乳酸菌菌液1,具体为乳双歧杆菌菌液1,其浓度为107cfu/ml。
66.下述实施例2中使用的乳酸菌为京川秀科技有限公司生产的双歧杆菌酸奶发酵菌粉,对应的乳双歧杆菌菌液2的制备方法与实施例1中乳双歧杆菌菌液1的制备方法相比,区别仅在于将实施例步骤(1)中接种的乳双歧杆菌不同。
67.实施例1
68.发酵底物的制备方法包括如下步骤:取适量全脂乳粉加入水中,在80℃条件下灭菌20min,得到发酵底物;发酵底物中全脂乳粉的质量百分比为5%;
69.采用上述方法制得的乳双歧杆菌菌液1和发酵底物为原料,制得乳双歧杆菌发酵溶胞物,具体包括如下步骤:将15ml乳双歧杆菌菌液1接种到300ml的发酵底物中,在温度为
43℃条件下发酵培养10小时;制得的物料转移到超声波细胞破碎仪中进行超声,用于破碎乳双歧杆菌,采用间歇超声的方式,每间隔10s超声2s,间隔和超声的总时间为20min,超声的功率为20%,超声后物料用孔径为0.45μm的过滤器进行过滤,收集滤液;滤液再于90℃条件下灭菌30min;灭菌后,降温,在65℃条件下与防腐剂(包括对羟基苯乙酮和1,2
‑
己二醇,对羟基苯乙酮占灭菌后制得物料的质量百分数为0.5%,1,2
‑
己二醇占灭菌后制得物料的质量百分数为0.5%)混合,制得乳酸菌发酵溶胞物,具体为乳双歧杆菌发酵溶胞物,乳双歧杆菌发酵溶胞物的折光率为1.342。
70.实施例2
71.与实施例1相比,区别仅在于将乳双歧杆菌菌液1替换为乳双歧杆菌菌液2,其他条件参数同实施例1,制得乳酸菌发酵溶胞物,乳酸菌发酵溶胞物的折光率为1.340。
72.实施例3
73.发酵底物的制备方法包括如下步骤:取适量全脂乳粉加入水中,在80℃条件下灭菌20min,得到发酵底物;发酵底物中全脂乳粉的质量百分比为2%;
74.采用上述方法制得的乳双歧杆菌菌液1和发酵底物为原料,制得乳双歧杆菌发酵溶胞物,具体包括如下步骤:将15ml乳双歧杆菌菌液1接种到300ml的发酵底物中,在温度为43℃条件下发酵培养8小时;制得的物料转移到超声波细胞破碎仪中进行超声,用于破碎乳双歧杆菌,采用间歇超声的方式,每间隔10s超声2s,间隔和超声的总时间为20min,超声的功率为20%,超声后物料用孔径为0.45μm的过滤器进行过滤,收集滤液;滤液再于90℃条件下灭菌30min;灭菌后,降温,在65℃条件下与防腐剂(包括对羟基苯乙酮和1,2
‑
己二醇,对羟基苯乙酮占灭菌后制得物料的质量百分数为0.5%,1,2
‑
己二醇占灭菌后制得物料的质量百分数为0.5%)混合,制得乳酸菌发酵溶胞物,具体为乳双歧杆菌发酵溶胞物,乳双歧杆菌发酵溶胞物的折光率为1.340。
75.效果实施例1超氧阴离子自由基清除率
76.将上述实施例1和实施例2制得的乳酸菌发酵溶胞物进行梯度稀释,分别配置成浓度为5g/l、10g/l、15g/l、20g/l和25g/l的实施例1待测液或实施例2待测液。
77.以5g/l实施例1待测液为例,其配置方法包括如下:取5g乳双歧杆菌发酵溶胞物,加水,配置成体积为1l的实施例1待测液,即可。
78.取0.05mol/l ph值为8.2的tris
‑
hcl缓冲液4.5ml于试管中,置于25℃水浴中预热20min;分别加入1ml不同浓度的待测液(实施例1待测液或实施例2待测液)和0.4ml浓度为25mmol/l的邻苯三酚溶液(由10mmol/l的hcl配制),混匀后于25℃水浴中反应5min;加入1ml浓度为8mol/l的盐酸终止反应,制得样品试液;空白组以0.1ml去离子水代替样品试液;以tris
‑
hcl缓冲液作参比,在299nm处测定吸光度,计算超氧阴离子自由基清除率,每个处理均3次重复,计算结果见表1和图1。超氧阴离子自由基清除率=(a1‑
a2)/a1×
100%;式中,a1为空白吸光度,a2为样品试液吸光度。
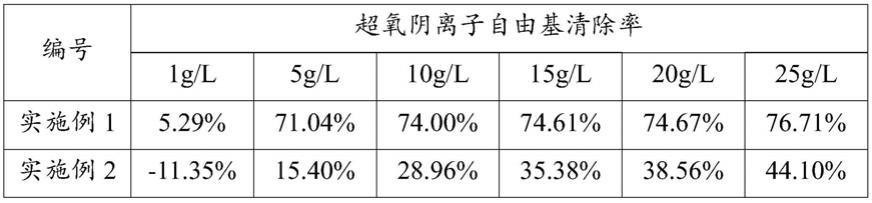
79.表1
[0080][0081]
结果可看出,实施例1制得乳双歧杆菌发酵溶胞物的超氧阴离子自由基清除率显著提高,具有更理想的抗氧化能力。
[0082]
效果实施例2乳酸菌发酵溶胞物对hsf细胞的保护作用
[0083]
取10g上述实施例1
‑
2制得的乳双歧杆菌发酵溶胞物,分别添加无血清的dmem培养液,定容至1l,分别配置成浓度为10g/l的实施例1待测液和浓度为10g/l的实施例2待测液;
[0084]
阳性对照组vc待测液的配置:以无血清的dmem培养液为溶剂,配制浓度为86mg/l的vc待测液。
[0085]
计数hsf细胞(人皮肤成纤维细胞),稀释细胞,最终加入96孔培养板中的细胞密度为1
×
104个/孔,在37℃,5%co2环境下培养过夜,吸弃旧培养基,阳性对照组中添加上述制得的86mg/l的vc待测液,实验组中分别添加上述制得的实施例1待测液或实施例2待测液,阴性对照组和空白组添加dmem培养基,添加后培养24h;培养后,阳性对照组、阴性对照组和实验组中加入100μmol/l h2o2处理细胞2h,空白对照组添加等量dmem代替,h2o2处理后吸弃旧液,用pbs洗3次,在显微镜下观察细胞形态,结果见图2所示。再用mtt法检测培养后hsf细胞的活性,结果见表2和图3,具体为向pbs洗后的板中添加mtt溶液,每孔加入100μl的mtt溶液(1g/l),放入细胞培养箱中孵育4h;弃mtt溶液后每孔加入150μl的dmso,培养箱中放置10min,采用infinite m200pro荧光酶标仪测定各孔od
490
值,每组设置5个副孔,取平均值。
[0086]
hsf细胞存活率(%)=(样品孔od值
‑
空白孔od值)/(空白对照组od值
‑
空白孔od值)
×
100%。此处空白孔是指培养板中不进行任何操作,只添加等量dmso的空白孔。
[0087]
表2
[0088]
编号hsf细胞存活率空白对照组100%阳性对照组50.5%阴性对照组63.4%实施例1103.7%实施例299.8%
[0089]
从表2、图2和图3可看出,阴性对照组中hsf细胞存活率较空白对照组明显减少,且细胞变细变短,可见h2o2对细胞具有较强的杀伤力。实施例1乳双歧杆菌发酵溶胞物可有效提高细胞存活率,结果比空白对照组更佳;与空白对照组相比,经实施例2制得的乳酸菌发酵溶胞物也可有效提高细胞存活率,效果比实施例1略差。
[0090]
效果实施例3实施例1制得的乳双歧杆菌发酵溶胞物对hsf的修复作用
[0091]
实验组待测液配置:取5g上述实施例1制得的乳双歧杆菌发酵溶胞物,加入无血清的dmem培养液,定容至1l,稀释成浓度为5g/l的待测液;
[0092]
阳性对照组vc待测液配置:以无血清的dmem培养液为溶剂,配制成浓度为86mg/l
的vc待测液。
[0093]
计数hsf细胞(人皮肤成纤维细胞),稀释细胞,最终加入96孔培养板中的细胞密度为1
×
104个/孔,在37℃,5%co2环境下培养过夜,吸弃旧培养基后,阴性对照组、阳性对照组和实验组先以100μmol/l h2o2处理细胞2h,吸弃h2o2,用pbs洗3次,空白对照组不进行h2o2处理;之后,阴性对照组加入2ml的dmem培养基作用细胞24h,阳性对照组加入上述制得的2ml的vc待测液作用细胞24h,实验组中加入2ml上述由实施例1制得的乳双歧杆菌发酵溶胞物配置而成的待测液,均作用细胞24h;培养结束后,吸弃旧培养基,用pbs洗两次。平行设置多组实验,其中:
[0094]
一组用于mtt实验测试细胞存活率:每孔加入100μl的mtt溶液(1g/l),放入细胞培养箱中孵育4h;弃mtt溶液后每孔加入150μl的dmso,培养箱中放置10min,采用infinite m200 pro荧光酶标仪测定各孔od
490
值,每组设置5个副孔,取平均值。计算hsf细胞存活率,结果见表3和图4。
[0095]
hsf细胞存活率(%)=(样品孔od值
‑
空白孔od值)/(空白对照组od值
‑
空白孔od值)
×
100%。
[0096]
第二组,用于测定阴性对照组、空白对照组、实施例1实验组中,处理后的细胞中gsh
‑
px的活力、sod活力和cat活力,结果见表3、图5
‑
7。
[0097]
其中,gsh
‑
px的活力、sod活力和cat活力分别采用碧云天生物技术提供的gsh
‑
px检测试剂盒、总sod活性检测试剂盒(wst
‑
8法)和cat检测试剂盒测得。
[0098]
第三组用于测定阴性对照组、阳性对照、空白对照组、实施例1实验组中,被处理后的细胞中col
‑
1的含量,结果见表3和图8。
[0099]
其中,col
‑
1含量检测采用南京建成生物工程研究所提供的i型胶原蛋白(col
‑
i)测试盒测得;通过elisacalc软件分析得到col
‑
1蛋白标准曲线方程;利用标准曲线计算处理后细胞中col
‑
1含量。
[0100]
y=(a
‑
d)/[1+(x/c)^b]+d,其中,a=1.68170,b=1.4621,c=13.65567,
[0101]
d=0.05707,r2=0.99994。
[0102]
表3
[0103][0104]
表中
“‑‑”
表示未测试。
[0105]
结果表明,实施例1制得的乳双歧杆菌发酵溶胞物溶液对受损细胞具有良好的修复作用,而vc对受损细胞没有显著的修复作用。
[0106]
与空白对照组相比,阴性对照组中h2o2刺激极显著的降低hsf细胞内的gsh
‑
px活
力、sod活力、cat活力和col
‑
1含量。与阴性对照组相比,实施例1制得的乳双歧杆菌发酵溶胞物显著的增加了hsf细胞内的gsh
‑
px的活力、sod活力、cat活力和col
‑
1含量。
[0107]
效果实施例4乳双歧杆菌发酵溶胞物保湿功效的测定
[0108]
找30名符合条件的志愿者参加测试。测试场所无光线直射、无风,室温22~24℃,湿度40%~60%。检测前用洗面奶清洗双侧前臂,静息30min,取受试者双侧前臂内侧用记号笔画出5个面积为3.5
×
3.5cm正常皮肤。将3#6#面膜分别剪成3
×
3cm大小,使其浸入实施例1乳双歧杆菌发酵溶胞物待测液中,并分别贴在前臂相应标记处,15min后取下,轻轻用化妆棉沾干测试部位未干的精华液,并开始计时。依次测量使用后5min、20min和60min时五个部位角质层含水量,每个部位测量3次取平均值,结果见表4和图9。
[0109]
表4
[0110]
时间水分含量(c.u.)使用前20.83使用后5min43.75使用后20min33.25使用后60min31.23
[0111]
结果表明,本发明实施例1制得的乳双歧杆菌发酵溶胞物具有良好的保湿功效。
[0112]
效果实施例5人体斑贴试验
[0113]
人体斑贴试验主要是用于检测化妆品终产品或原料的刺激性。根据《化妆品卫生规范》(2015)对实施例1
‑
3制得的乳双歧杆菌发酵溶胞物进行人体封闭式斑贴试验,旨在对其皮肤刺激性进行评估。
[0114]
1、试验对象:
[0115]
严格按照《化妆品接触性皮炎诊断标准及处理原则》要求,选择受试对象,皮肤的待测部位出现瘢痕、鲜红斑痣等影响结果判定的受试者、体质高度敏感者均不能参与试验。本试验选择选择合适的志愿者30人,年龄范围在18
‑
60岁随机选择。
[0116]
2、实验方法
[0117]
分别将0.02ml上述实施例1
‑
3制得的产品滴加在滤纸片上,再将滤纸片置于斑试器内。样品均设置空白对照,即在对照斑试器孔内加入与样品等量的样品溶剂蒸馏水。测试周期持续24h。为了试验结果的准确、可信和科学,在测试期间志愿者按照要求,不能摘掉斑试器,亦不可使受试部位接触水。24h后去除斑试器,静置30min后,等待压痕消失,观察皮肤的反应,接着于24h后观察皮肤的反应。体斑贴试验皮肤不良反应分级标准参见表5。
[0118]
表5皮肤不良反应分级标准
[0119][0120]
3、试验结果
[0121]
参见表6,从表中可以看出;本发明实施例1
‑
3得到的乳双歧杆菌菌发酵溶胞物试敏结果都是阴性反应,说明本发明制得的乳双歧杆菌发酵溶胞物具有安全性,不会给人体带来不良反应。
[0122]
表6
[0123][0124][0125]
效果实施例6总抗氧化能力
[0126]
将上述实施例1和实施例3制得的乳酸菌发酵溶胞物进行梯度稀释,分别配置成浓度为5g/l、10g/l、15g/l、20g/l和25g/l的实施例1待测液或实施例3待测液。
[0127]
以5g/l实施例1待测液为例,其配置方法包括如下:取5g乳双歧杆菌发酵溶胞物,加水,配置成体积为1l的实施例1待测液,即可。
[0128]
先将400ul的abts与400ul氧化剂溶液制备abts工作母液,室温避光存放14小时后以pbs稀释50倍得到abts工作液。
[0129]
标准曲线测定的准备:pbs来稀释标准品,把10mm trolox标准溶液稀释成0.15、0.3、0.6、0.9、1.2和1.5mm。
[0130]
96孔板的每个检测孔中加入200ul的abts工作液,空白对照孔中加入10ul的pbs溶液;标准曲线检测孔内加入10ul各种浓度的trolox标准溶液;样品检测孔内加入10ul各种样品,对照组加入10ul浓度为0.05mg/ml的vc。轻轻混匀。室温孵育4分钟后测定a734。根据标准曲线计算出样品的总抗氧化能力,结果见表7和图10。
[0131]
所得的标准曲线为:y=
‑
0.4357x+0.5565,r=0.9921;
[0132]
表7
[0133]
编号总抗氧化能力teac/mm实施例10.583实施例30.534vc(0.05mg/ml)0.544
[0134]
最后,还需要说明的是,在本发明中术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。
[0135]
尽管上面已经通过本公开的具体实施例的描述对本公开进行了披露,但是,应该理解,本领域技术人员可在所附方案的精神和范围内设计对本公开的各种修改、改进或者等同物。这些修改、改进或者等同物也应当被认为包括在本公开所要求保护的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1