一种精准可视化原位构建干细胞凝胶的方法及配套诊疗系统与流程
1.本发明涉及组织器官再生技术领域,具体涉及一种精准可视化原位构建干细胞凝胶的方法及配套诊疗系统。
背景技术:
2.大面积组织缺损的再生修复极为困难,采用自体组织移植会带来出血、感染及新的损伤,且来源有限。近年来,以间充质干细胞(msc)为核心的工程化组织移植治疗大体积病损组织已成为研究热点。但种子细胞由于面临血供重建的困难以及炎症因子、氧自由基等的毒性作用,使得细胞成活困难、组织修复效率低下,为解决这一难题,我们前期通过“介入微循环系统”,将msc、细胞营养泵入组织缺损原位,同时将局部的炎症因子、氧自由基、代谢废物等排出体外,在缺损原位重建了组织再生微环境。但“介入微循环系统”需要施行开放性手术才能植入体内,为了避免施行开放性手术,本发明提出一种精准的可视化原位固化干细胞凝胶及配套诊疗系统,实现精准再生修复效果。
技术实现要素:
3.本发明意在提供一种精准可视化原位构建干细胞凝胶的方法及配套诊疗系统,以实施精准的再生修复。
4.为达到上述目的,本发明采用如下技术方案:一种精准可视化原位构建干细胞凝胶的配套诊疗系统,包括微量注射泵、诊疗套管针和安装于微量注射泵上的注射器;
5.诊疗套管针包括外套管针和输液接头,输液接头与注射器连通,诊疗套管针上设置有光缆,光缆上设置有与诊疗套管针可拆卸连接的光纤座和与外套管针滑动配合的光缆杆,光缆杆包括保护套和位于保护套内的图像导光束、白光导光束和固化导光束;
6.光缆连接有分光器,分光器连接有与图像导电光束配合的摄像装置、与白光导光束配合的白光光源装置和与固化导电光束配合的固化光源装置,摄像装置电连接有显示器。
7.优选的,作为一种改进,诊疗套管针上可拆卸连接有穿刺针,穿刺针的针管部分与外套管针的针管部分相抵。
8.有益效果:将穿刺针伸入至诊疗套管针的外套管针内,可增大外套管针的强度,以便于利用外套管针进行穿刺工作,降低诊疗套管针损坏的几率。
9.优选的,作为一种改进,s1:配置prp/gelma溶液;
10.s2:将配置好的prp/gelma溶液抽取至注射器内,将注射器固定在微量注射泵固定架上,通过设置按钮设置微量注射泵上注射器的注射速度;
11.s3:使用诊疗套管针和穿刺针,穿刺到靶部位一侧,取出穿刺针后,在诊疗套管针上连接光纤座,并在诊疗套管针上连接输液接头且与注射器连通,开启白光光源装置和摄像装置,且显示器上显示摄像装置采集的图像;
12.s4:通过显示器上的图像便能找到组织受损区域,再将诊疗套管的针头部置于组
织缺损部位,通过脚踏开关控制启动微量注射泵同时启动固化光源装置,使得注射器按照设置好的注射速度向诊疗套管针注入prp/gelma溶液,同时接受固化光源照射;prp/gelma溶液逐步填充受损组织并同步固化,直至prp/gelma溶液固化成凝胶支架,完全填充缺损部位并牢固粘附在组织缺损部位。
13.优选的,作为一种改进,s1:配置prp/gelma溶液;
14.s2:将配置好的prp/gelma溶液抽取至注射器内,将注射器固定在微量注射泵固定架上,通过设置按钮设置微量注射泵上注射器的注射速度;
15.s3:使用一组诊疗套管针和穿刺针,穿刺到靶部位一侧,取出穿刺针后,在外套管针接口上连接光纤座,再使用另一组诊疗套管针和穿刺针,穿刺到靶部位另一侧,取出穿刺针后,在另一组诊疗套管针上连接输液接头,并在另一组诊疗套管针上连接输液接头且与注射器连通,开启白光光源装置和摄像装置,且显示器上显示摄像装置采集的图像;
16.s4:通过显示器上的图像便能找到组织受损区域,再将诊疗套管的针头部置于组织缺损部位,通过脚踏开关控制启动微量注射泵同时启动固化光源装置,使得注射器按照设置好的注射速度向诊疗套管针注入prp/gelma溶液,同时接受固化光源照射;prp/gelma溶液逐步填充受损组织并同步固化,直至prp/gelma溶液固化成凝胶支架,完全填充缺损部位并牢固粘附在组织缺损部位。
17.优选的,作为一种改进,配置prp/gelma溶液,包括如下步骤:
18.(1)配置0.5%(w/v)光引发剂lap溶液:
19.s11:在电子天平上称量0.05g的lap,装入棕色瓶中;
20.s12:取10mlpbs液,加入装有0.05g的光引发剂的棕色瓶中备用;
21.s13:以40~50℃水浴加热溶解15分钟,期间振荡数次;
22.(2)配置浓度为5%(w/v)gelma溶液:
23.s11:准备两管洁净离心管,分别标记为a与b,均用锡箔纸包裹;
24.s12:在电子天平上分别称量0.25g gelma明胶放入a与b离心管中;
25.s13:用移液枪分别取2.5ml已配好的0.5%(w/v)光引发剂溶液与2.5mlpbs溶液,加入上述a离心管中,振荡使gelma明胶充分浸润;
26.s14:把a离心管以60~70℃水浴避光加热溶解20~30分钟,期间振荡数次;
27.s15:溶解后将gelma溶液立即用0.22微米除菌过滤纸除菌,避光保存,备用;
28.s17:用移液枪分别取2.5ml已配好的0.5%(w/v)光引发剂溶液加入上述b离心管中,振荡使gelma明胶充分浸润;
29.s18:把b离心管以60~70℃水浴避光加热溶解20~30分钟,期间振荡数次,溶解后将gelma溶液立即用0.22微米除菌过滤纸除菌;
30.s19:b离心管中加入无菌兔的prp2.5ml和a离心管中的pbs溶液,充分混匀,成prp/gelma溶液,避光保存,备用。
31.优选的,作为一种改进,(1)制备nb修饰的ha溶液:
32.s11:4
‑
(4
‑
(羟甲基)
‑2‑
甲氧基
‑5‑
硝基苯氧基)丁酸甲酯和乙二胺溶解在甲醇溶液,反应完成后,溶剂在真空条件下蒸发,粗沉淀在甲醇中溶解,用乙酸乙酯重新沉淀三次,滤饼在30℃真空干燥12h,直至出现淡黄色粉末,将透明质酸溶于50ml去离子水中,室温下加入nb,然后加入sigma
‑
aldrich,将混合溶液的ph值调整为4.5,然后加入1
‑
(3
‑
二甲氨基
丙基)
‑3‑
乙基碳二胺盐酸盐,室温搅拌48h,溶液装入分子量3500的透析管中,在含0.1m的nacl的hcl(ph3.5)稀释液中透析2天,再在去离子水中透析2天,用冷冻干燥法得到ha
‑
nb粉末状溶液。
33.(2)配置强粘附力凝胶:
34.s12:按10%gelma,2.5%ha
‑
nb,0.2%lap的含量,将ha
‑
nb粉末状溶液加入至prp/gelma溶液中。
35.该溶液主要成分是甲基丙烯酸甲酯修饰的明胶(gelma)和邻硝基苄基类光扳机分子(nb)修饰的透明质酸(hanb)。光照后gelma上的双键自胶联,形成第一层网络,hanb上的光生醛基与gelma上的氨基反应胶联,形成第二层网络,从而极大的增强了胶体的力学。胶体与组织界面处,hanb的光生醛基与组织上的氨基反应,能增强胶体在湿面组织上的粘附力。这种极强的粘附力可以抵抗290mmhg的压力。
36.优选的,作为一种改进,还包括内套管针,内套管针与外套管针可拆卸连接,内套管针的针管部分位于外套管针的针管部分内,内套管针的针管部分与外套管针的针管部分之间构成间隙。
37.本方案的原理及优点是:(1)白光光源装置将白光通过分光器、光缆、光纤座、光缆杆头部照射出来,然后采集的图像信号通过光缆杆头部、光纤座、光缆、分光器到达摄像装置,摄像装置将采集到的光信号转化为电子信号并在显示器上显示,通过显示器上的图像便能找到组织受损区域,再将诊疗套管针头部置于受损组织上方,如此可以精准的找到组织受损位置,达到精准定位的目的。
38.(2)微量注射泵内驱动电机带动注射器按照设置好的速度输液,凝胶溶液经注射器、输液管、输液接头到达诊疗套管针,通过诊疗套管针内部管路从针头部分到达组织受损区域,如此达到精准注入凝胶的目的。
39.(3)凝胶填充受损组织完毕后,启动固化光源装置,405nm波段的窄带光从固化光源装置发出,经分光器、光缆从光缆杆部照射到凝胶溶液区域,当照射到凝胶溶液的能量达到一定程度的时候,凝胶溶液就会固化成凝胶支架,牢固粘附在组织缺损部位,以提高凝胶成型效率。综上所述,可精准的在组织受损部位实现再生修复技术。
40.(4)现有技术中组织缺损部位面临炎症因子、氧自由基等的毒性作用,使得细胞成活困难、修复效率低下,如中国专利cn104707181a公开的一种介入微循环系统,需要进行开放性手术才能将用于修复的支架安装于组织损缺部位,并且具有一定的手术难度。本方案中为了克服以上问题,进行精准可视化原位构建干细胞凝胶的方法的s1步骤之前,本方案可以:利用一种介入微循环系统的基本原理,将内套管针和外套管针穿刺至组织损缺部位,在内外套管针的针尖接触的靶点部位形成微循环,将细胞营养或生理盐水等通过内套管针泵入组织缺损部位,同时通过外套管针与内套管针之间的间隙将组织损缺部位的炎症因子、氧自由基、代谢废物等排出体外,在这个基础上再进行光固化凝胶成型,并牢固地与周围组织紧密地融为一体,因此我们的操作完全无需开刀,便可以在靶点部位构建组织工程化干细胞凝胶支架。
41.(5)本方案的配套诊疗系统可以用于:(1)各种软组织损伤坏死、颈肩腰腿痛、骨性关节炎、骨关节退行性病变、椎间盘退变、股骨头坏死等的治疗;(2)美容行业对高活性生物凝胶的迫切需求;(3)糖尿病性溃疡、褥疮等的治疗。
42.当然,实施本方案的必不一定需要同时达到以上所述的所有技术效果。
附图说明
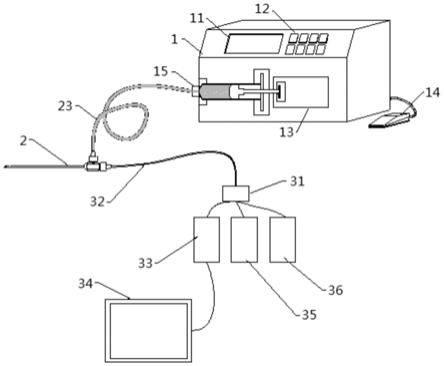
43.图1为本发明实施例一中配套诊疗系统的结构示意图。
44.图2为本发明实施例一中组织修复工作示意图。
45.图3为本发明实施例一、二中外套管针的结构示意图。
46.图4为本发明实施例一、二中穿刺针与外套管针的组合示意图。
47.图5为本发明实施例一、二中诊疗套管针的结构示意图。
48.图6为本发明实施例一、二中光线座示意图。
49.图7为图6的a部分放大图。
50.图8为本发明实施例二中配套诊疗系统的结构示意图。
51.图9为本发明实施例二中组织修复工作示意图。
52.图10为本发明实施例四中诊疗套管针的结构示意图。
具体实施方式
53.下面通过具体实施方式对本发明作进一步详细的说明:
54.说明书附图中的附图标记包括:微量注射泵1、显示屏11、设置按钮12、驱动电机13、脚踏开关14、注射器15、诊疗套管针2、外套管针21、针柄211、针体212、针头213、接口i214、接口ii215、输液接头22、输液管23、光纤座24、堵头25、穿刺针26、分光器31、光缆32、摄像装置33、显示器34、白光光源装置35、固化光光源装置36、光缆杆37、内套管针41。
55.实施例一:
56.基本如附图1至附图7所示,一种精准可视化原位构建干细胞凝胶的配套诊疗系统,包括微量注射泵1,微量注射泵1包括显示屏11、设置按钮12、脚踏开关14以及驱动电机13等,微量注射泵1为现有设备,微量注射泵1上安装有由驱动电机13驱动的注射器15。
57.本实施例中,还包括外套管针21,外套管针21包括针柄211,针柄211上设置有接口i214和接口ii215,针柄211上固定有与接口i214和接口ii215连通的针体212。
58.本实施例中,外套管针21与现有的穿刺针26组合时,如附图4所示,外套管针21与穿刺针26可拆卸连接,并且外套管针21的针体212部分与穿刺针26的针体212部分贴合且相抵。
59.本实施例中,外套管针21构成诊疗套管针2时,如附图5所示,外套管针21的接口i214连通有输液接头22,外套管针21的接口ii215上可拆卸连接有光纤座24,光纤座24上固定有光缆32和光缆杆37,光缆杆37位于针体212内并且从针头213延伸出,光缆杆37包括保护套管,保护套管内包裹有图像导光束、白光导光束和固化导光束。
60.光缆32连接有分光器31,分光器31连接有摄像装置33、白光光源装置35和固化光光源装置36,摄像装置33连接有显示器34。
61.精准可视化原位构建干细胞凝胶的配套诊疗系统构建干细胞凝胶的方法,包括如下步骤:
62.s1:(prp/gelma溶液)凝胶溶液配制:
63.(1)配置0.5%(w/v)光引发剂lap溶液
64.s11:在电子天平上称量0.05g的lap,装入棕色瓶中
65.s12:取10mlpbs液,加入装有0.05g的光引发剂的棕色瓶中备用
66.s13:以40~50℃水浴加热溶解15分钟,期间振荡数次
67.(2)配置浓度为5%(w/v)gelma溶液
68.s11:准备两管洁净离心管,分别标记为a与b,均用锡箔纸包裹,达到避光目的
69.s12:在电子天平上分别称量0.25g gelma明胶放入a与b离心管中
70.s13:用移液枪分别取上述2.5ml已配好的0.5%(w/v)光引发剂溶液与2.5mlpbs溶液,加入上述a离心管中,振荡使gelma明胶充分浸润
71.s14:把a离心管以60~70℃水浴避光加热溶解20~30分钟,期间振荡数次
72.s15:溶解后将gelma溶液立即用0.22微米除菌过滤纸除菌
73.s16:避光保存(常温),备用
74.s17:用移液枪分别取上述2.5ml已配好的0.5%(w/v)光引发剂溶液加入上述b离心管中,振荡使gelma明胶充分浸润
75.s18:把b离心管以60~70℃水浴避光加热溶解20~30分钟,期间振荡数次,溶解后将gelma溶液立即用0.22微米除菌过滤纸除菌
76.s19:b离心管中加入无菌兔的prp2.5ml和a离心管中的液体,充分混匀,成prp/gelma溶液,避光保存,备用。
77.s2:将配制好的prp/gelma溶液抽取到注射器15内。
78.s3:将注射器15固定在微量注射泵1固定架上,通过设置按钮12设置注射器15注射速度,显示器34显示相关设置参数。设置好微量泵参数后,踩下脚踏开关14,驱动电机13按照设置参数控制注射泵输液。断开脚踏开关14则微量泵停止工作。
79.s4:使用1组诊疗套管针2穿刺到组织一侧内部,取出穿刺针26后,在外套管针21接口ii215上连接光纤座24,接口i214连接输液接头22。开启白光光源装置35,白光光源装置35将白光通过分光器31、光缆32、光纤座24、光缆杆37头部照射出来,然后采集的图像信号通过光缆杆37头部、光纤座24、光缆32、分光器31到达摄像装置33,摄像装置33将采集到的光信号转化为电子信号并在显示器34上显示。
80.s5:通过显示器34上的图像便能找到组织受损区域,再将诊疗套管针的针头213部置于组织缺损部位,通过脚踏开关14控制启动微量注射泵1同时启动固化光源装置,使得注射器15和输液管23按照设置好的注射速度向诊疗套管针2注入prp/gelma溶液,同时接受固化光源照射;prp/gelma溶液逐步填充受损组织并同步固化,直至prp/gelma溶液固化成凝胶支架,完全填充缺损部位并牢固粘附在组织缺损部位。
81.实施例二:
82.实施例二与实施例一的不同之处在于,附图8和附图9所示,不同之处在于s4和s5。
83.s4:使用一组诊疗套管针2穿刺到组织一侧内部,取出穿刺针26后,在外套针接口ii215上连接光纤座24,接口i214连接堵头25。再使用另一组诊疗套管针2穿刺到组织另一侧内部,取出穿刺针26后,在外套针接口ii215上连接输液接头22,接口i214连接堵头25。
84.s5:开启白光光源装置35,白光光源装置35将白光通过分光器31、光缆32、连接诊疗套管针2的光纤座24、光缆杆37头部照射出来,然后采集的图像信号通过光缆杆37头部、光纤座24、光缆32、分光器31到达摄像装置33,摄像装置33将采集到的光信号转化为电子信
号并在显示器34上显示。
85.通过显示器34上的图像便能找到组织受损区域,再将诊疗套管针的针头213部置于组织缺损部位,通过脚踏开关14控制启动微量注射泵1同时启动固化光源装置,使得注射器15和输液管23按照设置好的注射速度向诊疗套管针2注入prp/gelma溶液,同时接受固化光源照射;prp/gelma溶液逐步填充受损组织并同步固化,直至prp/gelma溶液固化成凝胶支架,完全填充缺损部位并牢固粘附在组织缺损部位。
86.实施例三:
87.本实施例提供一种强粘附力凝胶,制备方式包括如下步骤:
88.s1:(prp/gelma溶液)凝胶溶液配制:
89.(1)配置0.5%(w/v)光引发剂lap溶液
90.s11:在电子天平上称量0.05g的lap,装入棕色瓶中
91.s12:取10mlpbs液,加入装有0.05g的光引发剂的棕色瓶中备用
92.s13:以40~50℃水浴加热溶解15分钟,期间振荡数次
93.(2)配置浓度为5%(w/v)gelma溶液
94.s11:准备两管洁净离心管,分别标记为a与b,均用锡箔纸包裹,达到避光目的
95.s12:在电子天平上分别称量0.25g gelma明胶放入a与b离心管中
96.s13:用移液枪分别取上述2.5ml已配好的0.5%(w/v)光引发剂溶液与2.5mlpbs溶液,加入上述a离心管中,振荡使gelma明胶充分浸润
97.s14:把a离心管以60~70℃水浴避光加热溶解20~30分钟,期间振荡数次
98.s15:溶解后将gelma溶液立即用0.22微米除菌过滤纸除菌
99.s16:避光保存(常温),备用
100.s17:用移液枪分别取上述2.5ml已配好的0.5%(w/v)光引发剂溶液加入上述b离心管中,振荡使gelma明胶充分浸润
101.s18:把b离心管以60~70℃水浴避光加热溶解20~30分钟,期间振荡数次,溶解后将gelma溶液立即用0.22微米除菌过滤纸除菌
102.s19:b离心管中加入无菌兔的prp2.5ml和a离心管中的液体,充分混匀,成prp/gelma溶液,避光保存,备用。
103.(3)配置ha
‑
nb溶液:
104.s11:4
‑
(4
‑
(羟甲基)
‑2‑
甲氧基
‑5‑
硝基苯氧基)丁酸甲酯(mnb,0.5g,1.8mmol)和乙二胺(1.1ml,2mmol,sigma
‑
aldrich)溶解在甲醇溶液。反应完成后,溶剂在真空条件下蒸发。粗沉淀在甲醇中溶解,用乙酸乙酯重新沉淀三次。滤饼在30℃真空干燥12h,直至出现淡黄色粉末(0.4g,1.2mmol,66.7%)。将透明质酸(408mg,1mmol二糖单位,镇江东源生物科技有限公司)溶于50ml去离子水中,室温下加入nb(224mg,0.69mmol),然后加入153mg,1mmol,sigma
‑
aldrich。将混合溶液的ph值调整为4.5,然后加入1
‑
(3
‑
二甲氨基丙基)
‑3‑
乙基碳二胺盐酸盐(200mg,1.04mmol,sigma
‑
aldrich),室温搅拌48h。溶液装入分子量3500的透析管中,在含0.1m的nacl的hcl(ph3.5)稀释液中透析2天,再在去离子水中透析2天。用冷冻干燥法得到ha
‑
nb粉末状溶液。
105.s12:按10%gelma,2.5%ha
‑
nb,0.2% lap的含量,将ha
‑
nb粉末状溶液加入至prp/gelma溶液中。该凝胶溶液注入至损缺组织位置时,具有如下效果:该溶液主要成分是
甲基丙烯酸甲酯修饰的明胶(gelma)和邻硝基苄基类光扳机分子(nb)修饰的透明质酸(hanb)。光照后gelma上的双键自胶联,形成第一层网络,hanb上的光生醛基与gelma上的氨基反应胶联,形成第二层网络,从而极大的增强了胶体的力学。胶体与组织界面处,hanb的光生醛基与组织上的氨基反应,能增强胶体在湿面组织上的粘附力。这种极强的粘附力可以抵抗290mmhg的压力。
106.实施例四:
107.实施例四与实施例一的不同之处在于,附图10所示,外套管针21可拆卸连接有内套管针41,以构成诊疗套管针2,内套管针41的针管部分位于外套管针21的针管部分内,内套管针41的针管部分与外套管针21的针管部分之间构成间隙。
108.在进行实施例一中精准可视化原位构建干细胞凝胶的配套诊疗系统构建干细胞凝胶的方法的s1步骤之前,利用一种介入微循环系统的基本原理,将内套管针41和外套管针21穿刺至组织损缺部位,在内套管针41和外套管针21的针尖接触的靶点部位形成微循环,将细胞营养或生理盐水等通过内套管针41泵入组织缺损部位,同时通过外套管针21与内套管针41之间的间隙将组织损缺部位的炎症因子、氧自由基、代谢废物等排出体外,在这个基础上再进行凝胶固化成型,因此我们的操作的无需开刀,便可以在靶点部位构建组织工程化干细胞凝胶支架。
109.以上所述的仅是本发明的实施例,方案中公知的具体技术方案和/或特性等常识在此未作过多描述。应当指出,对于本领域的技术人员来说,在不脱离本发明技术方案的前提下,还可以作出若干变形和改进,这些也应该视为本发明的保护范围,这些都不会影响本发明实施的效果和专利的实用性。本技术要求的保护范围应当以其权利要求的内容为准,说明书中的具体实施方式等记载可以用于解释权利要求的内容。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1