一种肿瘤靶区位移监测方法及设备
1.本发明涉及重离子放疗技术领域,尤其涉及一种肿瘤靶区位移监测方法及设备。
背景技术:
2.癌症治疗中,采用重离子放射治疗因为治愈率高且人性化,迅速普及。70%的肿瘤患者需要在肿瘤发展的不同阶段接受放射治疗(以下简称放疗)。传统的放疗流程中,首先通过ct扫描定位患者体内的肿瘤靶区位置,之后在患者体表覆盖量身定制的热塑膜,并根据ct扫描结果在热塑膜上设置标记点来标记肿瘤的位置,最后放疗过程中放疗射线瞄准热塑膜上的标记点对患者进行放疗。
3.但是由于放疗的时间周期较长,在放疗过程中,且患者的体形会发生明显变化,导致患者在热塑膜下具有一定的活动空间,采用在热塑膜上设置标记点来标记肿瘤的位置的方法会出现一定的误差。当重离子射线照射在健康组织上,不仅会降低治疗效果还会给患者带来额外的副作用。研究表明,在放疗过程中患者体位偏离5mm,放疗疗效就会下降18.4%;偏移6mm疗效会降低33.4%。当偏移量再大则对健康组织的损害就会大于对肿瘤的治疗。因此现在亟须一种方法或者设备来解决在放疗过程中对患者的肿瘤靶区位移进行监测问题。
技术实现要素:
4.针对背景技术中的不足,本发明公开了一种肿瘤靶区位移监测方法,
5.所述方法包括以下步骤:
6.步骤s1:在热塑膜上设置治疗点,其中,治疗点为放疗射线照射的位置;对标志物进行定位,其中,标志物位置对应肿瘤靶区;
7.步骤s2:根据标志物与治疗点的相对位移量计算肿瘤靶区的位移值。
8.优选的,对标志物进行定位的步骤包括:
9.sa101、提取具有物理特征标志物上的特征点;
10.sa102、采用特征点匹配算法匹配实时图像与参考图像中的特征点计算特征点的位移量对所述标志物进行定位。
11.优选的,所述标志物为几何形状标志物;
12.对标志物进行定位的步骤包括:
13.sa111、将标志物与背景进行分割;
14.sa112、采用拟合算法标记标志物轮廓;
15.sa113、确定标志物几何中心位置,对所述标志物进行定位。
16.优选的,其中标志物的颜色采用三原色之一;
17.步骤sa111具体包括以下步骤:
18.sa1111、将采集的彩色图像分别拆分成红色、绿色和蓝色三个通道的三个灰度图像;
19.sa1112、将图像中通过标志物颜色通道对应像素的灰度值减去通过其他两个通道对应像素的灰度值。
20.优选的,所述步骤sa112具体包括:
21.sa1121:用canny算法对包含标志物的灰度图计算轮廓;
22.sa1122:剔除轮廓中面积小于设定阈值的轮廓;
23.sa1123:对每个标志物的所有轮廓求取凸包,计算得到所述标志物的外轮廓。
24.优选的,步骤sa113具体包括以下步骤:
25.sa1131:提取所述标志物外轮廓上的点;
26.sa1132:采用最小二乘法拟合椭圆;
27.sa1133:计算所有拟合点到拟合椭圆中心的距离,采用格拉布斯准则剔除距离异常的噪声点;
28.sa1134:再次采用最小二乘法拟合椭圆;
29.sa1135:判断是否含有噪声点;若含有噪声点则跳转回步骤sa1133,若不存在噪声点则以椭圆中心定位标志物。
30.优选的,所述方法还包括步骤sa1136:以椭圆中心为中心,长宽以椭圆轴的预设倍数的矩形区域为下一帧图像的感兴趣区域,其中所述感兴趣区域表示之后的图像仅在所述感兴趣区域内进行椭圆拟合。
31.本发明的另一实施例中还公开了一种肿瘤靶区位移监测设备,所述设备包括:
32.图像采集单元,用于采集图像,其中所述图像采集单元同轴安装小发散角的环形光源,并且处置与所述标志物设置;
33.标志物,用于定位肿瘤位置,其中标志物表面附有微棱镜型反光膜;
34.图像处理单元,用于对图像进行处理计算得到肿瘤靶区位移信息。
35.在本发明的另一实施例中还公开了一种计算机可读存储介质,介质上存有计算机程序,计算机程序运行后执行任一项所述的肿瘤靶区位移监测方法。
36.本发明的另一实施例中还公开了一种计算机设备,包括处理器、存储介质,存储介质上存有计算机程序,处理器从存储介质上读取并运行计算机程序以执行任一项所述的肿瘤靶区位移监测方法。
37.有益效果:
38.(1)通过在热塑膜上设置治疗点和设置与肿瘤靶区位置实时对应的标志物,根据治疗点和标志物的相对位移实时计算肿瘤靶区的位移值,实现对肿瘤靶区位移的监测,提高放疗效果。
39.(2)提取标志物上的标志点可以根据标志点的位移量对标志物进行定位。
40.(3)将标志物与背景切割后可以更加精准的拟合标志物轮廓。
41.(4)省去了色彩空间转换的步骤,也无需考虑在不同光照条件下各分量阈值的选取。
42.(5)剔除轮廓小于设定阈值的轮廓可以提高定位标志物时的精度。
43.(6)考虑到了人体的立体情况,剔除噪声点,提高定位的精准度。
44.(7)考虑到在热塑膜的固定下,患者位移较小,限定了采集图像的区域,使得定位更加精准、快速。
附图说明
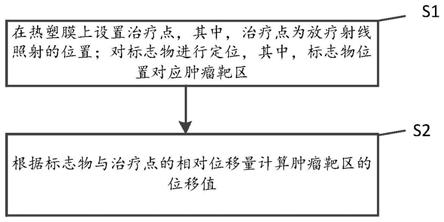
45.图1为本发明一实施例中肿瘤靶区位移监测方法的流程图;
46.图2为本发明一实施例中对标志物进行定位的流程图;
47.图3为本发明一实施例中拟合标志物并获取标志物中心位置进行定位的流程图;
48.图4为本发明实施例中肿瘤靶区位移监测设备的工作示意图;
49.图5a为本发明实施例中标志物附有微棱镜型反光膜时的环形光源发出的光线路径示意图;
50.图5b为当标志物发生漫反射时环形光源发出的光线路径示意图;
51.图6为本发明实施例中标志物的分布图;
52.图7a为当标志物为x角点形时,定位热塑膜下的标志物的示意图;
53.图7b为当标志物为矩形时,定位热塑膜下的标志物的示意图;
54.图7c为当标志物为圆形时,定位热塑膜下的标志物的示意图。
55.图中:1、工业相机;2、标志物;21、微棱镜型反光膜;3、患者体膜;4、环形光源;5、支架。
具体实施方式
56.针对上述问题,本发明一实施例中公开了一种肿瘤靶区位移监测方法,具体的,在通过ct扫描到患者体内的肿瘤位置后,在患者体表的肿瘤位置固定标志物,同时在热塑膜上设置治疗点,在第一次进行放疗治疗时,治疗点的位置于所述标志物的位置相同,均对应患者体内的肿瘤位置。当进行下一次放疗时,由于患者的体形或体位发生变化,所述治疗点所对应的患者体表位置会出现偏差,所述治疗点的位置不再对应患者体内的肿瘤位置。而由于标志物是固定在患者体表上,随着患者体形发生变化,所述标志物的位置也会发生变化,因此在下一次放疗时所述标志物所处的位置依旧对应患者体内的肿瘤位置。从热塑膜上设置的透气孔可以对标志物进行定位,根据标志物与治疗点的相对位移量可以准确计算肿瘤靶区的位移量,得到新的治疗点。即根据标志物可以准确的定位到患者体内肿瘤位置,不需要重新进行ct扫描,也不需要重新量体定制新的热塑膜。由上述可知,通过本发明可以较好的解决由于患者体形发生变化导致治疗点与患者体内肿瘤位置发生偏差的问题,另外患者如果在治疗过程中,在热塑膜中移动位置,也可以第一时间对治疗位置进行调整。
57.以下将结合附图对本发明进行详细描述,如图1所示。
58.步骤s1:在热塑膜上设置治疗点,其中,治疗点为放疗射线照射的位置;对标志物进行定位,其中,标志物位置对应肿瘤靶区。
59.具体的,在进行放疗时为了避免患者体位移动,采用热塑膜对患者的体位进行固定。热塑膜根据患者体形一次成型,后期无法进行调整。为了确定肿瘤靶区的位置,在热塑膜上设置治疗点,在进行放疗时,放射射线会瞄准治疗点位置进行放射性照射,以此来对患者体内的癌细胞进行灭活。第一次治疗时所述治疗点所代表的位置为肿瘤靶区的位置。由于患者在接受治疗的过程中不能始终保持一个相对静止的状态,所以需要对治疗点进行动态调整。
60.示例性的,标志物固定在患者体表,例如,可以将标志物粘贴在患者体表。其位置对应患者体内的肿瘤位置,即肿瘤靶区。当患者体形或体位发生变化时,固定在患者体表的
标志物位置会随着一起移动,标志物所对应的位置依旧是患者体内的肿瘤位置。标志物固定与患者体表上,被热塑膜所覆盖,无法通过肉眼观察到,只能通过热塑膜上的透气孔才能观察到标志物部分信息。因此对标志物进行准确定位显得尤为重要,对标志物的定位相关内容将在本发明的其他实施例中进行详细描述。
61.步骤s2:根据标志物与治疗点的相对位移量计算肿瘤靶区的位移值。
62.具体的,根据标志物在治疗过程中的相对位移量定位放疗射线照射的位置,以开始治疗点的位置为起始位置,治疗过程中标志物与治疗点的相对位移量为偏差区调整治疗点的位置,即放射性光线的照射位置。
63.示例性的,患者体形或者体位发生变化时标志物的位置会相应发生变化,但是热塑膜上的治疗点不会发生变化。因此当患者体形发生变化时,通过对标志物进行定位,然后计算原标志物和治疗点的相对位移量,可以得出肿瘤靶区相对于原治疗点的位移值,得出位移值后只需要根据位移值简单改变治疗点的位置记得准确定位到肿瘤靶区,对患者体内的肿瘤细胞进行精准打击。例如,以原始治疗点为坐标原点,标志物位移后的坐标为(x,y)。则后续放疗过程中,则对点(x,y)进行治疗。在实际治疗过程中肿瘤靶区为一个区域,在后续治疗过程中,肿瘤靶区的区域形状保持不变,其中点(x,y)可以为肿瘤靶区的中心点,也可以为肿瘤靶区内任意一点,只需要保持前后治疗过程中点(x,y)的肿瘤靶区内的相对位置保持不变即可。
64.在本发明的另一实施例中所述标志物为几何形状标志物;如图2所示,所述对标志物进行定位包括:
65.步骤sa111:将标志物与背景进行分割;
66.步骤sa112:采用拟合算法标志物轮廓;
67.步骤sa113:确定标志物几何中心位置,对所述标志物进行定位。
68.具体的,由于在放疗过程中标志物被热塑膜遮挡了一大部分,无法通过光学追踪观察到完整的标志物,从热塑膜透气孔中漏出的小部分标志物轮廓。因此需要将标志物轮廓与背景分割开,才能对标志物进行定位。
69.本实施例中利用标志物的颜色特征来进行分割。标志物的颜色采用三原色之一,具体包括如下步骤:
70.sa1111:将采集的彩色图像分别拆分成红色、绿色和蓝色三个通道的三个灰度图像;
71.sa1112:将图像中通过标志物颜色通道对应像素的灰度值减去通过其他两个通道对应像素的灰度值。
72.值得解释的是,由于工业相机采集到的彩色图像一般是rgb图像,rgb色彩空间用r、g、b三个分量分别描述一个颜色中红色、绿色和蓝色所占的比例来描述颜色。三个分量亮度值取值范围均为0-255,数值越大则说明该像素点中这一颜色分量所占比例越高。例如,所述标志物采用三原色之一的蓝色,将采集的彩色图像分别拆分成红色、绿色和蓝色三个通道的三个灰度图像后,由于图像背景仅包含白色和肤色,而目标物为蓝色。白色中红色分量和蓝色分量相同,不同人种的肤色主要是亮度差别,肤色的色度差别不大,均为红色分量大于蓝色分量,然而蓝色标志物的蓝色分量远大于红色分量。因此在蓝色通道的灰度图像里,标志物的亮度值明显偏高,因此将彩色图像中通过蓝色通道对应像素的灰度值减去通
过红色通道和绿色通道对应像素的灰度值即可去除背景杂色。相比起常见的在hsv色彩空间的目标分割,该方法充分利用了放疗监测范围内背景的色彩特征,省去了色彩空间转换的步骤,也无需考虑在不同光照条件下各分量阈值的选取。
73.得到剔除背景后仅包含标志物的灰度图像。拟合定位标志物需要标志物外轮廓上的点,因此在分离出标志物后还需要提取出标志物外轮廓上的点。具体的,所述步骤s22具体包括以下步骤:
74.步骤sa1121::用canny算法对包含标志物的灰度图计算轮廓;
75.步骤sa1122:剔除轮廓中面积小于设定阈值的轮廓;
76.步骤sa1123:对每个标志物的所有轮廓求取凸包,计算得到所述标志物的外轮廓。
77.通过步骤sa1122可以去除标志物分割后图像中的噪声点。此时得到的轮廓并非标志物最外层的轮廓,而是标志物被热塑膜遮挡后形成的许多个小的轮廓,需要对每个标志物的所有轮廓求取凸包,在步骤sa1123中采用graham扫描算法求取标志物轮廓的凸包,凸包的顶点就是标志物外轮廓上的点。graham扫描算法的用时与轮廓点的个数n正相关,n越大算法用时越长,因此将标志物设计为圆环可以减少算法用时,更好的保证实时性。
78.因为定位标志物只需要标志物的外轮廓信息,为了减少定位标志物时的运算量,在本发明另一实施例中对标志物中间部分的信息进行省略。提取标志物轮廓,然后采用拟合算法得出标志物的形状,然后就能确定标志物的几何中心位置,对所述标志物进行定位,即可得出肿瘤靶区的位置。
79.示例性的,在本实施例中所述标志物为圆环标志物,并且所述圆环标志物的环宽不小于所述热塑膜小孔之间的遮挡部分。例如,如图6所示,一般医用热塑膜小孔之间遮挡部分的宽度为2mm,可以将圆环标志物的环宽设置为3mm,保证始终有部分标志物漏出,避免由于标志物被遮挡导致标志物定位失败,并且将多个圆环标志物采用90mm*90mm的矩阵排列。示例性的,所述圆环标志物采用直径3mm的圆围成一个圆环,根据数学知识可知圆上三个点即可确定圆的位置,即只需要在热塑膜上找到标志物上的三个点即可定位出标志物的位置。相比较与矩形标志物需要定位出四条边才能定位出标志物的具体位置需要定位的点更少,更方面定位出标志物的位置。如图7a、图7b和图7c可知,x角点的标志物无法通过热塑膜进行定位,而矩形标志物当矩形平行的两条边被遮挡时,图中的三个不同位置的矩形具有相同的露出轮廓,即由矩形的外轮廓无法复原唯一的矩形标志物,从而无法准确定位。只有圆形(或圆环)标志物仅由三个点即可确定唯一确定的一个圆,因此将标志物设计成圆形(或圆环)可以最大限度减少热塑膜遮挡对标志物定位的影响。需要说明的是图7a、图7b和图7c中实线圆为热塑膜的透气孔,虚线代表在热塑膜下的标志物轮廓。
80.在本发明公开的另一实施例中对标志物进行定位的步骤包括:
81.sa101、提取具有物理特征标志物上的特征点;
82.sa102、采用特征点匹配算法匹配实时图像与参考图像中的特征点计算特征点的位移量对所述标志物进行定位。
83.具体的,标志物具有明显的物理特征,在对此类标志物进行定位时,对标志物上的特征点进行提取。示例性的,提取标志物特征点采用harris角点检测算法,提取特征点后采用特征点匹配算法匹配实时图像与参考图像中的特征点计算特征点的位移量,以此实现对所述标志物的定位。例如,标志物上存在特征点a,并且特征点a和位于标志物的特定部位
上。在监测特征点时监测到特征点a,由于标志物的形状已知,通过特征点a的位移量即为标志物的位移量,根据标志物的位移量即可对标志物进行定位。
84.本发明另一实施例中公开了定标志物几何中心位置,对所述标志物进行定位的具体步骤,具体如图3所示:
85.步骤sa1131:提取所述标志物外轮廓上的点;
86.步骤sa1132:采用最小二乘法拟合椭圆;
87.步骤sa1133:计算所有拟合点到拟合椭圆中心的距离,采用格拉布斯准则剔除距离异常的噪声点;
88.步骤sa1134:再次采用最小二乘法拟合椭圆;
89.步骤sa1135判断是否含有噪声点;若含有噪声点则跳转回步骤sa1133,若不存在噪声点则以椭圆中心定位标志物。
90.虽然设置的标志物为圆环形状,但是人体表面是立体的,不可能完全水平,使得拍摄到的标志物更接近椭圆环,所以本发明中采用椭圆对标志物进行拟合。标准的最小二乘椭圆拟合算法的原理如下:椭圆的一般方程如公式(1)所示。设图像中共提取到n个待拟合点,第i个待拟合点坐标为pi(xi,yi),(i=0,1,2,
…
,n),令所有待拟合点到椭圆的距离平方和最小,即式(2)取最小值时的椭圆就是最小二乘拟合结果。由极值理论,满足式(3)时式(2)取最小值。求解式(3)所得线性方程组可得拟合椭圆的一般方程的参数a,b,c,d,e,f。由椭圆一般方程的参数由式(4)可得椭圆的中心坐标(x
center
,y
center
)。
91.ax2+bxy+cy2+dx+ey+f=0
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(1)
[0092][0093][0094][0095]
优选的,为了提高最小二乘椭圆拟合算法对标志物进行定位的准确性和实时性。所述拟合标志物并获取标志物中心位置进行定位包括:
[0096]
提取所述标志物外轮廓上的点;
[0097]
采用最小二乘法拟合椭圆;
[0098]
计算所有拟合点到拟合椭圆中心的距离;
[0099]
采用格拉布斯准则剔除距离异常的噪声点;
[0100]
再次采用最小二乘法拟合椭圆,判断是否含有噪声点;若含有噪声点则跳转回采用格拉布斯准则剔除距离异常的噪声点,若不存在噪声点则以椭圆中心定位标志物。
[0101]
经过轮廓筛选后,图像中的大部分噪声被去除,但有时仍有少数提取的标志物外轮廓点并不在标志物外轮廓上,这些噪声点使得传统最小二乘椭圆拟合算法拟合出的椭圆与真实椭圆有较大偏差,因此需要剔除噪声点后重新拟合椭圆。具体的,计算所有待拟合点的x轴坐标和y轴坐标的中值,以此坐标为基准点。计算得到每个待拟合点到基准点之间的代数距离di(i=0,1,2
…
,n),将这组数据看做样本点集,根据格拉布斯准则按照90%的置
信概率剔除样本中的粗差点,并用剩余样本点重新拟合椭圆并检查是否含有粗差点,有粗差点则再剔除,直到没有粗差点,最终剩余的点进行拟合,结果用于标志的定位。
[0102]
优选的,由于患者在热塑膜固定下的位移有限,标志物只出现在图像的一部分区域,因此为了减少不必要的计算,在步骤sa1135后还包括步骤sa1136:截取以拟合的椭圆中心为中心且长宽为椭圆长短轴预设倍数的矩形为感兴趣区域(roi),其中所述感兴趣区域表示之后的图像仅在所述感兴趣区域内进行椭圆拟合。
[0103]
之后的每帧实时图像仅在roi内进行椭圆拟合,这样可以省去图像处理时遍历图像上不必要的像素点,同时待拟合点的坐标相比起以整个图像建立坐标系来说,坐标数值明显减小可以提升椭圆拟合算法的计算速度。
[0104]
本发明的另一实施例中还公开了一种肿瘤靶区位移监测设备,所述设备包括图像采集单元、标志物和图像处理单元。示例性的,所述图像采集单元用于采集图像。例如图像采集单元为工业相机,如图4所示,在工作中,工业相机1采用支架5固定在治疗床6上方,垂直于患者患有肿瘤的部位,对该部位进行拍摄,然后将图像传输至图像处理单元(图中未示出)。所述标志物2用于定位肿瘤位置,为反光材质,固定患者体表,其位置与肿瘤所在位置相对于,用于对肿瘤靶区进行标记,图中标记3为患者模型。所述图像处理单元对接收的图像进行分析处理,最终得出肿瘤靶区位移的结果,为医生治疗提供参考意见。具体的,所述图像处理单元处理图像用于执行上述任意方法实施例中步骤。相比于采用金属标志物通过x射线成型对肿瘤靶区位移进行实时监测,通过本发明所采用的反光标志物不会给患者带来额外的辐射和感染副作用。优选的,为了方便医生操作,所述设备还包括显示单元,所述显示单元与所述图像处理单元连接,将肿瘤靶区的位移进行图像显示。
[0105]
由于标志物反射的光线经过热塑膜遮挡后才能到达相机,大部分光线被热塑膜遮挡使得捕获的图像中,标志物亮度很暗,颜色特征不明显。
[0106]
进一步的,为了方便对标志物进行定位,所述标志物表面附有微棱镜型反光膜21。与所述工业相机同轴安装有小发散角的环形光源4,所述环形光源4垂直照射所述标志物。微棱镜型反光膜是基于立方角锥棱镜的折射和全反射原理制得的反光材料。如图5a和图5b可知,从相机周围发出的小角度光线照射到微棱镜结构后,光线大多数逆反射回相机,对比一般的漫反射材质的标志物,有更多光线反射到相机,使得图像中标志物的亮度提高,易于提取定位。
[0107]
示例性的,本发明的一实施例中,所述设备相关设备的主要参数如下:
[0108]
表1设备的硬件设备及主要参数
[0109]
[0110]
本发明另一实施例中还公开了一种计算机可读存储介质,介质上存有计算机程序,计算机程序运行后执行上述任一实施例中所述的肿瘤靶区位移监测方法。
[0111]
本发明的另一实施例中还公开了一种计算机设备,包括处理器、存储介质,存储介质上存有计算机程序,处理器从存储介质上读取并运行计算机程序以执行上述任一实施例中所述的肿瘤靶区位移监测方法。
[0112]
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1