一种预防鸭传染性浆膜炎三价基因工程亚单位疫苗组合物及其制备方法与流程
1.本发明涉及一种预防鸭传染性浆膜炎三价基因工程亚单位疫苗组合物及其制备方法,属于兽用生物制品领域。
背景技术:
2.鸭传染性浆膜炎,又称鸭疫里默氏杆菌病,是由鸭疫里默氏杆菌(riemerella anatipestifer,ra)引起的细菌性传染病,危害养鸭业的主要疫病之一。1932年,美国学者hendrickson和hilbert首次报道该病,1936年,美国伊利诺斯州的一个商品鸭场发生该病,曾被称为“鸭败血症”,dougherty等科研工作者于1995年经全面病理学研究后,将该病命名为“传染性浆膜炎”。leibovitz提议使用“鸭疫里默氏杆菌感染”名称。我国自1982年郭玉璞等从北京郊区鸭场首次分离到鸭疫里默氏杆菌以来,所有养鸭地区几乎均有该病的发生,鸭、鹅及火鸡等多种禽类易感,是一种接触性传染病,多呈急性或慢性败血症过程,以纤维素性肝周炎、心包炎、气囊炎、干酪性输卵管炎和脑膜炎为主要特征,传播速度快,死亡率较高,对抗生素的耐药性不断增加,疫苗免疫是控制该病的有效方法之一。
3.ra血清型众多,目前世界范围内已确定的有21种,各血清型之间的交叉保护作用差。根据我国学者的血清学研究结果表明流行菌株的优势血清型是血清1、2和10型。然而,目前我国有批准文号的市售疫苗均为1型、2型二价和1型、2型、7型三价灭活疫苗,未有1型、2型、10型疫苗在售,亟需研发一种1型、2型、10型三价疫苗。另外,目前我国商业化的只有灭活疫苗,生产中一般在雏鸭7日龄时注射鸭传染性浆膜炎灭活疫苗,由于疫苗接种后至产生有效保护性免疫应答需要7天或更长时间,所以在这段时期形成了一个免疫空白期,使得雏鸭容易在早期感染传染性鸭浆膜炎。灭活疫苗的免疫原性较差,需要多剂次加强,且在生产过程安全性要求较高,导致生产成本高。
4.因此研制一种生产成本低、生产效率高以及疫苗免疫效果好的预防鸭传染性浆膜炎的疫苗的生产方法具有重要的现实意义。
技术实现要素:
5.为解决上述技术问题,本发明的目的在于提供一种预防鸭传染性浆膜炎三价基因工程亚单位疫苗组合物及其制备方法和应用。该疫苗组合物生产成本低、生产效率高且免疫效果好。
6.为实现上述技术目的,达到上述技术效果,本发明通过以下技术方案实现:
7.本发明的第一个目的是提供一种组合物,所述组合物中含有鸭传染性浆膜炎的tbdr1-t 3、sip-t3、camp、gldg-t3、ompa-t3、trpb及ha-t3重组蛋白;其中tbdr1-t3、sip-t3、gldg-t3、ompa-t3、ha-t3重组蛋白为在tbdr1、sip、gldg、ompa及ha氨基酸序列的基础上,进行截短并进行了多次重复表达。
8.在一种实施方式中,所述tbdr1-t3蛋白的氨基酸序列如seq id no.1所示,si-t3p
蛋白片段的氨基酸序列如seq id no.3所示,camp蛋白片段的氨基酸序列如seq id no.5所示,gldg-t3蛋白片段的氨基酸序列如seq id no.7所示;ompa-t3蛋白片段的氨基酸序列如seq id no.9所示,trpb蛋白片段的氨基酸序列如seq id no.11所示,ha-t3蛋白片段的氨基酸序列如seq id no.13所示。
9.在一种实施方式中,编码所述tbdr1-t3蛋白的基因的核苷酸序列如seq id no.2所示,编码所述sip-t3蛋白的基因的核苷酸序列如seq id no.4所示,编码所述camp蛋白的基因的核苷酸序列如seq id no.6所示;编码所述gldg-t3蛋白的基因的核苷酸序列如seq id no.8所示,编码所述ompa-t3蛋白的基因的核苷酸序列如seq id no.10所示,编码所述trpb蛋白的基因的核苷酸序列如seq id no.12所示,编码所述ha-t3蛋白的基因的核苷酸序列如seq id no.14所示。
10.在一种实施方式中,所述组合物中的tbdr1-t3、sip-t3、camp、gldg-t3、ompa-t3、trpb及ha-t3重组蛋白的总含量为50~150μg/ml。
11.在一种实施方式中,所述组合物中的tbdr1-t3、sip-t3、camp、gldg-t3、ompa-t3、trpb及ha-t3重组蛋白的比例为1:1:1:1:1:1:1。
12.本发明的第二个目的是提供上述组合物在制备预防鸭传染性浆膜炎三价基因工程亚单位疫苗中的应用。
13.在一种实施方式中,所述三价基因工程亚单位疫苗还包括佐剂。
14.在一种实施方式中,所述佐剂包括但不限于:铝盐佐剂、脂质体佐剂、纳米颗粒佐剂、皂苷佐剂。
15.在一种实施方式中,所述三价基因工程亚单位疫苗中的佐剂为矿物油佐剂。
16.在一种实施方式中,所述三价基因工程亚单位疫苗的给药方式包括肌内、皮内或皮下给药。
17.本发明的第三个目的是提供一种预防鸭传染性浆膜炎三价基因工程亚单位疫苗,所述疫苗中含有鸭传染性浆膜炎的tbdr1-t3、sip-t3、camp、gldg-t3、ompa-t3、trpb及ha-t3重组蛋白;其中tbdr1-t3、sip-t3、gldg-t3、ompa-t3、ha-t3重组蛋白为在tbdr1、sip、gldg、ompa及ha氨基酸序列的基础上,进行截短并进行了多次重复表达。
18.在一种实施方式中,所述tbdr1-t3蛋白的氨基酸序列如seq id no.1所示,si-t3p蛋白片段的氨基酸序列如seq id no.3所示,camp蛋白片段的氨基酸序列如seq id no.5所示,gldg-t3蛋白片段的氨基酸序列如seq id no.7所示;ompa-t3蛋白片段的氨基酸序列如seq id no.9所示,trpb蛋白片段的氨基酸序列如seq id no.11所示,ha-t3蛋白片段的氨基酸序列如seq id no.13所示。
19.在一种实施方式中,所述预防鸭传染性浆膜炎三价基因工程亚单位疫苗中的tbdr1-t3、sip-t3、camp、gldg-t3、ompa-t3、trpb及ha-t3重组蛋白的总含量为50~150μg/ml。
20.在一种实施方式中,所述预防鸭传染性浆膜炎三价基因工程亚单位疫苗中的tbdr1-t3、sip-t3、camp、gldg-t3、ompa-t3、trpb及ha-t3重组蛋白的比例为1:1:1:1:1:1:1。
21.在一种实施方式中,所述预防鸭传染性浆膜炎三价基因工程亚单位疫苗还包括佐剂。
22.在一种实施方式中,所述佐剂包括但不限于:铝盐佐剂、脂质体佐剂、纳米颗粒佐剂、皂苷佐剂。
23.在一种实施方式中,所述预防鸭传染性浆膜炎三价基因工程亚单位疫苗中的佐剂为矿物油佐剂。
24.在一种实施方式中,所述预防鸭传染性浆膜炎三价基因工程亚单位疫苗的给药方式包括肌内、皮内或皮下给药。
25.本发明的第四个目的是提供一种制备所述预防鸭传染性浆膜炎三价基因工程亚单位疫苗组合物的方法,所述方法的具体步骤如下:
26.(1)将编码tbdr1-t3、sip-t3、camp、gldg-t3、ompa-t3、trpb及ha-t3蛋白的基因的核苷酸序列分别连接至至pfastbac i载体,获得重组质粒ra-a、ra-b、ra-c、ra-d、ra-e、ra-f和ra-g;
27.(2)将步骤(1)得到的重组质粒ra-a~ra-g分别转化dh10 bac感受态细胞,获得重组杆粒rbacmid-ra-a、rbacmid-ra-b、rbacmid-ra-c、rbacmid-ra-d、rbacmid-ra-e、rbacmid-ra-f和rbacmid-ra-g;
28.(3)将步骤(2)获得的重组杆粒rbacmid-ra-a~rbacmid-ra-g分别转染昆虫细胞,获得重组杆状病毒rra-a、rra-b、rra-c、rra-d、rra-e、rra-f和rra-g;
29.(4)将步骤(3)获得的重组杆状病毒rra-a~rra-g分别接种hf细胞进行大量培养,离心收集培养液上清,得到tbdr1-t3、sip-t3、camp、gldg-t3、ompa-t3、trpb及ha-t3重组蛋白。
30.(5)将步骤(4)的重组蛋白经过纯化,加入佐剂,乳化,最后混匀制备得到鸭传染性浆膜炎三价基因工程亚单位疫苗组合物。
31.在一种实施方式中,所述佐剂包括但不限于:铝盐佐剂、脂质体佐剂、水包油佐剂、油包水佐剂、纳米颗粒佐剂、皂苷佐剂。
32.在一种实施方式中,所述三价基因工程亚单位疫苗组合物中的佐剂为矿物油佐剂。
33.在一种实施方式中,所三价基因工程亚单位疫苗组合物中的tbdr1-t3、sip-t3、camp、gldg-t3、ompa-t3、trpb及ha-t3重组蛋白的总含量为50~150μg/ml。
34.在一种实施方式中,所述三价基因工程亚单位疫苗组合物中的tbdr1-t3、sip-t3、camp、gldg-t3、ompa-t3、trpb及ha-t3重组蛋白的比例为1:1:1:1:1:1:1。
35.本发明还提供了所述组合物和所述预防鸭传染性浆膜炎三价基因工程亚单位疫苗在制备预防和/或治疗鸭疫李默氏杆菌病相关疾病或由鸭疫李默氏杆菌病感染的相关疾病的药物中的应用。
36.本发明的有益效果是:
37.1、本发明对1型、2型和10型鸭疫李默氏杆菌的共同抗原抗原蛋白tbdr1、sip、gldg、ompa及ha进行截短和多重表达,将获得的片段tbdr1-t3、sip-t3、gldg-t3、ompa-t3及ha-t3与camp和trpb共同构建获得预防鸭传染性浆膜炎三价基因工程亚单位疫苗组合物。其免疫效果良好,免疫剂量小,一次接种就能有效预防鸭疫李默氏杆菌病相关疾病或由鸭疫李默氏杆菌病感染相关疾病。
38.2、本发明提供的1型、2型和10型三价基因工程亚单位疫苗组合物的制备方法简
单,能大量制备鸭疫李默氏杆菌病的抗原蛋白,耗时短,表达量高,大大降低了生产成本,有利于大规模生产,填补了现有市售鸭传染性浆膜炎疫苗中1型、2型和10型三价疫苗的空白。
附图说明
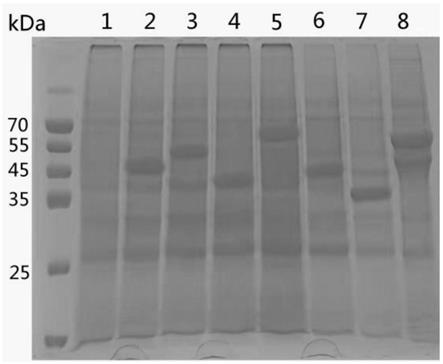
39.图1是sds-page检测重组杆状病毒表达产物;1:对照;2:tbdr1-t3;3:sip-t3;4:camp;5:gldg-t3;6:ompa-t3;7:trpb;8:ha-t3。
具体实施方式
40.以下结合说明书附图和具体实施例来进一步说明本发明,但实施例并不对本发明做任何形式的限定。除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。
41.除非特别说明,以下实施例所用试剂和材料均为市售商品或者可以通过已知方法制备。
42.下述实施例中涉及到的实验材料
43.鸭疫里默氏杆菌均由扬州优邦生物药品有限公司分离、鉴定、保存,1型鸭疫里默氏杆菌:riemerella anatipestifer yb-1株、2型鸭疫里默氏杆菌:riemerella anatipestifer yb-2株、10型鸭疫里默氏杆菌:riemerella anatipestifer yb-10株均由我公司分离获得。
44.商业化质粒pfastbac i、大肠杆菌dh10bac感受态细胞均购买于thermo公司。
45.实施例1:重组杆状病毒的构建
46.1、转移载体构建:将鸭疫李默氏杆菌的抗原蛋白tbdr1、sip、gldg、ompa及ha进行截短和多重表达,将获得的蛋白片段tbdr1-t3、sip-t3、gldg-t3、ompa-t3、ha-t3、camp和trpb委托安徽通用生物进行基因合成,并连接至商业化载体pfastbac i,获得转移载体ra-a、ra-b、ra-c、ra-d、ra-e、ra-f和ra-g。
47.2、重组杆状病毒构建:将步骤1中合成的转移载体ra-a~ra-g分别转入大肠杆菌dh10 bac感受态细胞中,并挑选阳性克隆用m13引物作pcr鉴定。
48.m13-f:tgtaaaacgacggccagt
49.m13-r:caggaaacagctatgac
50.pcr反应体系为(总体积25μl):dna模板0.5μl、m13-f和m13-r个0.5μl、dna聚合酶12.5μl及无菌水11μl。
51.pcr反应条件为:93℃,5min;94℃30s,55℃45s,72℃5min,30个循环;72℃10min。
52.pcr产物进行1%琼脂糖凝胶电泳,结果显示,成功扩增出约3000-5000bp的特异性条带,与预期大小相符。阳性重组杆粒命名为rbacmid-ra-a、rbacmid-ra-b、rbacmid-ra-c、rbacmid-ra-d、rbacmid-ra-e、rbacmid-ra-f和rbacmid-ra-g。
53.3、重组杆粒转染sf9细胞:将步骤2中的阳性重组杆粒用脂质体转染的方法将重组杆粒转染昆虫细胞sf9,具体操作方法参照赛默飞世尔科技(中国)有限公司的cellfectin转染试剂说明书进行,获得f1代重组杆状病毒rra-a、rra-b、rra-c、rra-d、rra-e、rra-f和rra-g。
54.实施例2:重组蛋白的制备
55.1、重组杆状病毒扩增:将实施例1获得的f1代重组杆状病毒rra-a、rra-b、rra-c、rra-d、rra-e、rra-f和rra-g分别接种昆虫细胞sf9,27℃培养4天,收集培养物,离心取上清即获得f2代重组杆状病毒;
56.2、表达蛋白鉴定:
57.(1)将步骤1中获得的f2代重组杆状病毒rra-a~rra-g以moi=5~10的接种量分别接入昆虫细胞sf9,27℃培养4天,收集培养物,离心取上清即获得重组蛋白tbdr1-t3、sip-t3、camp、gldg-t3、ompa-t3、trpb及ha-t3;
58.(2)sds-page鉴定:将步骤2获得的上清进行sds-page电泳;电泳结束后,经染色和脱色后发现,tbdr1-t3样品条带为45kda、sip-t3样品条带为49kda、camp样品条带为37kda、gldg-t3样品条带为60kda、ompa-t3样品条带为40kda、trpb样品条带为34kda及ha-t3样品条带为46kda。电泳结果条带大小均与目标蛋白理论分子量大小一致,证明蛋白表达成功(图1)。
59.(3)重组蛋白的大量表达:将鉴定正确的重组病毒以moi=1~10的接毒量接种hf细胞大量培养,离心收集培养液上清,即获得含有大量的tbdr1-t3、sip-t3、camp、gldg-t3、ompa-t3、trpb及ha-t3重组蛋白。
60.(4)蛋白纯化:蛋白纯化采用常规ni亲和层析进行纯化,具体实验操作参照千纯生物科技有限公司ni-nta purose 6fast flow填料说明书。
61.实施例3:疫苗制备
62.1、灭活:将实施例2中制备的tbdr1-t3、sip-t3、camp、gldg-t3、ompa-t3、trpb及ha-t3重组蛋白加入到灭活罐中,加入终浓度为0.2%~0.5%灭活剂bei,于37℃灭活24h。
63.2、半成品检验
64.(1)无菌检验:按现行《中国兽药典》附录进行无菌检验。
65.(2)蛋白含量测定:按bca法检测蛋白含量。
66.(3)灭活检验:将灭活后的重组蛋白分别接入昆虫细胞sf9,置于27℃继续培养72小时。观察无病变出现,判定灭活检验合格。
67.3、疫苗疫苗组合物制备:
68.经过检验合格后的半成品蛋白抗原进行疫苗制备(以下配制中各液体成分按体积比计)。
69.(1)油相制备:取兽用白油95份,硬脂酸铝1份,置于油相制备罐中加热至80℃后,再加5份司本-80,至温度达到115℃时,维持,冷却后备用。
70.(2)水相制备:将各重组蛋白使用生理盐水稀释成100μg/ml,并按适宜比例进行混合。取灭菌后的5份吐温-80,加入配液罐中,同时加入制苗用蛋白液95份,搅拌20~30min,使吐温-80完全溶解。
71.(3)乳化取油相2份放于高速剪切机内,开动电机慢速转动搅拌,同时徐徐加入水相1份,以10000rpm乳化5分钟。乳化后,取10ml,以3000rpm离心15min,管底析出的水相应不超过0.5ml。
72.实施例4:疫苗成品检验
73.1、性状
74.外观:疫苗应为乳白色白乳剂,无杂质并且外包装应合格;
75.剂型:油包水型。取一清洁吸管,吸取少量疫苗滴入冷水中,除第一滴外,均应不扩散。
76.稳定性:吸取疫苗10ml加入离心管中,以3000rpm离心15min,管底析出水相应不超过0.5ml。
77.黏度:按现行《中国兽药典》附录进行,应符合规定。
78.2、装量检查:按现行《中国兽药典》附录进行,应符合规定。
79.3、无菌检验:按现行《中国兽药典》附录进行,应符合规定。
80.4、安全检验:
81.鸭传染性浆膜炎三价基因工程亚单位疫苗,批号分别为rra-001p、rra-002p、rra-003p共3批。
82.取5-6日龄的健康易感鸭(血清1型、2型、10型鸭疫里默氏杆菌抗体凝集效价均不高于1:2)10只,每只颈部皮下注射疫苗0.3ml,观察14日内实验鸭有无局部或全身明显不良反应。结果显示,疫苗注射后实验动物无不良反应(如喜卧、废食,疫苗注射部位无结痂、肿胀,剖检显示疫苗注射部位无疫苗残留)
83.5、效力检验:
84.5.1分组及攻毒:取5-6日龄健康易感鸭(血清1型、2型、10型鸭疫里默氏杆菌抗体凝集效价均不高于1:2)90只,随机均分为a-i九组,每组10只。a、b、c组为免疫组,每只颈部皮下注射疫苗0.15ml,d、e、f组为市售疫苗对照(齐鲁动物保健品有限公司,该疫苗为包含1型、2型和7型三个血清型抗原),g、h、i为非免疫攻毒对照。免疫后14日,用1型、2型、10型鸭疫里默氏杆菌(yb-1、yb-2、yb-10)分别进行攻毒实验,其中a、d、g组使用活菌量约为4
×
109cfu/ml的yb-1株菌液1ml腿部肌肉注射攻毒,b、e、h组使用活菌量约为1
×
109cfu/ml的yb-2株菌液1ml腿部肌肉注射攻毒,c、f、i组使用活菌量约为6
×
109cfu/ml的yb-10株菌液1ml腿部肌肉注射攻毒,观察10日内实验鸭发病和死亡情况。
85.5.2效力检验结果:取5-6日龄健康易感鸭(血清1型、2型、10型鸭疫里默氏杆菌抗体凝集效价均不高于1:2)90只,随机均分为a-i九组,每组10只。a、b、c组为免疫组,每只颈部皮下注射疫苗0.15ml,d、e、f组为市售疫苗对照,g、h、i为非免疫攻毒对照组。免疫后14日,a、d、g组使用活菌量约为4
×
109cfu/ml的yb-1株菌液1ml腿部肌肉注射攻毒,b、e、h组使用活菌量约为1
×
109cfu/ml的yb-2株菌液1ml腿部肌肉注射攻毒,c、f、i组使用活菌量约为6
×
109cfu/ml的yb-10株菌液1ml腿部肌肉注射攻毒,观察10日内实验鸭发病和死亡情况。ra-002p疫苗免疫14日后攻毒,免疫鸭保护率均10/10,市售疫苗对照组保护率为(1型7/10、2型8/10、10型0/10),对照鸭发病均10/10。详见下表。
86.表1鸭传染性浆膜炎三价基因工程亚单位灭活疫苗效力检验结果
[0087][0088]
注:鸭传染性浆膜炎发病判断标准(符合条件之一即可判为发病)
[0089]
(1)精神不振、行动蹒跚、眼鼻有分泌物流出、排绿色或黄绿色稀薄粪便或死亡;
[0090]
(2)剖检出现心包炎或肝周炎或浆膜炎病变;
[0091]
采集的血清样本或肝脏或脾脏组织,接种巧克力琼脂平板分离细菌,分离到的细菌呈阳性。
[0092]
虽然本发明已以较佳实施例公开如上,但其并非用以限定本发明,任何熟悉此技术的人,在不脱离本发明的精神和范围内,都可做各种的改动与修饰,因此本发明的保护范围应该以权利要求书所界定的为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1