和厚朴酚口服自微乳剂及其制备方法
1.本发明涉及一种和厚朴酚口服自微乳剂及其制备方法,属于和厚朴酚制剂技术领域。
背景技术:
2.和厚朴酚(honokiol,hn)是从中草药厚朴(magnolia officinalis)中分离的一种联苯二酚类化合物,是厚朴的主要活性成分之一,其分子式为c
18
h
18
o2,外观呈红褐色至白色精细粉末状,易溶于苯、乙醚、三氯甲烷、乙醇等,难溶于水。和厚朴酚主要具有以下药理活性和功效:(1)抗氧化活性,通过增强抗氧化酶的活性,清除机体产生过多的自由基;(2)抗菌和抗病毒活性;(3)抗炎、镇痛活性;(4)抗肿瘤活性,能够抑制肿瘤细胞的增殖;(5)保护心血管功效,对心血管疾病有一定的治疗效果;(6)保护神经系统功效,可作为钠离子通道的阻断剂,阻断神经传递过程中钠离子的流动,阻止疼痛的产生和传导;(7)保护胃肠道功效。但是和厚朴酚极难溶于水,体内代谢快,血药浓度低,使用时难以均一分散,普通制剂生物利用度低。目前有研究报道将和厚朴酚制备成脂质体、滴丸剂、纳米混悬剂等剂型以方便使用,提高其生物利用度,但这类剂型制备过程复杂,成本和制备条件要求较高。
3.自微乳给药系统(self
‑
microemusifying drug delivery system,smedds)是近年来迅速发展起来的新型难溶性药物给药系统,其主要由油相、乳化剂、助乳化剂按一定配比复配而成,口服后在胃肠道蠕动下自发乳化形成水包油(o/w)型乳液,可增加难溶性药物的溶解度、稳定性以及其与胃肠道的接触面积,有助于控制药物释放和吸收,提高药物生物利用度和降低生物应激。smedds制备过程简单,无需复杂的机器操作即可完成,具有广阔的应用前景。
4.徐振中等(徐振中,杨坚,白娟,等.和厚朴酚口服自微乳制剂的制备及药代动力学研究[j].中国新药杂志,2012,21(08):857
‑
862,878.)报道了一种和厚朴酚自微乳剂,其配方是辛癸酸甘油酯,cremaphor el和labrasol(质量比为3:5:2),稀释成乳后的粒径和电势分别为(35.48
±
4.21)nm和(
‑
2.04
±
0.26)mv,最高载药量为2%。甘露等(甘露,田睿,郭锋,等.和厚朴酚自微乳化给药系统的研究[j].第三军医大学学报,2013,35(19):2073
‑
2076.)。报道了一种和厚朴酚自微乳剂,其配方是其处方组成为辛癸酸甘油酯:聚氧乙烯氢化蓖麻油:二乙二醇单乙基醚(质量比为20.0:53.3:26.7),载药量为1%、5%、10%时,形成微乳的粒径分别为29.23、29.05、28.00nm,粒径仍然比较大。
[0005]
申请号为cn 201410350015.0的专利申请公开了一种含厚朴酚或和厚朴酚的纳米微球及其制备方法和应用公开了一种含厚朴酚或和厚朴酚的纳米微球及其制备方法和应用,本发明以壳聚糖为载体,三聚磷酸钠为交联剂,通过离子交联法,包封厚朴酚或和厚朴酚药物,然后经过滤、透析除去溶液中未包埋的药物和小分子物质,最后冷冻干燥即得含厚朴酚或和厚朴酚的纳米微球。其工艺复杂,制备成本高,并且所制备的载药纳米微球的平均粒径为40~150nm,粒径大。
技术实现要素:
[0006]
本发明要解决的技术问题是提供一种新的和厚朴酚口服自微乳剂。
[0007]
为解决本发明的问题,所述和厚朴酚口服自微乳剂的组份为:tween
‑
80 52.5~76.5%,peg200 10.5~22.5%,花生油7.5~25.5%,蓖麻油1.5~7.5%,载药量1~6%。
[0008]
在一种具体实施方式中,所述tween
‑
80 70~76.5%,peg200 10.5~15%,花生油7.5~10.56%,蓖麻油1.5~3.28%;优选所述tween
‑
80 71.54%,peg200 14.62%,花生油10.56%,蓖麻油3.28%。
[0009]
在一种具体实施方式中,所述载药量6%。
[0010]
在一种具体实施方式中,所述微乳剂微乳加水稀释后的平均粒径20nm以下,优选为16~17.5nm,优选加水稀释的倍数为3倍以上,更优选为5~400倍。加水稀释的倍数为3倍以上可形成o/w型微乳,5~400倍稀释下稳定性良好。
[0011]
所述的水可以为纯水、海水、pbs缓冲液、人工胃液、人工小肠液等等分散介质。
[0012]
在一种具体实施方式中,和厚朴酚口服自微乳剂由以下方法制备得到:
[0013]
a.将tween
‑
80,peg200,花生油,蓖麻油在300~600r/min搅拌混合均匀得到混合物a;
[0014]
b.再将厚朴酚原料药与混合物a在300~600r/min搅拌混合均匀,得和厚朴酚自微乳制剂。
[0015]
在一种具体实施方式中,b步骤所述厚朴酚原料药的纯度≥98%。
[0016]
在一种具体实施方式中,所述搅拌的温度为16~28℃。
[0017]
在一种具体实施方式中,所述和厚朴酚口服自微乳剂的剂型为微乳液、软胶囊、颗粒剂、片剂或微丸剂型。
[0018]
本发明要解决的第二个技术问题是提供一种和厚朴酚口服自微乳剂的制备方法。
[0019]
为解决本发明的第二个技术问题,所述方法包括:
[0020]
a.将tween
‑
80,peg200,花生油,蓖麻油在300~600r/min搅拌混合均匀得到混合物a;
[0021]
b.再将厚朴酚原料药与混合物a在300~600r/min搅拌混合均匀,得和厚朴酚自微乳制剂。
[0022]
在一种具体实施方式中,b步骤所述厚朴酚原料药的纯度≥98%。
[0023]
在一种具体实施方式中,所述搅拌的温度为16~28℃。
[0024]
有益效果:
[0025]
本发明采用特定的乳化剂、助乳化剂和混合油相、特定的自微乳体系的配比,厚朴酚在水中的溶解度好,载药量6%以下均能同时获得平均粒径小于20nm的自微乳,使其更容易透过表皮吸收,提高和厚朴酚的生物利用度。
附图说明
[0026]
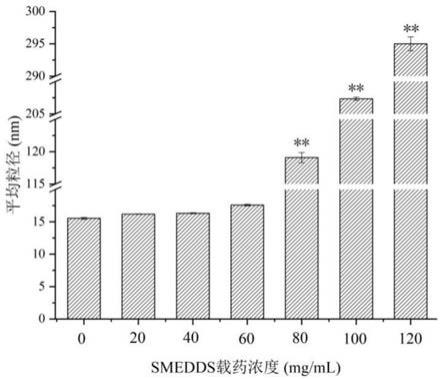
图1为实施例1
‑
3及对比例1
‑
3中不同和厚朴酚浓度对应的smedds平均粒径图。
[0027]
图2为实施例1
‑
3及对比例1
‑
3中和厚朴酚自微乳制剂和稀释成乳后外观照片;和厚朴酚自微乳(a)和100倍稀释成乳(b)效果图。
[0028]
图3为实施例4中和厚朴酚自微乳制剂的粒径分布图。
[0029]
图4为实施例4中和厚朴酚自微乳制剂的电位分布图。
[0030]
图5为实施例4中和厚朴酚自微乳制剂电导率随水分含量变化的曲线。
[0031]
图6为实施例4中和厚朴酚自微乳制剂和其混悬液分别在人工胃液和人工小肠液中的体外药物累积释放曲线。
具体实施方式
[0032]
为解决本发明的问题,所述和厚朴酚口服自微乳剂的组份为:tween
‑
80 52.5~76.5%,peg200 10.5~22.5%,花生油7.5~25.5%,蓖麻油1.5~7.5%,载药量1~6%。
[0033]
在一种具体实施方式中,所述tween
‑
80 70~76.5%,peg200 10.5~15%,花生油7.5~10.56%,蓖麻油1.5~3.28%;优选所述tween
‑
80 71.54%,peg200 14.62%,花生油10.56%,蓖麻油3.28%。
[0034]
在一种具体实施方式中,所述载药量6%。
[0035]
在一种具体实施方式中,所述微乳剂微乳加水稀释后的平均粒径20nm以下,优选为16~17.5nm,优选加水稀释的倍数为3倍以上,更优选为5~400倍。加水稀释的倍数为3倍以上可形成o/w型微乳,5~400倍稀释下稳定性良好。
[0036]
所述的水可以为纯水、海水、pbs缓冲液、人工胃液、人工小肠液等等分散介质。
[0037]
在一种具体实施方式中,和厚朴酚口服自微乳剂由以下方法制备得到:
[0038]
a.将tween
‑
80,peg200,花生油,蓖麻油在300~600r/min搅拌混合均匀得到混合物a;
[0039]
b.再将厚朴酚原料药与混合物a在300~600r/min搅拌混合均匀,得和厚朴酚自微乳制剂。
[0040]
在一种具体实施方式中,b步骤所述厚朴酚原料药的纯度≥98%。
[0041]
在一种具体实施方式中,所述搅拌的温度为16~28℃。
[0042]
在一种具体实施方式中,所述和厚朴酚口服自微乳剂的剂型为微乳液、软胶囊、颗粒剂、片剂或微丸剂型。
[0043]
本发明要解决的第二个技术问题是提供一种和厚朴酚口服自微乳剂的制备方法。
[0044]
为解决本发明的第二个技术问题,所述方法包括:
[0045]
a.将tween
‑
80,peg200,花生油,蓖麻油在300~600r/min搅拌混合均匀得到混合物a;
[0046]
b.再将厚朴酚原料药与混合物a在300~600r/min搅拌混合均匀,得和厚朴酚自微乳制剂。
[0047]
在一种具体实施方式中,b步骤所述厚朴酚原料药的纯度≥98%。
[0048]
在一种具体实施方式中,所述搅拌的温度为16~28℃。
[0049]
下面结合实施例对本发明的具体实施方式做进一步的描述,并不因此将本发明限制在所述的实施例范围之中。
[0050]
实施例1
‑
3及对比例1
‑3[0051]
tween
‑
80:71.37%,peg200:14.52%,花生油:10.76%,蓖麻油:3.34%制备空白自微乳剂,在空白自微乳中实施例1
‑
3及对比例1
‑
3分别加入20、40、60、80、100、120mg/ml和厚朴酚制成和厚朴酚自微乳,用纯水稀释100倍,然后采用激光粒度分析仪测定其平均粒
径。结果显示(附图1)实施例1
‑
3的乳剂平均粒径平稳在(17.60
±
0.119)nm,无显著变化,对比例1浓度为80mg/ml时,乳剂平均粒径为(119.10
±
0.779)nm,超出了微乳的定义范围。
[0052]
制剂外观
[0053]
和厚朴酚自微乳外观呈橙色油状物,随着载药浓度增加,颜色逐渐加深,稀释成乳后其外观转变为淡蓝色乳光澄清透明溶液,随着载药浓度增加,浊度增加,如图2所示。
[0054]
实施例4
[0055]
称取tween
‑
80 71.54g,peg200 14.62g,花生油10.56g,蓖麻油3.28g在400r/min磁力搅拌,(25
±
3)℃下混合均匀;加入6g和厚朴酚原料药,在400r/min磁力搅拌,(25
±
3)℃下混合均匀,得和厚朴酚自微乳制剂;
[0056]
取上述和厚朴酚自微乳剂10g,在400r/min磁力搅拌,(25
±
3)℃下分次加入990g纯水,形成和厚朴酚微乳。
[0057]
采用马尔文激光粒度分析仪检测形成的微乳液粒径和电位,结果如附图3、4所示,微乳的粒径大小为(16.83
±
0.3521)nm,多分散系数(pdi)为(0.189
±
0.021),zeta电位为(
‑
15.53
±
0.205)mv,符合微乳要求。表明和厚朴酚自微乳制备成功。
[0058]
包封率测试
[0059]
取1ml制备得到的和厚朴酚自微乳,加入2ml甲醇,超声10min,转移到100ml容量瓶中,冷却至室温后加甲醇稀释至刻度,用hplc测定和厚朴酚浓度并计算其质量(w1);另精密量取1ml制备得到的和厚朴酚自微乳于锥形瓶中,在磁力搅拌条件下逐滴加入5ml纯水稀释成乳,转移到100ml容量瓶中,继续加入纯水至刻度,摇匀,制成微乳,转移至离心管中,10000r/min离心15min,取上层液体1ml,加入2ml甲醇,超声10min,过0.45μm微孔滤膜,用hplc测定和厚朴酚浓度并计算其质量(w2)。根据公式(1)计算包封率。经计算,制备得到的和厚朴酚自微乳包封率为(99.72
±
0.001)%(n=3)。结果显示该自微乳包封率良好。
[0060]
包封率=w2/w1(1)
[0061]
注:w1:制备得到的和厚朴酚自微乳中和厚朴酚的质量;w2:制备得到的和厚朴酚自微乳经高速离心后和厚朴酚的质量。
[0062]
冻融稳定性测试
[0063]
将本实施例的和厚朴酚自微乳,在
‑
20℃条件下冷冻24h,再将其在37℃水浴条件下解冻24h,如此反复冻融3次。待恢复至室温后用37℃的纯水释20倍,用激光粒度分析仪测定其平均粒径,平行3次试验。测得其平均粒径为(14.58
±
0.105)nm,pdi为(0.263
±
0.080),zeta电位为(
‑
14.86
±
0.188)mv,表明和厚朴酚自微乳冻融稳定性良好。
[0064]
贮藏稳定性测试
[0065]
将本实施例的和厚朴酚自微乳,将分别于4℃、25℃条件下保存15d,每隔5d测定。取样用蒸馏水稀释20倍,用激光粒度分析仪测定其平均粒径以及zeta电位,结果(表1)显示微乳平均粒径无显著性变化,表明和厚朴酚自微乳15d储存稳定性良好。
[0066]
表1和厚朴酚自微乳贮存稳定性
[0067][0068]
将纯水逐滴滴加至和厚朴酚自微乳,记录其电导率。结果如图5所示,和厚朴酚自微乳电导率随着纯水加入量的增加,电导率历经上升、平稳和下降三个阶段。其中上升阶段在水相占比0~65%阶段,该阶段所形成微乳为油包水(w/o)型,主要由分散于油相中的水分子相互碰撞导电。平稳阶段在水相占比65~75%阶段,该阶段液体发生了粘性碰撞,油相与水相互相交错,微乳由油包水型转变成双连续型,随着水相占比增加,电导率处稳定期。下降阶段在水相占比>75%阶段,随着水相占比增加,导电率迅速下降,此时微乳由双连续型转变成水包油(o/w)型微乳,作为导电粒子的油滴被逐渐稀释,导电率下降。故在稀释成乳时,水相占比应大于75%,即在该处方下要形成o/w型微乳,则至少应稀释3倍以上。
[0069]
体外释放度
[0070]
采用透析袋扩散法测定和厚朴酚自微乳和和厚朴酚混悬液在人工胃液和人工小肠液中的释放行为。采用本实施例配制的和厚朴酚自微乳,再使用人工胃液和人工小肠液稀释10倍成乳,分别取13ml于截留相对分子质量12000~14000的透析袋中备用,同时精密称取78mg和厚朴酚分别加入装有13ml的人工胃液和人工小肠液中制成和厚朴酚混悬液。以150ml人工胃液和人工小肠液作为溶出介质,控制温度为(37.0
±
0.5)℃,转速为100r/min,于释放后0.5、1、2、4、6、12、24、36、48、60、72h取样0.5ml,同时补足等温等量的溶出介质。取出的样品加入0.5ml甲醇,超声后过0.45μm微孔滤膜,用hplc测定和厚朴酚溶出量并绘制累积释放曲线,结果(附图6)显示,和厚朴酚混悬液在人工胃液和人工小肠液中初期释放量大于微乳液,在12h内即达到饱和。而和厚朴酚自微乳在人工胃液和人工小肠液中释放速度缓慢,累积释放量均大于混悬液,并且在人工小肠液中有更高的释放量。与和厚朴酚混悬液相比,和厚朴酚自微乳延长了和厚朴酚在人工胃液中的释放时间,在人工小肠液中有更高的释放度。
[0071]
实施例5
‑
11
[0072]
其它与实施例子4相同,不同的是实施例5
‑
11分别加入5、10、20、50、100、200和400倍的37℃纯水稀释,以外观和粒径为指标,考察稀释倍数对自微乳性能的影响,并观察其室温放置24h后物理状态的变化(有无沉淀或相分离)。结果显示,不同稀释倍数对该和厚朴酚自微乳微乳平均粒径无显著性影响,平均粒径稳定在(16.16
±
0.096)nm,在放置24h后依然呈澄清透明淡蓝乳光状态,稳定性良好。
[0073]
实施例12
‑
16
[0074]
其它与实施例子4相同,不同的是实施例12
‑
16分别以37℃的纯水、过滤海水、ph 6.8的pbs缓冲液,人工胃液、人工小肠液作为分散介质,将和厚朴酚自微乳稀释20倍,采用
激光粒度分析仪测定微乳平均颗粒。结果显示所考察的分散介质对微乳的平均粒径没有显著性影响,粒径大小稳定在16.29~17.12nm,该处方在不同分散介质中的稳定性良好。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1