一种抗鲍曼不动杆菌化合物stemphol的制备方法和应用
:
1.本发明属于工业微生物领域,具体涉及一种抗鲍曼不动杆菌化合物stemphol的制备方法和应用。
背景技术:
2.由于临床上抗生素的广泛使用,革兰氏阴性菌耐药现象加剧,院内感染严重。同时因为革兰氏阴性菌含有细胞膜、含薄肽聚糖层的周质和含脂多糖的外膜,大部分抗菌药物无法穿过细胞膜发挥作用。
3.鲍曼不动杆菌是一种革兰氏阴性条件致病菌,可引起肺炎、泌尿系统感染、脑膜炎等严重疾病。2017年世界卫生组织公布的最需抗生素的12种细菌中鲍曼不动杆菌处于第一优先级,且中国细菌耐药监测网2020年公布数据显示鲍曼不动杆菌占临床耐药菌株约8%,位于分离耐药菌株第五位。
4.药物治疗是治疗革兰氏阴性菌的主要手段,因此抗菌药物的挖掘仍是生物医药公司及科研机构的研究热点。红树林生态系统的特殊性及蕴含微生物的多样性使得红树林内生真菌形成独特的次级代谢产物合成途径,为产生结构独特的小分子天然产物提供了可能,具有挖掘新型抗菌药物的巨大潜力。
5.文献[shingo marumo,hiroyuki hattori,masato katayama.stemphol from pleospora herbarum as a self-inhibitor.agric.bioi.chem.,1985,49(5),1521-1522]公开了从枯叶格孢腔菌中制备化合物stemphol的方法以及其自我抑制功能。
技术实现要素:
[0006]
本发明的第一个目的是提供化合物stemphol(2-丁基,5-戊基间二苯酚)的新用途,即化合物stemphol在制备抗鲍曼不动杆菌的药物中的应用。
[0007]
本发明的第二个目的是一种抗鲍曼不动杆菌的药物,其含有化合物stemphol作为活性成分。
[0008]
本发明的第三个目的是提供一种化合物stemphol的制备方法,所述的化合物stemphol是从匐柄霉(stemphylium sp.)wh2的发酵培养物中分离得到的。
[0009]
优选,具体步骤为:
[0010]
a、制备匐柄霉wh2的发酵培养物;
[0011]
b、将发酵培养物用丙酮浸泡破碎浸取,浸取液经蒸馏浓缩后得到浸膏,浸膏用sephadex lh-20凝胶柱层析,以氯仿/甲醇1:1v/v洗脱,将含有stemphol的流份fr.3进一步用sephadex lh-20凝胶柱层析,以氯仿/甲醇1:1v/v洗脱,将含有stemphol的亚流份fr.3c利用高效液相色谱分离纯化,得到化合物stemphol。
[0012]
优选,所述的制备匐柄霉wh2的发酵培养物是将匐柄霉wh2接种到种子培养基中经发酵获得种子液,再将种子液接种到发酵培养基中,经发酵获得发酵培养物;
[0013]
所述的种子培养基是含质量分数2%海盐的pdb培养基;
7.2,其配制方法是将上述组分按其含量混合均匀后调ph值,然后115℃,灭菌30min,备用;
[0031]
发酵培养基配制,大米15g,15ml质量分数2%海盐水;燕麦15g,15ml质量分数2%海盐水,将两者混合,然后115℃,灭菌30min,备用。
[0032]
b.发酵:
[0033]
种子培养:将在平板上活化的红树林来源内生真菌匐柄霉wh2用灭菌竹签挑取适量菌丝体到20ml种子培养基中,28℃,200rpm,培养3天至对数生长期制得种子液;
[0034]
规模发酵培养:将20ml种子液分别接入到含15g大米和15g燕麦的发酵培养基的发酵瓶中,静置培养32d后合并得到发酵培养物。
[0035]
3、发酵液的萃取:
[0036]
发酵培养物用100ml丙酮浸泡超声破碎,离心分离(3900r
·
min-1,10min)浸取液和菌体,合并浸取液,经蒸馏浓缩后得到浸膏,浸膏经高效液相分析含有化合物stemphol,具体见图1。
[0037]
4、化合物的分离:
[0038]
a)浸膏经凝胶sephadex lh-20柱层析(氯仿/甲醇1:1,v/v)作为洗脱液,洗脱200ml,每20ml收集为一个馏分,先后依次得馏分fr.1-fr.10。
[0039]
b)fr.3经凝胶sephadex lh-20柱层析,用体积比为1:1的氯仿-甲醇作为流动相洗脱,洗脱100ml,每10ml收集为一个馏分,先后依次得馏分fr.3a至fr.4j,把收集的第3个馏分fr.3c使用半制备型高效液相色谱(phenomenex c18柱,5μm,150mm
×
4.6mm,流速2.5ml/min)以乙腈/水体系(a相:0.08%hcooh/h2o;b相:ch3cn)等度洗脱(vb:va=50:50)洗脱分离纯化,收集保留时间为第18分钟的馏分,旋转蒸干制备获得化合物stemphol。
[0040]
5、化合物的鉴定:
[0041]
通过结构分析,对本发明的从匐柄霉属真菌(stemphylium sp.)wh2的发酵培养物中制备得到的化合物stemphol(式(i))对其进行鉴定,其鉴定结果如下:
[0042]
图2化合物stemphol的晶体衍射结构。
[0043]
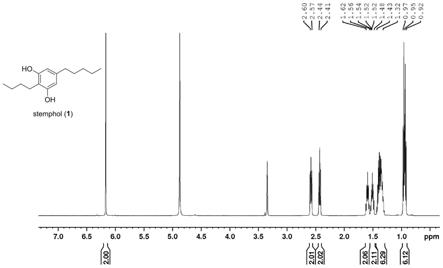
图3化合物stemphol的h谱图。
[0044]
图4化合物stemphol的c谱图。
[0045]
化合物stemphol:无色晶体,正源高分辨电喷雾质谱图显示其准分子离子峰m/z 237.1854[m+h]
+
,推测其分子式为c
15h25
o2(计算值为237.1849)。1h nmr(500mhz,methonal-d4)δh:6.16(1h,s,h-4/6),2.59(2h,t,j=7.46,h-11),2.44(2h,t,j=7.40,h-7),1.62(2h,m,h-12),1.53(2h,m,h-8),1.42(6h,m,h-9/13/14),0.97(6h,overlapping,h-10/15)ppm.
13
c nmr(125mhz,methonal-d4)δc:155.6(c-1/3),140.8(c-5),113.1(c-2),106.4(c-4/6),35.3(c-11),31.3(c-13),31.2(c-8),30.8(c-12),22.5(c-7),22.3(c-9),22.2(c-14),13.1(c-15),13.0(c-10)ppm。波谱数据与文献[zhou xm,zheng cj,chen gy,song xp,han cr,tang xz,liu rj,ren ll.two new stemphol sulfates from the mangrove endophytic fungus stemphylium sp.33231.j antibiot(tokyo)2015,68(8):501-3.]报道基本一致,x-ray单晶衍射进一步确定其为stemphol。
[0046]
化合物stemphol,结构式如下:
[0047][0048]
实施例2:化合物stemphol的抗鲍曼不动杆菌活性测定
[0049]
化合物stemphol针对鲍曼不动杆菌atcc 19606进行抑制活性测定,采用微量肉汤稀释法测定分离化合物的最小抑菌浓度(mic),实验方法参考文献[黄艳冰,蒋晓东,刘威,黄春帅,张丽萍,诸晗宁,张长生,张文军.叶状蔷薇珊瑚来源真菌parengyodontium album scsio40430次级代谢产物研究.微生物学通报,2018,45(09):1881-1888.],以ciprofloxacin作为对照(对鲍曼不动杆菌的最小抑制浓度为0.125μg ml-1
)。结果表明stemphol对鲍曼不动杆菌atcc 19606的最小抑菌浓度为8μg ml-1
,对鲍曼不动杆菌具有良好抑制活性,通过生物工程或化学修饰可望开发成为抗鲍曼不动杆菌新药。
[0050]
表1.化合物stemphol的抗鲍曼不动杆菌最小抑制浓度测定。
[0051][0052]
a ciprofloxacin,positive control.
[0053]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1