组织透明化维持试剂和用于组织透明化的试剂盒的制作方法
1.本发明涉及生物技术领域,特别是涉及一种组织透明化维持试剂和用于组织透明化的试剂盒。
背景技术:
2.脑皮层脉管网络的可视化研究是揭示诸多脑疾病发生发展过程的重要途径。近年来,成像技术及多种标记技术的快速发展使得活体水平监测脑脉管网络结构与功能的变化成为可能。通过对脑脉管网络实施长期的在体监测及操控,有望揭示其发育规律以及脑疾病诱发的脑脉管结构及功能变化的时空特征。
3.然而,浑浊的颅骨组织严重制约了光学成像技术实施穿颅活体皮层成像的效果。为解决这一问题,目前已发展了多种用于实施高分辨的皮层脉管成像的颅窗技术,包括:开颅玻璃颅窗、磨薄颅窗及相关衍生颅窗等。但这些技术仍存在诸多弊端。例如:手术操作过程复杂,磨薄颅窗仅能满足1次~2次的成像需求,开颅玻璃颅窗会造成大脑微环境的改变及出血,极大地限制了对皮层微脉管网络结构与功能的研究。
4.目前,也有一些研究报道了基于活体组织光透明技术的光透明颅窗模型,然而,这些光透明颅窗仅能满足几小时内的成像需求,若需进行重复成像研究,则要求再次的手术及颅骨透明化处理,极大地增加了研究难度。
技术实现要素:
5.基于此,有必要提供一种可以延长颅窗透明化状态的组织透明化维持试剂。
6.此外,还有必要提供一种可以延长颅窗透明化状态的组织透明化的试剂盒。
7.一种组织透明化维持试剂,包括第一试剂、第二试剂和封闭剂,所述第一试剂与所述第二试剂用于在透明化的组织上形成透明层,所述封闭剂用于在所述透明胶层上形成透明保护层,所述第一试剂包括丙烯酸-丙烯酸酯共聚物、聚二甲基硅氧烷、三羟甲基丙烷三丙烯酸酯和聚甲基丙烯酸甲酯,所述第二试剂包括丙烯酸酯预聚物、丙烯酸酯单体和引发剂。
8.本技术的发明人经研究发现,在利用光透明剂对小鼠颅骨实施透明化处理后,利用第一试剂与第二试剂固化形成的透明层可以使颅骨长期稳定的透明化状态,可满足对大脑皮层脉管网络的在体长期追踪。
9.在其中一个实施例中,以质量百分含量计,所述第一试剂包括25%~50%的丙烯酸-丙烯酸酯共聚物、15%~40%的聚二甲基硅氧烷、5%~25%的三羟甲基丙烷三丙烯酸酯、和10%~20%的聚甲基丙烯酸甲酯;所述第二试剂包括70%~80%的丙烯酸酯预聚物、15%~25%丙烯酸酯单体和3%~6%的引发剂。
10.在其中一个实施例中,所述封闭剂包括聚丙烯酸酯、三羟甲基丙烷三丙烯酸酯、聚氨酯-10和引发剂。
11.在其中一个实施例中,以质量百分含量计,所述封闭剂包括20%~40%的聚丙烯
酸酯、25%~50%的三羟甲基丙烷三丙烯酸酯、20%~35%的聚氨酯-10和3%~5%的引发剂。
12.在其中一个实施例中,所述第一试剂与所述第二试剂的质量之比为(1~2):(1~8)。
13.在其中一个实施例中,所述第二试剂的引发剂为光引发剂。
14.一种用于组织透明化的试剂盒,包括上述组织透明化维持试剂和用于组织透明化的光透明试剂。
15.在其中一个实施例中,所述光透明剂选自甘油、山梨醇、乙醇、丙二醇、尿素、十二烷基苯磺酸钠和乙二胺四乙酸二钠中的至少一种。
16.在其中一个实施例中,所述光透明剂包括第一透明试剂和第二透明试剂,所述第一透明试剂包括尿素和乙醇,所述第二透明试剂包括十二烷基苯磺酸钠。
17.在其中一个实施例中,所述第一透明试剂为75%乙醇的尿素饱和溶液;所述第二透明试剂为质量百分含量为15%~20%的十二烷基苯磺酸钠水溶液。
18.在其中一个实施例中,所述第二透明试剂的ph为7~8。
附图说明
19.图1~图2为实施例1中对两个月月龄小鼠颅骨光透明前后的大脑皮层血管成像结果;
20.图3为实施例2中建立颅窗后的大脑皮层血管成像结果;
21.图4是实施例3中建立颅窗后的大脑皮层血管成像结果;
22.图5是实施例4中建立颅窗后的大脑皮层血管成像结果;
23.图6是实施例5中建立颅窗后的大脑皮层血管成像结果;
24.图7是实施例6中利用光学相干断层成像系统拍摄得到的两个月月龄小鼠建立长期稳定光透明颅窗前后的大脑皮层血管成像结果;
25.图8是实施例6中建立透明颅窗后的两个月内的多次重复成像结果。
具体实施方式
26.为了便于理解本发明,下面将对本发明进行更全面的描述,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施例。相反地,提供这些实施例的目的是使本发明公开内容更加透彻全面。
27.需要说明的是,术语“第一”、“第二”等仅用于描述目的,而不能理解为指示或暗示相对重要性。术语“和/或”或“及/或”包括一个或多个相关的所列项目的任意的和所有的组合。
28.除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。
29.本技术一实施方式提供了一种用于组织透明化的试剂盒,该试剂盒包括组织透明化维持试剂和用于组织透明化的光透明剂,该组织透明化维持试剂包括第一试剂、第二试剂和封闭剂。该组织透明化维持试剂可用于维持活体组织透明化,例如用于维持颅骨透明
化。
30.具体地,光透明剂用于将组织透明化。
31.在一些实施例中,光透明剂选自甘油、山梨醇、乙醇、丙二醇、尿素、十二烷基苯磺酸钠和乙二胺四乙酸二钠中的至少一种。
32.在一些实施例中,光透明剂包括第一透明试剂和第二透明试剂,第一透明试剂包括尿素和乙醇,第二透明试剂包括十二烷基苯磺酸钠。第一透明试剂用于解离胶原,以便于第二透明试剂渗透;第二透明试剂用于使得组织的折射率均一化而呈现透明状态。
33.在其中一个实施例中,第一透明试剂为75%乙醇的尿素饱和溶液。其中,尿素用于解离胶原;75%乙醇用于加快尿素解离胶原。乙醇的浓度不宜过高,乙醇浓度过高时尿素溶解速度较慢。可以理解的是,在其他实施例中,乙醇的浓度不限于75%,还可以是其他浓度。需要说明的是,此处的“75%乙醇”是指体积百分数为75%的乙醇。
34.在其中一个实施例中,第一透明试剂的制备方法包括以下步骤:将尿素加入75%乙醇的溶液中并搅拌,制备尿素饱和溶液,静置后取上清,制得第一透明试剂。
35.在其中一个实施例中,第二试剂为质量百分含量为15%~20%的十二烷基苯磺酸钠水溶液。在一个可选地具体示例中,第二试剂为质量百分含量为15%、16%、17%、18%、19%或20%的十二烷基苯磺酸钠水溶液。可以理解的是,在其他实施例中,第二试剂不限于上述,还可以是其他可以使得组织折射率均一化而呈现透明状态的试剂。进一步地,第二透明试剂的ph为7~8。
36.在其中一个实施例中,第二透明试剂的制备方法包括以下步骤:将摩尔浓度为0.7m的氢氧化钠水溶液,滴加至十二烷基苯磺酸中,持续搅拌至透明无色。在其中一个实施例中,0.7m的氢氧化钠水溶液与十二烷基苯磺酸的体积比约为24:5。
37.经本技术研究发现,只用第二试剂,组织不能呈现透明化状态,只用第一试剂维持透明状态的时间短,而采用第一试剂与第二试剂的配合,能够使得透明化后的组织长期维持透明状态。第一试剂和第二试剂混合固化后形成透明凝胶,并能长期维持组织透明化。具体地,第一试剂包括丙烯酸-丙烯酸酯共聚物、聚二甲基硅氧烷、三羟甲基丙烷三丙烯酸酯和聚甲基丙烯酸甲酯,第二试剂包括丙烯酸酯预聚物、丙烯酸酯单体和引发剂。
38.在一些实施例中,第一试剂包括25%~50%的丙烯酸-丙烯酸酯共聚物、15%~40%的聚二甲基硅氧烷、5%~25%的三羟甲基丙烷三丙烯酸酯和10%~20%的聚甲基丙烯酸甲酯;第二试剂包括70%~80%的丙烯酸酯预聚物、15%~25%丙烯酯单体和3%~6%的引发剂。
39.在其中一个实施例中,第二试剂的引发剂为光引发剂。可选地,光引发剂选自2,4,6一三甲基苯甲酰基膦酸乙酯、2-羟基-2-甲基-1-苯基-1-丙酮和1-羟基-环已基-苯基甲酮中的至少一种。可以理解的是。引发剂不限于光引发剂,光引发剂也不限于上述,还可以是其他能促进聚合的物质。
40.进一步地,在一些实施例中,以质量百分含量计,第一试剂包括25%~45%的丙烯酸-丙烯酸酯共聚物、20%~35%的聚二甲基硅氧烷、10%~25%的三羟甲基丙烷三丙烯酸酯、和10%~20%的聚甲基丙烯酸甲酯;第二试剂包括75%~80%的丙烯酸预聚物、18%~22%的丙烯酸酯单体和2%~4%的引发剂。
41.在一些实施例中,第一试剂与第二试剂的质量之比为(1~2):(1~8)。第一试剂与
第二试剂的质量之比设置为(1~2):(1~8)可以更好地保持颅骨的透明度以及颅窗的维持周期。封闭剂用于在透明胶层上形成透明保护层。在一些实施例中,封闭剂包括聚丙烯酸酯、三羟甲基丙烷三丙烯酸酯、聚氨酯-10和引发剂。可选地,以质量百分含量计,封闭剂包括20%~40%的聚丙烯酸酯、25%~50%的三羟甲基丙烷三丙烯酸酯、25%~40%的聚氨酯-10和3%-5%的引发剂。进一步地,封闭剂包括25%~40%的聚丙烯酸酯、25%~40%的三羟甲基丙烷三丙烯酸酯和25%~35%的聚氨酯-10和4%的引发剂。可以理解的是,在其他实施例中,封闭剂不限于上述,还可以是其他能形成透明保护层的物质。
42.采用上述组织透明化维持试剂可以在使活体维持组织(例如颅骨)透明化,使得机体内部组织可视化,进而利于疾病研究;重要的是,上述组织透明化维持试剂可以使得可视化窗口较长时间存在(可以至少达到2个月以上),使得重复成像时不必再次手术和再次透明化处理,降低了研究难度。
43.基于上述,本技术一实施方式还提供了一种活体透明颅窗的建立方法,该方法包括采用上述任一实施例的组织透明化维持试剂对活体的颅骨进行处理。
44.在一些实施例中,上述活体透明颅窗的建立方法包括以下步骤:
45.步骤s1:对颅骨预处理。
46.通过对活体的颅骨预处理,除去颅骨表面粘膜。
47.在一些实施例中,活体为活小鼠。可以理解的是,在其他实施例中,活体为其他具有生命特征的动物或人。
48.在其中一个实施例中,活体为小鼠。此时,对颅骨预处理的操作包括:剪去麻醉小鼠头皮,擦除颅骨表面粘膜并将颅骨表面吹干;及将带孔金属固定片固定在干燥颅骨表面。通过将带孔金属固定片固定在干燥颅骨表面可以使得第一透明试剂能充分与颅骨表面作用,充分解离颅骨组织上的胶原。固定片的孔用于滴加第一透明试剂。也即是说,固定片的孔与待可视化区域的大小相适应。的可以理解的是,在其他实施例中,固定片不限的材质不限于金属,还可以是其他材料。
49.步骤s2:将第一透明试剂滴加到预处理后的颅骨表面。
50.在其中一个实施例中,向固定在颅骨表面的固定片的孔中滴加透明溶液一号,10min~15min后将其擦除。
51.在一些实施例中,在向颅骨表面递交第一透明试剂后,还包括采用脱脂棉球不断摩擦颅骨表面以加速透明化过程的步骤。
52.步骤s3:向第一透明试剂处理后的颅骨表面滴加第二透明试剂。
53.在其中一个实施例中,向第一透明试剂处理后的颅骨表面上滴加第二透明试剂,5min~8min后即实现颅骨组织的光透明化。透明化后,将第二透明试剂擦除。
54.步骤s4:将第一试剂与第二试剂混合后加到透明化后颅骨表面,以在颅骨表面形成透明层。
55.在本实施方式中,第二试剂中的引发剂为光引发剂。采用led激光光源局部照射第一试剂与第二试剂形成的混合物,使其凝固而形成透明层。在其中一个实施例中,光照时间为3min~5min。
56.在一些实施例中,第一试剂与第二试剂的使用质量之比为(1~2):(1~8)
57.在其中一个实施例中,第一试剂与第二试剂的使用质量之比为1:1、1:2、1:3或1:
4。
58.在其中一个实施例中,第一试剂与第二试剂混合之后的体积为0.1ml。可以理解的是,在其他实施例中,第一试剂与第二试剂混合之后的体积不限于上述,还可以根据实际情况进行调整。
59.步骤s6:在透明层上添加封闭剂以在透明层上形成透明保护层。
60.在其中一个实施例中,在透明层远离颅骨一侧的表面薄涂封闭剂后,用led激光光源照射1min~3min使封闭剂凝固形成透明保护层。保护层形成后即建立了长期稳定的透明颅窗,可利用光学显微成像系统实施成像。可选地,采用宽场成像系统成像,例如采用光学相干断层成像系统成像。
61.可以理解的是,在成像结束后正常饲养小鼠,待下一次成像时用压缩空气清理干净颅窗表面即可再次成像。
62.上述活体透明颅窗的建立方法采用上述组织透明化维持试剂在活体上建立透明颅窗,在第一成像结束后一段时间仍可以再进行多次成像,透明颅窗的保存时间久,避免多次成像时的多次手术及颅骨透明化处理,使得疾病研究更为便利。
63.具体实施例
64.以下结合具体实施例进行详细说明。以下实施例如未特殊说明,则不包括除不可避免的杂质外的其他组分。实施例中采用试剂和仪器如非特别说明,均为本领域常规选择。实施例中未注明具体条件的实验方法,按照常规条件,例如文献、书本中所述的条件或者生产厂家推荐的方法实现。在以下实施例中,光引发剂为2,4,6一三甲基苯甲酰基膦酸乙酯;聚丙烯酸酯的数均分子量为1000~7000;丙烯酸酯预聚物的数均分子量为140~1500;丙烯酸-丙烯酸酯共聚物的数均分子量为700~10000;聚二甲基硅氧烷的数均分子量为800~3800;聚丙烯酸的数均分子量为1000~5000;聚甲基丙烯酸甲酯的数均分子量为1500~7500。
65.实施例1
66.步骤1:将一只2月龄雄性balb/c小鼠麻醉后刮除头部毛发,用眼科剪剪去头部皮肤后,用湿润的棉球擦除颅骨表面的粘膜,用压缩空气将颅骨表面吹干。
67.步骤2:将一个铝制带孔固定片用牙科水泥固定在小鼠单侧颅骨表面,等待其凝固后将小鼠移放于小鼠定位器上并对其头部进行固定,并采用ccd相机对颅骨表面进行成像,结果如图1所示。
68.步骤3:在颅骨表面滴加第一透明试剂(75%乙醇的尿素饱和溶液,其配制方法为:将尿素缓慢加入75%体积分数的乙醇中,持续搅拌至饱和,静置后取其上清液),反应10min后用棉球擦除。
69.步骤4:在颅骨表面滴加第二透明试剂(质量百分含量为17.5%的十二烷基苯磺酸钠水溶液,其配制方法为:将0.7m的氢氧化钠水溶液缓慢滴加至十二烷基苯磺酸中,持续搅拌至透明无色,体积比约为24:5,ph值在7.6),反应5min后,实现颅骨组织的光透明化。
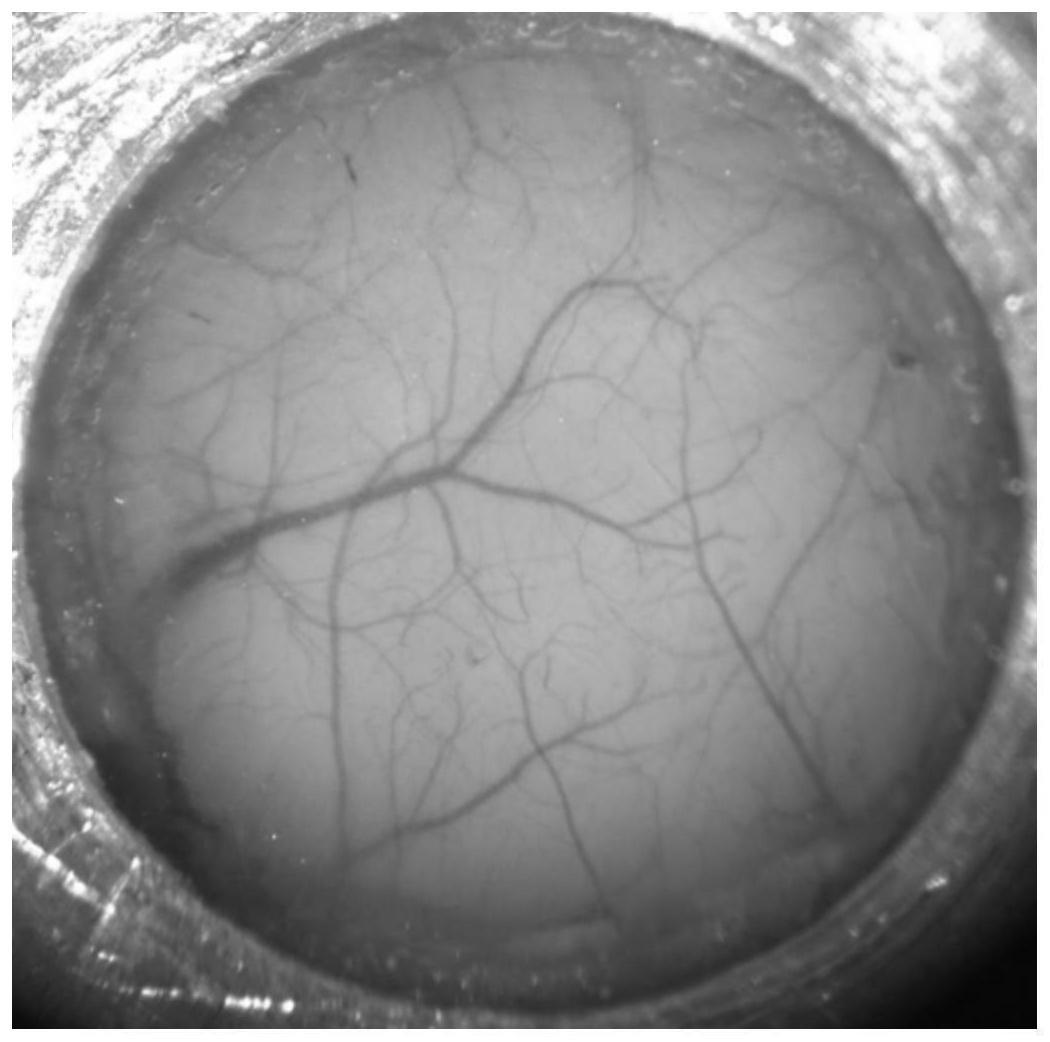
70.步骤5:利用ccd相机对颅骨表面进行成像,结果如图2所示。
71.由图1和图2可知,在光透明作用前,颅骨呈浑浊状态,无法观察到任何皮层血管信息;光透明作用后,皮层血管清晰可见。
72.实施例2
73.步骤1:将实施例1中小鼠颅骨上的第二透明试剂擦除,仅滴加第二试剂,然后用led激光光源辐照5min使其凝固,形成透明层。在本实施例中,第二试剂为丙烯酸酯预聚物、丙烯酸酯单体和引发剂的混合物,其中,丙烯酸酯预聚物质量百分含量77%,丙烯酸酯单体的质量百分含量20%,引发剂的质量百分含量为3%。
74.步骤2:在透明层表面薄涂封闭剂,用led激光光源辐照3min使其凝固,形成透明保护层。在本实施例中,封闭剂为聚丙烯酸酯、三羟甲基丙烷三丙烯酸酯、聚氨酯-10和引发剂的混合物,其中,聚丙烯酸酯的质量百分含量为39%,三羟甲基丙烷三丙烯酸酯的质量百分含量为25%,聚氨酯-10的质量百分含量为32%,引发剂的质量百分含量为4%。
75.步骤3:利用ccd相机对颅骨表面进行成像,结果如图3所示。
76.由图3可知,仅利用第二试剂和封闭剂所得的颅窗透明程度有限,无法清晰辨别皮层血管的形态结构。
77.实施例3
78.步骤1:去除实施例2的小鼠颅骨上的透明保护层和透明层。
79.步骤2:在颅骨表面滴加第一试剂与第二试剂的混合液,用led激光光源辐照5min使其凝固,形成新的透明层。在本实施例中,第一试剂为丙烯酸-丙烯酸酯共聚物、聚二甲基硅氧烷、聚丙烯酸和对羟基苯乙酮的混合物,其中,丙烯酸-丙烯酸酯共聚物的质量百分含量为40%,聚二甲基硅氧烷的质量百分含量为30%,聚丙烯酸的质量百分含量为20%,对羟基苯乙酮的质量百分含量为10%;第二试剂的组成与实施例2中的第二试剂相同;第一试剂与第二试剂的使用质量之比为1:4。
80.步骤3:在透明层远离颅骨一侧的表面薄涂封闭剂,用led激光光源辐照3min使其凝固,形成透明保护层。其中:封闭剂的组成与实施例2的封闭剂的组成相同。
81.步骤4:利用ccd相机对颅骨表面进行成像,结果如图4所示。
82.由图4可知,采用本实施例的第一试剂、第二试剂及封闭剂进行的透明颅窗建立时,颅骨透明程度较实施例2有提升,但皮层血管形态结构无法清晰分辨。
83.实施例4
84.步骤1:去除实施例3的小鼠颅骨上的透明保护层和透明层。
85.步骤2:在颅骨表面滴加第一试剂与第二试剂的混合液,用led激光光源辐照5min使其凝固,形成新的透明层。在本实施例中:第一试剂为丙烯酸-丙烯酸酯共聚物、聚二甲基硅氧烷、三羟甲基丙烷三丙烯酸酯和聚甲基丙烯酸甲酯的混合物,其中,丙烯酸-丙烯酸酯共聚物的质量百分含量为40%,聚二甲基硅氧烷的质量百分含量为30%、三羟甲基丙烷三丙烯酸酯的质量百分含量为25%、聚甲基丙烯酸甲酯的质量百分含量为5%。本实施例的第二试剂的组成与实施例2中的第二试剂相同;第一试剂与第二试剂的使用质量之比为1:1。
86.步骤3:在透明层远离颅骨一侧的表面薄涂封闭剂,用led激光光源辐照3min使其凝固,形成透明保护层。其中:封闭剂的组成与实施例2的封闭剂的组成相同。
87.步骤4:利用ccd相机对颅骨表面进行成像,结果如图5所示。
88.由图5可知,采用本实施例的第一试剂、第二试剂及封闭剂进行的透明颅窗建立成功,颅窗透明效果较佳,但周围有鼓胀。
89.实施例5
90.步骤1:去除实施例4的小鼠颅骨上的透明保护层和透明层。
91.步骤2:在颅骨表面滴加第一试剂与第二试剂的混合液,用led激光光源辐照5min使其凝固,形成新的透明层。在本实施例中:第一试剂的组成与实施例4中的第二试剂相同;本实施例的第二试剂的组成与实施例2中的第二试剂相同;第一试剂与第二试剂的使用质量之比为1:4。
92.步骤3:在透明层远离颅骨一侧的表面薄涂封闭剂,用led激光光源辐照3min使其凝固,形成透明保护层。其中:封闭剂的组成与实施例2的封闭剂的组成相同。
93.步骤4:利用ccd相机对颅骨表面进行成像,结果如图6所示。
94.由图6可知,采用本实施例的第一试剂、第二试剂及封闭剂进行的透明颅窗建立成功,颅窗透明效果较佳,周围无鼓胀,可作为长期稳定光透明颅窗。
95.实施例6
96.步骤1:将一只2月龄雄性balb/c小鼠麻醉后刮除头部毛发,用眼科剪剪去头部皮肤,再用湿润的棉球擦除颅骨表面的粘膜,用压缩空气将颅骨表面吹干。
97.步骤2:将一个铝制带孔固定片用牙科水泥固定在小鼠单侧颅骨表面,等待5min~8min凝固后将小鼠移放于小鼠定位器上并对其头部进行固定;采用光学相干断层成像系统拍摄大脑皮层血管网络结构,并对图像实施最大值投影处理,结果如图7所示。
98.步骤3:在颅骨表面滴加第一透明试剂(第一透明试剂的组成同实施例1),反应10min后用棉球擦除。
99.步骤4:在颅骨表面滴加第二透明试剂(第二透明试剂的组成同实施例1),反应5min后,实现颅骨组织的光透明化;
100.步骤5:擦除第二透明试剂,在颅骨表面滴加第一试剂与第二试剂的混合液,用led激光光源辐照5min使其凝固,形成透明层。在本实施例中,第一试剂的组成与实施例4中的第二试剂相同;本实施例的第二试剂的组成与实施例2中的第二试剂相同;第一试剂与第二试剂的使用质量之比为1:4。
101.步骤6:在透明层远离颅骨一侧的表面薄涂封闭剂,用led激光光源辐照3min使其凝固,形成透明保护层。其中:封闭剂的组成与实施例2的封闭剂的组成相同。
102.步骤7:采用光学相干断层成像系统拍摄大脑皮层血管网络结构,并对图像实施最大值投影处理,结果如图7所示。
103.由图7可知,采用本实施例的第一试剂、第二试剂及封闭剂进行的透明颅窗建立成功,皮层血管清晰可见。
104.步骤8:选择不同的时间点进行重复成像。重复成像时,将小鼠固定于小鼠固定器中,用压缩空气清理颅窗表面后,利用光学相干断层成像系统拍摄大脑皮层血管结构;每次成像结束后正常饲养小鼠,待再次实施成像,结果如图8所示。
105.在图8中,“第一周”的图像是形成具有透明保护层的透明颅窗时拍摄的图像,“第二周”的图像是指在形成具有透明保护层的透明颅窗后一周拍摄的图像,其他依次类推。
106.由图8可知,采用本实施例第一试剂、第二试剂及封闭剂建立的透明颅窗能够至少两个月内可以重复成像。
107.以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
108.以上所述实施例仅表达了本发明的几种实施方式,便于具体和详细地理解本发明的技术方案,但并不能因此而理解为对发明专利保护范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。应当理解的是,在本领域技术人员在本发明提供的技术方案的基础上,通过合乎逻辑的分析、推理或有限的试验得到的技术方案,均在本发明所附权利要求的保护范围内。因此,本发明专利的保护范围应以所附权利要求的内容为准,说明书及附图可以用于解释权利要求的内容。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1