一种盐酸头孢唑兰制剂的制备工艺的制作方法
1.本发明涉及药品领域,特别涉及一种盐酸头孢唑兰制剂的制备工艺。
背景技术:
2.盐酸头孢唑兰,化学名为(-)-1-[[(6r,7r)-7-[(z)-2-(5-氨基-1,2,4-噻二唑-3-基)-2-(甲氧亚氨基)乙酰氨基]-2-羧基-8-氧代-5-硫杂-1-氮杂双环[4,2,0]辛-2-烯-3-基]甲基]咪唑并[1,2-b]哒嗪鎓内盐盐酸盐。
[0003]
盐酸头孢唑兰具有显著的抗菌作用,对革兰氏阴性菌、革兰氏阳性菌、铜绿假单胞菌均有效。
[0004]
头孢克肟(cefixime)为口服用的第三代头孢菌素类抗生素,适用于治疗敏感菌所致的呼吸、泌尿和胆道等部位的感染。头孢克肟对革兰阴性杆菌产生的β-内酰胺酶高度稳定,对革兰阴性杆菌抗菌作用强于第一代和第二代头孢菌素,对革兰阳性球菌抗菌作用不如第一代和第二代头孢菌素。
[0005]
专利cn102697742b涉及头孢唑兰,特别涉及注射用盐酸头孢唑兰的制备工艺,采用了co2作为ph调节剂,处理后解决了盐酸头孢唑兰难以溶于水且不稳定,特别是有碱性物质存在下易降解的难题,专利cn102512375a涉及医药技术领域,具体涉及盐酸头孢唑兰组合物注射用粉针剂。盐酸头孢唑兰组合物注射用粉针剂,由盐酸头孢唑兰、无水碳酸钠、氯化钠、盐酸利多卡因组成;所述盐酸头孢唑兰、无水碳酸钠、氯化钠、盐酸利多卡因的质量比为500∶103∶60∶7.92~9.9。目前盐酸头孢唑兰注射剂中没有涉及到与其他抗生素类的联用,且多采用co2作为过程中ph的调节剂,或者需要在过程中监测ph的的变化。制备过程比较复杂。
技术实现要素:
[0006]
鉴以此,本发明的目的在于提出一种盐酸头孢唑兰制剂的制备工艺,所述盐酸头孢唑兰制剂用于静脉注射。
[0007]
一种盐酸头孢唑兰制剂的制备工艺,包括以下步骤:
[0008]
步骤1:取部分注射用水,用水浴加热,恒温5-10min后加入无水碳酸钠和氯化钠,缓慢滴加注射用水,配置饱和溶液;
[0009]
步骤2:称取盐酸头孢唑兰和头孢克肟,加入乙醇中,得到平衡稳态混悬溶液;
[0010]
步骤3:将步骤2中的溶液滴加到步骤1中,搅拌,控制水浴温度;
[0011]
步骤4:缓慢加入剩余注射用水,搅拌,控制水浴温度;
[0012]
步骤5:加入盐酸溶液,搅拌,调节ph,控制水浴温度;
[0013]
步骤6:将步骤5中的溶液用活性炭处理,过滤,再无菌过滤,得到无菌溶液;
[0014]
步骤7:全检合格后,将步骤6所得无菌溶液灌装在瓶中,半压塞,进箱冻干,压塞、复压、出箱扎盖,包装,成品入库。
[0015]
进一步的,所述盐酸头孢唑兰制剂用于静脉注射,由以下成分:无水碳酸钠、氯化
钠、盐酸头孢唑兰、头孢克肟、乙醇和水制备获得。
[0016]
进一步的,各组分的用量为:无水碳酸钠206份、氯化钠120份、盐酸头孢唑兰1000份,头孢克肟50份和注射用水8000-12000份。
[0017]
进一步的,所述步骤1中,称取的注射用水量为无水碳酸钠的质量的1.9-2.2倍,温度在33-37℃。
[0018]
进一步的,所述步骤1中,温度在35-36℃。
[0019]
进一步的,所述步骤2中,乙醇与盐酸头孢唑兰的体积比为3-5:1。
[0020]
进一步的,所述步骤3中,搅拌速度为100-150rpm/min,水浴温度为30-37℃。
[0021]
进一步的,所述步骤4中,搅拌速度为50-100rpm/min,水浴温度为25-30℃。
[0022]
进一步的,所述步骤5中,盐酸溶液的浓度为0.5-1mol/l,搅拌速度为50-100rpm/min,水浴温度为25℃,调节ph至7.5-8.5。
[0023]
进一步的,所述步骤6中,活性炭的用量为0.05-0.08%,g/ml。
[0024]
进一步的,所述步骤7中,冻干参数为:-50~-45℃,冻干30min;一次干燥,-10~-5℃,真空度15~20pa,10-12h;二次干燥,20~30℃,3-5h。
[0025]
与现有技术相比,本发明的有益效果为:
[0026]
1)本技术中添加了头孢克肟,对革兰氏阴性菌、革兰氏阳性菌等细菌的抗菌效果更强;
[0027]
2)本技术制备工艺简单,不需要通过co2,也不需要监测过程中的ph值;
[0028]
3)本技术制备获得的盐酸头孢制剂稳定性较好。
具体实施方式
[0029]
为对本发明中的技术方案进行清楚、完整地描述,显然,发明人结合实施例进行说明,但以下实施例所描述的仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0030]
实施例1:
[0031]
称取:无水碳酸钠206g、氯化钠120g、盐酸头孢唑兰1000g,头孢克肟20g,注射用水10000g。
[0032]
制备过程:
[0033]
步骤1:取400g注射用水,用水浴加热,保持温度在35℃,恒温5-10min后加入206g无水碳酸钠和120g氯化钠,缓慢滴加注射用水,配置饱和溶液;
[0034]
步骤2:称取1000g盐酸头孢唑兰和头孢克肟,加入乙醇中,得到平衡稳态混悬溶液,乙醇与盐酸头孢唑兰的体积比为4:1;
[0035]
步骤3:将步骤2中的溶液滴加到步骤1中,搅拌,控制水浴温度,搅拌速度为100rpm/min,水浴温度为33℃;
[0036]
步骤4:缓慢加入剩余注射用水,搅拌,控制水浴温度,搅拌速度为75rpm/min,水浴温度为25℃;
[0037]
步骤5:加入0.5mol/l盐酸溶液,搅拌速度为75rpm/min,调节ph至8,控制水浴温度为25℃;
[0038]
步骤6:将步骤5中的溶液用活性炭处理,活性炭的用量为0.06%(g/ml),过滤,再无菌过滤,得到无菌溶液;
[0039]
步骤7:全检合格后,将步骤6所得无菌溶液灌装成1000瓶,半压塞,进箱冻干,压塞、复压、出箱扎盖,包装,成品入库;冻干参数为:-50℃,冻干30min;一次干燥,-10℃,真空度15pa,10h;二次干燥,20℃,4h。
[0040]
实施例2:
[0041]
称取:无水碳酸钠206g、氯化钠120g、盐酸头孢唑兰1000g,头孢克肟20g,注射用水10000g。
[0042]
制备过程:
[0043]
步骤1:取440g注射用水,用水浴加热,保持温度在37℃,恒温5-10min后加入206g无水碳酸钠和120g氯化钠,缓慢滴加注射用水,配置饱和溶液;
[0044]
步骤2:称取1000g盐酸头孢唑兰和头孢克肟,加入乙醇中,得到平衡稳态混悬溶液,乙醇与盐酸头孢唑兰的体积比为5:1;
[0045]
步骤3:将步骤2中的溶液滴加到步骤1中,搅拌,控制水浴温度,搅拌速度为150rpm/min,水浴温度为30℃;
[0046]
步骤4:缓慢加入剩余注射用水,搅拌,控制水浴温度,搅拌速度为100rpm/min,水浴温度为30℃;
[0047]
步骤5:加入1mol/l盐酸溶液,搅拌速度为100rpm/min,调节ph至7.5,控制水浴温度为25℃;
[0048]
步骤6:将步骤5中的溶液用活性炭处理,活性炭的用量为0.05%(g/ml),过滤,再无菌过滤,得到无菌溶液;
[0049]
步骤7:全检合格后,将步骤6所得无菌溶液灌装成1000瓶,半压塞,进箱冻干,压塞、复压、出箱扎盖,包装,成品入库;冻干参数为:-45℃,冻干30min;一次干燥,-5℃,真空度20pa,12h;二次干燥,30℃,5h。
[0050]
实施例3:
[0051]
称取:无水碳酸钠206g、氯化钠120g、盐酸头孢唑兰1000g,头孢克肟20g,注射用水10000g。
[0052]
制备过程:
[0053]
步骤1:取395g注射用水,用水浴加热,保持温度在33℃,恒温5-10min后加入206g无水碳酸钠和120g氯化钠,缓慢滴加注射用水,配置饱和溶液;
[0054]
步骤2:称取1000g盐酸头孢唑兰和头孢克肟,加入乙醇中,得到平衡稳态混悬溶液,乙醇与盐酸头孢唑兰的体积比为3:1;
[0055]
步骤3:将步骤2中的溶液滴加到步骤1中,搅拌,控制水浴温度,搅拌速度为120rpm/min,水浴温度为37℃;
[0056]
步骤4:缓慢加入剩余注射用水,搅拌,控制水浴温度,搅拌速度为50rpm/min,水浴温度为25℃;
[0057]
步骤5:加入1mol/l盐酸溶液,搅拌速度为50rpm/min,调节ph至8.5,控制水浴温度为25℃;
[0058]
步骤6:将步骤5中的溶液用活性炭处理,活性炭的用量为0.08%(g/ml),过滤,再
无菌过滤,得到无菌溶液;
[0059]
步骤7:全检合格后,将步骤6所得无菌溶液灌装成1000瓶,半压塞,进箱冻干,压塞、复压、出箱扎盖,包装,成品入库;冻干参数为:-45℃,冻干30min;一次干燥,-10℃,真空度15pa,11h;二次干燥,30℃,3h。
[0060]
对比例1:
[0061]
不添加头孢克肟,其他参数同实施例1。
[0062]
对比例2:
[0063]
步骤1,3中的温度为20℃,其他参数同实施例1。
[0064]
对比例3:
[0065]
无水碳酸钠206g、氯化钠120g、盐酸头孢唑兰1000g,注射用水10000g。
[0066]
制备步骤:
[0067]
步骤1:称取处方量无水碳酸钠、氯化钠加入处方量50%注射用水中,搅拌至完全溶解;上述溶液温度控制在50℃,用co2调节溶液ph值至8,保温备用;
[0068]
步骤2:称取处方量50%注射用水,将其温度控制在50℃,保温备用;称取处方量盐酸头孢唑兰,加入上述已备好的注射用水中,快速搅拌溶解,温度控制在50℃;
[0069]
步骤3:确认辅料溶液的温度在50℃,ph在8;持续通co2保护,快速搅拌,将现配好的盐酸头孢唑兰溶液加入辅料溶液,混合;混合溶液的温度控制在50℃,保温搅拌20分钟;
[0070]
步骤4:称取药液总量0.1%重量比的针用活性炭加入上述混合溶液中,搅拌25分钟,过滤除炭;
[0071]
步骤5:药液降温至10℃,co2保护,再无菌过滤,得到无菌溶液;
[0072]
步骤6:全检合格后,所得无菌溶液灌装成1000瓶,半压塞,进箱冻干,压塞、复压、出箱扎盖,包装,成品入库;冻干参数为:-50℃,冻干30min;一次干燥,-10℃,真空度15pa,10h;二次干燥,20℃,4h。
[0073]
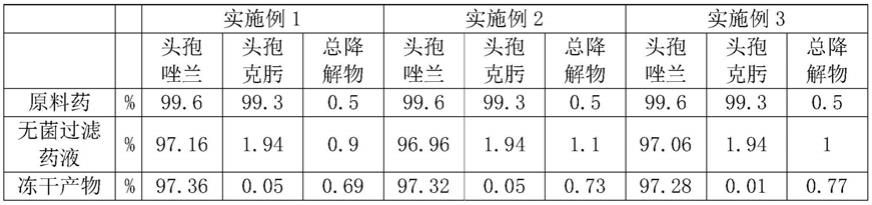
对实施例1-3,对比例1-3,制备过程中的药物进行高效液相色谱分析,结果如表1-2。
[0074]
表1:
[0075][0076]
表2:
[0077]
[0078]
由此可见,本技术所给方法制备获得的制剂杂质较少。
[0079]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1