壳寡糖肠溶滴丸及其在制备非酒精性脂肪肝药物中的应用
1.本发明属于医药领域,具体涉及一种壳寡糖肠溶滴丸及其在制备非酒精性脂肪肝药物中的应用。
背景技术:
2.非酒精性脂肪肝病(nafld)是当前最广泛的慢性肝病,进一步发展为非酒精性脂肪性肝炎(nash),nafld相关并发症主要包括高脂血症、肥胖和ii型糖尿病等,nafld和nash的肝特异性死亡率和总死亡率为0.77%和11.77%。nafld给人类带来的危害不可忽视,目前市场治疗nafld的药物较少,并且大多数仍在试验阶段,有许多应用缺陷且治疗效果不佳。因此,迫切需要研制安全、有效、副作用少的治疗nafld药物。
3.壳寡糖是(chitosanoligosaccharides,cos)由氨基葡萄糖和少量n-乙酰氨基葡萄糖通过β-1,4-糖苷键连接而成的海洋寡糖,具有多种生物活性,有一定调节肠道菌群的能力,同时还具有抑菌、抗肥胖、抗炎、抗氧化、降压、抗阿尔兹海默症和抗肿瘤等生理作用,但是将其应用于治疗非酒精性脂肪肝却鲜有报道。肠溶滴丸具有生物利用度高、药物稳定性强、同时能够控制药物于肠道中释放等特性。但是目前滴丸的制备过程中影响因素较多,滴距、药液熔融温度等都会影响滴丸的圆整度。
4.专利公开号为cn112826876a的专利文本公开了藤茶水提取在制备改善肝损伤的制剂中的应用,其公开了肝损伤包括酒精性肝损伤、药物性肝损伤、酒精性脂肪肝和非酒精性脂肪肝,并进一步公开了一种用于调节肠道微生态的藤茶组合物,该药物组合物含有藤茶水提物、益生元和药用辅料;所述益生元为木寡糖、果寡糖、壳寡糖、甘露寡糖和葡寡糖中的至少一种。虽然其公开了壳寡糖在治疗肝损伤上的应用,但是其组合物并非肠溶包衣滴丸,壳寡糖易被空气氧化水解,降低治疗效果。
5.专利公开号为cn105030816a的专利文本公开了一种用于治疗非酒精性脂肪肝的复合保肝中药,其配方为壳寡糖、红景天苷、白藜芦醇、虾青素和刺参糖胺聚糖,其中,红景天苷、壳寡糖、白藜芦醇和刺身糖胺聚糖经过科学配比后,能够调节脂质代谢相关基因,显著降低nafld肝脏细胞内甘油三酯含量,可以减轻脂肪酸诱导的细胞凋亡,可以减轻高脂饮食小鼠肝脏脂肪变性,降低肝内tg含量,且无明显副作用。但是其起到主要作用的组分并非壳寡糖,也没有给出壳寡糖治疗nafld的活性研究和机制研究,同时,此配方也并非肠溶包衣滴丸,同样存在壳寡糖易被空气氧化水解,降低治疗效果的技术问题。
6.综上所述,现有技术中普遍存在壳寡糖稳定性差、肠溶包衣滴丸圆整度差等技术问题。
技术实现要素:
7.为了克服上述技术问题,本发明的目的在于提供一种壳寡糖肠溶滴丸及其制备非酒精性脂肪肝药物中的应用。本发明提供的壳寡糖肠溶滴丸能够改善机体高血糖水平和高脂高蔗糖饮食引起的脂代谢异常,在一定程度上改善高脂高蔗糖饮食引起的肝功能指标异
常,增强非酒精性脂肪肝小鼠的血清抗氧化功能,促进抗炎因子的释放,达到减轻炎症的目的,增强了壳寡糖的稳定性,且壳寡糖肠溶滴丸的圆整性较好。
8.为了实现上述目的,本发明的技术方案如下:
9.一种壳寡糖肠溶滴丸,由肠溶层包衣和丸芯按照质量比为6-10:13-17组成。
10.进一步的,所述壳寡糖肠溶滴丸中的肠溶层包衣由以下组分及其重量份数组成:尤特奇l100-55 20-40份、滑石粉10-20份、聚乙二醇6000 2-4份、乙醇218-436份。
11.更进一步的,所述壳寡糖肠溶滴丸中的肠溶层包衣的制备方法为:称取配方量的尤特奇l100-55,缓慢加入至预先与滑石粉和聚乙二醇6000混合均匀的95%乙醇中,制备成l100-55质量分数为8%的混悬液,过80目筛,即得。
12.进一步的,所述壳寡糖肠溶滴丸中的丸芯由壳寡糖和基质按照质量比为1:2-4组成。
13.更进一步的,所述壳寡糖肠溶滴丸中的丸芯基质由聚乙二醇6000和硬脂酸按照质量比为3-5:7-11组成。
14.更进一步的,所述壳寡糖肠溶滴丸中的丸芯的制备方法为:取适量基质,置入烧杯,水浴加热磁力搅拌至充分熔融,搅拌同时缓慢加入壳寡糖,充分混匀后,装入自制滴丸器中,在滴距为15-30cm、滴速为25-30滴/min的条件下,滴入至预冷至5-10℃的液体石蜡冷凝介质中,冷凝、固化,形成滴丸后,通过离心去除冷凝介质,干燥密封保存。
15.更进一步的,所述壳寡糖肠溶滴丸中丸芯的制备过程中熔融温度为80-90℃。
16.本发明还提供了所述壳寡糖肠溶滴丸的制备方法,具体为:将丸芯放入高效包衣机中,设置包衣机转速为22-27rpm,进风温度为40-50℃,出风温度为25-30℃,物料温度为25-30℃,预热15min,然后进行包衣,肠溶层包衣液在雾化压力值为0.11-0.13mpa的喷枪中喷出,当包衣重量达到丸芯重量的20%时取出,放入鼓风烘箱中,30℃干燥1h,即得。
17.进一步的,所述壳寡糖肠溶滴丸在制备治疗非酒精性脂肪肝药物中的应用。
18.本发明壳寡糖肠溶滴丸丸芯中的基质是主药壳寡糖的药物载体,在稳定有效使药物释放的同时也不会影响药物的稳定性。聚乙二醇6000为应用较多的水溶性基质,但是研究过程中发现聚乙二醇6000常常会使病人产生依赖性,而硬脂酸与聚乙二醇6000采用3-5:7-11的比例共同组成丸芯的基质,不仅可以降低病人对聚乙二醇6000的依赖性,而且能够有效提高药物在小肠中的分散性,增强药物的吸收率。
19.本发明中研究发现,在丸芯的制备过程中,基质的熔融温度和滴距会影响丸芯的圆整度,当熔融温度较低时,滴丸滴入冷凝介质时,由于来不及成球形便过早冷凝,所以更容易拖尾,圆整度较差;当熔融温度较高时,滴丸滴入冷凝介质时,不会立刻凝结,而是以熔融状态在冷凝介质中下沉一段时间,此时冷凝介质的表面张力会促使滴丸团聚成圆整的球形。当滴距较大时,滴丸至液面时,由于速度较大,产生的冲击使得滴丸圆整性较差,多数滴丸会有小药液分出,导致最终成型滴丸上有小孔,同时,由于滴入液面速度较大,可能导致滴丸尚未凝固,即触及底部,导致部分滴丸黏连的现象;而滴距较小时,滴丸尚未在空气中形成球体,即进入冷凝介质中,故产生大量拖尾。
20.在包衣过程中,包衣机转速起到了至关重要的作用,包衣机工作时,包衣液经喷头喷至被匀速旋转包衣桶搭载的物料上,包衣桶旋转使物料能够充分与包衣液接触,若物料桶转速过快,包衣包覆不均匀,而转速过慢,包衣液将不易挥干。
21.与现有技术相比,本发明提供的壳寡糖肠溶滴丸及其在制备非酒精性脂肪肝药物中的应用具有如下优势:
22.(1)本发明提供的壳寡糖肠溶滴丸对非酒精性脂肪肝小鼠的食欲和体重没有影响,能够改善机体高血糖水平和高脂高蔗糖饮食引起的脂代谢异常;
23.(2)本发明提供的壳寡糖肠溶滴丸能够在一定程度上改善高脂高蔗糖饮食引起的肝功能指标异常,增强非酒精性脂肪肝小鼠的血清抗氧化功能;
24.(3)本发明提供的壳寡糖肠溶滴丸能够促进抗炎因子的释放,达到减轻炎症的目的;
25.(4)本发明提供的壳寡糖肠溶滴丸将壳寡糖制备为肠溶滴丸,一方面能够避免壳寡糖被空气所氧化及水解,增强制剂的稳定性,另一方面能够靶向释药于肠道,增强壳寡糖对肠道菌群调节的能力。
具体实施方式
26.以下通过具体实施方式进一步描述本发明,但本发明不仅仅限制于以下实施例。本领域的技术人员根据本发明的基本思想,可以做出各种修改,但是只要不脱离本发明的基本思想,均在本发明的范围之内。
27.本实施方式中,所述壳寡糖肠溶滴丸的制备方法中的包衣温度包括物料温度、进风温度和出风温度。为方便动物实验的进行,本具体实施方式中控制壳寡糖肠溶滴丸的粒径为1.9mm。
28.实施例1、一种壳寡糖肠溶滴丸及其制备方法
29.所述壳寡糖肠溶滴丸,由肠溶层包衣和丸芯按照质量比为6:13组成。
30.所述壳寡糖肠溶滴丸中的肠溶层包衣由以下组分及其重量份数组成:尤特奇l100-55 20份、滑石粉10份、聚乙二醇6000 2份、乙醇218份。
31.所述壳寡糖肠溶滴丸中的肠溶层包衣的制备方法为:称取配方量的尤特奇l100-55,缓慢加入至预先与滑石粉和聚乙二醇6000混合均匀的95%乙醇中,制备成l100-55质量分数为8%的混悬液,过80目筛,即得。
32.所述壳寡糖肠溶滴丸中的丸芯由以下组分及其重量份数组成:壳寡糖:基质=1:2;所述基质由聚乙二醇6000和硬脂酸按照质量比为3:7组成。
33.所述壳寡糖肠溶滴丸中的丸芯的制备方法为:取适量基质,置入烧杯,水浴加热磁力搅拌至充分熔融,熔融温度为80℃,搅拌同时缓慢加入壳寡糖,充分混匀后,装入自制滴丸器中,在滴距为15cm、滴速为25滴/min的条件下,滴入至预冷至5℃的液体石蜡冷凝介质中,冷凝、固化,形成滴丸后,通过离心去除冷凝介质,干燥密封保存。
34.所述壳寡糖肠溶滴丸的制备方法,具体为:将丸芯放入高效包衣机中,设置包衣机转速为22rpm,进风温度为40℃,出风温度为25℃,物料温度为25℃,预热15min,然后进行包衣,肠溶层包衣液在雾化压力值为0.11mpa的喷枪中喷出,当包衣重量达到丸芯重量的20%时取出,放入鼓风烘箱中,30℃干燥1h,即得。
35.实施例2、一种壳寡糖肠溶滴丸及其制备方法
36.所述壳寡糖肠溶滴丸,由肠溶层包衣和丸芯按照质量比为10:17组成。
37.所述壳寡糖肠溶滴丸中的肠溶层包衣由以下组分及其重量份数组成:尤特奇
l100-55 40份、滑石粉20份、聚乙二醇6000 4份、乙醇436份。
38.所述壳寡糖肠溶滴丸中的肠溶层包衣的制备方法为:称取配方量的尤特奇l100-55,缓慢加入至预先与滑石粉和聚乙二醇6000混合均匀的95%乙醇中,制备成l100-55质量分数为8%的混悬液,过80目筛,即得。
39.所述壳寡糖肠溶滴丸中的丸芯由以下组分及其重量份数组成:壳寡糖:基质=1:4;所述基质由聚乙二醇6000和硬脂酸按照质量比为5:11组成。
40.所述壳寡糖肠溶滴丸中的丸芯的制备方法为:取适量基质,置入烧杯,水浴加热磁力搅拌至充分熔融,熔融温度为90℃,搅拌同时缓慢加入壳寡糖,充分混匀后,装入自制滴丸器中,在滴距为30cm、滴速为30滴/min的条件下,滴入至预冷至10℃的液体石蜡冷凝介质中,冷凝、固化,形成滴丸后,通过离心去除冷凝介质,干燥密封保存。
41.所述壳寡糖肠溶滴丸的制备方法,具体为:将丸芯放入高效包衣机中,设置包衣机转速为27rpm,进风温度为50℃,出风温度为30℃,物料温度为30℃,预热15min,然后进行包衣,肠溶层包衣液在雾化压力值为0.13mpa的喷枪中喷出,当包衣重量达到丸芯重量的20%时取出,放入鼓风烘箱中,30℃干燥1h,即得。
42.实施例3、一种壳寡糖肠溶滴丸及其制备方法
43.所述壳寡糖肠溶滴丸,由肠溶层包衣和丸芯按照质量比为8:15组成。
44.所述壳寡糖肠溶滴丸中的肠溶层包衣由以下组分及其重量份数组成:尤特奇l100-55 31份、滑石粉16份、聚乙二醇6000 3份、乙醇326份。
45.所述壳寡糖肠溶滴丸中的肠溶层包衣的制备方法为:称取配方量的尤特奇l100-55,缓慢加入至预先与滑石粉和聚乙二醇6000混合均匀的95%乙醇中,制备成l100-55质量分数为8%的混悬液,过80目筛,即得。
46.所述壳寡糖肠溶滴丸中的丸芯由以下组分及其重量份数组成:壳寡糖:基质=1:3;所述基质由聚乙二醇6000和硬脂酸按照质量比为4:9组成。
47.所述壳寡糖肠溶滴丸中的丸芯的制备方法为:取适量基质,置入烧杯,水浴加热磁力搅拌至充分熔融,熔融温度为86℃,搅拌同时缓慢加入壳寡糖,充分混匀后,装入自制滴丸器中,在滴距为21cm、滴速为27滴/min的条件下,滴入至预冷至8℃的液体石蜡冷凝介质中,冷凝、固化,形成滴丸后,通过离心去除冷凝介质,干燥密封保存。
48.所述壳寡糖肠溶滴丸的制备方法,具体为:将丸芯放入高效包衣机中,设置包衣机转速为25rpm,进风温度为46℃,出风温度为27℃,物料温度为28℃,预热15min,然后进行包衣,肠溶层包衣液在雾化压力值为0.12mpa的喷枪中喷出,当包衣重量达到丸芯重量的20%时取出,放入鼓风烘箱中,30℃干燥1h,即得。
49.对比例1、一种壳寡糖肠溶滴丸及其制备方法
50.所述壳寡糖肠溶滴丸,由肠溶层包衣和丸芯按照质量比为8:15组成。
51.所述壳寡糖肠溶滴丸中的肠溶层包衣由以下组分及其重量份数组成:尤特奇l100-55 31份、滑石粉16份、聚乙二醇6000 3份、乙醇326份。
52.所述壳寡糖肠溶滴丸中的丸芯由以下组分及其重量份数组成:壳寡糖:基质=1:3;所述基质为聚乙二醇6000。
53.本对比例中所述肠溶包衣、丸芯和壳寡糖肠溶滴丸的制备方法与实施例3类似。
54.本对比例与实施例3的区别为:本对比例中所述基质全部为聚乙二醇6000。
55.对比例2、一种壳寡糖肠溶滴丸及其制备方法
56.所述壳寡糖肠溶滴丸,由肠溶层包衣和丸芯按照质量比为8:15组成。
57.所述壳寡糖肠溶滴丸中的肠溶层包衣由以下组分及其重量份数组成:尤特奇l100-55 31份、滑石粉16份、聚乙二醇6000 3份、乙醇326份。
58.所述壳寡糖肠溶滴丸中的丸芯由以下组分及其重量份数组成:壳寡糖:基质=1:3;所述基质由聚乙二醇6000和硬脂酸按照质量比为4:9组成。
59.本对比例中所述肠溶包衣、丸芯和壳寡糖肠溶滴丸的制备方法与实施例3类似。
60.本对比例与实施例3的区别为:本对比例中所述基质由聚乙二醇6000和硬脂酸按照质量比为1:1组成。
61.对比例3、一种壳寡糖肠溶滴丸及其制备方法
62.所述壳寡糖肠溶滴丸,由肠溶层包衣和丸芯按照质量比为8:15组成。
63.所述壳寡糖肠溶滴丸中的肠溶层包衣由以下组分及其重量份数组成:尤特奇l100-55 31份、滑石粉16份、聚乙二醇6000 3份、乙醇326份。
64.所述壳寡糖肠溶滴丸中的丸芯由以下组分及其重量份数组成:壳寡糖:基质=1:3;所述基质由聚乙二醇6000和硬脂酸按照质量比为4:9组成。
65.本对比例中所述肠溶包衣、丸芯和壳寡糖肠溶滴丸的制备方法与实施例3类似。
66.本对比例与实施例3的区别为:本对比例丸芯的制备过程中所述基质的熔融温度为110℃。
67.对比例4、一种壳寡糖肠溶滴丸及其制备方法
68.所述壳寡糖肠溶滴丸,由肠溶层包衣和丸芯按照质量比为8:15组成。
69.所述壳寡糖肠溶滴丸中的肠溶层包衣由以下组分及其重量份数组成:尤特奇l100-55 31份、滑石粉16份、聚乙二醇6000 3份、乙醇326份。
70.所述壳寡糖肠溶滴丸中的丸芯由以下组分及其重量份数组成:壳寡糖:基质=1:3;所述基质由聚乙二醇6000和硬脂酸按照质量比为4:9组成。
71.本对比例中所述肠溶包衣、丸芯和壳寡糖肠溶滴丸的制备方法与实施例3类似。
72.本对比例与实施例3的区别为:本对比例丸芯的制备过程中所述基质的熔融温度为60℃。
73.对比例5、一种壳寡糖肠溶滴丸及其制备方法
74.所述壳寡糖肠溶滴丸,由肠溶层包衣和丸芯按照质量比为8:15组成。
75.所述壳寡糖肠溶滴丸中的肠溶层包衣由以下组分及其重量份数组成:尤特奇l100-55 31份、滑石粉16份、聚乙二醇6000 3份、乙醇326份。
76.所述壳寡糖肠溶滴丸中的丸芯由以下组分及其重量份数组成:壳寡糖:基质=1:3;所述基质由聚乙二醇6000和硬脂酸按照质量比为4:9组成。
77.本对比例中所述肠溶包衣、丸芯和壳寡糖肠溶滴丸的制备方法与实施例3类似。
78.本对比例与实施例3的区别为:本对比例丸芯的制备过程中所述滴距为40cm。
79.对比例6、一种壳寡糖肠溶滴丸及其制备方法
80.所述壳寡糖肠溶滴丸,由肠溶层包衣和丸芯按照质量比为8:15组成。
81.所述壳寡糖肠溶滴丸中的肠溶层包衣由以下组分及其重量份数组成:尤特奇l100-55 31份、滑石粉16份、聚乙二醇6000 3份、乙醇326份。
82.所述壳寡糖肠溶滴丸中的丸芯由以下组分及其重量份数组成:壳寡糖:基质=1:3;所述基质由聚乙二醇6000和硬脂酸按照质量比为4:9组成。
83.本对比例中所述肠溶包衣、丸芯和壳寡糖肠溶滴丸的制备方法与实施例3类似。
84.本对比例与实施例3的区别为:本对比例中丸芯的制备过程中所述滴距为10cm。
85.试验例一、壳寡糖改善非酒精性脂肪肝的活性测试
86.试验方法:模型建立:在温度为22-26℃,相对湿度为55
±
5%,12h明暗循环时间的spf级实验室下进行小鼠喂养、造模及给药实验。使用许可证号:syxk(粤)2017-0125。将70只7周龄(20-24g)c57bl/6小鼠,给予维持饲料(nfd)适应喂养1周后,随机将所有小鼠分为2组:空白组10只,给予维持饲料;造模组60只,给予高脂高蔗糖饲料(hfhsd)。喂养8周后,随机将小鼠分为7组:空白组(control)、nafld模型组(model)、实施例1-3组、对比例1-2组,10只小鼠/组。给药剂量为:425mg/kg/d。
87.每日根据按体重灌胃各组小鼠试验样品,其中control组和model组灌胃等量超纯水。给药干预6周后,采用眼球取血法取血,留取血样、肝脏、回肠、结肠、盲肠内容物、粪便等样品,于-80℃下保存,以供后续实验使用。
88.维持饲料配比为:粗蛋白20%,水分9.7%,粗纤维4.8%,粗脂肪4.3%,钙1.19%,磷0.77%,粗灰分为6.60%,购于广东省医学实验动物中心;高脂高蔗糖饲料热量主要来源:40%来自脂肪,17%来自蔗糖,购于美国research diets公司,lot:d1237。
89.小鼠体重:动物实验期间,每周称量小鼠体重,并记录每组平均值;每周称量各组小鼠饲料剩余量以及饲料给予量,以推算其每组小鼠的每日进食量;留意小鼠的身心情况,同时做好记录。
90.口服葡萄糖耐量实验:实验结束前一周,每组随机选取小鼠5只进行实验,受试小鼠提前12h更换干净垫料并禁食。试验进行时,先称量小鼠体重,再用消毒棉片轻拭鼠尾消毒,剪去末端约0.1cm,将血液滴于血糖试纸测定处测定血糖值,即得0min时刻的血糖值;以小鼠体重按2.0g/kg快速灌注小鼠20%葡萄糖,于15、30、60、90和120min时刻分别测定血糖值并记录,计算曲线下面积(auc)。计算公式为:auc=15min值
×
0.25+30min值
×
0.5+60min值
×
0.75+120min值
×
0.5。
91.血清与肝脏指标测定:血清指标测定:血样常温静置30min,4℃3000rpm离心15min,取上层血清,按试剂盒说明书要求测定血清tc、tg、hdl-c、ldl-c、ffa、ast、alt、cat、t-aoc水平,并使用elisa试剂盒测定血清il-6、il-10、tnf-α、insulin及lps的水平。肝脏指标测定:精密称取等量肝脏组织,加入适量无水乙醇及匀浆钢珠,于-20℃预冷的匀浆机中匀浆,于4℃2500rpm离心10min,取上清液,采用试剂盒测定其中tg和tc的含量。
92.试验结果见下表。
93.表1 试验样品对nafld小鼠体重的影响
94.组别1周2周3周4周5周6周实施例1323742475359实施例2343942485460实施例3333741455158对比例1343843485360对比例2333944495561
model组283336404449control组343944505663
95.表2 试验样品对nafld小鼠摄食量的影响
96.组别摄食量/g实施例1198.6实施例2199.3实施例3199.1对比例1200.4对比例2199.7model组201.3control组176.5
97.由表1和表2可知,模型组小鼠的体重和摄食量均高于空白组小鼠,这说明本实施例中模型建立成功。实施例1-3组小鼠的体重及摄食量与模型组小鼠的体重及摄食量差别不大,这说明本发明提供的壳寡糖肠溶滴丸不会影响小鼠的体重及摄食量。
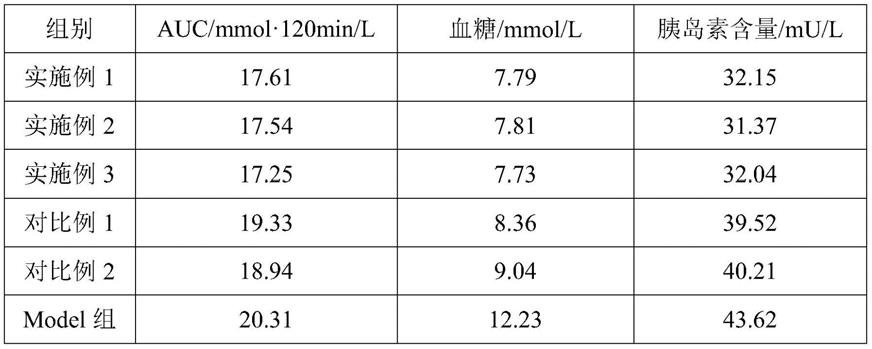
98.表3 试验样品对胰岛素抵抗的影响
[0099][0100][0101]
由表3可知,本发明提供的壳寡糖肠溶滴丸能够显著改善hfhsd小鼠的高血糖水平,同时改善hfhsd诱导的机体高胰岛素水平,这说明本发明提供的壳寡糖肠溶滴丸能够通过改善机体的胰岛素抵抗,改善高血糖水平。其中,实施例3组小鼠的auc和血糖最低,胰岛素含量适中,为本发明最佳实施例。
[0102]
与实施例3相比,对比例1和对比例2改变了丸芯中基质的用量比,但是对应组小鼠的auc、血糖和胰岛素含量均增加,这充分说明本发明提供的壳寡糖肠溶滴丸丸芯基质能够有效提高药物在小肠中的分散性,增强基药物的吸收率。
[0103]
表4 试验样品对nafld小鼠血脂的影响
[0104][0105]
由表4可知,本发明提供的壳寡糖肠溶滴丸能够显著改善hfhsd小鼠血清甘油三酯和血清总胆固醇水平,降低hfhsd小鼠血清低密度脂蛋白胆固醇和游离脂肪酸,提高血清高密度脂蛋白胆固醇,这充分说明本发明提供的壳寡糖肠溶滴丸能够改善hfhsd饮食引起的脂代谢异常。
[0106]
表5 试验样品对nafld小鼠肝功能的影响
[0107][0108][0109]
由表5可知,相对于空白组,模型组小鼠的血清谷草转氨酶含量和血清谷丙转氨酶水平明显升高,说明长时间高脂高蔗糖饲料喂养已经导致小鼠一定程度肝功能损伤。而实施例1-3组小鼠的血清谷草转氨酶含量和血清谷丙转氨含量显著降低,这充分说明壳寡糖肠溶滴丸能够在一定程度上改善高脂高蔗糖引起的肝功能指标异常。
[0110]
表6 试验样品对nafld小鼠血清抗氧化功能的影响
[0111]
组别血清过氧化氢酶/u/l血清总氧化能力/u/mg
·
prot实施例149.890.47实施例250.150.46
实施例350.350.47对比例140.160.40对比例245.350.43model组30.920.38control组56.770.49
[0112]
由表6可知,高脂高蔗糖饲料喂养能够显著降低血清抗氧化功能指标过氧化氢酶和总抗氧化能力,而壳寡糖肠溶滴丸能够在一定程度改善非酒精性脂肪肝小鼠的血清过氧化氢酶和血清总氧化能力的水平,这说明壳寡糖肠溶滴丸能够增强非酒精性脂肪肝小鼠的抗氧化功能。
[0113]
表7 试验样品对nafld小鼠血清炎症因子的影响
[0114][0115][0116]
由表7可知,相对于空白组,模型组小鼠血清中的tnf-α、il-6水平显著升高,说明长时间的高脂高蔗糖饲料喂养引起了小鼠全身性炎症反应。而实施例1-3组小鼠的tnf-α、il-6水平显著降低,il-10水平明显升高,这说明本发明提供的壳寡糖肠溶滴丸能够促进抗炎因子的释放,最终达到减轻炎症的目的,即壳寡糖肠溶滴丸具有一定改善非酒精性脂肪肝小鼠炎症的能力。
[0117]
试验例二、壳寡糖肠溶滴丸质量测试
[0118]
试验样品:实施例1-3、对比例3-6制得的壳寡糖肠溶滴丸;
[0119]
试验方法:取试验样品,观察滴丸是否光泽、均匀、圆整度是否完好;
[0120]
散溶时限:按2020版《中国药典》四部制剂通则0108丸剂项下测定,取供试品6丸,选择孔径为2.00mm的筛网,置于崩解时限仪中。先于人工胃液中检查2h,不得有裂缝、崩解或软化现象。再取出吊篮,加入少量超纯水润洗,各置入1块挡板,再按上法在人工肠液中检查,1h内应全部溶散。
[0121]
试验结果见下表。
[0122]
表8 壳寡糖肠溶滴丸外观
[0123]
组别外观实施例1光泽、均匀、圆整实施例2光泽、均匀、圆整
实施例3光泽、均匀、圆整对比例3光泽、不均匀、有拖尾对比例4光泽、不均匀、有拖尾对比例5不均匀、有拖尾、滴丸表面有孔洞对比例6不均匀、拖尾严重
[0124]
由表8可知,本发明提供壳寡糖肠溶滴丸为均匀光泽的类圆形丸,对比例3-4改变了丸芯基质的熔融温度、对比例5-6改变了丸芯的滴距,但是制得的壳寡糖肠溶滴丸的圆整性差,说明本发明提供的丸芯的熔融温度和滴距已达到最优化。
[0125]
表9 容散时限测试
[0126]
组别容散时限/min实施例19.52实施例29.64实施例39.49对比例39.79对比例410.01对比例59.81对比例69.92
[0127]
由表9可知,本发明提供的壳寡糖肠溶滴丸的容散时限均在10min之内,符合《中国药典》2020版的规定。
[0128]
上述实施例仅例示性说明本发明的制备方法,而并非限制本发明。本领域任何熟悉此技术的认识皆不可在违背本发明的精神及范畴下,对上述实施例进行修改。因此,举凡所属技术领域中具有通常知识者在未脱离本发明所提供的技术思想下完成的一切等效修饰或改变,仍由本发明的权利要求所涵盖。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1