Amuc_1100在制备缓解阿霉素化疗心脏毒性药物中的用途的制作方法
amuc_1100在制备缓解阿霉素化疗心脏毒性药物中的用途
技术领域
1.本发明涉及一种药物的新用途,具体涉及一种amuc_1100在制备缓解阿霉素化疗心脏毒性药物中的用途。
背景技术:
2.阿霉素(doxorubicin,dox)是目前临床上常规使用的一种广谱、高效的蒽环类抗癌药物,广泛应用于白血病、恶性淋巴瘤、乳腺癌、卵巢癌和成骨肉瘤等治疗。尽管以dox为代表的蒽环类药物增加了癌症患者的长期生存率,但其造成的剂量依赖性心脏毒性副作用,以及最终可能导致的不可逆心肌损伤和充血性心力衰竭,极大限制了其在临床上的应用。
3.目前预防蒽环类药物毒性的心脏保护策略主要包括使用心脏保护剂或降低化疗药累积用量以减轻心脏毒性效力。右丙亚胺是目前唯一获批的蒽环类药物心脏毒性保护剂。尽管右丙亚胺在与蒽环类化疗药物联合使用时可以防止静息性左心室射血分数的降低,减少心力衰竭发生率,但是,其可加重化疗药物引起的骨髓抑制,影响抗肿瘤效果,并且临床研究表明采用fac方案(氟尿嘧啶、阿霉素、环磷酰胺)加右丙亚胺可能使患者接受较高的阿霉素累积量(与未加右丙亚胺组比较),但并不能消除蒽环类药物诱导的心脏毒性。除此以外,使用大量活性氧(ros)清除剂和铁螯合剂治疗也并不能有效预防dox诱导的癌症患者心肌病或有明显的临床应用缺陷。正是由于当前临床用药中存在的上述问题,因此,开发治疗蒽环类药物化疗心脏毒性的新型药物和干预方式迫在眉睫。临床中dox化疗可刺激胃黏膜,出现恶心、呕吐、腹胀、腹痛或便秘等症状,化疗病人补充益生菌可以改善上述症状,帮助消化食物,然而并不能缓解dox引起的心脏毒性。dox治疗还可引起肠上皮功能、潘氏细胞和黏液的损伤改变,造成肠道屏障粘膜损伤。肠道屏障具有维持肠道内环境平衡、阻碍致病菌及毒素向肠腔外组织、器官移位和释放。肠道屏障受损,将会导致大量细菌和内毒素吸收、迁移至血液循环和淋巴系统,可能引起包括脓毒症、血管和心脏不良重构在内的全身多器官功能损害。研究发现在肠道屏障损伤过程中被激活的肠道免疫细胞会发生迁移并导致远端器官炎症。我们推测除了dox经循环对心脏的直接影响外,由其造成的肠道屏障损伤,进而引起的机体及心脏免疫细胞稳态失衡,可能是加剧dox心脏毒性的重要因素之一。
4.基于上述观点,本发明采用具有肠道屏障保护功能的生物大分子amuc1100在dox治疗前期进行提前干预,以此维持dox化疗期间的肠道屏障完整性,并进一步改善机体和心脏免疫细胞稳态失衡,减轻dox化疗的心脏毒性风险。
5.amuc_1100是肠道细菌akkermansia muciniphila的外膜蛋白,研究发现,amuc_1100可改善肥胖和糖尿病小鼠的代谢,改善结直肠炎及预防炎性结直肠癌,另外还可改善免疫治疗引起的肠道屏障损伤。
6.尽管amuc_1100显示出在改善代谢性疾病方面潜在的生物学功能,但是并没有报道其在缓解肿瘤dox化疗造成的心脏毒性方面的作用和保护机理。
7.本发明提供了一种减轻阿霉素化疗心脏毒性的潜在药物和干预方式,并兼顾改善
阿霉素造成的肠道功能损伤,同时由于上述干预方式便捷,因此本发明可以有效减轻肿瘤患者化疗痛苦,及心理和经济负担。
技术实现要素:
8.本发明的目的在于克服现有药物和技术存在的不足,提供一种amuc_1100在制备缓解阿霉素化疗心脏毒性药物中的用途。本发明首次提出通过口服amuc_1100防治阿霉素(dox)化疗诱导的心脏毒性,克服了目前关于dox临床用药限制和现有化疗心脏保护药物的弊端,同时解决了dox化疗中诱导产生的心脏毒性的防治问题。
9.本发明的目的是通过以下技术方案来实现的:
10.本发明涉及一种膜蛋白amuc_1100在制备缓解阿霉素化疗心脏毒性药物中的用途。
11.所述amuc_1100氨基酸序列为:
12.ivnskrseldkkisiaakeiksanaaeitpsrssneelekelnryakavgsletaykpflassalvpttptafqnelktfrdslissckkknilitdtsswlgfqvystqapsvqaastlgfelkainslvnklaecglskfikvyrpqlpietpannpeesdeadqapwtpmpleiafqgdresvlkamnaitgmqdylftvnsirirnermmpppianpaaakpaaaqpatgaasltpadeaaapaapaiqqvikpymgkeqvfvqvslnlvhfnqpkaqepsed。
13.作为本发明的一个实施方案,amuc_1100用法为:dox治疗前一周开始每天口服灌胃一次,dox治疗后隔天口服灌胃一次。
14.作为本发明的一个实施方案,amuc_1100针对小鼠用量为:按200μl/只进行灌胃,每只3ug/day。
15.作为本发明的一个实施方案,amuc_1100针对成人用量为:按70kg体重,口服药量约为0.58~2.31mg/day。
16.与现有技术相比,本发明具有如下有益效果:
17.1、本发明通过采用先于化疗前1周灌胃amuc_1100行口服干预,能非常有效的防治阿霉素dox化疗导致的心脏毒性,包括明显改善心脏左室收缩和舒张功能,提高射血分数,减少循环中心肌酶含量,降低心脏纤维化和凋亡水平;同时兼有保护化疗引起的肠道屏障损伤的作用。
18.2、amuc_1100缓解dox化疗心脏毒性的机理在于:
19.2.1、肠道上皮屏障损伤可导致大量细菌和内毒素吸收、迁移至血液循环和淋巴系统,可能引起包括脓毒症、血管和心脏不良重构在内的全身多器官功能损害;amuc_1100调节肠道免疫屏障,并调节紧密连接蛋白(tj)的结构和表达,促进肠道屏障损伤恢复。
20.2.2、amuc_1100可以有效恢复肠道屏障完整性,因此可能有效减轻肠屏障损伤造成的内毒素血症或肠道黏膜免疫细胞的激活和迁移,这对于减轻dox造成的内毒素由肠道进入循环进而影响心脏功能的相关保护途径是重要的。
21.2.3、本发明发现,经过amuc_1100干预的dox小鼠,其脾脏指数下降,脾脏ifn-γ(th1)水平显著下降,而il-4(th2)水平无显著改变,心脏ros水平下降,流式细胞分析结果显示,心脏t细胞比例显著下降。amuc_1100通过改善肠道屏障功能,减少脾脏免疫细胞经循环向肠道及心脏等器官的输出和累积,维持机体和心脏免疫细胞稳态,减轻t细胞对心肌组织的过度反应,降低ros水平,进而抑制心肌细胞凋亡,这可能是amuc_1100缓解dox心脏毒
性的重要机制。
附图说明
22.通过阅读参照以下附图对非限制性实施例所作的详细描述,本发明的其它特征、目的和优点将会变得更明显:
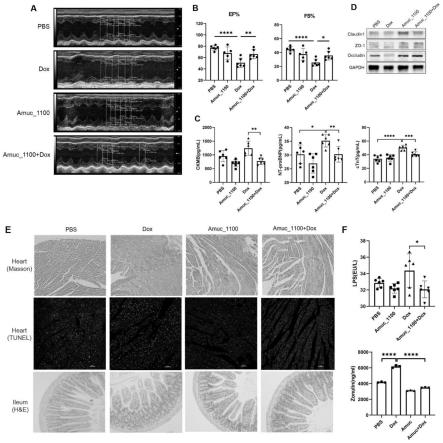
23.图1中a-b.amuc_1100干预后小鼠心脏左室超声检查;c.心肌酶谱测定结果;d.western blot分析肠道紧密连接蛋白zo-1,occludin和claudin1的表达水平;e.病理组织切片分析小鼠心脏(masson和tunel)和肠道(h&e);f.elisa分析血浆中反映肠道屏障损伤的标志物lps和zonulin水平;
24.图2中a为脾脏指数、脾脏中ifn-γ和il-4水平和心脏中ros水平;b为流式细胞分析心脏免疫细胞组成。
具体实施方式
25.下面结合实施例对本发明进行详细说明。以下实施例将有助于本领域的技术人员进一步理解本发明,但不以任何形式限制本发明。应当指出的是,对本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干调整和改进。这些都属于本发明的保护范围。
26.实施例1
27.1.实验动物及分组
28.spf级6-8周雄性c57bl/6小鼠,体重约18-20g,购自北京斯贝福实验动物有限公司。在郑州大学实验动物中心饲养。
29.实验分组包括:口服pbs组(pbs组),口服pbs+注射dox组(dox组),口服amuc_1100组(amuc组),口服amuc_1100+注射dox组(amuc+dox组)。
30.2.处理方法
31.pbs组和dox组:在第一次注射dox前1周进行,两组均每天进行灌胃pbs 200μl,待第一次dox注射后按照隔天灌胃的方式持续进行并至实验终点为止。
32.amuc组和amuc+dox组:在第一次注射dox前1周进行,每天灌胃amuc 3ug,待第一次dox注射后按照隔天灌胃的方式持续进行并至实验终点为止。
33.待三次注射dox完毕后观察3-4周进行后续实验操作。
34.3.造模方法
35.dox诱导慢性心脏毒性小鼠模型:按照终浓度15mg/kg分三次对小鼠进行尾静脉注射dox,每次5mg/kg,每间隔7天注射一次。建立模型后,密切观察小鼠进食、精神状态及活动反应等。于造模后隔天称量小鼠体重。
36.4.小动物超声
37.分别在dox注射前,及注射后每隔一周的时间,定时监测各组小鼠左室心功能改变,当出现明显的心功能改变时,安乐死小鼠,收集肠管、血液和心脏标本。
38.5.肠道组织和心脏组织病理学检查
39.取回肠远端2cm肠管,迅速予以冷生理盐水冲洗,清除肠内容物后,置于组织固定液中固定24-48小时。经h&e染色后,在光镜下观察肠道组织形态学改变,并进行病理评分。
40.收集小鼠心脏组织,清除腔内外血液后,置于组织固定液中固定24-48小时。经h&e、masson和tunel染色,分析心脏组织结构变化,心肌纤维化程度和心肌细胞凋亡水平的差异。
41.6.血清心肌酶谱和肠道屏障完整性监测
42.使用elisa分析各组小鼠心肌酶谱(ckmb、ctnt、ntpro-bnp)的表达水平,证实各组小鼠心功能存在的差异;分析各组小鼠肠道组织形态,评估肠道屏障改善情况。
43.7.结果
44.7.1生长情况:
45.pbs组:小鼠进食和排便正常,活动情况良好,实验过程中体重增加,未出现死亡;
46.dox组:小鼠在前两针注射dox后的3天内,出现不同程度活动度下降、行动缓慢、身体蜷缩、毛色暗淡竖起、体重明显减轻,3天之后体重逐渐恢复,行动力缓慢恢复;但在第三、四针dox注射后,活动度明显下降,体重维持或下降;
47.amuc组:大鼠进食和排便正常,活动状况良好,实验过程中体重增加,未出现死亡;
48.amuc+dox组:小鼠在注射dox后的3天内,体重轻微下降,之后体重恢复并维持;活动度没有明显下降。
49.7.2心功能改善情况(图1、2):
50.pbs组:小鼠左室心功能在实验阶段正常,心肌酶水平正常,心肌组织没有明显纤维化,心肌细胞没有明显凋亡改变;
51.dox组:小鼠在注射dox三针,累积剂量达到15mg后,心脏左室功能开始下降,血清心肌酶表达显著上升,心肌纤维化加重,心肌细胞凋亡明显;
52.amuc组:小鼠左室心功能在实验阶段正常,心肌酶水平正常,心肌组织没有明显纤维化,心肌细胞没有明显凋亡改变;
53.amuc+dox组:小鼠在注射dox三针,累积剂量达到15mg后,心脏左室功能没有明显下降,血清心肌酶表达与dox组相比显著下降,心肌组织没有明显纤维化,心肌细胞凋亡不显著;
54.7.3肠道屏障改善情况(图1):
55.pbs组:模型终点,小鼠肠道组织形态正常,回肠炎性细胞浸润不明显,绒毛舒展正常,lps和zonulin水平正常;
56.dox组:模型终点,小鼠肠道组织质地较脆,回肠炎性细胞浸润明显,绒毛断裂,lps和zonulin水平显著升高,肠道上皮紧密连接蛋白zo-1,occludin,cludin-1表达显著下降;
57.amuc组:模型终点,小鼠肠道组织形态正常,回肠炎性细胞浸润不明显,绒毛舒展正常,lps和zonulin水平正常;
58.amuc+dox组:模型终点,小鼠肠道组织形态正常,回肠炎性细胞浸润不明显,绒毛舒展正常,lps和zonulin水平恢复正常,显著低于dox组,肠道上皮紧密连接蛋白zo-1,occludin,cludin-1表达显著上升。
59.以上对本发明的具体实施例进行了描述。需要理解的是,本发明并不局限于上述特定实施方式,本领域技术人员可以在权利要求的范围内做出各种变形或修改,这并不影响本发明的实质内容。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1