一种用于治疗类风湿关节炎的生物制剂及其制备方法与流程
1.本发明涉及类风湿关节炎治疗技术领域,具体涉及一种用于治疗类风湿关节炎的生物制剂及其制备方法。
背景技术:
2.类风湿关节炎(ra)是一种慢性、以炎性滑膜炎为主的系统性疾病。其特征是手、足小关节的多关节、对称性、侵袭性关节炎症,经常伴有关节外器官受累及血清类风湿因子阳性,可以导致关节畸形及功能丧失。
3.针对类风湿关节炎治疗手段主要包括药物和手术,其中,用于治疗类风湿关节炎的药物包括布洛芬、非甾体抗炎药、甲氨蝶呤、波尼松等药物,上述药物虽具有一定的抗炎、止痛、改善关节功能的作用,但不可避免的会对机体造成一些副作用,比如,非甾体抗炎药会导致胃肠道不适,激素会导致骨质疏松等问题。
4.外泌体是由细胞分泌到细胞外液中盘状囊泡(30-150nm);多种细胞在正常及病理状态下均可分泌外泌体。其主要来源于细胞内溶酶体微粒内陷形成的多囊泡体,经多囊泡体外膜与细胞膜融合后释放到胞外基质中;研究表明,外泌体涉及多种生物学活性,例如,调节免疫反应,运输蛋白质、rna等。
5.因此,如何提供一种有效治疗类风湿关节炎且无副作用生物制剂尤为关键。
技术实现要素:
6.本发明的目的在于提供一种用于治疗类风湿关节炎的生物制剂及其制备方法,该生物制剂对类风湿关节炎具有显著疗效,且由外泌体复合天然植物成分制得,对人体无任何毒副作用。
7.为了实现本发明的上述目的,特采用以下技术方案:
8.本发明第一方面提供一种用于治疗类风湿关节炎的生物制剂,所述生物制剂由如下原料制得:
9.人脐带间充质干细胞外泌体、藻青蛋白、金银花提取物、海藻酸钠和生理盐水。
10.本发明中藻青蛋白是从蓝绿色藻类提取出的一种深蓝色色素,是自然界中少见的色素蛋白之一,不仅颜色鲜艳,而且本身是一种营养丰富的蛋白质,其氨基酸组成齐全,必需氨基酸含量高;它既是一种蛋白质,又是一种极好的天然食用色素,同时又具有抗氧化、抗肿瘤、调控免疫系统、抗炎特性。
11.本发明采用天然的海藻酸钠为聚合物基质,使得制备得到的生物制剂具有良好的生物相容性,且体内易降解,同时能够响应关节炎处钙离子形成水凝胶,实现外泌体、藻青蛋白、金银花提取物缓慢释放,达到持久治疗的效果;此外,经外泌体、藻青蛋白和金银花提取物联合作用,能够有效改善局部炎症细胞因子水平,促进关节部位血液循环和骨关节损伤修复,达到治疗类风湿关节炎的目的。
12.优选地,所述生物制剂由如下百分含量原料制得:
13.人脐带间充质干细胞外泌体0.1%~0.4%、藻青蛋白1%~5%、金银花提取物0.5%~0.8%和海藻酸钠2%~3%,余量为生理盐水。
14.更优先地,所述生物制剂由如下百分含量原料制得:
15.人脐带间充质干细胞外泌体0.2%、藻青蛋白3%、金银花提取物0.6%和海藻酸钠2.5%,余量为生理盐水。
16.在本发明中,通过对各原料配比的限定,能够更好的调节各原料协同作用,提高生物制剂的整体疗效。
17.优选地,所述人脐带间充质干细胞外泌体通过如下方法制得:
18.将原代脐带间充质干细胞进行传代培养,收集脐带间充质干细胞的第三代培养上清液;再将上清液以(3000~4000)
×
g进行离心去除细胞和细胞碎片;
19.向上清液中添加外泌体沉淀试剂进行充分混匀、静置,再以(10000~50000)
×
g离心20~40min,收集沉淀;
20.采用pbs重悬沉淀后置于纯化柱中,并将纯化柱置于收集管中,将收集管在4℃下以(3000~4000)
×
g进行离心8~12min,将收集管内溶液进行冷冻干燥,得到所述人脐带间充质干细胞外泌体。
21.优选地,所述金银花提取物通过如下方法制得:
22.将金银花粉碎后置于水中进行搅拌提取,连续提取2~3次,合并提取液,再经浓缩、冷冻干燥,得到所述金银花提取物。
23.优选地,所述金银花粉碎后的目粒度不低于50目。
24.优选地,所述搅拌提取温度为50~60℃,提取时间为3~4h。
25.本发明第二方面提供一种上述生物制剂的制备方法,所述制备方法包括如下步骤:
26.(a)将人脐带间充质干细胞外泌体置于生理盐水中并混匀,得到混合液;
27.(b)将金银花提取物和藻青蛋白置于混合液中并搅拌混匀,然后,加入海藻酸钠,震荡混合,即得所述生物制剂。
28.与现有技术相比,本发明的有益效果至少包括:
29.本发明采用天然的海藻酸钠为聚合物基质,使得制备得到的生物制剂具有良好的生物相容性,且体内易降解,同时能够响应关节炎处钙离子形成水凝胶,实现外泌体、藻青蛋白、金银花提取物缓慢释放,达到持久治疗的效果;此外,经外泌体、藻青蛋白和金银花提取物联合作用,能够有效改善局部炎症细胞因子水平,促进关节部位血液循环和骨关节损伤修复,达到治疗类风湿关节炎的目的。
附图说明
30.为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍。在所有附图中,类似的元件或部分一般由类似的附图标记标识。附图中,各元件或部分并不一定按照实际的比例绘制。
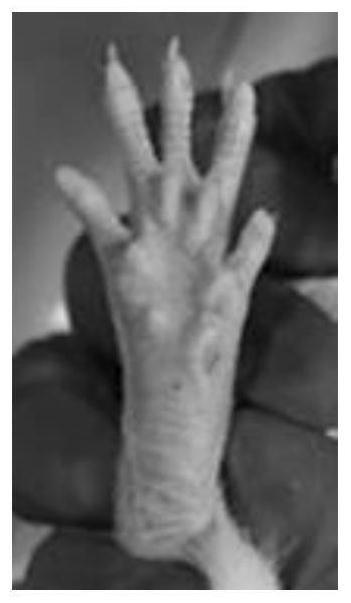
31.图1为本发明实验例中第30天对照组小鼠足趾拍照图;
32.图2为本发明实验例中第30天模型小鼠足趾拍照图;
33.图3为本发明实验例中第30天evs-lj-phy-sa组小鼠足趾拍照图;
34.图4为本发明实验例中第30天evs-lj-sa组小鼠足趾拍照图;
35.图5为本发明实验例中第30天evs-lj-phy组小鼠足趾拍照图;
36.图6为本发明实验例中第30天lj-phy-sa组小鼠足趾拍照图。
具体实施方式
37.下面将结合实施例对本发明技术方案的实施例进行详细的描述。以下实施例仅用于更加清楚地说明本发明的技术方案,因此只作为示例,而不能以此来限制本发明的保护范围。
38.需要注意的是,除非另有说明,本技术使用的技术术语或者科学术语应当为本发明所属领域技术人员所理解的通常意义。
39.本发明实施例提供了一种用于治疗类风湿关节炎的生物制剂,该生物制剂由如下原料制得:
40.人脐带间充质干细胞外泌体、藻青蛋白、金银花提取物、海藻酸钠和生理盐水。
41.本发明采用天然的海藻酸钠为聚合物基质,使得制备得到的生物制剂具有良好的生物相容性,且体内易降解,同时能够响应关节炎处钙离子形成水凝胶,实现外泌体、藻青蛋白、金银花提取物缓慢释放,达到持久治疗的效果;此外,经外泌体、藻青蛋白和金银花提取物联合作用,能够有效改善局部炎症细胞因子水平,促进关节部位血液循环和骨关节损伤修复,达到治疗类风湿关节炎的目的。
42.下面通过具体的实施例进一步说明本发明,但是,应当理解为,这些实施例仅仅是用于更详细地说明之用,而不应理解为用于以任何形式限制本发明。
43.实施例1
44.本实施例为一种人脐带间充质干细胞外泌体制备方法,该制备方法包括如下步骤:
45.1、仪器及耗材、d-mem/f12培养基、胎牛血清、倒置显微镜、超净工作台、co2培养箱、离心机、细胞因子、its和pbs等;
46.2、试剂配置
47.1.d-mem/f12培养基配置:含10%胎牛血清,细胞因子一只,its5ml的d-mem/f12培养基;
48.2、细胞因子:含20ng/ml egf,5ng/ml bfgf;
49.3、实验前的准备
50.5把剪刀,5把止血钳,3把组织镊,3把普通镊子,2个肾形盘,3个50ml烧杯,2个药勺(20cm左右),500ml pbs 121℃高压灭菌30分钟;
51.4、实验操作
52.(1)、超净工作台紫外照射30分钟,擦拭台面;
53.(2)、将灭菌的实验器械放入工作台,点燃酒精灯,拿出一个肾形盘,倒入75%酒精一半,将脐带放进肾形盘中,消毒30秒;
54.(3)、取一个50ml烧杯,倒入一半灭菌的pbs,将脐带放入烧杯中,反复洗3次;
55.(4)、拿出另一个肾形盘,将脐带放入其中,倒入适量pbs,右手拿剪刀,左手拿普通镊子,将脐带剪成2cm左右的小段;
56.(5)、左手拿止血钳,右手拿组织镊,慢慢的将脐带外皮和血管去掉;
57.(6)、将剩余组织放入一个干净的烧杯中,用剪刀剪成大概3mm左右;
58.(7)、用药勺将组织块铺在t75的瓶子里,每瓶100左右组织块,将所有组织块铺完;
59.(8)、在t75瓶子一侧慢慢加入培养基15ml;放入co2培养箱孵育;
60.(9)、48h换液一次,待一星期后观察干细胞爬出情况,若爬出情况较好,将组织块拍掉弃之,加入培养基;
61.(10)、48h后消化细胞,加入1ml胰蛋白酶消化,收集离心(1200转,5分钟),弃上清,加入培养基重悬细胞,根据细胞数量(1
×
106)接种细胞,即为p1代;
62.(11)、48h后消化离心,计数,传代,即为p2代;
63.(12)、两天后消化离心,取上清(检测无菌,支原体,内毒素,)计数细胞,以4.5
×
106冻存;
64.(13)、根据生产需要复苏p2代细胞,传至p3代取上清液;
65.(14)、将上清液以4000
×
g进行离心去除细胞和细胞碎片;
66.(15)、向上清液中添加外泌体沉淀试剂进行充分混匀、静置,再以10000
×
g离心30min,收集沉淀;
67.(16)、采用pbs重悬沉淀后置于纯化柱中,并将纯化柱置于收集管中,将收集管在4℃下以4000
×
g进行离心10min,将收集管内溶液进行冷冻干燥,得到人脐带间充质干细胞外泌体。
68.实施例2
69.本实施例为金银花提取物的制备方法,该制备方法包括如下步骤:
70.将金银花粉碎,过80目筛,收集筛下物,将筛下物置于55℃水中进行搅拌提取4h,连续提取3次,合并提取液,再经浓缩、冷冻干燥,得到上述金银花提取物。
71.实施例3
72.本实施例为一种用于治疗类风湿关节炎的生物制剂,该生物制剂由如下百分含量原料制得:
73.实施例1的人脐带间充质干细胞外泌体0.2%、藻青蛋白3%、实施例2的金银花提取物0.6%和海藻酸钠2.5%,余量为生理盐水。
74.上述用于治疗类风湿关节炎的生物制剂通过如下方法制得:
75.(a)将人脐带间充质干细胞外泌体置于生理盐水中并混匀,得到混合液;
76.(b)将金银花提取物和藻青蛋白置于混合液中并搅拌混匀,然后,加入海藻酸钠,震荡混合,即得上述生物制剂(记为evs-lj-phy-sa)。
77.对比例1
78.本对比例为一种用于治疗类风湿关节炎的生物制剂,该生物制剂与实施例3中的生物制剂基本相同,区别仅在于未添加藻青蛋白。
79.上述用于治疗类风湿关节炎的生物制剂通过如下方法制得:
80.(a)将人脐带间充质干细胞外泌体置于生理盐水中并混匀,得到混合液;
81.(b)将金银花提取物和藻青蛋白置于混合液中并搅拌混匀,即得上述生物制剂(记为evs-lj-sa)。
82.对比例2
83.本对比例为一种用于治疗类风湿关节炎的生物制剂,该生物制剂与实施例3中的生物制剂基本相同,区别仅在于未添加海藻酸钠。
84.上述用于治疗类风湿关节炎的生物制剂通过如下方法制得:
85.(a)将人脐带间充质干细胞外泌体置于生理盐水中并混匀,得到混合液;
86.(b)将金银花提取物置于混合液中并搅拌混匀,然后,加入海藻酸钠,震荡混合,即得上述生物制剂(记为evs-lj-phy)。
87.对比例3
88.本对比例为一种用于治疗类风湿关节炎的生物制剂,该生物制剂与实施例3中的生物制剂基本相同,区别仅在于未添加人脐带间充质干细胞外泌。
89.上述用于治疗类风湿关节炎的生物制剂通过如下方法制得:
90.将金银花提取物和藻青蛋白置于生理盐水中并搅拌混匀,然后,加入海藻酸钠,震荡混合,即得上述生物制剂(记为lj-phy-sa)。
91.实验例
92.本实验例为不同生物制剂对类风湿关节炎影响的研究:
93.实验分组:获取wistar雄性大鼠36只,随机分为6组(每组6只),包括对照组、模型组、evs-lj-phy-sa组、evs-lj-sa组、evs-lj-phy组和lj-phy-sa组;
94.动物造模:将模型组、evs-lj-phy-sa组、evs-lj-sa组、evs-lj-phy组和lj-phy-sa组大鼠进行造模,造模方法如下:
95.在每只大鼠右后足跖皮内注射0.1ml完全弗氏佐剂,正常饲养12天后大鼠出现类风湿关节炎病灶。
96.给药:
97.造模后各组给药情况如下:对照组和模型组注射生理盐水,evs-lj-phy-sa组、evs-lj-sa组、evs-lj-phy组和lj-phy-sa组分别注射evs-lj-phy-sa、evs-lj-sa、evs-lj-phy和lj-phy-sa,注射量为0.02ml/只,注射方式为关节腔注射;两周注射1次;给药周期为45天,在给药第1天、15天、30天测量大鼠右后足的足跖厚度,并计算平均值,其中第30天各组小鼠中典型小鼠足趾图如图1~6所示,图1为对照组,图2为模型组,图3为evs-lj-phy-sa组,图4为evs-lj-sa组,图5为evs-lj-phy组,图6为lj-phy-sa组。
98.结果:不同组足跖厚度平均值计算结果如表1所示:
99.表1
100.101.由表1数据可知:
102.与对照组相比,模型组和实验组第1天的足跖厚度较高,证明造模成功;实验组和模型组相比,均能够有效降低足跖厚度,能够有效缓解炎症导致的肿胀;与evs-lj-phy-sa组相比,evs-lj-sa组、evs-lj-phy组和lj-phy-sa组的足跖厚度较高,证明本技术evs-lj-phy-sa对类风湿关节炎具有最佳的抑制效果,然而,在15天时,evs-lj-phy组抑制效果优于evs-lj-phy-sa组,但其长期9(第30)抑制关节炎效果差于evs-lj-phy-sa组,由此表明,通过海藻酸钠的添加,能够更好的缓慢释放各成分,达到持久抑制炎症的效果。
103.最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围,其均应涵盖在本发明的权利要求和说明书的范围当中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1