CDK7抑制剂与伊马替尼联合在治疗胃肠间质瘤的应用
cdk7抑制剂与伊马替尼联合在治疗胃肠间质瘤的应用
技术领域
1.本发明涉及cdk7抑制剂与伊马替尼联合在治疗胃肠间质瘤的应用,属于生物医药技术领域。
背景技术:
2.胃肠间质瘤(gastrointestinal stromal tumor,gist)作为消化道最常见的间叶来源肿瘤之一,其发病率占胃肠恶性肿瘤的1-3%,具有间质干细胞多向分化的潜能,被认为是消化道潜在的恶性肿瘤。gist可发生于消化道的任何地方,其中以胃及小肠居多,分别占60%-70%及20%-30%,也可生长于结肠,直肠,食管,腹腔等部位。目前,保证瘤体完整的r0手术切除是治愈gist的唯一方法。对于已发生复发转移或其他情况而无法手术的患者,因gist对放疗与化疗均不敏感,晚期gist预后不容乐观。c-kit(v-kit hardy-zuckerman 4feline sarcoma viral oncogene homolog)或血小板衍生生长因子受体(platelet-derived growth factor receptor a,pdgfra)的激活突变存在于85%的gist中。甲磺酸伊马替尼(imatinib mesylate,im)作为一种选择性的酪氨酸激酶受体抑制剂(tyrosine kinase inhibitors,tki)通过竞争性抑制atp结合从而对bcr-abl,kit和pdgfr活性产生抑制作用,进而抑制细胞的增殖。2001年h joensuu等首次将im用于治疗不可切除的晚期gist,取得显著疗效。im对于治疗胃肠gist的疗效及安全性被发掘,并迅速成为晚期gist患者的首选治疗方式,大大改善了晚期gist患者的预后。虽然im对于gist有疗效显著,但超过50%的晚期患者在口服im治疗的2年左右发生继发耐药,导致疾病的进展。为解决gist继发耐药问题,研发出各种新型多靶点tki,包括了二线用药舒尼替尼(sunitinib)及三线用药瑞戈非尼(regorafenib),但仅能延长患者无进展生存率(progression-free survival,pfs)约4-5月。最新的四线用药瑞派替尼(ripretinib)虽然能延长pfs至6.3个月,但伴随着较多不良反应,包括脱发、乏力、恶心、腹痛等,这些相对严重的不良反应也限制其疗效。因此,寻找新型治疗gist的手段迫在眉睫。
3.细胞周期是细胞增殖的基本过程,其调控细胞从静止期转向细胞分裂增殖期,而细胞周期失控是恶性肿瘤发生进展的重要原因之一。周期蛋白依赖性激酶(cyclin-dependent kinases,cdk)属于丝氨酸/苏氨酸激酶家族成员之一,为细胞周期调控机制中的核心分子。目前有多项研究表明在多种恶性肿瘤中cdk7表达显著增高,且其与肿瘤恶性分期和不良预后显著相关,如乳腺癌、胰腺癌、膀胱癌等。研究表明cdk7调控多种恶性肿瘤的原癌基因的转录表达。thz1为人工合成的cdk7抑制剂,其特异性抑制cdk7的激酶活性。同样,在多项不同肿瘤研究发现,thz1可显著抑制肿瘤细胞活性,并抑制相关致病基因的表达,但是在胃肠间质瘤中尚未见报道。
技术实现要素:
4.本发明要解决的技术问题之一是如何获得一种有效治疗胃肠间质瘤的技术方案的技术问题。
5.为达到解决上述问题的目的,本发明所采取的技术方案是提供一种cdk7抑制剂联合伊马替尼在制备治疗胃肠间质瘤药物中的应用。
6.优选地,所述cdk7抑制剂为thz1。
7.优选地,所述cdk7抑制剂联合伊马替尼用于抑制胃肠间质瘤细胞的增殖,并诱导其凋亡。
8.优选地,所述胃肠间质瘤细胞为gist-t1和gist-882细胞。
9.优选地,所述制备治疗胃肠间质瘤药物的剂型包括片剂、粉剂、颗粒剂、胶囊、口服液、针剂或缓释剂。
10.相比现有技术,本发明具有如下有益效果:
11.本发明提供了一种cdk7抑制剂thz1与伊马替尼联合在制备治疗胃肠间质瘤药物中的应用;thz1联合伊马替尼治疗是治疗胃肠间质瘤的更有效方法。
附图说明
12.图1为不同浓度梯度的thz1和伊马替尼联合处理胃肠间质瘤细胞t1和882的细胞增殖活性热图;
13.图2为thz1和伊马替尼联合应用显著抑制细胞增殖活性图;
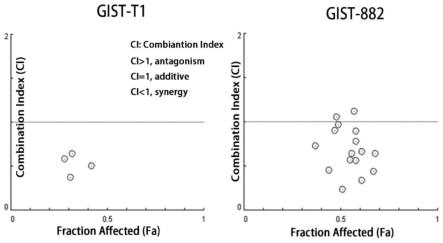
14.图3为应用compusyn软件定量计算药物组合指数(combination index,ci),评估thz1和伊马替尼对胃肠间质瘤细胞的作用效应。
15.图4为thz1和伊马替尼联用可显著促进细胞凋亡图;
16.图5为thz1与伊马替尼处理后western blot实验结果图;
17.图6为thz1与伊马替尼联合用药显著抑制裸鼠gist肿瘤的生长结果图;
18.图7为各治疗组间小鼠体重变化图;
具体实施方式
19.为使本发明更明显易懂,兹以优选实施例作详细说明如下:
20.本发明提供了一种cdk7抑制剂联合伊马替尼在制备治疗胃肠间质瘤药物中的应用。
21.应用中,cdk7抑制剂为thz1。
22.应用中,cdk7抑制剂联合伊马替尼用于抑制胃肠间质瘤细胞的增殖,并诱导其凋亡。
23.应用中的胃肠间质瘤细胞为gist-t1和gist-882细胞。
24.应用中制备治疗胃肠间质瘤药物的剂型包括片剂、粉剂、颗粒剂、胶囊、口服液、针剂或缓释剂等。
25.实施例
26.1.thz1和伊马替尼联合处理胃肠间质瘤细胞,绘制增殖热图;
27.将处于对数生长期的gist-t1和gist-882细胞消化离心重悬后,使用细胞计数仪计数,按每孔5000个细胞加入96孔板中,补充培养基至100ul,放置于恒温培养箱中过夜。对照组为含0.01%浓度dmso的培养基。thz1用dmso溶解,将伊马替尼用pbs溶解,按0.01,0.02,0.05,0.1umol/l的各种不同浓度组合配置成工作液。吸去旧培养基,按浓度梯度,每
孔加入150ul等量工作液或对照培养基。置于恒温培养箱中培养72h。吸去旧培养基,每孔中分别加入培养基及cck-8试剂(cell counting kit-8细胞计数试剂)100ul和10ul。避光置于恒温培养箱中避光孵育2小时。于450nm波长下检测吸光度。按细胞活性=(n浓度下吸光度-空白孔吸光度)/(对照dmso吸光-空白孔吸光度)公式计算药物浓度梯度作用后的细胞活性。thz1和伊马替尼联合用药抑制gist-t1和gist-882细胞增殖活性热图。每一小格对应一种药物浓度组合,颜色指示细胞增殖活性大小。随着thz1和伊马替尼组合浓度越高,gist-t1和gist-882细胞增殖活性显著受到抑制(如图1所示)。
28.结论:
29.利用不同浓度梯度的thz1和伊马替尼联合处理胃肠间质瘤细胞gist-t1和gist-882,利用cck8技术检测药物处理后的细胞活性,并绘制增殖活性热图,发现随着thz1和伊马替尼组合浓度越高,gist-t1和gist-882细胞增殖活性显著受到抑制(如图1)。
30.2.thz1和伊马替尼联合应用显著抑制细胞增殖活性,且效果显著优于单独用药;
31.20nmol/l thz1和20nmol/l伊马替尼作用于gist-t1细胞,单独用药应用均抑制细胞增殖活性,且联合应用抑制效果显著高于单独用药。50nom/l thz1和50nmol/l伊马替尼作用于gist-882细胞,单独用药均抑制细胞增殖活性,且联合应用抑制效果显著高于单独用药的应用(如图2所示)。
32.结论:
33.用thz1、伊马替尼单独与联合用药,发现thz1和伊马替尼均可抑制细胞活性,且两药联用治疗组的gist细胞抑制最为显著,抑制效果显著大于单药治疗(如图2)
34.3.联合指数(ci)计算表明,thz1与伊马替尼发挥协同作用
35.chou-talalay法检验,并应用compusyn软件定量计算药物组合指数(combination index,ci)评估thz1和伊马替尼对胃肠间质瘤细胞的作用效应。其中ci》1为拮抗效应,ci=1为无相互作用关系,ci《1为协同效应。通过compusyn软件计算ci值表明,thz1和伊马替尼作用于gist-t1 ci值均小于1,而gist-882细胞除个别值外均小于1,提示thz1和伊马替尼发挥协同抑制作用(如图3所示)。
36.结论:
37.thz1和伊马替尼作用于gist-t1和gist-882细胞后,通过compusyn软件计算联合指数(combination index,ci)均小于1,表明两者可发挥协同抑制作用(如图3所示)。
38.4.thz1和伊马替尼联用可显著促进细胞凋亡;
39.取处于对数生长期的gist-t1和gist-882细胞消化离心重悬后,使用细胞计数仪计数,按50%密度铺入6孔板中,补充培养基至2ml,放置于恒温培养箱中过夜。thz1用dmso溶解,伊马替尼用pbs溶解。gist-t1细胞加入并补足培养基至2ml,使thz1和伊马替尼浓度分别均为50nmol/l,联合用药组为50nmol/l thz1+50nmol/l伊马替尼。gist-882细胞加入并补足培养基至2ml,使thz1和伊马替尼浓度均为100nmol/l,联合用药组为100nmol/l thz1+100nmol/l伊马替尼。转移至恒温培养箱培养72h。thz1和伊马替尼联合应用后显著促进gist-t1和gist-882细胞凋亡,并且联合应用后凋亡细胞比例显著大于单药应用(p《0.05,如图4所示)。
40.结论:
41.thz1和伊马替尼联合作用于gist-t1和gist-882细胞,显著促使细胞凋亡,凋亡细
胞比例显著大于单药应用(如图4)。
42.5.western blot实验表明,thz1与伊马替尼处理后凋亡蛋白显著上升;
43.thz1和伊马替尼单独用药作用于gist-t1和gist-882细胞后,cleaved-parp和cleaved-caspase3蛋白表达显著升高,并且联合应用后,蛋白表达升高比单药应用更为显著(如图5所示)。
44.结论:
45.thz1和伊马替尼共同作用于gist-t1和gist-882细胞,促使cleaved-parp和cleaved-caspase3细胞蛋白表达升高,并且联合应用效果显著高于单药作用(如图5)
46.6.thz1与伊马替尼联合用药显著抑制裸鼠gist肿瘤的生长;
47.取处于对数生长期的gist-t1细胞,细胞密度为80-90%左右。胰酶消化细胞后用预冷的pbs洗两遍,用pbs重悬至密度为(3
×
106/100ul),并用等量bd martrigel基质胶(1:1)混合,皮下注射于裸鼠背部平坦处,剂量为100ul。待肿瘤细胞成瘤肉眼可见时,将裸鼠随机分为对照组、thz1处理组、伊马替尼处理组、thz1和伊马替尼联合处理组共4组(n=6)。thz1用pbs溶解,thz1组每2天腹腔注射10mg/kg浓度的thz1溶液,伊马替尼组每日腹腔注射50mg/kg,联合用药组两种药物均腹腔注射,连续用药一周。连续观察20天,每3日测量小鼠体重,肿瘤体积。小鼠对照组的小鼠皮下肿瘤体积随时间逐渐增大,联合用药药物处理组的小鼠皮下肿瘤最终体积及重量显著小于对照pbs注射组小鼠(p《0.05,如图6所示)。裸鼠体内,各治疗组之间体重水平相当,提示裸鼠对thz1和伊马替尼耐受可;各治疗组间小鼠体重变化无显著性差异(p》0.05,如图7),提示裸鼠对thz1联合伊马替尼治疗的耐受度可,10mg/kg的量对于裸鼠属于安全剂量。
48.结论:
49.利用裸鼠gist荷瘤模型,分别给予thz1、伊马替尼以及二者联合用药处理,与体外实验类似,thz1与伊马替尼联合用药更能发挥抑制肿瘤的效果(如图6)。而且各治疗组之间体重无明显差异,提示裸鼠对thz1以及两药联用耐受可(如图7)。
50.本发明在细胞水平:通过药物实验,初步确定了thz1和伊马替尼联合对于gist-t1细胞较佳的处理浓度均为20nm,对于gist-882细胞的处理浓度分别为50nm。
51.在动物水平:通过裸鼠gist荷瘤实验,造模两周后连续1周每2天予10mg/kg的thz1和每日50mg/kg伊马替尼联合处理可使gist肿瘤生长受到显著抑制。
52.本发明通过体外细胞实验,表明thz1与伊马替尼联合处理能显著降低细胞增殖活性,诱导细胞凋亡,且二者联用可发挥协同抑制作用,治疗效果大于单一用药;在裸鼠gist荷瘤模型中,再次证明thz1与伊马替尼联合治疗可以带来最佳的治疗效果,并且裸鼠对联合治疗耐受可,说明thz1联合伊马替尼治疗是治疗胃肠间质瘤的更有效方法。
53.以上所述,仅为本发明的较佳实施例,并非对本发明任何形式上和实质上的限制,应当指出,对于本技术领域的普通技术人员,在不脱离本发明的前提下,还将可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。凡熟悉本专业的技术人员,在不脱离本发明的精神和范围的情况下,当可利用以上所揭示的技术内容而做出的些许更动、修饰与演变的等同变化,均为本发明的等效实施例;同时,凡依据本发明的实质技术对上述实施例所作的任何等同变化的更动、修饰与演变,均仍属于本发明的技术方案的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1