血府逐瘀制剂在制备防治卒中后痛觉异常的药物中的应用的制作方法
血府逐瘀制剂在制备防治卒中后痛觉异常的药物中的应用
1.本技术要求2021年07月22日提交的中国专利申请202110829428.7的优先权,在此通过参考将其全部内容并入本文。
技术领域
2.本发明属于制药技术领域,特别是涉及血府逐瘀制剂在制备防治卒中后痛觉异常的药物中的应用。
背景技术:
3.慢性疼痛是脑卒中后遗留的常见症状,包括头痛、肩痛、肢体痛、卒中后丘脑痛(cpsp)等。不同的疼痛症状其发病机制也所有不同:头痛主要发生于颅内痛敏组织,例如脑卒中引起颅内压增高可导致颅内血管受牵拉或位移而产生血管性头痛,血液流至蛛网膜下腔后血浆中的游离肽和血小板破坏后释放出的5-羟色胺可刺激颅内小血管收缩或痉挛而产生刺激性疼痛,脑出血早期脑脊液中的红细胞或胆红素可刺激神经根,引起颈部肌肉收缩,进而挤压肌肉神经导致头疼。由于出血性卒中与缺血性卒中的发病机制不同,故二者所致头痛的发病机制也有差别,且脑出血引起头痛的发生率高于脑缺血。卒中后肩痛的大多由于卒中期间长时间不活动导致关节韧带松弛、肩关节半脱位、肌张力异常、神经损伤等。肢体痛的起因一般包括血液循环障碍、运动不足所致的关节囊、韧带、肌肉、肌腱等挛缩,肌肉粘连,不正确的牵拉引起的扭伤、关节脱位等。
4.卒中后丘脑痛不同于上述头痛、肩痛、肢体痛,是一种与卒中病灶直接相关的神经病理性疼痛,疼痛范围较大,涉及卒中累及的躯干(偏身或偏侧肢体)或肢体同侧的感觉障碍区域,以远端(如手部、足部)多见。大多数患者在疼痛区域感觉减退,同时痛觉超敏、感觉倒错,可出现针刺样、烧灼样、刀割样疼痛等痛觉异常敏感的情况,严重影响了患者的生活质量。由于卒中后丘脑痛与其他疼痛的病因不同,并不是致痛因素引发,而是感觉倒退、痛觉超敏、感觉倒错所致,故常用于头痛、肩痛、肢体痛的镇痛剂,例如非甾体抗炎药、局部麻醉剂等对于卒中后丘脑痛的临床治疗效果并不理想,一般不作为临床推荐药物。
技术实现要素:
5.针对以上技术问题,本发明提供了一种血府逐瘀制剂在制备防治卒中后痛觉异常的药物中的应用。
6.为达到上述发明目的,本发明实施例采用了如下技术方案:
7.一种血府逐瘀制剂在制备防治卒中后痛觉异常的药物中的应用,所述脑损伤痛觉异常为卒中后脑出血或缺血导致的脑损伤痛觉异常;所述血府逐瘀制剂包括以下重量份数的原料:柴胡24~30份、当归75~85份、地黄72~88份、赤芍50~56份、红花75~86份、炒桃仁100~110份、麸炒枳壳50~56份、甘草24~30份、川芎32~45份、牛膝75~83份、桔梗45~55份。
8.本发明通过研究发现,血府逐瘀制剂对于大鼠脑卒中后痛觉异常具有潜在的治疗
作用,有望用于制备防治卒中后痛觉异常的药物,特别是防治卒中后丘脑痛的药物。
9.优选的,本发明的上述应用,所述血府逐瘀制剂的用量或者用药浓度为0.43~2.16g/kg/d,即血府逐瘀药物制剂的用量为0.43~2.16g克/kg/天,相当于临床1~5倍的等效剂量。有关血府逐瘀制剂的制备方法可参考天津宏仁堂药业有限公司专利号为cn100422737c、cn100560103c、cn101647895b、cn103356796b、cn1320904c中公开的制备方法。
10.优选的,本发明的上述应用,所述血府逐瘀制剂包括药学上可接受的载体。
11.优选的,本发明的上述应用,所述载体优选自常用的药用辅料或者生理盐水或者蒸馏水。
12.进一步地,所述药学上可接受的辅料为:填充剂、崩解剂、润滑剂、助悬剂、黏合剂、甜味剂、矫味剂、防腐剂、基质等。填充剂包括:淀粉、预胶化淀粉、乳糖、甘露醇、甲壳素、微晶纤维素、蔗糖等;崩解剂包括:淀粉、预胶化淀粉、微晶纤维素、羧甲基淀粉钠、交联聚乙烯吡咯烷酮、低取代枪兵纤维素、交联羧甲基纤维素钠等;润滑剂包括:硬脂酸镁、十二烷基硫酸钠、滑石粉、二氧化硅等;助悬剂包括:聚乙烯吡咯烷酮、味精纤维素、蔗糖、琼脂、羟丙基甲基纤维素等;黏合剂包括:淀粉浆、聚乙烯吡咯烷酮、羟丙基甲基纤维素等;甜味剂包括:糖精钠、阿斯帕坦、蔗糖、甜蜜素、甘草次酸等;矫味剂包括:甜味剂及各种香精;防腐剂包括:尼泊金甲酯或乙酯苯甲酸、苯甲酸钠、山梨酸及其盐类、苯扎溴铵、醋酸氯己定、桉叶油等;基质包括:peg6000、peg4000、虫蜡等。
13.进一步地,本发明的上述应用,所述药物为血府逐瘀制剂按照常规工艺加入常规辅料制成临床上可接受的片剂、胶囊剂、散剂、合剂、汤剂、丸剂、颗粒剂、糖浆剂。
14.可选地,当制成胶囊剂时,制备方法为:按重量份数取各原料,用水提取后收集水提液,浓缩后加入乙醇至含醇量为65%~75%v/v,静置沉淀后取上清液浓缩,制成浸膏;向所述浸膏中加入填充剂,干燥,再加入助流剂,整理,灌装胶囊,即得。
15.其中用水提取的次数可选1~3次,优选采用2次;每次用水量优选为原料总质量的7~9倍,每次提取0.5~1.5h;填充剂、助流剂可选硬质胶囊剂常用辅料,例如填充剂可选淀粉、微晶纤维素等,助流剂可选二氧化硅、硬脂酸镁、滑石粉等。
16.所述防治卒中后痛觉异常的药物还可制成外用制剂,如软膏剂、硬膏剂、巴布剂。
17.优选地,所述卒中后痛觉异常为卒中后丘脑痛。
18.优选地,所述卒中后痛觉异常为缺血性卒中后痛觉异常。
19.优选地,所述卒中后痛觉异常为缺血性卒中后丘脑痛。
20.优选地,所述防治卒中后痛觉异常的药物为提高脑内bdnf表达水平的药物。
21.优选地,所述防治卒中后痛觉异常的药物为减少炎症因子的药物。所述炎症因子包括tnf-α。
22.优选地,所述防治卒中后痛觉异常的药物为减轻丘脑继发损伤的药物。
23.与现有技术相比,本发明具有以下优点:
24.本发明通过研究发现,血府逐瘀制剂干预对卒中后脑损伤导致的痛觉异常的热痛阈值降低现象具有一定的改善作用,可以作为制备卒中后脑损伤导致的痛觉异常的药物。经进一步试验验证发现,本发明实验研究中涉及的卒中后导致的痛觉异常为卒中后丘脑痛的临床表现,故血府逐瘀制剂可作为制备用于卒中后丘脑痛的药物,特别是用于缺血性卒
中后丘脑痛的药物。本发明经试验验证还发现,血府逐瘀制剂能够升高脑内bdnf表达水平、降低炎症因子水平、减轻丘脑的继发损伤,因此血府逐瘀制剂还可作为制备提高脑内bdnf表达水平、减少炎症因子、减轻丘脑继发损伤的药物,在临床应用中可根据具体的治疗方案和药物作用机理来开展联合用药。
附图说明
25.图1为本发明实施例1复制大鼠mcao模型前各试验组的痛阈值测试结果图。
26.图2为本发明实施例1的mcao模型大鼠痛觉异常敏感的筛选结果图。
27.图3为本发明实施例1血府逐瘀制剂对脑卒中后痛觉异常大鼠约1周后热痛阈值测试的结果图。
28.图4为本发明实施例1血府逐瘀制剂对脑卒中后痛觉异常大鼠约2周后热痛阈值测试的结果图。
29.图5为本发明实施例1血府逐瘀制剂对脑卒中后痛觉异常大鼠约3周后热痛阈值测试的结果图。
30.图6为本发明实施例1假手术组大鼠在术后3、7、14、21天的热痛阈值测试的结果图。
31.图7为本发明实施例1模型组大鼠在术后3、7、14、21天的热痛阈值测试结果图。
32.图8为本发明实施例1zfxy低剂量组大鼠在术后3、7、14、21天的热痛阈值测试结果图。
33.图9为本发明实施例1zfxy高剂量组大鼠在术后3、7、14、21天的热痛阈值测试结果图。
34.图10为本发明实施例2复制大鼠mcao模型前各试验组的痛阈值测试结果图(以大鼠舔后足为观察指标)。
35.图11为本发明实施例2复制大鼠mcao模型前各试验组的痛阈值测试结果图(大鼠舔右足次数与舔后足次数的比例)。
36.图12为本发明实施例2的mcao模型大鼠痛觉异常敏感的筛选结果图(以大鼠舔后足为观察指标)。
37.图13为本发明实施例2的mcao模型大鼠痛觉异常敏感的筛选结果图(大鼠舔右足次数与舔后足次数的比例)。
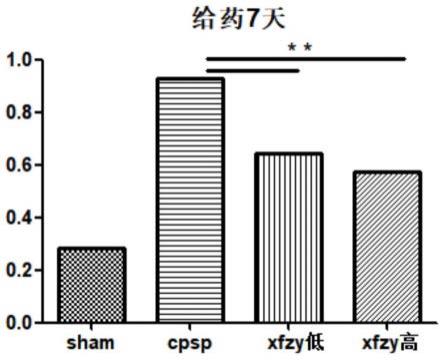
38.图14为本发明实施例2给药1周后热痛阈值测试的结果图(以大鼠舔后足为观察指标)。
39.图15为本发明实施例2给药1周后热痛阈值测试的结果图(大鼠舔右足次数与舔后足次数的比例)。
40.图16为本发明实施例2给药2周后热痛阈值测试的结果图(以大鼠舔后足为观察指标)。
41.图17为本发明实施例2给药2周后热痛阈值测试的结果图(大鼠舔右足次数与舔后足次数的比例)。
42.图18为本发明实施例2给药3周后热痛阈值测试的结果图(以大鼠舔后足为观察指标)。
43.图19为本发明实施例2给药3周后热痛阈值测试的结果图(大鼠舔右足次数与舔后足次数的比例)。
44.图20为本发明实施例2给药4周后热痛阈值测试的结果图(以大鼠舔后足为观察指标)。
45.图21为本发明实施例2给药4周后热痛阈值测试的结果图(大鼠舔右足次数与舔后足次数的比例)。
46.图22为本发明实施例3中各组大鼠血清中的tnf-α含量。
47.图23为本发明实施例4中各组大鼠丘脑的bdnf表达水平。
48.图24为本发明实施例5中各组大鼠丘脑组织尼氏染色切片。
具体实施方式
49.下面结合附图和实验例,对本发明的技术方案进行清楚、完整的描述,显然,所描述的实施例仅是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明的保护范围。
50.以下实施例中所采用的原料、试剂等,如无特殊说明,均从商业途径获得。
51.实施例1
52.本实施例提供一种血府逐瘀制剂在制备卒中后脑损伤痛觉异常药物中的应用,下面通过具体的实验例来证明本发明的技术方案。
53.1、实验材料
54.1.1实验动物
55.270-300g的wistar雄性大鼠多只,购于北京维通利华实验动物技术有限公司,许可证号:scxk(京)2016-0006。饲养于中国医学科学院放射医学研究所spf级屏障室,饲养室温度为21
±
2℃,气压恒定,昼夜12小时交替。
56.1.2药物配制
57.本实验例采用天津宏仁堂药业有限公司生产的血府逐瘀胶囊,该血府逐瘀胶囊每粒含生药0.4g,成人每次服用6粒,每日服两次,每日服药量4.8g,按正常成人体重50kg来计算,参考徐叔云教授主编的《药理实验方法学》,大鼠临床等效剂量是0.43g/kg/d,根据文献1(血府逐瘀胶囊对自发性高血压大鼠心肌肥厚的作用及机制研究[d].中国中医科学院,2012),选用5倍临床等效剂量2.16g/kg/d为给药剂量。精密称取血府逐瘀胶囊内药粉适量,加少量纯净水调匀后稀释,超声波助溶,4℃保存,供大鼠灌胃给药用,每天现用现配。术后7天开始灌胃给药。
[0058]
2、实验方法
[0059]
2.1痛觉异常模型的建立
[0060]
卒中后丘脑痛大鼠模型的建立分为两个部分。
[0061]
2.1.1脑卒中模型的建立
[0062]
采用大脑中动脉闭塞(mcao)的方法,沿右侧颈内动脉插入线栓并向前推进,直至大脑中动脉起始部被阻断,造成脑卒中模型,假手术组仅分离颈总动脉。阻断大脑供血时间为60min,60min后缓慢拔除线栓,恢复供血。
[0063]
2.1.2脑卒中后痛觉异常的筛选
[0064]
术前一天测定大鼠热痛阈值,将大鼠置于热板仪上,以大鼠舔后足为指标,筛选出热痛阈值在5-30s内的大鼠用于后续实验。文献中脑卒中1周后,大鼠会出现对侧后肢的热刺激和机械刺激的敏感上升,但经过前期预实验,术后三天大鼠即可出现对侧后肢热痛阈的降低,故术后3天,对造模大鼠进行热痛阈测试,以术前1天测量值为参考值,在模型组中挑选出发生痛觉异常的大鼠,随机分为模型组与给药组。
[0065]
2.2实验分组及给药种类和用量
[0066]
术后3天通过对mcao大鼠的热痛阈进行测试后,筛选出发生痛觉异常的实验大鼠22只进行分组给药(给药第一天,由于灌胃原因死亡大鼠1只,故每组均为7只大鼠),随机分为3组:模型组,血府逐瘀胶囊低剂量给药组与血府逐瘀胶囊高剂量给药组,每组7只,每天灌胃给药1次,连续给药21天。假手术组10只。实验分组、用药量及方法如下表1所示:
[0067]
表1:实验分组及给药数据表
[0068]
组别n给药种类及用量假手术组(sham)10灌胃等体积蒸馏水模型组(cpsp)7灌胃等体积蒸馏水低剂量给药组(xfzy低)70.43g/kg/d(临床等效剂量)高剂量给药组(xfzy高)72.16g/kg/d(5倍临床等效剂量)
[0069]
2.3热痛阈测定
[0070]
术前1天、术后3天,给药后7天,14天,21天,测定大鼠热痛阈值。
[0071]
热板法:为了避免后足基线温度的差异,先将大鼠置于37℃的热板仪上进行2分钟的适应期。然后将大鼠置于50℃的热板仪上,以60秒为上限值,以舔后足为观察指标,测试完毕,将大鼠放回笼中,间隔至少15分钟后重复测试,重复三次,取其平均值。
[0072]
2.4统计学方法
[0073]
采用graphpad prism 5.0软件进行统计学分析,计量数据以均数
±
标准差表示,大鼠热痛阈的比较选用单因素方差分析,p<0.05表明差异具有显著性。
[0074]
3、实验结果
[0075]
3.1模型筛选结果
[0076]
复制大鼠mcao模型,在复制模型前后利用热板法对实验动物进行筛选,筛选结果如附图1所示,复制模型前实验各组痛阈值无显著差异(p>0.05)。复制大鼠mcao后3天利用热板法对痛觉敏感大鼠进行筛选,筛选出其中发生痛觉敏感的大鼠68只。测定68只mcao大鼠的热痛阈值,结果显示其中22只存在痛觉敏感情况,发病率32.35%。测定结果如附图2所示,从中可以得出:术后三天出现痛觉异常的大鼠与sham组相比,其他各组热痛阈值均下降。相比假手术组10~20s的热痛阈值,模型组的热痛阈值下降为7~10s,血府逐瘀胶囊低剂量组和血府逐瘀胶囊高剂量组的热痛阈值下降为8~11s,热痛阈值显著降低(p<0.05),提示脑缺血导致了实验大鼠痛觉异常,但给药各组之间均无统计学差异(p<0.05)。其中术前热板仪温度为55℃,术后3天由于仪器问题,热板仪温度仅能达到50℃,故术后加假手术组热痛阈较术前升高,且给药后每周测定热板仪温度均为50℃。
[0077]
3.2血府逐瘀胶囊对卒中后脑损伤痛觉异常大鼠热痛阈的影响
[0078]
对痛觉异常大鼠进行筛选后开始灌胃给予血府逐瘀胶囊进行干预,给药1周后,如
附图3所示,与假手术组比较,模型组的热痛阈值显著降低(p<0.05),提示脑缺血导致了实验大鼠痛觉异常。
[0079]
但模型组与假手术组之间的差异仍存在(p<0.05),提示mcao引起的痛觉异常现象并不会自愈,除此之外,各组均无统计学差异(p>0.05)。通过对低剂量的自身对照,低剂量给药组在给药1周后,热痛阈值升高(p<0.05),症状改善。
[0080]
给药2周后,如附图4所示,zfxy低剂量组的大鼠的热痛阈值相比术后三天以及给药一周后的热痛阈值逐渐增大,热痛阈值由术后三天的7~10s恢复到用药一周后的8~16s,再到用药两周后的8~15s,证明zfxy低剂量组大鼠的热痛阈值在逐渐恢复,大鼠的疼痛敏感性降低。
[0081]
与假手术组比较,模型组热痛阈值显著降低(p<0.05),提示脑缺血导致的实验大鼠痛觉异常无自行恢复现象;与模型组比较,血府逐瘀胶囊干预组热痛阈值显著升高(p<0.05)。仅zfxy高剂量组与模型组之间存在统计学差异,但zfxy高剂量组数据标准差过大,数据存在差异,证明xfzy高剂量组药效不稳定。
[0082]
给药3周后,如附图5所示,假手术组和血府逐瘀低剂量组均与模型组出现统计学差异(p<0.05),表明通过给药使脑卒中后出现痛觉异常的实验大鼠的热痛阈值逐渐恢复到正常水平,可以作为药物存在药效的证据,提示血府逐瘀胶囊对mcao引起的缺血性脑卒中后热痛阈值降低具有一定改善作用。
[0083]
下面通过对各组大鼠术前以及术后给药热痛阈值的变化进行数据对比:
[0084]
如附图6所示,假手术组大鼠的热痛阈值在术后3-21天内除个别极值外基本没有变化。
[0085]
如附图7所示,模型组大鼠的热痛阈值在术后3-21天热痛阈值相较假手术组降低,但组内整体未发生较大变化,排除极值点外,热痛阈值始终在7~11s范围内。
[0086]
如附图8所示,zfxy低剂量组在给药1周后,热痛阈值升高(p<0.05),说明热痛阈值在恢复,大鼠的疼痛敏感性在降低,在给药2-3周时段内,热痛阈值基本维持在这一范围内。
[0087]
如附图9所示,zfxy高剂量组在给药三周后,热痛阈值未出现明显变化,仍在7~18s范围内。
[0088]
以上实验过程证明:通过mcao的方法制造的缺血性脑卒中模型可以引起实验大鼠痛觉异常,发生率约为30%,血府逐瘀胶囊干预对卒中后脑损伤导致的痛觉异常大鼠的热痛阈降低现象具有改善作用,可以将脑卒中后痛觉异常的大鼠热痛阈将6~10s恢复至10~20s,说明血府逐瘀制剂能够降低疼痛的敏感性,缓解给患者带来的疼痛感,使痛觉感知恢复正常,即血府逐瘀制剂可以作为制备卒中后脑损伤痛觉异常的药物,以应用在制备治疗卒中后脑损伤痛觉异常的药物中。
[0089]
本发明还研究了血府逐瘀制剂干预复制大鼠局灶性脑缺血损伤模型和利用丘脑注射内皮素直接诱导丘脑缺血模型,并分别采用热板法考察实验动物对热刺激疼痛的反应情况,实验结果证明:血府逐瘀制剂对两种模型的热刺激疼痛反应,均能够降低疼痛的敏感性,缓解疼痛感,使患者的痛觉感知恢复正常。
[0090]
本发明的研究发现,血府逐瘀制剂干预对脑卒中后痛觉异常的热痛阈值降低现象具有改善作用,可以作为潜在的制备卒中后脑损伤痛觉异常的药物,以治疗或减缓脑损伤
患者的痛觉异常。
[0091]
实施例2
[0092]
本发明在前期实验中发现线栓法复制的大鼠脑卒中模型可导致大鼠出现热痛阈降低的现象,而右侧肢体尤为明显,在同样的热刺激下,大鼠舔右足的比例显著高于左侧。故本实施例结合热板法以及大鼠对右侧肢体的反应,考察了血府逐瘀制剂防治缺血性卒中后丘脑痛的应用效果。
[0093]
1、实验材料
[0094]
1.1实验动物
[0095]
270-300g的wistar雄性大鼠,购于北京维通利华实验动物技术有限公司,许可证号:scxk(京)2016-0006。饲养于中国医学科学院放射医学研究所spf级屏障室,饲养室温度为21
±
2℃,气压恒定,昼夜12小时交替。
[0096]
1.2药物配制
[0097]
按以下重量份数称取各味中药:柴胡27份、当归80份、地黄80份、赤芍54份、红花80份、炒桃仁105份、麸炒枳壳54份、甘草27份、川芎38份、牛膝80份、桔梗50份。将上述中药用水提取2次,每次用水量为原料总质量的8倍,每次提取时间1h,滤过,收集滤液,减压浓缩至60℃的相对密度为1.16-1.19,待冷放置室温,加入乙醇使含醇量为70%v/v,搅匀,静置使沉淀,取上清液减压浓缩至60℃的相对密度为1.35-1.43,加入浸膏量15%w/w的淀粉,于70~75℃的干燥箱中干燥9h,得干燥物,向所述干燥物中加入所述干燥物重量6%的二氧化硅,粉碎过40目筛,装入胶囊,制成1000粒。每粒胶囊相当于生药0.4g。
[0098]
按成人每次服用6粒,每日服两次,每日服药量4.8g,正常成人体重50kg来计算,参考徐叔云教授主编的《药理实验方法学》,大鼠临床等效剂量是0.43g/kg/d,选用2倍临床等效剂量0.86g/kg/d为高剂量给药剂量。精密称取血府逐瘀胶囊内药粉适量,加少量纯净水调匀后稀释,超声波助溶,4℃保存,供大鼠灌胃给药用,每天现用现配。术后7天开始灌胃给药。
[0099]
2、实验方法
[0100]
2.1痛觉异常模型的建立:同实施例1。
[0101]
2.2实验分组及给药种类和用量
[0102]
术后3天通过对mcao大鼠的热痛阈进行测试后,筛选出发生痛觉异常的实验大鼠21只进行分组给药,随机分为3组:模型组,血府逐瘀胶囊低剂量给药组与血府逐瘀胶囊高剂量给药组,每组7只,每天灌胃给药1次,连续给药21天。假手术组10只。实验分组、用药量及方法如下表2所示:
[0103]
表2:实验分组及给药数据表
[0104]
组别n给药种类及用量假手术组(sham)10灌胃等体积蒸馏水模型组(cpsp)7灌胃等体积蒸馏水低剂量给药组(xfzy低)70.43g/kg/d(临床等效剂量)高剂量给药组(xfzy高)70.86g/kg/d(5倍临床等效剂量)
[0105]
2.3热痛阈测定
[0106]
术前1天、术后3天,给药后7天,14天,21天,28天,测定大鼠热痛阈值、舔右足次数
与舔后足次数的比例和右足抬脚率。
[0107]
热板法:为了避免后足基线温度的差异,先将大鼠置于37℃的热板仪上进行2分钟的适应期。然后将大鼠置于50℃的热板仪上,以60秒为上限值,以舔后足、舔右足和右足抬脚率为观察指标,测试完毕,将大鼠放回笼中,间隔至少15分钟后重复测试,重复三次,取其平均值。
[0108]
2.4统计学方法:同实施例1。
[0109]
3、实验结果
[0110]
3.1模型筛选结果
[0111]
复制大鼠mcao模型,在复制模型前后利用热板法对实验动物进行筛选,筛选结果如附图10、11所示,复制模型前实验各组痛阈值无显著差异(p>0.05)。复制大鼠mcao后3天利用热板法对痛觉敏感大鼠进行筛选,筛选出其中发生痛觉敏感的大鼠77只。测定77只mcao大鼠的热痛阈值,结果显示其中21只存在痛觉敏感情况,发病率27.27%。测定结果如附图12所示,从中可见:术后三天出现痛觉异常的大鼠与sham组相比,其他各组热痛阈值均下降;相比假手术组19~22s的热痛阈值,模型组的热痛阈值下降为7~10s,血府逐瘀胶囊低剂量给药组和血府逐瘀胶囊高剂量给药组的热痛阈值分别下降为10~12s和8~10s,热痛阈值显著降低(p<0.05),提示脑缺血导致了实验大鼠痛觉异常,但给药各组之间均无统计学差异(p<0.05)。
[0112]
并且,比较附图10与附图11,附图12与附图13可见,线栓法复制的大鼠脑卒中模型可导致大鼠出现热痛阈降低的现象在右侧肢体表现尤为明显,在同样的热刺激下,大鼠舔右足的比例显著高于左侧,该表现与卒中后丘脑痛的临床表现之一(肢体同侧的痛觉异常敏感)基本一致,初步提示本发明线栓法复制的大鼠脑卒中模型所导致的卒中后痛觉异常可能为卒中后丘脑痛。
[0113]
3.2血府逐瘀胶囊对卒中后脑损伤痛觉异常大鼠热痛阈的影响
[0114]
对痛觉异常大鼠进行筛选后开始灌胃给予血府逐瘀胶囊进行干预。
[0115]
给药1周后,以舔后足为观察指标的结果如附图14所示,与假手术组比较,模型组的热痛阈值均显著降低(p<0.05),提示脑缺血导致了实验大鼠痛觉异常,并提示mcao引起的痛觉异常现象并不会自愈;与模型组比较,血府逐瘀低剂量给药组、高剂量给药组在给药1周后,热痛阈值均升高(p<0.05),症状改善。大鼠舔右足次数与舔后足次数的比例如附图15所示,模型组大鼠舔右足的比例相比术后3天从0.8上升至0.9以上,进一步提示本发明线栓法复制的大鼠脑卒中模型所导致的卒中后痛觉异常可能为卒中后丘脑痛;与模型组比较,血府逐瘀低剂量给药组、高剂量给药组在给药1周后,大鼠舔右足的比例显著降低(p<0.05),提示血府逐瘀制剂能显著改善卒中后丘脑痛症状。
[0116]
给药2周后,以舔后足为观察指标的结果如附图16所示,血府逐瘀低剂量给药组和血府逐瘀高剂量给药组的大鼠的热痛阈值相比给药一周后的热痛阈值均无明显变化。但与模型组比较,血府逐瘀低剂量给药组、高剂量给药组在给药2周后,热痛阈值升高(p<0.05),仍说明症状改善。大鼠舔右足次数与舔后足次数的比例如附图17所示,模型组和血府逐瘀低剂量给药组大鼠舔右足的比例相比给药1周时无明显变化,血府逐瘀高剂量给药组的大鼠舔右足的比例相比给药1周进一步降低,对比附图16可进一步提示本发明线栓法复制的大鼠脑卒中模型所导致的卒中后痛觉异常为卒中后丘脑痛,并提示血府逐瘀制剂能
够显著改善卒中后丘脑痛症状。
[0117]
给药3周后,以舔后足为观察指标的结果如附图18所示,模型组和血府逐瘀低剂量给药组相比给药2周后的热痛阈值无明显变化,血府逐瘀高剂量给药组的大鼠的热痛阈值相比给药2周后的热痛阈值有所降低。大鼠舔右足次数与舔后足次数的比例如附图19所示,模型组相比给药2周后大鼠舔右足的比例无明显变化,血府逐瘀低剂量给药组和血府逐瘀高剂量给药组相比给药2周时大鼠舔右足的比例均明显降低,对比附图18可再次提示本发明线栓法复制的大鼠脑卒中模型所导致的卒中后痛觉异常为卒中后丘脑痛,并提示血府逐瘀制剂能够显著改善卒中后丘脑痛症状。
[0118]
给药4周后,以舔后足为观察指标的结果如附图20所示,模型组和血府逐瘀低剂量给药组相比给药3周后的热痛阈值无明显变化,血府逐瘀高剂量给药组的大鼠的热痛阈值相比给药3周后的热痛阈值有所升高。但与模型组比较,血府逐瘀低剂量给药组、高剂量给药组在给药4周后,热痛阈值升高(p<0.05),仍说明症状改善。大鼠舔右足次数与舔后足次数的比例如附图21所示,血府逐瘀低剂量给药组相比给药3周时大鼠舔右足的比例继续降低。
[0119]
以上实验过程证明:本发明线栓法复制的大鼠脑卒中模型所导致的卒中后痛觉异常即为卒中后丘脑痛,并非其他类型的疼痛,而血府逐瘀胶囊干预能减轻大鼠右侧肢体热痛阈降低的症状,提示血府逐瘀胶囊能够减轻缺血性卒中后脑损伤导致的卒中后丘脑痛,缓解痛觉超敏给患者带来的疼痛感,使痛觉感知恢复正常,即血府逐瘀制剂可以作为制备缺血性卒中后丘脑痛的药物。
[0120]
实施例3
[0121]
缺血性脑卒中会升高大鼠血清中的tnf-α含量。本实施例考察了血府逐瘀制剂对大鼠血清中的tnf-α含量的影响。
[0122]
对实施例2中给药4周后各组大鼠进行眼球后取血,分别离心分离血清,检测各组大鼠血清中的tnf-α含量,采用grapgpad prism软件进行数据处理、分析和作图,数据均以均数
±
标准差(x
±
s)表示。选用单因素方差分析,p<0.05表明差异具有显著性。
[0123]
结果如图22所示,血府逐瘀制剂可以降低卒中后痛觉异常大鼠血清中的tnf-α含量(p<0.05)。
[0124]
实施例4
[0125]
卒中后,大鼠丘脑的bdnf表达量会显著下降。本实施例考察了血府逐瘀制剂对大鼠丘脑bdnf含量的影响。
[0126]
将实施例2中给药4周后的大鼠每组各取3只,麻醉心脏灌流后置于冰盒上,迅速断头取脑,取患侧丘脑组织,分别提取总rna后进行pcr扩增,进而进行bdnf表达量的检测,采用grapgpad prism软件进行数据处理、分析和作图,数据均以均数
±
标准差(x
±
s)表示。选用单因素方差分析,p<0.05表明差异具有显著性。
[0127]
结果如图23所示,血府逐瘀制剂可以提高卒中后丘脑痛大鼠丘脑的bdnf表达水平(p<0.05)。
[0128]
实施例5
[0129]
缺血性脑卒中会导致大鼠丘脑组织的继发损伤。本实施例考察了血府逐瘀制剂对大鼠丘脑损伤的影响。
[0130]
将实施例2中给药4周后的大鼠每组各取3只,麻醉心脏灌流固定后取丘脑组织,将其在4%多聚甲醛中固定24h,接着依次用10%,20%,30%浓度的蔗糖梯度脱水。尼氏染色后,用oct包埋剂将固定好的脑组织于-40℃冰箱中包埋成形,在冰冻切片机载物架进行切片,光镜观察。结果如图24所示,血府逐瘀制剂可以减轻大鼠卒中导致的丘脑损伤。
[0131]
通过上述实施例可见,血府逐瘀制剂可以有效治疗大鼠脑卒中后的卒中后丘脑痛,减轻丘脑的继发损伤,其作用机制可能与其升高脑内bdnf表达水平、降低炎症因子水平有关。
[0132]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换或改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1