重组免疫检查点受体及其应用的制作方法
本发明涉及生物医药领域,具体地,本发明涉及重组免疫检查点受体及其应用,更具体地,本发明涉及重组受体、核酸、转基因淋巴细胞、构建体、制备转基因淋巴细胞的方法、治疗癌症的治疗组合物以及提高淋巴细胞免疫杀伤能力的方法。
背景技术:
癌症,由于细胞内基因突变导致细胞增殖失控的一种疾病。目前已成为人类健康的重大威胁,是导致人类死亡的主要原因之一。世界卫生组织(who)在发表的《全球癌症报告2014》中指出,2012年全球癌症患者和死亡病例都在迅速增加,而新增癌症病例有近一半出现在亚洲,其中大部分在中国,中国新增癌症病例高居第一位。《2012年中国肿瘤登记年报》数据显示,中国每年新增癌症病例约350万,约有250万人因此死亡。因此,寻找高效特异的癌症治疗方法具有重大的临床价值。
传统的肿瘤治疗方法主要包括手术、放疗和化疗,但这几种方法都具有较大的局限性,比如由于癌细胞的近端入侵或远端转移,手术切除后的肿瘤转移复发率较高,而放疗和化疗对于机体自身的正常细胞尤其是造血系统和免疫系统会造成严重的损害,因此对于已发生肿瘤转移的患者也很难达到较好的远期疗效。随着肿瘤分子机制的深入研究和生物技术的进一步发展,靶向药物治疗和免疫治疗在肿瘤的综合治疗中发挥着愈来愈大的作用。靶向疗法主要包括单克隆抗体(有时归为被动胞回输和肿瘤疫苗等。免疫疗法通过调动机体的免疫系统,增强肿瘤微环境抗肿瘤免免疫疗法)和小分子靶向药物,而免疫疗法主要包括细胞因子疗法、免疫检验点单抗、过继免疫疗法,从而控制和杀伤肿瘤细胞,因此有效率高,特异性强,耐受性好的优点,在肿瘤治疗中具有广阔的前景。
然而,肿瘤的免疫疗法,仍有待进一步深入研究和开发,来增强临床疗效。
技术实现要素:
本发明旨在至少在一定程度上解决相关技术中的技术问题之一。为此,本发明的一个目的在于提出一种重组受体及利用其有效增强淋巴细胞免疫杀伤肿瘤细胞的方法。
在本发明的第一方面,本发明提出了一种重组受体。根据本发明的实施例,所述重组受体包括:细胞免疫检查点分子片段;免疫刺激分子片段;以及t细胞受体zeta链。根据本发明的实施例,使淋巴细胞表达本发明实施例的重组受体,可有效增强淋巴细胞对肿瘤细胞的特异性杀伤效果。
根据本发明的实施例,上述重组受体还可以进一步包括如下附加技术特征至少之一:
根据本发明的实施例,所述细胞免疫检查点分子为pd1。pd1可与肿瘤细胞上特异性表达的pd-l1或pd-l2相结合。进而,淋巴细胞表达本发明实施例的重组受体,其对肿瘤细胞,特别是pd-l1或pd-l2阳性肿瘤细胞的靶向杀伤性进一步增强。
根据本发明的实施例,所述细胞免疫检查点分子片段包括所述pd1的胞外区以及任选的跨膜区,所述免疫刺激分子片段包括cd28的胞内区以及任选的跨膜区。pd1的胞外区具有与肿瘤细胞上特异性表达的pd-l1或pd-l2相结合的功能区,cd28的胞内区具有激活免疫刺激信号通路的功能区,进而淋巴细胞细胞表达本发明实施例的重组受体,其对肿瘤细胞的靶向性杀伤效果进一步提高。
根据本发明的实施例,所述重组受体包括:(a)所述pd1的胞外区和跨膜区;以及(b)所述cd28的胞内区,或者包括:(i)所述pd1的胞外区;以及(ii)所述cd28的胞内区和跨膜区。这两种组合方式均保留了pd1与肿瘤细胞上特异性表达的pd-l1或pd-l2相结合的功能区以及cd28激活免疫刺激信号通路的功能区,同时不论是pd1跨膜区还是cd28的跨膜区,均可使重组受体跨膜表达,进而淋巴细胞细胞表达本发明实施例的重组受体,其对肿瘤细胞的靶向性杀伤效果进一步提高。
根据本发明的实施例,所述t细胞受体zeta链为cd3zeta链。cd3zeta链可特异性激活下游t细胞受体信号通路,进而淋巴细胞细胞表达本发明实施例的重组受体,其对肿瘤细胞的杀伤效果进一步提高。
根据本发明的实施例,所述细胞免疫检查点分子片段的c端与所述免疫刺激分子片段的n端相连,所述免疫刺激分子片段的c端与所述t细胞受体zeta链的n端相连。本发明实施例的重组受体的相关片段在上述连接顺序下,有利于相关片段在细胞中的定位,进而更有利于发挥相应的功能-靶向、跨膜、激活免疫刺激信号通路以及激活t细胞受体信号通路,其对肿瘤细胞的靶向性杀伤能力进一步提高。
在本发明的第二方面,本发明提出了一种重组受体。根据本发明的实施例,所述重组受体具有seqidno:1或2所示的氨基酸序列。
mqipqapwpvvwavlqlgwrpgwfldspdrpwnpptfspallvvtegdnatftcsfsntsesfvlnwyrmspsnqtdklaafpedrsqpgqdcrfrvtqlpngrdfhmsvvrarrndsgtylcgaislapkaqikeslraelrvterraevptahpspsprpagqfqtlvvgvvggllgslvllvwvlaviskrsrllhsdymnmtprrpgptrkhyqpyapprdfaayrsrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr(seqidno:1)。
mqipqapwpvvwavlqlgwrpgwfldspdrpwnpptfspallvvtegdnatftcsfsntsesfvlnwyrmspsnqtdklaafpedrsqpgqdcrfrvtqlpngrdfhmsvvrarrndsgtylcgaislapkaqikeslraelrvterraevptahpsplfpgpskpfwvlvvvggvlacysllvtvafiifwvrskrsrllhsdymnmtprrpgptrkhyqpyapprdfaayrsrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr(seqidno:2)。
根据本发明的实施例,使淋巴细胞表达本发明实施例的重组受体,可有效增强淋巴细胞对肿瘤细胞,特别是pd-l1或pd-l2阳性肿瘤细胞的特异性杀伤效果。
在本发明的第三方面,本发明提出了一种核酸。根据本发明的实施例,所述核酸编码前面所述的重组受体,任选地,所述核酸具有seqidno:3或4所示的核苷酸序列。
atgcagatcccacaggcgccctggccagtcgtctgggcggtgctacaactgggctggcggccaggatggttcttagactccccagacaggccctggaacccccccaccttctccccagccctgctcgtggtgaccgaaggggacaacgccaccttcacctgcagcttctccaacacatcggagagcttcgtgctaaactggtaccgcatgagccccagcaaccagacggacaagctggccgccttccccgaggaccgcagccagcccggccaggactgccgcttccgtgtcacacaactgcccaacgggcgtgacttccacatgagcgtggtcagggcccggcgcaatgacagcggcacctacctctgtggggccatctccctggcccccaaggcgcagatcaaagagagcctgcgggcagagctcagggtgacagagagaagggcagaagtgcccacagcccaccccagcccctcacccaggccagccggccagttccaaaccctggtggttggtgtcgtgggcggcctgctgggcagcctggtgctgctagtctgggtcctggccgtcatcagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctccagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgctaa(seqidno:3)。
atgcagatcccacaggcgccctggccagtcgtctgggcggtgctacaactgggctggcggccaggatggttcttagactccccagacaggccctggaacccccccaccttctccccagccctgctcgtggtgaccgaaggggacaacgccaccttcacctgcagcttctccaacacatcggagagcttcgtgctaaactggtaccgcatgagccccagcaaccagacggacaagctggccgccttccccgaggaccgcagccagcccggccaggactgccgcttccgtgtcacacaactgcccaacgggcgtgacttccacatgagcgtggtcagggcccggcgcaatgacagcggcacctacctctgtggggccatctccctggcccccaaggcgcagatcaaagagagcctgcgggcagagctcagggtgacagagagaagggcagaagtgcccacagcccacccaagtcccctatttcccggaccttctaagcccttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctccagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgctaa(seqidno:4)。
将本发明实施例的核酸导入受体淋巴细胞中,核酸所编码的重组受体在淋巴细胞中跨膜表达,该淋巴细胞对肿瘤细胞的特异性杀伤效果显著提高。
在本发明的第四方面,本发明提出了一种构建体。根据本发明的实施例,所述构建体携带前面所述的核酸。将本发明实施例的构建体导入受体淋巴细胞中,构建体所携带的核酸所编码的重组受体在淋巴细胞中跨膜表达,该淋巴细胞对肿瘤细胞的特异性杀伤效果显著提高。
根据本发明的实施例,所述构建体还可以进一步包括如下附加技术特征至少之一:
根据本发明的实施例,所述构建体进一步携带编码无功能egfr的核酸,所述编码无功能egfr的核酸具有seqidno:5所示的核苷酸序列。
atggctctgcccgtcaccgctctgctgctgcctctggctctgctgctgcacgccgcacgccctgggagtcgcaaagtctgtaatgggatcggcatcggcgagttcaaggacagcctgtccatcaacgccaccaatatcaagcactttaagaattgcacatctatcagcggcgacctgcacatcctgccagtggccttccggggcgattcttttacccacacaccccctctggaccctcaggagctggatatcctgaagaccgtgaaggagatcacaggcttcctgctgatccaggcctggcctgagaacagaaccgatctgcacgcctttgagaatctggagatcatccggggcagaacaaagcagcacggccagttctccctggccgtggtgtctctgaacatcaccagcctgggcctgaggtccctgaaggagatctctgacggcgatgtgatcatctccggcaacaagaacctgtgctacgccaacacaatcaattggaagaagctgtttggcacctctggccagaagacaaagatcatctctaaccggggcgagaatagctgcaaggcaaccggacaggtgtgccacgcactgtgcagcccagagggatgttggggcccagagccacgggactgcgtgagctgtagaaacgtgtccaggggccgcgagtgcgtggataagtgtaatctgctggagggcgagccaagggagttcgtggagaactccgagtgcatccagtgtcaccccgagtgcctgcctcaggccatgaacatcacctgtacaggccgcggccccgacaattgcatccagtgtgcccactatatcgatggccctcactgcgtgaagacctgtccagccggcgtgatgggcgagaacaatacactggtgtggaagtacgcagacgcaggacacgtgtgccacctgtgccaccccaattgcacctatggctgtacaggaccaggcctggagggatgcccaaccaacggccctaagatcccaagcatcgccacaggcatggtgggggcactgctgctgctgctggtggtggctctggggattgggctgtttatgagaaggtaa(seqidno:5)。
根据本发明的实施例,无功能egfr受体缺少n-端配体结合区和细胞内受体酪氨酸激酶活性,但包括野生型egfr受体的跨膜区和完整的与抗egfr抗体结合的序列,所以无功能egfr受体可作为淋巴细胞的自杀标记。本发明实施例的构建体导入受体淋巴细胞中,无功能egfr受体的表达可在有效保证淋巴细胞的对肿瘤细胞的靶向杀伤作用的前提下,如果病人出现严重不良反应,淋巴细胞可被抗egfr抗体清除,进而提高了本发明实施例的构建体治疗肿瘤病人的安全性。
根据本发明的实施例,所述构建体进一步携带内部核糖体进入位点序列,所述内部核糖体进入位点序列具有seqidno:6所示的核苷酸序列,并且所述内部核糖体进入位点序列设置于前面所述的核酸和所述编码无功能egfr的核酸之间。
cccctctccctcccccccccctaacgttactggccgaagccgcttggaataaggccggtgtgcgtttgtctatatgttattttccaccatattgccgtcttttggcaatgtgagggcccggaaacctggccctgtcttcttgacgagcattcctaggggtctttcccctctcgccaaaggaatgcaaggtctgttgaatgtcgtgaaggaagcagttcctctggaagcttcttgaagacaaacaacgtctgtagcgaccctttgcaggcagcggaaccccccacctggcgacaggtgcctctgcggccaaaagccacgtgtataagatacacctgcaaaggcggcacaaccccagtgccacgttgtgagttggatagttgtggaaagagtcaaatggctctcctcaagcgtattcaacaaggggctgaaggatgcccagaaggtaccccattgtatgggatctgatctggggcctcggtgcacatgctttacatgtgtttagtcgaggttaaaaaaacgtctaggccccccgaaccacggggacgtggttttcctttgaaaaacacgatgataatatggccacaacc(seqidno:6)。
内部核糖体进入位点序列的引入,使得编码无功能egfr的核酸的起始表达不依赖5’帽子结构,并且编码重组受体的核酸和编码无功能egfr的核酸成比例表达,进而更加有利于表达调控,将本发明实施例的构建体导入受体淋巴细胞,所获得的转基因淋巴细胞的治疗安全性更高。
根据本发明的实施例,所述构建体进一步携带编码连接肽的核酸,所述编码连接肽的核酸具有seqidno:7~10所示的核苷酸序列,并且所述编码连接肽的核酸设置于前面所述的核酸和所述编码无功能egfr的核酸之间。
ggcagcggcgagggcaggggcagcctgctgacctgcggcgacgtggaggagaaccccggcccc(seqidno:7)。
ggcagcggcgccaccaacttcagcctgctgaagcaggccggcgacgtggaggagaaccccggcccc(seqidno:8)。
ggcagcggccagtgcaccaactacgccctgctgaagctggccggcgacgtggagagcaaccccggcccc(seqidno:9)。
ggcagcggcgtgaagcagaccctgaacttcgacctgctgaagctggccggcgacgtggagagcaaccccggcccc(seqidno:10)。
根据本发明的实施例,将本发明实施例的构建体导入受体淋巴细胞,所编码的连接肽能够在所述淋巴细胞中被切割,连接肽的引入使得所表达的重组受体以及无功能egfr呈非融合状态表达在淋巴细胞膜上。
根据本发明的实施例,所述构建体进一步携带第一启动子,所述第一启动子与前面所述的核酸可操作地连接,任选地,所述第一启动子包括选自cmv,ef-1,ltr或rsv启动子。上述第一启动子可独立地启动表达第一核酸分子,进而更加有利于相应核酸分子表达的调控。发明人发现,cmv,ef-1,ltr或rsv启动子能够高效启动表达前面所述的核酸,前面所述的核酸的表达效率显著提高。
根据本发明的实施例,所述构建体进一步携带第二启动子,所述第二启动子与所述编码无功能egfr的核酸可操作地连接,任选地,所述第二启动子包括选自cmv,ef-1,ltr或rsv启动子。上述第二启动子可独立地启动表达编码无功能egfr的核酸,进而更加有利于编码无功能egfr的核酸的表达调控。发明人发现,cmv,ef-1,ltr或rsv启动子能够高效启动表达编码无功能egfr的核酸,编码无功能egfr的核酸的表达效率显著提高。
根据本发明的实施例,所述构建体的载体为反转录病毒载体、慢病毒载体或腺病毒相关病毒载体。上述载体可实现所携带核酸在受体细胞的高效表达,治疗效率高。
在本发明的第五方面,本发明提出了一种构建体。根据本发明的实施例,所述构建体携带下列核酸分子:(1)编码免疫检查点分子片段的核酸分子,所述免疫检查点分子片段具有seqidno:11或12所示的氨基酸序列,所述编码免疫检查点分子片段的核酸分子具有seqidno:13或14所示的核苷酸序列;(2)编码免疫刺激分子片段的核酸分子,所述免疫刺激分子片段具有seqidno:15或16所示的氨基酸序列,所述编码免疫刺激分子片段的核酸分子具有seqidno:17或18所示的核苷酸序列;以及(3)编码t细胞受体zeta链的核酸分子,所述t细胞受体zeta链具有seqidno:19所示的氨基酸序列,所述编码t细胞受体zeta链的核酸分子具有seqidno:20所示的核苷酸序列。
mqipqapwpvvwavlqlgwrpgwfldspdrpwnpptfspallvvtegdnatftcsfsntsesfvlnwyrmspsnqtdklaafpedrsqpgqdcrfrvtqlpngrdfhmsvvrarrndsgtylcgaislapkaqikeslraelrvterraevptahpspsprpagqfqtlvvgvvggllgslvllvwvlavi(seqidno:11)。
mqipqapwpvvwavlqlgwrpgwfldspdrpwnpptfspallvvtegdnatftcsfsntsesfvlnwyrmspsnqtdklaafpedrsqpgqdcrfrvtqlpngrdfhmsvvrarrndsgtylcgaislapkaqikeslraelrvterraevptah(seqidno:12)。
atgcagatcccacaggcgccctggccagtcgtctgggcggtgctacaactgggctggcggccaggatggttcttagactccccagacaggccctggaacccccccaccttctccccagccctgctcgtggtgaccgaaggggacaacgccaccttcacctgcagcttctccaacacatcggagagcttcgtgctaaactggtaccgcatgagccccagcaaccagacggacaagctggccgccttccccgaggaccgcagccagcccggccaggactgccgcttccgtgtcacacaactgcccaacgggcgtgacttccacatgagcgtggtcagggcccggcgcaatgacagcggcacctacctctgtggggccatctccctggcccccaaggcgcagatcaaagagagcctgcgggcagagctcagggtgacagagagaagggcagaagtgcccacagcccaccccagcccctcacccaggccagccggccagttccaaaccctggtggttggtgtcgtgggcggcctgctgggcagcctggtgctgctagtctgggtcctggccgtcatc(seqidno:13)。
atgcagatcccacaggcgccctggccagtcgtctgggcggtgctacaactgggctggcggccaggatggttcttagactccccagacaggccctggaacccccccaccttctccccagccctgctcgtggtgaccgaaggggacaacgccaccttcacctgcagcttctccaacacatcggagagcttcgtgctaaactggtaccgcatgagccccagcaaccagacggacaagctggccgccttccccgaggaccgcagccagcccggccaggactgccgcttccgtgtcacacaactgcccaacgggcgtgacttccacatgagcgtggtcagggcccggcgcaatgacagcggcacctacctctgtggggccatctccctggcccccaaggcgcagatcaaagagagcctgcgggcagagctcagggtgacagagagaagggcagaagtgcccacagcccac(seqidno:14)。
skrsrllhsdymnmtprrpgptrkhyqpyapprdfaayrs(seqidno:15)。
psplfpgpskpfwvlvvvggvlacysllvtvafiifwvrskrsrllhsdymnmtprrpgptrkhyqpyapprdfaayrs(seqidno:16)。
agtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctcc(seqidno:17)。
ccaagtcccctatttcccggaccttctaagcccttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctcc(seqidno:18)。
rvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr(seqidno:19)。
agagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgctaa(seqidno:20)。
将本发明实施例的构建体导入受体淋巴细胞中,构建体所携带的核酸所编码的分子片段组成融合受体蛋白,并在在淋巴细胞中跨膜表达,该淋巴细胞对肿瘤细胞的特异性杀伤效果显著提高。
根据本发明的实施例,上述构建体还可以进一步包括如下附加技术特征至少之一:
根据本发明的实施例,所述构建体进一步携带编码无功能egfr的核酸分子,所述编码无功能egfr的核酸分子具有seqidno:5所示的核苷酸序列,所述无功能egfr具有seqidno:21所示的氨基酸序列。
malpvtalllplalllhaarpgsrkvcngigigefkdslsinatnikhfknctsisgdlhilpvafrgdsfthtppldpqeldilktvkeitgflliqawpenrtdlhafenleiirgrtkqhgqfslavvslnitslglrslkeisdgdviisgnknlcyantinwkklfgtsgqktkiisnrgensckatgqvchalcspegcwgpeprdcvscrnvsrgrecvdkcnllegeprefvenseciqchpeclpqamnitctgrgpdnciqcahyidgphcvktcpagvmgenntlvwkyadaghvchlchpnctygctgpglegcptngpkipsiatgmvgalllllvvalgiglfmrr(seqidno:21)。
如前所述,本发明实施例的构建体导入受体淋巴细胞中,无功能egfr受体的表达可在有效保证淋巴细胞的对肿瘤细胞的靶向杀伤作用的前提下,如果病人出现严重不良反应,淋巴细胞可被抗egfr抗体清除,进而提高了本发明实施例的构建体、淋巴细胞等治疗肿瘤病人的安全性。
根据本发明的实施例,所述构建体进一步携带内部核糖体进入位点序列的核酸分子,所述内部核糖体进入位点序列的核酸分子具有seqidno:6所示的核苷酸序列,并且所述编码内部核糖体进入位点序列的核酸分子设置于所述编码t细胞受体zeta链的核酸分子和所述编码无功能egfr的核酸分子之间。如前所述,内部核糖体进入位点序列的引入更加有利于表达调控,所获得的转基因淋巴细胞的治疗安全性更高。
根据本发明的实施例,所述构建体进一步携带编码连接肽的核酸,所述编码连接肽的核酸具有seqidno:7~10所示的核苷酸序列,所述连接肽具有seqidno:22~25所示的氨基酸序列,并且所述编码连接肽的核酸设置于所述编码t细胞受体zeta链的核酸分子和所述编码无功能egfr的核酸分子之间。
egrgslltcgdveenpgp(seqidno:22)。
atnfsllkqagdveenpgp(seqidno:23)。
qctnyallklagdvesnpgp(seqidno:24)。
vkqtlnfdllklagdvesnpgp(seqidno:25)。
如前所述,将本发明实施例的构建体导入受体淋巴细胞,所编码的连接肽能够在所述淋巴细胞中被切割,连接肽的引入使得所表达的分子片段所组成的重组受体与无功能egfr呈非融合状态表达在淋巴细胞膜上。
根据本发明的实施例,所述构建体进一步携带第一启动子,所述第一启动子与所述编码免疫检查点分子片段的核酸分子可操作地连接,任选地,所述第一启动子包括选自cmv,ef-1,ltr或rsv启动子。如前所述,cmv,ef-1,ltr或rsv启动子能够高效启动表达前面所述的编码免疫检查点分子片段的核酸分子、编码免疫刺激分子片段的核酸分子以及编码t细胞受体zeta链的核酸分子,前面所述的核酸分子片段的表达效率显著提高。
根据本发明的实施例,所述构建体进一步携带第二启动子,所述第二启动子与所述编码无功能egfr的核酸分子可操作地连接,任选地,所述第二启动子包括选自,cmv,ef-1,ltr或rsv启动子。如前所述,cmv,ef-1,ltr或rsv启动子能够高效启动表达所述的编码无功能egfr的核酸分子,编码无功能egfr的核酸分子的表达效率显著提高。
根据本发明的实施例,所述构建体的载体为反转录病毒载体、慢病毒载体或腺病毒相关病毒载体。上述载体可实现所携带核酸在受体细胞的高效表达,治疗效率高。
在本发明的第六方面,本发明提出了一种转基因淋巴细胞。根据本发明的实施例,所述转基因淋巴细胞表达前面所述的重组受体,任选地,所述转基因淋巴细胞表达无功能egfr。本发明实施例的转基因淋巴细胞对肿瘤细胞的特异性杀伤效果强、安全。
根据本发明的实施例,上述转基因淋巴细胞还可以进一步包括如下附加技术特征至少之一:
根据本发明的实施例,所述淋巴细胞为抗原特异性t淋巴细胞,任选地,所述淋巴细胞是肿瘤浸润t淋巴细胞,任选地,所述淋巴细胞是外周血t淋巴细胞,任选地,所述淋巴细胞是自然杀伤t淋巴细胞,任选地,所述淋巴细胞是自然杀伤细胞。根据本发明实施例的抗原特异性t淋巴细胞、肿瘤浸润t淋巴细胞、外周血t淋巴细胞、自然杀伤t淋巴细胞或自然杀伤细胞,可实现对肿瘤细胞的特异性免疫杀伤,安全性高。
在本发明的第七方面,本发明提出了一种制备前面所述的转基因淋巴细胞的方法。根据本发明的实施例,所述方法包括:将前面所述的构建体引入到淋巴细胞中或者t淋巴细胞。利用根据本发明实施例的上述方法,可简便、高效地获得前面所述的转基因淋巴细胞,如前所述,所获得的转基因淋巴细胞对肿瘤细胞的特异性杀伤显著提高、安全。
在本发明的第八方面,本发明提出了一种用于治疗癌症的治疗组合物。根据本发明的实施例,所述治疗组合物包括:前面所述的重组受体、前面所述的核酸、前面所述的构建体或者前面所述的转基因淋巴细胞。利用根据本发明实施例的治疗组合物,能够实现对肿瘤细胞的有效、安全地杀伤。
在本发明的第九方面,本发明提出了一种提高淋巴细胞治疗免疫杀伤能力的方法。根据本发明的实施例,所述方法包括:使所述淋巴细胞表达前面所述的重组受体。利用根据本发明实施例上述方法,能够有效提高淋巴细胞对肿瘤细胞的特异性免疫杀伤。
附图说明
图1是根据本发明实施例慢病毒载体的结构示意图;
图2是根据本发明实施例的共表达pd1-cd28-cd3zeta重组受体和无功能egfr受体的淋巴细胞被抗egfr抗体介导adcc杀伤清除的结果图;以及
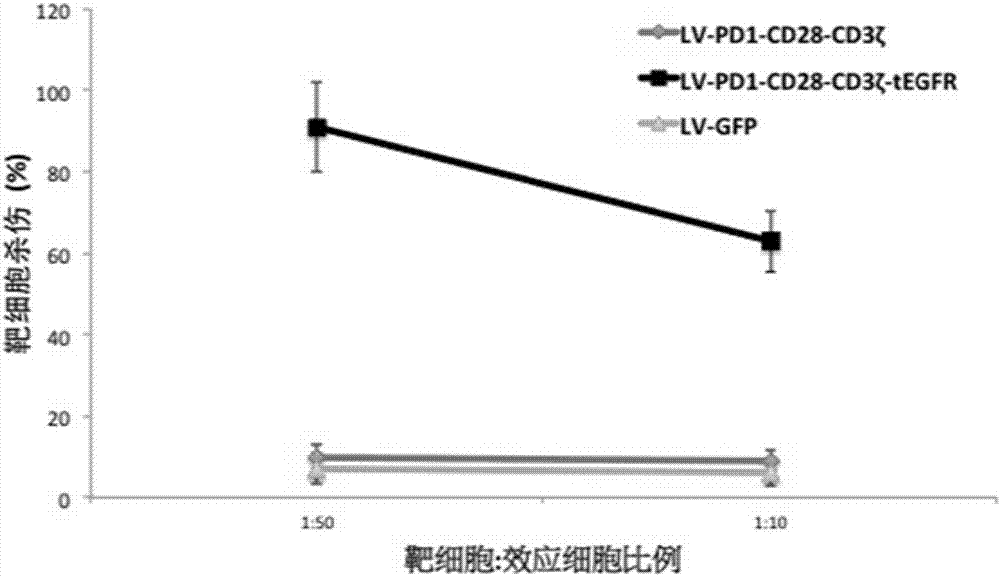
图3是根据本发明实施例的共表达pd1-cd28-cd3zeta重组受体和无功能egfr受体的淋巴细胞杀伤pd-l1阳性肿瘤细胞的结果图。
具体实施方式
下面详细描述本发明的实施例。下面描述的实施例是示例性的,仅用于解释本发明,而不能理解为对本发明的限制。
需要说明的是,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括一个或者更多个该特征。进一步地,在本发明的描述中,除非另有说明,“多个”的含义是两个或两个以上。
重组受体蛋白
一方面,本发明提出了一种重组受体。根据本发明的实施例,该重组受体包括:细胞免疫检查点分子片段;免疫刺激分子片段;以及t细胞受体zeta链。根据本发明的实施例,使淋巴细胞表达本发明实施例的重组受体,可有效增强淋巴细胞对肿瘤细胞的特异性杀伤效果。
根据本发明的具体实施例,所述细胞免疫检查点分子为pd1。pd1可与肿瘤细胞上特异性表达的pd-l1或pd-l2相结合,进而,淋巴细胞表达本发明实施例的重组受体,淋巴细胞在pd1的引导下,特异性靶向肿瘤细胞,其对肿瘤细胞的靶标性进一步增强。
根据本发明的再一具体实施例,细胞免疫检查点分子片段包括pd1的胞外区以及任选的跨膜区,免疫刺激分子片段包括cd28的胞内区以及任选的跨膜区。例如,根据本发明的实施例,重组受体可以包括:(a)pd1的胞外区和跨膜区;以及(b)cd28的胞内区,或者包括:(i)pd1的胞外区;以及(ii)cd28的胞内区和跨膜区。pd1的胞外区具有与肿瘤细胞上特异性表达的pd-l1或pd-l2相结合的功能区,cd28的胞内区具有激活免疫刺激信号通路的功能区,同时不论是pd1跨膜区还是cd28的跨膜区,均可使重组受体跨膜表达,进而淋巴细胞细胞表达本发明实施例的重组受体,其对肿瘤细胞的靶向性杀伤效果进一步提高。
另外,根据本发明的再一实施例,t细胞受体zeta链为cd3zeta链。cd3zeta链关联t细胞受体(tcr)信号通路,cd3zeta链触发后,zeta链可以同一胞浆内称为zeta链相关蛋白70(zap-70)相结合,zap-70为一种胞浆内具有酪氨酸激酶(ptk)活性的信号蛋白,含有两个sh-2(srchomologyregion2,sh-2)结构域,zap-70分子中sh-2与zeta链中磷酸化的酪氨酸残基相结合,zap-70激活可进一步激活ras蛋白,进而最终活化淋巴细胞。cd3zeta链可特异性激活下游t细胞受体信号通路,进而淋巴细胞表达本发明实施例的重组蛋白,在免疫刺激分子活化功能片段以及cd3zeta链活化作用的协同作用下,其对肿瘤细胞的杀伤效果进一步提高。
最后,根据本发明的实施例,上述重组蛋白中相应分子片段的连接顺序可为:细胞免疫检查点分子片段的c端与免疫刺激分子片段的n端相连,免疫刺激分子片段的c端与t细胞受体zeta链的n端相连。发明人发现,本发明实施例的重组蛋白的相关片段在上述连接顺序下,有利于相关片段在细胞中的定位,进而更有利于发挥相应的功能-靶向、跨膜、激活免疫刺激信号通路以及激活t细胞受体信号通路,其对肿瘤细胞的靶向性杀伤能力进一步提高。
具体地,根据本发明的实施例,重组受体具有seqidno:1或2所示的氨基酸序列。其中,seqidno:1表示包含人pd1胞外区和跨膜区、cd28胞内区以及cd3zeta链的重组受体(pd1-ecd-tm-cd28-icd-cd3zeta)的氨基酸序列;seqidno:2表示包含人pd1胞外区、cd28跨膜区和胞内区以及cd3zeta链的重组受体(pd1-ecd-cd28-tm-icd-cd3zeta)的氨基酸序列。根据本发明的实施例,重组受体具有上述氨基酸序列,使其表达在淋巴细胞中,可有效增强淋巴细胞对肿瘤细胞的特异性杀伤效果。
核酸
另一方面,本发明提出了一种核酸。根据本发明的实施例,该核酸编码前面所述的重组受体,任选地,所述核酸具有seqidno:3或4所示的核苷酸序列。其中,seqidno:3所示的核苷酸序列编码包含人pd1胞外区和跨膜区、cd28胞内区以及cd3zeta链的重组受体(pd1-ecd-tm-cd28-icd-cd3zeta),seqidno:4所示的核苷酸序列编码包含人pd1胞外区、cd28跨膜区和胞内区以及cd3zeta链的重组受体(pd1-ecd-cd28-tm-icd-cd3zeta)。将本发明实施例的核酸导入受体淋巴细胞中,核酸所编码的重组受体在淋巴细胞中跨膜表达,该淋巴细胞对肿瘤细胞的特异性杀伤效果显著提高。
构建体
另一方面,本发明提出了一种构建。根据本发明的实施例,所述构建体携带前面所述的核酸。将本发明实施例的构建体导入受体淋巴细胞中,构建体所携带的核酸所编码的重组受体在淋巴细胞中跨膜表达,该淋巴细胞对肿瘤细胞的特异性杀伤效果显著提高。
或者,根据本发明的实施例,所述构建体携带下列核酸分子:(1)编码免疫检查点分子片段的核酸分子,所述免疫检查点分子片段具有seqidno:11或12所示的氨基酸序列,所述编码免疫检查点分子片段的核酸分子具有seqidno:13或14所示的核苷酸序列;其中,seqidno:11所示的氨基酸序列是人pd1胞外区和跨膜区的氨基酸序列(pd1-ecd-tm),seqidno:12所示的氨基酸序列是人pd1胞外区的氨基酸序列(pd1-ecd);seqidno:13是编码pd1-ecd-tm的核苷酸序列,seqidno:14是编码pd1-ecd的核苷酸序列。(2)编码免疫刺激分子片段的核酸分子,所述免疫刺激分子片段具有seqidno:15或16所示的氨基酸序列,所述编码免疫刺激分子片段的核酸分子具有seqidno:17或18所示的核苷酸序列,其中,seqidno:15所示的氨基酸序列是人cd28胞内区的氨基酸序列(cd28-icd),seqidno:16所示的氨基酸序列是人cd28跨膜区和胞内区的氨基酸序列(cd28-tm-icd),seqidno:17是编码cd28-icd的核苷酸序列,seqidno:18是编码cd28-tm-icd的核苷酸序列;以及(3)编码t细胞受体zeta链的核酸分子,所述t细胞受体zeta链具有seqidno:19所示的氨基酸序列,所述编码t细胞受体zeta链的核酸分子具有seqidno:20所示的核苷酸序列。将本发明实施例的构建体导入受体淋巴细胞中,构建体所携带的核酸所编码的分子片段组成上述重组受体,并在淋巴细胞中跨膜表达,该淋巴细胞对肿瘤细胞的特异性杀伤效果显著提高。
根据本发明的具体实施例,所述构建体进一步携带编码无功能egfr的核酸,所述编码无功能egfr的核酸具有seqidno:5所示的核苷酸序列。根据本发明的实施例,无功能egfr受体缺少n-端配体结合区和细胞内受体酪氨酸激酶活性,但包括野生型egfr受体的跨膜区和完整的与抗egfr抗体结合的序列,所以无功能egfr受体可作为淋巴细胞的自杀标记。本发明实施例的构建体导入受体淋巴细胞中,无功能egfr受体的表达可在有效保证淋巴细胞的对肿瘤细胞的靶向杀伤作用的前提下,如果病人出现严重不良反应,淋巴细胞可被抗egfr抗体清除,进而提高了本发明实施例的构建体治疗肿瘤病人的安全性。
其中,发明人是通过如下方式的至少之一实现上述重组受体以及任选的无功能egfr受体分别独立地表达的:
携带内部核糖体进入位点序列(ires):根据本发明的实施例,所述构建体进一步携带内部核糖体进入位点序列,所述内部核糖体进入位点序列具有seqidno:6所示的核苷酸序列,并且所述内部核糖体进入位点序列设置于前面所述的核酸和所述编码无功能egfr的核酸之间。内部核糖体进入位点序列的引入,使得编码无功能egfr的核酸的起始表达不依赖5’帽子结构,并且编码重组受体的核酸和编码无功能egfr的核酸成比例表达,进而更加有利于表达调控,将本发明实施例的构建体导入受体淋巴细胞,所获得的转基因淋巴细胞的治疗安全性更高。
连接肽:根据本发明的实施例,所述构建体还可以进一步携带编码连接肽的核酸,所述编码连接肽的核酸具有seqidno:7~10所示的核苷酸序列,该连接肽是2a连接肽,并且所述编码连接肽的核酸设置于前面所述的核酸和所述编码无功能egfr的核酸之间,其中,seqidno:7编码的连接肽具有seqidno:22所示的氨基酸序列,seqidno:8编码的连接肽具有seqidno:23所示的氨基酸序列,seqidno:9编码的连接肽具有seqidno:24所示的氨基酸序列,seqidno:10编码的连接肽具有seqidno:25所示的氨基酸序列。根据本发明的实施例,将本发明实施例的构建体导入受体淋巴细胞,所编码的连接肽能够在所述淋巴细胞中被切割,连接肽的引入使得所表达的重组受体以及无功能egfr呈非融合状态表达在淋巴细胞膜上。
启动子:根据本发明的实施例,所述构建体还可以进一步携带第一启动子,所述第一启动子与前面所述的核酸可操作地连接,任选地,所述第一启动子包括选自cmv,ef-1,ltr或rsv启动子。根据本发明的实施例,所述构建体进一步携带第二启动子,所述第二启动子与所述编码无功能egfr的核酸可操作地连接,任选地,所述第二启动子包括选自cmv,ef-1,ltr或rsv启动子。上述第一、第二启动子可独立地启动表达上述重组蛋白、编码无功能egfr的核酸,进而更加有利于重组蛋白、编码无功能egfr的核酸的表达调控。发明人发现,cmv,ef-1,ltr或rsv启动子能够高效启动表达上述重组蛋白、编码无功能egfr的核酸,重组蛋白、编码无功能egfr的核酸的表达效率显著提高。
通过上述内部核糖体进入位点序列、或第一、第二启动子或编码连接肽的核酸分子的引入,使得无功能egfr受体高效地表达以及上述重组受体高效地表达在本发明实施例的转基因淋巴细胞膜上,并且无功能egfr受体和重组受体呈非融合状态表达在淋巴细胞膜上,从而保证了重组蛋白增强免疫的生物学作用,或有效实现了转基因淋巴细胞的及时清除,从而使得淋巴细胞的靶向杀伤作用更加显著,免疫杀伤的安全性进一步提高。
根据本发明的实施例,所述构建体的载体为反转录病毒载体、慢病毒载体或腺病毒相关病毒载体。本发明实施例的病毒的载体在病毒包装和感染过程中,病毒感染范围广泛,既可感染终末分化细胞,又可感染处于分裂期的细胞,既可整合到宿主染色体,又可游离在宿主染色体之外,进而可实现广谱而高效的感染效率。上述载体可实现所携带核酸在受体细胞的高效表达,治疗效率高。
根据本发明的具体实施例,以构建一个慢病毒载体为例,发明人为了构建一个慢病毒载体,在某些病毒序列的位置,将目的核酸插入到病毒基因组中,从而产生复制缺陷的病毒。为了产生病毒体,发明人进而构建包装细胞系(包含gag,pol和env基因,但不包括ltr和包装成分)。发明人将含有目的基因的重组质粒,连同慢病毒ltr和包装序列,一起引入包装细胞系中。包装序列允许重组质粒rna转录产物被包装到病毒颗粒中,然后被分泌到培养基中。进而发明人收集包含重组慢病毒的基质,有选择性地浓缩,并用于基因转移。慢载体可以感染多种细胞类型,包括可分裂细胞和不可分裂细胞。
另外,根据本发明的实施例,本发明实施例的慢病毒是复合慢病毒,除了常见的慢病毒基因gag,pol和env,还包含有调控和结构功能的其他基因。慢病毒载体是本领域技术人员所熟知的,慢病毒包括:人类免疫缺陷病毒hiv–1,hiv–2和猿猴免疫缺陷病毒siv。慢病毒载体通过多重衰减艾滋病毒致病基因产生,例如全部删除基因env,vif,vpr,vpu和nef,使慢病毒载体形成生物安全型载体。重组慢病毒载体能够感染非分裂细胞,同时可用于体内和体外基因转移和核酸序列表达。例如:在合适的宿主细胞中,和带有包装功能(gag,pol,env,rev和tat)的两个或更多的载体一起,能够感染非分裂细胞。重组病毒的靶向性,是通过抗体或特定配体(靶向特定细胞类型受体)与膜蛋白的结合来实现的。同时,重组病毒的靶向性通过插入一个有效序列(包括调控区域)到病毒载体中,连同另一个编码了特定靶细胞上的受体的配体的基因,使载体具有了特定的靶向。各种有用的慢病毒载体,以及各种方法和操作等产生的载体,用于改变细胞的表达。根据本发明的实施例,本发明实施例的腺关联病毒载体(aav)可使用一种或多种为人熟知的血清类型腺关联病毒载体的dna构建。
另外,根据本发明的实施例,本发明实施例的也包含微基因。微基因意味着用组合(选定的核苷酸序列和可操作的必要的相关连接序列)来指导转化、转录和/或基因产物在体内或体外的宿主细胞中的表达。应用“可操作的连接”序列包含连续目的基因的表达控制序列,和作用于反式或远距离控制目的基因的表达控制序列。
另外,本发明实施例的载体还包括常规控制元素。大量的表达控制序列(包括天然的,可诱导和/或特定组织的启动子)可能被使用。根据本发明的实施例,启动子为组织特异型启动子。根据本发明的实施例,启动子为诱导型启动子。根据本发明的实施例,启动子为选自基于所选载体的启动子。根据本发明的实施例,当选择慢病毒载体时,启动子为cmvie基因,ef-1α,泛素c,或磷酸甘油激酶(pgk)启动子。其他常规表达控制序列包括可选标记或报告基因,包括编码遗传霉素,潮霉素,氨苄青霉素或嘌呤霉素耐药性等的核苷酸序列。载体的其他组件包括复制起点。
构建载体的技术为本领域技术人员所熟知的,这些技术包括常规克隆技术。
根据本发明的实施例,发明人构建了共表达任选的无功能egfr受体以及重组受体的病毒载体。本发明实施例的运送表达任选的无功能egfr受体的核酸分子以及表达重组受体的病毒载体或质粒是复合的,此病毒载体或质粒可结合聚合物或其他材料来增加其稳定性,或协助其靶向运动。
转基因淋巴细胞
另一方面,本发明提出了一种转基因淋巴细胞。根据本发明的实施例,所述转基因淋巴细胞表达前面所述的重组受体,任选地,所述转基因淋巴细胞表达无功能egfr。本发明实施例的转基因淋巴细胞对肿瘤细胞的特异性杀伤效果强、安全。
根据本发明的具体实施例,所述淋巴细胞为抗原特异性t淋巴细胞、肿瘤浸润t淋巴细胞、外周血t淋巴细胞、自然杀伤t淋巴细胞、自然杀伤细胞。根据本发明实施例的抗原特异性t淋巴细胞、肿瘤浸润t淋巴细胞、外周血t淋巴细胞、自然杀伤t淋巴细胞或自然杀伤细胞,可实现对肿瘤细胞的特异性免疫杀伤,安全性高。
制备转基因淋巴细胞的方法
另一方面,本发明提出了一种制备前面所述的转基因淋巴细胞的方法。根据本发明的实施例,所述方法包括:将前面所述的构建体引入到淋巴细胞中或者t淋巴细胞。利用根据本发明实施例的上述方法,可简便、高效地获得前面所述的转基因淋巴细胞,如前所述,所获得的转基因淋巴细胞对肿瘤细胞的特异性杀伤显著提高、安全。
用于治疗癌症的治疗组合物
再一方面,本发明提出了一种用于治疗癌症的治疗组合物。根据本发明的实施例,所述治疗组合物包括:前面所述的构建体、前面所述的转基因淋巴细胞、前面所述的重组受体或者前面所述的核酸。利用根据本发明实施例的治疗组合物,能够实现对肿瘤细胞的有效、安全地杀伤。
根据本发明的实施例,提供给患者的本发明实施例的治疗组合物,较好的应用于生物兼容溶液或可接受的药学运载载体。作为准备的各种治疗组合物被悬浮或溶解在医药上或生理上可接受的载体,如生理盐水;等渗的盐溶液或其他精于此道的人的比较明显的配方中。适当的载体在很大程度上取决于给药途径。其他有水和无水的等渗无菌注射液和有水和无水的无菌悬浮液,是医药上可接受的载体。
根据本发明的实施例,足够数量的病毒载体被转导入靶向t细胞中,并提供足够强度的转基因,表达任选的无功能egfr受体以及表达特有的重组受体。治疗试剂的剂量主要取决于治疗状况,年龄,体重,病人的健康程度,从而可能造成病人的变异性。
表达任选的无功能egfr受体以及表达特有的上述重组受体这些方法是联合治疗的一部分。这些病毒载体和用于过继免疫治疗的抗肿瘤t细胞,可以被单独或结合其他治疗癌症的方法一起执行。在合适的条件下,一个治疗方法的包括使用一个或多个药物疗法。
根据本发明的实施例,所述癌症的类型不受特别限制,根据本发明实施例的药物组合物对pd-l1阳性肿瘤细胞的特异性杀伤效果显著。
提高淋巴细胞免疫杀伤能力的方法
在本发明最后一方面,本发明提出了一种提高淋巴细胞免疫杀伤能力的方法。根据本发明的实施例,该方法包括:所述淋巴细胞表前面所述的重组受体。利用根据本发明实施例的上述方法,能够有效提高淋巴细胞对肿瘤细胞的特异性免疫杀伤。
需要说明的是,本发明中所涉及的“重组受体”为重组蛋白或融合蛋白,该重组受体表达在受体细胞(如淋巴细胞)的膜上,发挥受体蛋白的功能,即能与细胞外专一信号分子结合进而激活细胞内一系列生物化学反应,使细胞对外界刺激产生相应的效应。
下面将结合实施例对本发明的方案进行解释。
本领域技术人员将会理解,下面的实施例仅用于说明本发明,而不应视为限定本发明的范围。实施例中未注明具体技术或条件的,按照本领域内的文献所描述的技术或条件(例如参考j.萨姆布鲁克等著,黄培堂等译的《分子克隆实验指南》,第三版,科学出版社)或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
在以下实施例中所用到的细胞系和基本实验技术如下所述:
慢病毒的产生和人t淋巴细胞的转导
目的是产生复制缺陷的慢病毒载体,并将慢病毒载体离心收集用于人t淋巴细胞的转导。
下面简要介绍慢病毒载体的产生、收集的实验过程:将293t细胞铺在底面积为150-平方厘米的细胞培养皿中,并根据说明书,使用express-in(购自openbiosystems/thermoscientific,waltham,ma)对293t细胞进行病毒转导。每盘细胞加入15μg的慢病毒转基因质粒、5μg的pvsv-g(vsv糖蛋白表达质粒)、10μg的pcmvr8.74质粒(gag/pol/tat/rev表达质粒)和174μl的express-in(浓度为1μg/μl)。分别于24小时和48小时收集上清,并使用超速离心机在28,000rpm(离心机转子为beckmansw32ti,购自beckmancoulter,brea,ca)的条件下离心2小时。最后用0.75ml的rpmi-1640培养基对病毒质粒沉淀进行重悬。
从志愿者供体上分离人原代t淋巴细胞。人t淋巴细胞培养在rpmi-1640培养基中并使用抗cd3和cd28的单克隆抗体包被的珠(购自invitrogen,carlsbad,ca)进行刺激激活。人t淋巴细胞激活后的18~24小时,采用自旋-接种的方法对t淋巴细胞进行转导,转导过程如下所述:在24-孔板中,每孔铺有0.5×106t淋巴细胞,向每孔细胞中加入0.75ml的上述重悬的病毒上清和polybrene(浓度为8μg/ml)。细胞和病毒质粒的混合液在台式离心机(购自sorvallst40;thermoscientific)中离心,离心条件是室温,2500rpm,时间为90分钟。人重组白细胞介素-2(il-2;购自novartis,basel,switzerland)每隔2~3天加入t淋巴细胞培养液中,il-2的终浓度为100-iu/ml,在t淋巴细胞培养过程中,保持细胞的密度为0.5×106~1×106/ml。一旦被转导的t淋巴细胞出现休眠,例如细胞生长速度变慢和细胞变小,其中,细胞生长速度和大小是通过coultercounter(购自beckmancoulter)评估的,或被转导的t淋巴细胞在某个计划的时间点上,t淋巴细胞即可用来做功能分析。
本申请的实施例中所用的流式细胞仪为bdfacscantoii(购自bdbiosciences),并且流式细胞分析数据使用flowjoversion7.2.5软件(购自treestar,ashland,or)进行分析。
抗体依赖性细胞介导的细胞毒作用(adcc)
在以下实施例中,采用4小时-51cr-释放法评估抗-egfr抗体诱导表达无功能egfr受体的淋巴细胞的细胞依赖性裂解的能力。被转导了慢病毒载体的人类t淋巴细胞被用作靶细胞。100μcina251cro4(购自gehealthcarelifesciences,marlborough,ma)标定2~5x106靶细胞,标定条件是37℃下震荡孵育1小时。细胞采用pbs润洗三次,并且用培养基重悬(细胞密度是1x105/ml)。继而,被标定的细胞铺在96-孔板中(每孔铺有5×103个细胞,加有50μl培养基),并加入50μl的抗-egfr抗体(购自erbitux,genentech)(终浓度为20μg/ml),在常温条件下预培养30分钟.继而将含有抗体的培养基换成普通培养基,由此来检测51cr的自发释放。加入终浓度为1%的tritonx-100以保证51cr的最大释放量。在以下具体实施中,人pbmc(效应细胞)加入孔板中(每孔5×105个细胞)并将细胞在37℃培养过夜。第二天,收集细胞上清,并利用γ计数器计算cpm以此来确定51cr的释放。细胞毒性比例用以下公式计算:%特异性裂解=(实验释放cpm数据-自发释放cpm数据)/(最大释放cpm数据-自发释放cpm数据)*100,其中,最大释放cpm数据通过靶细胞中加入tritonx-100实现的,自发释放cpm数据是在没有抗egfr抗体和效应细胞的条件下测量的。
铬释放实验
实施例中应用4–小时51铬释放法分析评估重组受体t细胞的细胞毒活性。具体步骤如下:目标测试细胞用51cr在37摄氏度下标记1小时。标记后,用含有10%胎牛血清(fcs)的rpmi培养基润洗细胞。润洗后,将细胞重悬在相同的培养基中,重悬细胞的浓度是1×105/ml。转导后t细胞以不同的效靶细胞比值(e:t)加入目标测试细胞悬浮液中,并将细胞种在96-孔中,每孔体积是200微升。将细胞在37度培养箱中培养4小时。4小时后,从每孔中取出30微升的上清放于计数器的96-微孔板进行计数分析。分析仪器是顶级计数nxt微闪烁计数器(购自packardbioscience)。所有计数孔中效应细胞的数目是基于t细胞总数来计算的。被标记的目标测试细胞是pd-l1阳性肿瘤细胞。
实施例1构建共表达无功能egfr受体和pd1-cd28-cd3zeta重组受体的载体
本实施例中,发明人将编码有人pd1胞外片段序列、cd28穿膜及胞内段和t细胞受体组合的ζ-链序列克隆到含有ef-1启动子的慢病毒载体(lentiviralvector)上,克隆过程中,选择的限制性酶切是xbai和noti双酶切,以及noti和xhoi双酶切,通过酶切、连接、筛选和目的质粒的扩增,生成表达重组受体的慢病毒质粒(lv-pd1-cd28-cd3ζ)。包含ires和表达无功能egfr受体的序列被克隆进lv-pd1-cd28-cd3ζ载体质粒,构建成lv-pd1-cd28-cd3ζ-tegfr。图1是慢病毒载体的示意图(其中e表示胞外段;tegfr表示无功能egfr),包含编码pd1-cd28-cd3ζ重组受体的序列,ires、及编码无功能egfr受体序列。编码pd1-cd28-cd3ζ重组受体的序列在启动子ef-1的启动调控下,表达无功能egfr受体的序列作为一个单独的mrna转录单元从ires序列后开始翻译。
另外,将编码有人pd1胞外片段和跨膜段序列、cd28胞内段和t细胞受体组合的ζ-链序列克隆到含有ef-1启动子的慢病毒载体的过程如上所述。
实施例2抗egfr抗体可有效杀伤清除共表达无功能egfr受体和重组受体的t淋巴细胞
在本实施例中,外周血淋巴细胞取自不记名供血者。外周血淋巴细胞通过梯度离心进行分离,梯度离心机为ficoll-hypaque。t淋巴细胞与t细胞激活因子磁珠cd3/cd28(购自invitrogen,carlsbad,ca)在5%co2、37摄氏度下孵育培养72小时,培养基是加有2mmol/l谷氨酰胺,10%高温灭活的胎牛血清(fcs)(购自sigma-aldrichco.)和100u/ml的青霉素/链霉素双抗的rpmi培养基1640(购自invitrogengibcocat.no.12633-012)。激活培养72小时后,用洗液润洗细胞,将磁珠洗去。将t细胞种在铺有重组纤连蛋白片段(fnch-296;retronectin)细胞培养皿上,并用慢病毒转导,转导慢病毒分别为lv-pd1-cd28-cd3ζ-tegfr,lv-pd1-cd28-cd3ζ或空载(lv-gfp)转导过程如前所述。转导后表达无功能egfr受体的t细胞用抗egfr抗体染色后,然后流式细胞细胞(facs)分离,分离后t细胞培养在rpmi-1640培养基中并用重组人类il-2因子(100ng/ml;购自r&dsystems)进行诱导扩增7-10天,然后作为实验的靶细胞。发明人用adcc检测法测量抗egfr抗体介异的对转导了不同慢病毒的t细胞的杀伤作用,测量方法采用标准4–小时51铬释放法,4–小时51铬释放法如实施例1所述。结果如图2所示。如图2所示,抗egfr抗体可有效介异杀伤共表达pd1-cd28-cd3ζ重组受体和无功能egfr受体的t淋巴细胞,但抗egfr抗体不能介异杀伤只表达pd1-cd28-cd3ζ重组受体的t淋巴细胞,抗egfr抗体不能介异杀伤空载慢病毒转导的t淋巴细胞,统计数据代表三个孔的平均值±sem。
实施例3共表达无功能egfr受体和pd1-cd28-cd3ζ重组受体的t淋巴细胞肿瘤细胞溶解能力
在本实施例中,外周血淋巴细胞通过梯度离心进行分离,梯度离心机为ficoll-hypaque。t淋巴细胞与t细胞激活因子磁珠cd3/cd28(购自invitrogen,carlsbad,ca)在5%co2、37摄氏度下孵育培养72小时,培养基是加有2mmol/l谷氨酰胺,10%高温灭活的胎牛血清(fcs)(购自sigma-aldrichco.)和100u/ml的青霉素/链霉素双抗的rpmi培养基1640(购自invitrogengibcocat.no.12633-012)。激活培养72小时后,用洗液润洗细胞,将磁珠洗去。将t细胞种在铺有重组纤连蛋白片段(fnch-296;retronectin)细胞培养皿上,并用慢病毒转导,转导慢病毒分别为lv-pd1-cd28-cd3ζ-tegfr,lv-pd1-cd28-tegfr(结构如图1所示),lv-tegfr(结构如图1所示),或空载(lv-gfp),转导过程如前所述。转导后的t细胞培养在rpmi-1640培养基中并用重组人类il-2因子(100ng/ml;购自r&dsystems)进行诱导扩增7-10天,然后进行功能测试实验。发明人测量转导了不同慢病毒的t细胞对pd-l1阳性的脑胶质瘤细胞的杀伤作用,效靶细胞比例是10:1或25:1或50:1,测量方法采用标准4–小时51铬释放法,其中,4–小时51铬释放法如前所述。
测试结果如图3所示,图3结果显示:共表达pd1-cd28-cd3ζ受体和无功能egfr受体的慢病毒转导的t淋巴细胞(lv-pd1-cd28-cd3ζ-tegfrt淋巴细胞)能够显著杀死pd-l1+的脑瘤细胞。共表达pd1-cd28受体(没有连接cd3zeta链片段)和无功能egfr受体的慢病毒转导的t淋巴细胞(lv-pd1-cd28-tegfrt淋巴细胞)无明显杀伤pd-l1+的脑瘤细胞作用。仅表达无功能egfr受体的慢病毒转导的t淋巴细胞(lv-tegfrt淋巴细胞)或空载慢病毒转导的t淋巴细胞(对照lv-gfpt淋巴细胞)对pd-l1+脑瘤细胞无明显杀伤作用。
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
- 还没有人留言评论。精彩留言会获得点赞!