具有荧光性能的金属‑有机框架材料的合成方法及其应用与流程
本发明属于涉及农药残留检测领域,具体涉及一种具有荧光性能的金属-有机框架材料(MOFs)的合成方法,还涉及一种所述金属-有机框架材料(MOFs)在检测农药残留上的应用。
背景技术:
对硫磷(O,O-二乙基-O-(4-硝基苯基)硫代磷酸酯),是一种广谱高毒的有机磷酸酯类杀虫、杀螨剂,对硫磷对人畜的毒性高,且在食品和蔬菜中的残留量季节性超标情况较多,使得中毒事件常有发生,广泛使用对硫磷会对人类和环境造成危害。因此,很多国家和地区已禁用对硫磷,并将其列为作物农药残留的重要检测对象。
目前现有技术中对对硫磷的传统的分析方法包括气相色谱法、高压液相色谱法和薄层层析法等。这些方法往往需要复杂的提取和净化程序,其测定也需要贵重的分析仪器,难以用来进行大量样品的常规检测。
基于材料荧光性质的分析检测方法以其高灵敏性、高选择性、高稳定性等特点日益受到关注。金属-有机框架材料(Metal-Organic Frameworks,MOFs)因其独特的组成、可设计剪裁的结构和丰富的主-客体相互作用而成为荧光检测材料的研究热点之一。本发明正是利用了具有良好荧光性能的MOFs材料,并研究了其制备方法以及对对硫磷的荧光检测用途。
技术实现要素:
本发明针对现有检测方法中提取和净化程序复杂,且测定所需的分析仪器贵重等缺点,提供一种具有荧光性能的金属-有机框架材料(MOFs)的合成方法以及利用所述金属-有机框架材料(MOFs)快速简便地进行农药残留检测的应用。
本发明提供的技术方案如下:
本发明提供了一种具有荧光性能的金属-有机框架材料(MOFs)的合成方法,步骤如下:
步骤1、取具有大共轭结构的卟啉、1,2,4,5-四(4-羧基苯基)苯和Zn(NO3)2·6H2O于烧杯中,再加入N,N-二甲基甲酰胺(DMF),超声使其混合成均匀分散液;
步骤2、将混合均匀的所述分散液倒入反应釜,在温度100~120℃下反应24~48h;
步骤3、将步骤2反应后的产物离心去除上层液体,加入乙醇重复离心洗涤3次以上;
步骤4、将步骤3反应后的产物在温度60-100℃下干燥12-24h,即可得到红棕色MOFs固体粉末。
所述步骤1中,所述具有大共轭结构的卟啉优选中-四-(4-羧基苯基)卟吩;所述中-四(4-羧基苯基)卟吩:1,2,4,5-四(4-羧基苯基)苯:Zn(NO3)2·6H2O的质量比为(150~180):(200~250):(100~150),所述质量比优选为160:223:131;所述N,N-二甲基甲酰胺的加入量为34mL;所述超声的时间为10~20min,优选为15min。
所述步骤2中,所述温度优选为110℃,所述反应的时间优选为32~40h,最优选为36h。
所述步骤3中,所述离心的转速为6000~10000r/min,优选为8000r/min;所述离心的时间为4~6min,优选为5min。
所述步骤4中,所述温度优选为70~90℃,最优选为80℃;所述干燥的时间为16~20h,最优选为18h。
本发明合成了一种金属-有机框架材料(MOFs),经大量实验研究,本发明发现本材料具有良好的荧光性能,且该荧光信号能够特异性的被对硫磷猝灭;另外其荧光淬灭程度与对硫磷的量有关,加入的对硫磷越多,荧光猝灭也越明显,且其荧光强度与对硫磷浓度的对数呈现线性关系。
利用上述性能,本发明还公开了一种利用合成的所述金属-有机框架材料(MOFs)快速简便地对农药残留中对硫磷检测的应用。
所述金属-有机框架材料的醇溶液中含有锌。
所述应用具有很好的特异性,因为对硫磷含有硝基苯强拉电子基团,与MOFs的大共轭结构卟啉之间产生能量转移,导致荧光淬灭,所以当农药中残留对硫磷就会有很强的荧光淬灭响应。
所述金属-有机框架材料的浓度最为0.4mg·mL-1时,检测取得最优效果。
对农药残留中对硫磷检测包括以下步骤:将待测样品与所述金属-有机框架材料的醇溶液混合后检测荧光强度;根据荧光强度值和预定的标准曲线得到待测样品中对硫磷的浓度;其中,所述标准曲线为荧光强度和对硫磷浓度对数的关系曲线。
所述标准曲线的线性范围为5ppb~1000ppb。
本发明与现有技术相比,具有的优点和有益效果如下:
(1)本发明的MOFs制备方法简便,性能稳定,适用于食品安全中对硫磷残留检测;使用的MOFs这一材料可以提前合成,一次合成的MOFs可多次使用。
(2)本发明利用了对硫磷对MOFs荧光信号特异性的猝灭,当加入的对硫磷越多时,荧光猝灭也越明显;在对硫磷浓度在5ppb到1000ppb内,荧光强度与对硫磷浓度的对数成反比,实现了对硫磷的高灵敏高特异性检测;并且检测步骤简单快捷,仅需要几秒钟的时间,无需训练有素的专业人员操作,适用于现场检测;检测过程均是在均相中实现的,反应速度快,降低了操作的复杂程度,实现了对硫磷快速、简便、灵敏的检测。
(3)本发明的实验中仅利用MOFs这一试剂,避免了因繁琐的实验操作带来的很多干扰因素。
附图说明
图1为MOFs在不同物质溶液中的荧光响应强度图;
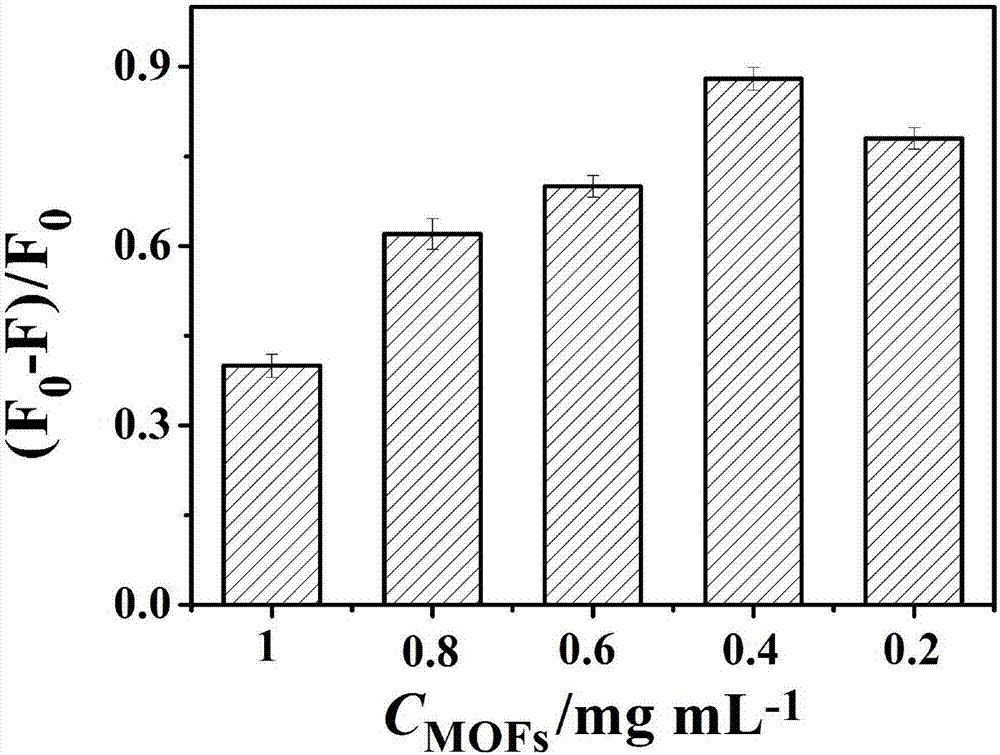
图2为不同浓度的MOFs在相同浓度对硫磷的标准溶液中荧光响应强度和信噪比图;
图3A为MOFs在不同浓度的对硫磷标准溶液中的荧光响应强度图;图3B为发射峰395nm处MOFs在不同浓度的对硫磷标准溶液中荧光强度(F)与对硫磷标准溶液浓度(C)的对数的标准曲线;
图4为不同种类农药对MOFs的荧光响应强度的干扰;
图5为本发明合成方法制备的MOFs的热重分析图;
图6为本发明合成方法制备的MOFs和在乙醇中重溶的MOFs的XRD图;
具体实施方式
为了加深对本发明的理解,下面将结合附图和具体实施例对本发明的合成方法和对农药残留的检测方法作进一步详细的说明:
一种具有荧光性能的金属-有机框架材料(MOFs)的合成方法,步骤如下:
实施例1
步骤1、取中-四(4-羧基苯基)卟吩160mg或0.201mmol、1,2,4,5-四(4-羧基苯基)苯223mg或0.399mmol和Zn(NO3)2·6H2O 131mg或0.440mmol于烧杯中,再加入N,N-二甲基甲酰胺34mL,超声15min使其混合成均匀分散液;
步骤2、将步骤1所述的分散液倒入反应釜,在温度110℃下反应36h;
步骤3、将步骤2反应后的产物离心去除上层液体,加入乙醇重复离心洗涤3次以上;所述转速为8000r/min,所述转速时间为5min;
步骤4、将步骤3反应后的产物在温度80℃下干燥18h,即可得到红棕色MOFs固体粉末。
实施例2
步骤1、取中-四(4-羧基苯基)卟吩160mg或0.201mmol、1,2,4,5-四(4-羧基苯基)苯223mg或0.399mmol和Zn(NO3)2·6H2O 131mg或0.440mmol于烧杯中,再加入N,N-二甲基甲酰胺34mL,超声15min使其混合成均匀分散液;
步骤2、将步骤1所述的分散液倒入反应釜,在温度100℃下反应24h;
步骤3、将步骤2反应后的产物离心去除上层液体,加入乙醇重复离心洗涤3次以上;所述转速为6000r/min,所述转速时间为4min;
步骤4、将步骤3反应后的产物在温度60℃下干燥12h,即可得到红棕色MOFs固体粉末。
实施例3
步骤1、取中-四(4-羧基苯基)卟吩160mg或0.201mmol、1,2,4,5-四(4-羧基苯基)苯223mg或0.399mmol和Zn(NO3)2·6H2O 131mg或0.440mmol于烧杯中,再加入N,N-二甲基甲酰胺34mL,超声15min使其混合成均匀分散液;
步骤2、将步骤1所述的分散液倒入反应釜,在温度120℃下反应48h;
步骤3、将步骤2反应后的产物离心去除上层液体,加入乙醇重复离心洗涤3次以上;所述转速为10000r/min,所述转速时间为6min;
步骤4、将步骤3反应后的产物在温度100℃下干燥24h,即可得到红棕色MOFs固体粉末。
一种具有荧光性能的金属-有机框架材料(MOFs)在对农药残留中对硫磷的快速检测上的应用,所述快速检测的检测方法步骤如下:
步骤1、称取0.4mg上述实施例1制备的MOFs于2mL的离心管中,加入1mL无水乙醇,配置成0.4mg·mL-1的MOFs分散液;
步骤2、取100ppm的对硫磷标准溶液,以无水乙醇为溶剂,配置10ppm的对硫磷标准溶液;
步骤3、向编号为A1、A2、A3、A4的96微孔板中均加入0.4mg·mL-1的MOFs溶液90μL,再分别向孔A1中加入乙醇10μL,向孔A2中加入10ppm的对硫磷标准溶液10μL,向孔A3中加入40ppm的速灭威10μL,向孔A4中加入16ppm的辛硫磷溶液10μL,采用酶标仪检测325nm~500nm波长范围下的荧光光谱并对荧光强度大小进行比较;得到在395nm处出,荧光光谱达到最大峰值。
孔A1、A2、A3、A4的荧光对比如附图1所示,曲线a为不加入任何农药时的荧光响应,曲线b是加入对硫磷时的荧光响应,曲线c是加入速灭威时的荧光响应,曲线d是加入辛硫磷时的荧光响应。结果表明,当没有农药时,MOFs的荧光强度最强,最强的峰处于395nm处;当有速灭威或辛硫磷等杀虫剂或农药成分时,MOFs的荧光强度略微有减弱,即当用其他农药代替对硫磷时,MOFs的荧光响应不会受到太大影响;当对硫磷的最终浓度是1ppm时,MOFs的荧光被猝灭。
1)相同对硫磷浓度环境下,MOFs的浓度对其荧光响应强度和信噪比的影响
步骤1、称取1mg上述实施例1制备的MOFs于2mL的离心管中,加入1mL无水乙醇,配置成1mg·mL-1的MOFs溶液,再分别稀释成浓度为0.8mg·mL-1,0.6mg·mL-1,0.4mg·mL-1,0.2mg·mL-1的MOFs分散液,并对应编号为B1/C1、B2/C2、B3/C3、B4/C4、B5/C5;
步骤2、取100ppm的对硫磷标准溶液,以无水乙醇为溶剂,配置10ppm的对硫磷标准溶液;
步骤3、向编号为B1、C1的96微孔板中加入1mg·mL-1的MOFs 90μL,向B2、C2的96微孔板中加入0.8mg·mL-1的MOFs 90μL,向B3、C3的96微孔板中加入0.6mg·mL-1MOFs 90μL,向B4、C4的96微孔板中加入0.4mg·mL-1的MOFs 90μL,向B5、C5的96微孔板中加入0.2mg·mL-1的MOFs90μL,向孔B1、B2、B3、B4、B5中加入乙醇10μL,向孔C1、C2、C3、C4、C5中加入10ppm的对硫磷标准溶液10μL,采用酶标仪检测275nm激发波长下的荧光光谱,记录最大荧光发射峰395nm左右的荧光强度;
步骤4、设不加对硫磷时的荧光响应是F0,加对硫磷时的荧光响应是F,计算每个编号离心管中MOFs对应的(F0-F)/F0值,可以找出能使空白响应信号差距最大的MOFs浓度。
其结果如附图2所示,从图2中可以看出,当浓度为0.4mg·mL-1时,MOFs的信噪比最高;当浓度为0.2mg·mL-1时,MOFs的信噪比次之;当浓度为1mg·mL-1时,MOFs的信噪比最低。
2)不同浓度的对硫磷对MOFs的荧光响应强度的影响
步骤1、称取0.4mg上述实施例1制备的MOFs于2mL的离心管中,加入1mL无水乙醇,配置成0.4mg·mL-1的MOFs分散液;
步骤2、取100ppm的对硫磷标准溶液,以无水乙醇为溶剂,配置10ppm的对硫磷标准溶液;
步骤3、向编号为D1、D2、D3、D4、D5、D6、D7、D8、D9、D10、D11、D12的96微孔板中均加入0.4mg·mL-1的MOFs分散液90μL,再依次分别加入10μL初始浓度为10ppm,7.5ppm,5ppm,2.5ppm,1ppm,0.75ppm,0.5ppm,0.25ppm,0.1ppm,75ppb,50ppb的对硫磷标准溶液以及10μL的乙醇,采用酶标仪检测275nm激发波长下的荧光光谱,记录最大荧光发射峰395nm左右的荧光强度。
其结果如附图3所示,附图3A中a-l分别对应的对硫磷标准溶液终浓度为1000ppb,750ppb,500ppb,250ppb,100ppb,75ppb,50ppb,25ppb,10ppb,7.5ppb,5ppb,0ppb;实验发现,荧光强度随对硫磷标准溶液浓度的增大而降低。
从附图3B中可以看出,在对硫磷标准溶液浓度在5ppb到1000ppb内,发射峰395nm处荧光强度与对硫磷标准溶液浓度的对数成反比,荧光强度(F)与对硫磷标准溶液浓度(C)的关系是:F=-3110.04logC+10344.27,其线性相关系数是0.988;当对硫磷标准溶液浓度低于5ppb时,荧光强度变化不明显,到达检测下限。
3)不同种类农药对MOFs的荧光响应强度的干扰
步骤1、称取0.4mg上述实施例1制备的MOFs于2mL的离心管中,加入1mL无水乙醇,配置成0.4mg·mL-1的MOFs分散液;
步骤2、取100ppm的对硫磷标准溶液,以无水乙醇为溶剂,配置10ppm的对硫磷标准溶液;
步骤3、向编号为E1、E2、E3、E4、E5、E6、E7、E8、E9、E10、E11、E12、F1、F2、F3、F4的96微孔板中均加入0.4mg·mL-1的MOFs溶液90μL,再依次分别加入10μL的乙醇、对硫磷(10ppm)、杀虫双(40ppm)、仲丁威(40ppm)、速灭威(40ppm)、异丙威(40ppm)、4-氯苯氧乙酸钠(40ppm)、多菌灵(16ppm)、氟啶脲(16ppm)、甲维盐(16ppm)、甲拌磷砜(16ppm)、辛硫磷(16ppm)、啶虫脒(16ppm)、3-羟基克百威(16ppm)、咪鲜胺(16ppm)、甲霜灵(100ppm)(分别对应附图4中的a-p),采用酶标仪检测275nm激发波长下的荧光光谱,记录最大荧光发射峰395nm左右的荧光强度。
其结果如附图4所示,从图4中可以看出,对硫磷可猝灭MOFs的荧光,而其他的农药则不能猝灭MOFs的荧光,表明对硫磷对MOFs的荧光响应强度的影响具有良好的特异性。
4)MOFs对农田污水中对硫磷的加标检测应用
步骤1、称取0.4mg上述实施例1制备的MOFs于2mL的离心管中,加入1mL无水乙醇,配置成0.4mg·mL-1的MOFs分散液;
步骤2、取5支离心管分别编号为1-5,将农田污水样品仅以无水乙醇稀释十倍而没有做其他预处理形成农田污水的预处理液,以所述农田污水的预处理液为溶剂,分别将对硫磷溶液加入到农田污水样品中配置一系列浓度分别为1000ppb,750ppb,500ppb,250ppb,100ppb的对硫磷标准溶液;
步骤3、向编号为G1、G2、G3、G4、G5的96微孔板中均加入0.4mg·mL-1的MOFs分散液90μL,再依次分别加入添加有农药的样品和乙醇10μL,G1~G5对硫磷的标准溶液终浓度分别为100ppb、75ppb、50ppb、25ppb、10ppb,采用酶标仪检测275nm激发波长下的荧光光谱,记录最大荧光发射峰395nm左右的荧光强度;
其荧光及回收率的检测结果列于表1,如表1中可以看出,本方法可以有效检测农田污水样品中的对硫磷浓度,并且编号G1~G5均取得了很好的回收率,回收率平均达到95%以上,通过未加入农田污水前原始对硫磷标准溶液与测定农田污水样品中对硫磷浓度的衡量对比,说明本检测应用具有广阔的潜在应用前景;所述回收率=本方法测定的浓度/加标浓度;所述加标浓度是指未加入农田污水前对硫磷标准溶液的浓度(ppb);所述测定的浓度是指添加农田污水后样品中对硫磷的浓度(ppb),可成功用于实际农田污水的检测。
表1
表1:对硫磷的实际样品检测
5)MOFs的热稳定性表征
为研究该MOFs材料的热稳定性,对实施例1制备的MOFs材料进行热重表征,所述热重的实验条件:温度0-600℃,氮气气氛下以10℃/min的速度升温;实验结果如附图5所示,所述MOFs材料在410℃下有较好的稳定性,即重量>实验前重量的90%;410-525℃时,失重明显;升温至600℃失重至实验前重量的48.7%。
6)MOFs在乙醇中的稳定性表征
为进一步探究MOFs材料的晶型结构以及在乙醇中的稳定性,对实施例1制备和在乙醇中重溶的MOFs材料进行了XRD的表征,扫描区间:5°<2θ<50°。所述重溶的步骤:将实施例1制备的MOFs材料分散在乙醇中24h,离心去除上层清液后干燥。
实验结果如附图6所示,从图6中可以看出,实施例1制备的MOFs为典型的多晶结构,且重溶后没有显示明显的晶型改变,表明了在乙醇中MOFs的结构具有很强的稳定性,同时也说明以乙醇为溶剂对对硫磷进行检测不会对MOFs的结构产生干扰。
最后需要说明的是,上面虽然结合实施例对本发明做了详细的说明,但是上述实施例并非具体实施方式的穷举,上述实施例目的在于说明本发明,而非限制本发明的保护范围,对于本领域的技术人员而言,在不脱离本发明的原理和精神的情况下,可以对这些具体实施方式或实施例进行多种变化、修改、替换和变型,这些不经创造性的劳动而设计出与发明技术方案相同或相似的结构、装置、设备或产品及其制备方法、使用方法和/或用途,均应涵盖在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!