从牛尾蒿中分离槲皮素鼠李糖苷的方法与流程
本发明属于天然植物有效成分提取分离的技术领域。
背景技术
槲皮素3-o-α-l-鼠李糖苷,为黄酮苷类成分,多存在于天然植物中,具有较强的抗氧化作用。其结构式如下:
高速逆流色谱是20世纪80年代年由美国国立卫生院ito博士研发的一种新型的液-液分配色谱技术,利用组分在逆向移动的互不相溶的两相溶剂中分配系数的不同进行分离,是不需要固态吸附剂的全液态色谱分离方法。
目前还未见使用hsccc从牛尾蒿中分离槲皮素3-o-α-l-鼠李糖苷的方法。
技术实现要素:
本发明的目的在于提供一种从牛尾蒿中分离槲皮素3-o-α-l-鼠李糖苷的方法。
具体地,它包括如下操作:
取正己烷-乙酸乙酯-甲醇-水=3:10:3:10v/v充分混合,分层后,上层溶剂和下层溶剂备用;取下层溶剂,溶解牛尾蒿乙酸乙酯提取部位,所得样品溶液通过高速逆流色谱进行分离;
高速逆流色谱的操作如下:
设备温度30~40℃,将上层溶剂以15~25ml/min的流速泵入高速逆流色谱仪,打开主机,待主机正转转速稳定在800~1000rpm后,再以1~3ml/min流速泵入下层溶剂,待两相平衡后,由进样阀注入样品溶液,在254±3nm或280±3nm下检测流出物,并收集出峰时间在30min后的第二段色谱峰。
本发明中所述“溶解牛尾蒿乙酸乙酯提取部位”,是指尽可能充分地溶解,不排除有无法溶解的成分。
进一步地,高速逆流色谱中,温度为35℃。
进一步地,高速逆流色谱中,上层溶剂泵入流速为20ml/min。
进一步地,主机正转转速850rpm。
进一步地,下层溶剂泵入的流速为2ml/min。
进一步地,收集出峰时间在40min后的第二段色谱峰。
进一步地,所述第二段色谱峰收集时间为出峰时间75~95min,更进一步选自80~91min。
进一步地,所述牛尾蒿乙酸乙酯提取部位,是通过如下方法制备得到:
取牛尾蒿,以水、c1-c2的醇类溶剂中的一种或两种以上的混合溶液作为溶剂进行提取,提取物再采用乙酸乙酯提取,收集乙酸乙酯提取物,即得乙酸乙酯提取部位。
c1-c2的醇类溶剂,目前为甲醇、乙醇。
更进一步地,提取牛尾蒿所用溶剂为水和c1-c2的醇类溶剂的混合溶液。
其中,混合溶液中,醇类溶剂的浓度为10~30%v/v;进一步选自20%;优选地,所述醇类溶剂选自乙醇。
更进一步地,提取物采用乙酸乙酯提取前,依次用石油醚、二氯甲烷提取。
本发明一个具体实施方式中,采用乙酸乙酯、石油醚、二氯甲烷进行提取,是指萃取。
本发明采用hsccc可以较为方便、快捷地从牛尾蒿中提取分离出纯度在90%以上的槲皮素3-o-α-l-鼠李糖苷,为该化合物的制备提供了新的途径。
后续使用时,如果还需要提高该化合物的纯度,可以采用已知方法进行纯化,例如柱层析、制备色谱、重结晶等方法。
附图说明
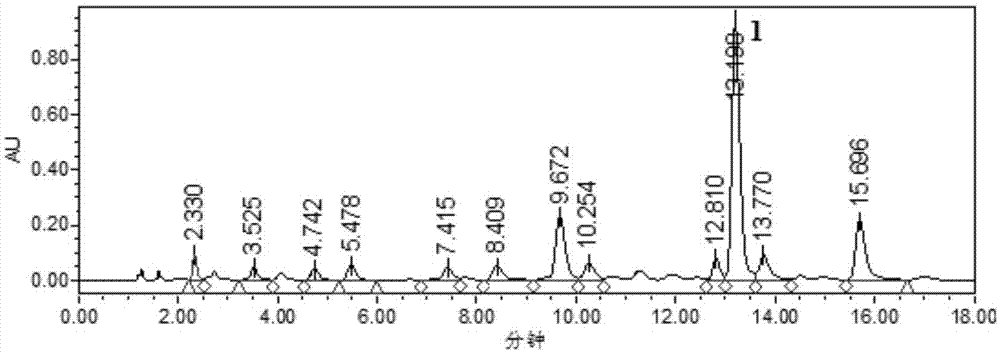
图1乙酸乙酯部位uplc色谱图(1为目标化合物)
图2正己烷-乙酸乙酯-甲醇-水(3:10:3:10,v/v)体系高速逆流色谱图
具体实施方式
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
实施例1
仪器
tbe-300b型hsccc(上海市同田生物技术股份有限公司);dc-0506型低温恒温槽(上海市同田生物技术股份有限公司);
材料与试剂
牛尾蒿药材于2013年7月3日自采于四川省阿坝藏族羌族自治州松潘县水晶乡川盘村(川主寺药泉山庄,海拔3300米),经阿坝藏族羌族自治州藏医院华尔江主任医师、西南民族大学刘圆教授鉴定为菊科蒿属植物牛尾蒿artemisiasubdigitatamattf.的地上部分,粉碎,过3号筛,备用;水为纯净水;试剂为分析纯。
1、方法与结果
1.1样品的制备
取牛尾蒿药材粉末20g,加入20%乙醇1000ml,回流提取1h,过滤,减压浓缩至无醇味,加适量水混悬,依次用石油醚、二氯甲烷、乙酸乙酯和正丁醇萃取,减压浓缩后经冷冻干燥得各极性部位。取乙酸乙酯部位进行hsccc的分离。
1.2uplc分析条件
色谱柱:acquity
表1梯度洗脱程序
1.3乙酸乙酯部位的uplc检测
取乙酸乙酯部位样品,加入适量50%甲醇,超声充分溶解后,0.25μm滤膜过滤得样品溶液,按1.2液相条件进样检测,检测波长254nm。色谱图如图1所示。
1.4hsccc分配系数的测定
利用uplc测定样品在不同溶剂体系中的分配系数。于10ml试管中加入适量乙酸乙酯萃取物,加入预先分配平衡的两相溶剂系统的上相和下相各5ml,振荡使充分混合溶解,待静置分层后,分别取上相和下相各2ml,旋蒸挥去溶剂后用等量50%甲醇溶解,经uplc检测后得到上相中目标化合物的峰面积au,下相中目标化合物的峰面积al,分配系数则为k=au/al。
选取不同溶剂体系,用上述方法测定目标化合物分配系数,结果见表2。
表2目标化合物在个溶剂体系下的分配系数
1.5两相溶剂体系及样品溶液的制备
选取正己烷-乙酸乙酯-甲醇-水(3:10:3:10,v/v)作为hsccc的溶剂体系,将各溶剂组分按体积比例加入2l分液漏斗中,剧烈摇晃使其充分混合,待静置过夜,分别取上相、下相于广口瓶中,加盖超声脱气20min后备用。取牛尾蒿提取物乙酸乙酯部位200mg,加入20ml下相超声使其充分溶解,过滤备用。
1.6hsccc的分离制备过程
开启低温恒温循环装置,设置温度35℃,待温度恒定以后,将已超声脱气的上相(固定相)以20ml/min的流速泵入hsccc仪的螺旋管(上相流出约80ml后停泵),打开hsccc主机,缓慢调节转速至850rpm,待主机正转稳定后,再以2ml/min泵入下相(流动相),待两相平衡后,由进样阀注入已经准备好的20ml样品溶液,通过检测器(254nm)检测流出物,按照色谱图手动收集各色谱峰组分。色谱图见图2。
1.7纯度分析与结构鉴定
利用uplc分析所接样品组份,判断其纯度,利用uv、ir、uplc-ms、1h-nmr、13c-nmr对所得产物进行结构分析。
1.7.1纯度分析
取适量分离得到的化合物,50%甲醇溶解进样,按色谱条件检测,纯度达到93.20%。
1.7.2化合物结构鉴定
根据ir、uv、esi-ms、1h-nmr和13c-nmr的数据来确定目标化合物的化学结构,具体数据如下:
黄色粉末。esi-ms(m/z):449.1350[m+h]+、447.3154[m-h]-,推出分子量为448,结合1h-nmr和13c-nmr推测其分子式为c21h20o11,ω=12。
红外光谱ir(kbr)v(cm-1):3414.87(宽,羟基),1663.69(c=o),1613.51、1454.02(芳环),1092.02(c-o),716.99(苯环三取代)。
核磁共振氢谱1h-nmr(400mhz,dmso-d6)δppm:12.66(s,1h,oh-5),9.52(br,2h),7.29(s,1h,h-2′),7.25(d,j=8.4hz,1h,h-6′),6.86(d,j=8.3hz,1h,h-5′),6.38(s,1h,h-8),6.20(s,1h,h-6),5.25(s,1h,h-1″),3.97(s,1h),3.18(dt,j=18.6,7.1hz,3h),0.81(d,j=5.7hz,3h,ch3-)。
核磁共振碳谱13c-nmr(100mhz,dmso-d6)δppm:156.50(c-2),134.23(c-3),177.77(c-4),161.33(c-5),98.79(c-6),164.41(c-7),93.71(c-8),157.33(c-9),104.07(c-10),120.75(c-1′),115.68(c-2′),145.26(c-3′),148.51(c-4′),115.51(c-5′),121.16(c-6′),101.85(c-1″),70.38(c-2″),70.66(c-3″),71.21(c-4″),70.11(c-5″),17.57(c-6″)。
以上数据鉴定目标化合物为槲皮素3-o-α-l-鼠李糖苷(quercetin3-o-α-l-rhamnopyranoside),结构式如下
2、小结
试验釆用的高速逆流色谱仪所配置的检测器有两个波长:254nm和280nm,对牛尾蒿20%乙醇提取物的乙酸乙酯萃取部位用uplc进行全波长扫描,选取254nm和280nm两个波长下的uplc色谱图比较,发现在254nm时目标化合物吸收强度较大,且峰型较好,故确定254nm为hsccc分离的检测波长。在设定的条件下,分离得到一个化合物单体,并通过uv、ir、ms及nmr等方法对其进行结构鉴定,确定为槲皮素3-o-α-l-鼠李糖苷。
- 还没有人留言评论。精彩留言会获得点赞!