假单胞菌zjut126及在生产L-草铵膦中的应用的制作方法
本发明涉及一株假单胞菌(pseudomonassp.)zjut126及在生物催化领域的应用,该菌株具有高手性选择性拆分外消旋n-癸酰-(d,l)-草铵膦生产l-草铵膦的能力。用简单的萃取法,就可以从反应混合物中分离得到高纯度的l-草铵膦。
背景技术:
随着环保观念的加强和可持续发展战略的实施,高效、低毒、高活性、低残留已成为农药发展的必然趋势。一些手性化合物的不同对映体往往表现出不同活性。比如一种对映体活性是高效,另一种对映体却是低效甚至起相反的作用。草铵膦是一种高效、低毒、非选择性(灭杀性)触杀型除草剂,也是一种手性农药,只有l型草铵膦具备植物毒性。市售的草铵膦多为外消旋体。若能以单一的l-构型的形式投入使用,不仅可以提高产品药效,而且其使用量可以降低一倍。随着国家农药减量增效政策的实施,绿色生物农药成为研究热点,高光学纯度的l-草铵膦具有广阔的市场前景。
单一对映异构体可以由化学、生物法等合成。生物催化法优于化学法的优点是:酶(或细胞)催化反应通常有高的立体选择性和区域选择性,而且在温和的条件下进行,可以避免使用严酷的条件,从而避免副反应的发生。此外,生物催化法可以减少对环境污染,节省成本,符合当今绿色化学发展趋势。
目前工业上合成l-草铵膦的方法是化学法,例如日本的明治制果公司和中国永农生物科技有限公司合作开发的酮酸不对称加氢合成l-草铵膦的技术。但是化学方法能耗高而且污染严重。鉴于生物催化反应条件比较温和、立体选择性高、污染少等特点,未来生物法生产l-草铵膦将更有前景。本发明就是筛选生物法生产l-草铵膦的微生物细胞催化剂,将外消旋的n-癸酰-(d,l)-草铵膦立体选择性水解,生成l-草铵膦。
美国专利us6,686,181b1(2004)报道了一种酶法生产l-草铵膦的方法。该酶是从能水解n-乙酰-(d,l)-氨基酸的氨基酸酰基转移酶中筛选出来的,它能立体选择性水解n-乙酰-(d,l)-草铵膦(注:草铵膦是一个非蛋白氨基酸)产生l-草铵膦,选择性接近100%。美国专利us4,226,941(1980)报道了几种微生物菌种及其所含胞内酰基转移酶立体选择性水解n-短链脂肪酰-(d,l)-草铵膦生产l-草铵膦的方法,选择性接近100%。这些短链脂肪酰包括乙酰、丙酰和丁酰等,菌种的催化水解活性与脂肪酰的长度相关,随着链长的增加,细胞催化活性逐渐下降。当底物中酰基供体的链长增加2个,即从乙酰变成丁酰,细胞催化活性下降一半以上。该专利用于分离水解混合物得到纯l-草铵膦的方法是,用强酸性离子交换柱将混合物中未反应的n-短链脂肪酰-d-草铵膦,以及水解生成的短链脂肪酸和l-草铵膦分开。这三种物质水溶性都较好,不能用简单的方法(如萃取)分开,只能用操作复杂、成本高昂的离子交换法分离。由于分离成本在一个完整的产品生产工艺中往往占大头,所以本发明在发明起始的时候就考虑降低l-草铵膦分离的成本。方法是筛选能立体选择性水解n-长链脂肪酰-(d,l)-草铵膦的菌种,因水解混合物中未反应的n-长链脂肪酰-d-草铵膦,以及水解生成的长链脂肪酸和l-草铵膦这三种物质,只有l-草铵膦易溶于水,另外两种物质(因为含长链脂肪酰)都难溶于水,因此用萃取的方法可以简单地将它们分开。
技术实现要素:
本发明目的是提供一种具有很好立体选择性的菌株——假单胞菌(pseudomonassp.)zjut126及其在选择性水解n-长链脂肪酰-(d,l)-草铵膦(即n-癸酰-(d,l)-草铵膦)生成l-草铵膦中的应用。先将外消旋的(d,l)-草铵膦化学酰化得到外消旋的n-癸酰-(d,l)-草铵膦,再用该菌催化该底物不对称水解生成l-草铵膦。本发明从特定环境样品中,以n-癸酰-(d,l)-草铵膦为唯一碳源,筛选到了目标微生物菌种,该菌种的选择性是l型,即能优先水解n-癸酰-l-草铵膦生成l-草铵膦,不能水解n-癸酰-d-草铵膦,选择性接近100%。
本发明采用的技术方案是:
本发明提供一株新菌株——假单胞菌(pesudomonassp.)zjut126,保藏于中国典型培养物保藏中心,保藏日期为2017年10月30日,保藏编号cctccno:m2017635,保藏地址:中国,武汉,武汉大学,邮编430072。
本发明假单胞菌zjut126筛选方法:以外消旋n-癸酰-(d,l)-草铵膦为唯一碳源,先液体培养来自环境样品中的微生物,进行目标微生物的富集,然后将富集培养物涂布在以n-癸酰-(d,l)-草铵膦为唯一碳源的固体培养基平板上,因为n-癸酰草铵膦为白色,难溶于水,平板呈白色不透明状,当它被降解后会形成透明圈,利用该方法可以快速筛选出目标菌株。
本发明还提供一种所述假单胞菌zjut126在生产l-草铵膦中的应用,具体所述的应用以假单胞菌zjut126经发酵培养获得的湿菌体为催化剂,以外消旋体n-癸酰-(d,l)-草铵膦钠盐为底物,以ph7.5~8.5(优选ph8.0)的磷酸缓冲液为反应介质构成反应体系,在30~35℃、150~200r/min(优选30℃、180rpm)条件下进行草铵膦的拆分反应,反应完全后,获得含(l)-草铵膦和未反应n-癸酰-(d)-草铵膦的反应液,将反应液分离纯化,获得(l)-草铵膦。
进一步,所述催化剂用量以湿菌体重量计为3~8g/l反应体系,优选8g/l反应体系,所述底物n-癸酰-(d,l)-草铵膦加入量为2~10g/l反应体系,优选8g/l反应体系。
进一步,外消旋n-癸酰-(d,l)-草铵膦钠盐的合成方法为:利用癸酰氯和外消旋(d,l)-草铵膦在碱性条件下反应获得n-癸酰-(d,l)-草铵膦钠盐,具体实验操作步骤如下:
(1)向反应器中加入(d,l)-草铵膦铵盐,用质量浓度20%碳酸钠水溶液调节ph到9.0,加热溶解草胺磷,冰浴冷却至0℃,向其中缓慢滴加癸酰氯,优选滴加时间为15分钟;滴加过程中,保持反应体系的温度0℃,并通过滴加质量浓度20%碳酸钠水溶液保持ph在9.0~10.0之间,滴加完后升温至25℃再反应2.5h,获得原溶液;所述草铵膦铵盐与癸酰氯物质的量之比为1:1.2;
(2)将步骤(1)原溶液用盐酸酸化至ph值为1.0~2.0,n-癸酰-(d,l)-草铵膦转化为n-癸酰-(d,l)-草铵膦酸,从而与水溶性杂质分开,结晶,抽滤,滤饼用质量浓度10%氢氧化钠乙醇溶液中和至ph值为7.0,抽滤,所得白色粉末状滤饼,即为n-癸酰-(d,l)-草铵膦钠盐。
进一步,本发明所述湿菌体的制备方法为:
(1)斜面培养:将假单胞菌zjut126接种至斜面培养基,30℃培养2天,获得斜面菌体;所述斜面培养基组成为:k2hpo4·3h2o2.1g/l,kh2po40.4g/l,nacl0.1g/l,mgso4·7h2o0.2g/l,cacl20.025g/l,nh4no30.5g/l、n-癸酰-(d,l)-草铵膦1.0g/l,琼脂20g/l,溶剂为去离子水,ph值自然;
(2)种子培养:将步骤(1)斜面菌体接种至种子培养基,30℃、180rpm培养24h,获得种子液;所述种子培养基组成为:nacl0.5g/l,kh2po40.4g/l,k2hpo41.6g/l,nh4cl1.0g/l,mgso4·7h2o0.2g/l,cacl20.03g/l,n-癸酰-(d,l)-草铵膦1.0g/l,微量元素液10ml/l,用naoh调节ph值为8.0,溶剂为去离子水,ph值自然;微量元素液组成为:cocl20.1g/l,mnso40.5g/l,feso4·7h2o0.1g/l,cuso40.1g/l,znso4·7h2o0.1g/l,h3bo30.01g/l,al(so4)2·12h2o0.01g/l,na2moo4·2h2o0.01g/l,edta·2na1g/l,溶剂为去离子水;
(3)发酵培养:将假单胞菌zjut126菌株种子液以体积浓度10%的接种量接种于发酵培养基,30℃、180rpm培养24h,离心,倒掉上清液,将湿菌体用200mm磷酸盐缓冲液(ph8.0)洗涤3次,获得湿菌体;
所述发酵培养基组成为:nacl0.5g/l,mgso4·7h2o0.2g/l,k2hpo41.6g/l,kh2po40.4g/l,nh4cl5.0g/l,微量元素液10ml/l,葡萄糖5.0g/l,溶剂为去离子水,用naoh调节ph值为8;微量元素液组成:cocl20.1g/l,mnso40.5g/l,feso4·7h2o0.1g/l,cuso40.1g/l,znso4·7h2o0.1g/l,h3bo30.01g/l,al(so4)2·12h2o0.01g/l,na2moo4·2h2o0.01g/l,edta·2na1g/l,溶剂为去离子水。
进一步,本发明反应液分离纯化的方法为:反应结束后,将反应液离心,保留上清液,用盐酸调节ph约6,乙酸乙酯萃取未反应的n-癸酰-(d)-草铵膦,水相离心,去除沉淀,得到l-草铵膦的水溶液,旋蒸浓缩至无液体流出,-30℃冷冻干燥,得到l-草铵膦产品。
与现有技术相比,本发明的优势主要体现在:
本发明首次报道了一株新菌株--假单胞菌pseudomonassp.zjut126,它能选择性水解外消旋n-癸酰-(d,l)-草铵膦生成l-草铵膦,选择性接近100%。此外,本发明采用萃取法分离反应生成的混合物,萃余液经浓缩、冷冻干燥,得到l-草铵膦产品。l-草铵膦萃取分离的收率94.6%,产品中l-草铵膦含量92%,ee值>95.2%。本发明方法成本低,效率高,易于规模化。
附图说明
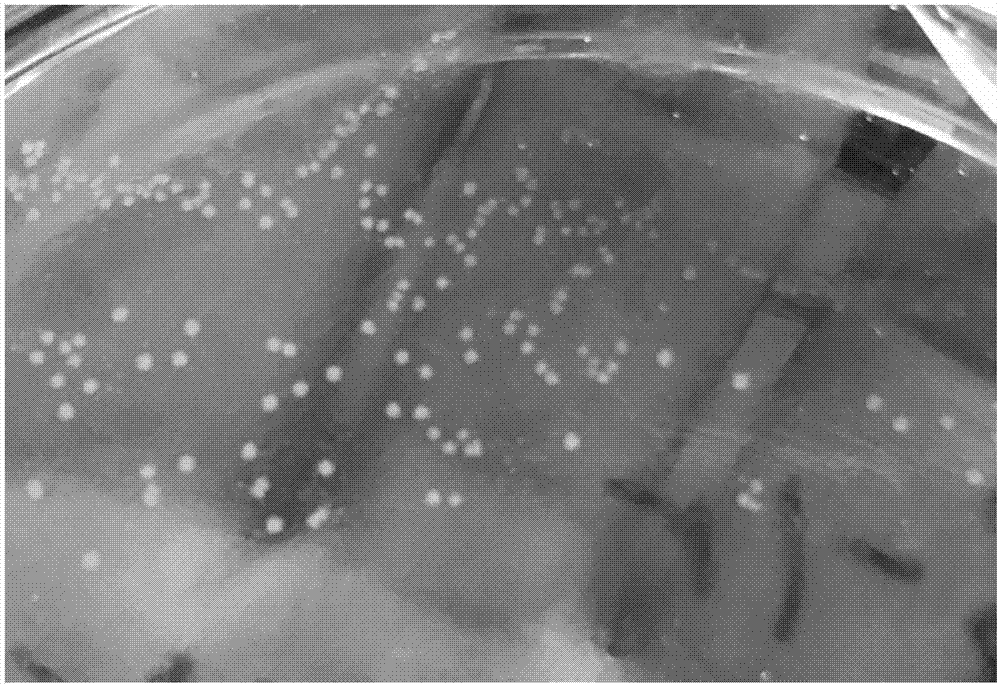
图1为假单胞菌zjut126在固体培养基上培养2d的菌落形态;
图2为显微镜下,假单胞菌zjut126经革兰氏染色后的菌株形态;
图3为假单胞菌zjut126的16srdna系统发育分析树。
具体实施方式
下面结合具体实施例对本发明进行进一步描述:
实施例1外消旋n-癸酰-(d,l)-草铵膦的合成
利用癸酰氯和外消旋(d,l)-草铵膦在碱性条件下反应获得n-癸酰-(d,l)-草铵膦,具体实验操作步骤如下:
(1)向反应器中加入0.1mol(21.5g)(d,l)-草铵膦铵盐,用质量浓度20%碳酸钠水溶液调节ph到9.0,加热溶解草胺磷,冰浴冷却至0℃,向其中缓慢滴加0.12mol癸酰氯,滴加时间为15分钟;滴加过程中,保持反应体系的温度在0℃、并通过滴加质量浓度为20%的碳酸钠水溶液保持ph在9.0~10.0之间,滴加完后升温至25℃再反应2.5h,获得原溶液;
(2)将步骤(1)原溶液用盐酸酸化至ph值为1.0~2.0,n-癸酰-(d,l)-草铵膦转化为n-癸酰-(d,l)-草铵膦酸,从而与水溶性杂质分开,结晶,抽滤,滤饼用质量浓度10%氢氧化钠乙醇溶液中和ph至7.0,抽滤,所得白色粉末状滤饼,即为n-癸酰-(d,l)-草铵膦的钠盐,产物的质量收率为85%。
实施例2假单胞菌(pseudomonassp.)zjut126菌株筛选
1.富集培养:
将水中采集的污泥样品加入到50ml以外消旋n-癸酰-(d,l)-草铵膦为唯一碳源的富集培养基中振荡培养(30℃,180rpm)1周,取5ml上层浊液于50ml新鲜的富集培养基中继续培养1周,重复上述操作,n-癸酰-(d,l)-草铵膦的浓度从0.1g/l用2个月的时间逐渐提高到1g/l。
富集培养基:k2hpo4·3h2o2.1g/l,kh2po40.4g/l,nacl0.1g/l,mgso4·7h2o0.2g/l,cacl20.025g/l,nh4no30.5g/l,微量元素液10ml/l,n-癸酰-(d,l)-草铵膦0.1~1g/l,溶剂为去离子水。
微量元素液组成:cocl20.1g/l,mnso40.5g/l,feso4·7h2o0.1g/l,cuso40.1g/l,znso4·7h2o0.1g/l,h3bo30.01g/l,al(so4)2·12h2o0.01g/l,na2moo4·2h2o0.01g/l,edta·2na1g/l,溶剂为去离子水。配制方法:取1gedta·2na溶于800ml去离子水中,再将其他组分依次加入,最后加水至1l。
2.初筛:
将富集培养物涂布在以外消旋n-癸酰-(d,l)-草铵膦为唯一碳源的固体培养基平板上,30℃培养,因为n-癸酰草铵膦为白色,难溶于水,平板呈白色不透明状,当它被降解后会形成透明圈。
固体培养基组成:k2hpo4·3h2o2.1g/l,kh2po40.4g/l,nacl0.1g/l,mgso4·7h2o0.2g/l,cacl20.025g/l,nh4no30.5g/l、n-癸酰-(d,l)-草铵膦1.0g/l,琼脂20g/l,溶剂为水,调节ph=7.0,115℃灭菌30min。
3.复筛:
选取初筛中有透明圈的菌株接种在复筛液体培养基中,30℃,180r/min培养2天,定期取样进行高效液相色谱分析,得到了一株目标菌株,记为菌株zjut126。
复筛液体培养基:nacl0.5g/l,mgso4·7h2o1.0g/l,k2hpo41.0g/l,nh4no31.0g/l,酵母浸出粉5.0g/l,甘油5.0g/l,cacl20.03g/l,n-癸酰-(d,l)-草铵膦1.0g/l,溶剂为去离子水,ph值自然,115℃灭菌30min。
实施例3菌株zjut126形态学与生理生化鉴定
取以实施例2获得的菌株zjut126接种到固体培养基(见实施例2),显微镜观察,菌落呈圆形,表面凸起,边缘整齐,湿润,乳白色,不透明,随着时间的推移,菌落的颜色形态未见有明显变化,如图1所示。
对菌株zjut126进行革兰氏染色,显微镜下观察,为革兰氏阴性菌,呈短棒状,如图2所示。
菌株zjut126的生理生化鉴定如表1、表2所示,该鉴定利用biolog(genⅲ)自动微生物鉴定系统对菌株进行了94种表型测试,包括71种碳源利用情况检测以及23种化学敏感性检测:将菌株接种于特定的平板培养基,33℃恒温培养2天,用无菌棉签将平板上的菌体洗下,与接种液(if-a)混合,制成菌悬液,用浊度计调整至92%t/if-a。用8孔电动加液器将菌悬液分别加在biologgenⅲ微孔鉴定板的各孔中,每孔100μl。将微孔鉴定板放在33℃培养箱中,分别在培养12h、24h、36h、48h后将其置于biolog读数仪上读取结果。
表1菌株zjut126对biologgenⅲ板上23种化学物质的化学敏感性
注:+表示阳性或利用,-表示阴性或不利用
表2菌株zjut126对biologceniii板上71种碳源的利用能力
注:+表示阳性或利用,-表示阴性或不利用
实施例4菌株zjut126的16srdna分子生物学鉴定
以实施例2获得菌株zjut126送到某生物公司进行16srdna鉴定,测序所得的序列进行处理(去载体、进行拼接)获得较完整的16srdna序列(seqidno.1所示),该序列长度为1484bp。将该序列在ncbi网站上用blast检索后发现它与pseudomonasaeruginosastrainx1506等8个假单胞菌种相似性达到99%(见表3)。该菌株的系统进化树如图3所示,将该菌株命名为假单胞菌(pseudomonassp.)zjut126,保藏于中国典型培养物保藏中心,保藏日期为2017年10月30日,保藏编号cctccno:m2017635,保藏地址:中国,武汉,武汉大学,邮编430072。
表3与菌株zjut126相似度高的物种
实施例5、假单胞菌zjut126湿菌体的制备和催化拆分底物生成l-草铵膦
1、湿菌体的制备
(1)斜面培养
将假单胞菌zjut126接种至斜面培养基,30℃培养2天,获得斜面菌体;所述斜面培养基组成为:k2hpo4·3h2o2.1g/l,kh2po40.4g/l,nacl0.1g/l,mgso4·7h2o0.2g/l,cacl20.025g/l,nh4no30.5g/l、n-癸酰-(d,l)-草铵膦1.0g/l,琼脂20g/l。
(2)种子培养
将步骤(1)斜面菌体接种至种子培养基,30℃培养24h,获得种子液;所述种子培养基组成为:nacl0.5g/l,kh2po40.4g/l,k2hpo41.6g/l,nh4cl1.0g/l,mgso4·7h2o0.2g/l,cacl20.03g/l,n-癸酰-(d,l)-草铵膦1.0g/l,微量元素液10ml/l,用naoh调节ph值为8.0,溶剂为去离子水。微量元素液组成:cocl20.1g/l,mnso40.5g/l,feso4·7h2o0.1g/l,cuso40.1g/l,znso4·7h2o0.1g/l,h3bo30.01g/l,al(so4)2·12h2o0.01g/l,na2moo4·2h2o0.01g/l,edta·2na1g/l,溶剂为去离子水。
(3)发酵培养
将假单胞菌zjut126菌株种子液以体积浓度10%的接种量接种于发酵培养基,30℃、180rpm培养24h,离心,倒掉上清液,将湿菌体用200mm磷酸盐缓冲液(ph8.0)洗涤3次,获得湿菌体。
所述发酵培养基组成为:nacl0.5g/l,mgso4·7h2o0.2g/l,k2hpo41.6g/l,kh2po40.4g/l,nh4cl5.0g/l,微量元素液10ml/l,葡萄糖5.0g/l,溶剂为去离子水,用naoh调节ph值为8。微量元素液组成:cocl20.1g/l,mnso40.5g/l,feso4·7h2o0.1g/l,cuso40.1g/l,znso4·7h2o0.1g/l,h3bo30.01g/l,al(so4)2·12h2o0.01g/l,na2moo4·2h2o0.01g/l,edta·2na1g/l,溶剂为去离子水。
2、制备l-草铵膦
湿菌体催化拆分反应体系100ml,含n-癸酰-(d,l)-草铵膦0.8g,湿菌体0.8g,以磷酸缓冲液(ph=8.0)为反应介质,180r/min,30℃下摇瓶中反应24h,反应液中l-草铵膦的浓度用衍生化高效液相色谱分析,产物l-草铵膦的质量收率为16.3%,对映体过量值eep>99%。
分析前样品处理:样品离心,取上清液500μl与500μl衍生化试剂反应5min后进样。
衍生化试剂:10mg邻苯二甲醛(opa),12mgn-乙酰半胱氨酸(nac),1ml无水乙醇,0.2mol/l硼酸缓冲液ph9.8稀释至5ml,-4℃冰箱保存。
高效液相色谱检测条件:150mmol/l醋酸铵溶液(ph5.6)-甲醇(体积比9:1)为流动相,流速为:1ml/min柱温:35℃;进样量:10微升。荧光检测波长:激发波长350nm发射波长450nm。
产物对映体过量值(ee)和l-草铵膦得率c按以下公式计算:
公式1:
公式2:
式中,eep(%)为产物的对映体过量值,[p]l和[p]d分别为样品中产物l-草铵膦和d-草铵膦的质量含量。c(%)为l-草铵膦收率,cp为产物l-草铵膦的摩尔浓度,cs为剩余的n-癸酰草铵膦摩尔浓度。
实施例6、从实施例5反应结束后的反应液中分离(l)-草铵膦
实施例5反应24h后,将反应液离心,保留上清,用盐酸调节ph约6,乙酸乙酯萃取未反应的n-癸酰草铵膦和生成的癸酸,取水相离心,去除沉淀,得到l-草铵膦的水溶液,旋蒸浓缩至无液体流出,-30℃冷冻干燥,得到l-草铵膦产品。l-草铵膦的萃取分离质量收率94.6%,产品中l-草铵膦含量92%,ee值>95.2%。
序列表
<120>假单胞菌zjut126及在生产l-草铵膦中的应用
<160>1
<170>siposequencelisting1.0
<210>1
<211>1484
<212>dna
<213>假单胞菌(pseudomonassp.)
<400>1
cctggctcagattgaacgctggcggcaggcctaacacatgcaagtcgagcggatgatggg60
agcttgctcccggattcagcggcggacgggtgagtaatgcctaggaatctgcctggtagt120
gggggacaacgtttcgaaaggaacgctaataccgcatacgtcctacgggagaaagcaggg180
gaccttcgggccttgcgctatcagatgagcctaggtcggattagctagttggtggggtaa240
aggcctaccaaggcgacgatccgtaactggtctgagaggatgatcagtcacactggaact300
gagacacggtccagactcctacgggaggcagcagtggggaatattggacaatgggcgaaa360
gcctgatccagccatgccgcgtgtgtgaagaaggtcttcggattgtaaagcactttaagt420
tgggaggaagggcagtaagttaataccttgctgttttgacgttaccaacagaataagcac480
cggctaacttcgtgccagcagccgcggtaatacgaagggtgcaagcgttaatcggaatta540
ctgggcgtaaagcgcgcgtacgtggtttggtaagatggatgtgaaatccccgggctcaac600
ctgggaactgcatcccataactgcctgactagagtacggtagagggtggtggaatttcct660
gtgtagcggtgaaatgcgtagatataggaaggaacaccagtggcgaaggcgaccacctgg720
actgatactgacactgaggtgcgaaagcgtggggagcaaacaggattagataccctggta780
gtccacgccgtaaacgatgtcgactagccgttgggatccttgagattttagtggcgcagc840
taacgcgataagtcgaccgcctggggagtacggccgcaaggttaaaactcaaatgaattg900
acgggggcccgcacaagcggtggagcatgtggtttaattcgaagcaacgcgaagaacctt960
acctggccttgacatgtccggaaccttgcagagatgcgagggtgccttcgggaatcggaa1020
cacaggtgctgcatggctgtcgtcagctcgtgtcgtgagatgttgggttaagtcccgtaa1080
cgagcgcaacccttgtccttagttaccagcacgttatggtgggcactctaaggagactgc1140
cggtgacaaaccggaggaaggtggggatgacgtcaagtcatcatggcccttacggccagg1200
gctacacacgtgctacaatggtcggtacagagggttgccaagccgcgaggtggagctaat1260
cccataaaaccgatcgtagtccggatcgcagtctgcaactcgactgcgtgaagtcggaat1320
cgctagtaatcgtgaatcagaatgtcacggtgaatacgttcccgggccttgtacacaccg1380
cccgtcacaccatgggagtgggttgctccagaagtagctagtctaaccgcaagggggacg1440
gttaccacggagtgattcatgactggggtgaagtcgtaacaagg1484
- 还没有人留言评论。精彩留言会获得点赞!