一种脐带血再生粒子及其制备方法与应用与流程
本发明涉及生物医学技术领域,尤其涉及再生医学、疾病治疗和药物用途等,特别涉及一种脐带血再生粒子及其制备方法与应用。
背景技术:
损伤组织器官的再生与修复,其最终目标是通过再生组织细胞,实现器官功能来达到治愈疾病的目标,再生出来的组织器官需要与个体可以长期共存,因此,对于损伤组织器官再生研究中的核心挑战是开发其能够重构损伤组织器官的细胞并能长期实现其功能的再生组合物。目前用于损伤组织的再生与修复的方法主要有组织器官移植和干细胞治疗技术。
组织器官移植虽可以替换受损或患病的组织,但是受制于供体器官来源有限和移植排斥等。
干细胞治疗技术前景光明,但存在的安全性风险尚待解决:异常的免疫反应(异源细胞的免疫排斥以及异常炎症反应);异常增生和促瘤、致瘤性:即便是已在多国获批的骨髓间充质干细胞也具有危险的致瘤性,研究表明过量使用成体间充质干细胞具有很大致瘤风险,可促进癌症生长转移;异常的分化行为:非目标细胞分化、分化紊乱导致的增生性疾病和肿瘤,或细胞无效、低效分化及提前老化导致的器官修复不全或器官衰竭等退行性疾病;对于基因修饰的干细胞,存在导致基因突变和基因组疾病的风险。相关安全性问题的解决尚有赖技术进步和研究深入。
技术实现要素:
为了克服现有技术的缺点和不足,本发明的首要目的是旨在提供一种脐带血再生粒子的制备方法;第二目的是旨在通过上述制备方法得到脐带血再生粒子;第三目的是提供一种所述脐带血再生粒子在组织细胞再生与修复中的应用。
本发明的目的是采用如下的技术方案来实现的:
一种脐带血再生粒子的制备方法,包含以下步骤:
(1)取脐带血进行离心,离心后分为一级上层溶液和一级下层沉淀;
(2)取一级下层沉淀,加入无菌缓冲液,进行离心,离心后分为二级上层溶液和二级下层沉淀;
(3)取二级下层沉淀,加入无菌红细胞裂解液,置于水平摇床摇动,待完全裂解后进行离心,离心后分为三级上层溶液和三级下层沉淀,三级上层溶液直接弃掉。
(4)取三级下层沉淀,加入无菌缓冲液,剧烈晃动,之后进行离心,离心后分为四级上层溶液和四级下层沉淀,四级下层沉淀直接弃掉。
(5)分别取一级上层溶液、二级上层溶液、四级上层溶液,进行离心,离心后,收集所有沉淀,加入ph值7.0-7.4、含有血清的培养基,置于37℃、5%co2的培养箱中进行培养,每2-3天更换培养基一次。
(6)经培养处理,检测合格后,收集所有培养成分,离心收集脐带血再生粒子。
以上所有步骤均在无菌环境下进行操作。
步骤(1)中所述的脐带血必须是新鲜、无菌、无病原体的。
步骤(1)、(2)中所述的离心,优选的离心力为30g-1000g。
步骤(2)、(4)中所述的无菌缓冲液,可以是现有技术已知的任何一种,优选的是pbs缓冲液。
步骤(2)中所述的取一级下层沉淀,加入无菌缓冲液,优选的是按体积比1:2-10加入无菌缓冲液。
步骤(3)中所述的离心,优选的离心力为500g-5000g。
步骤(3)中所述的无菌红细胞裂解液,可以是现有技术已知的任何一种,优选的是155mmnh4cl或10mmkhco3或0.1mmedta。
步骤(3)中所述的取二级下层沉淀,加入无菌红细胞裂解液,优选的按体积比1:3-10加入无菌红细胞裂解液。
步骤(4)中所述的离心,优选的离心力为30g-800g。
步骤(4)中所述的取三级下层沉淀,加入无菌缓冲液,优选的是按体积比1:2-10加入无菌缓冲液。
步骤(5)中所述的血清,优选的是自体脐带血血清。
步骤(5)中所述的培养基,优选的是memalpha培养基。
步骤(5)(6)中所述的离心,优选的离心力为2000g-10000g。
步骤(6)中所述的经培养处理,涵盖多种有效处理方式和其他的等同处理方式,例如洗涤/培养、过滤/培养等;优选的是洗涤/培养,培养天数可从0天到14天不等;进一步地,洗涤/培养可以是pbs洗涤/培养,如次数超过2次(包括2次),培养时间可缩短,甚至不用培养。
本发明另一方面提供了一种脐带血再生粒子的制备方法,所述方法包括如下步骤:
(1)取脐带血进行30g-1000g离心,离心后分为一级上层溶液和一级下层沉淀;
(2)取一级下层沉淀,加入无菌pbs缓冲液,进行30g-1000g离心,离心后分为二级上层溶液和二级下层沉淀;
(3)取二级下层沉淀,加入无菌红细胞裂解液,置于水平摇床摇动,待完全裂解后进行500g-5000g离心,离心后分为三级上层溶液和三级下层沉淀,三级上层溶液直接弃掉。
(4)取三级下层沉淀,加入无菌pbs缓冲液,剧烈晃动,之后进行30g-800g离心,离心后分为四级上层溶液和四级下层沉淀,四级下层沉淀直接弃掉。
(5)分别取一级上层溶液、二级上层溶液、四级上层溶液,进行2000g-10000g离心,离心后,收集所有沉淀,加入ph值7.0-7.4、含有血清的培养基,置于37℃、5%co2的培养箱中进行培养,每2-3天更换培养基一次。
(6)经培养处理,检测合格后,收集所有培养成分,2000g-10000g离心收集脐带血再生粒子。
以上所有步骤均在无菌环境下进行操作。
步骤(1)中所述的脐带血必须是新鲜、无菌、无病原体的。
步骤(2)中所述的取一级下层沉淀,加入无菌缓冲液,优选的是按体积比1:2-10加入无菌缓冲液。
步骤(3)中所述的无菌红细胞裂解液,可以是现有技术已知的任何一种,优选的是155mmnh4cl或10mmkhco3或0.1mmedta。
步骤(3)中所述的取二级下层沉淀,加入无菌红细胞裂解液,优选的按体积比1:3-10加入无菌红细胞裂解液。
步骤(4)中所述的取三级下层沉淀,加入无菌缓冲液,优选的是按体积比1:2-10加入无菌缓冲液。
步骤(5)中所述的血清,优选的是自体脐带血血清。
步骤(5)中所述的培养基,优选的是memalpha培养基。
步骤(6)中所述的经培养处理,涵盖多种有效处理方式和其他的等同处理方式,例如洗涤/培养、过滤/培养等;优选的是洗涤/培养,培养天数可从0天到14天不等;进一步地,洗涤/培养可以是pbs洗涤/培养,如次数超过2次(包括2次),培养时间可缩短,甚至不用培养。
本发明第二方面提供了通过第一方面所述制备方法得到的脐带血再生粒子,其方法包括如下步骤:
(1)取新鲜、无菌、无病原体的脐带血进行30g-1000g离心,离心后分为一级上层溶液和一级下层沉淀;
(2)取一级下层沉淀,按体积比1:2-10加入无菌pbs缓冲液,进行30g-1000g离心,离心后分为二级上层溶液和二级下层沉淀;
(3)取二级下层沉淀,按体积比1:3-10加入无菌红细胞裂解液(155mmnh4cl,10mmkhco3和0.1mmedta),置于水平摇床摇动,待完全裂解后进行500g-5000g离心,离心后分为三级上层溶液和三级下层沉淀,三级上层溶液直接弃掉。
(4)取三级下层沉淀,按体积比1:2-10加入无菌pbs缓冲液,剧烈晃动,之后进行30g-800g离心,离心后分为四级上层溶液和四级下层沉淀,四级下层沉淀直接弃掉。
(5)分别取一级上层溶液、二级上层溶液、四级上层溶液,进行2000g-10000g离心,离心后,收集所有沉淀,加入ph值7.0-7.4、含有脐带血血清的memalpha培养基,置于37℃、5%co2的培养箱中进行培养,每2-3天更换培养基一次。
(6)经培养0天-14天处理,检测合格后,收集所有培养成分,2000g-10000g离心收集脐带血再生粒子。
以上所有步骤均在无菌环境下进行操作。
本发明第三方面提供了本发明的脐带血再生粒子在组织细胞再生与修复中的应用。
本发明的脐带血再生粒子可以制备成制剂在组织细胞再生与修复中应用,也可以制备成制剂组合物在组织细胞再生与修复中应用。
本发明的脐带血再生粒子在用于哺乳动物的组织细胞再生与修复时,其使用剂量是每公斤体重用量为(0.1-10)x1010个脐带血再生粒子的。例如人,每公斤体重用量为0.1x1010个脐带血再生粒子,每公斤体重用量为1x1010个脐带血再生粒子,每公斤体重用量为10x1010个脐带血再生粒子。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
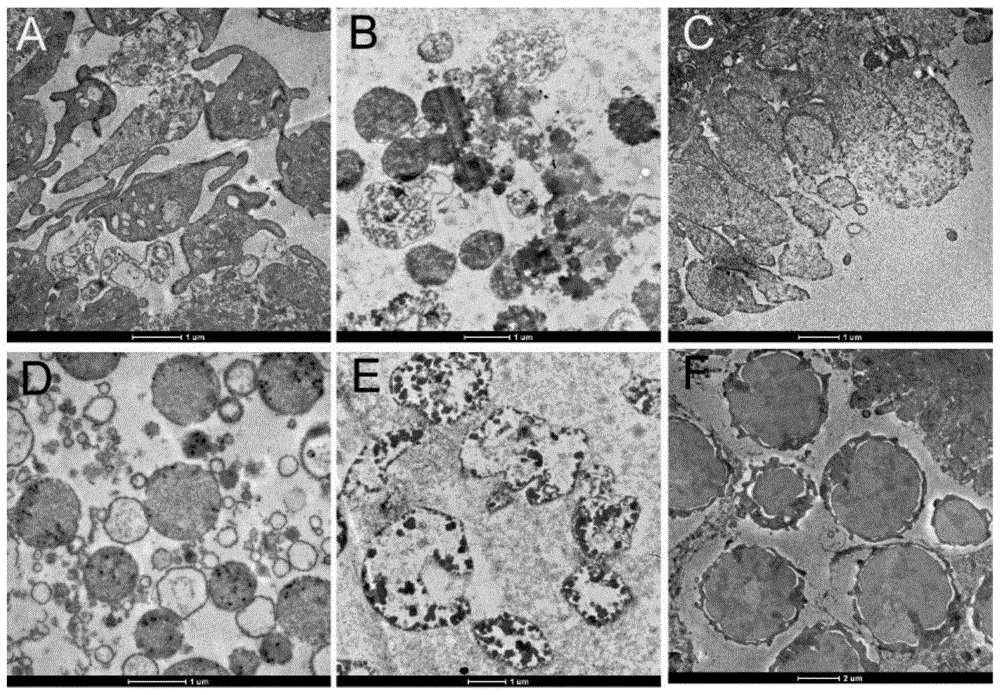
图1:脐带血再生粒子的显微观察图。图1a是血小板的显微观察图;图1b-1f分别是5种不同类型脐带血再生粒子的显微观察图。
图2:脐带血再生粒子的核酸电泳检测图。其中左图显示的是脐带血再生粒子主要包含小rna,小于200nt;右图显示的是进一步的检测结果,脐带血再生粒子主要包含mirna。
图3:脐带血再生粒子的免疫组织荧光检测图。脐带血再生粒子表达多种蛋白,有oct4,sox2,ddx4,tubulin,actin。
图4:再生粒子再生肾管上皮细胞的过程。图4a是在肾缺血损伤后1天时出现在小鼠肾管内的再生粒子he染色图;图4b是在肾缺血损伤后1周时,出现在小鼠肾管内的再生粒子融合he染色图;图4c是再生粒子在融合过程中,出现的与规则核相似的细胞核(箭头所示)he染色图;图4d是再生粒子在再生肾管上皮细胞的过程中,再生形成新的细胞核(箭头所示)he染色图。其中标尺为20μm。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述。以便于进一步理解本发明。以下实施例中所有使用的实验方法如无特殊说明,均为常规方法。以下实施例中所用的材料、试剂等,如无特殊说明,均可通过商业途径获得。
通过下面的实施例可以对本发明进行进一步的描述,而本发明的范围并不局限下述实施例。
本发明对实验中所用到的材料及实验方法进行一般性和/或具体的描述。虽然为实现本发明目的所使用的许多材料和操作方法是本领域公知的,但是本发明仍在此作尽可能详细的描述。
实施例1:脐带血
新鲜健康脐带血是从北京市三甲医院妇产科获得,之后通过冷藏方式运输回单位,温度控制在2℃到8℃之间。
实施例2:脐带血再生粒子的制备
在本实施例中,示例性说明了脐带血再生粒子的制备,方法步骤如下:
制备环境:无菌条件,即千级背景下的百级环境。
(1)取新鲜健康的脐带血进行250g离心,离心后分为两部分,一级上层溶液和一级下层沉淀;
(2)取一级下层沉淀,按体积比1:4加入无菌pbs缓冲液混匀,进行250g离心,离心后又分为两部分,二级上层溶液和二级下层沉淀;
(3)取二级下层沉淀,按体积比1:6加入无菌红细胞裂解液置于水平摇床摇动,待完全裂解后进行1000g离心,离心后又分为两部分,三级上层溶液和三级下层沉淀,三级上层溶液直接弃掉。
(4)取三级下层沉淀,按体积比1:4无菌pbs缓冲液剧烈晃动2-10分钟,之后进行300g离心,离心后又分为两部分,四级上层溶液和四级下层沉淀,四级下层沉淀直接弃掉。
(5)分别取一级上层溶液、二级上层溶液、四级上层溶液,进行6000g离心,离心后,收集所有沉淀,加入ph值7.0-7.4、含有脐带血血清的memalpha培养基,置于37℃,5%co2培养箱中进行培养,每2-3天更换培养基一次。
(6)经培养14天处理,检测合格后,收集所有培养成分,2000g-10000g离心收集脐带血再生粒子。
实施例3:脐带血再生粒子的显微观察
通过对实施例2中获得脐带血再生粒子进行电子显微镜和标准光学显微镜的观察发现,脐带血再生粒子至少有5种不同的形态类型(见图1b,1c,1d,1e,1f),且每种形态与血小板(见图1a)相比较都存在明显的差异。图1a观察,显示单个血小板整体呈完全不规则形,胞体外延有明显长的突起部分,且部分突起散落在胞体附近,胞体整体颜色深浅较为均匀,部分区域差异明显。图1b观察,显示脐带血再生粒子大致呈圆形或椭圆形,胞体有大有小,胞体颜色深浅不一,有致密颗粒呈点状聚集分散在胞体内外。图1c观察,显示脐带血再生粒子呈不规则形,胞体颜色随脐带血再生粒子的聚集而增加,分散而减少,存在小的深颜色胞体和空胞体。图1d观察,显示脐带血再生粒子大致呈圆形,胞体有大有小,颜色深的胞体内部不均匀的分布着高致密颗粒,空胞体内部零散的分布一些致密颗粒物质。图1e观察,显示脐带血再生粒子形状不一,但具有明显的边界,且每个胞体的内部分散含有高致密颗粒物质,越是靠近胞体外延,致密颗粒物质越多。图1f观察,显示脐带血再生粒子形态较为均一,大致呈圆形,胞体明显有两部分组成,外延为明显的不规则致密颗粒带,内部为深颜色的胞体区。另外观察还显示出所有类型的脐带血再生粒子的直径范围为1μm-5μm。
实施例4:脐带血再生粒子的核酸检测
通过对实施例2中获得脐带血再生粒子进行dna标准方法检测和rna电泳分析检测发现,脐带血再生粒子含有微量核酸成分,包括微量dna和小rna,其中小rna主要是mirna。
实施例5:脐带血再生粒子的蛋白检测
通过对实施例2中获得脐带血再生粒子进行免疫组织荧光检测发现,脐带血再生粒子含有一种或多种蛋白成分:oct4,sox2,ddx4,tubulin,actin。
实施例6:肾管上皮细胞的再生与修复
在本实施例中,我们展示了肾动脉结扎和再灌注损伤后小鼠肾管上皮细胞的再生过程。其中实验组小鼠尾静脉注射150ul的再生粒子。对照组小鼠在尾静脉仅注射150ul普通生理盐水。
注射后的再生粒子在肾缺血损伤后1天时出现在小鼠肾小管内(见图4a)。缺血1天肾组织中的再生粒子与未损伤肾中的红细胞形态不同。虽然红细胞染色呈红色,但红细胞呈圆盘状,中心凹陷,扁平面旁扁平,形成一个整体。再生粒子没有中心凹陷,也没有实心成分。损伤后1周,再生肾管中显示出再生粒子的融合(见图4b),此外,再生粒子融合过程中还出现了苏木精染色较弱但大小与规则核相似的细胞核(见图4c)。此外,在再生肾管中出现了新的细胞核,小而微弱,沿管道排列良好(见图4d)。所有这些再生过程都可以在1周缺血损伤的肾管中观察到。tunel法检测肾损伤显示,苏木精(见图4c)染色较弱的细胞核是细胞凋亡细胞核。然而,由于dna片段的小尺寸,很难追踪到细胞凋亡。因此,可以通过再生粒子融合机制再生修复肾管上皮细胞。
以上所述,仅是本发明的较佳实施例而已,并非对本发明作任何形式上的限制,虽然本发明已以较佳实施例揭露如上,然而并非用以限定本发明,任何熟悉本专业的技术人员,在不脱离本发明技术方案范围内,当可利用上述揭示的技术内容做出些许更动或修饰为等同变化的等效实施例,但凡是未脱离本发明技术方案的内容,依据本发明的技术实质对以上实施例所作的任何的简单修改、等同变化与修饰,均仍属于本发明技术方案的范围内。
- 还没有人留言评论。精彩留言会获得点赞!