艾替班特的合成的制作方法
发明的技术领域
本发明涉及由式-i表示的艾替班特的有效的固相合成。
艾替班特
发明背景
艾替班特是对缓激肽b2受体具有选择性的竞争性拮抗剂,具有与缓激肽类似的亲和性。遗传性血管性水肿由c1酯酶抑制剂(导致缓激肽产生的因子xii/激肽释放酶蛋白质水解级联的关键调节剂)的缺失或功能紊乱引起。缓激肽是一种血管舒张药,其被认为是特征性hae症状局部肿胀、炎症和疼痛的原因。艾替班特抑制缓激肽结合b2受体并且由此治疗hae的急性偶发性发作的临床症状。
由shireorphantherapies开发的艾替班特
us5,648,333b1公开了艾替班特及其制备方法。
cn102532267公开了用于制备艾替班特的方法,其使用ctc树脂、利用不同偶联剂用于偶联不同的氨基酸。
cn103992383公开了用于制备艾替班特的方法,其利用boc-d-arg-arg-oh.2hcl的液相合成,之后通过固相合成使用王树脂与剩余的片段偶联。
cn104072585公开了用于制备艾替班特的方法,其使用利用王树脂或p-羟甲基苯氧基甲基苯乙烯树脂作为固体支持物的氨基酸的顺序偶联。
wo2016157177公开了用于在生物相容性叔胺烟酰胺作为催化剂存在下制备艾替班特的方法。
5473/che/2014公开了用于制备艾替班特的方法,其使用在王树脂上的氨基酸的顺序偶联。
之前的用于制备艾替班特的方法具有缺点。由于技术复杂且成本高,所述方法不适合于大规模生产艾替班特;因此,所述方法在商业上不可行或者会持续存在执行问题。
在固相合成期间,观察到在采用的条件下肽聚集的强烈趋势。这是由于以下原因:
生长的肽序列易于形成β片型结构,其导致肽基树脂的崩塌;在此种情况下,试剂分散到肽基树脂中受限,偶联和去保护反应将是迟缓和不完全的,由此产生缺失/添加,外消旋肽杂质,导致难以纯化并且导致低产率。
因此,仍然需要提供用于制备艾替班特的有效方法,所述方法通过避免重复繁复且冗长的纯化步骤而产率高、可扩展、有成本效益、环境友好并且具有商业可行性。
发明目的
本发明的目的是开发用于制备式i的艾替班特的简单稳健且具有商业可行性的顺序方法,所述方法是在无机盐、新的且有效的偶联条件、序列中各氨基酸后的去保护和洗涤条件的帮助下进行的。
附图简述
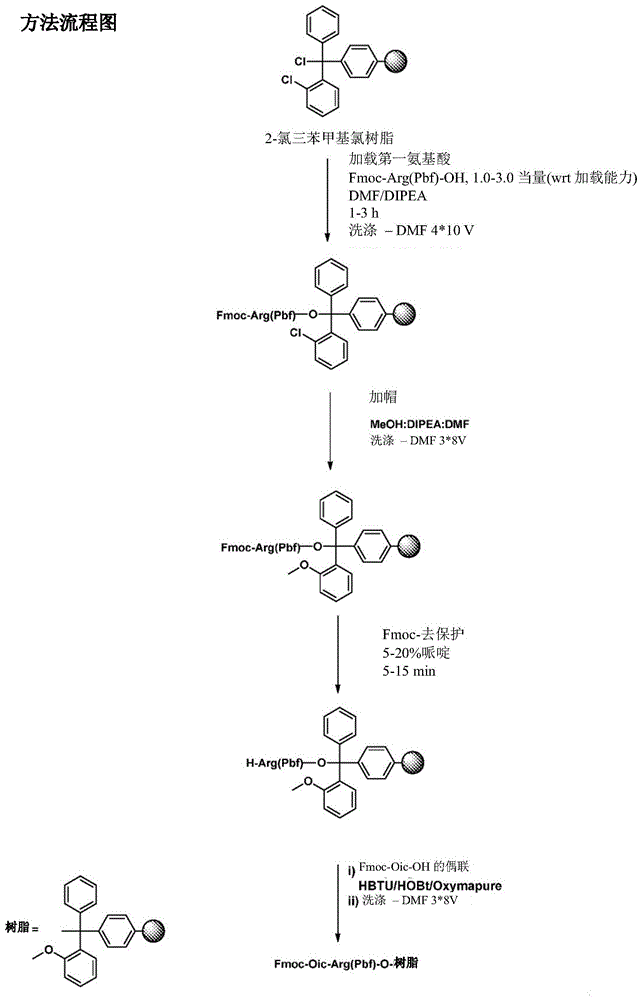
图1:根据本发明的用于艾替班特(式-i)的固相合成的方法的流程图。
发明概述
本发明的一个实施方案涉及用于制备艾替班特的合成方法,所述方法包括以下步骤:
a)在偶联剂存在下将精氨酸加载至树脂固相支持物,
b)给未反应的功能位点加帽(capping),
c)在偶联剂和无机盐存在下顺序偶联侧链保护的氨基酸以制备艾替班特的主链,
d)通过去除保护基并且将肽从所述树脂上切解获得粗艾替班特,
e)纯化粗艾替班特。
所述方法的示意性描述如图1所示。
采用的方法是通过顺序方法的艾替班特的固相肽合成并且在偶联期间涉及无机盐以及常规偶联剂和添加剂。所述方法提供偶联和去保护反应的完成以及外消旋的减少并且由此控制与目标分子非常接近的异构杂质并且由此易化了所述肽的纯化方法。
发明详述
本发明涉及通过采用固相方法顺序偶联个体氨基酸来制备艾替班特的有效方法。本发明采用的方法是固相手工肽合成,其使用2-氯三苯甲基氯作为固体支持物,采用fmoc-/tbu方法,并且包括偶联期间使用的位点特异性的有效的偶联剂和无机盐以及常规偶联剂和添加剂。并且在使用15-20%哌啶的fmoc基团的去保护后,用0.01-0.5mhobt/dmf而不是普通dmf洗涤肽基树脂以保证哌啶的完全去除,这有利于避免插入杂质。通过顺序方法实现完全的合成。所述方法提供偶联和去保护反应的完成以及外消旋的减少并且由此控制与目标分子非常接近的异构杂质并且由此易化了所述肽的纯化方法。
本发明以下面的实施例作为代表。这些实施例仅用于说明并且因此不应当被视为本发明范围的限制。
缩写:
acn:乙腈
boc:叔丁基氧基羰基
comu:1-氰基-2-乙氧基-2-氧代亚乙基氨基氧基)二甲基氨基-吗啉基-碳鎓六氟磷酸盐
cucl2:氯化铜
depbt:3-(二乙氧基磷酰基氧基)-1,2,3-苯并三嗪-4(3h)-酮
dic:n,n'-二异丙基碳二亚胺
dmap:二甲基氨基吡啶
dmf:n,n'-二甲基甲酰胺
dipea:二异丙基乙胺
fmoc:9-芴基甲氧基羰基
hbtu:o-苯并三唑-n,n,n',n'-四甲基脲六氟磷酸盐
hobt:n-羟基苯并三唑
hfip:1,1,1,3,3,3-六氟-2-丙醇
mtt:甲基三苯甲基
meoh:甲醇
mgcl2:氯化镁
nmm:n-甲基吗啉
nmp:n-甲基-2-吡咯烷酮
tes:三乙基硅烷
tfe:三氟乙醇
tfa:三氟乙酸
pbf:2,2,4,6,7-五甲基二氢苯并呋喃
rt:室温
tbu:叔丁基
tis:三异丙基硅烷
trt:三苯甲基
tmp:2,4,6-三甲基吡啶
本发明以下面的实施例作为代表。这些实施例仅用于说明并且因此不应当被视为本发明范围的限制。
实施例1:将具有取代的1.22mmol/g的ctc树脂(10g)放入固相肽合成容器中。在dmf(80-100ml)中进行树脂的溶胀达1h并沥干。将fmoc-arg(pbf)-oh(7.9g,1.0当量)溶解在dmf(80-100ml)中并加入至溶胀的树脂。在搅拌下加入dipea、nmm和tmp(2.0-4.0当量),优选dipea。在室温持续搅拌2-3h并将反应混合物沥干。用dmf(80-100ml)洗涤树脂。进行第一氨基酸加载评估并且发现其为0.61mmol/g。使用在dmf(86ml)中的甲醇(10%)、dipea(4%)进行树脂的未反应位点的加帽。用dmf(80-100ml*3)洗涤树脂。通过用在dmf中的5-20%哌啶处理树脂两次达5-15min来进行fmoc的去封闭。用在dmf中的0.01–0.5mhobt溶液(100ml*2)洗涤树脂并且继之以dmf(80-100ml*2)。
将fmoc-oic-oh(2.0-4.0当量)和hobt(2.0-4.0当量)溶解在dmf(80-100ml)中并加入至反应容器。搅拌反应物质并加入溶解在dmf(20ml)中的hbtu(2.0-4.0当量)。加入dipea(4.0-6.0当量)并在氮气氛下将物质搅拌1.0–2.0h。通过kaiser测试监测偶联的完成。在偶联完成后,将树脂用dmf(80-100ml*3)洗涤并用于fmoc的去封闭。序列中其余的氨基酸偶联使用hbtu/hobt进行。在根据序列偶联所有氨基酸后,进行fmoc的去保护并将肽基树脂用dmf、dcm、甲醇和mtbe洗涤。每次洗涤进行两次,达3min的时间。将肽基树脂干燥并进行完全切解(cleavage)。在室温将肽基树脂(30g)用比率为90:5:5的tfa:tis:水处理。搅拌3h,过滤并将滤液浓缩至其体积的一半并使用mtbe分离固体。分离的粗肽(14.4g)的纯度为68.69%。0.88rrt杂质为3.55%,0.97rrt杂质为1.46%并且1.09rrt杂质为0.15%。
实施例2:类似实施例1进行肽的合成,但是所有的偶联和去保护在约38℃进行。同样类似实施例1进行完全切解,产生纯度67.08%的粗肽。0.88rrt杂质为4.51%,0.97rrt杂质为2.61%并且1.09rrt杂质为0.80%。
实施例3:类似实施例1进行肽的合成。氨基酸的偶联反应,特别是fmoc-oic-oh,fmoc-d-tic-oh,fmoc-thi-oh,fmoc-gly-oh,fmoc-hyp(tbu)-oh,fmoc-pro-oh,使用hbtu/hobt在dipea和催化量的氯化铜(ii)/氯化镁存在下进行。并且,fmoc-ser(tbu)-oh,fmoc-arg(pbf)-oh和fmoc-d-arg(pbf)-oh偶联反应使用depbt/oxymapure在dipea、nmm、tmp(优选dipea)以及催化量的氯化铜(ii)/氯化镁存在下进行。在根据序列偶联所有氨基酸后,进行fmoc基团的去封闭并将肽基树脂用dmf、dcm、甲醇和mtbe洗涤。每次洗涤进行两次达3min的时间。将肽基树脂干燥并且进行完全切解。在室温将肽基树脂(30g)用比率为90:5:5的tfa:tis:水处理。搅拌3h,过滤并将滤液浓缩至其体积的一半并使用mtbe分离固体并在真空中干燥。纯度:72.38%,0.88rrt杂质为0.26%。
实施例4:类似实施例3进行肽的合成。在完成序列后,使用在mdc中的1%tfa将受保护的肽从树脂上释放。将肽基树脂(12g)用在mdc中的1%tfa处理(120ml*12次洗涤)。每次洗涤进行5min的时间。将合并的洗液汇集并浓缩至干燥。将获得的剩余物用比率为70:10:10:5:5的tfa:mdc:苯酚:间甲酚:tis混合物(120ml)在室温处理3h。使用mtbe分离粗肽(5.6g)。纯度为约77.92%,0.88rrt杂质为0.17%。
实施例5:类似实施例1进行肽的合成。氨基酸的偶联反应,特别是fmoc-oic-oh,fmoc-d-tic-oh,fmoc-thi-oh,fmoc-gly-oh,fmoc-hyp(tbu)-oh,fmoc-pro-oh,fmoc-arg(pbf)-oh和fmoc-d-arg(pbf)-oh的偶联反应,使用hbtu/hobt在dipea和催化量的氯化铜(ii)/氯化镁存在下进行。并且,fmoc-ser(tbu)-oh偶联使用dic/hobt在dipea、nmm、tmp(优选dipea)和催化量的氯化铜(ii)/氯化镁存在下进行。在根据序列偶联所有氨基酸后,进行fmoc基团的去封闭并将肽基树脂用dmf、dcm、甲醇和mtbe洗涤。每次洗涤进行两次达3min的时间。将肽基树脂干燥并且使用在mdc中的1%tfa进行切解。肽基树脂(12g)用在mdc中的1%tfa处理(120ml*12次洗涤)。每次洗涤进行5min的时间。将合并的滤液浓缩至干燥并用比率为70:10:10:5:5的tfa:mdc:苯酚:间甲酚:tis混合物(120ml)在室温处理3h。使用mtbe分离粗肽。纯度:64.97%,0.88rrt杂质为0.97%。
实施例6:类似实施例1进行肽的合成。氨基酸的偶联反应,特别是fmoc-oic-oh,fmoc-d-tic-oh,fmoc-thi-oh,fmoc-gly-oh,fmoc-hyp(tbu)-oh,fmoc-pro-oh,fmoc-arg(pbf)-oh和fmoc-d-arg(pbf)-oh的偶联反应,使用hbtu/hobt在dipea和催化量的氯化铜(ii)/氯化镁存在下进行。并且,fmoc-ser(tbu)-oh偶联使用hatu/hobt在dipea、nmm、tmp(优选dipea)和催化量的氯化铜(ii)/氯化镁存在下进行。在根据序列偶联所有氨基酸后,进行fmoc基团的去封闭并将肽基树脂用dmf、dcm、甲醇和mtbe洗涤。每次洗涤进行两次达3min的时间。将肽基树脂干燥并且使用在mdc中的1%tfa进行切解。肽基树脂(12g)用在mdc中的1%tfa处理(120ml*12次洗涤)。每次洗涤进行5min的时间。将合并的滤液浓缩至干燥并用比率为70:10:10:5:5的tfa:mdc:苯酚:间甲酚:tis混合物(120ml)在室温处理3h。使用mtbe分离粗肽。纯度:74.54%,0.88rrt杂质为1.55%。
实施例7:类似实施例1进行肽的合成。氨基酸的偶联反应,特别是fmoc-oic-oh,fmoc-d-tic-oh,fmoc-thi-oh,fmoc-gly-oh,fmoc-hyp(tbu)-oh,fmoc-pro-oh,fmoc-arg(pbf)-oh和fmoc-d-arg(pbf)-oh的偶联反应,使用hbtu/hobt/oxymapure在dipea和催化量的氯化铜(ii)/氯化镁存在下进行。并且,fmoc-ser(tbu)-oh偶联使用pybop/hobt/oxymapure在dipea、nmm、tmp(优选dipea)和催化量的氯化铜(ii)/氯化镁存在下进行。在根据序列偶联所有氨基酸后,进行fmoc基团的去封闭并将肽基树脂用dmf、dcm、甲醇和mtbe洗涤。每次洗涤进行两次达3min的时间。将肽基树脂干燥并且使用在mdc中的1%tfa进行切解。肽基树脂(12g)用在mdc中的1%tfa处理(120ml*12次洗涤)。每次洗涤进行5min的时间。将合并的滤液浓缩至干燥并用比率为70:10:10:5:5的tfa:mdc:苯酚:间甲酚:tis混合物(120ml)在室温处理3h。使用mtbe分离粗肽。
实施例8:类似实施例1进行肽的合成。氨基酸的偶联反应,特别是fmoc-oic-oh,fmoc-d-tic-oh,fmoc-thi-oh,fmoc-gly-oh,fmoc-hyp(tbu)-oh,fmoc-pro-oh,fmoc-arg(pbf)-oh和fmoc-d-arg(pbf)-oh的偶联反应,使用hbtu/hobt在dipea和催化量的氯化铜(ii)/氯化镁存在下进行。并且,fmoc-ser(tbu)-oh偶联使用comu/oxymapure在dipea、nmm、tmp(优选dipea)和催化量的氯化铜(ii)/氯化镁存在下进行。在根据序列偶联所有氨基酸后,进行fmoc基团的去封闭并将肽基树脂用dmf、dcm、甲醇和mtbe洗涤。每次洗涤进行两次达3min的时间。将肽基树脂干燥并且使用在mdc中的1%tfa进行切解。肽基树脂(12g)用在mdc中的1%tfa处理(120ml*12次洗涤)。每次洗涤进行5min的时间。将合并的滤液浓缩至干燥并用比率为70:10:10:5:5的tfa:mdc:苯酚:间甲酚:tis混合物(120ml)在室温处理3h。使用mtbe分离粗肽。
实施例9:以35mmol的规模类似实施例1进行肽的合成。所有氨基酸的偶联使用hbtu/oxymapure在dipea和催化量的氯化铜(ii)/氯化镁存在下进行并且在完成序列后将肽基树脂用dmf、dcm、甲醇和mtbe洗涤,将肽基树脂在真空中干燥并且使用在mdc中的1%tfa释放受保护的肽。将肽基树脂(130g)用在mdc中的1%tfa处理(1.3l*15次洗涤)。每次洗涤进行5min的时间。将合并的滤液浓缩至干燥并且通过以70:10:5:5:5:5的比率用tfa:mdc:苯酚:间甲酚:tis:h2o混合物在室温处理3h来进行肽的完全切解。使用mtbe分离粗肽,纯度为76.8%并且产率为68%。
- 还没有人留言评论。精彩留言会获得点赞!