一种线粒体靶向刺激响应性光敏剂的制备及应用的制作方法
本发明涉及一种线粒体靶向光敏剂的制备及应用,属于光动力治疗技术领域。
背景技术:
线粒体作为细胞呼吸必不可少的细胞器,为细胞的新陈代谢提供能量,并在细胞程序性死亡如细胞凋亡中起关键作用。因此线粒体成为临床应用中有希望的治疗靶标。众所周知,光动力疗法是一种新兴的治疗方式,通过有效光源照射光敏剂,产生具有细胞毒性的单线态氧,进而对病患细胞造成不可逆的杀伤。以上二者相结合,线粒体靶向光敏剂应运而生,通过制造线粒体功能障碍,导致病患细胞的死亡,进而达到治疗目的。然而,大多数的线粒体靶向光敏剂不具有开关可控性,并且在生物介质中的应用受到其低水溶性的限制,导致大量聚集体形成,降低单线态氧量子产率。因此设计一个开关可控、生物相容性好的线粒体靶向光敏剂势在必行。
技术实现要素:
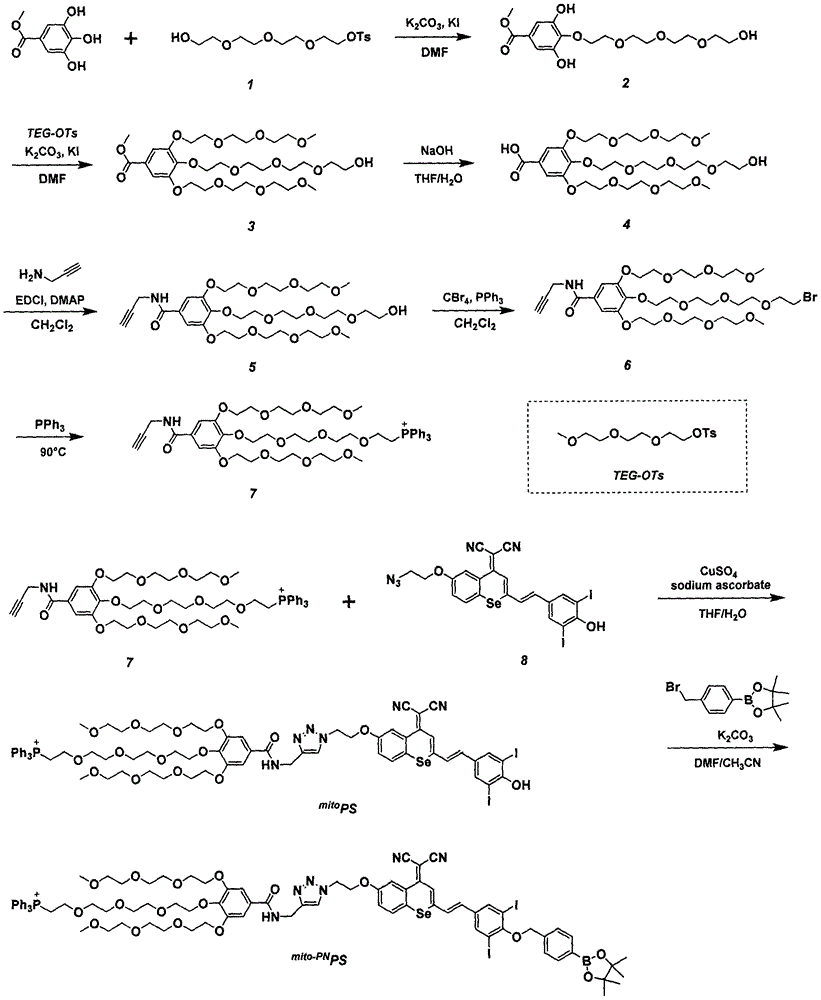
本发明的目的就是为了解决现有技术中存在的上述问题,提供了一种线粒体靶向刺激响应性光敏剂的制备方法及应用,合成路线如下:
本发明提供的一种线粒体刺激响应性光敏剂,具有如mito-pnps所示结构的化合物。
优选地,化合物1和没食子酸甲酯的摩尔比为1∶1。
优选地,化合物3和氢氧化钠的摩尔比为1∶10,四氢呋喃和水的体积比为2∶1。
优选地,化合物4和炔丙胺的摩尔比为1∶4,先将二者溶于二氯甲烷,搅拌均匀,再缓慢滴加含有edci和dmap的二氯甲烷混合溶液。
优选地,化合物6与三苯基磷的摩尔比为1∶3,该反应不加任何溶剂,90℃搅拌24h。
优选地,化合物7和azidepsse-i的摩尔比为1∶1,四氢呋喃和水的体积比为4∶1,室温反应24h。
优选地,化合物mitops和
mito-pnps所示结构的化合物在病患细胞线粒体内和线粒体过表达的ros(oono-)相互作用,通过自降解化学,生成具有光毒性的mitops所示结构的化合物,实现线粒体靶向光敏剂的开关可控性。
mito-pnps所示结构的化合物在可见光区无吸收,无光动力能力,和线粒体过表达的ros(oono-)相互作用后,生成具有光毒性的mitops所示结构的化合物,在可见光区的吸收恢复,光动力能力也随之恢复。
本发明还提供了一种线粒体靶向激活式光敏剂的通用制备策略,可以在mitops所示结构的化合物上醚化不同的生物响应性基团,特异性识别不同的生物信号分子,打开光敏性。
本发明所述光敏剂,碘原子的引入,一方面有效降低了光敏剂去磷酸化后酚羟基的pka,使光敏剂更加适应生理ph值;另一方面有利于隙间穿越,提高光动力能力。
附图说明
图1线粒体靶向光敏剂的合成路线。
图2线粒体靶向光敏剂在刺激响应前后的吸收。
图3线粒体靶向光敏剂刺激响应前后的光敏性。
图4线粒体靶向光敏剂在病患细胞中的特异性定位(与商业线粒体探针相比较)。
图5线粒体靶向光敏剂对病患细胞的杀伤(mtt)。
图6线粒体靶向光敏剂的结构式。
具体实施方式
为了使本领域的技术人员可以更好地理解本发明,下面结合附图和具体实施例对本发明做出进一步的解释和说明,但所举实施例不作为本发明的限定,在没有做出创造性的劳动成果下所获得的其他实施例,都属于本发明的保护范围。
实施例一:合成化合物7,合成路线见附图1
没什子酸甲酯(3.0g,16.3mmol)溶于干燥的dmf(15ml)中,加入碳酸钾(4.5g,32.6mmol)和碘化钾(0.27g,1.63mmol),80℃搅拌10min,逐滴滴加含有化合物1(5.68g,16.3mmol)的干燥的dmf(5ml)溶液,在该温度下搅拌过夜。反应结束后,旋蒸除去溶剂,将混合物溶于乙酸乙酯,饱和食盐水洗涤3次,无水硫酸钠干燥,旋蒸除去溶剂,以石油醚和乙酸乙酯为洗脱剂进行柱层析得到无色油状物化合物2(1.82g,31.0%)。1hnmr(400mhz,cdcl3)δ(ppm)7.63(s,2h),7.15(s,2h),4.20-4.14(t,j=3.2hz,2h),3.85(s,3h),3.74(m,8h),3.69(s,4h),3.62(t,j=4.4hz,2h),3.48-3.38(s,1h).13cnmr(100mhz,cdcl3)δ(ppm)166.95,149.94,138.14,126.36,109.59,72.88,72.27,70.50,70.43,70.19,70.14,69.89,61.57,52.13.
根据化合物2的合成方法合成化合物3。1hnmr(400mhz,cdcl3)δ(ppm)7.30(s,2h),4.22(m,6h),3.88(m,7h),3.84-3.78(t,j=4.8hz,2h),3.77-3.70(m,8h),3.66(m,14h),3.60(m,2h),3.57-3.52(m,4h),3.38(s,6h),2.80(s,h).13cnmr(100mhz,cdcl3)δ(ppm)166.54,152.23,142.47,124.93,108.94,72.58,72.41,71.89,70.77,70.64,70.59,70.51,70.47,70.29,69.57,68.79,61.64,58.96,52.13.
化合物3(1.0g,1.53mmol)溶于thf(10ml),慢慢滴加含有12%naoh的水溶液(5ml),在室温下搅拌过夜。盐酸调节ph至3,乙酸乙酯萃取,无水硫酸钠干燥,旋蒸除去溶剂。以二氯甲烷和甲醇为洗脱剂进行柱层析得到淡黄色油状物化合物4(0.93g,95.0%)。1hnmr(400mhz,cdcl3)δ(ppm)7.34(s,2h),4.23(m,6h),3.88(m,4h),3.84-3.79(t,j=5.2hz,2h),3.74(m,8h),3.67(m,14h),3.61(t,j=4.8hz,2h),3.58-3.53(m,4h),3.38(s,6h).13cnmr(100mhz,cdcl3)δ(ppm)169.63,152.21,142.80,124.53,109.36,72.57,72.42,71.90,70.76,70.64,70.58,70.50,70.46,70.27,69.62,68.78,61.61,58.97.
化合物4(1.9g,2.97mmol)和炔丙胺(0.66g,11.98mmol)溶于二氯甲烷(20ml),搅拌均匀,缓慢滴加含有edcl(0.68g,3.55mmol)和dmap(0.036g,0.295mmol)的二氯甲烷(10ml),滴加完毕后,室温反应过夜。反应结束后,饱和食盐水洗涤3次,无水硫酸钠干燥,旋蒸除去溶剂,以二氯甲烷和甲醇为洗脱剂进行柱层析得到淡黄色油状物化合物5(1.51g,75.2%)。1hnmr(400mhz,cdcl3)δ(ppm)7.14(s,2h),6.95(t,j=5.2hz,1h),4.21(m,8h),3.87-3.81(t,j=4.8hz,4h),3.81-3.77(t,j=4.8hz,2h),3.74-3.58(m,24h),3.57-3.52(m,4h),3.36(s,6h),2.80(t,j=6.0hz,1h),2.27(t,j=2.4hz,1h).13cnmr(100mhz,cdcl3)δ(ppm)166.66,152.40,141.76,128.85,107.62,79.92,72.50,72.34,71.89,71.39,70.65,70.63,70.61,70.49,70.42,70.37,69.73,69.12,61.71,58.95,29.66.
化合物5(2.0g,2.96mmol)和四溴化碳(1.18g,3.6mmol)溶于二氯甲烷(20ml),搅拌均匀,在0℃逐滴滴加含有三苯基磷(1.16g,4.42mmol)的二氯甲烷(5ml),滴加完毕后,继续反应4h。反应结束后,以二氯甲烷和甲醇为洗脱剂进行柱层析得到淡黄色油状物化合物6(1.83g,83.7%)。1hnmr(400mhz,cdcl3)δ(ppm)7.15(s,2h),7.09(t,j=5.2hz,1h),4.26-4.14(m,8h),3.87-3.76(m,8h),3.75-3.61(m,20h),3.58-3.51(m,4h),3.47(t,j=6.4hz,2h),3.36(s,6h),2.27(t,j=2.4hz,1h).13cnmr(100mhz,cdcl3)δ(ppm)166.61,152.37,141.65,128.86,107.53,79.97,72.35,71.87,71.33,71.15,70.69,70.63,70.60,70.54,70.49,70.40,69.70,69.05,58.91,30.37,29.61.
化合物6(1.3g,1.76mmol)和三苯基磷(1.5g,5.72mmol)加入到50ml的圆底烧瓶中,直接加热至90℃,三苯基磷融化,在该温度下搅拌24h。反应结束后,以二氯甲烷和甲醇为洗脱剂进行柱层析得到淡黄色油状物化合物7(1.58g,97.5%)。1hnmr(400mhz,cdcl3)δ(ppm)8.37(t,j=5.6hz,1h),7.79-7.60(m,15h),7.33(s,2h),4.29-4.14(m,8h),3.97-3.79(m,8h),3.78-3.73(t,j=4.8hz,2h),3.69(m,4h),3.67-3.55(m,10h),3.52(m,4h),3.42-3.36(m,2h),3.34(s,6h),3.33-3.28(m,2h),3.27-3.22(m,2h),2.15(t,j=2.4hz,1h).13cnmr(100mhz,cdcl3)δ(ppm)166.46,151.89,140.51,134.74,134.72,133.80,133.70,130.11,129.99,128.97,119.00,118.14,107.14,80.85,77.54,72.22,71.75,70.66,70.45,70.40,70.29,70.26,70.16,70.07,69.58,68.78,63.82,63.74,58.85,29.18,25.49,24.96.hrms(maldi):m/z[m]calcdforc50h67no13p+920.4345;found920.4348.
实施例二:合成mito-pnps,合成路线见附图1
化合物7(129mg,0.14mmol)、azidepsse-i(100mg,0.14mmol)、抗坏血酸钠(2.8mg,0.014mmol)和无水硫酸铜(2.2mg,0.0014mmol)溶解在四氢呋喃/水(4ml/1ml)的混合溶液中,室温反应24h。反应结束后,二氯甲烷萃取,无水硫酸钠干燥,旋蒸除去溶剂,以二氯甲烷和甲醇为洗脱剂进行柱层析得到黑绿色固体化合物mitops(0.15g,65.6%)。1hnmr(400mhz,cdcl3)δ(ppm)8.99(s,1h),8.17(s,1h),8.08(s,1h),7.81-7.56(m,18h),7.53-7.41(m,2h),7.34(s,2h),7.13(d,j=8.8hz,1h),6.75(d,j=15.6hz,1h),6.64(d,j=16.0hz,1h),4.86-4.66(m,4h),4.45(s,2h),4.15(m,6h),3.92-3.71(m,10h),3.66(m,4h),3.64-3.53(m,10h),3.50(m,4h),3.38-3.30(m,8h),3.26(m,2h),3.21(m,2h).13cnmr(100mhz,cdcl3)δ(ppm)166.76,158.70,157.36,157.29,151.96,138.39,149.90,145.88,140.51,138.39,134.76,134.74,134.49,133.88,133.78,130.47,130.17,130.04,129.35,128.79,127.21,125.76,124.80,124.44,122.66,122.06,119.19,118.33,117.70,116.19,112.28,107.15,86.12,77.27,72.31,71.88,70.95,70.56,70.50,70.42,70.37,70.20,70.10,69.70,68.75,66.71,63.90,63.83,58.98,49.36,35.64,29.69,25.31,24.78.hrms(maldi):m/z[m]calcdforc72h80i2n6o15sep+1633.2668;found1633.2675.
化合物mitops(0.15g,91.8μmol)和碳酸钾(0.051g,0.37mmol)依次加入到干燥的dmf/ch3cn(2ml/2ml)中,80℃搅拌10min,缓慢滴加含有
为了进一步探究线粒体靶向光敏剂定位至病患细胞线粒体的能力,我们使用商业的线粒体探针进行对比,结果二者荧光高度重合,皮尔森系数高达95%,说明mito-pnps的线粒体靶向性非常好。
为了进一步探究线粒体靶向光敏剂在刺激响应前后的光动力,使用9,10-二甲基蒽(dma)作为单线态氧探针对其进行定量测试。测试条件为氙灯光源490-700nm,功率为5mw/cm2,溶液中含有dma(60μm),mito-pnps(2.5μm),dmf(5%),f127(0.3%),ph为7.4,刺激响应前后光动力能力如附图3所示,刺激响应前dma的变化量和对照组(无光敏剂)几乎一致,刺激响应后,dma的变化量骤然增加,这标志着刺激响应前光动力完全被抑制,刺激响应后光动力的恢复。
为了更进一步探究光敏剂对病患细胞的杀伤作用,利用mtt法研究了mito-pnps在光照条件下对raw264.7细胞的毒性,结果如附图5所示,mito-pnps在与线粒体中过表达的oono-相互作用后生成具有光毒性的mitops,在光照条件下杀死病患细胞。
以上所述仅为本发明的优选实施例,凡依照本发明做出的等同于替代或变换(例如,以mitops为底物,分别醚化不同的响应基团),均在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!