Actinoxocine及其异构体制备和应用的制作方法
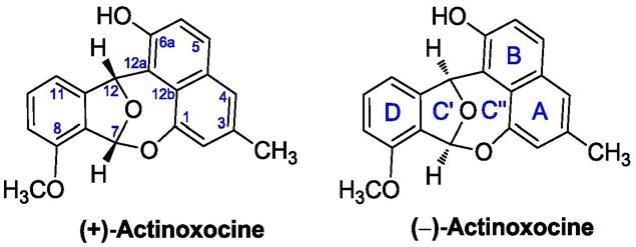
actinoxocine及其异构体制备和应用
技术领域
1.本发明中涉及的actinoxocine及其异构体指的是(+)-actinoxocine与(-)-actinoxocine,以及(+)-actinoxocine与(-)-actinoxocine的结构、制备方法,在抗菌、抗炎及抗肿瘤新药研发中的应用。
背景技术:
2.当今,肿瘤、炎症等重大疾病不但严重威胁着我国人民健康及生命安全,同时也对国民经济带来了沉重的负担。因此,研发新型、高效低毒且作用机制独特的抗肿瘤及抗炎新药具有重要的社会及经济意义。
3.创新药物研发经验表明,从天然产物中寻找活性先导物进而创制新药是最有效途径之一,天然产物特有的化学结构复杂性和生物活性多样性,奠定了从天然产物中发现活性先导物进而创制新药的成功几率。海洋放线菌是一类重要的药源微生物,生活在大洋中的放线菌,因其生理生化和16s rrna等分子生物学特征与陆生放线菌有明显差别,致使其次生代谢产物结构类型更加新颖、生物活性更加显著,因此,从海洋放线菌中寻找新型先导化合物进而研发抗炎及抗肿瘤新药具有巨大的潜力。
4.本发明所涉及的(+)-actinoxocine及(-)-actinoxocine为新化合物,是发明申请人从海洋活性放线菌streptomyces griseus sp.kcb-132的次生代谢产物中分离得到的新结构化合物。药理活性实验发现,(+)-actinoxocine及(-)-actinoxocine对多种细菌及真菌具有较好的生长抑制作用,同时,(-)-actinoxocine对人胃腺癌ags细胞的生长具有良好的抑制作用,而(+)-actinoxocine对tnf-α蛋白释放表现出抑制作用,因此,2个新化合物具有开发成新型抗炎、抗菌及抗肿瘤药物的潜力。(+)-actinoxocine及(-)-actinoxocine的化学结构、制备方法及其抗菌、抗炎及抗肿瘤活性研究均为首次公开,因此具有突出的实质性特点。
技术实现要素:
5.本发明提供新化合物(+)-actinoxocine与(-)-actinoxocine的制备方法,以及在抗肿瘤、抗炎及抗菌新药研发中的应用。
6.本发明所涉及的用于抗肿瘤、抗炎及抗菌新药研发的2个新化合物为一对对映异构体,命名为(+)-actinoxocine及(-)-actinoxocine,其分子式为c
20
h
16
o4,化学结构式分别如下:
[0007][0008]
本发明所涉及的(+)-actinoxocine及(-)-actinoxocine的制备方法为:将海洋活性放线菌streptomyces griseus sp.kcb-132划线接种于固体培养基上,于28℃培养3-4天,直至长出白色的孢子,然后将孢子接种到液体培养基,在28℃及150-220转/分钟条件下,摇床培养8-12天,收获发酵物。过滤发酵物获得发酵液和菌丝体,发酵液经大孔吸附树脂柱吸附、洗脱及浓缩,菌丝体经丙酮破碎提取,减压浓缩提取物;合并浓缩物,利用有机溶剂萃取,减压浓缩得总浸膏。总浸膏通过硅胶柱层析,梯度洗脱,收集洗脱液体积比1:20的洗脱组分,将收集的洗脱组分进行ods反相柱层析,收集35-45%有机醇洗脱部分,洗脱液浓缩,冷藏结晶;结晶液过滤,减压干燥,即得到(+)-actinoxocine及(-)-actinoxocine的混合物。通过手性填料的hplc,即将对映异构体混合物分为纯度达98%以上的(+)-actinoxocine及(-)-actinoxocine单体化合物。
[0009]
本工艺中所用涉及的培养基,为半海水isp2培养基、纯海水isp2培养基的一种,优选为半海水isp2培养基。
[0010]
本工艺中所涉及的用作提取溶剂的有机醇,为甲醇、乙醇中的一种,优选为乙醇作为提取剂。
[0011]
本工艺中所涉及的大孔吸附树脂柱,为弱极性或非极性的大孔吸附树脂,优选弱极性型号。
[0012]
本工艺中所涉及的萃取剂,为石油醚、乙酸乙酯、正丁醇中的一种,优选为乙酸乙酯作为萃取剂。
[0013]
本工艺中所涉及的重结晶溶剂,为甲醇、乙醇、丙酮、乙酸乙酯、氯仿、二氯甲烷等溶剂中的一种或几种,优选甲醇作为重结晶溶剂。
[0014]
本工艺中所涉及的手性分离填料,可用chiralpak as-h、chiralpak ad-h、chiralcel od-h及(r,r)whelk 01,优选(r,r)whelk 01作为分离填料。
[0015]
本发明还提供了(+)-actinoxocine与(-)-actinoxocine的抗肿瘤、抗炎及抗菌实验方法、结果及新药研发中的应用前景。
[0016]
本发明涉及的新化合物(+)-actinoxocine及(-)-actinoxocine,其化学结构、制备方法及其抗炎、抗菌及抗肿瘤活性研究,均为首次公开,不存在通过其他化合物给出任何启示的可能,具备突出的实质性特点,且有望用于一种新型抗炎、抗菌或抗肿瘤药物的开发。
附图说明
[0017]
图1、新化合物(
±
)-actinoxocine的核磁共振氢谱
[0018]
图2、新化合物(
±
)-actinoxocine的核磁共振碳谱
[0019]
图3、新化合物(
±
)-actinoxocine的dept-135图谱
[0020]
图4、新化合物(
±
)-actinoxocine的氢-氢相关图谱
[0021]
图5、新化合物(
±
)-actinoxocine的hsqc图谱
[0022]
图6、新化合物(
±
)-actinoxocine的hmbc图谱
[0023]
图7、新化合物(
±
)-actinoxocine的noesy图谱
[0024]
图8、新化合物(
±
)-actinoxocine的高分辨质谱
[0025]
图9、新化合物(+)-actinoxocine的单晶x-射线衍射图
[0026]
图10、新化合物(-)-actinoxocine的单晶x-射线衍射图
[0027]
图11、新化合物(+)-actinoxocine的cd图谱
[0028]
图12、新化合物(-)-actinoxocine的cd图谱
[0029]
图13、新化合物(+)-actinoxocine的紫外吸收图谱
[0030]
图14、新化合物(-)-actinoxocine的紫外吸收图谱
[0031]
图15、(+)-actinoxocine及(-)-actinoxocine的抗炎活性
具体实施方式
[0032]
下面的实施例用以解释本发明,但是并非对本发明实质内容的限制。
[0033]
实施例1、(+)-actinoxocine及(-)-actinoxocine的制备
[0034]
将海洋放线菌streptomyces griseus sp.kcb-132划线接种于isp2半海水固体培养基上,28℃条件下培养3天后,取1cm2菌苔接种到isp2半海水isp2液体培养基中,于28℃及180转/分钟条件下,摇床培养10天后收获发酵物。过滤发酵物获得发酵液和菌丝体,发酵液经xad-16大孔吸附树脂柱吸附、洗脱并减压浓缩,菌丝体经丙酮破碎、提取并减压浓缩,浓缩物合并后利用乙酸乙酯萃取,萃取液减压浓缩得总浸膏。总浸膏经硅胶柱层析,梯度洗脱,收集甲醇-二氯甲烷的洗脱组分(1:20,体积比),将收集的洗脱组分通过ods反相柱层析,收集35-45%(体积比)甲醇水洗脱部分,洗脱液减压浓缩,冷藏结晶,过滤,减压干燥,即得(+)-actinoxocine及(-)-actinoxocine的混合物结晶体。对映异构体混合物通过手性填料hplc分离,即得到纯度达98%以上的(+)-actinoxocine及(-)-actinoxocine单体化合物。
[0035]
实施例2、(+)-actinoxocine及(-)-actinoxocine的结构确定
[0036]
(1)仪器与材料
[0037]
jasco p-1020数字式旋光仪,agilent tof/6500高分辨率质谱仪,岛津uv-2401可见-紫外分光光度计,bruker avance iiitm 600核磁共振仪,smart apex ii duo单晶x-射线衍射仪。
[0038]
(2)化学结构鉴定
[0039]
(+)-actinoxocine:无色晶体(甲醇),易溶于二甲基亚砜、乙酸乙酯、丙酮、氯仿,[α]
25d
+168.8(ch2cl2,c 0.08);uv(ch2cl2)λ
max
(logε)281(2.65),308(2.54),339(2.52),349(2.50)nm,见附图-13;hr-esims[m-h]
-
,m/z 319.0975(δ=0.3ppm),见图8;1d和2d nmr数据下见表1及图1至7,单晶x-射线衍射见图9。
[0040]
(
–
)-actinoxocine:无色晶体(甲醇),易溶于二甲基亚砜、乙酸乙酯、丙酮、氯仿,[α]
25d-186.1(ch2cl2,c 0.08);uv(ch2cl2)λ
max
(logε)281(2.49),306(2.33),340(2.22),
353(2.23)nm,见图14;hr-esims[m-h]
-
,m/z 319.0975(δ=0.3ppm),见图8;1d和2d nmr数据下见表1及图1至图7,单晶x-射线衍射图见图10。
[0041]
表1、(
±
)-actinoxocine的nmr数据(1h nmr 600mhz,
13
c nmr 150mhz)
[0042][0043]
依据以上化合物理化参数、波谱数据(图11及图12)、及单晶x-射线衍射实验(图9及图10),确定(+)-actinoxocine的绝对构型为7r、12r,而(-)-actinoxocine的绝对构型为7s、12s,其化学结构分别如下图所示。
[0044][0045]
实施例3、(+)-actinoxocine及(-)-actinoxocine的抗肿瘤活性
[0046]
将人胃腺癌ags细胞、肝癌hepg2细胞、宫颈癌hela细胞、胶质瘤u251细胞、肝癌hep3b细胞、结肠癌hct116细胞及ls180细胞置于96孔板,每孔加入100微升dmem培养基,细胞浓度约为5000个细胞/孔,37℃,5%co2温箱内培养过夜。化合物(+)-actinoxocine及(-)-actinoxocine设置3个浓度,每浓度设3个平行孔,培养72小时后,每孔加入20微升mtt溶液,37℃,5%co2条件下继续培养4小时,弃去上清液,然后每孔加入150微升二甲基亚砜以溶解fomazan晶体,轻度振荡5分钟后,酶标仪下检测570nm处的吸光度,以对照组为参考,用图解法计算出ic
50
值(小于100为无活性),见下表2。
[0047]
表2、(+)-actinoxocine及(-)-actinoxocine的抗肿瘤细胞活性研究结果
[0048][0049]
实施例4、(+)-actinoxocine及(-)-actinoxocine的抗炎活性
[0050]
将小鼠巨噬细胞raw264.7置于含10%fbs的1640培养基中,37℃,5%co2条件下,置加湿培养箱中培养。分别加入(+)-actinoxocine及(-)-actinoxocine,再加入0.1%的dmso,培养24小时,以观察细胞毒活性。然后每孔加入10微升cck-8试剂,培养3个小时,通过微板阅读器(biotek,elx808,美国),在450nm(650nm校准)读取od值。将巨噬细胞raw264.7置于含10%fbs的1640培养基中,分别加入化合物样品,再加入0.1%dmso,培养24小时,分别用脂多糖lps(0.1μg/ml)和三酰酯酞pam3csk4(50nm)诱导细胞24小时,以观察抗炎活性。弃去上清液,利用试剂盒elisa测定小鼠肿瘤坏死因子-α,以地塞米松作为阳性对照,见图15。
[0051]
实施例5、(+)-actinoxocine及(-)-actinoxocine的抗菌活性
[0052]
以青霉素和制霉菌素为阳性对照,通过微孔板生物实验法,对化合物(+)-actinoxocine及(-)-actinoxocine进行了抗革兰氏阳性菌(5株菌,分别为枯草芽孢杆菌cmcc63501、金黄色葡萄球菌cmcc 26003、肠道球菌atcc 29212,以及从临床分离发现的蜡样芽胞杆菌、诺卡氏杆菌)、抗革兰氏阴性菌(3株菌,分别为宋内志贺氏菌atcc 25931、大肠杆菌cmcc 44102、乙型副伤寒沙门菌cmcc 50094)及抗植物病原真菌(黄瓜炭疽病菌)活性筛选,发现2个新化合物对4种细菌及真菌的生长显示较好的抑制作用,在浓度为64μg/ml时,其mic值如下表3所示(-代表不显示活性)。
[0053]
表3、(+)-actinoxocine及(-)-actinoxocine的抗菌活性研究结果
[0054]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1