持续过表达IFN-γ的间充质干细胞及其用途的制作方法
本发明属于干细胞技术领域,具体涉及一种持续过表达ifn-γ的间充质干细胞及其用途。
背景技术:
异基因造血干细胞移植(allogeneichematopoieticstemcelltransplantation,allo-hsct)的主要特征是供者t淋巴细胞等免疫细胞的激活,通过免疫机制,最大化地消灭受者残存的白血病细胞,以期达到移植物抗白血病效应(graft-versus-leukemia,gvl)。而供者t细胞在受者体内激活,常会引起急性移植物抗宿主病(acutegraftversushostdisease,agvhd),是allo-hsct最严重的并发症,严重影响移植成功率。其发生机理主要是供者t细胞通过激活抗原呈递细胞和诱导细胞因子的释放作用于受者细胞,引起患者皮肤,肺,肝脏等靶器官损伤。
目前针对agvhd的治疗推荐主要在allo-hsct后的预防,药物包括环孢霉素a、甲氨蝶呤、抗胸腺细胞球蛋白等;而针对已经发生的agvhd一线用药推荐为甲基强的松龙,二线治疗包括吗替麦考酚酯胶囊、甲氨蝶呤、他克莫司、抗tnf抗体、间充质干细胞(mesenchymalstemcell,msc)输注等。但上述方法的临床治疗效果仍不理想。
ifn-γ是一种由多种细胞如cd4+th1细胞、cd8+细胞、nk细胞、b细胞等分泌的多效细胞因子,在免疫调节中具有重要意义,可以通过参与调节免疫应答、调节细胞周期,促进细胞凋亡、抗肿瘤新生血管形成、抗病毒作用及与化学药物组合的协同作用等发挥抗肿瘤作用,如能够通过促进fas和fasl蛋白表达来抑制白血病k562细胞增殖并促进凋亡。
mscs是一类来源广泛且具有多向分化潜能的多能干细胞,研究证明mscs因为低表达主要组织性相容复合体(majorhistocompatibilitycomplex,mhc)ⅰ类分子,不表达mhcⅱ类分子、fasl、cd80、cd86、cd40、cd40l,具有低免疫原性及免疫调节能力。在agvhd环境中,mscs可通过可溶性抗增殖因子:如转化生长因子β(tgf-β)、肝细胞生长因子、吲哚胺-2,3-双加氧酶(ido)、可诱导性一氧化氮合酶(inos)、血红素氧合酶(ho-1)、前列环素e2(pge2)、ifn-γ、白细胞介素-10(il-10)、及人类白细胞抗原-g5(hla-g5)共同组成免疫抑制微环境,阻断t淋巴细胞的活化、加速t淋巴细胞的凋亡而发挥免疫抑制作用抑制agvhd的进展。但从目前使用mscs预防agvhd的报道来看,治疗效果尚不确定。脐带来源的mscs由于其原始性、高扩增率、高分化能力、易获取、无伦理争论和菌污染机会小等优势,成为mscs研究中的优势选择。
综上,现有技术中缺乏有效的预防agvhd的方法,本发明拟提供一种持续过表达ifn-γ的人脐带间充质干细胞,以期预防agvhd的发生或减轻其严重程度,同时不影响gvl效应。
技术实现要素:
本发明要解决的技术问题为:现有技术中缺乏有效的预防agvhd的方法的问题。
本发明解决技术问题的技术方案为:提供一种持续过表达ifn-γ的间充质干细胞。该间充质干细胞含有的重组载体中含有能持续编码ifn-γ的基因,能够持续过表达ifn-γ。
其中,上述持续过表达ifn-γ的间充质干细胞中,所述的持续编码ifn-γ的基因的核苷酸序列如seqidno:1所示。
seqidno:1ifn-γ的核苷酸序列
atgaaatatacaagttatatcttggcttttcagctctgcatcgttttgggttctcttggctgttactgccaggacccatatgtaaaagaagcagaaaaccttaagaaatattttaatgcaggtcattcagatgtagcggataatggaactcttttcttaggcattttgaagaattggaaagaggagagtgacagaaaaataatgcagagccaaattgtctccttttacttcaaactttttaaaaactttaaagatgaccagagcatccaaaagagtgtggagaccatcaaggaagacatgaatgtcaagtttttcaatagcaacaaaaagaaacgagatgacttcgaaaagctgactaattattcggtaactgacttgaatgtccaacgcaaagcaatacatgaactcatccaagtgatggctgaactgtcgccagcagctaaaacagggaagcgaaaaaggagtcagatgctgtttcgaggtcgaagagcatcccagtag。
其中,上述持续过表达ifn-γ的间充质干细胞中,所述的重组载体为病毒载体。进一步的,所述的病毒载体为慢病毒载体。
其中,上述持续过表达ifn-γ的间充质干细胞中,所述的间充质干细胞为人脐带间充质干细胞。
本发明还提供了一种上述持续过表达ifn-γ的间充质干细胞的制备方法,包括以下步骤:
构建表达ifn-γ的慢病毒载体,并包装病毒颗粒;复苏冻存的第3代人脐带间充质干细胞,换液、培养、传代后,选择第5代处于对数生长期的人脐带间充质干细胞,细胞生长至80~90%汇合时,用胰酶消化并计数,37℃、5%co2条件下培养过夜;病毒颗粒感染细胞,37℃、5%co2条件下培养24h后换液,48h后更换为筛选培养基,37℃、5%co2条件下培养,即获重组基因修饰的间充质干细胞。
进一步的,所述的筛选培养基为含1ug/ml嘌呤霉素的dmem/f12完全培养基。
本发明还提供了一种上述持续过表达ifn-γ的间充质干细胞在预防或治疗急性移植物抗宿主病中的用途。
与现有技术相比,本发明的有益效果为:
本发明构建了一种持续表达ifn-γ的慢病毒载体,感染人脐带间充质干细胞,得到一种能持续过表达ifn-γ的间充质干细胞,并研究了ifn-γ在humscs免疫调节中的作用机制,首次发现重组修饰后的间充质干细胞在异基因造血干细胞移植后的机体内同时发挥抗肿瘤及免疫作用,降低急性移植物抗宿主病的发生率或严重程度,同时不影响gvl效应,为异基因造血干细胞移植后急性移植物抗宿主病的预防及治疗提供一类新方法。本发明的表达载体表达效率更高,感染的效率更高,表达的稳定性更好。
附图说明
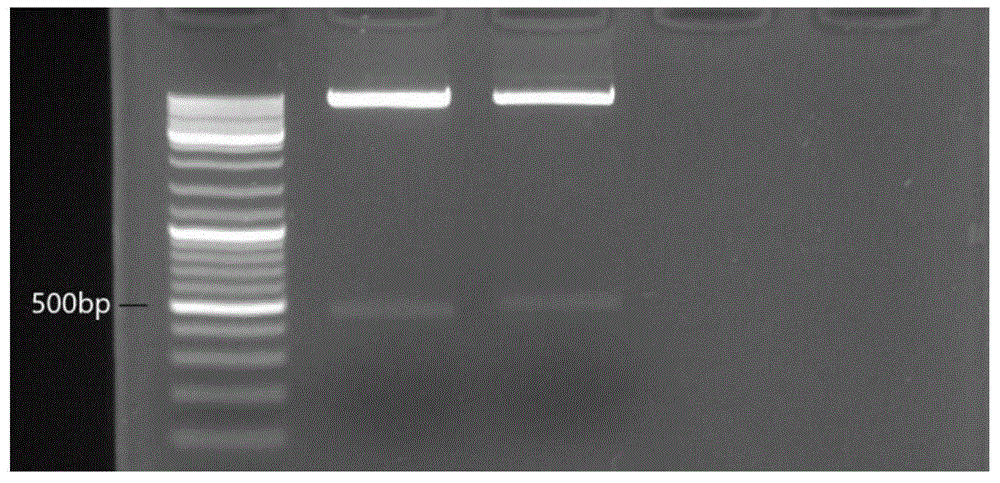
图1所示为重组慢病毒载体质粒pcdh-hifn-γ酶切鉴定结果;
图2所示为qpcr检测hifn-γ的表达结果;转干扰素-γ组与对照组相比,p<0.05,有统计学意义,同时空载组与对照组相比,p>0.05,二者无显著差异;
图3所示为elisa法检测hifn-γ蛋白的表达结果;转干扰素-γ组与对照组相比,p<0.05,hifn-γ的浓度为(459.9+2.232pg/ml),而空载组与对照组相比,p>0.05,无明显差异;
图4所示为humscs与t淋巴细胞共培养结果;与单独t细胞组相比,对照组(0.7707+0.02605),空载组(0.7494+0.06716)及转干扰素-γ组(0.4209+0.02816)p<0.05,其中转干扰素-γ组更加明显,p<0.05。
图5a所示为humscs与k562细胞共培养结果,与k562细胞组相比,对照组(0.5847+0.01067),空载组(0.5919+0.01780)及转干扰素-γ组(0.3450+0.006082)p<0.05,其中转干扰素-γ组更加明显,p<0.05;
图5b所示为humscs与hl-60细胞共培养结果;与hl-60细胞组相比,对照组(0.9223+0.02592),空载组(0.9759+0.02237)及转干扰素-γ组(0.6229+0.01476)p<0.05,其中转干扰素-γ组更加明显,p<0.05;
图5c所示为humscs与molm-13细胞共培养结果;与molm-13细胞组相比,对照组(0.7382+0.01877),空载组(0.7329+0.02198)及转干扰素-γ组(0.6345+0.006068)p<0.05,其中转干扰素-γ组更加明显,p<0.05;
图5d所示为humscs与thp-1细胞共培养结果;与thp-1细胞组相比,对照组(0.8344+0.001391),空载组(0.8059+0.02384)及转干扰素-γ组(0.8348+0.01519)p<0.05,三组之间无显著性差异,p<0.05;
图5e所示为humscs与u937细胞共培养结果;与u937细胞组相比,对照组(0.8763+0.009838),空载组(0.8785+0.03000)及转干扰素-γ组(0.8671+0.04155)p<0.05,三组之间无显著性差异,p<0.05。
具体实施方式
本发明提供了一种持续过表达ifn-γ的间充质干细胞,该间充质干细胞含有的重组载体中含有能持续编码ifn-γ的基因,能够持续过表达ifn-γ。
其中,上述持续过表达ifn-γ的间充质干细胞中,所述的持续编码ifn-γ的基因的核苷酸序列如seqidno:1所示。
其中,上述持续过表达ifn-γ的间充质干细胞中,所述的重组载体为病毒载体。进一步的,所述的病毒载体为慢病毒载体。
慢病毒载体作为一种外源性基因载体,是以hiv-1的主要功能元件为基础构建起来的基因治疗载体,该载体可以感染分裂的细胞,静止细胞及对难感染的原代细胞进行高效整合和表达,可携带10kb以内的基因片段,且由于其可持续表达、免疫反应小等特点,慢病毒载体成为体外细胞转染和基因治疗的有效工具。
本发明的表达载体特别的选用慢病毒载体,慢病毒载体具有以下优势:(1)慢病毒有更广泛的宿主,既可以感染分裂期的细胞,也可以感染静止期的细胞,尤其对于较难感染的细胞(原代细胞、干细胞、不分化的细胞等),能显著提高转染效率。(2)慢病毒感染宿主细胞,可以将目的基因整合到宿主染色体中,在其分裂和分化过程中不会丢失,可在体内长期、稳定表达。(3)相比腺病毒载体,慢病毒作为一种复制活性的假病毒,免疫活性低,不会引起宿主免疫反应。
其中,上述持续过表达ifn-γ的间充质干细胞中,所述的间充质干细胞为人脐带间充质干细胞。人脐带间充质干细胞来源广泛,可以从多种人体组织分离获得,如骨髓,脂肪,外周血,脐带及脐带血等;间充质干细胞具有非特异性的免疫抑制活性和免疫调节作用,可以作用于各种免疫细胞发挥对免疫系统的调节作用。
本发明还提供了一种上述持续过表达ifn-γ的间充质干细胞的制备方法,包括以下步骤:
构建表达ifn-γ的慢病毒载体,并包装病毒颗粒;复苏冻存的第3代人脐带间充质干细胞,换液、培养、传代后,选择第5代处于对数生长期的人脐带间充质干细胞,细胞生长至80~90%汇合时,用胰酶消化并计数,37℃、5%co2条件下培养过夜;病毒颗粒感染细胞,37℃、5%co2条件下培养24h后换液,48h后更换为筛选培养基,37℃、5%co2条件下培养,即获重组基因修饰的间充质干细胞。
进一步的,所述的筛选培养基为含1ug/ml嘌呤霉素的dmem/f12完全培养基。
本发明还提供了一种上述持续过表达ifn-γ的间充质干细胞在预防或治疗急性移植物抗宿主病中的用途。
下面将通过实施例对本发明的具体实施方式做进一步的解释说明,但不表示将本发明的保护范围限制在实施例所述范围内。
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
实施例1构建ifn-γ过表达载体
(1)选择目的基因:通过pubmed查找确定ifn-γ的cdna序列。目的基因的核苷酸序列如seqidno:1所示。
目的基因的引物如seqidno:2和seqidno:3所示。
上游引物:5’-cggaattcatgaaatatacaagttat-3’。(seqidno:2)
下游引物:5’-cgggatccttactgggatgctcttcga-3’。(seqidno:3)
限制性内切酶为:ecori和bamhi。
(2)目的基因和穿梭载体连接及结果分析鉴定:
将目的基因从质粒中进行pcr扩增,用ecori和bamhi两个限制性内切酶酶切pcdh载体和ifn-γ基因;用t4连接酶分别将ifn-γ基因和pcdh载体片段相连接从而构建重组质粒pcdh-ifn-γ。
目的基因扩增的基本流程如下:
①目的基因pcr
反应体系如下:50ul
ifn-γ:
pcr反应循环设置(每个pcr采用25个循环)
②目的基因和载体的酶切:胶回收pcr产物后再进行酶切。
酶切体系如下:进行酶切反应前测量确定待切样品浓度。
ifn-γ基因及pcdh酶切体系:
pcdh酶切:
pcdh1ug
ifn-γ基因酶切:
③目的基因与载体连接:
目的基因与载体的酶切产物在连接之前需进行胶回收,具体操作参见axygendna凝胶回收试剂盒(爱思进生物技术有限公司)。具体操作见说明书(axyprepdna凝胶回收试剂盒说明书)。
ifn-γ和pcdh连接反应体系(20ul):
自连体系(阴性对照):
pcdh酶切片段16μl
buffer2μl
t4连接酶2μl。
其中目的基因与载体按照摩尔比值:目的基因:载体=10:1,两者总体积为16ul,计算相应的体积加样。
④目的基因与载体连接后验证:
验证方式:pcr后电泳验证;酶切后电泳验证;目的基因测序验证。
实施例1成功构建得到了重组慢病毒载体质粒。对连接产物采用ecori和bamhi两个限制性内切酶进行酶切验证,琼脂糖电泳显示条带大小和位置为目的基因ifn-gamma(如图1所示)。
实施例2构建重组慢病毒载体
制备原理和流程如下:
慢病毒包装系统为三质粒系统,辅助质粒为pspax2、pmd2g(来自于由四川大学生物治疗国家重点实验室),其中筛选标记为嘌呤霉素。
(1)质粒制备:
使用tiangen无内毒素质粒大提试剂盒(天根生化科技有限公司,北京)进行质粒制备。
质粒的制备步骤详细按照天根无内毒素质粒大提试剂盒dp-117说明书进行。
(2)转染
①转染前24小时,用胰蛋白酶消化对数生长期的293t细胞,以含10%胎牛血清的dmem培养基调整细胞浓度6×10*5/ml,重新接种于10cm培养皿,置37℃含5%co2的培养箱中培养待细胞生长至底面积的70-80%时,可用于转染;
②转染前2-6h将细胞培养液更换为无血清培养液;
③取灭菌离心管配成相应病毒转染反应体系;
三质粒系统反应体系:1ml
④每孔加入1ml病毒悬液,37℃,3%co2培养箱中孵育;
⑤转染12小时后,更换新鲜10%血清的培养液,于37℃,5%co2培养箱内继续培养至48小时。
(3)病毒收集
转染293t细胞后,收集48小时培养上清,2000rpm,离心10min,收集上清并用0.22um滤器过滤去除细胞碎片,将病毒液分装,直接进行靶细胞感染或置于-80℃保存。
(4)慢病毒滴度检测
使用病毒基因组dna/rna提取试剂盒(天根生化科技有限公司,北京),并参照病毒基因组dna/rna提取试剂盒dp-315说明书步骤进行操作。
实施例3重组慢病毒质粒转染人脐带间充质干细胞
(1)humscs的复苏、传代
复苏:先将保种的三代humscs迅速从液氮中取出并置于37℃水箱中迅速复苏。300g,5分钟,去除上清,用含有10%胎牛血清和1%双抗(青霉素和链霉素)的dmem/f12培养基重悬,放置37℃、5%co2孵箱培养。
传代:当细胞长至约80-90%密度时,便可进行细胞传代。先用pbs缓冲液洗涤培养皿,弃pbs;加入0.2%的胰酶消化液1ml左右,humscs变圆脱落(在显微镜下观察);立即加入等体积的培养基终止反应,300g离心5min,弃上清,加入培养基重悬,按1:3进行传代,置于37℃、5%co2孵箱中培养。
(2)转染
当humscs长至70-80%时,胰酶消化细胞,按照1×10*5/孔细胞数加入到6孔板中,37℃、5%co2孵箱中培养过夜。待细胞贴融合度达30%后,加入上述收集病毒原液进行感染。24h后更换正常的培养液或筛选培养液(含1ug/ml嘌呤霉素的完全培养基)或进行相关检测。
(3)体外感染pcdh-ifn-γ后检测目的基因hifn-γ的表达水平
收集六孔板中的humscs,采用trizol法提取细胞总rna并测量其浓度(trireagent,mrc公司),使用takara去基因组逆转录试剂盒(clontech公司)将rna逆转录成cdna,采用实时荧光定量pcr法检测目的基因的表达量,其中hifn-γ基因正向引物为:5’-tgaatgtccaacgcaaagca-3’(seqidno:4),反向引物为:5’-ctgggatgctcttcgacctc-3’(seqidno:5)。mifn-γ基因正向引物为:5’-cagcaacagcaaggcgaaaaagg-3’(seqidno:6),反向引物为:5’-tttccgcttcctgaggctggat-3’(seqidno:7)。
qpcr结果显示,重组慢病毒修饰的humscs在目的基因的mrna相对表达水平上较对照组和空载组明显升高(p<0.05),同时对照组和空载组之间无明显差异(p>0.05)(如图2所示)。elisa检测结果与qpcr结果一致,与对照组相比,重组慢病毒修饰后的humscs能在培养上清中检测到hifn-γ蛋白的表达(如图3所示)。
实施例4过表达ifn-γ的humscs的体外实验研究
收集六孔板中培养基上清液,2000rpm,4℃,离心10分钟,留取上清,按照elisa试剂盒(杭州联科生物技术股份有限公司)操作说明(ek180-01)检测目的基因的表达。
(1)过表达ifn-γ的humscs与t淋巴细胞共培养
胰酶消化计数humscs,用rpmi1640完全培养基重悬后接种于96孔板,1*10^4/孔,每组设3个复孔,于37℃,5%co2孵育过夜。无菌条件下取健康成人静脉血5ml,淋巴细胞分离液ficoll分离单个核细胞(mnc)并计数,按1*10^4/孔接种于前述96孔板,200ul/孔,与humscs共培养。每孔同时加入抗cd3mab(1ug/ml),抗cd28mab(1ug/ml)(天津三箭生物公司)。72小时后,轻轻吹匀后,取100ul细胞悬液加入新的96孔板,每孔加入10ulcck-8(cck-8细胞活性检测试剂盒,大连美仑生物技术有限公司),继续孵育4小时,酶标仪检测各孔od值。
结果显示:humscs对t淋巴细胞增殖有抑制作用。humscs和t淋巴细胞共培养72h后,与单独的t细胞组相比,共培养结果提示humscs对t淋巴细胞增殖有抑制作用(如图4所示),其中hifn-γ组较对照组和空载组抑制作用更加明显(p<0.05)。
(2)过表达ifn-γ的humscs与白血病细胞共培养
胰酶消化计数humscs,用rpmi1640完全培养基重悬后接种于96孔板,1*10^4/孔,每组设3个复孔,于37℃,5%co2孵育过夜。将白血病细胞系按1*10^4,200ul/孔接种于前述96孔板,与humscs共培养。72小时后,取细胞悬液100ul于96孔板中,每孔加入10ulcck8,37℃,5%co2孵育4小时后,设置酶标仪在450nm处检测各孔od值。
结果显示:humscs对白血病细胞系增殖有抑制作用(如图5a-5e所示)。humscs与白血病细胞共培养72h后,cck8检测结果提示humscs对白血病细胞系增殖有抑制作用,其中k562、hl-60、molm-13细胞系,转干扰素-γ组较对照组和空载组抑制作用更加明显(p<0.05)(图5a-5c),而在thp-1和u937细胞系中,三组之间的抑制作用无明显差异(p>0.05)(图5d-5e)。
本发明构建了能够持续过表达ifn-γ的人脐带间充质干细胞,并将重组的间充质干细胞与t淋巴细胞和白血病细胞共培养,结果显示本发明的重组间充质干细胞对t淋巴细胞增殖和白血病细胞系增殖都有显著的抑制作用。因此,本发明的重组间充质干细胞可用在异基因造血干细胞移植后的机体内同时发挥抗肿瘤及免疫作用,能够降低agvhd的发生率或严重程度,同时不影响gvl效应。本发明为异基因造血干细胞移植后agvhd的预防及治疗提供了一种新的方法,具有很好的现实意义。
序列表
<110>四川大学
<120>持续过表达ifn-γ的间充质干细胞及其用途
<130>a191205k
<141>2019-11-04
<160>7
<170>siposequencelisting1.0
<210>1
<211>501
<212>dna
<213>人工序列(artificialsequence)
<400>1
atgaaatatacaagttatatcttggcttttcagctctgcatcgttttgggttctcttggc60
tgttactgccaggacccatatgtaaaagaagcagaaaaccttaagaaatattttaatgca120
ggtcattcagatgtagcggataatggaactcttttcttaggcattttgaagaattggaaa180
gaggagagtgacagaaaaataatgcagagccaaattgtctccttttacttcaaacttttt240
aaaaactttaaagatgaccagagcatccaaaagagtgtggagaccatcaaggaagacatg300
aatgtcaagtttttcaatagcaacaaaaagaaacgagatgacttcgaaaagctgactaat360
tattcggtaactgacttgaatgtccaacgcaaagcaatacatgaactcatccaagtgatg420
gctgaactgtcgccagcagctaaaacagggaagcgaaaaaggagtcagatgctgtttcga480
ggtcgaagagcatcccagtag501
<210>2
<211>26
<212>dna
<213>人工序列(artificialsequence)
<400>2
cggaattcatgaaatatacaagttat26
<210>3
<211>27
<212>dna
<213>人工序列(artificialsequence)
<400>3
cgggatccttactgggatgctcttcga27
<210>4
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>4
tgaatgtccaacgcaaagca20
<210>5
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>5
ctgggatgctcttcgacctc20
<210>6
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>6
cagcaacagcaaggcgaaaaagg23
<210>7
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>7
tttccgcttcctgaggctggat22
- 还没有人留言评论。精彩留言会获得点赞!