用于检测产毒无乳链球菌的荧光定量PCR方法及相应的试剂盒与流程
本发明属于分子检测技术领域,具体涉及一种通过特异性基因对产毒无乳链球菌进行荧光定量pcr检测的方法和相应的检测试剂盒。
背景技术:
无乳链球菌(streptococcusagalactiae)是一种成对或成短链状排列的革兰氏阳性球菌。它是一种具有β-溶血性、过氧化氢酶阴性、vp试验阳性的兼性厌氧型细菌。无乳链球菌也称b群链球菌,根据其多糖荚膜的免疫学活性,无乳链球菌可划分为10个血清型(ia、ib、ii–ix)。
一般来说,无乳链球菌是一种无害的共生型细菌,它是人类微生物菌群的一部分,这些微生物群在30%的健康人类成年人的胃肠道和泌尿生殖道中定殖,当人体免疫功能降低时,会给无乳链球菌感染提供机会。然而,亦可引起严重的侵入性感染,是侵入性新生儿感染的重要致病菌。
无乳链球菌是造成孕妇产褥期脓毒血症和新生儿脑膜炎的一个重要原因。它寄生在产妇生殖道,可致婴儿感染的发生。新生儿感染有两种不同的临床类别:早发型新生儿感染,其特点为出生后7日内出现脓毒症、脑膜炎与肺炎;晚发型新生儿感染,出生后7日~3月之间出现脑膜炎与脓毒症。
目前,国内外对无乳链球菌及其病原学、分子流行病学进行了大量研究,建立了很多有效的分离鉴定方法,包括乳胶凝集试验、β-溶血试验、环磷酸腺苷(camp)elisa检测等。这些方法不仅耗时、灵敏度低,而且出现的反应并非无乳链球菌所在b群菌株的特异性反应,c、f、g群部分链球菌亦可出现阳性结果。近年来,荧光定量pcr检测技术以其高灵敏度、高特异性、实验周期短等优势逐步应用于无乳链球菌的检测。
技术实现要素:
本发明的目的之一是提供一种用于检测产毒无乳链球菌的荧光定量pcr方法。
具体地,上述方法包括如下步骤:
s1、收集样品;
s2、提取基因组dna;
s3、检测无乳链球菌属特异性基因rpob以及产毒特异性基因gene1、gene2、gene3和gene4;
s4、读取扩增ct值;当所述无乳链球菌属特异性基因和所述产毒特异性基因中至少1个基因的ct值均小于35时,产毒无乳链球菌的检测结果为阳性;当所述无乳链球菌属特异性基因rpob的ct值大于35和/或所述产毒特异性基因gene1、gene2、gene3和gene4的ct值大于35时,产毒无乳链球菌的检测结果为阴性。
作为一种优选技术方案,所述无乳链球菌属特异性基因rpob(ncbiaccessionnumber:dq232501.1)的检测引物如seqidno:1~2所示;
seqidno:1(5'-acaacttcgaggatgcggtt-3');
seqidno:2(5'-cccatttcgtccaagttgcg-3')。
所述产毒特异性基因gene1(ncbiaccessionnumber:ayy67640.1)的检测引物如seqidno:3~4所示;
seqidno:3(5'-atgcagggccgagaaactc-3');
seqidno:4(5'-accaatcaccccaacgtcat-3')。
所述产毒特异性基因gene2(ncbiaccessionnumber:ayz04668.1)的检测引物如seqidno:5~6所示;
seqidno:5(5'-tcgaagaagcaggctacaagg-3');
seqidno:6(5'-tcaaccaaacctgcttcaactg-3')。
所述产毒特异性基因gene3(ncbiaccessionnumber:ayz05235.1)的检测引物如seqidno:7~8所示;
seqidno:7(5'-ccaaaccctcaaagcacagg-3');
seqidno:8(5'-tgggagcaatgtgggagatg-3')。
所述产毒特异性基因gene4(ncbiaccessionnumber:ayz05496.1)的检测引物如seqidno:9~10所示;
seqidno:9(5'-acaaaacacatcgcccttgc-3');
seqidno:10(5'-tctctggcaacccgttcttc-3')。
本发明另一目的是提供一种用于检测产毒无乳链球菌的荧光定量pcr试剂盒,其包含上述的无乳链球菌属特异性基因rpob的检测引物和产毒特异性基因gene1、gene2、gene3和gene4的检测引物。
与现有技术相比,本发明具有如下有益效果:
(1)本发明通过前期对无乳链球菌属和其他链球菌属,产毒和非产毒链球菌属的微生物的大量研究数据中,挖掘出能够区分无乳链球菌属和其他链球菌属,产毒和非产毒链球菌属的特异性的孤儿基因,通过对特异性基因的检测,准确的判断出菌类样品和环境样品中是否含有产毒的无乳链球菌,具有前期大数据的挖掘和不同种属之间比对基础,选择的特异性基因具有物种和菌属的特异性。
(2)本发明中,通过对设计条件和实验条件的优化,选取针对于每个基因检测扩增条件处于最优化的引物作为检测引物,提高引物扩增的效率,能够达到稳定、高效、高灵敏度和重现性的检测引物,实现微量样品的正确检出。
(3)本发明检测方法与市面上其他的检测方法相比,本发明的两部分检测策略,能够分步判断无乳链球菌属和其他链球菌属、产毒和非产毒链球菌属,判断必须两项同时阳性检出才最终判断为产毒无乳链球菌,结果更加严谨和准确。
(4)本发明能够实现从10个阳性菌到10000个阳性菌的检测范围,灵敏度高,应用范围广,更高浓度的样品可以通过稀释折算同样被检测出来,检测结果稳定,具有很好的重现性。
(5)本发明检测方法能够应用于对于临床医学中的阴道分泌物、皮肤分泌物、尿液和粪便排泄物、过滤水等多方面来源临床样品筛查和检测,精准地判断出该临床样品中是否含有产毒无乳链球菌,操作方便、快速、灵敏。本发明检测试剂盒能够应用于多种临床样品的快速检验,无需额外进行微生物培养,使基因检验在日常民生中得到应用,具有灵敏度高、操作性强、快速、高效等优点。
附图说明
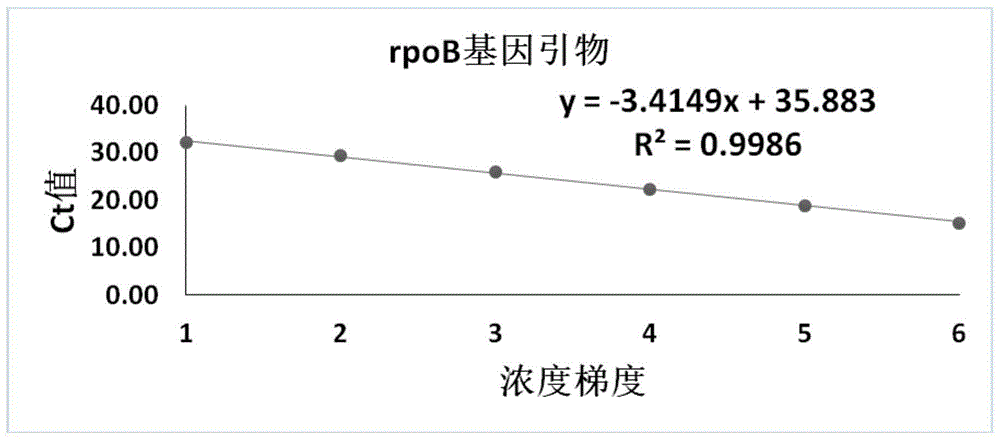
图1是rpob基因检测引物标准曲线。
图2的gene1基因检测引物标准曲线。
图3是gene2基因检测引物标准曲线。
图4是gene3基因检测引物标准曲线。
图5是gene4基因检测引物标准曲线。
具体实施方式
为了能够更清楚地理解本发明的技术内容,特举以下实施例结合附图详细说明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(newyork:coldspringharborlaboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。实施例中所用到的各种常用化学试剂,均为市售产品。
本发明所用的以下试剂可通过常规途径购买得到。
表1
在一些实施方案中,使用扩增产物构建阳性标准品质粒,并进行引物的扩增标准曲线检测和绘制,得到每对检测引物的扩增效率,本发明所提供的引物序列其扩增效率和置信程度均在最优化的水平。
在一些实施方案中,通过对不同的阳性菌株检测特异性的基因,能够正确的区分出无乳链球菌属和其他链球菌属,产毒和非产毒链球菌属,从而准确检测并判断出产毒无乳链球菌。
在一些实施方案中,通过对10个、100个、1000个和10000个阳性菌进行提取和检测,能够精确区分出无乳链球菌属和其他链球菌属,产毒和非产毒链球菌属,从而准确检测并判断出产毒无乳链球菌。并且能够保证低至10个阳性菌仍然能够准确检出,而更高滴度的微生物样品可以通过稀释至检测区间,同样可以准确检出。
在一些实施方案中,采集肺阴道分泌物、皮肤分泌物、尿液、粪便、过滤水的样品,通过对特异性基因的检测,能够快速和准确的检验出样品中是否含有产毒无乳链球菌,方便快捷。
本领域技术人员应能理解,本方法中检测的基因和设计的特异性引物,同样可以通过相同检测对象的其他区段的设计达到相应的检测目的。
本发明所描述的用于检测产毒无乳链球菌荧光定量pcr的方法及试剂盒可以广泛应用于临床检测中组织灌洗液检测、体外分泌物的检测以及排泄物的检测等多个临床医学检验范畴,能够为临床医学检测提供方便、快捷、准确、高效的基于基因检测的监控产品。
实施例1检测引物扩增标准曲线
1.微生物培养
使用碱性蛋白胨水作为无乳链球菌的培养基,ph8.8~9.0的碱性蛋白胨水或平板中生长良好。在碱性平板上菌落直径为2mm,圆形,光滑,透明。选取处于生长旺盛的微生物样品进行后续的实验。
2.基因组dna提取
按照qiagen的qiaampdnaminikit说明书指示进行基因组dna的提取。
3.扩增产物标准品质粒制作
使用源自无乳链球菌提取的dna,分别以rpob基因、gene1、gene2、gene3和gene4的引物进行扩增,扩增产物经过加a处理后,使用t4连接酶连入t载体,并且通过转导感受态细胞后,质粒得到大规模扩增。5个基因的引物序列如seqidno:1~10所示,具体如表2。
表2
4.质粒的提取和标准曲线梯度的配置
分别涂板扩增rpob基因、gene1、gene2、gene3和gene4对应的引物扩增产物的标准品克隆菌,收集单克隆的菌斑,并通过lb培养摇菌过夜扩增,最后得到5ml指数生长期的质粒阳性菌株,按照qiagenplasmidmidikit说明书指示进行质粒dna的提取。提取后检测质粒dna的浓度,并通过10倍稀释的方法,配置6个浓度梯度的标准品,浓度梯度分别为1μg/μl,100ng/μl,10ng/μl,1ng/μl,100pg/μl,10pg/μl。
5.检测引物标准曲线绘制
按照bioradiqsybrgreensupermix说明书指示进行浓度梯度标准曲线的qpcr扩增,并且绘制对应的扩增曲线,得到每对引物的扩增效率。每一个qpcr的反应设置3个生物学重复及3个技术重复,qpcr反应体系和扩增反应条件如表3所示。
表3
6.结果分析
检测引物扩增标准曲线结果显示,rpob基因、gene1、gene2、gene3和gene4对应的引物均为经过优化的引物设计和反应体系。其中线性的标准曲线可信度r2>0.980,高扩增效率在90-105%,证明引物设计和反应体系是最优状态。分析5个基因的扩增曲线的相关性系数和可信度,以及6个浓度梯度下的扩增效率,均达到最优状态的要求,5对引物在该反应条件下能够满足检测要求。
表4
实施例2阳性及阴性样品检测情况
1.微生物培养
同实施例1。
2.基因组dna提取
同实施例1。
3.5个目标基因的qpcr检测
按照bioradiqsybrgreensupermix说明书指示进行样品的qpcr扩增,并且得到每对引物对应的ct值读数。每一个qpcr的反应设置3个生物学重复及3个技术重复,qpcr反应体系和扩增反应条件如表5所示。
表5
4.结果分析
如表6和表7所示,5对引物的qpcr扩增结果显示,无乳链球菌属呈现rpob基因的阳性结果,而其他链球菌属均显示阴性结果。因此,对于无乳链球菌属和其他链球菌属,进行rpob基因的检测,能够较好的区分无乳链球菌属和其他链球菌属。同时,gene1、gene2、gene3和gene4的检测结果,产毒的链球菌属呈现检测结果阳性,而其他非产毒无乳链球菌属和其他链球菌属呈现阴性。因此,进行gene1、gene2、gene3和gene4的检测,能够较好的区分产毒和非产毒的链球菌属。综上所述,rpob基因的对应引物,能够满足链球菌属中无乳链球菌属的检测判断,gene1、gene2、gene3和gene4的对应引物,能够满足产毒和非产毒链球菌属的检测判断。
表6
表7
实施例3检测体系的灵敏度
1.微生物培养
使用碱性蛋白胨水作为无乳链球菌的培养基,ph8.8~9.0的碱性蛋白胨水或平板中生长良好。在碱性平板上菌落直径为2mm,圆形,光滑,透明。选取处于生长旺盛的微生物样品进行后续的实验,收集菌体后进行浓度计算,并且10稀释得到10个菌/ml,100个菌/ml,1000个菌/ml,和10000个菌/ml,对不同浓度梯度的菌液进行后续的dna提取实验。
2.基因组dna提取
同实施例1。
3.5个目标基因的qpcr检测
同实施例2。
4.结果分析
如表8和表9所示,5对引物的qpcr扩增结果显示,从10个菌至10000个菌的范围内,无乳链球菌属呈现rpob基因的阳性结果。因此,通过进行rpob基因的检测,能够较好的达到从10个菌至10000个菌的范围内无乳链球菌属的检出。同时,从10个菌至10000个菌的范围内,gene1、gene2、gene3和gene4基因的检测结果,产毒的链球菌属呈现检测结果阳性,而其他非产毒链球菌属呈现阴性。因此,进行gene1、gene2、gene3和gene4基因的检测,能够较好的达到从10个菌至10000个菌的范围内产毒和非产毒的链球菌属的检测和区分。综上所述,可以通过rpob基因、gene1、gene2、gene3和gene4的搭配检测,较好的完成产毒无乳链球菌的检测,检测范围可以从10个菌株至10000个菌株,更高的菌株浓度也可以通过稀释的方法稀释至最佳检测范围内,能够达到预期的检测要求。
表8
表9
实施例4临床样品的检测
1.临床样品收集和基因组dna的提取
分别收集不同的阴道分泌物、皮肤分泌物、尿液、粪便和过滤水,按照qiagen的qiaampdnaminikit说明书指示进行基因组dna的提取。
2.5个目标基因的qpcr检测
同实施例2。
3.结果分析
表10和表11所示,5对引物的qpcr扩增结果显示,除了一个粪便样本和过滤水,其他样品均检出rpob基因,证明相应的样品来源中含有无乳链球菌。而除了一个阴道分泌物样本、一个尿液样本、粪便样本、皮肤分泌物样本和过滤水外,其他样品均检出gene1、gene2、gene3和gene4基因的一个或者两个,证明对应的样品来源中含有产毒的链球菌。最终判断为产毒无乳链球菌阳性的准则为,rpob基因检测得到ct值小于35个循环,同时gene1、gene2、gene3和gene4基因中的一个及以上检测得到ct值小于35个循环。如果rpob基因检测得到ct值大于35个循环,或者,gene1、gene2、gene3和gene4基因均检测得到ct值大于35个循环,则判断为产毒无乳链球菌阴性未检出。
表10
表11
以上实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
以上实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
序列表
<110>广州微芯生物科技有限公司
<120>用于检测产毒无乳链球菌的荧光定量pcr方法及相应的试剂盒
<160>10
<170>siposequencelisting1.0
<210>1
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>1
cactagtccgtgcacttggt20
<210>2
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>2
accaacagccgctaagtcat20
<210>3
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>3
tcttacggctacttcttcggc21
<210>4
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>4
ccaacccaagaagccattgac21
<210>5
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>5
ggctgagtttgttatggcgaat22
<210>6
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>6
tgacattttgctcatccataccg23
<210>7
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>7
caggttctgctgctatcggt20
<210>8
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>8
tgttaacccttgaccaccatact23
<210>9
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>9
gcaacgatgtctggataggaac22
<210>10
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>10
ccaattccaccactgagatgc21
- 还没有人留言评论。精彩留言会获得点赞!