卡宾化合物、卡宾–金属纳米粒子复合物及其制备方法与流程
本发明涉及一种卡宾化合物、卡宾–金属纳米粒子复合物(complex)及其制备方法。
背景技术:
金的价值在工业和现实生活中非常重要,并且取决于其尺寸和形状,金在各种领域(半导体存储器件、有机化学反应催化剂、下一代能源、侧向层析检测(lfa)、生物传感器等)中显示出独特的物理和化学性质。近年来,由于纳米科学的发展,其应用范围随着金加工方法(如金纳米制造)的发展而更加多样化。
随着金纳米探针(纳米颗粒、纳米棒等)的大规模生产技术的发展,金纳米探针已经用于生物工业中疾病的诊断和治疗,但是在金纳米探针中,特别是金表面处理技术对性能具有非常大的影响。在此金表面处理中,由于在水或有机溶剂中的分散性、生物探针部分的易粘接性等优点,使用烷基胺、羧酸(癸酸、柠檬酸等)、硫醇、铵等的常规处理方法已被广泛使用。
其中,硫醇对金(au)具有高结合强度。此外,在高盐浓度溶液和酸/碱溶液中,硫醇–金键在其表面上不稳定,从而发生聚集,特别是在60℃以上和0℃以下,聚集非常严重,因此对产品的储存存在严重限制。例如,金纳米探针作为在lfa中用于现场诊断的产品被释放,以通过用硫醇围绕其表面来实现水性分散,并且需要冷藏。然而,当生物探针部分(例如抗体、dna等)被固定在金纳米颗粒上时,产品不能被冷藏,结果,存在产品需要立即使用的缺点。另外,由于lfa产品的特性,由于产品也被输送到许多炎热区域,例如非洲,因此需要能够承受高温的具有高稳定性的金纳米探针。
为了解决上述问题,因为卡宾化合物和金原子之间的反应性高且能够强结合的优点,在相关技术中,使用了通过使咪唑盐与金离子反应形成有机金属复合物,然后进行还原反应,来制备卡宾–金纳米颗粒的方法(j.am.chem.soc.2015,137,7974-7977),但是金纳米颗粒的形状或大小似乎不均匀。此外,苯并咪唑盐被阴离子转化为金酸根离子,并且有机金属复合物的形成和还原反应在低温(0.6℃)下同时进行,以合成均匀形式的金纳米颗粒(chem.mater.2015,27,414-423),但是因为金纳米颗粒是在有机溶剂中合成,所以存在金纳米颗粒在水中不分散且不能应用于生物传感器的缺点。另外,首先,常规的卡宾–金纳米粒子在末端没有官能团,因此不可能应用于生物传感器等。
【现有技术】
(专利文献1)美国专利公开号2006/0100365(2006年5月11日)
技术实现要素:
【技术问题】
本发明的目的是通过合成在末端含有官能团以稳定卡宾金属纳米颗粒表面的卡宾化合物,提供一种即使在高浓度盐溶液、强酸或强碱、高温和超低温的各种环境下也具有化学和物理稳定性的卡宾–金纳米颗粒复合物,以用于生物传感器领域,例如lfa等。
【技术方案】
本发明提供了一种由以下化学式1或2表示的卡宾化合物,其被末端具有含氮官能团的聚乙二醇(peg)取代:
[化学式1]
在上述化学式1和2中,
r1、r2、r5和r6彼此相同或不同,并且各自独立地为氢、具有1至20个碳原子的烷基、具有3至20个碳原子的环烷基、具有6至30个碳原子的芳基或具有2至30个碳原子的杂芳基,
r3、r4、r7、r8、r9和r10彼此相同或不同,并且各自独立地为氢、具有1至20个碳原子的烷基、具有3至20个碳原子的环烷基、具有6至30个碳原子的芳基、具有2至30个碳原子的杂芳基、或由以下化学式3表示的结构,或者r7至r10中彼此相邻的两个或更多个取代基彼此结合形成烃环,
r3和r4中的至少一个是由以下化学式3表示的结构,
r7至r10中的至少一个是由以下化学式3表示的结构,或者当r7至r10中彼此相邻的两个或更多个取代基彼此结合形成烃环时,结合至形成烃环的碳的至少一个氢被由以下化学式3表示的结构取代,
[化学式3]
在上述化学式3中,
n是1至30的整数,作为括号内重复单元的数量,且
a是含有氮(n)原子的碳原子数为1至20的芳香族烃基或含有氮(n)原子的碳原子数为2至30的脂肪族烃基。
此外,本发明还提供了卡宾–金属纳米颗粒复合物,其中上述卡宾化合物与金属纳米颗粒结合。
本发明提供了一种卡宾–金属纳米粒子复合物的制备方法,包括将金属纳米粒子与含有硫醇基的聚乙二醇混合;和混合上述卡宾化合物和与含有硫醇基的与聚乙二醇结合的金属纳米颗粒。
此外,本发明提供了一种包含上述卡宾–金属纳米粒子复合物的生物传感器。
【有益效果】
根据本发明,由于卡宾化合物具有优异的稳定性,在通过将卡宾化合物与金属结合而制备的卡宾–金属纳米颗粒复合物中,与常规的金属纳米颗粒相比,即使在各种类型的溶剂和各种ph或温度范围内,卡宾化合物也不容易与金属纳米颗粒分离。因此,本发明的卡宾–金属纳米粒子复合物用于更牢固地固定生物探针部分(生物材料),并可有效地应用于生物传感器等。
附图说明
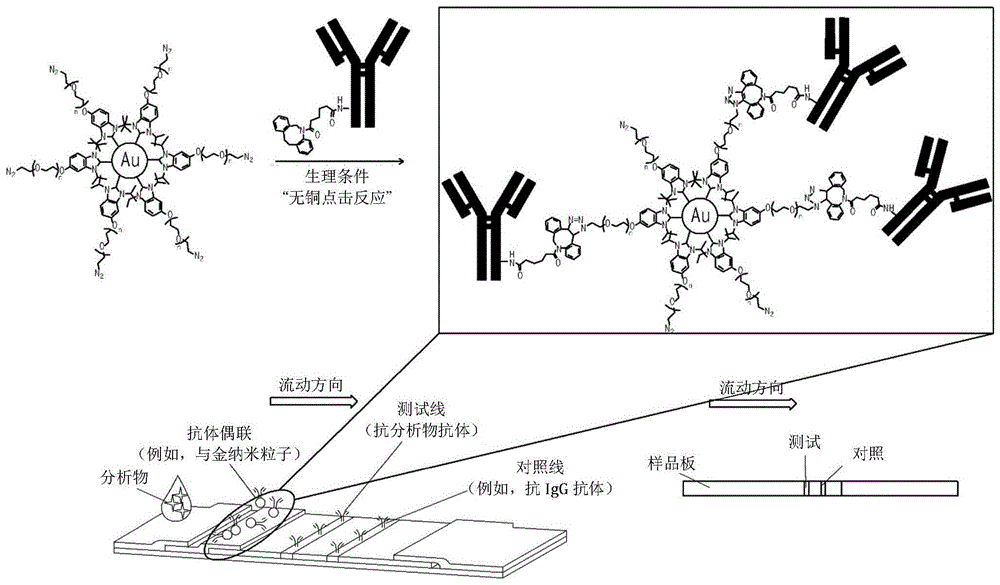
图1是示出根据本发明的实施方案的使用卡宾–金纳米颗粒络合物的lfa的示意图。
图2是示出本发明实验例1的ph稳定性的实验结果的图。
图3是示出本发明实验例2〈1〉的盐稳定性实验结果的图。
图4是示出本发明实验例2〈2〉的溶剂稳定性的实验结果的图。
图5是示出本发明实验例3〈1〉中的温度稳定性的实验结果的图。
图6是示出本发明实验例3〈2〉的金纳米粒子的温度稳定性的实验结果的图。
图7是示出本发明实验例4的疟疾诊断试剂盒的实验结果的图。
图8是示出本发明实验例5的ph稳定性的实验结果的图。
图9是示出本发明实验例6的高温稳定性的实验结果的图。
图10是示出本发明实验例7的低温稳定性实验结果的图。
图11是示出根据本发明制备实施例1制备的卡宾化合物的1h-nmr光谱的图。
图12是示出根据本发明制备实施例3制备的卡宾化合物的1h-nmr光谱的图。
图13是示出根据本发明制备实施例4制备的卡宾化合物的1h-nmr光谱的图。
图14是示出根据本发明制备实施例5制备的卡宾化合物的1h-nmr光谱的图。
图15是示出根据本发明制备实施例6制备的卡宾化合物的1h-nmr光谱的图。
图16是示出本发明一个实施方式的卡宾–金属纳米粒子复合物的tem图像的图。
图17是比较金–硫键和金–卡宾键的结合能/键距的图。
具体实施方式
以下,将详细描述本发明。
1.卡宾化合物
本发明提供了一种由以下化学式1或2表示的卡宾化合物,其被末端具有含氮官能团的聚乙二醇(peg)取代。
卡宾化合物可以通过将用含氮官能团取代的聚乙二醇(peg)引入到末端来制备。
卡宾化合物通过引入聚乙二醇基团到其末端位点以增加水分散性,并将含氮官能团引入到聚乙二醇末端以官能化,从而通过以下点击反应(clickreaction)促进生物探针部分(例如抗体、dna、适体、引物等)粘附到含氮官能团。因此,在lfa等中,与生物探针部分通常通过金属纳米颗粒之间的静电吸引结合不同,存在生物探针部分可以通过点击反应用强化学共价键固定的优点。
含氮官能团可以是叠氮化物、邻苯二甲酰亚胺或胺。
r1、r2、r5和r6可以彼此相同或不同,并且各自独立地为氢、具有1至20个碳原子的烷基或具有6至30个碳原子的芳基。
r1、r2、r5和r6可以彼此相同或不同,并且各自独立地为氢或具有1至20个碳原子的烷基。
r1、r2、r5和r6可以彼此相同或不同,并且各自独立地为氢、异丙基或苄基。
r1和r2中的至少一个与r5和r6中的至少一个可以彼此相同或不同,并且各自独立地为具有1至20个碳原子的烷基或具有6至30个碳原子的芳基。
r1和r2中的至少一个和r5和r6中的至少一个可以彼此相同或不同,且各自独立地为异丙基或苄基。
r3、r4、r7、r8、r9和r10彼此相同或不同,各自独立地为氢、具有1至20个碳原子的烷基、具有3至20个碳原子的环烷基、具有6至30个碳原子的芳基、具有2至30个碳原子的杂芳基、或由以下化学式3表示的结构,或者r7至r10中彼此相邻的两个或更多个取代基彼此结合形成烃环。
r3、r4、r7、r8、r9和r10彼此相同或不同,各自独立地为氢或由以下化学式3表示的结构,或者r7至r10中彼此相邻的两个或更多个取代基彼此结合以形成烃环。
当r7至r10中两个或多个彼此相邻的取代基彼此结合形成烃环时,结合至形成烃环的碳的至少一个氢可被化学式3表示的结构取代。
r3和r4中的至少一个可以是由化学式3表示的结构。此外,r7至r10中的至少一个可以是由化学式3表示的结构。
n可以是1至30的整数,作为括号中重复单元的数量,且优选1至10。当n小于1时,卡宾化合物的水分散性降低,当n大于30时,生物探针部分之间的距离由于聚乙二醇的长链而增加,因此,生物传感效率反而降低。
a是含有氮(n)原子的碳原子数为1至20的烷基或含有氮(n)原子的碳原子数为2至30的杂芳基。具体地,a可以是叠氮化物、邻苯二甲酰亚胺或胺。
在本发明中,“相邻”基团可以指取代至直接与被相应取代基取代的原子连接的原子的取代基、立体上最接近相应取代基的取代基、或取代至被相应取代基取代的原子的另一取代基。例如,在苯环的邻位取代的两个取代基和在脂族环中取代至相同碳的两个取代基,被解释为彼此“相邻”的基团。
烷基可以是直链或支链,并且可以具有1至20个碳原子,优选1至10个碳原子。更优选地,烷基可以具有1至6个碳原子。烷基的具体实例包括甲基、乙基、丙基、正丙基、异丙基、丁基、正丁基、异丁基、叔丁基、仲丁基、1-甲基丁基、1-乙基丁基、戊基、正戊基、异戊基、新戊基、叔戊基、己基、正己基、1-甲基戊基、2-甲基戊基、4-甲基-2-戊基、3,3-二甲基异丁基、2-乙基丁基、庚基、正庚基、1-甲基己基、环戊基甲基、环己基甲基、辛基、正辛基、叔辛基、1-甲基庚基、2-乙基己基、2-丙基戊基、正壬基、2,2-二甲基庚基、1-乙基丙基、1,1-二甲基丙基、己基、4-甲基己基、5-甲基己基、苄基等,但不限于此。
环烷基可以具有3至20个碳原子,优选3至10个碳原子。环烷基的具体实例包括环丙基、环丁基、环戊基、3-甲基环戊基、2,3-二甲基环戊基、环己基、3-甲基环己基、4-甲基环己基、2,3-二甲基环己基、3,4,5-三甲基环己基、4-叔丁基环己基、环庚基、环辛基等,但不限于此。
芳基可以具有6至30个碳原子,优选6至10个碳原子。芳基可以是单环芳基或多环芳基。单环芳基的具体实例包括苯基、联苯基、三联苯基等,多环芳基的具体实例包括萘基、蒽基、菲基、芘基、苝基、
杂芳基可以是包括选自n、o、p、s、si和se中的一种或多种作为杂原子的芳族环基,并且可以具有2至30个碳原子,优选2至20个碳原子。杂芳基的具体实例包括噻吩基、呋喃基、吡咯基、咪唑基、噻唑基、噁唑基、噁二唑基、三唑基、吡啶基、嘧啶基、三嗪基、三唑基、丙烯酰胺基、喹啉基、喹唑啉基、喹喔啉基、酞吡啉基、异喹啉基、吲哚基、咔唑基、苯并噁唑基、苯并咪唑基、苯并噻唑基、苯并咔唑基、苯并噻吩基、二苯并噻吩基、苯并呋喃基等,但不限于此。
另外,烷基、环烷基、芳基、杂芳基或烃环可以再次被烷基、环烷基、芳基或杂芳基取代或未取代。
2.卡宾–金属纳米粒子复合物及其制备方法
本发明还提供卡宾–金属纳米颗粒复合物,其中上述卡宾化合物与金属纳米颗粒结合。
金属纳米颗粒的粒径可以是1nm至40nm。当金属纳米颗粒的粒径小于1nm时,难以将所需水平的卡宾化合物引入到金属纳米颗粒的表面,因此,作为生物传感器的效率劣化。当金属纳米颗粒的粒径大于40nm时,卡宾–金属纳米颗粒复合物不均匀,因此,生物传感器的效率和再现性可能劣化。即,如果金属纳米粒子的粒径超过40nm,则仅通过环境的微小变化,金属纳米粒子可能发生团聚的可能性增加。
金属纳米颗粒可以是选自由铜(cu)、钴(co)、铋(bi)、银(ag)、铝(al)、金(au)、铪(hf)、铬(cr)、铟(in)、锰(mn)、钼(mo)、镁(mg)、镍(ni)、铌(nb)、铅(pb)、钯(pd)、铂(pt)、铼(re)、铑(rh)、锑(sb)、钽(ta)、钛(ti)、钨(w)、钒(v)、锆(zr)、锌(zn)、铁(fe)及其混合物组成的组中的任一种(例如,双金属纳米颗粒)。考虑到应用卡宾–金属纳米粒子复合物的生物传感器在各种环境中的稳定性和可结晶性以及卡宾化合物与金属纳米粒子表面之间的结合力,金属优选为金(au)。
卡宾–金属纳米粒子复合物可具有均匀的形式,如图16的tem图像所示,并且水分散性变得优异,因为卡宾–金属纳米粒子复合物具有均匀的形式。
此外,本发明提供一种制备卡宾–金属纳米粒子复合物的方法,其包括通过将在一个末端含有硫醇基且在另一末端含有含氮官能团的聚乙二醇与金属纳米粒子混合来制备硫–金属纳米粒子,并将所述硫–金属纳米粒子与上述卡宾化合物混合。
具体地,在将在一个末端含有硫醇基和在另一个末端含有含氮官能团的聚乙二醇与金属纳米颗粒混合的情况下,可以通过在金属表面上介导硫醇基的硫的金属–硫键,将在末端含有含氮官能团的聚乙二醇引入到金属纳米颗粒的表面。当将上述本发明的卡宾化合物引入到上述形成的硫–金属纳米粒子中时,在金属纳米粒子表面存在的金属–硫键被金属–卡宾键取代,最终形成卡宾–金属纳米粒子复合物。
此时,用金属–卡宾键取代金属纳米颗粒表面上存在的金属–硫键的反应可以在室温(20℃至30℃)下发生。由于金属–卡宾键的结合力强于上述已知的金属–硫键的结合力,因此即使在室温下放置1至10小时,也可能发生取代反应。特别地,参考图17,当金属是金(au)时,金–卡宾键的强度(结合能:-63.55kcal/mol,键距离:
由于如上所述氮基团暴露于末端,卡宾–金属纳米粒子复合物具有更容易结合生物探针部分(生物材料)的优点。特别是,与金属–硫键不同,由于金属–卡宾键的稳定性,即使在高浓度盐条件、强酸或弱碱条件、高温和超低温的各种环境中,金属–卡宾键也被保持,从而存在卡宾–金属纳米颗粒复合物不会发生团聚的效果。
3.生物传感器
本发明提供了一种包含上述卡宾–金属纳米粒子复合物的生物传感器。
所述生物传感器,特别是,其颜色随金属纳米颗粒的颗粒尺寸、材料、形状和周围环境而改变,且结果是,所述生物传感器可以是使用改变的金属纳米颗粒的表面等离子体带的纳米生物传感器,但不限于此。所述生物传感器可以是用于现场诊断的侧向层析检测(lfa)诊断试剂盒,其被制造为易于携带,此外,可以应用基于表面增强拉曼光谱(sers)的生物传感器、基于暗场的生物传感器等。
此时,将与待分析的生物材料特异性结合的生物探针部分(例如抗体、dna、适体、引物等)固定到基质或金属纳米颗粒上是重要的。
在生物传感器中,本发明的卡宾–金属纳米粒子复合物可用于固定生物探针部分。具体地,本发明的卡宾–金属纳米粒子复合物在末端包括含氮官能团,使得生物探针部分(例如抗体、dna、适体、引物等)可利用点击反应附着到含氮官能团。因此,通常,与生物探针部分通过静电吸引结合到金属纳米颗粒不同,由于生物探针部分可以通过更强的化学键固定到金属纳米颗粒,因此当生物探针部分应用于诸如生物传感器等领域时,除了产品的优异的可储存性和易于储存之外,还具有增强对各种环境的适用性的优点。
以下,将参考优选实施例更详细地描述本发明。
然而,这些实施例是为了更详细地描述本发明,本发明的范围并不限于此。
〈制造实例〉卡宾化合物的制备
〈制造实例1〉
根据上述反应式,制备卡宾化合物1。
图11表示卡宾化合物1的1h-nmr分析结果。
〈制造实例2〉
根据上述反应式,制备卡宾化合物2。
〈制造实例3〉
根据上述反应式,制备卡宾化合物3。
图12表示卡宾化合物3的1h-nmr分析结果。
〈制造实例4〉
根据上述反应式,制备卡宾化合物4。
图13表示卡宾化合物4的1h-nmr分析结果。
〈制造实例5〉
根据上述反应式,制备卡宾化合物5。
图14表示卡宾化合物5的1h-nmr分析结果。
〈制造实例6〉
根据上述反应式,制备卡宾化合物6。
图15表示卡宾化合物6的1h-nmr分析结果。〈实施例〉卡宾–金属纳米粒子复合物的制备〈实施例1〉
首先,将末端导入了叠氮化物的硫醇–peg化合物添加到分散在有机溶剂中的金纳米粒子中,通过金–硫键制备金纳米粒子复合物(金纳米粒子–硫醇)。
然后,添加制造实例1中得到的卡宾化合物1,用金–卡宾键取代金–硫键,得到卡宾–金纳米粒子复合体(金纳米粒子–卡宾)。
〈比较例1〉
制备了如下结构的金纳米粒子复合物。
〈比较例2〉
制备了如下结构的金纳米粒子复合物。
〈实验例〉
〈实验例1〉ph稳定性实验
分别制备ph为1至12的溶液,并加入实施例1的卡宾–金纳米颗粒络合物(金纳米粒子–卡宾)和金纳米颗粒复合物(金纳米粒子–硫醇),然后观察溶液颜色的变化,结果示于图2中。
〈实验例2〉盐稳定性实验
〈1〉分别制备10mm、50mm、100mm、250mm、500mm和1,000mm浓度的水和nacl的水溶液,并向其中加入实施例1的卡宾–金纳米粒子复合物(金纳米粒子–卡宾)和金纳米粒子复合物(金纳米粒子–硫醇),然后观察溶液颜色的变化,结果示于图3中。
〈2〉为了确认在高浓度盐离子水溶液中的稳定性,向1,000mm的nacl水溶液中加入实施例1的卡宾–金纳米粒子复合物(金纳米粒子–卡宾)和比较例2的金纳米粒子复合物,然后观察溶液颜色的变化,结果示于图4中。
〈实验例3〉温度稳定性实验
〈1〉制备其中混合了卡宾–金纳米颗粒复合物(金纳米粒子–卡宾)的-20℃的低温和-78℃的超低温的水溶液,在室温下放置,然后在1天、3天、5天和7天后观察溶液颜色的变化,结果示于图5中。
〈2〉通过制备5nm的金纳米粒子(aldrich)和20nm的金纳米粒子(bbisolution)制备水溶液,然后分别冷冻至-20℃,并再次在室温下放置5天,观察水溶液的变化,结果示于图6中。
〈实验例4〉疟疾诊断试剂盒
在实施例1的卡宾–金纳米粒子复合体(金纳米粒子–卡宾)中导入疟疾抗体,制备疟疾诊断试剂盒(lfa)。
用100ng/ml、10ng/ml和1ng/ml的疟疾抗原样品进行诊断测试,结果如图7所示。
〈实验例5〉ph稳定性实验
分别制备ph为1至12的溶液,并加入实施例1的卡宾–金纳米颗粒络合物(金纳米粒子–卡宾)和比较例1的金纳米颗粒络合物,观察溶液的颜色变化,结果示于图8中。
〈实验例6〉高温稳定性实验
分别制备加入了实施例1的卡宾–金纳米颗粒复合物(金纳米粒子–卡宾)和比较例1的金纳米颗粒复合物的水溶液,并在100℃下放置6小时,然后观察溶液颜色的变化,结果示于图9中。
〈实验例7〉低温稳定性实验
分别制备加入了实施例1的卡宾–金纳米颗粒复合物(金纳米粒子–卡宾)和比较例1的金纳米颗粒复合物的水溶液,并在-20℃下放置6小时,然后观察溶液颜色的变化,结果示于图10中。
根据实验例1和5,由于金纳米颗粒的聚集,与硫醇–peg结合的金纳米颗粒(金纳米粒子–硫醇)和金纳米颗粒(金纳米粒子)显示出紫色(由图2中的虚线方框表示),因为结合到金纳米颗粒上的配体在强酸(约ph1至3)或强碱(约ph12)条件下分离。另一方面,在本发明的卡宾–金纳米粒子复合物(金纳米粒子–卡宾)中,确认金纳米粒子没有聚集,而是在整个ph范围内稳定保持(在整个ph范围内没有颜色变化)。另外,根据图8,在比较例1的金纳米粒子复合物的情况下,确认金纳米粒子在强酸条件下(ph1至3)聚集,显示紫色。
根据实验例2〈1〉和〈2〉,由于金纳米粒子的聚集,与硫醇–peg结合的金纳米粒子(金纳米粒子–硫醇)和金纳米粒子(金纳米粒子)显示暗红色,因为结合到金纳米粒子的配体分别在50mm和100mm的浓度附近分离(逐渐从暗红色到紫色)。另一方面,在本发明的卡宾–金纳米颗粒复合物(金纳米粒子–卡宾)中,确认金纳米颗粒不聚集,而是在nacl盐的整个浓度范围(0至1,000mm)内稳定地保持(没有颜色变化)。根据实验例3〈1〉、6和7,由于金纳米粒子的聚集,通过金–硫键引入的金纳米粒子显示紫色,因为结合到金纳米粒子上的配体在高温(70℃)和低温(-20℃)下分离。另一方面,在本发明的卡宾–金纳米颗粒复合物(金纳米粒子–卡宾)中,确认金纳米颗粒不聚集,而是即使在高温(70℃)、低温(-20℃)和超低温(-78℃)下也稳定保持(没有颜色变化)。
同时,根据实验例3〈2〉,在金纳米粒子作为对照组的情况下,确认金纳米粒子在低温(-20℃)下在水中在几小时内聚集并沉淀。
根据实验例4,如图7所示,在应用了本发明的卡宾–金纳米粒子复合物(金纳米粒子–卡宾)的疟疾诊断试剂盒中,通过发现即使在10ng/ml的低浓度下也观察到对照线和测试线,而确认了能够进行诊断。
- 还没有人留言评论。精彩留言会获得点赞!