化合物、有机光电装置以及显示装置的制作方法
本说明书主张于2018年12月26日在韩国知识产权局提出申请的韩国专利申请案第10-2018-0169375号的优先权及权利,所述韩国专利申请案的全部内容并入本案供参考。
本说明书涉及一种化合物、一种有机光电二极管及一种显示装置。
背景技术:
有机光电二极管(organicoptoelectronicdiode)为一种能够相互转换电能及光能的装置。
根据操作原理,有机光电二极管可分为两种类型。一种为其中由光能形成的激子(excition)被分成电子及空穴,且在将电子及空穴各自转移至不同电极的同时产生电能的光电二极管,且另一种为通过向电极提供电压或电流自电能产生光能的发光二极管。
有机光电二极管的实例可包括有机光电式二极管、有机发光二极管、有机太阳能电池、有机光导鼓(organicphotoconductordrum)等。
其中,随着对平板显示装置(flatpaneldisplaydevice)的需求增加,有机发光二极管(organiclightemittingdiode,oled)最近备受关注。有机发光二极管为将电能转换成光的装置,且有机发光二极管的效能受设置在电极之间的有机材料的极大影响。
技术实现要素:
技术问题
本说明书的一个实施例旨在提供一种能够获得具有高效率及长寿命的有机光电二极管的化合物。
本说明书的另一实施例旨在提供一种包含所述化合物的有机光电二极管。
本说明书的又一实施例旨在提供一种包括有机光电二极管的显示装置。
技术解决方案
本说明书的一个实施例提供一种由以下化学式1表示的化合物。
[化学式1]
在化学式1中,ar1至ar4各自独立地为经取代或未经取代的c6至c60芳基或者经取代或未经取代的c2至c60杂芳基,ar1及ar2中的任一者为经取代或未经取代的芴基,ar3为经取代或未经取代的芴基,l1为单键、经取代或未经取代的c6至c60亚芳基或者经取代或未经取代的c2至c60亚杂芳基,n为0至2的一个整数,且r1至r7各自独立地为氢、氘、氰基、经取代或未经取代的c1至c60烷基或者经取代或未经取代的c6至c60芳基。
本说明书的另一实施例提供一种有机光电二极管,所述有机光电二极管包括彼此面对的阳极及阴极以及设置在阳极与阴极之间的至少一个有机层,其中有机层包含所述化合物。
本说明书的又一实施例提供一种包括有机光电二极管的显示装置。
有利效果
可获得具有高效率及长寿命的有机光电二极管。
附图说明
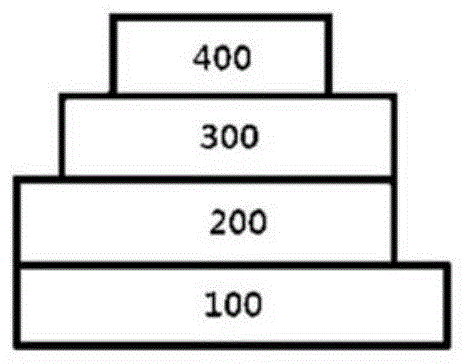
图1至图3为各自示出根据本说明书的一个实施例的有机发光二极管的截面图。
100:基板
200:阳极
300:有机材料层
301:空穴注入层
302:空穴传输层
303:发光层
304:空穴阻挡层
305:电子传输层
306:电子注入层
400:阴极
具体实施方式
以下,将详细地阐述本公开的实施例。然而,该些仅是用于说明的目的,且本公开不限于此,并仅由稍后阐述的权利要求的类别来定义。
在本说明书中,“经取代或未经取代的”意指经选自由氘;卤素基;-cn;c1至c60直链或支链烷基;c2至c60直链或支链烯基;c2至c60直链或支链炔基;c3至c60单环或多环环烷基;c2至c60单环或多环杂环烷基;c6至c60单环或多环芳基;c2至c60单环或多环杂芳基;-sirr'r”;-p(=o)rr';c1至c20烷基胺基;c6至c60单环或多环芳基胺基;c2至c60单环或多环杂芳基胺基以及经取代或未经取代的烷氧基组成的群组中的一或多个取代基取代,或者未被取代,或被键结所述取代基中两者或更多者的取代基取代,或者未被取代,或被连接选自上述取代基中的二或更多个取代基的取代基取代,或者未被取代。此外,该些可进一步与相邻的取代基形成环。
举例而言,“连接二或更多个取代基的取代基”可包括联苯基。换言之,联苯基可为芳基,或者被理解为连接两个苯基的取代基。额外取代基可被进一步取代。r、r'及r”彼此相同或不同,且各自独立地为氢;氘;-cn;经取代或未经取代的c1至c60直链或支链烷基;经取代或未经取代的c3至c60单环或多环环烷基;经取代或未经取代的c6至c60单环或多环芳基;或者经取代或未经取代的c2至c60单环或多环杂芳基。
根据本申请案的一个实施例,“经取代或未经取代的”意指经选自由氘、卤素基、-cn、-sirr'r”、-p(=o)rr'、c1至c20直链或支链烷基、c6至c60单环或多环芳基及c2至c60单环或多环杂芳基组成的群组中的一或多个取代基取代,或者未取代,并且r、r'及r”彼此相同或不同且彼此独立地为氢;氘;-cn;c1至c60烷基,未经取代或经选自由氘、卤素基、-cn、c1至c20烷基、c6至c60芳基及c2至c60杂芳基组成的群组中的一或多个取代基取代;c3至c60环烷基,未经取代或经选自由氘、卤素、-cn、c1至c20烷基、c6至c60芳基及c2至c60杂芳基组成的群组中的一或多个取代基取代;c6至c60芳基,未经取代或经选自由氘、卤素、-cn、c1至c20烷基、c6至c60芳基及c2至c60杂芳基组成的群组中的一或多个取代基取代;或c2至c60杂芳基,未经取代或经选自由氘、卤素、-cn、c1至c20烷基、c6至c60芳基及c2至c60杂芳基组成的群组中的一或多个取代基取代。
用语“取代”意指键结至化合物的碳原子的氢原子变为另一取代基,且取代的位置不受限制,只要其为氢原子被取代的位置,亦即,取代基可进行取代的位置即可,且当二或更多个取代基进行取代时,所述二或更多个取代基可彼此相同或彼此不同。
在本说明书中,卤素可包括氟、氯、溴或碘。
在本说明书中,烷基包括c1至c60直链或支链的,且可进一步被其他取代基取代。烷基的碳原子数可为1至60、具体而言为1至40且更具体而言为1至20。其具体实例可包括甲基、乙基、丙基、正丙基、异丙基、丁基、正丁基、异丁基、第三丁基、第二丁基、1-甲基-丁基、1-乙基-丁基、戊基、正戊基、异戊基、新戊基、第三戊基、己基、正己基、1-甲基戊基、2-甲基戊基、4-甲基-2-戊基、3,3-二甲基丁基、2-乙基丁基、庚基、正庚基、1-甲基己基、环戊基甲基、环己基甲基、辛基、正辛基、第三辛基、1-甲基庚基、2-乙基己基、2-丙基戊基、正壬基、2,2-二甲基庚基、1-乙基-丙基、1,1-二甲基-丙基、异己基、2-甲基戊基、4-甲基己基、5-甲基己基等,但不限于此。
在本说明书中,烯基包括c2至c60直链或支链的,且可进一步被其他取代基取代。烯基的碳原子数可为2至60、具体而言为2至40且更具体而言为2至20。其具体实例可包括乙烯基、1-丙稀基、异丙稀基、1-丁烯基、2-丁烯基、3-丁烯基、1-戊烯基、2-戊烯基、3-戊烯基、3-甲基-1-丁烯基、1,3-丁二烯基、烯丙基、1-苯基乙烯基-1-基、2-苯基乙烯基-1-基、2,2-二苯基乙烯基-1-基、2-苯基-2-(萘基-1-基)乙烯基-1-基、2,2-双(二苯基-1-基)乙烯基-1-基、二苯乙烯基、苯乙烯基等,但不限于此。
在本说明书中,炔基包括c2至c60直链或支链的,且可进一步被其他取代基取代。炔基的碳原子数可为2至60、具体而言为2至40且更具体而言为2至20。
在本说明书中,环烷基包括c3至c60单环或多环的,且可进一步被其他取代基取代。在本文中,多环意指环烷基与另一环状基直接连接或稠合的基团。本文中,所述另一环状基可为环烷基,但亦可包括其他类型的环状基,例如杂环烷基、芳基及杂芳基。环烷基的碳原子数可为3至60、具体而言为3至40且更具体而言为5至20。其具体实例可包括环丙基、环丁基、环戊基、3-甲基环戊基、2,3-二甲基环戊基、环己基、3-甲基环己基、4-甲基环己基、2,3-二甲基环己基、3,4,5-三甲基环己基、4-第三丁基环己基、环庚基、环辛基等,但不限于此。
在本说明书中,烷氧基可包括c1至c10烷氧基,且更具体而言甲氧基、乙氧基、丙氧基、丁氧基、戊氧基等。
在本说明书中,硅烷基可由-sirr'r”表示,且r、r'及r”具有与上述相同的定义。更具体而言,可包括二甲基硅烷基、二乙基硅烷基、甲基乙基硅烷基等。
在本说明书中,氧化膦基可由-p(=o)rr'表示,且r及r'具有与上述相同的定义。更具体而言,可包括二甲基膦基、二乙基膦基、甲基乙基膦基等。
在本说明书中,芴基意指在9号位置包括各种取代基的取代基。具体而言,可使用包括芴基的概念,其中9号位置被两个氢、两个烷基、两个芳基或两个杂芳基取代。更具体而言,可使用9-二-h-芴基、9-二-甲基-芴基、9-二-苯基-芴基等。此外,芴基包括具有在9号位置形成的环的螺环基。
在本说明书中,杂环烷基包括o、s、se、n或si作为杂原子,包括c2至c60单环或多环的,且可进一步被其他取代基取代。在本文中,多环意指杂环烷基与另一环状基直接连接或稠合的基团。本文中,所述另一环状基可为杂环烷基,但亦可包括其他类型的环状基,例如环烷基、芳基及杂芳基。杂环烷基的碳原子数可为2至60、具体而言为2至40且更具体而言为3至20。
在本说明书中,芳基包括c6至c60单环或多环的,且可进一步被其他取代基取代。在本文中,多环意指芳基与另一环状基直接连接或稠合的基团。本文中,所述另一环状基可为芳基,但亦可包括其他类型的环状基,例如环烷基、杂环烷基及杂芳基。芳基包括螺环基。芳基的碳原子数可为6至60、具体而言为6至40且更具体而言为6至25。芳基的具体实例可包括苯基、联苯基、三苯基、萘基、蒽基,
在本说明书中,螺环基为包括螺环结构的基团,且可为c15至c60。例如,螺环基可包括其中2,3-二氢-1h-茚基或环己烷基螺环键结至芴基的结构。具体而言,螺环基可包括以下结构式的基团中的任一种。
在本说明书中,杂芳基包括s、o、se、n或si作为杂原子,包括c2至c60单环或多环的,且可进一步被其他取代基取代。在本文中,多环意指杂芳基与另一环状基直接连接或稠合的基团。本文中,另一环状基可为杂芳基,但亦可包括其他类型的环状基,例如环烷基、杂环烷基及芳基。杂芳基的碳原子数可为2至60、具体而言为2至40且更具体而言为3至25。杂芳基的具体实例可包括吡啶基、吡咯基、嘧啶基、哒嗪基、呋喃基、噻吩基、咪唑基、吡唑基、恶唑基、异恶唑基、噻唑基、异噻唑基、三唑基、呋呫基、恶二唑基、噻二唑基、二噻唑基、四唑基、吡喃基、噻喃基、二嗪基、恶嗪基、噻嗪基、二恶英基、三嗪基、四嗪基、喹啉基、异喹啉基、喹唑啉基、异喹唑啉基、喹唑啉基、萘啶基、吖啶基、菲啶基、咪唑并吡啶基、二氮杂萘基、三氮杂茚基、吲哚基、中氮茚基、苯并噻唑基、苯并恶唑基、苯并咪唑基、苯并噻吩基、苯并呋喃基、二苯并噻吩基、二苯并呋喃基、咔唑基、苯并咔唑基、二苯并咔唑基、啡嗪基、二苯并硅杂环戊二烯基、螺环二(二苯并硅杂环戊二烯基)、二氢啡嗪基、啡恶嗪基、菲啶基、咪唑并吡啶基、噻吩基、吲哚并[2,3-a]咔唑基、吲哚并[2,3-b]咔唑基、二氢吲哚基、10,11-二氢-二苯并[b,f]氮环庚烯基、9,10-二氢吖啶基、菲蒽吖嗪基、噻啡嗪基、酞嗪基、萘啶基、菲咯啉基、苯并[c][1,2,5]噻二唑基、5,10-二氢二苯并[b,e][1,4]氮杂硅啉基、吡唑并[1,5-c]喹唑啉基、吡啶并[1,2-b]吲唑基、吡啶并[1,2-a]咪唑并[1,2-e]二氢吲哚基、5,11-二氢茚并[1,2-b]咔唑基等,但不限于此。
在本说明书中,胺基可选自由单烷基胺基;单芳基胺基;单杂芳基胺基;-nh2;二烷基胺基;二芳基胺基;二杂芳基胺基;烷基芳基胺基;烷基杂芳基胺基;及芳基杂芳基胺基组成的群组,且尽管不特别受限于此,但碳原子数较佳为1至30。胺基的具体实例可包括甲基胺基、二甲基胺基、乙基胺基、二乙基胺基、苯基胺基、萘基胺基、联苯基胺基、二联苯基胺基、蒽基胺基、9-甲基-蒽基胺基、二苯基胺基、苯基萘基胺基、二甲苯基胺基、苯基甲苯基胺基、三苯基胺基、联苯基萘基胺基、苯基联苯基胺基、联苯基芴基胺基、苯基联三亚苯基胺基、联苯基联三亚苯基胺基等,但不限于此。
在本说明书中,亚芳基意指具有两个键结位点的芳基,即二价基。除分别为二价基以外,可对其应用以上对芳基所提供的说明。此外,亚杂芳基意指具有两个键结位点的杂芳基,即二价基。除分别为二价基以外,可对其应用以上对杂芳基所提供的说明。
在本说明书中,由彼此键结的取代基形成的环为脂族烃环、芳族烃环、脂族杂环、芳族杂环或其稠环,且可分别使用以上关于环烷基、芳基、杂环烷基及杂芳基说明的结构。
在本说明书中,空穴性质是指能够在施加电场(electricfield)时通过贡献电子来形成空穴的性质,且意指通过具有沿最高占用分子轨域能阶的导电性质,有利于将在阳极中形成的空穴注入发光层,将发光层中形成的空穴迁移至阳极并在发光层中迁移的性质。
具有空穴性质的取代基包括具有空穴性质的经取代或未经取代的c6至c60芳基、具有空穴性质的经取代或未经取代的c2至c60杂芳基、经取代或未经取代的芳基胺基、经取代或未经取代的杂芳基胺基等。
更具体而言,具有空穴性质的经取代或未经取代的c6至c60芳基可为经取代或未经取代的苯基、经取代或未经取代的萘基、经取代或未经取代的菲基、经取代或未经取代的蒽基、经取代或未经取代的芴基、经取代或未经取代的联三亚苯基、经取代或未经取代的螺环-芴基、经取代或未经取代的三联苯基、经取代或未经取代的芘基、经取代或未经取代的苝基或其组合。
更具体而言,具有空穴性质的经取代或未经取代的c2至c60杂芳基为经取代或未经取代的咔唑基、经取代或未经取代的二苯并呋喃基、经取代或未经取代的二苯并噻吩基、经取代或未经取代的吲哚咔唑基等。
更具体而言,芳基或杂芳基、与经取代或未经取代的芳基胺基及经取代或未经取代的杂芳基胺基的氮键结的取代基可为经取代或未经取代的苯基、经取代或未经取代的萘基、经取代或未经取代的蒽基、经取代或未经取代的菲基、经取代或未经取代的稠四苯基、经取代或未经取代的芘基、经取代或未经取代的联苯基、经取代或未经取代的对三联苯基、经取代或未经取代的间三联苯基、经取代或未经取代的
此外,电子性质是指能够在施加电场时接收电子的性质,且意指通过具有沿着最低占用分子轨域能阶的导电性质,有利于将在阴极中形成的电子注入至发光层,将在发光层中形成的电子迁移至阴极及在发光层中迁移的性质。
具有电子性质的经取代或未经取代的c2至c60杂芳基可为经取代或未经取代的咪唑基、经取代或未经取代的四唑基、经取代或未经取代的亚喹啉基、经取代或未经取代的亚异喹啉基、经取代或未经取代的亚吡啶基、经取代或未经取代的亚嘧啶基、经取代或未经取代的亚三嗪基、经取代或未经取代的呋喃基、经取代或未经取代的苯并呋喃基、经取代或未经取代的异呋喃基、经取代或未经取代的苯并异呋喃基、经取代或未经取代的恶唑啉基、经取代或未经取代的苯并恶唑啉基、经取代或未经取代的恶二唑啉基、经取代或未经取代的苯并恶二唑啉基、经取代或未经取代的恶三唑基、经取代或未经取代的噻吩基、经取代或未经取代的苯并噻吩基、经取代或未经取代的异噻唑啉基、经取代或未经取代的苯并异噻唑啉基、经取代或未经取代的噻唑啉基、经取代或未经取代的苯并噻唑啉基、经取代或未经取代的哒嗪基、经取代或未经取代的苯并哒嗪基、经取代或未经取代的吡嗪基、经取代或未经取代的苯并吡嗪基、经取代或未经取代的酞嗪基、经取代或未经取代的苯并喹啉基、经取代或未经取代的喹恶啉基、经取代或未经取代的喹唑啉基、经取代或未经取代的吖啶基、经取代或未经取代的菲咯啉基、经取代或未经取代的啡嗪基或其组合。
更具体而言,具有电子性质的经取代或未经取代的c2至c60杂芳基可为以下化学式x-1至化学式x-5中的任一者。
[化学式x-1]
[化学式x-2]
[化学式x-3]
[化学式x-4]
[化学式x-5]
在本申请案的一个实施例中,ln可为直接键(或单键);经取代或未经取代的亚芳基;或者经取代或未经取代的亚杂芳基。
在另一实施例中,ln可为直接键;经取代或未经取代的c6至c60亚芳基;或者经取代或未经取代的c2至c60亚杂芳基。
在另一实施例中,ln可为直接键;经取代或未经取代的c6至c40亚芳基;或者经取代或未经取代的c2至c40亚杂芳基。
在ln中,n意指区分取代基的数字。
在本申请案的一个实施例中,l1可为直接键(或单键);经取代或未经取代的亚芳基;或者经取代或未经取代的亚杂芳基。
在另一实施例中,l1可为直接键;经取代或未经取代的c6至c60亚芳基;或者经取代或未经取代的c2至c60亚杂芳基。
在另一实施例中,l1可为直接键;经取代或未经取代的c6至c40亚芳基;或者经取代或未经取代的c2至c40亚杂芳基。
在下文中,将阐述根据本说明书的一个实施例的化合物。
根据一个实施例的化合物由以下化学式1表示。
[化学式1]
在化学式1中,ar1至ar4各自独立地为经取代或未经取代的c6至c60芳基或者经取代或未经取代的c2至c60杂芳基,ar1及ar2中的任一者为经取代或未经取代的芴基,ar3为经取代或未经取代的芴基,l1为单键、经取代或未经取代的c6至c60亚芳基或者经取代或未经取代的c2至c60亚杂芳基,n为0至2的一个整数,且r1至r7各自独立地为氢、氘、氰基、经取代或未经取代的c1至c60烷基或者经取代或未经取代的c6至c60芳基。
由化学式1表示的化合物具有采用胺基作为基本结构且在胺基的两个取代基中包括亚苯基的结构。经取代或未经取代的芴基键结至所述两个亚苯基。
通过经由亚苯基自胺基连接至芴基,homo电子云被扩展,且通过藉此增加homo能阶,空穴注入及空穴转移能力被进一步增强,进而降低使用其的装置的驱动电压。
此外,胺的氮及经取代或未经取代的芴基可具有基于亚苯基的间位键结位置。在此种情况下,空间大小增加,以减少分子间的相互作用,且结果,抑制材料的结晶化,并且增强薄膜稳定性。
此外,通过将各种取代基引入至化学式1的结构,可合成具有所引入取代基的独特性质的化合物。举例而言,通过将通常用作制造有机发光二极管的空穴注入层材料、空穴传输层材料、发光层材料、电子传输层材料及电荷产生层材料的取代基引入至核心结构,可合成满足每一有机材料层所需要的条件的材料。
此外,通过将各种取代基引入化学式1的结构,可精密地控制能带间隙,且同时增强有机材料之间的界面处的性质,且材料应用可变得多样化。
同时,所述化合物具有高玻璃转变温度(tg),因此具有优异的热稳定性。热稳定性的此种增加变为为装置提供驱动稳定性的重要因素。
更具体而言,所述化合物可由以下化学式2表示。
[化学式2]
在化学式2中,ar1至ar4各自独立地为经取代或未经取代的c6至c60芳基或者经取代或未经取代的c2至c60杂芳基,ar1及ar2中的任一者为经取代或未经取代的芴基,ar3为经取代或未经取代的芴基,l1为单键、经取代或未经取代的c6至c60亚芳基或者经取代或未经取代的c2至c60亚杂芳基,n为0至2的一个整数,且r1至r7各自独立地为氢、氘、氰基、经取代或未经取代的c1至c60烷基或者经取代或未经取代的c6至c60芳基。
由化学式2表示的化合物具有其中皆具有亚苯基的胺基的两个取代基在间位键结至经取代或未经取代的芴基的结构。通过在上述间位进行键结,可获得进一步改善的效果。
作为更具体的实例,经取代或未经取代的芴基可为以下化学式3-1至化学式3-4中的任一者。
[化学式3-1]
[化学式3-2]
[化学式3-3]
[化学式3-4]
在化学式3-1至化学式3-4中,x为-crxry-,rb至re各自独立地为氢、氘、氰基、经取代或未经取代的c1至c60烷基或者经取代或未经取代的c6至c60芳基,rx及ry各自独立地为氢、氘、氰基、经取代或未经取代的c1至c60烷基或者经取代或未经取代的c6至c60芳基,或rx及ry可彼此键结以形成环。
在化学式3-1至化学式3-4中,*为键结位点。
更具体而言,经取代或未经取代的芴基的键结位点可进行不同地选择。
更具体而言,ar1及ar3可为由化学式3-1表示的芴基。
更具体而言,ar1及ar3可为由化学式3-2表示的芴基。
更具体而言,ar1及ar3可为由化学式3-3表示的芴基。
更具体而言,ar1及ar3可为由化学式3-4表示的芴基。
此外,ar4可为经取代或未经取代的苯基、经取代或未经取代的联苯基、经取代或未经取代的三联苯基、经取代或未经取代的萘基、经取代或未经取代的二苯并呋喃基、经取代或未经取代的二苯并噻吩基或者经取代或未经取代的芴基。
通过选择ar4的类型,可将整个化合物的空穴性质及电子性质控制至目标范围内。
ar4可为以下群组i的取代基中的任一者。
[群组i]
在群组i中,*意指键结位点。
作为另一选择,ar4可为以下化学式4-1至化学式4-4中的任一者。
[化学式4-1]
[化学式4-2]
[化学式4-3]
[化学式4-4]
在化学式4-1至化学式4-4中,x为-o-、-s-或-crxry-,rb至re各自独立地为氢、氘、氰基、经取代或未经取代的c1至c60烷基或者经取代或未经取代的c6至c60芳基,且
rx及ry各自独立地为氢、氘、氰基、经取代或未经取代的c1至c60烷基或者经取代或未经取代的c6至c60芳基,或者rx及ry可键结至彼此以形成环。
作为具体实例,所述由化学式1表示的化合物可为以下群组ii的化合物中的任一者。
[群组ii]
作为具体实例,所述由化学式1表示的化合物可为以下群组iii的化合物中的任一者。
[群组iii]
作为具体实例,所述由化学式1表示的化合物可为以下群组iv的化合物中的任一者。
[群组iv]
作为具体实例,所述由化学式1表示的化合物可为以下群组v的化合物中的任一者。
[群组v]
所述化合物可用于有机光电二极管,且用于有机光电二极管的化合物可使用例如化学气相沉积等干膜形成方法来形成。
在下文中,将阐述使用用于有机光电二极管的化合物的有机光电二极管。
有机光电二极管没有特别限制,只要其为能够相互转换电能及光能的装置,且其实例可包括有机光电式二极管、有机发光二极管、有机太阳能电池、有机光导鼓等。
本申请案的另一实施例提供一种有机发光二极管,所述有机发光二极管包括:第一电极;第二电极,设置成与所述第一电极相对;以及一或多个有机材料层,设置于所述第一电极与所述第二电极之间,其中所述有机材料层中的一或多个层包含所述由化学式1表示的化合物。
在本申请案的一个实施例中,第一电极可为阳极,而第二电极可为阴极。
在另一实施例中,第一电极可为阴极,而第二电极可为阳极。
关于由化学式1表示的化合物的具体细节与上面提供的说明相同。
在本申请案的一个实施例中,有机发光二极管可为蓝色有机发光二极管,且根据化学式1的化合物可用作蓝色有机发光二极管的材料。
在本申请案的一个实施例中,有机发光二极管可为绿色有机发光二极管,且根据化学式1的化合物可用作绿色有机发光二极管的材料。
在本申请案的一个实施例中,有机发光二极管可为红色有机发光二极管,且根据化学式1的化合物可用作红色有机发光二极管的材料。
除使用上述化合物形成一或多个有机材料层以外,本公开的有机发光二极管可使用常见有机发光二极管制造方法及材料来制造。
当制造有机发光二极管时,所述化合物可通过溶液涂布方法以及真空沉积方法而被形成为有机材料层。在本文中,所述溶液涂布方法意指旋转涂布、浸涂、喷墨印刷、网版印刷、喷雾方法、辊涂等,但不限于此。
本文中,将参考附图阐述有机发光二极管、即有机光电二极管的一个实例的另一实例。
图1至图3示出根据本申请案的一个实施例的有机发光二极管的电极及有机材料层的积层顺序。然而,本申请案的范围不限于该些图,且此项技术中已知的有机光电二极管的结构亦可用于本申请案。
图1示出其中阳极(200)、有机材料层(300)及阴极(400)连续积层在基板(100)上的有机发光二极管。然而,所述结构不限于此种结构,且如图2所示,亦可获得其中阴极、有机材料层及阳极连续积层在基板上的有机发光二极管。
图3示出有机材料层为多层的情况。根据图3的有机发光二极管包括空穴注入层(301)、空穴传输层(302)、发光层(303)、空穴阻挡层(304)、电子传输层(305)及电子注入层(306)。然而,本申请案的范围不限于此种积层结构,且根据需要,可不包括除发光层之外的层,并且可进一步包括其他需要的功能层。
在有机发光二极管中,由化学式1表示的化合物可用作电子传输层、空穴传输层、发光层等的材料。
作为阳极材料,可使用具有相对大的功函数的材料,且可使用透明导电氧化物、金属、导电聚合物等。阳极材料的具体实例包括:金属,例如钒、铬、铜、锌及金,或其合金;金属氧化物,例如氧化锌、氧化铟、氧化铟锡(ito)及氧化铟锌(izo);金属与氧化物的组合,例如zno:al或sno2:sb;导电聚合物,例如聚(3-甲基噻吩)、聚[3,4-(乙烯-1,2-二氧)噻吩](pedt)、聚吡咯及聚苯胺等,但不限于此。
作为阴极材料,可使用具有相对小的功函数的材料,且可使用金属、金属氧化物、导电聚合物等。阴极材料的具体实例包括:金属,例如镁、钙、钠、钾、钛、铟、钇、锂、钆、铝、银、锡及铅,或其合金;多层结构材料,例如lif/al或lio2/al等,但不限于此。
作为空穴注入材料,可使用已知的空穴注入材料,且例如,可使用酞菁化合物,例如美国专利第4,356,429号中公开的铜酞菁;或星形猝发型胺衍生物,例如文献[高级材料(advancedmaterial),6,第677页(1994)]中阐述的三(4-咔唑基-9-基苯基)胺(tcta)、4,4',4”-三[苯基(间甲苯基)胺基]三苯基胺(m-mtdata)或1,3,5-三[4-(3-甲基苯基苯胺基)苯基]苯(m-mtdapb)、作为具有溶解度的导电聚合物的聚苯胺/十二烷基苯磺酸(polyaniline/dodecylbenzenesulfonicacid)、聚(3,4-乙烯二氧噻吩)/聚(4-苯乙烯磺酸酯)(poly(3,4-ethylenedioxythiophene)/poly(4-styrenesulfonate))、聚苯胺/樟脑磺酸(polyaniline/camphorsulfonicacid))或聚苯胺/聚(4-苯乙烯-磺酸酯)(polyaniline/poly(4-styrene-sulfonate))等。
作为空穴传输材料,可使用吡唑啉衍生物、芳基胺系衍生物、二苯乙烯衍生物、三苯基二胺衍生物等,且亦可使用低分子或高分子材料。
作为电子传输材料,可使用恶二唑衍生物、蒽醌二甲烷及其衍生物、苯醌及其衍生物、萘醌及其衍生物、蒽醌及其衍生物、四氰基蒽醌二甲烷及其衍生物、芴酮衍生物、二苯基二氰基乙烯及其衍生物、二苯醌衍生物、8-羟基喹啉及其衍生物等的金属错合物,且亦可使用高分子材料以及低分子材料。
作为电子注入材料的实例,此项技术中通常使用lif,然而,本申请案不限于此。
作为发光材料,可使用红色、绿色或蓝色发光材料,且根据需要,可混合并使用两种或更多种发光材料。本文中,可通过沉积为单独的供应源或者通过预混合并沉积为一种供应源来使用两种或更多种发光材料。此外,荧光材料亦可用作发光材料,然而,亦可使用磷光材料。作为发光材料,可单独使用通过结合分别自阳极及阴极注入的电子及空穴来发光的材料,然而,亦可使用具有一起参与发光的主体材料及掺杂剂材料的材料。
当混合发光材料主体时,可混合相同系列的主体,或者可混合不同系列的主体。例如,可选择n型主体材料或p型主体材料中的任何两种或更多种材料,并将其用作发光层的主体材料。
根据所使用的材料,根据本申请案的一个实施例的有机发光二极管可为顶部发射型、底部发射型或双发射型。
实例
以下,将通过实例更详细地阐述上述实施例。然而,以下实例仅用于说明目的,且不限制权利的范围。
除非另外特别提及,否则实例及合成例中使用的起始材料及反应材料购自西格玛-奥德里奇公司、锑希爱公司、东京化学工业公司或p&h技术公司(p&htech),或者使用已知方法合成。
(制备用于有机光电二极管的化合物)
[制备例a1-1]合成中间物a1
合成中间物a1
将(9,9-二甲基-9h-芴-1-基)硼酸((9,9-dimethyl-9h-fluoren-1-yl)boronicacid)(30克,1当量)、1-溴-3-碘苯(46克,1.3当量)、pd(pph3)4(四(三苯基膦)钯(0))(4.4克,0.03当量)、k2co3(26克,1.5当量)、甲苯(tol)(650毫升)、乙醇(etoh)(150毫升)及h2o(150毫升)引入1颈圆底烧瓶(1-neck-r.b.f)中,并搅拌了6小时。
仅使用乙酸乙酯进行后处理,且蒸发后,进行hx热过滤以获得37克。步骤产率=84%
[制备例a1-2]合成中间物a2
除了使用(9,9-二甲基-9h-芴-2-基)硼酸代替(9,9-二甲基-9h-芴-1-基)硼酸以外,所有步骤与中间物a1的合成相同。
[制备例a1-3]合成中间物a3
除了使用(9,9-二甲基-9h-芴-3-基)硼酸代替(9,9-二甲基-9h-芴-1-基)硼酸以外,所有步骤与中间物a1的合成相同。
[制备例a1-4]合成中间物a4
除了使用(9,9-二甲基-9h-芴-4-基)硼酸代替(9,9-二甲基-9h-芴-1-基)硼酸以外,所有步骤与中间物a1的合成相同。
合成化合物a1-1
将中间物a1(12克,2.1当量)、9,9-二苯基-9h-芴-2-胺(5.5克,1当量)、pd2(dba)3(三(二亚苄基丙酮)二钯(0))(0.8克,0.05当量)、t-buona(4.8克,3当量)、t-bu3p(0.34克,0.1当量)及甲苯(150毫升)引入至1颈圆底烧瓶中,并搅拌了4小时。
反应材料通过二氧化硅路径,且管柱分离两次。将所得物(约7克,步骤产率=50%)制成ea/meoh浆状物,以获得高效液相层析99.86%的材料(6克)。将总量升华纯化以获得白色固体(3.1克)。
下表1的化合物合成如下。
除了使用以下置换的化合物代替9,9-二苯基-9h-芴-2-胺以外,所有步骤与使用中间物a1的化合物相同。
[表1]
下表2的化合物合成如下。
除了使用中间物i代替中间物a1且使用中间物ii代替9,9-二苯基-9h-芴-2-胺以外,自化合物a2-1至化合物a4-44所有者皆为相同的。
[表2]
作为比较例,使用以下化合物。
比较例1
所制备的化合物是根据质谱及核磁共振结果来识别。
[表3]
[表4]
(制造有机发光二极管)
用蒸馏水超音波对上面ito被涂布至1500埃厚度的薄膜的玻璃基板进行了清洗。用蒸馏水清洗完成后,用例如丙酮、甲醇及异丙醇等溶剂对基板进行了超音波清洗,然后干燥,并在紫外清洁器中紫外臭氧处理了5分钟。之后,将基板转移至等离子体清洁器(pt),且在真空下进行等离子体处理以移除氧化铟锡功函数及残留膜之后,将基板转移至热沉积设备以进行有机沉积。
在透明ito电极(阳极)上,使用4,4',4”-三[2-萘基(苯基)胺基]三苯基胺(4,4',4”-tris[2-naphthyl(phenyl)amino]triphenylamine)作为空穴注入层、即共用层,且使用实例中所包括的材料作为空穴传输层,并且使用比较例1作为比较材料。
发光层如下热真空沉积在其上。作为发光层,将9-[(4-4,6-二苯基-1,3,5-三嗪-2-基)苯基]-9'-苯基-3,3'-双-9h-咔唑化合物沉积至400埃作为主体,且对ir(ppy)3绿色磷光掺杂剂进行7%掺杂并沉积。此后,将浴铜灵(bathocuproine)沉积至60埃作为空穴阻挡层,且将alq3在其上沉积至200埃作为电子传输层。最后,将氟化锂(lithiumfluoride:lif)在电子传输层上沉积至10埃的厚度以形成电子注入层,然后将铝(al)阴极在电子注入层上沉积至1,200埃的厚度以形成阴极,且结果,制造了有机电致发光二极管。
同时,对于在有机发光二极管制造中使用的每种材料,制造有机发光二极管所需的全部有机化合物在10-8托至10-6托下进行真空升华纯化。
评价:识别驱动电压改善以及发光效率及寿命增加的效果
对于根据实例及比较例的有机发光二极管,评价了驱动电压及寿命性质。具体测量方法如下,且结果如下。
(1)测量根据电压变化的电流密度的变化
对于所制造的有机发光二极管,在将电压自0伏特增加至10伏特的同时,使用电流-电压计(keithley2400)测量流向单元装置的电流值,且将所测量的电流值除以面积以获得结果。
(2)测量根据电压变化的亮度的变化
对于所制造的有机发光二极管,电压自0伏特增加至10伏特,且使用亮度计(minoltacs-1000a)测量了当时的亮度以获得结果。
(3)测量发光效率
使用自(1)及(2)测量的亮度、电流密度及电压,计算相同电流密度(10毫安/平方厘米)的电流效率(坎德拉/安)。
(4)测量寿命
对所制造的有机发光二极管使用极化子寿命测量系统,使下表5的实例及比较例的每一装置以24000坎德拉/平方米的初始亮度(坎德拉/平方米)发射。测量亮度随时间的降低,且测量亮度相对于初始亮度降低至90%的时间作为t90寿命。
(5)测量驱动电压
使用电流-电压计(keithley2400)以15毫安/平方厘米测量了每一装置的驱动电压,以获得结果。
[表5]
当将实例a1至实例a80的有机发光二极管与比较例1进行比较时,识别出获得了相等或高级水平的驱动电压降低及效率性质,且寿命性质特别优异。
当将比较例1与本公开的化合物比较时,相似的是具有芳基胺基,然而,不同的是芴基及苯基在对位被取代。
当芴基及苯基如比较例1中在对位被取代时,化合物为平的,且具有π键的苯基在分子中形成π-π堆叠(pi-pi-stacking),因此,有机发光二极管具有增加的驱动电压,因而具有降低的装置性质。在表5中,识别出比较例1相较于其他实例具有更高的驱动电压。
上文已详细阐述了本公开的较佳实例,然而,本公开的权利范围不限于此,且本领域技术人员使用随附权利要求中定义的本公开的基本概念作出的各种修改及改进亦落在本公开的权利范围内。
- 还没有人留言评论。精彩留言会获得点赞!