恩曲替尼晶型及其制备方法与流程
本发明是涉及药物化学领域,尤其涉及恩曲替尼的晶型及其制备方法。
背景技术:
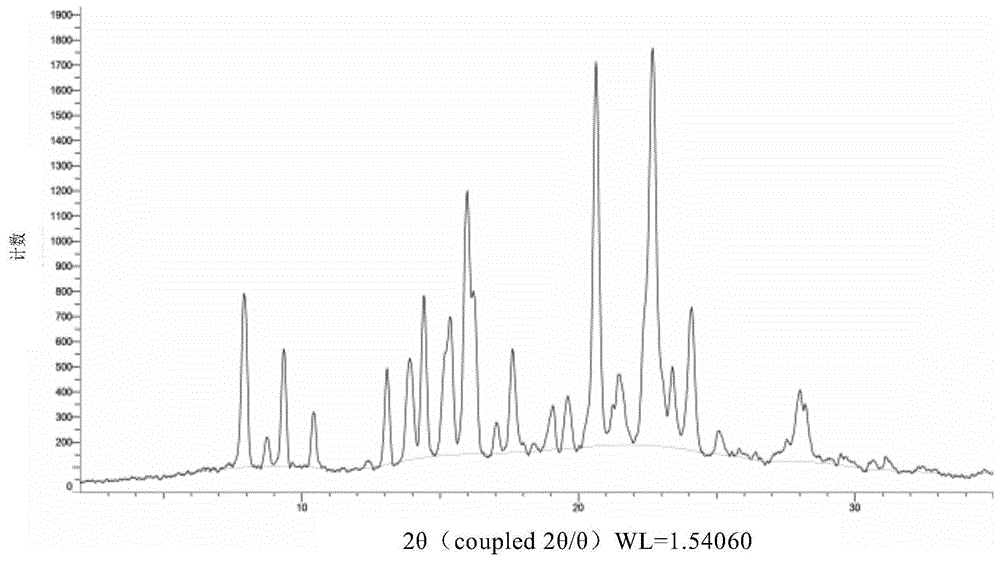
:恩曲替尼,英文名entrectinib,其化学名为:n-(5-(3,5-二氟苄基)-1h-吲唑-3-基)-4-(4-甲基哌嗪-1-基)-2-((四氢-2h-吡喃-4-基)氨基)苯甲酰胺,商品名为:rozlytrek,分子式为:c31h34f2n6o2,分子量为:560.64,cas号为:1108743-60-7,化学结构式为:该药是由罗氏开发的一种治疗ntrk融合阳性的晚期或复发性实体瘤的疾病,于2019.6.19在日本申请上市。专利wo2013174876公开了恩曲替尼的晶型1、晶型2和晶型3及其制备方法。其中,晶型1和晶型2是无水物,晶型3为乙酸乙酯和正己烷的溶剂化物,晶型2晶型稳定性较好,晶型1晶型稳定性差容易转为晶型2。专利wo2017202674公开了恩曲替尼的无水物晶型4,其在40℃以上晶型热力学稳定性更好。显然,现有的恩曲替尼晶型1存在晶型稳定性差的问题,晶型2和晶型4存在溶解性较差的问题。而且,根据fda资料显示,恩曲替尼是低溶解度药物。综上所述,本领域迫切需要开发一种既具有良好溶解性又有良好晶型稳定性的新晶型,以满足制剂药用的需要。技术实现要素:本发明的目的就是提供一种既具有良好溶解性又有良好晶型稳定性的新晶型,以满足制剂药用的需要。在本发明的第一方面,提供了一种如式i所示的化合物的晶型,所述的晶型为晶型azt-a、晶型azt-b或晶型azt-e。在另一优选例中,所述的晶型为晶型azt-a,且所述晶型azt-a的xrpd图包括4个或4个以上选自下组的2θ值:7.9±0.2°、9.4±0.2°、14.4±0.2°、15.4±0.2°、16.0±0.2°、20.6±0.2°。在另一优选例中,所述晶型azt-a的xrpd图还包括1个或多个选自下组的2θ值:13.1±0.2°、13.9±0.2°、15.4±0.2°、16.2±0.2°、17.6±0.2°、22.7±0.2°、23.4±0.2°、24.1±0.2°、28.0±0.2°。在另一优选例中,所述晶型azt-a的xrpd图包括6个或6个以上选自下组的2θ值:7.9±0.2°、9.4±0.2°、13.1±0.2°、13.9±0.2°、14.4±0.2°、15.4±0.2°、16.0±0.2°、16.2±0.2°、17.6±0.2°、20.6±0.2°、22.7±0.2°、23.4±0.2°、24.1±0.2°、28.0±0.2°。在另一优选例中,所述晶型azt-a在30℃-150℃范围内失重0.3±0.1%。在另一优选例中,所述晶型azt-a在162.5±0.5℃和196.78±0.5℃各有一个吸热峰。在另一优选例中,所述晶型azt-a具有基本如图1所示的xrpd谱图。在另一优选例中,所述晶型azt-a具有基本如图2所示的tga谱图。在另一优选例中,所述晶型azt-a具有基本如图3所示的dsc谱图。在另一优选例中,所述晶型azt-a具有基本如图4所示的1h-nmr谱图。在另一优选例中,所述的晶型为晶型azt-b,且所述晶型azt-b的xrpd图包括3个或3个以上选自下组的的2θ值:7.4±0.2°、8.1±0.2°、14.8±0.2°、17.2±0.2°、19.9±0.2°。在另一优选例中,所述晶型azt-b的xrpd图还包括1个或多个选自下组的的2θ值:11.4±0.2°、12.0±0.2°、20.9±0.2°、22.3±0.2°、23.5±0.2°、24.1±0.2°。在另一优选例中,所述晶型azt-b的xrpd图包括6个或6个以上选自下组的的2θ值:7.4±0.2°、8.1±0.2°、11.4±0.2°、12.0±0.2°、14.8±0.2°、17.2±0.2°、19.9±0.2°、20.9±0.2°、22.3±0.2°、23.5±0.2°、24.1±0.2°。在另一优选例中,所述晶型azt-b在30℃-150℃范围内失重0.8±0.1%;在另一优选例中,所述晶型azt-b在147.3±0.5℃有熔融吸热峰。在另一优选例中,所述晶型azt-b具有基本如图5所示的xrpd谱图。在另一优选例中,所述晶型azt-b具有基本如图6所示的tga谱图。在另一优选例中,所述晶型azt-b具有基本如图7所示的dsc谱图。在另一优选例中,所述晶型azt-b具有基本如图8所示的1h-nmr谱图。在另一优选例中,所述的晶型为晶型azt-e,且所述晶型azt-e的xrpd图包括3个或3个以上选自下组的的2θ值:8.9±0.2°、10.5±0.2°、16.6±0.2°、17.2±0.2°。在另一优选例中,所述晶型azt-e的xrpd图还包括1个或多个选自下组的2θ值:15.9±0.2°、17.0±0.2°、17.9±0.2°、22.8±0.2°、24.7±0.2°。在另一优选例中,所述晶型azt-e的xrpd图包括6个或6个以上选自下组的2θ值:8.9±0.2°、10.5±0.2°、15.9±0.2°、16.6±0.2°、17.0±0.2°、17.2±0.2°、17.9±0.2°、22.8±0.2°、24.7±0.2°。在另一优选例中,所述晶型azt-e在50℃-150℃范围内失重约3.3±0.1%;在另一优选例中,所述晶型azt-e在126.35±0.5℃有脱水峰,在197.15±0.5℃有熔融吸热峰。在另一优选例中,所述晶型azt-e具有基本如图11所示的xrpd谱图。在另一优选例中,所述晶型azt-e具有基本如图12所示的tga谱图。在另一优选例中,所述晶型azt-e具有基本如图13所示的dsc谱图。在另一优选例中,所述晶型azt-e具有基本如图14所示的1h-nmr谱图。在本发明的第二方面,提供了一种如第一方面所述的晶型的制备方法;包括步骤:(i)提供恩曲替尼原料于第一溶剂中的溶液,使溶液中析出固体,收集析出的固体,从而得到所述的晶型;或者,包括步骤:(ii)提供恩曲替尼原料于第二溶剂中的混合物,对混合物进行处理,收集其中固体,从而得到所述的晶型;其中,所述的处理是指搅拌、打浆和/或研磨;或者,包括步骤:(iii)将恩曲替尼原料进行处理,从而得到所述晶型;其中,所述的处理是指热处理和/或干燥处理;其中,所述恩曲替尼原料为恩曲替尼的无定型和/或晶型。在另一优选例中,步骤(i)中,通过加入晶种、使溶液冷却和/或去除第一溶剂使溶液中析出固体。在另一优选例中,所述晶种为如第一方面所述的晶型,较佳地,为晶型azt-a。在另一优选例中,步骤(i)中,所述溶液中恩曲替尼的浓度为0.005~1.0g/ml,优选为0.01~0.2g/ml。在另一优选例中,步骤(i)中,收集析出的固体后还包括任选的干燥步骤。在另一优选例中,步骤(i)中,收集析出的固体的方法为过滤。在另一优选例中,步骤(i)中,通过使溶液冷却来使溶液中析出固体时,溶液的温度为所述溶液的温度为10~100℃(较佳地,20~80℃;更佳地,40~70℃);和/或冷却至≤20℃(更佳地,≤10℃;最佳地,≤5℃)。在另一优选例中,步骤(ii)中,所述处理在0-70℃(优选地0-50℃)下进行。在另一优选例中,步骤(ii)中,恩曲替尼原料与第二溶剂的质量体积(mg/ml)比为(10~500):1。在另一优选例中,步骤(ii)中,所述处理的时间为1-48h;较佳地,2-36h;更佳地,3-24h。在另一优选例中,步骤(ii)中,收集其中固体的方法为过滤。在另一优选例中,步骤(ii)中,收集其中固体后还包括任选的干燥步骤。在另一优选例中,步骤(iii)中,所述热处理是指加热至50-100℃和/或保温1-5h。在另一优选例中,所述第一溶剂选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、芳类溶剂,或其组合;或者,所述第一溶剂为水与选自下组溶剂组成的混合溶剂:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂,或其组合。在另一优选例中,所述第二溶剂选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、醚类溶剂,或其组合;或者,所述第一溶剂为水与选自下组溶剂组成的混合溶剂:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、芳类溶剂,或其组合。在另一优选例中,所述酯类溶剂为c2-c6酯类溶剂;较佳地,所述酯类溶剂选自:乙酸乙酯、乙酸异丙酯、甲酸乙酯、乙酸甲酯、乙酸正丙酯、乙酸丁酯,或其组合。在另一优选例中,所述醇类溶剂为c1-c4醇类溶剂;较佳地,所述醇类溶剂选自:甲醇、乙醇、异丙醇,或其组合。在另一优选例中,所述卤代烃类溶剂为c1-c4卤代烃类溶剂;较佳地,所述卤代烃类溶剂为二氯甲烷。在另一优选例中,所述酮类溶剂为c2-c6酮类溶剂;较佳地,所述酮类溶剂选自:丙酮、mibk,或其组合物。在另一优选例中,所述芳类溶剂为c6-c10芳烃;较佳地,为甲苯。在另一优选例中,所述醚类溶剂为环醚类溶剂或链状醚类溶剂。在另一优选例中,所述环醚类溶剂选自下组:1.4-二氧六环、四氢呋喃、2-甲基四氢呋喃,或其组合。在另一优选例中,所述第一溶剂选自:甲醇、乙醇、乙腈、甲苯、丙酮、乙酸乙酯、甲酸乙酯、乙酸甲酯、乙酸正丙酯、乙酸异丙酯、乙酸丁酯、二氯甲烷、mibk,或其组合;或者,水与选自下组溶剂组成的混合溶剂:甲醇、乙醇、乙腈、甲苯、丙酮、乙酸乙酯、甲酸乙酯、乙酸甲酯、乙酸正丙酯、乙酸异丙酯、乙酸丁酯、二氯甲烷、mibk,或其组合。在另一优选例中,所述第二溶剂选自:甲醇、乙醇、乙腈、甲苯、丙酮、乙酸乙酯、二氯甲烷、mibk、1.4-二氧六环、四氢呋喃、2-甲基四氢呋喃(2-methf),或其组合;或者,水与选自下组溶剂组成的混合溶剂:甲醇、乙醇、乙腈、甲苯、丙酮、乙酸乙酯、二氯甲烷、mibk、1.4-二氧六环、四氢呋喃、2-甲基四氢呋喃,或其组合。在另一优选例中,当所述的晶型为晶型azt-a时,所述的制备方法为方法a1或方法a2。在另一优选例中,所述的方法为方法a1,且所述方法a1包括步骤:提供恩曲替尼原料于溶剂a中的溶液,冷却析晶,收集析出固体,干燥所得的固体,从而得到晶型azt-a。在另一优选例中,方法a1中,所述的溶剂a是能够在10~150℃的温度范围内使恩曲替尼原料完全溶解的溶剂。在另一优选例中,方法a1中,所述溶剂a选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、芳类溶剂,或其组合。在另一优选例中,方法a1中,所述溶剂a为酯类溶剂,或者含酯类溶剂的混合溶剂;其中,所述含酯类溶剂的混合溶剂为酯类溶剂与选自下组的溶剂组成的混合溶剂:醇类溶剂、酮类溶剂、卤代烃类溶剂,或其组合。在另一优选例中,方法a1中,所述溶液中,恩曲替尼的浓度为0.005~1.0g/ml,优选为0.01~0.2g/ml。在另一优选例中,方法a1中,所述溶液的温度为10~100℃;较佳地,20~80℃;更佳地,40~70℃。在另一优选例中,方法a1中,所述冷却析晶的析晶温度为≤20℃;更佳地,≤10℃;最佳地,≤5℃。在另一优选例中,方法a1中,所述冷却析晶的析晶温度<溶液温度。在另一优选例中,方法a1中,所述恩曲替尼原料为恩曲替尼的无定型和/或晶型。在另一优选例中,所述的方法为方法a2,且所述方法a2包括步骤:将恩曲替尼原料在ta温度下保温ta时间,从而得到晶型azt-a。在另一优选例中,方法a2中,所述恩曲替尼原料为恩曲替尼的无定型和/或晶型;较佳地,为恩曲替尼的晶型azt-c。在另一优选例中,所述晶型azt-c的xrpd图包括所有选自下组的2θ值18.1±0.2°、23.1±0.2°、25.5±0.2°。在另一优选例中,方法a2中,ta=60~100℃;较佳地,ta=70~90℃。在另一优选例中,方法a2中,ta=1~10h;较佳地,ta=3~7h。在另一优选例中,当所述的晶型为晶型azt-b时,所述的制备方法为方法b1或方法b2。在另一优选例中,所述的制备方法为方法b1,且所述方法b1包括步骤:提供恩曲替尼原料于溶剂b中的混合物,打浆或搅拌,收集所述混合物中固体,干燥所得固体,从而得到晶型azt-b。在另一优选例中,方法b1中,在0-70℃(较佳地为0-50℃,更佳地为10~40℃)下打浆或搅拌。在另一优选例中,方法b1中,打浆或搅拌的时间为1-24h;较佳地,为2-24h。在另一优选例中,方法b1中,恩曲替尼原料与溶剂b的质量体积(mg/ml)比为(10~500):1;较佳地,为(10~50):1或(150~300):1。在另一优选例中,所述溶剂b选自:醇类溶剂、乙腈,或其组合。在另一优选例中,所述溶剂b选自:甲醇、乙醇、乙腈、甲苯、丙酮、乙酸乙酯、二氯甲烷、mibk,或其组合;较佳地,选自:甲醇、乙醇、乙腈,或其组合。在另一优选例中,方法b1中,所述恩曲替尼原料为恩曲替尼的无定型和/或晶型。在另一优选例中,所述的制备方法为方法b2,且所述方法b2包括步骤:将恩曲替尼原料在tb温度下干燥,从而得到晶型azt-b;在另一优选例中,方法b2中,所述恩曲替尼原料为恩曲替尼的无定型和/或晶型。在另一优选例中,方法b2中,所述恩曲替尼原料为恩曲替尼的晶型azt-d。在另一优选例中,所述晶型azt-d的xrpd图包括3个或3个以上选自下组的2θ值7.1±0.2°、7.4±0.2°、13.4±0.2°、17.6±0.2°、19.8±0.2°、22.6±0.2°。在另一优选例中,方法b2中,tb=40~80℃;较佳地,tb=50~60℃。在另一优选例中,方法b2中,所述干燥的时间为1~48h;较佳地,2~36h;更佳地,12~24h。在另一优选例中,当所述的晶型为晶型azt-e时,所述的制备方法为方法e。在另一优选例中,所述的方法为方法e,且所述方法e包括步骤:提供恩曲替尼原料于溶剂e与水中的混合物,打浆或搅拌,收集所述混合物中固体,干燥所得固体,从而得到晶型azt-e。在另一优选例中,方法e中,在te1温度下打浆或搅拌,且te1=0-50℃;较佳地,te1=0~40℃;更佳地,te1=0~5℃或15~30℃。在另一优选例中,方法e中,打浆时间为te1且te1≥2h;较佳地,te1≥12h。在另一优选例中,方法e中包括步骤:(e1)在te2温度下,先将恩曲替尼原料于溶剂e中打浆或搅拌te2时间,加入水,从而得到恩曲替尼原料于溶剂e与水中混合物;或者将恩曲替尼原料与溶剂e和水的混合溶剂混合,从而得到恩曲替尼原料于溶剂e与水中混合物;(e2)在te1温度下,将恩曲替尼原料于溶剂e与水中的混合物打浆或搅拌te1时间,收集所述混合物中固体,干燥所得固体,从而得到晶型azt-e。在另一优选例中,方法e中,te2=0.1~1小时;较佳地,te2=0.4~0.6小时。在另一优选例中,te2=0~50℃;较佳地,te2=10~40℃;更佳地,te2=15~30℃。在另一优选例中,所述溶剂e选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、芳类溶剂,或其组合。在另一优选例中,所述溶剂e为醇类溶剂。在另一优选例中,所述溶剂e选自:甲醇、乙醇,或其组合。在另一优选例中,方法e中,溶剂e与水的体积比为(0.1~10):1;较佳地,为(0.2~5):1。在另一优选例中,方法e中,恩曲替尼与溶剂e的质量体积(g/ml)比为(0.05~0.5):1。在另一优选例中,方法e中,恩曲替尼与水的质量体积(g/ml)比为(0.015~1.5):1。在另一优选例中,方法e中,所述恩曲替尼原料为恩曲替尼的无定型和/或晶型;较佳地,选自:晶型azt-a、晶型azt-b、晶型azt-c,或其组合。在本发明的第三方面中,提供一种如式i所示的化合物的无定型,所述无定型具有基本如图21所示的xprd谱图。在另一优选例中,在dsc图中,所述无定型在80~100℃具有玻璃化转变峰。在另一优选例中,所述无定型具有基本如图22所示的dsc图。在另一优选例中,所述无定型在15℃-100℃范围内失重0.2±0.1%。在另一优选例中,所述无定型具有基本如图23所示的tga图。在本发明的第四方面中,提供了一种第三方面所述无定型的制备方法,包括步骤:1)提供恩曲替尼原料于溶剂1中的溶液;2)向所述溶液中添加溶剂2进行析晶,收集析出固体,从而得到无定型。在另一优选例中,在所述溶液中,恩曲替尼的浓度为0.005~1.0g/ml;较佳地,为0.01~0.1g/ml;更佳地,为0.01~0.02g/ml。在另一优选例中,所述恩曲替尼原料为恩曲替尼的晶型和/或无定型。在另一优选例中,所述的溶剂1选自下组:甲醇、乙醇、异丙醇、乙腈、甲苯、丙酮、乙酸乙酯、二氯甲烷、mibk、甲苯,或其组合;和/或所述溶剂2选自下组:正庚烷、正己烷、甲叔醚、水、苯甲醚,或其组合。在另一优选例中,溶剂2为正己烷。在本发明的第五方面提供了一种药物组合物,所述药物组合物包括(i)如第一方面所述的的晶型;以及(ii)药学上可接受的载体。在本发明的第六方面,提供了一种如第一方面所述的晶型的用途,其用于制备用于治疗癌症和/或肿瘤的药物。在另一优选例中,所述的癌症为非小细胞肺癌;更佳地,为转移性ros1阳性非小细胞肺癌(nsclc)。在另一优选例中,所述的肿瘤为实体瘤。在本发明的第七方面,提供了一种如式i所示化合物的晶型,所述晶型为晶型azt-c;且所述晶型azt-c的xrpd图包括所有选自下组的2θ值18.1±0.2°、23.1±0.2°、25.5±0.2°。在另一优选例中,所述晶型azt-c用于制备晶型azt-a。在本发明的第八方面,提供了一种如式i所示化合物的晶型,所述晶型为晶型azt-d;且所述晶型azt-d的xrpd图包括3个或3个以上选自下组的2θ值7.1±0.2°、7.4±0.2°、13.4±0.2°、17.6±0.2°、19.8±0.2°、22.6±0.2°。在另一优选例中,所述晶型azt-d用于制备晶型azt-b。应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。附图说明图1是本发明所述的恩曲替尼的晶型azt--a的xrpd谱图;图2是本发明所述的恩曲替尼的晶型azt-a的tga谱图;图3是本发明所述的恩曲替尼的晶型azt-a的dsc谱图;图4是本发明所述的恩曲替尼的晶型azt--a的1h-nmr谱图;图5是本发明所述的恩曲替尼的晶型azt-b的xrpd谱图;图6是本发明所述的恩曲替尼的晶型azt--b的tga谱图;图7是本发明所述的恩曲替尼的晶型azt--b的dsc谱图;图8是本发明所述的恩曲替尼的晶型azt--b的1h-nmr谱图;图9是本发明所述的恩曲替尼的晶型azt-c的xrpd谱图;图10是本发明所述的恩曲替尼的晶型azt-d的xrpd谱图;图11是本发明所述的恩曲替尼的晶型azt-e的xrpd谱图;图12是本发明所述的恩曲替尼的晶型azt-e的tga谱图;图13是本发明所述的恩曲替尼的晶型azt-e的dsc谱图;图14是本发明所述的恩曲替尼的晶型azt-e的1h-nmr谱图;图15是本发明所述的恩曲替尼的晶型azt-f的xrpd谱图;图16是本发明所述的恩曲替尼的晶型azt-g的xrpd谱图;图17是本发明所述的恩曲替尼的晶型azt-h的xrpd谱图;图18是本发明所述的恩曲替尼的晶型azt-h的tga谱图;图19是本发明所述的恩曲替尼的晶型azt-i的xrpd谱图;图20是本发明所述的恩曲替尼的晶型azt-i的tga谱图;图21是本发明所述的恩曲替尼的无定型的xrpd谱图;图22是本发明所述的恩曲替尼的无定型的dsc谱图;图23是本发明所述的恩曲替尼的无定型的tga谱图。具体实施方式发明人经过长期而深入地研究。意外地制备了一系列具有优异稳定性(如高湿和/或高热、压力稳定性等)、溶解性的恩曲替尼的新晶型。且制备这些晶型的方法简单,易于工业化。基于此发明人完成了本发明。术语如本文所用,“mibk”是指甲基异丁酮。在本文中,除非特别说明,各缩写均为本领域技术人员所理解的常规含义。如本文所用,术语“恩曲替尼原料”是指恩曲替尼的无定型(形)和/或各种晶型(包括本文提及的各种晶型和无定型、公开或未公开的各种文献或专利(如wo2013174876、wo2017202674)中提及的晶型或无定型)。如本文所用,“本发明的晶型”是指如本文中所述的恩曲替尼的晶型azt-a、晶型azt-b、晶型azt-c、晶型azt-d、晶型azt-e、晶型azt-f、晶型azt-g、晶型azt-h、和晶型azt-i,尤其是指晶型azt-a、晶型azt-b、和晶型azt-e。通用方法本发明所有的测试方法均为通用方法,测试参数如下:xrpd图测定方法:x-射线粉末衍射仪器:brukerd2phaserx-射线粉末衍射仪;辐射源cu发生器(generator)kv:30kv;发生器(generator)ma:10ma;起始的2θ:2.000°,扫描范围:2.0000~35.000°。tga图测定方法:热重分析法(tga)仪器:美国ta公司的tga55型,20~300℃范围内,加热速率10℃/min,氮气流速40ml/min。dsc图测定方法:差示扫描量热法(dsc)仪器:美国ta公司的taq2000型,25~300℃范围内,加热速率10℃/min,氮气流速50ml/min。1h-nmr图的测定方法:核磁共振氢谱(1h-nmr)仪器:;频率:400mhz;溶剂:dmso。在本发明中,除非特别说明,干燥所用的方法为本领域的常规干燥方法,例如在本发明的实施例中干燥是指在常规干燥用烘箱进行真空干燥或常压干燥。一般地,干燥0.1~50h或1~30h。恩曲替尼的晶型azt-a及其制备方法在一个具体实施例中,本发明提供的恩曲替尼的晶型为晶型azt-a。优选地,所述晶型azt-a为恩曲替尼的无水物。在一个具体实施例中,本发明的晶型azt-a,在粉末x射线衍射下,在2θ为7.9±0.2°、9.4±0.2°、14.4±0.2°、15.4±0.2°、16.0±0.2°、20.6±0.2°处具有特征峰。在另一优选例中,在粉末x射线衍射下,所述晶型azt-a还在2θ为13.1±0.2°、13.9±0.2°、15.4±0.2°、16.2±0.2°、17.6±0.2°、20.6±0.2°、22.7±0.2°、23.4±0.2°、24.1±0.2°、和/或28.0±0.2°处具有特征峰。在另一优选例中,在粉末x射线衍射下,所述晶型azt-a在2θ为7.9±0.2°、9.4±0.2°、13.1±0.2°、13.9±0.2°、14.4±0.2°、15.4±0.2°、16.0±0.2°、16.2±0.2°、17.6±0.2°、20.6±0.2°、22.7±0.2°、23.4±0.2°、24.1±0.2°、28.0±0.2°处具有特征峰。在另一优选例中,在粉末x射线衍射下,所述晶型azt-a在2θ为22.7±0.2°处的特征峰的相对强度≥90%;更优选地,≥95%;最优选地,约为100%。在另一优选例中,在粉末x射线衍射下,所述晶型azt-a在2θ为20.6±0.2°处的特征峰的相对强度≥90%;更优选地,20.6±0.2°处的特征峰的相对强度<22.7±0.2°处的特征峰的相对强度。在另一优选例中,在粉末x射线衍射下,除2.7±0.2°处和20.6±0.2°处的特征峰外,,所述晶型azt-a的其余特征峰的相对强度≤90%;较佳地,≤75%。更优选地,本发明所述的恩曲替尼的晶型azt-a,在粉末x射线衍射下具有以下特征峰及相对强度:在另一优选例中,所述晶型azt-a具有基本如图1所示的xrpd谱图。在另一优选例中,在tga图中,所述晶型azt-a在30℃-150℃范围内失重0.3±0.1%。在另一优选例中,所述晶型azt-a具有基本如图2所示的tga谱图。在另一优选例中,在dsc图中,所述晶型azt-a在162.5±0.5℃和196.78±0.5℃各有一个吸热峰。在另一优选例中,所述晶型azt-a具有基本如图3所示的dsc谱图。在另一优选例中,所述晶型azt-a具有基本如图4所示的1h-nmr谱图。在另一个具体实施例中,本发明还提供了一种制备本发明的恩曲替尼的晶型的方法,其中,所述的晶型为晶型azt-a,所述的方法(即方法a1)包括步骤:a1)将恩曲替尼原料溶解于溶剂a中(较佳地,在10~100℃下溶解;更佳地,20~80℃下溶解;最佳地,40~70℃下溶解),从而得到恩曲替尼原料于溶剂a中的溶液(澄清);a2)将溶液a进行冷却析晶,优选地冷却至为20℃以下(更佳地,10℃以下;最佳地,5℃以下)析晶,收集析出晶体并干燥,从而得到晶型azt-a;或者,所述的方法(即方法a2)包括步骤:将恩曲替尼原料(较佳地,恩曲替尼原料为本文所述的azt-c)在ta温度下保温ta时间,从而得到晶型azt-a。在另一优选例中,ta=60~100℃;较佳地,ta=70~90℃。在另一优选例中,ta=1~10h;较佳地,ta=3~7h。在另一优选例中,所述的溶剂a是指在10~150℃,能使恩曲替尼原料完全溶解于其中的溶剂。在另一优选例中,所述溶剂a选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、芳类溶剂,或其组合;或者,所述溶剂a为水与选自下组溶剂组成的混合溶剂:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂,或其组合。在另一优选例中,所述溶剂a选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、芳类溶剂,或其组合。在另一优选例中,所述酯类溶剂为c2-c6酯类溶剂;较佳地,所述酯类溶剂选自:乙酸乙酯、乙酸异丙酯、甲酸乙酯、乙酸甲酯、乙酸正丙酯、乙酸丁酯,或其组合。在另一优选例中,所述醇类溶剂为c1-c4醇类溶剂;较佳地,所述醇类溶剂选自:甲醇、乙醇、异丙醇,或其组合。在另一优选例中,所述卤代烃类溶剂为c1-c4卤代烃类溶剂;较佳地,所述卤代烃类溶剂为二氯甲烷。在另一优选例中,所述酮类溶剂为c2-c6酮类溶剂;较佳地,所述酮类溶剂选自:丙酮、mibk,或其组合物。在另一优选例中,所述芳类溶剂为c6-c10芳烃;较佳地,为甲苯。在另一优选例中,所述溶剂a包括:甲醇、乙醇、乙腈、甲苯、丙酮、乙酸乙酯、乙酸异丙酯、甲酸乙酯、乙酸甲酯、乙酸正丙酯、乙酸丁酯、二氯甲烷、mibk或其组合。在另一优选例中,所述的溶剂a为酯类溶剂,或者含酯类溶剂的混合溶剂。在另一优选例中,含酯类溶剂的混合溶剂为酯类溶剂与选自下组的溶剂组成的混合溶剂:醇类溶剂、酮类溶剂、卤代烃类溶剂,或其组合。在另一优选例中,所述的溶剂a选自:乙酸乙酯或含乙酸乙酯的混合溶剂。在另一优选例中,所述由乙酸乙酯组成的混合溶剂为由乙酸乙酯和选自下组的溶剂组成的混合溶剂:甲醇、乙醇、乙腈、甲苯、丙酮、二氯甲烷、mibk,或其组合。在另一优选例中,步骤a1)中,所得的澄清的溶液a的浓度可以为0.005~1.0g/ml,优选为0.01~0.2g/ml。在另一优选例中,步骤a1)中,溶解温度为10-100℃;较佳地,20~80℃;更佳地,40~70℃。与现有技术相比,本发明具有如下显著性有益效果:(1)所述的晶型azt-a相对于已知的无水物晶型(如晶型1和晶型2),有更好的溶解度,对后续制剂的溶出具有重要意义;(2)所述的晶型azt-a现对于现有的无水物具有静电作用小(实验中发现本发明的晶型相比现有无水晶型不易因静电吸附于金属表面如金属刮刀表面),适宜制剂生产的优势;(3)所述的晶型azt-a的制备工艺简单,可操作性强,产率高,质量稳定,生产周期短,易于实现规模化生产。(4)所述的晶型azt-a相比无定型更不易扬尘、在高湿度和/或高温下稳定性更好,不易吸湿、流动性好适合制剂工艺。恩曲替尼的晶型azt-b及其制备方法在一个具体实施例中,本发明提供的恩曲替尼的晶型为晶型azt-b。在另一优选例中,所述晶型azt-b为恩曲替尼的无水物。在一个具体实施例中,在粉末x射线衍射下,晶型azt-b在2θ为7.4±0.2°、8.1±0.2°、14.8±0.2°、17.2±0.2°、19.9±0.2°处具有特征峰。在另一优选例中,在粉末x射线衍射下,所述晶型azt-b还在2θ为11.4±0.2°、12.0±0.2°、20.9±0.2°、22.3±0.2°、23.5±0.2°、和/或24.1±0.2°处具有特征峰。在另一优选例中,本发明所述的恩曲替尼的晶型azt-b,在粉末x射线衍射下,在2θ为7.4±0.2°、8.1±0.2°、11.4±0.2°、12.0±0.2°、14.8±0.2°、17.2±0.2°、19.9±0.2°、20.9±0.2°、22.3±0.2°、23.5±0.2°、24.1±0.2°处具有特征峰。在另一优选例中,在粉末x射线衍射下,所述晶型azt-b在2θ为14.8±0.2°处的特征峰的相对强度≥90%;更优选地,≥95%;最优选地,约为100%。在另一优选例中,在粉末x射线衍射下,除14.8±0.2°处的特征峰外,所述晶型azt-b的其余特征峰的相对强度≤90%;较佳地,≤75%。在另一优选例中,本发明所述的恩曲替尼的晶型azt-b,在粉末x射线衍射下具有以下特征峰及相对强度:2θ/°相对强度7.4±0.240%8.1±0.219%14.8±0.2100%16.7±0.216%17.2±0.262%19.9±0.266%22.3±0.239%23.5±0.225%24.1±0.226%在另一优选例中,所述晶型azt-b具有基本如图5所示的xrpd谱图;在另一优选例中,在tga图中,所述晶型azt-b在30℃-150℃范围内失重0.8±0.1%。在另一优选例中,所述晶型azt-b具有基本如图6所示的tga谱图。在另一优选例中,在dsc图中,所述晶型azt-b在147.3±0.5℃有熔融吸热峰。在另一优选例中,所述晶型azt-b具有基本如图7所示的dsc谱图;在另一优选例中,所述晶型azt-b具有基本如图8所示的1h-nmr谱图。在一个具体实施例中,本发明还提供了一种制备本发明所述的恩曲替尼的晶型的方法,其中,所述晶型为晶型azt-b;所述方法(即方法b1)包括步骤:将恩曲替尼原料于溶剂b中打浆,优选地打浆温度为0-50℃(较佳地,10~40℃,如室温下),干燥,从而得到晶型azt-b;或者,所述方法(即方法b2)包括步骤:将恩曲替尼原料(较佳地,恩曲替尼原料为本文所述的晶型azt-d)在tb温度下干燥,从而得到晶型azt-b。在另一优选例中,方法b2中,tb=40~80℃;较佳地,tb=50~60℃。在另一优选例中,方法b2中,所述干燥的时间为1~48h;较佳地,2~36h;更佳地,12~24h。在另一优选例中,所述的溶剂b是指在0~50℃,能使恩曲替尼原料部分溶解于其中的溶剂。在另一优选例中,所述打浆时间为1-24h,优选为2-24。在另一优选例中,恩曲替尼原料与溶剂b的质量体积(mg/ml)比为(50~500):1;较佳地,(150~300):1。在另一优选例中,所述溶剂b选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、芳类溶剂,或其组合;或者,所述溶剂b为水与选自下组溶剂组成的混合溶剂:醇类溶剂、酯类溶剂、酮类溶剂、卤代烃类溶剂、芳类溶剂,或其组合。在另一优选例中,所述溶剂b选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烃类溶剂、乙腈、芳类溶剂,或其组合。在另一优选例中,所述酯类溶剂、所述醇类溶剂、芳类溶剂、所述卤代烃类溶剂和所述酮类溶剂如前定义。在另一优选例中,所述溶剂b选自:醇类溶剂、乙腈,或其组合。在另一优选例中,所述溶剂b选自:甲醇、乙醇、乙腈、甲苯、丙酮、乙酸乙酯、二氯甲烷、mibk,或其组合;较佳地,选自:甲醇、乙醇、乙腈,或其组合。与现有技术相比,本发明具有如下显著性有益效果:(1)所述的晶型azt-b相对于已知的无水物晶型(如晶型1和晶型2),有更好的溶解度,对后续制剂的溶出具有重要意义;(2)所述的晶型azt-b现对于现有的无水物具有静电作用(实验中发现本发明的晶型相比现有无水晶型不易因静电吸附于金属表面如金属刮刀表面)小,适宜制剂生产的优势;(3)所述的晶型azt-b的制备工艺简单,可操作性强,产率高,质量稳定,生产周期短,易于实现规模化生产。(4)所述的晶型azt-b相比无定型更不易扬尘、在高湿度和/或高温下稳定性更好,不易吸湿、流动性好适合制剂工艺。恩曲替尼的晶型azt-c及其制备方法在一个具体实施例中,本发明提供的恩曲替尼的晶型为晶型azt-c。在另一优选例中,所述的晶型azt-c,在粉末x射线衍射下,在2θ为18.1±0.2°、23.1±0.2°、25.5±0.2°处具有特征峰。在另一优选例中,在粉末x射线衍射下,所述的晶型azt-c在2θ为7.6±0.2°、11.0±0.2°、13.1±0.2°、15.3±0.2°、18.1±0.2°、18.6±0.2°、22.4±0.2°、23.1±0.2°、25.5±0.2°处具有特征峰。在另一优选例中,在粉末x射线衍射下,所述晶型azt-c在2θ为18.1±0.2°处的特征峰的相对强度≥90%;更优选地,≥95%;最优选地,约为100%。在另一优选例中,在粉末x射线衍射下,除18.1±0.2°处的特征峰外,所述晶型azt-c的其余特征峰的相对强度≤80%;较佳地,≤60%。在另一优选例中,本发明所述的恩曲替尼的晶型azt-c,在粉末x射线衍射下具有以下特征峰及相对强度:2θ/°相对强度7.6±0.213%11.0±0.214%13.1±0.218%15.3±0.212%18.1±0.2100%18.6±0.220%22.4±0.214%23.1±0.253%25.5±0.222%在另一优选例中,所述晶型azt-c具有基本如图9所示的xrpd谱图;在另一个具体实施例中,本发明提供了一种制备本发明所述的恩曲替尼的晶型的方法,其中,所述晶型为晶型azt-c,所述的方法(方法c)包括步骤:提供恩曲替尼原料于溶剂c中的溶液,使溶液析晶(较佳地,通过加入晶种使溶液析晶),收集析出固体,从而得到晶型azt-c。在另一优选例中,所述的晶种为晶型azt-a。在另一优选例中,在收集析出固体前还包括打浆或搅拌的步骤。在另一优选例中,打浆或搅拌1~48h;较佳地,打浆或搅拌2~30h;更佳地,10~24h。在另一优选例中,在0~50℃(较佳地,10~40℃;更佳地,15~30℃)下搅拌或打浆。在另一优选例中,所述的方法包括步骤:c1)将恩曲替尼原料溶解于溶剂c中,较佳地溶解温度为10-100℃(如50~70℃),从而得到得到恩曲替尼原料于溶剂c中的溶液(澄清);c2)向得到的溶液中加入晶种析晶,并搅拌或打浆,收集析出固体,从而得到晶型azt-c。在另一优选例中,恩曲替尼原料于溶剂c中的溶液的浓度可以为0.005~1.0g/ml,优选为0.01~0.1g/ml。在另一优选例中,所述的溶剂c是指在10~100℃,能使恩曲替尼原料完全溶解于其中的溶剂。在另一优选例中,所述溶剂c选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、芳类溶剂,或其组合;或者,所述溶剂c为水与选自下组溶剂组成的混合溶剂:醇类溶剂、酯类溶剂、酮类溶剂、芳类溶剂、卤代烷烃类溶剂,或其组合。在另一优选例中,所述溶剂c选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、芳类溶剂,或其组合。在另一优选例中,所述酯类溶剂、所述醇类溶剂、芳类溶剂、所述卤代烷烃类溶剂和所述酮类溶剂如前定义。在另一优选例中,所述溶剂c为酯类溶剂;较佳地选自:乙酸乙酯、乙酸异丙酯、乙酸丁酯,或其组合。恩曲替尼的晶型azt-d及其制备方法在一个具体实施例中,本发明提供的恩曲替尼的晶型为晶型azt-d。在另一优选例中,在粉末x射线衍射下,晶型azt-d在2θ为7.1±0.2°、7.4±0.2°、13.4±0.2°、17.6±0.2°、19.8±0.2°、22.6±0.2°处具有特征峰。在另一优选例中,本发明所述的恩曲替尼的晶型azt-d,在粉末x射线衍射下,在2θ为7.1±0.2°、7.4±0.2°、7.6±0.2°、12.3±0.2°、13.4±0.2°、14.4±0.2°、15.0±0.2°、16.0±0.2°、16.7±0.2°、17.6±0.2°、19.5±0.2°、19.8±0.2°、20.3±0.2°、22.3±0.2°、22.6±0.2°24.7±0.2°处具有特征峰。在另一优选例中,在粉末x射线衍射下,所述晶型azt-d在2θ为13.4±0.2°处的特征峰的相对强度≥90%;更优选地,≥95%;最优选地,约为100%。在另一优选例中,在粉末x射线衍射下,除13.4±0.2°处的特征峰外,所述晶型azt-d的其余特征峰的相对强度≤80%;较佳地,≤50%。在另一优选例中,本发明所述的恩曲替尼的晶型azt-d,在粉末x射线衍射下具有以下特征峰及相对强度:2θ/°相对强度7.1±0.248%7.4±0.238%7.6±0.225%12.3±0.221%13.4±0.2100%14.4±0.226%16.7±0.224%17.6±0.237%19.5±0.224%19.8±0.240%22.3±0.224%22.6±0.231%24.7±0.223%在另一优选例中,所述晶型azt-c具有基本如图10所示的xrpd谱图;在另一个具体实施例中,本发明还提供了一种制备本发明所述的恩曲替尼的晶型的方法,其中,所述晶型为晶型azt-d,所述方法包括如下步骤:d1)提供恩曲替尼原料于溶剂d中的混合物,打浆或搅拌(优选地打浆或搅拌温度为0-70℃;较佳地,0-50℃;更佳地,10-40℃;最佳地,15-30℃),收集其中固体,从而得到晶型azt-d。在另一优选例中,恩曲替尼原料与溶剂c的质量体积(g/ml)比为(0.01-0.5):1;较佳地,(0.02-0.2):1;更佳地,为(0.05-0.1):1。在另一优选例中,所述的溶剂d是指在0~70℃,能使恩曲替尼原料部分溶解于其中的溶剂。在另一优选例中,所述恩曲替尼原料为晶型azt-c。在另一优选例中,所述溶剂d选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、芳类溶剂,或其组合;或者,所述溶剂d为水与选自下组溶剂组成的混合溶剂:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂,或其组合。在另一优选例中,所述溶剂d选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、芳类溶剂,或其组合。在另一优选例中,所述酯类溶剂、所述醇类溶剂、芳类溶剂、所述卤代烷烃类溶剂和所述酮类溶剂如前定义。在另一优选例中,所述溶剂d选自:醇类溶剂、乙腈,或其组合;较佳地,溶剂d为乙腈。在另一优选例中,步骤a)为将恩曲替尼原料于溶剂d中打浆,打浆温度为0-70℃,收集溶剂中的固体,从而得到azt-d。恩曲替尼的晶型azt-e及其制备方法在一个具体实施例中,本发明提供的恩曲替尼的晶型为晶型azt-e。在另一优选例中,所述晶型azt-e为恩曲替尼的一水合物。在另一优选例中,在粉末x射线衍射下,晶型azt-e在2θ为8.9±0.2°、10.5±0.2°、16.6±0.2°、17.2±0.2°处具有特征峰。在另一优选例中,在粉末x射线衍射下,晶型azt-e还在2θ为15.9±0.2°、17.0±0.2°、17.9±0.2°、22.8±0.2°、和/或24.7±0.2°处具有特征峰。在另一优选例中,在粉末x射线衍射下,晶型azt-e在2θ为8.9±0.2°、10.5±0.2°、15.9±0.2°、16.6±0.2°、17.0±0.2°、17.2±0.2°、17.9±0.2°、22.8±0.2°、24.7±0.2°处具有特征峰。在另一优选例中,在粉末x射线衍射下,除除2.7±0.2°处和20.6±0.2°处的特征峰外,所述晶型azt-e的其余特征峰的相对强度≤80%;更优选地,≤60%;最优选地,≤40%。在另一优选例中,本发明所述的恩曲替尼的晶型azt-e,在粉末x射线衍射下具有以下特征峰及相对强度:2θ/°相对强度8.9±0.2100%10.5±0.216.3%15.9±0.2°9.7%16.6±0.230%17.0±0.221%17.3±0.229%18.0±0.223%22.8±0.220%24.7±0.220%在另一优选例中,所述晶型azt-e在50℃-150℃范围内失重约3.3±0.1%;在另一优选例中,所述晶型azt-e在126.35±0.5℃有脱水峰,在197.15±0.5℃有熔融吸热峰。在另一优选例中,所述晶型azt-e具有基本如图11所示的xrpd谱图。在另一优选例中,所述晶型azt-e具有基本如图12所示的tga谱图。在另一优选例中,所述晶型azt-e具有基本如图13所示的dsc谱图。在另一优选例中,所述晶型azt-e具有基本如图14所示的1h-nmr谱图。在另一个具体实施例中,本发明还提供了一种制备本发明所述的恩曲替尼的晶型的方法,其中,所述晶型为晶型azt-e;所述方法(即方法e)包括步骤:1)提供恩曲替尼原料于溶剂e与水中的混合物,打浆或搅拌,收集混合物中的固体,从而得到晶型azt-e。在另一优选例中,打浆或搅拌的温度为te1且te1=0-50℃;较佳地,te1=0~40℃;更佳地,te1=0~5℃或15~30℃(如室温)。在另一优选例中,打浆或搅拌的时间为te1且te1≥2h较佳地,te1≥12h。在另一优选例中,步骤1)前还包括步骤:0)在te2温度下,先将恩曲替尼原料于溶剂e打浆te2时间(较佳地,te2=0.1~1小时;更佳地,te2=0.4~0.6小时),加入水,从而得到恩曲替尼原料于溶剂e与水的体系中混合物。在另一优选例中,所述恩曲替尼原料选自下组:晶型azt-a、晶型azt-b、晶型azt-c,或其组合。在另一优选例中,溶剂e与水的体积比为(0.1~10):1;较佳地,为(0.2~5):1。在另一优选例中,恩曲替尼与溶剂e的质量体积(g/ml)比为(0.05~0.5):1。在另一优选例中,恩曲替尼与水的质量体积比为(0.015~1.5):1。在另一优选例中,所述溶剂e选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、芳类溶剂,或其组合。在另一优选例中,所述酯类溶剂、所述醇类溶剂、芳类溶剂、所述卤代烃类溶剂和所述酮类溶剂如前定义。在另一优选例中,所述溶剂e选自:甲醇、乙醇、乙腈、甲苯、丙酮、乙酸乙酯、二氯甲烷、mibk,或其组合。在另一优选例中,所述溶剂e为醇类溶剂。在另一优选例中,所述溶剂e选自:甲醇、乙醇,或其组合。在另一优选例中,当所述溶剂e为乙醇时,溶剂e与水的体积比为(1~10):1;较佳地,为(3~5):1。在另一优选例中,当所述溶剂e为乙醇时,恩曲替尼与溶剂e的质量体积(g/ml)比为(0.1~0.5):1。在另一优选例中,当所述溶剂e为乙醇时,恩曲替尼与水的质量体积比为(0.8~1.5):1。在另一优选例中,当所述溶剂e为甲醇时,溶剂e与水的体积比为(0.1~1):1;较佳地,为(0.2~0.5):1。在另一优选例中,当所述溶剂e为甲醇时,恩曲替尼与溶剂e的质量体积(g/ml)比为(0.05~0.1):1。在另一优选例中,当所述溶剂e为甲醇时,恩曲替尼与水的质量体积比为(0.015~0.05):1。与现有技术相比,本发明具有如下显著性有益效果:(1)所述的晶型azt-e相对于已知的各种溶剂化物,不存在溶剂毒性问题;(2)所述的晶型azt-e具有更好的热稳定性、高湿稳定性和压力稳定性,对后续制剂的制备及存储具有重要意义;(3)所述的晶型azt-e具有静电作用小(实验中发现本发明的晶型相比现有无水晶型不易因静电吸附于金属表面如金属刮刀表面),适宜制剂生产的优势;(4)所述的晶型azt-e的制备工艺简单,可操作性强,产率高,质量稳定,生产周期短,易于实现规模化生产。(5)所述的晶型azt-e比无定型更不易扬尘、在高湿度和/或高温下稳定性更好,不易吸湿、流动性好适合制剂工艺。恩曲替尼的晶型azt-f及其制备方法在一个具体实施例中,本发明提供的恩曲替尼的晶型为晶型azt-f。在另一优选例中,在粉末x射线衍射下,晶型azt-f在2θ为4.8±0.2°、8.2±0.2°、10.2±0.2°、14.3±0.2°、17.4±0.2°、18.3±0.2°、19.2±0.2°、19.7±0.2°、20.6±0.2°、22.0±0.2°、22.4±0.2°、22.7±0.2°、23.5±0.2°处具有特征峰。优选地,本发明所述的恩曲替尼晶型azt-f,在粉末x射线衍射下,在2θ为2θ为4.8±0.2°、8.2±0.2°、9.3±0.2°、10.2±0.2°、13.6±0.2°、14.3±0.2°、16.5±0.2°、17.2±0.2°、17.4±0.2°、18.3±0.2°、19.2±0.2°、19.7±0.2°、20.6±0.2°、22.0±0.2°、22.4±0.2°、22.7±0.2°、23.5±0.2°、24.0±0.2°、25.3±0.2°、26.4±0.2°处具有特征峰。在另一优选例中,本发明所述的恩曲替尼的晶型azt-f,在粉末x射线衍射下具有以下特征峰及相对强度:在另一优选例中,所述晶型azt-f具有基本如图15所示的xrpd谱图。在一个实施例中,本发明还提供了一种制备本发明所述的恩曲替尼的晶型的方法,其中所述晶型为晶型azt-f,所述的方法(方法f)包括步骤:提供恩曲替尼原料于溶剂f中的溶液,浓缩,收集析出固体,从而得到晶型azt-f。在另一优选例中,所述的方法包括步骤:d1)将恩曲替尼原料溶解于溶剂f中,优选地溶解温度为10-100℃,得到恩曲替尼原料于溶剂f中的溶液(澄清);d2)将步骤d1)得到溶液f中进行浓缩,收集析出固体,从而得到晶型azt-f。在另一优选例中,所述的溶剂f是指在10~100℃,能使恩曲替尼原料完全溶解于其中的溶剂。在另一优选例中,溶剂f的定义与溶剂c相同。在另一优选例中,所述溶剂f包括甲醇、dmf、乙腈、甲苯、丙酮、mibk、和/或甲苯等溶剂。优选地,所述溶剂f为甲苯。在另一优选例中,浓缩的时间≤24h。在另一优选例中,浓缩的温度为30~70℃;较佳地,为40~60℃。恩曲替尼的晶型azt-g及其制备方法在一个具体实施例中,本发明提供的恩曲替尼的晶型为晶型azt-g。在另一优选例中,在粉末x射线衍射下,晶型azt-g在2θ为8.1±0.2°、9.3±0.2°、10.2±0.2、14.3±0.2°、17.2±0.2°、17.4±0.2°、18.2±0.2°、19.1±0.2°、20.6±0.2°、22.0±0.2°、22.4±0.2°、23.5±0.2°处具有特征峰。在另一优选例中,本发明所述的恩曲替尼的晶型azt-g,在粉末x射线衍射下具有以下特征峰及相对强度:在另一优选例中,所述晶型azt-g具有基本如图16所示的xrpd谱图。在一个具体实施例中,本发明提供了一种制备本发明所述的恩曲替尼的晶型的方法,其中所述晶型为晶型azt-g,所述方法(方法g)包括步骤:提供恩曲替尼原料于溶剂g中的溶液,挥发溶剂g,收集析出固体,从而得到晶型azt-g。在另一优选例中,所述方法包括步骤:g1)将恩曲替尼原料溶解于溶剂g中,优选地溶解温度为10-100℃,得到恩曲替尼原料于溶剂g中的溶液(澄清);和g2)挥发除去步骤g1)得到的溶液g中的溶剂,从而得到azt-g。在另一优选例中,所述的溶剂g是指在10~100℃,能使恩曲替尼原料完全溶解于其中的溶剂。在另一优选例中,溶剂g的定义同溶剂c。在另一优选例中,溶剂g包括甲醇、异丙醇、甲苯、丙酮、硝基甲烷、二氯甲烷、和/或mibk等溶剂,或者溶剂g为上述溶剂与水的混合溶剂。在另一优选例中,所述溶剂g为甲苯。在另一优选例中,挥发的时间≥48h;较佳地,≥96h。在另一优选例中,挥发的温度为20~60℃;较佳地,为30~50℃。恩曲替尼的无定型及其制备方法在一个具体实施例中,本发明提供了恩曲替尼的无定型,所述无定型具有基本如图21所示的xprd谱图。在另一优选例中,在dsc图中,所述无定型在80~100℃具有玻璃化转变峰。在另一优选例中,所述无定型具有基本如图22所示的dsc图。在另一优选例中,所述无定型在15℃-100℃范围内失重0.2±0.1%。在另一优选例中,所述无定型具有基本如图23所示的tga图。本发明所述的恩曲替尼无定型其制备方法,包括如下步骤:a)将恩曲替尼原料溶解于溶剂1中,较佳地溶解温度为0-100℃,得到澄清的溶液1;b)向溶液1中添加溶剂2进行析晶,收集析出固体,从而得到无定型。在另一优选例中,所述的溶剂1是指在10~100℃,能使恩曲替尼原料完全溶解于其中的溶剂。在另一优选例中,所述溶剂1选自:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂、乙腈、芳类溶剂,或其组合;或者,所述溶剂1为水与选自下组溶剂组成的混合溶剂:醇类溶剂、酯类溶剂、酮类溶剂、卤代烷烃类溶剂,或其组合。在另一优选例中,所述酯类溶剂、所述醇类溶剂、芳类溶剂、所述卤代烷烃类溶剂和所述酮类溶剂如前定义。在另一优选例中,所述溶剂1为酯类溶剂、醇类溶剂,或其组合。在另一优选例中,所述溶剂1选自:甲醇、乙醇、异丙醇、乙腈、甲苯、丙酮、乙酸乙酯、二氯甲烷、mibk、甲苯,或其组合。在另一优选例中,所述溶剂2是指对恩曲替尼溶解度较差的溶剂。在另一优选例中,所述溶剂2选自:饱和烃类溶剂、醚类溶剂、水,或其组合。在另一优选例中,所述饱和烃类溶剂为c1-c10脂肪烷烃;较佳地,选自下组:正庚烷、正己烷,或其组合。在另一优选例中,所述醚类溶剂为链状醚类溶剂;较佳地,选自下组:甲叔醚、苯甲醚,或其组合。在另一优选例中,所述溶剂2选自下组:正庚烷、正己烷、甲叔醚、水、苯甲醚等,或其组合;较佳地,所述溶剂2选自:正己烷、水,或其组合物。恩曲替尼的晶型azt-h及其制备方法在一个具体实施例中,本发明提供的恩曲替尼的晶型为晶型azt-h。在另一优选例中,晶型azt-h是恩曲替尼2分子1.4-二氧六环溶剂合物。在另一优选例中,在粉末x射线衍射下,晶型azt-h在2θ为12.5±0.2°、12.8±0.2°、16.4±0.2、16.8±0.2°、18.5±0.2°、19.0±0.2°、20.1±0.2°、20.8±0.2°、21.1±0.2°处具有特征峰。优选地,本发明所述的恩曲替尼的晶型azt-h,在粉末x射线衍射下具有以下特征峰及相对强度:在另一优选例中,所述晶型azt-h具有基本如图17所示的xrpd谱图。在另一优选例中,所述晶型azt-h具有基本如图18所示的tga谱图。在另一个具体实施例中,提供了一种制备本发明所述的恩曲替尼的晶型的方法,其中所述晶型为晶型azt-h,所述方法(方法h)步骤:a)将恩曲替尼原料于醚类溶剂(如1,4-二氧六环等)中搅拌或打浆,优选地打浆温度为0-50℃,优选地打浆时间为1-24h;b)收集固体,从而得到晶型azt-h。在另一优选例中,恩曲替尼原料与于1,4-二氧六环的质量体积(g:ml)比为(0.01~0.1):1;较佳地,为(0.02~0.05):1。恩曲替尼的晶型azt-i及其制备方法在一个具体实施例中,本发明提供的恩曲替尼的晶型为晶型azt-i。在另一优选例中,在粉末x射线衍射下,晶型azt-i在2θ为8.1±0.2°、10.1±0.2°、14.4±0.2、17.3±0.2°、18.1±0.2°、19.0±0.2°、20.2±0.2°、22.0±0.2°、23.2±0.2°处具有特征峰。在另一优选例中,本发明所述的恩曲替尼的晶型azt-i,在粉末x射线衍射下具有以下特征峰及相对强度:2θ/°相对强度8.1±0.245%10.1±0.223%14.4±0.221%17.3±0.219%18.1±0.233%19.0±0.232%20.2±0.261%22.1±0.2100%23.2±0.248%在另一优选例中,所述晶型azt-i具有基本如图19所示的xrpd谱图。在另一优选例中,所述晶型azt-i具有基本如图20所示的tga谱图。在另一个具体实施中,本发明提供了一种制备本发明所述的恩曲替尼的晶型的方法,其中所述晶型为晶型azt-i,所述方法(方法g)包括步骤:提供恩曲替尼原料于溶剂i中的混合物,打浆或搅拌,收集混合物中的固体,从而得到晶型azt-i。在另一优选例中,打浆或搅拌的温度为0-50℃。在另一优选例中,打浆或搅拌的时间为1-24h。在另一优选例中,所述溶剂i是指在10~100℃不能使恩曲替尼原料完全溶解于其中的溶剂。在另一优选例中,溶剂i包括硝基甲烷、二氯甲烷、苯甲醚、2-methf,或其组合,或者溶剂i为上述溶剂与水的混合溶剂。在另一优选例中,恩曲替尼原料与溶剂i的质量体积(g:ml)比为(0.01~0.1):1;较佳地,为(0.02~0.05):1。本发明的主要优点包括:(1)本发明提供的式i化合物的晶型高温高湿条件下放置稳定性高。(2)本发明的晶型还具有不易扬起,不易吸湿生物利用度高等优点;且本发明的晶型制备方法简单,易于工业化生产。(3)本发明的晶型的溶解度相比现有技术中的其他晶型更高。(4)本发明的晶型具有优异的压力稳定性。药物组合物和施用方法由于本发明的晶型或无定型具有优异的对癌症或肿瘤的治疗和预防作用,因此本发明的晶型或无定型以及含有本发明的晶型或无定型为主要活性成分的药物组合物可用于治疗和/或预防癌症或肿瘤。例如,本发明的晶型或无定型可以用于制备治疗成人转移性ros1阳性非小细胞肺癌(nsclc)患者,12岁及以上患有实体瘤的成人和儿童患者的药物,该药物可以通过本领域常用方法制得。本发明的药物组合物包含安全有效量范围内的本发明的晶型及药学上可以接受的赋形剂或载体。其中,“安全有效量”指的是:化合物(或晶型)的量足以明显改善病情,而不至于产生严重的副作用。通常,药物组合物含有1-2000mg本发明的晶型/剂,更佳地,含有10-200mg本发明的晶型/剂。较佳地,所述的“一剂”为一个胶囊或药片。“药学上可以接受的载体”指的是:一种或多种相容性固体或液体填料或凝胶物质,它们适合于人使用,而且必须有足够的纯度和足够低的毒性。“相容性”在此指的是组合物中各组份能和本发明的活性成分以及它们之间相互掺和,而不明显降低活性成分的药效。药学上可以接受的载体部分例子有纤维素及其衍生物(如羧甲基纤维素钠、乙基纤维素钠、纤维素乙酸酯等)、明胶、滑石、固体润滑剂(如硬脂酸、硬脂酸镁)、硫酸钙、植物油(如豆油、芝麻油、花生油、橄榄油等)、多元醇(如丙二醇、甘油、甘露醇、山梨醇等)、乳化剂润湿剂(如十二烷基硫酸钠)、着色剂、调味剂、稳定剂、抗氧化剂、防腐剂、无热原水等。本发明的多晶型物或药物组合物的施用方式没有特别限制,代表性的施用方式包括(但并不限于):口服、瘤内、直肠、肠胃外(静脉内、肌肉内或皮下)、和局部给药。用于口服给药的固体剂型包括胶囊剂、片剂、丸剂、散剂和颗粒剂。在这些固体剂型中,活性成分与至少一种常规惰性赋形剂(或载体)混合,如柠檬酸钠或磷酸二钙,或与下述成分混合:(a)填料或增容剂,例如,淀粉、乳糖、蔗糖、葡萄糖、甘露醇和硅酸;(b)粘合剂,例如,羟甲基纤维素、藻酸盐、明胶、聚乙烯基吡咯烷酮、蔗糖和阿拉伯胶;(c)保湿剂,例如,甘油;(d)崩解剂,例如,琼脂、碳酸钙、马铃薯淀粉或木薯淀粉、藻酸、某些复合硅酸盐、和碳酸钠;(e)缓溶剂,例如石蜡;(f)吸收加速剂,例如,季胺化合物;(g)润湿剂,例如鲸蜡醇和单硬脂酸甘油酯;(h)吸附剂,例如,高岭土;和(i)润滑剂,例如,滑石、硬脂酸钙、硬脂酸镁、固体聚乙二醇、十二烷基硫酸钠,或其混合物。胶囊剂、片剂和丸剂中,剂型也可包含缓冲剂。固体剂型如片剂、糖丸、胶囊剂、丸剂和颗粒剂可采用包衣和壳材制备,如肠衣和其它本领域公知的材料。它们可包含不透明剂,并且,这种组合物中活性成分的释放可以延迟的方式在消化道内的某一部分中释放。可采用的包埋组分的实例是聚合物质和蜡类物质。必要时,活性成分也可与上述赋形剂中的一种或多种形成微胶囊形式。用于口服给药的液体剂型包括药学上可接受的乳液、溶液、悬浮液、糖浆或酊剂。除了活性成分外,液体剂型可包含本领域中常规采用的惰性稀释剂,如水或其它溶剂,增溶剂和乳化剂,例知,乙醇、异丙醇、碳酸乙酯、乙酸乙酯、丙二醇、1,3-丁二醇、二甲基甲酰胺以及油,特别是棉籽油、花生油、玉米胚油、橄榄油、蓖麻油和芝麻油或这些物质的混合物等。除了这些惰性稀释剂外,组合物也可包含助剂,如润湿剂、乳化剂和悬浮剂、甜味剂、矫味剂和香料。除了活性成分外,悬浮液可包含悬浮剂,例如,乙氧基化异十八烷醇、聚氧乙烯山梨醇和脱水山梨醇酯、微晶纤维素、甲醇铝和琼脂或这些物质的混合物等。用于肠胃外注射的组合物可包含生理上可接受的无菌含水或无水溶液、分散液、悬浮液或乳液,和用于重新溶解成无菌的可注射溶液或分散液的无菌粉末。适宜的含水和非水载体、稀释剂、溶剂或赋形剂包括水、乙醇、多元醇及其适宜的混合物。用于局部给药的本发明的多晶型物的剂型包括软膏剂、散剂、贴剂、喷射剂和吸入剂。活性成分在无菌条件下与生理上可接受的载体及任何防腐剂、缓冲剂,或必要时可能需要的推进剂一起混合。本发明的晶型可以单独给药,或者与其他药学上可接受的化合物联合给药。使用药物组合物时,是将安全有效量的本发明的多晶型物适用于需要治疗的哺乳动物(如人),其中施用时剂量为药学上认为的有效给药剂量,对于60kg体重的人而言,日给药剂量通常为1~2000mg,优选20~500mg。当然,具体剂量还应考虑给药途径、病人健康状况等因素,这些都是熟练医师技能范围之内的。下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数是重量百分比和重量份数。在本发明中,晶型的结晶水来自空气或溶剂。本发明中所用的溶剂均为分析纯,含水量约为0.1%。对比例1制备恩曲替尼晶型1按照wo2013174876中[0133]记载的方法:将5.5g干燥的无定型n-(5-(3,5-二氟苄基)-1h-吲唑-3-基)-4-(4-甲基哌嗪-1-基)-2-((四氢-2h-吡喃-4-基)氨基)苯甲酰胺混悬在130ml乙醇中,加热回流10分钟;在冷却至室温前蒸馏约70ml乙醇。加入110ml水用55mg晶型1向混悬液中加入晶种。将混悬液搅拌约72小时,采样以通过dsc监测向晶型1的转化。最后将混悬液过滤和干燥,制备得到4.3g晶型1。对比例2制备恩曲替尼晶型2按照wo2013174876中[0134]记载的方法:将干燥的无定型n-(5-(3,5-二氟苄基)-1h-吲唑-3-基)-4-(4-甲基哌嗪-1-基)-2-((四氢-2h-吡喃-4-基)氨基)苯甲酰胺在10体积的乙醇中浆液化,以能够转化为期望的晶型2;然后加入20体积的水并过滤悬浊液。最后将产物在真空下干燥,制备得到晶型2。对比例3制备恩曲替尼晶型4按照wo2017202674中实施例1记载的方法:将干燥的无定型n-(5-(3,5-二氟苄基)-1h-吲唑-3-基)-4-(4-甲基哌嗪-1-基)-2-((四氢-2h-吡喃-4-基)氨基)苯甲酰胺悬浮于10倍体积的乙醇中(悬浮液a)。取20ml悬浮液a加热至60℃以得到溶液,然后将所述溶液冷却至室温。往溶液中加入20ml水获得悬浮液并且过滤沉淀物。将产物在真空下干燥,制备得到晶型4。实施例1恩曲替尼晶型azt-a的制备实施例1-1将2g恩曲替尼晶型2和10ml乙酸乙酯混合,加热至50℃溶解,降温至10℃,室温干燥得到晶型azt-a。其x-射线粉末衍射图如图1所示;对所得固体进行tga测试其谱图如图2所示;对所得固体进行dsc测试其谱图如图3所示;对所得固体进行1h-nmr测试其谱图如图4所示。图2tga显示,晶型azt-a在30℃-150℃失重0.3%,为无水物。图3dsc显示,晶型azt-a在162.5℃的第1个吸热峰和196.78℃的第2个吸热峰。实施例1-2将20mg恩曲替尼晶型2和0.8ml乙酸异丙酯混合,加热至40℃溶解,降温至20℃,30℃干燥得到晶型azt-a。实施例1-3在室温下,将20mg恩曲替尼原料azt-b(实施例2中提到晶型azt-b)于1ml乙酸乙酯/乙醇(1:1)混合溶剂溶解(40-50℃下),降温至5℃,干燥得到晶型azt-a。实施例1-4在室温下,将15mg恩曲替尼原料azt-d于0.7ml甲酸乙酯或乙酸甲酯或乙酸正丙酯或乙酸丁酯中,在60℃下溶解,降温至10℃,干燥得到晶型azt-a。实施例1-5将恩曲替尼晶型azt-c加热至80℃,保温5h,得到晶型azt-a。实施例2恩曲替尼晶型azt-b的制备实施例2-1在室温条件下,将15mg恩曲替尼原料(本专利中提到晶型azt-a)于0.1ml乙醇中打浆24h,干燥得到晶型azt-b;对得到的固体进行xrpd测试,其x-射线粉末衍射图如图5所示;对所得固体进行tga测试其谱图如图6所示;对所得固体进行dsc测试其谱图如图7所示;对所得固体进行1h-nmr测试其谱图如图8所示。图6tga显示,晶型azt-b在30℃-150℃失重0.8%,为无水物。图7dsc显示,晶型azt-b在147.3℃有熔融吸热峰。实施例2-2在40℃条件下,将15mg恩曲替尼原料(国际专利wo2013174876申请中所称的晶型2)于0.6ml乙腈中打浆24h,干燥得到晶型azt-b。实施例2-3在室温条件下,将15mg恩曲替尼无定型于50μl乙醇中,于5℃打浆24h,过滤干燥得到晶型azt-b。实施例2-4将晶型azt-d(实施例4中得到的晶型)在60℃干燥24h,得到晶型azt-b。实施例3恩曲替尼晶型azt-c的制备在60℃下,将20mg恩曲替尼原料(国际专利wo2013174876申请中所称的晶型2)于1.5ml乙酸丁酯溶剂溶清中后过滤,加入少量晶种azt-a(实施例1中提到的晶型azt-a)室温打浆24h,得到晶型azt-c。对得到的固体进行xrpd测试,其x-射线粉末衍射图如图9所示。实施例4恩曲替尼晶型azt-d的制备在室温条件下,将15mg恩曲替尼晶型azt-c于0.3ml乙腈中打浆24h,得到晶型azt-d;其x-射线粉末衍射图如图10所示。实施例5恩曲替尼晶型azt-e的制备实施例5-1在室温条件下,将0.2g恩曲替尼晶型azt-b于1ml乙醇中打浆0.5h后加入0.2ml的纯化水,室温搅拌24h,干燥得到晶型azt-e,对得到的固体进行xrpd测试,其x-射线粉末衍射图如图11所示;进行tga测试,其谱图如图12所示;进行dsc测试,其谱图如图13所示;进行1h-nmr测试,其谱图如图14所示。kf测试显示水分为3.0%(理论一分子水为3.1%)。图12tga显示,晶型azt-e在50℃-150℃失重3.3%,与kf水分吻合,确定是恩曲替尼一水合物。图13dsc显示,晶型azt-e在126.35℃脱水峰和197.15℃的熔融吸热峰。实施例5-2在室温条件下,将0.3g原料azt-a加入1ml乙醇和纯化水比例为3:1的混合溶剂,于5℃搅拌24h得到晶型azt-e。实施例5-3在室温条件下,将15mg原料azt-c于1ml甲醇/水(1:5)中打浆24h,得到晶型azt-e。实施例6恩曲替尼晶型azt-f的制备在室温条件下,将15mg恩曲替尼原料(实施例1中的晶型azt-a)于甲苯中溶清,于50℃浓缩得到固体azt-f;其x-射线粉末衍射图如图15所示。实施例7恩曲替尼晶型azt-g的制备在室温条件下,将15mg恩曲替尼原料(实施例1中的晶型azt-a)于甲苯中溶清,40℃挥发1周,得到固体azt-g;其x-射线粉末衍射图如图16所示。实施例8恩曲替尼晶型azt-h的制备在室温条件下,将15mg恩曲替尼原料(实施例1中的晶型azt-a)于0.5ml1.4-二氧六环中打浆,干燥得到固体azt-h;其x-射线粉末衍射图如图17所示,其tga图如图18所示。图18tga显示,晶型azt-h在50-110℃失重24.208%,应为2分子1.4-二氧六环溶剂合物。实施例9恩曲替尼晶型azt-i的制备实施例9-1在室温条件下,将15mg恩曲替尼原料(实施例1中的晶型azt-a)于0.5ml2-methf中打浆,干燥得到固体azt-i;其x-射线粉末衍射图如图19所示,其tga图如图20所示。kf测试水分为6.5%(理论而分子水为6.2%)图20tga显示,晶型azt-i在60-110℃失重4.8%,110-160℃失重2.5%,与kf水分吻合,应为2水合物。实施例10恩曲替尼无定型的制备实施例10-1:恩曲替尼无定型的制备在室温条件下,将15mg恩曲替尼原料于1ml乙酸乙酯中溶清,于5℃加入正己烷,室温干燥得到无定型;其x-射线粉末衍射图如图21所示,dsc图如图22所示,tga图如图23所示。图22dsc显示,无定型在80-100℃有玻璃化转变峰;图23dsc显示,无定型在室温到100度失重0.2%。实施例10-2:恩曲替尼无定型的制备在室温条件下,将15mg恩曲替尼原料于1.5ml乙醇中溶清,并快速加入15ml纯化水中,室温干燥得到无定型。测试例1晶型稳定性分别将恩曲替尼晶型1(对比例1)、晶型2(对比例2)、晶型4(对比例3)、晶型azt-a(实施例1-1)、晶型azt-b(实施例2-1)、晶型azt-e(实施例5-1)、无定型(实施例10-1)样品各准备多份,分别置于不同条件(60℃、92.5%rh、60℃&92.5%rh及装有五氧化二磷的干燥器(湿度10%))下敞口放置10天,以及在研钵中研磨5min,取样样品检测xrpd和hplc,以检测各实施例的晶型种类和纯度是否发生变化。具体条件及晶型变化情况如表1和表2所示。表1不同晶型的晶型稳定性晶型高温60℃下高湿92.5%低湿10%60℃&92.5%研磨晶型azt-a(实施例1-1)azt-aazt-aazt-aazt-aazt-a晶型azt-b(实施例2-1)azt-bazt-bazt-bazt-bazt-b晶型azt-e(实施例5-1)azt-eazt-eazt-eazt-eazt-e无定型(实施例10-1)无定型无定型无定型--晶型1(对比例1)晶型2晶型1晶型1晶型2晶型2晶型2(对比例2)晶型2晶型2晶型2晶型2晶型2晶型4(对比例3)晶型4晶型4晶型4晶型4晶型4注:’-’代表未检测。表2不同晶型的化学稳定性晶型原始纯度高温60℃高湿92.5%低湿10%60℃&92.5%晶型azt-a(实施例1-1)99.85%99.84%99.86%99.85%99.83%晶型azt-b(实施例2-1)99.81%99.81%99.78%99.81%99.80%晶型azt-e(实施例5-1)99.87%99.85%99.84%99.87%99.86%无定型(实施例10-1)99.78%99.73%99.72%99.78%99.70%晶型1(对比例1)94.1%93.5%93.4%94.1%93.1%晶型2(对比例2)95.0%94.9%95.0%95.0%94.7%晶型4(对比例3)94.8%94.7%94.8%94.8%94.7%注:’-’代表未检测。由表1可以看出,本发明的晶型azt-a、晶型azt-b、晶型azt-e和无定型的晶型稳定性良好,与对比例2和对比例3相当;对比例1的晶型稳定性较差,容易在高温条件下或研磨后转晶为晶型2.由表2可以看出,本发明的晶型azt-a、晶型azt-b、晶型azt-e、无定型化学稳定性良好,与对比例2和对比例3相当。对比例1化学稳定性较差,在高温或高湿度条件下的纯度均有所下降。测试例2溶解度分别称取恩曲替尼晶型azt-a(实施例1-1)、晶型azt-b(实施例2-1)、晶型azt-e(实施例5-1)、无定型(实施例10-1)晶型1(对比例1)、晶型2(对比例2)、晶型4(对比例3)各4份,每份7mg,在37℃环境下分别加入纯化水、ph1.2缓冲液、ph4.5缓冲液和ph6.8缓冲液,直至溶解,结果如表3所示。表3不同晶型的溶解度从以上数据发现,本发明的晶型azt-a、晶型azt-b、晶型azt-e、无定型在ph1.2缓冲液中溶解度均比对比例中的晶型1、晶型2和晶型4好。在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1