结合人NGF的抗体、其制备方法和用途与流程
结合人ngf的抗体、其制备方法和用途
技术领域
1.本发明属于疼痛治疗和生物技术领域,涉及一种结合人ngf的抗体、其制备方法和用途。
背景技术:
2.神经生长因子(ngf)对神经系统的生长发育具有十分重要的作用,为神经元增殖、分化和存活以及功能维持所必需,并能促进神经损伤后的修复和再生。ngf的主要受体是trka。ngf有疼痛信号传递功能,罕见人体基因变异表明阻断ngf或其受体trka可以终止疼痛信号。大量的动物和人体实验表明,ngf的表达水平在创伤、炎症和慢性疼痛中都有所升高。阻断ngf-trka信号可显著抑制疼痛,并且不会对中枢神经系统造成严重影响。
3.疼痛是影响人们生活质量和致残的主要疾病,是未被满足的重大医疗需求之一。虽然阿片类止痛药效果很好,但其成瘾性和大规模使用带来的滥用已成为一个严重的社会问题,美国阿片止痛药滥用已经到了影响人均寿命的程度。但是疼痛也是动物感知环境风险的重要机制,所以高选择性止痛药物发现难度极大。临床试验结果显示,ngf中和抗体是少有的疗效能和吗啡类药物媲美但无成瘾风险的止痛药。
4.tanezumab是第一个进入临床的ngf中和抗体,最早由rinat neuroscience开发。由于阿片类和非甾体抗炎类(nonsteroidal anti-inflammatory drugs,nsaids)止痛药的滥用,理论上没有成瘾风险的tanezumab备受监管机构和业内期待。2017年6月,fda授予tanezumab治疗骨关节炎、慢性腰背痛的快速通道资格。目前尚无此机制产品上市。然而,仍亟待开发新型、特异、高效、无风险的ngf中和抗体满足临床治疗需求,从而能够改善患有创伤、炎症和慢性疼痛类疾病人群的生活质量,为患者提供更多、更有效的治疗方案。
技术实现要素:
5.为了解决上述技术问题,本发明的发明人进行了大量试验,从抗原免疫、杂交瘤筛选、抗体表达纯化到生物活性鉴定,筛选获得了特异性结合人ngf的鼠源抗体,并在此基础上,进一步构建获得其嵌合抗体以及人源化抗体。
6.因此,本发明的目的在于提供一种结合人ngf的抗体或其抗原结合片段;提供编码所述结合人ngf的抗体或其抗原结合片段的核苷酸分子;提供包含所述核苷酸分子的表达载体;提供所述表达载体的宿主细胞;提供所述结合人ngf的抗体或其抗原结合片段制备方法;提供包含所述结合人ngf的抗体或其抗原结合片段药物组合物;提供所述结合人ngf的抗体或其抗原结合片段在制备药物中的应用。
7.为了实现上述目的,本发明采用了如下技术方案:
8.本发明一方面提供一种结合人ngf的抗体或其抗原结合片段,包括:
9.(a)重链互补决定区h-cdr1、h-cdr2、h-cdr3,所述的h-cdr1的氨基酸序列如seq id no:7所示,所述的h-cdr2的氨基酸序列如seq id no:8所示,所述的h-cdr3的氨基酸序列如seq id no:9所示,和
10.(b)轻链互补决定区l-cdr1、l-cdr2、l-cdr3,所述的l-cdr1的氨基酸序列如seq id no:10所示,所述的l-cdr2的氨基酸序列如seq id no:11所示,所述的l-cdr3的氨基酸序列如seq id no:12所示。
11.本发明“抗体(ab)”是约150000道尔顿的异四聚糖蛋白,其由两个相同的轻链(l)和两个相同的重链(h)组成。每条轻链通过一个共价二硫键与重链相连,而不同免疫球蛋白同种型的重链间的二硫键数目不同。每条重链和轻链也有规则间隔的链内二硫键。每条重链的一端有可变区(vh),其后是恒定区。每条轻链的一端有可变区(vl),另一端有恒定区;轻链的恒定区与重链的第一个恒定区相对,轻链的可变区与重链的可变区相对。本发明的抗体包括单克隆抗体、多克隆抗体、由至少两种抗体形成的多特异性抗体(例如双特异性抗体)等。
12.本发明“单克隆抗体”指从一类基本均一的群体获得的抗体,即该群体中包含的单个抗体是相同的,除少数可能存在的天然发生的突变外。单克隆抗体高特异性地针对单个抗原位点。而且,与常规多克隆抗体制剂(通常是具有针对不同决定簇的不同抗体)不同,各单克隆抗体是针对抗原上的单个决定簇。除了它们的特异性外,单克隆抗体的好处还在于它们是通过杂交瘤培养来合成的,不会被其它免疫球蛋白污染。修饰语“单克隆”表示了抗体的特性,是从基本均一的抗体群中获得的,这不应被解释成需要用任何特殊方法来生产抗体。
13.本发明“抗原结合片段”是指能够与人ngf特异性结合的抗体的片段。本发明的抗原结合片段的例子包括fab片段、f(ab’)2片段、fv片段等。fab片段是用木瓜蛋白酶消化抗体产生的片段。f(ab’)2片段是用胃蛋白酶消化抗体产生的片段。fv片段是由抗体的重链可变区和轻链可变区紧密非共价关联的二聚物组成。
14.作为优选的方案,所述的抗体为鼠源抗体、嵌合抗体或人源化抗体。
15.本发明“鼠源抗体”是指来源于大鼠或小鼠的抗体,优选小鼠。本发明的鼠源抗体为使用人ngf为抗原免疫小鼠并进行杂交瘤细胞筛选获得。
16.本发明“嵌合抗体”是指包含来源于一个物种的重和轻链可变区序列以及来源于另一个物种的恒定区序列的抗体,例如具有与人恒定区连接的鼠重和轻链可变区的抗体。优选的,本发明的嵌合抗体是由鼠源抗体183c6重链可变区和轻链可变区序列与人的恒定区拼接获得。更优选的,本发明的嵌合抗体选自183c6-chimeric。
17.本发明“人源化抗体”是指其cdr来源于非人物种(优选小鼠)抗体,抗体分子中残余的部分(包括框架区和恒定区)来源于人抗体。此外,框架区残基可被改变以维持结合亲和性。优选的,本发明的人源化抗体由鼠源抗体183c6的cdr区和来源自人抗体的非cdr区重组,增加第四个框架区并对部分有重要影响的残基进行突变获得。更优选的,本发明的人源化抗体选自183c6-humanized。
18.作为优选的方案,所述的抗原结合片段包括fab片段、f(ab’)2片段、fv片段。
19.作为优选的方案,所述的结合人ngf的抗体或其抗原结合片段的重链可变区的氨基酸序列如seq id no:4所示,轻链可变区的氨基酸序列如seq id no:6所示;或所述的结合人ngf的抗体或其抗原结合片段的重链可变区的氨基酸序列如seq id no:13所示,轻链可变区的氨基酸序列如seq id no:14所示。
20.作为优选的方案,所述的结合人ngf的抗体或其抗原结合片段的重链的氨基酸序
列如seq id no:19所示,轻链的氨基酸序列如seq id no:20所示。
21.本发明另一方面提供了一种核苷酸分子,所述核苷酸分子编码上述结合人ngf的抗体或其抗原结合片段。
22.作为优选的方案,所述核苷酸分子编码重链可变区的核苷酸序列如seq id no:3所示,编码轻链可变区的核苷酸序列如seq id no:5所示;或所述核苷酸分子编码重链可变区的核苷酸序列如seq id no:15所示,编码轻链可变区的核苷酸序列如seq id no:17所示。
23.作为优选的方案,所述核苷酸分子编码重链的核苷酸序列如seq id no:16所示,编码轻链的核苷酸序列如seq id no:18所示。
24.本发明所述核苷酸分子的制备方法为本领域常规的制备方法,较佳地包括以下制备方法:通过基因克隆技术例如pcr方法等,获得编码上述单克隆抗体的核苷酸分子,或者通过人工全序列合成的方法得到编码上述单克隆抗体的核苷酸分子。
25.本领域技术人员知晓,编码上述结合人ngf的抗体或其抗原结合片段的氨基酸序列的核苷酸序列可以适当引入替换、缺失、改变、插入或增加来提供一个多聚核苷酸的同系物。本发明中多聚核苷酸的同系物可以通过对编码该结合人ngf的抗体或其抗原结合片段基因的一个或多个碱基在保持抗体活性范围内进行替换、缺失或增加来制得。
26.本发明另一方面提供了一种表达载体,所述表达载体含有上述的核苷酸分子。
27.其中所述表达载体为本领域常规的表达载体,是指包含适当的调控序列,例如启动子序列、终止子序列、多腺苷酰化序列、增强子序列、标记基因和/或序列以及其他适当的序列的表达载体。所述表达载体可以是病毒或质粒,如适当的噬菌体或者噬菌粒,更多技术细节请参见例如sambrook等,molecular cloning:a laboratory manual,第二版,cold spring harbor laboratory press,1989。许多用于核酸操作的已知技术和方案请参见current protocols in molecular biology,第二版,ausubel等编著。本发明所述表达载体较佳地为pdr1,pcdna3.1(+),pcdna3.1/zeo(+),pdhfr,pcdna4,pdhff,pgm-csf或pcho 1.0。
28.本发明另外提供了一种宿主细胞,所述宿主细胞含有上述的表达载体。
29.本发明所述的宿主细胞为本领域常规的各种宿主细胞,只要能满足使上述重组表达载体稳定地自行复制,且所携带所述的核苷酸可被有效表达即可。其中所述宿主细胞包括原核表达细胞和真核表达细胞,所述宿主细胞较佳地包括:cos、cho(中国仓鼠卵巢,chinese h amster ovary)、ns0、sf9、sf21、dh5α、bl21(de3)或tg1,更佳地为e.coli tg1、bl21(de3)细胞(表达单链抗体或fab抗体)或者cho-k1细胞(表达全长igg抗体)。将前述表达载体转化至宿主细胞中,即可得本发明优选的重组表达转化体。其中所述转化方法为本领域常规转化方法,较佳地为化学转化法,热激法或电转法。
30.本发明另一方面提供了上述的结合人ngf的抗体或其抗原结合片段的方法,其特征在于,所述方法包括以下步骤:
31.a)在表达条件下,培养上述的宿主细胞,从而表达所述的结合人ngf的抗体或其抗原结合片段;
32.b)分离并纯化a)所述的结合人ngf的抗体或其抗原结合片段。
33.本发明所述的宿主细胞的培养方法、所述抗体的分离和纯化方法为本领域常规方
法,具体操作方法请参考相应的细胞培养技术手册以及抗体分离纯化技术手册。本发明中公开的结合人ngf的抗体或其抗原结合片段的制备方法包括:在表达条件下,培养上述的宿主细胞,从而表达所述的结合人ngf的抗体或其抗原结合片段;分离和纯化所述的所述的结合人ngf的抗体或其抗原结合片段。利用上述方法,可以将重组蛋白纯化为基本均一的物质,例如在sds-page电泳上为单一条带。
34.可以利用亲和层析的方法对本发明公开的所述的结合人ngf的抗体或其抗原结合片段进行分离纯化,根据所利用的亲和柱的特性,可以使用常规的方法例如高盐缓冲液、改变ph等方法洗脱结合在亲和柱上的所述的结合人ngf的抗体或其抗原结合片段。本发明的发明人对所得所述的结合人ngf的抗体或其抗原结合片段进行了检测实验,实验结果表明该所述的结合人ngf的抗体或其抗原结合片段能很好地与抗原结合,具有较高的亲和力。
35.本发明另一方面提供了一种组合物,所述组合物含有上述的结合人ngf的抗体或其抗原结合片段和药学上可接受的载体。
36.本发明提供的结合人ngf的抗体或其抗原结合片段,可以和药学上可以接受的载体一起组成药物制剂组合物从而更稳定地发挥疗效,这些制剂可以保证本发明公开的结合人ngf的抗体或其抗原结合片段的构像完整性,同时还保护蛋白质的多官能团防止其降解(包括但不限于凝聚、脱氨或氧化)。通常情况下,对于液体制剂,通常可以在2℃-8℃条件下保存至少稳定一年,对于冻干制剂,在30℃至少六个月保持稳定。所述双特异性抗体制剂可为制药领域常用的混悬、水针、冻干等制剂。
37.对于本发明公开的结合人ngf的抗体或其抗原结合片段水针或冻干制剂,药学上可以接受的载体较佳地包括但不限于:表面活性剂、溶液稳定剂、等渗调节剂和缓冲液之一或其组合。其中表面活性剂较佳地包括但不限于:非离子型表面活性剂如聚氧乙烯山梨醇脂肪酸酯(吐温20或80);poloxamer(如poloxamer 188);triton;十二烷基硫酸钠(sds);月桂硫酸钠;十四烷基、亚油基或十八烷基肌氨酸;pluronics;monaquattm等,其加入量应使结合人ngf的抗体或其抗原结合片段的颗粒化趋势最小。溶液稳定剂较佳地包括但不限于以下列举之一或其组合:糖类,例如,还原性糖和非还原性糖;氨基酸类,例如,谷氨酸单钠或组氨酸;醇类,例如:三元醇、高级糖醇、丙二醇、聚乙二醇等,溶液稳定剂的加入量应该使最后形成的制剂在本领域的技术人员认为达到稳定的时间内保持稳定状态。等渗调节剂较佳地包括但不限于氯化钠、甘露醇之一或其组合。缓冲液较佳地包括但不限于:tris、组氨酸缓冲液、磷酸盐缓冲液之一或其组合。
38.本发明另一方面提供了上述的结合人ngf的抗体或其抗原结合片段或药物组合物在制备治疗创伤、炎症、慢性疼痛药物中的应用。
39.本发明所述的慢性疼痛较佳地包括但不限于:关节炎或癌症引发的疼痛、慢性腰背痛。
40.本发明结合人ngf的抗体或其抗原结合片段及其组合物在对包括人在内的动物给药时,给药剂量因病人的年龄和体重,疾病特性和严重性,以及给药途径而异,可以参考动物实验的结果和种种情况,总给药量不能超过一定范围。具体讲静脉注射的剂量是1-1800mg/天。
41.在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
42.本发明所用试剂和原料均市售可得。
43.本发明的积极进步效果在于:
44.目前临床上亟待开发新型、特异、高效、无成瘾风险的止痛药,从而能够改善患有创伤、炎症和慢性疼痛类疾病人群的生活质量,为患者提供更多、更有效的治疗方案。本发明的183c6-humanized对人ngf具有很高的亲和力,能够有效地中和人ngf,具有良好的临床应用前景。
附图说明
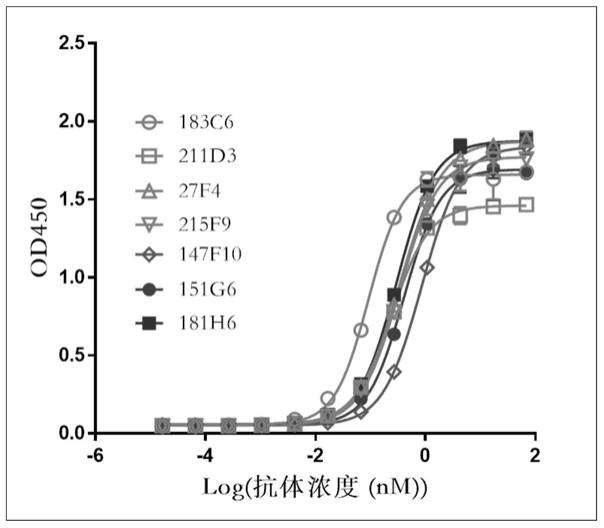
45.图1:elisa检测鼠源抗人ngf单克隆抗体对人ngf的相对亲和力。
46.图2:elisa检测183c6-chimeric和183c6-humanized对人ngf的相对亲和力。
47.图3a:检测183c6-chimeric和183c6-humanized对人ngf诱导的tf-1细胞增殖的抑制。
48.图3b:检测183c6-chimeric和183c6-humanized对人ngf诱导的tf-1细胞增殖的抑制。
49.图4:elisa检测183c6-humanized结合小鼠和大鼠ngf的能力。
具体实施方式
50.以下实施例是对本发明进行进一步的说明,不应理解为是对本发明的限制。实施例不包括对传统方法的详细描述,如那些用于构建载体和质粒的方法,将编码蛋白的基因插入到这样的载体和质粒的方法或将质粒引入宿主细胞的方法.这样的方法对本领域中具有普通技术的人员是众所周知的,并且在许多出版物中都有所描述,包括sambrook,j.,fritsch,e.f.and maniais,t.(1989)molecular cloning:a laboratory manual,2
nd edition,cold spring harbor laboratory press.
51.以下实施例中使用的实验材料和来源以及实验试剂的配制方法具体说明如下。
52.实验材料:
53.hek293f细胞:购自thermo fisher scientific。
54.人ngf:购买自sino biological,货号:11050-hnac。
55.balb/c小鼠:购自上海灵畅生物科技有限公司。
56.杂交瘤sp2/0细胞:购自中国科学院典型培养物保藏委员会细胞库。
57.逆转录试剂盒:购自takara。
58.tf-1细胞系:购自atcc,货号crl-2003
tm
。
59.羊抗鼠二抗:购自sigma,货号sab3701283。
60.小鼠ngf:购自sino biological,货号50385-mnac。
61.大鼠ngf:购自r&d systems,货号7815-ng-025。
62.实验试剂:
63.碳酸钠缓冲液:1.59g na2co3和2.93g nahco3溶于1l纯水中。
64.磷酸盐缓冲液:简写为pbst,配方为:kh2po
4 0.2g,na2hpo4·
12h2o 2.9g,nacl 8.0g,kcl 0.2g,tween-20 0.5ml,加纯水至1l。
65.显色液:底物显色a液:醋酸钠
·
三水13.6g,柠檬酸
·
一水1.6g,30%双氧水
0.3ml,纯水500ml;底物显色b液:乙二胺四乙酸二钠0.2g,柠檬酸
·
一水0.95g,甘油50ml,tmb 0.15g溶于3ml dmso中,纯水500ml;使用前a和b液等体积混匀。
66.终止液:2m硫酸溶液。
67.rpmi-1640培养基:购自thermo fisher scientific。
68.free style 293expression medium:购自thermo fisher scientific。
69.pcdna4:购自thermo fisher scientific。
70.电融合仪ecm2001和细胞融合缓冲液:购自btx。
71.胎牛血清:购自thermo fisher scientific。
72.hat:购自thermo fisher scientific。
73.hybridoma-sfm:购自thermo fisher scientific。
74.trizol:购自thermo fisher scientific。
75.gm-csf:购自厦门特宝生物工程股份有限公司。
76.cck-8:购自dojindo。
77.实验仪器:
78.酶标仪:购自molecular devices,型号spectramax 190。
79.biacore 8k:购自ge healthcare。
80.co2振荡培养箱:购自infors。
81.实施例1阳性对照抗体的制备
82.本发明实施例中所述的阳性对照抗体e3的重链和轻链可变区氨基酸序列分别来自美国专利中us20170342143a1的seq id no 1和2,即本发明的seq id no 1和2。
83.由上海生工生物工程有限公司合成编码阳性对照重链可变区和轻链可变区的dna。将合成的阳性对照重链可变区基因与人igg1重链恒定区基因相连,获得全长的重链基因,命名为e3-hc-igg1;将上述轻链可变区基因与人kappa链恒定区基因相连,获得全长的轻链基因,命名为e3-lc。将e3-hc-igg1和e3-lc基因分别构建到pcdna4表达载体中,利用pei转染法将所得重链和轻链表达载体一起转入hek293f细胞中以表达抗体,hek293f细胞用free style293 expression medium培养。转染后的hek293f细胞置于co2振荡培养箱中培养5天,离心收集细胞上清,利用protein a亲和层析法纯化上清中的抗体,所得抗体命名为e3-igg1。
84.实施例2鼠源抗人ngf单克隆抗体的制备和筛选
85.步骤1:抗原免疫小鼠
86.将作为抗原的人ngf用生理盐水稀释成到合适的浓度,与等体积的弗氏完全佐剂混合,并经超声乳化完全后对4-5周龄的balb/c小鼠进行皮下多点注射,每只小鼠注射50μg抗原/100μl。三周后,等量蛋白与等体积弗氏不完全佐剂混合,超声乳化完全后对小鼠进行皮下多点免疫,两周后再次重复此免疫步骤。所有小鼠在第三次免疫后的第七天取一滴血,分离血清,利用elisa进行血清滴度的检测。对于血清抗体效价>100000的小鼠,在滴度测定后一周进行冲击免疫:尾静脉注射10μg抗原蛋白/100μl生理盐水/鼠。
87.其中,利用elisa进行血清滴度检测的方法说明如下:用碳酸钠缓冲液将人ngf稀释至100ng/ml,然后100μl每孔加入elisa板中,室温孵育2小时;用含0.05%tween-20的pbst洗板;每孔加入含有1%牛血清白蛋白(bsa)的pbst进行封闭,室温孵育1小时;用pbst
洗板两遍,加入梯度稀释的小鼠血清,孵育半小时;用pbst洗板两遍,加入适当稀释的hrp标记的羊抗鼠二抗,孵育半小时;洗板后加入显色液进行显色,用终止液终止显色反应;用酶标仪读取od450;用graphpad prism6进行数据分析,作图并计算血清滴度。
88.步骤2:杂交瘤的制备和筛选
89.小鼠冲击免疫三天后取脾细胞进行融合。生长状态良好的杂交瘤sp2/0细胞在37℃、5%co2孵箱中培养,融合前一天换液。融合与筛选过程如下:取小鼠脾脏,研磨洗涤后计数;按照脾细胞:sp2/0细胞=2:1混合两种细胞,离心后弃掉上清液;然后加入20ml细胞融合缓冲液洗涤细胞三次;细胞沉淀以1
×
107个/ml的密度悬浮于细胞融合缓冲液中;加2ml细胞悬液于融合池中,置于电融合仪ecm2001上,30秒内按一定条件(ac 60v,30s;dc 1700v,40μs,3x;post ac 60v,3s)进行电融合;电融合后轻轻地将融合细胞转移至37℃预热的含有10%胎牛血清的rpmi-1640培养基中,室温继续放置60min;将细胞按104个/孔接种入96孔板,100μl/孔。次日每孔补加100μl的含有2
×
hat和10%血清的rpmi-1640培养基。于融合后第四天用新鲜的含有1
×
hat和rpmi-1640培养基置换一半旧培养液。于融合后第七天用新鲜的含有1
×
hat和rpmi-1640培养基置换大部分旧培养液。于融合后第九天取样进行elisa检测,方法如上述实施例2步骤1中所述。挑选出阳性杂交瘤克隆于24孔板中扩大培养并通过有限稀释法进行亚克隆。通过前述方法获得稳定表达目的抗体的杂交瘤株,对这些克隆进行扩增和细胞冻存。用hybridoma-sfm培养前述杂交瘤株7天,然后用protein a/g亲和层析柱从培养上清中纯化鼠源抗人ngf单克隆抗体。经过纯化后获得7株能够结合人ngf的鼠源单抗,它们的名称分别是183c6、211d3、27f4、215f9、147f10、151g6和181h6,用紫外分光光度法测定所得抗体浓度。
90.用elisa方法检测上述鼠源抗人ngf单抗对人ngf的相对亲和力。实验方法参见实施例2步骤1。
91.结果如图1所示,183c6、211d3、27f4、215f9、147f10、151g6和181h6均能够有效结合人ngf,它们的ec
50
分别是0.09205nm、0.2433nm、0.3459nm、0.3355nm、
92.0.8581nm、0.409nm和0.2988nm。ec
50
越小表示相对亲和力越高,上述结果显示183c6单抗的相对亲和力最高,因此选择183c6进行下一步开发。
93.实施例3鼠源抗人ngf单克隆抗体的人源化
94.步骤1:鼠源抗人ngf单克隆抗体可变区序列的确定
95.使用trizol从183c6杂交瘤单克隆细胞株中提取总rna,用逆转录试剂盒将mrna逆转录成cdna,通过文献报道的组合引物(《antibody engineering》volume 1,edited by roland kontermann and stefan d
ü
bel,组合引物的序列来自第323页)用pcr扩增183c6的轻链可变区和重链可变区基因,然后将pcr产物克隆入pmd18-t载体,测序并分析可变区基因序列。鼠源183c6可变区序列信息如下:重链可变区基因序列全长357bp,编码119个氨基酸残基,核苷酸序列如seq id no:3所示,氨基酸序列如seq id no:4所示;轻链可变区基因序列全长321bp,编码107个氨基酸残基,核苷酸序列如seq id no:5所示,氨基酸序列如seq id no:6所示。
96.步骤2:鼠源抗人ngf单克隆抗体的人源化
97.通对鼠源183c6抗体的重链可变区和轻链可变区氨基酸序列进行分析,依据kabat规则分别确定183c6单抗重链和轻链的抗原互补决定区(cdr)和框架区(fr)。183c6抗体重
链cdr的氨基酸序列为h-cdr1:seq id no:7、h-cdr2:seq id no:8和h-cdr3:seq id no:9,轻链cdr的氨基酸序列为l-cdr1:seq id no:10、l-cdr2:seq id no:11和l-cdr3:seq id no:12。
98.在https://www.ncbi.nlm.nih.gov/igblast/,将鼠源183c6单抗的重链可变区与人igg胚系序列进行同源性比较,选择ighv1-46*01为重链cdr移植模板,将鼠源的183c6抗体的重链cdr移植入ighv1-46*01骨架区,并在h-cdr3之后加入wgqgtlvtvss作为第四个框架区,获得cdr移植重链可变区序列。同样地,将鼠源183c6抗体的轻链可变区与人igg胚系序列同源性比较,选择igkv1-39*01为轻链cdr移植模板,将鼠源183c6抗体的轻链cdr移植入igkv1-39*01的骨架区,并在l-cdr3之后加入fgqgtkveik作为第四个框架区,获得cdr移植轻链可变区序列。在cdr移植可变区的基础上,对一些框架区的氨基酸位点进行突变。在进行突变时,将氨基酸序列进行kabat编码,位点的位置由kabat码指示。优选的,对于cdr移植重链可变区,根据kabat编码,将第30位的t突变为s,将第37位的v突变为i,将第48位的m突变为i,将第67位的v突变为a,将第69位的m突变为l,将第71位的r突变为a,将第73位的t突变为q。对于cdr移植轻链可变区,将第43位的a突变为t,将第44位的p突变为v,将第71位的f突变为y,第87位的y突变为f。上述带有突变位点的重链可变区和轻链可变区分别定义为人源化的重链可变区和轻链可变区,分别命名为183c6-hu-vh(seq id no:13)和183c6-hu-vl(seq id no:14)。
99.由上海生工生物工程有限公司合成编码上述人源化的重链和轻链可变区的dna。将合成的人源化重链可变区基因(seq id no:15)与人igg1重链恒定区相连,获得全长的人源化重链基因(seq id no:16),命名为183c6-hu-hc;将人源化轻链可变区基因(seq id no:17)与人kappa链恒定区相连,获得全长的人源化轻链基因(seq id no:18),命名为183c6-hu-lc。将183c6-hu-hc和183c6-hu-lc基因分别构建到pcdna4表达载体中,利用上述实施例中描述的方法表达并纯化抗体,其重链氨基酸序列为seq id no:19,轻链氨基酸序列为seq id no:20,所得抗体命名为183c6-humanized。
100.另外,将鼠源183c6重链可变区与人igg1重链恒定区相连,获得嵌合重链基因,命名为183c6-chi-hc;将鼠源183c6轻链可变区与人kappa链恒定区相连,获得嵌合轻链基因,命名为183c6-chi-lc。将183c6-chi-hc和183c6-chi-lc基因分别构建到pcdna4表达载体中,利用上述实施例中描述的方法表达并纯化抗体,所得抗体命名为183c6-chimeric。
101.实施例4酶联免疫吸附法(elisa)测定183c6-chimeric和183c6-humanized对抗原的亲和力
102.用elisa方法检测183c6-chimeric和183c6-humanized对人ngf的相对亲和力实验方法参见实施例2步骤1。不同之处在于,此处使用的是hrp标记的羊抗人二抗。
103.结果如图2所示,e3-igg1、183c6-chimeric和183c6-humanized均能有效结合人ngf,它们的ec
50
分别是0.1118nm、0.07049nm和0.06848nm。ec
50
越小表示相对亲和力越高,上述结果显示183c6-chimeric和183c6-humanized的相对亲和力相当,并且两者明显高于e3-igg1。
104.实施例5 biacore 8k测定183c6-chimeric和183c6-humanized对抗原的亲和力
105.本实施例利用biacore 8k检测抗ngf抗体与ngf之间的结合和解离动力学参数,以及平衡解离常数。在biacore 8k上,使用偶联有protein a的芯片捕获抗ngf抗体,被捕获的
抗体称为固化配体,再将人ngf作为分析物进样,得到结合-解离曲线,用6m盐酸胍再生缓冲液洗脱后重复下一个循环;利用biacore 8k evaluation software对数据进行分析。结果如表1所示。
106.表1.检测抗ngf抗体与人ngf之间的结合和解离动力学参数
107.抗体名称kon(1/ms)koff(1/s)kd(m)e3-igg18.76e+051.64e-041.87e-10183-chimeric1.51e+073.57e-052.37e-12183-humanized1.55e+073.71e-052.39e-12
108.注:kon表示结合常数;koff表示解离常数;kd=koff/kon,表示平衡解离常数。
109.实验结果显示,e3-igg1、183c6-chimeric和183c6-humanized均能够有效结合人ngf,但183c6-chimeric和183c6-humanized结合ngf的速率(kon)明显快于e3-igg1,并且解离速率明显慢于e3-igg1,因此183c6-chimeric和183c6-humanized的平衡解离常数明显小于e3-igg1,这表明183c6-chimeric和183c6-humanized的亲和力明显高于e3-igg1。
110.实施例6 183c6-chimeric和183c6-humanized中和ngf生物活性的能力
111.tf-1细胞用含10%胎牛血清的rpmi-1640培养基在37℃、5%co2孵箱中培养,培养基中需要添加5ng/ml的gm-csf;具体培养和传代方法参照https://www.atcc.org/products/all/crl-2003.aspx。人ngf能够诱导tf-1细胞增殖,本实施例采用tf-1细胞检测上述抗ngf单抗对ngf诱导tf-1细胞增殖的抑制作用。
112.用37℃预热的rpmi-1640培养基将处于对数生长期的tf-1细胞洗涤2遍,每次300g离心5min;对tf-1细胞计数,用含10%胎牛血清的rpmi-1640培养基悬浮到适当密度,接种到96孔细胞培养板中,10000个/150μl/孔;在rpmi-1640完全培养基中加入人ngf使其浓度达到80ng/ml;用添加人ngf的培养基将上述抗体稀释到适当浓度,按照适当倍率连续稀释9个梯度;将稀释过的抗原和抗体混合物加入96孔细胞培养板中,50μl/孔;96孔板周围添加蒸馏水,200μl/孔;在37℃、5%co2孵箱中孵育3天;3天后在96孔板中每孔加入20μl cck-8溶液,在孵箱中继续培养8h;震荡混匀后用酶标仪读取od450值;graphpad prism6进行数据分析,作图并计算ic
50
。
113.图3a和图3b是两次独立重复实验的结果。图3a和图3b显示,e3-igg1、183c6-chimeric和183c6-humanized均能够有效抑制ngf诱导tf-1细胞增殖,图3a中它们的ic
50
分别为0.145nm、0.1623nm和0.1373nm;图3b中它们的ic
50
分别为0.1162nm、0.1273nm和0.1104nm,它们中和ngf生物活性的能力基本相当。其中同型对照抗体为不结合ngf的人igg1单抗。
114.实施例7 183c6-humanized的种属交叉能力
115.用elisa方法检测上述抗人ngf单抗对其它种属ngf的识别能力。实验方法参见实施例2步骤1。不同之处在于,此处使用的是hrp标记的羊抗人二抗。
116.结果如图4所示,183c6-humanized均能够有效结合小鼠和大鼠的ngf,它们的ec
50
分别是0.2041nm和0.5310nm。其中同型对照抗体为不结合ngf的人igg1单抗。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1