共轭聚合物及其制备方法、给体受体材料和光电器件与流程
本发明涉及一种共轭聚合物及其制备方法、给体受体材料和光电器件。
背景技术:
随着全球能源需求的日益增加,如何高效利用取之不尽、用之不竭的太阳能资源无疑是解决人类能源危机的重要途径之一。太阳能电池是将太阳能转换为电能的装置,被认为是最有效和最直接的太阳能利用形式。有机活性材料具有质量轻、价格低、加工性能佳、化合物结构可设计性好、制作的器件柔性好,便于生产大面积实用性等优点,所以有机太阳能电池的研究对于大规模推广和运用太阳能电池,为人类提供价格低廉的电能具有重大意义。迄今为止,经过对分子结构、器件结构和加工工艺的优化,基于窄带隙聚合物给体或小分子给体与富勒烯受体共混制备的太阳能电池的光电转化效率已突破10%,这显示出窄带隙有机太阳能电池的巨大应用前景。
富勒烯及其衍生物作为受体材料虽然有它独特的优势,但是富勒烯类受体材料也存在一些缺点,例如它们在可见光内吸光系数低、制备和提纯困难、成本较高、由于能级结构难于调节器件的开路电压受到限制等,一定程度上限制了有机太阳能电池效率的进一步提高。商业化的聚合物受体ν2200使用最为广泛、性能也最好,基于此材料的太阳能电池已实现了9.16%的能量转换效率。然而由于聚合物受体n2200具有较低的摩尔吸光系数,导致制备的全聚合物电池器件中长波长方向光响应较弱,致使短路电流较低,成为其效率进一步提升的瓶颈。全聚合物太阳能电池的进一步发展需要开发具有高摩尔吸光系数的性能优良的n-型聚合物受体。
目前以多元稠环共轭单元为核,末端连接吸电子单元的a-d-a型芳香稠环受体已实现了超过16%的能量转换效率。由于其平面性好,分子堆积较有序,并且可以通过调整不同的核及拉电子单元来调整其能级和吸收,因此备受科学界关注。此类a-d-a型分子最大的优点是其吸收能够在红外和远红外区域有效调控,通常为窄带隙n-型受体材料。尽管此类小分子材料能量转换效率最为优异,但这类材料的成膜性较差、对热敏感。
技术实现要素:
基于此,有必要提供一种摩尔吸光系数较高、成膜性好且热稳定高的共轭聚合物。
一种共轭聚合物,所述共轭聚合物的结构如式i所示:
所述共聚单元1为a-d-a型分子单元,所述共聚单元2为共轭芳环基团,n为4~100之间的整数;
所述a-d-a型分子单元中,基团d选自具有下述结构的基团中的一种:
所述式iii-1和所述式iii-2中的r1、r2、r3和r4均分别独立地选自h、碳原子数为1~60的直链烷基、碳原子数为3~60的支链烷基、碳原子数为1~60的直链烷氧基、碳原子数为3~60的支链烷氧基和烷基取代的芳基中的一种,所述烷基取代的芳基中的烷基为碳原子数为1~60的直链烷基或碳原子数为3~60的支链烷基,所述烷基取代的芳基中的芳基为苯环或者噻吩环,所述式iii-i和所述式iii-2中的虚线均表示基团d与基团a的连接位点;
所述a-d-a型分子单元中,基团a选自具有如下结构的基团中的一种:
所述式iv-1至所述式iv-3中所示的虚线中:①表示基团a与基团d的连接位点,②表示基团a与所述共聚单元2的连接位点。
在其中一个实施例中,所述共聚单元2选自具有如下结构的基团中的一种:
其中,所述式v-1至所述式v-8中的r5分别独立的选自h、f、碳原子数为1~60的直链烷基、碳原子数为3~60的支链烷基、碳原子数为1~60的直链烷氧基、碳原子数为3~60的支链烷氧基和烷基取代的芳基中的一种,所述烷基取代的芳基中的烷基为碳原子数为1~60的直链烷基或碳原子数为3~60的支链烷基,所述烷基取代的芳基中的芳基为苯环或者噻吩环,式v-1至式v-8中的虚线表示所述共聚单元2与所述共聚单元1的连接位点。
在其中一个实施例中,所述共聚单元1选自具有如下结构的基团中的一种:
在其中一个实施例中,所述共轭聚合物的选自如下结构中的一种:
所述式vii-1和vii-2中,r1、r2、r3和r4分别独立选自碳原子数为1~60的直链烷基和碳原子数为3~60的支链烷基中的一种。
在其中一个实施例中,所述共聚单元2选自
一种共轭聚合物的制备方法,包括以下步骤:
在惰性气体保护下,如式viii所示的化合物与如式ⅸ所示的化合物在催化剂的作用下进行共聚反应,得到如式i所示的共轭聚合物,
所述如式viii所示的化合物为:
所述如式ⅸ所示的化合物为:
所述如式viii所示的化合物中,基团d选自具有如下结构的基团中的一种:
所述式iii-1和所述式iii-2中的r1、r2、r3和r4均分别独立地选自h、碳原子数为1~60的直链烷基、碳原子数为3~60的支链烷基、碳原子数为1~60的直链烷氧基、碳原子数为3~60的支链烷氧基和烷基取代的芳基中的一种,所述烷基取代的芳基中的烷基为碳原子数为1~60的直链烷基或碳原子数为3~60的支链烷基,所述烷基取代的芳基中的芳基为苯环或者噻吩环,所述式iii-i和所述式iii-2中的虚线均表示基团d与基团a的连接位点;
所述如式viii所示的化合物中,基团a选自具有如下结构的基团中的一种:
所述式iv-1至所述式iv-3中所示的虚线中:①表示基团a与基团d的连接位点,②表示基团a与所述共聚单元2的连接位点;
x为卤素;
所述如式ⅸ所示的化合物中,所述ar为共轭芳环基团,所述y为硼酸基团、硼酸酯基团或三烷基锡基团。
在其中一个实施例中,所述y为硼酸基团或硼酸酯基团,采用suzuki法制备所述如式i所示的共轭聚合物,所述suzuki法中:溶剂为四氢呋喃、甲苯、或甲苯与水的混合物,催化剂为四(三苯基膦)钯或三(二亚苄基丙酮)二钯,所述催化剂的加入量为所述如式viii所示的化合物与所述如ⅸ所示的化合物的总摩尔量的0.01%~20%;及/或,所述如式viii所示的化合物与所述如式ⅸ所示的化合物的摩尔比为1:0.8~5;及/或,所述共聚反应的温度为30℃~150℃。
在其中一个实施例中,所述y为三烷基锡基团,采用stille法制备所述如式i所示的共轭聚合物,所述stille法中:溶剂为四氢呋喃、甲苯和氯苯中至少一种,催化剂为四(三苯基膦)钯、三(二亚苄基丙酮)二钯、氯化钯或醋酸钯,所述催化剂的加入量为所述如式viii所示的化合物与所述如式ⅸ所示的化合物的总摩尔量的0.01%~20%;及/或,所述如式viii所示的化合物与所述如式ⅸ所示的化合物的摩尔比为1:0.8~5;及/或,反应温度为30℃~150℃。
一种给体受体材料,所述给体受体材料包括上述的共轭聚合物或上述的共轭聚合物的制备方法制得的共轭聚合物,及至少另一种有机功能材料,所述另一种有机功能材料为p-型电子给体聚合物,所述p-型电子给体聚合物为pbdb-t或pbdb-tf,所述共轭聚合物与p-型电子给体聚合物的摩尔比为1:(0.1~10)。
一种光电器件,所述光电器件为太阳能电池,所述太阳能电池中的活性层包含上述的共轭聚合物、或上述的共轭聚合物的制备方法制得的共轭聚合物,或上述的给体受体材料。
附图说明
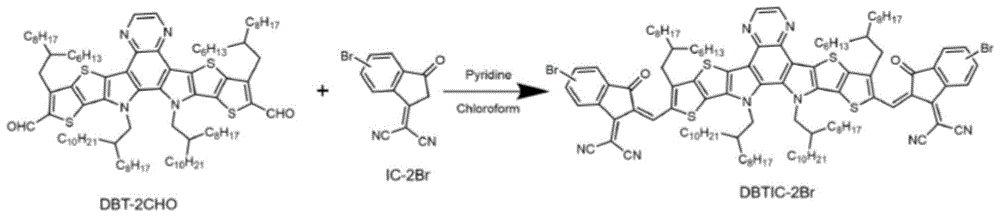
图1为实施例1制备dbtic-2br的反应方程式;
图2为实施例2制备dbtmic-2br的反应方程式;
图3为实施例3制备dbthic-2br的反应方程式;
图4为实施例4制备btic-2br的反应方程式;
图5为实施例5制备btmic-2br的反应方程式;
图6为实施例6制备dbobic-2br的反应方程式;
图7为实施例7制备p1的反应方程式;
图8为实施例8制备p2的反应方程式;
图9为实施例9制备p3的反应方程式;
图10为实施例10制备p4的反应方程式;
图11为实施例11制备p5的反应方程式;
图12为实施例12制备p6的反应方程式。
具体实施方式
为了便于理解本发明,下面将参照相关附图对本发明进行更全面的描述。附图中给出了本发明的部分实施例。但是,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施例。相反地,提供这些实施例的目的是使本发明公开内容更加透彻全面。
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。
本发明一实施方式提供一种共轭聚合物,该共轭聚合物的结构如式i所示:
具体地,在式i中,共聚单元1为a-d-a型分子单元,共聚单元2为共轭芳环基团,n为4~100之间的整数。n代表共轭聚合物的重复单元个数。n为5~100的整数。
具体地,a-d-a型分子单元的结构如式ii所示:
在式ii中,基团d选自具有下述结构的基团中的一种:
式iii-1和式iii-2中的r1、r2、r3和r4均分别独立地选自h、碳原子数为1~60的直链烷基、碳原子数为3~60的支链烷基、碳原子数为1~60的直链烷氧基、碳原子数为3~60的支链烷氧基和烷基取代的芳基中的一种;烷基取代的芳基中的烷基为碳原子数为1~60的直链烷基或碳原子数为3~60的支链烷基,烷基取代的芳基中的芳基为苯环或者噻吩环。式iii-i和式iii-2中的虚线均表示基团d与基团a的连接位点。
在其中一个实施例中,式iii-1和式iii-2中的r1、r2、r3和r4均分别独立地选自h、碳原子数为1~60的直链烷基和碳原子数为3~60的支链烷基中的一种。
具体地,在式ii中,基团a选自具有如下结构的基团中的一种:
式iv-1至式iv-3中所示的虚线中:①表示基团a与基团d的连接位点,②表示基团a与共聚单元2的连接位点。
具体地,共聚单元2选自具有如下结构的基团中的一种:
式v-1至式v-8中的r5分别独立的选自h、f、碳原子数为1~60的直链烷基、碳原子数为3~60的支链烷基、碳原子数为1~60的直链烷氧基、碳原子数为3~60的支链烷氧基和烷基取代的芳基中的一种,烷基取代的芳基中的烷基为碳原子数为1~60的直链烷基或碳原子数为3~60的支链烷基,烷基取代的芳基中的芳基为苯环或者噻吩环。
进一步地,共聚单元1选自具有如下结构的基团中的一种:
在其中一个实施例中,共轭聚合物的选自如下结构中的一种:
式vii-1和vii-2中,r1、r2、r3和r4分别独立选自碳原子数为1~60的直链烷基和碳原子数为3~60的支链烷基中的一种。进一步地,共聚单元2选自
上述共轭聚合物具有较高的摩尔吸光系数、良好的成膜性能和热稳定性,同时具有优良的电荷传输性能以及合适的能级,能够作为代替富勒烯及其衍生物的窄带隙聚合物受体与p-型电子给体材料匹配,应用于光电器件中。
本发明还提供一种共轭聚合物的制备方法,该制备方法包括以下步骤:
在惰性气体保护下,如式viii所示的化合物与如式ⅸ所示的化合物在催化剂的作用下进行共聚反应,得到如式i所示的共轭聚合物。
具体地,惰性气体为氮气或氩气。
具体地,如式viii所示的化合物为:
如式viii所示的化合物中,基团d选自具有如下结构的基团中的一种:
式iii-1和式iii-2中的r1、r2、r3和r4均分别独立地选自h、碳原子数为1~60的直链烷基、碳原子数为3~60的支链烷基、碳原子数为1~60的直链烷氧基、碳原子数为3~60的支链烷氧基和烷基取代的芳基中的一种,烷基取代的芳基中的烷基为碳原子数为1~60的直链烷基或碳原子数为3~60的支链烷基,烷基取代的芳基中的芳基为苯环或者噻吩环,式iii-i和式iii-2中的虚线均表示基团d与基团a的连接位点;
如式viii所示的化合物中,基团a选自具有如下结构的基团中的一种:
式iv-1至式iv-3中所示的虚线中:①表示基团a与基团d的连接位点,②表示基团a与共聚单元2的连接位点。
x为卤素。进一步地,x为br或i。
具体地,如式ⅸ所示的化合物为:
进一步地,ar选自具有如下结构的基团中的一种:
其中,式v-1至式v-8中的r5分别独立的选自h、f、碳原子数为1~60的直链烷基、碳原子数为3~60的支链烷基、碳原子数为1~60的直链烷氧基、碳原子数为3~60的支链烷氧基和烷基取代的芳基中的一种,烷基取代的芳基中的烷基为碳原子数为1~60的直链烷基或碳原子数为3~60的支链烷基,烷基取代的芳基中的芳基为苯环或者噻吩环,式v-1至式v-8中的虚线表示共聚单元2与共聚单元1的连接位点。
在其中一个实施例中,y为硼酸基团或硼酸酯基团,采用suzuki法制备如式i所示的共轭聚合物。具体地,suzuki法中:溶剂为四氢呋喃、甲苯、或甲苯和水的混合物,催化剂为四(三苯基膦)钯或三(二亚苄基丙酮)二钯。进一步地,催化剂的加入量为如式viii所示的化合物与如ⅸ所示的化合物的总摩尔量的0.01%~20%。如式viii所示的化合物与如式ⅸ所示的化合物的摩尔比为1:0.8~1.5。共聚反应的温度为30℃~150℃;反应时间为6小时~120小时。
在其中一个实施例中,y为三烷基锡基团,采用stille法制备如式i所示的共轭聚合物。具体地,suzuki法中:溶剂为四氢呋喃、甲苯和氯苯中至少一种,催化剂为四(三苯基膦)钯、三(二亚苄基丙酮)二钯、氯化钯或醋酸钯。进一步地,催化剂的加入量为如式viii所示的化合物与如式ⅸ所示的化合物的总摩尔量的0.01%~20%。如式viii所示的化合物与如式ⅸ所示的化合物的摩尔比为1:0.8~1.5。共聚反应的温度为30℃~150℃;反应时间为6小时~120小时。如式i所示的共轭聚合物为:
上述共轭聚合物的制备方法,将多元稠环结构引入到共轭聚合物的主链中,即通过在稠环受体末端引入官能团,并与其它共轭单体共聚,从而保持原有稠环受体结构与性能上的优势,同时通过共聚单元调控其光电性能并发挥聚合物成膜性好的优势,构筑性能更为优良的n-型聚合物类受体。上述共轭聚合物的制备方法简捷,制备的目标产物溶解性好,吸光度强,吸收范围宽,对太阳光有较高的利用率,且具有较好的电荷传输性能以及合适的电子能级,能够作为电子受体材料与给体材料匹配,在光电器件中得到应用。
上述共轭聚合物或上述共轭聚合物的制备方法制得的共轭聚合物在制备光电器件中的应用。进一步地,光电器件为薄膜半导体器件、光探测器件或聚合物太阳能电池器件。更进一步地,聚合物太阳能电池器件为全聚合物太阳能电池器件。
本发明一实施方式还提供一种给体受体材料,该给体受体材料包括上述共轭聚合物或上述共轭聚合物的制备方法制得的共轭聚合物,及至少另一种有机功能材料。进一步地,另一种有机功能材料为p-型电子给体聚合物。
在其中一个实施例中,共轭聚合物与p-型电子给体聚合物的摩尔比为1:0.1~10。
在其中一个实施例中,p-型电子给体聚合物为中间带隙聚合物或者宽带隙聚合物。优选地,p-型电子给体聚合物为pbdb-t或pbdb-tf(简称pm6)。
上述给体受体材料包括上述共轭聚合物、或上述共轭聚合物的制备方法制得的共轭聚合物,具有上述共轭聚合物对应的优良性能。
本发明一实施方式还提供一种组合物,该组合物包括上述共轭聚合物、或上述共轭聚合物的制备方法制得的共轭聚合物、或上述的给体受体材料,及至少一种有机溶剂。
具体地,有机溶剂选自甲苯、二甲苯、三甲苯、氯仿、氯苯、二氯苯和三氯苯中至少一种。进一步地,上述组合物中的共轭聚合物的浓度为0.5mg/ml~50mg/ml。优选地,上述组合物中的共轭聚合物的浓度为4mg/ml~20mg/ml。上述组合物中的p-型电子给体聚合物的浓度为0.5mg/ml~50mg/ml。上述组合物中的p-型电子给体聚合物的浓度为3mg/ml~20mg/ml。
上述组合物包括上述共轭聚合物或上述共轭聚合物的制备方法制得的共轭聚合物,具有上述共轭聚合物对应的优良性能。
本发明一实施方式还提供一种光电器件,该光电器件包括上述共轭聚合物、或上述共轭聚合物的制备方法制得的共轭聚合物、或上述给体受体材料。进一步地,光电器件为太阳能电池,太阳能电池中的活性层包括上述共轭聚合物、或上述共轭聚合物的制备方法制得的共轭聚合物、或上述给体受体材料。
上述光电器件包括上述共轭聚合物,具有上述共轭聚合物对应的优良性能。
具体实施例
以下结合具体实施例进行详细说明。实施例中采用药物和仪器如非特别说明,均为本领域常规选择。实施例中未注明具体条件的实验方法,按照常规条件,例如文献、书本中的条件或者生产厂家推荐的方法实现。
实施例1、制备dbtic-2br
制备dbtic-2br的反应方程式如图1所示,dbt-2cho、ic-br和dbtic-2br的结构式如下:
具体反应步骤和反应条件如下:
在氮气保护下,将dbt-2cho(1.50g,1mmol)和ic-br(0.86g,3mmol)加入到反应瓶中,然后加入100ml干燥的氯仿溶解。用氩气排空气5分钟,再加入吡啶1毫升,然后70℃反应10小时后停止。将反应液浓缩后沉析到甲醇(300ml)中,沉析出的固体过滤,用甲醇冲洗,真空干燥后得到dbtic-2br化合物1.3克,产率为65%,ms(maldi-tof):m/z2007.57(m+)。
实施例2、制备dbtmic-2br
制备dbtmic-2br的反应方程式如图2所示。dbtm-2cho、ic-br和dbtmic-2br的结构式如下:
具体反应步骤和反应条件如下:
在氮气保护下,将dbtm-2cho(1.512g,1mmol)和ic-br(0.86g,3mmol)加入到反应瓶中,然后加入100ml干燥的氯仿溶解。用氩气排空气5分钟,再加入吡啶1毫升,然后70℃反应10小时后停止。将反应液浓缩后沉析到甲醇(300ml)中,沉析出的固体过滤,用甲醇冲洗,真空干燥后得到dbtmic-2br化合物1.6克,产率为71%,ms(maldi-tof):m/z2021.54(m+)。
实施例3、制备dbthic-2br
制备dbthic-2br的反应方程式如图3所示。dbth-2cho、ic-br和dbthic-2br的结构式如下:
具体反应步骤和反应条件如下:
在氮气保护下,将dbth-2cho(1.6g,1mmol)和ic-br(0.86g,3mmol)加入到反应瓶中,然后加入100ml干燥的氯仿溶解。用氩气排空气5分钟,再加入吡啶1毫升,然后70℃反应10小时后停止。将反应液浓缩后沉析到甲醇(300ml)中,沉析出的固体过滤,用甲醇冲洗,真空干燥后得到dbthic-2br化合物1.6克,产率为68%,ms(maldi-tof):m/z2105.82(m+)。
实施例4、制备btic-2br
制备btic-2br的反应方程式如图4所示,bt-2cho、ic-br和btic-2br的结构式如下:
具体反应步骤和反应条件如下:
在氮气保护下,将bt-2cho(1.385g,1mmol)和ic-br(0.86g,3mmol)加入到反应瓶中,然后加入100ml干燥的氯仿溶解。用氩气排空气5分钟,再加入吡啶1毫升,然后70℃反应10小时后停止。将反应液浓缩后沉析到甲醇(300ml)中,沉析出的固体过滤,用甲醇冲洗,真空干燥后得到btic-2br化合物1.2克,产率为63%,ms(maldi-tof):m/z1895.44(m+)。
实施例5、制备btmic-2br
制备btmic-2br的反应方程式如图5所示,btm-2cho、ic-br和btmic-2br的结构式如下:
具体反应步骤和反应条件如下:
在氮气保护下,将btm-2cho(1.4g,1mmol)和ic-br(0.86g,3mmol)加入到反应瓶中,然后加入100ml干燥的氯仿溶解。用氩气排空气5分钟,再加入吡啶1毫升,然后70℃反应10小时后停止。将反应液浓缩后沉析到甲醇(300ml)中,沉析出的固体过滤,用甲醇冲洗,真空干燥后得到btmic-2br化合物1.3克,产率为67%,ms(maldi-tof):m/z1909.66(m+)。
实施例6、制备btobic-2br
制备btobic-2br的反应方程式如图6所示,btob-2cho、ic-br和btobic-2br的结构式如下:
具体反应步骤和反应条件如下:
在氮气保护下,将btob-2cho(1.5g,1mmol)和ic-br(0.86g,3mmol)加入到反应瓶中,然后加入100ml干燥的氯仿溶解。用氩气排空气5分钟,再加入吡啶1毫升,然后70℃反应10小时后停止。将反应液浓缩后沉析到甲醇(300ml)中,沉析出的固体过滤,用甲醇冲洗,真空干燥后得到btobic-2br化合物1.3克,产率为64%,ms(maldi-tof):m/z1791.13(m+)。
实施例7、制备p1
制备p1的反应方程式如图7所示,m1和p1的结构式如下:
具体反应步骤和反应条件如下:
将ml和实施例1制备得到的单体dbtic-2br各取0.03mmol,溶于甲苯(15ml)和dmf(4ml)的混合溶剂后,氮气排空气30分钟后,加入催化剂四(三苯基膦)钯(0)(20mg)在110℃下聚合48小时后停止。将聚合物溶液冷却至室温,沉析到甲醇(200ml)中,沉析出的聚合物通过索式提取从氯仿中得到聚合物pl,产率为78%,gpc:mn=12.12kda,mw=25.14kda。
实施例8、制备p2
制备p2的反应方程式如图8所示。m2和p2的结构式如下:
具体反应步骤和反应条件如下:
将m2和实施例2制得的单体dbtmic-2br各取0.03mmol,溶于甲苯(15ml)和dmf(4ml)的混合溶剂后,氮气排空气30分钟后,加入催化剂四(三苯基膦)钯(0)(20mg)在110℃下聚合48小时后停止。将聚合物溶液冷却至室温,沉析到甲醇(200ml)中,沉析出的聚合物通过索式提取从氯仿中得到聚合物p2,产率为86%,gpc:mn=15.76kda,mw=37.24kda。
实施例9、制备p3
制备p3的反应方程式如图9所示。m3和p3的结构式如下:
具体反应步骤和反应条件如下:
将m3和实施例3制备的单体dbthic-2br各取0.03mmol,溶于甲苯(15ml)和dmf(4ml)的混合溶剂后,氮气排空气30分钟后,加入催化剂四(三苯基膦)钯(0)(20mg)在110℃下聚合48小时后停止。将聚合物溶液冷却至室温,沉析到甲醇(200ml)中,沉析出的聚合物通过索式提取从氯仿中得到聚合物p3,产率为81%,gpc:mn=14.71kda,mw=27.94kda
实施例10、制备p4
制备p4的反应方程式如图10所示。m1和p4的结构式如下:
具体反应步骤和反应条件如下:
将m1和实施例4制备的单体btic-2br各取0.03mmol,溶于甲苯(15ml)和dmf(4ml)的混合溶剂后,氮气排空气30分钟后,加入催化剂四(三苯基膦)钯(0)(20mg)在110℃下聚合48小时后停止。将聚合物溶液冷却至室温,沉析到甲醇(200ml)中,沉析出的聚合物通过索式提取从氯仿中得到聚合物p4,产率为86%,gpc:mn=35.77kda,mw=79.91kda。
实施例11、制备p5
制备p5的反应方程式如图11所示。m2和p5的结构式如下:
具体反应步骤和反应条件如下:
将m2和实施例5制备的单体btmic-2br各取0.03mmol,溶于甲苯(15ml)和dmf(4ml)的混合溶剂后,氮气排空气30分钟后,加入催化剂四(三苯基膦)钯(0)(20mg)在110℃下聚合48小时后停止。将聚合物溶液冷却至室温,沉析到甲醇(200ml)中,沉析出的聚合物通过索式提取从氯仿中得到聚合物p5,产率为86%,gpc:mn=42.74kda,mw=90.32kda。
实施例12、制备p6
制备p6的反应方程式如图12所示。m3和p6的结构式如下:
具体反应步骤和反应条件如下:
将m3和实施例6制备的单体btobic-2br各取0.03mmol,溶于甲苯(15ml)和dmf(4ml)的混合溶剂后,氮气排空气30分钟后,加入催化剂四(三苯基膦)钯(0)(20mg)在110℃下聚合48小时后停止。将聚合物溶液冷却至室温,沉析到甲醇(200ml)中,沉析出的聚合物通过索式提取从氯仿中得到聚合物p6,产率为88%,gpc:mn=57.14kda,mw=112.32kda。
测试
将实施例7~12合成的聚合物p1~p6作为电子受体用于有机太阳电池器件中(阳极/空穴传输层/活性层/电子传输层/阴极),阳极的材料为银,空穴传输层的材料为三氧化钼,电子传输层的材料为氧化锌,阴极的材料为ito导电玻璃。
聚合物p1~p6对应的有机太阳电池器件的制备方法如下:
依次用肥皂水、去离子水、丙酮、正己烷和异丙醇(每个清洗过程20分钟)
超声清洗ito玻璃基底。随后在真空干燥箱内80℃干燥1小时。接着紫外-臭氧(uv-ozone)处理30分钟。随之将氧化锌前驱体溶液(0.5m无水醋酸锌溶于乙醇胺和2-甲氧基乙醇)以4500转40秒旋涂于ito玻璃基底上,空气中200℃退火30分钟。接着,转移ito玻璃片到充满氮气的手套箱内,旋涂活性层:活性层溶解于氯苯溶剂中,浓度为:电子给体10mg/ml,电子受体15mg/ml,同时添加不同含量的cn。接着在手套箱内80℃退火5分钟。在高真空条件下(1×10-5pa),依次蒸镀氧化钼(moo3)10nm和银电极(ag)100nm。
器件性能测试:
在oriel91192型am1.5g太阳光模拟灯的照射下进行,辐射度为1kw/m2,使用keithley2400型数字源表测试j-v曲线。
按照上述方法测试的聚合物p1~p6对应的有机太阳电池器件的性能如下表1所示,器件结构:ito/zno/pm6:acceptor/moo3/ag,“/”表示层叠。
表1
由表1可看出,聚合物p1~p6作为电子受体材料,在保证较高的开路电压前提下,能够极大地提升电池器件的短路电流,同时获得较高的填充因子,基于p3与pm6匹配的电池器件效率最高可达13.73%。
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!