检测抗双链DNA抗体的试剂盒、组合物及用途的制作方法
本发明涉及抗双链dna抗体的检测,尤其涉及基于化学发光的双链dna抗体的检测。
背景技术:
抗双链dna抗体是识别天然的双链dna的抗体。一方面,抗双链dna抗体可用作系统性红斑狼疮(sle)高度特异性抗体,其在活动期sle中阳性率较高,而在非活动期sle中阳性率较低。但需注意,抗双链dna抗体检测阴性时并不一定可以排除sle,需结合其他指标进行综合评估。另一方面,据报道双链dna抗体也与干燥综合征、药物性狼疮、混合性结缔组织病、肾脏损害、血管炎等有一定关联。抗双链dna抗体的检测结果应结合临床分析,必要时应动态观察。
目前,抗双链dna抗体检测方法包括间接免疫荧光法、印迹法、酶联免疫吸附法、化学发光免疫分析法等。间接免疫荧光法、印迹法、酶联免疫吸附法存在操作繁琐、耗时长的缺点,且对操作者有一定的专业技能要求。化学发光免疫分析法可配合全自动分析仪,具有操作简便、高通量的特性,正在越来越得到广泛使用。根据标记物的不同,化学发光免疫分析法通常分为酶促化学发光和直接化学发光,后者通常采用吖啶类化学发光物质作为标记物。
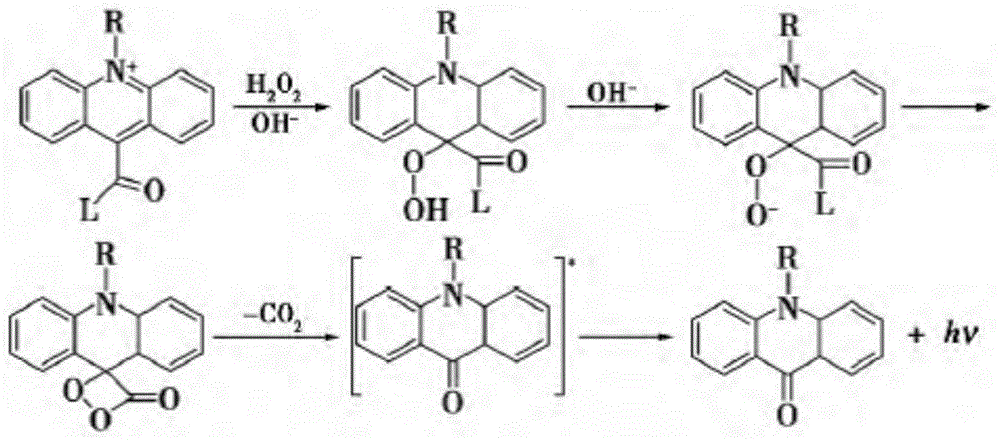
吖啶类标记物是一类量子产率非常高的化学发光试剂,其具有无须催化剂即可发光、灵敏度高、线性范围范宽等优势。吖啶类标记物的分子结构至少由两部分组成:发光基团(emitter)和离去基团(leavinggroup)),它们的结构中都有共同的吖啶环。吖啶类化学发光反应机理的研究已经比较成熟,常规的反应机理是在碱性条件下,过氧化氢与吖啶类标记物的9位碳原子发生加成,加成产物在碱性条件下形成的过氧负离子再亲核进攻羰基碳,离去基团离去并进一步形成不稳定的四元环中间体,开环后形成激发态的吖啶酮,其返回到基态的过程中释放出光子。
尽管如此,在基于直接化学发光法对抗双链dna抗体进行免疫检测的情况下,由于反应体系中存在双链dna,而吖啶类化学发光标记物具有三元芳香环的平面结构,可通过π-π共轭作用插入到双链dna的双螺旋结构之间。在检测过程中,吖啶类化学发光标记物可能出现不可控地与反应体系中的(如固相载体上的)双链dna嵌合,从而影响后续发光过程。由于该结合过程随机且不可控,导致对整个反应过程的影响没有规律性,最终表现为cv值偏大,即检测结果精密度低。
由于吖啶类化学发光试剂检测双链dna抗体时存在精密度低的缺点,通常,在抗双链dna抗体的体外检测研发过程中会避免使用这一方法,转而采用其他发光物质如鲁米诺等,或采用其他检测技术如,酶联免疫吸附法、酶促化学发光法等。但如此一来,吖啶类化学发光法的发光效率高、操作简便、灵敏度高和线性范围宽等优势就无法得以利用。
因此,在抗双链dna抗体检测领域,存在着提高吖啶类化学发光法的检测精密度的强烈需求。
技术实现要素:
在整个说明书中,除非另有特别说明,本文使用的术语应理解为如本领域中通常所使用的含义。因此,除非另有定义,本文使用的所有技术和科学术语具有与本发明所属领域技术人员的一般理解相同的含义。若存在矛盾,本说明书优先。
如前所述,基于吖啶类化学发光标记物的直接化学发光法是一种高效、简便的分析方法,但当其应用于抗双链dna抗体检测的情形下,却存在发光标记物与反应体系中的双链dna不可控地嵌合的问题,由此导致检测精密度较低,难以符合体外检测试剂的要求。
有鉴于此,在第一方面,本发明提供了一种用于检测抗双链dna抗体的组合物,包括:
标记有吖啶类化学发光物质的第一组分;和
吖啶类非化学发光物质。
如下文实施例中所证实的,通过将吖啶类非化学发光物质与标记有吖啶类化学发光物质的第一组分联合用于抗双链dna抗体的免疫分析,样本重复检测后结果的相对变异系数(cv)得到了明显地改善。
在具体的实施方式中,在碱性条件下,本发明的吖啶类非化学发光物质的9号位不能与过氧化物(过氧化氢)形成四元环;或者,在碱性条件下,本发明的吖啶类非化学发光物质是在加入过氧化物(过氧化氢)后,其9号位不能形成四元环的吖啶类物质/吖啶衍生物;又或者,在碱性条件下,本发明的吖啶类非化学发光物质不能与过氧化物(过氧化氢)反应继而释放出足以实现化学发光免疫分析光子。
具体地,在本发明中,抗双链dna抗体的检测是基于化学发光免疫分析法。
在本文中,“吖啶类化学发光物质”与“吖啶类标记物”、“吖啶类化学发光标记物”、“吖啶类化学发光剂”和“吖啶类化学发光底物”可以互换使用,是指可用作化学发光标记的吖啶衍生物。再进一步是指在碱性条件下与过氧化物(过氧化氢)反应并能用于化学发光检测的物质。又进一步是指通过以下机理发光并因此能够用于化学发光检测的物质:在碱性条件下,过氧化物(如过氧化氢)与吖啶标记物的9位碳原子(c9)发生加成,加成产物在碱性条件下形成的过氧负离子再亲核进攻羰基碳,离去基团离去并进一步形成不稳定的四元环中间体,开环后形成激发态的吖啶酮,其返回到基态的过程中释放出光子。
示例性的吖啶类化学发光物质可以是吖啶酯和吖啶磺酰胺。
式a-i示出了吖啶酯的通式:
其中,r为烷基、烷氧基及芳基等其他取代基;x、x'为偶联基团。
式a-ii示出了吖啶磺酰胺的通式:
其中,r为烷基、烷氧基及芳基等其他取代基;x、x'、x”可为偶联基团。
图1以吖啶酯为例,示出了吖啶类化学发光物质在用于化学发光免疫分析时的反应机理。
另外,吖啶类化学发光物质还可以是双吖啶衍生物,如9,9'-双吖啶衍生物。双吖啶衍生物的例子可以是光泽精和dmba。
在涉及双吖啶衍生物的情况下,本发明中“9号位”、“9位碳原子”或“c9”,还可包括9'号位、9'位碳原子或c9'。
在本发明中,吖啶类化学发光物质标记于第一组分上,以用于与样本中的抗双链dna抗体(若存在)形成复合物,从而对后者进行检测。
例如,本发明的第一组分可以是抗人igg抗体和/或双链dna。其中,抗人igg抗体可选自由鼠抗人igg抗体、兔抗人igg抗体、山羊抗人igg抗体、绵羊抗人igg抗体和鸡抗人igg组成的组。
在本发明中,可以使用任何本领域技术人员熟知的方法将吖啶类化学发光物质标记在第一组分上。示例性的标记方法可以是:
1)取适量第一组分于适当容器中,用缓冲液稀释;
2)将吖啶类化学发光物质用二甲基亚砜稀释并混匀,随后立即加入到第一组分的溶液中并混匀,于避光条件下进行反应;
3)加入l-赖氨酸溶液以终止反应;
4)脱盐;以及
5)纯化。
如本发明所使用的,“吖啶类非化学发光物质”是指在碱性条件下,9号位不能与过氧化物(过氧化氢)形成四元环的吖啶衍生物。可以理解,由于9号位不能与过氧化物形成四元环,吖啶类非化学发光物质无法依据图1所示原理来释放出光子,从而无法作为化学发光标记物与第一组分连接来实现化学发光免疫分析。
在一些实施方式中,吖啶类非化学发光物质选自由9-氨基吖啶、9-甲基吖啶、3,6-二氨基吖啶、吖啶酮、2-氨基吖啶酮和吖啶母体组成的组。
示例性的吖啶类非化学发光物质的结构如下所示:
9-氨基吖啶:
9-甲基吖啶:
3,6-二氨基吖啶:
吖啶酮:
2-氨基吖啶酮:
吖啶母体:
不希望受到理论的束缚,本发明的吖啶类非化学发光物质与吖啶类化学发光物质结构类似,均可与双链dna嵌合,但前者不会发光,从而起到了阻断吖啶类化学发光物质与双链dna嵌合的作用,避免了不规则发光现象。
在一些实施方式中,本发明的组合物可进一步包括其他用于检测抗双链dna抗体的成分,如包被在固相支持物上的第二组份和/或分析缓冲液等。
在本文中,“固相支持物”、“固体支持物”、“固相载体”和“固体载体”可以互换使用,其是指可以附着双链dna抗原的固体表面。对用于本发明的固相支持物没有特别的限制,商品化的固相支持物及任何可用于免疫检测的固相支持物均可用于本发明。示例性的固相支持物可以是磁微粒、酶标板、塑料板、塑料管、乳胶珠、琼脂糖珠、玻璃、硝酸纤维素膜、尼龙膜、二氧化硅板或微芯片,但本发明不限于此。
在一个具体的实施方式中,所述固相支持物为磁微粒。
本发明的第二组份例如是在免疫分析中用作抗原的双链dna。
本发明的组合物中第一组份和第二组份能与同一待检测的抗双链dna抗体形成复合体结构;例如,当第一组分为抗人抗体时,第二组分、抗双链dna抗体和第一组分可形成抗原+抗双链dna抗体+抗人抗体的复合体;又例如,当第一组分为双链dna抗原时,第二组分、抗双链dna抗体和第一组分可形成抗原+抗双链dna抗体+抗原的复合体。
本发明的第二组分可以经由本领域的常规技术(例如,偶联)包被在固相支持物上。
在第二方面,本发明提供了一种用于检测抗双链dna的试剂盒,包括:
第一试剂,包括包被有第二组分的固相支持物;和
第二试剂,包括标记有吖啶类化学发光物质的第一组分,
其特征在于,所述试剂盒进一步包括吖啶类非化学发光物质。
在具体的实施方式中,所述吖啶类非化学发光物质可存在于第二试剂中。
在本发明试剂盒的一个变型中,其包括:
第一试剂,包括包被有第二组分的固相支持物;
第二试剂,包括标记有吖啶类化学发光物质的第一组分;和
第三试剂,分析缓冲液,
其特征在于,所述试剂盒进一步包括吖啶类非化学发光物质。
在该变型的一些实施方式中,所述吖啶类非化学发光物质可存在于第二试剂中。
在该变型的另一些实施方式中,所述吖啶类非化学发光物质可存在于第三试剂中。
在该变型的又一些实施方式中,所述吖啶类非化学发光物质可存在于第二试剂和第三试剂中。
除非特殊说明,本发明中的用语“第一”、“第二”和“第三”等仅用于区分多个相似的要素,而不意在表示要素之间重要性或次序等方面的任何差异,也不限定物质特定种类。
本发明的吖啶类非化学发光物质可以约0.008至约1.20mg/l的浓度存在。
优选地,吖啶类非化学发光物质可以约0.016至约0.6mg/l的浓度存在。更优选地,吖啶类非化学发光物质可以约0.02至约0.50mg/l的浓度存在。例如,吖啶类非化学发光物质可以约0.01mg/l、约0.02mg/l、约0.05mg/l、约0.10mg/l、约0.20mg/l、约0.50mg/l、约0.75mg/l或约1.00mg/l的浓度存在。在一个示例性的实施方式中,吖啶类非化学发光物质可以约0.10mg/l存在于本发明的第二试剂中。
通过选择吖啶类非化学发光物质的浓度,本发明的组合物和试剂盒进一步优化了样本重复检测后结果的cv的改善效果,例如,平均cv可控制在3%左右。
本领域技术人员能够理解,除第一试剂、第二试剂和第三试剂外,本发明的试剂盒还可以包括稀释液、清洗缓冲液、质控品和/或校准品等。
在具体的实施方式中,所述固相支持物为磁微粒。
在优选的实施方式中,吖啶类非化学发光物质选自由式b-i至b-vi所示化合物所组成的组。
分析缓冲液旨在为免疫分析提供适宜的环境。对于分析缓冲液的种类,本发明没有特别的限制,任何可用于抗体双链dna抗体免疫分析的分析缓冲液均可用于本发明。示例性的分析缓冲液可包括缓冲基质(如磷酸盐缓冲液、tris缓冲液、mes等)、无机盐(如nacl等)、蛋白质(如bsa、酪蛋白等)、糖类(如蔗糖、海藻糖等)及防腐剂(如pc950、叠氮钠等),但本发明不限于此。
具体地,本发明的试剂盒是基于化学发光免疫分析法的试剂盒。
在第三方面,本发明提供了本发明的组合物或试剂盒用于检测抗双链dna抗体的用途。
在示例性的实施方式中,在存在第三试剂的情况下,抗双链dna抗体的检测步骤可包括
1)将样本、第一试剂和第三试剂混合并反应一段时间;
2)加入第二试剂并反应一段时间;
3)加入过氧化氢,进行发光反应;以及
4)测量发光值,根据发光值相与中抗双链dna抗体的浓度的比例关系得到样本中抗双链dna抗体的浓度。
附图说明
图1示出了示例性的吖啶类化学发光物质的发光机理,其中r为取代基,l为离去基团。
具体实施方式
下文将结合具体实施方式和实施例,具体阐述本发明,本发明的优点和各种效果将由此更加清楚地呈现。本领域技术人员应理解,这些具体实施方式和实施例是用于说明本发明,而非限制本发明。
实施例1反应试剂的制备
r1:
1.取双链dna抗原(购自四川迈克生物新材料技术有限公司,下文简写为四川新材料),加入到磁微粒(购自四川新材料)中混匀按照双链dna与磁微粒比例为1~10ug/mg添加,置于滚轴混匀仪上室温混匀反应2小时;
2.反应完成后,将包被好双链dna的磁微粒置于磁分离器上2min;带液体澄清后弃上清,加入缓冲液重悬磁微粒,室温下采用滚轴混匀仪混匀反应0.5小时;
3.取包被好的免疫磁微粒,置于磁分离器上静置,待液体澄清后,弃上清;在加入缓冲液重悬磁微粒,将磁微粒置于磁分离器上2min,小心抽走上清,重复用缓冲液洗涤磁珠3次;
4.待洗涤结束后,用缓冲液将磁微粒稀释至终浓度为0.2mg/ml。
r2:
1.取1mg鼠抗人igg单克隆抗体(购自四川新材料)于适当容器中,用pbs缓冲液(0.02m,ph7.30±0.20)稀释至0.5mg/ml;
2.将吖啶酯(购自四川新材料)用二甲基亚砜稀释至2.5mmol/l,混匀后取20μl立即加入鼠抗人igg单克隆抗体溶液中,立即涡旋混匀,在避光条件下,室温于血液混匀仪上反应1h;
3.加入10mg/ml的l-赖氨酸溶液50μl,立即涡旋混匀以终止反应,避光条件下,室温在血液混匀仪上反应10min;
4.取2支5ml脱盐柱,剪去下端封口,将其装入合适规格的离心管中,1000×g离心2min,弃离心液,再用2.5mlpbs缓冲液(0.02m,ph7.30±0.20)清洗3次,每次1000×g离心2min,弃离心液,将脱盐柱插入干净的离心管中;
5.纯化:平均加入标记好的鼠抗人igg单克隆抗体至2支脱盐柱中,1000×g离心2min,收集纯化后的标记物(离心管中)并测量体积,加等体积丙三醇,并计算浓度。
6.将标记好的鼠抗人igg单克隆抗体用缓冲液稀释至0.25μg/ml。
r3:
按照下表配置分析缓冲液,备用。
表1
实施例2检测方法
使用迈克生物i3000全自动化学发光仪进行下述检测;
1.将样本(10μl)与实施例1中的r3(100μl)、r1(50μl)混合,37℃下反应10min;
2.洗涤后加入r2(100μl),37℃下反应10min;
3.再次洗涤后加入过氧化氢溶液和碱溶液后发生化学发光反应,测量相对发光值(rlu)。
实施例3评估吖啶酮对改善变异系数的影响
按照实施例2中的方法,以临床诊断为系统性红斑狼疮患者血清中抗双链dna抗体为检测对象,考察同一样本重复检测后rlu的变异系数(cv)。
其中,对照组a中使用实施例1所制备的r1、r2和r3。实验组加入了吖啶酮,其余与对照组a相同。具体地,实验组a1的r2和r3中分别加入0.01mg/l的吖啶酮;实验组a2的r2和r3中分别加入0.02mg/l的吖啶酮;实验组a3的r2和r3中分别加入0.10mg/l的吖啶酮;实验组a4的r2和r3中分别加入0.50mg/l的吖啶酮;实验组a5的r2和r3中分别加入1.00mg/l的吖啶酮,其余与对照组相同。每个样本测定3次。
通过如下公式计算cv:
其中,sd为3次测定结果的标准差;
测定结果如下表2a至表2c所示。
表2a
表2b
表2c
由表2a至2c可知,对照组a的cv高达22.12%,难以满足抗双链dna抗体检测试剂的需要。在加入吖啶酮之后,检测结果得到明显改善,尤其是当吖啶酮浓度在0.02mg/l~0.50mg/l时,检测结果的cv最佳,单样本cv均在8%以内,平均cv均在3%左右。
实施例4评估其它吖啶类非化学发光物质对改善变异系数的影响
按照实施例2中的方法,以临床诊断为系统性红斑狼疮患者血清中抗双链dna抗体为检测对象,考察同一样本重复检测后rlu的变异系数(cv)。
其中对照组b中使用实施例1所制备的r1、r2和r3。实验组分别加入了吖啶酮、9-氨基吖啶、9-甲基吖啶、3,6-二氨基吖啶和2-氨基吖啶酮,其余与对照组相同。具体地,实验组b1的r2中加入0.10mg/l的吖啶酮;实验组b2的r2中加入0.10mg/l的9-氨基吖啶;实验组b3的r2中加入0.10mg/l的9-甲基吖啶;实验组b4的r2中加入0.10mg/l的3,6-二氨基吖啶;实验组b5的r2中加入0.10mg/l的2-氨基吖啶酮。每个样本测定3次。cv的计算方式与实施例3相同。
测定结果如下表3a至表3c所示。
表3a
表3b
表3c
由表3a至3c可知,对照组检测结果的cv高达20.25%,难以满足抗双链dna抗体检测的需要。在按0.10mg/l分别加入吖啶酮、9-氨基吖啶、9-甲基吖啶、3,6-二氨基吖啶和2-氨基吖啶酮之后,检测结果均得到明显改善,单样本cv均在8%以内,平均cv均在3%左右。
- 还没有人留言评论。精彩留言会获得点赞!