倒千里光碱的半抗原、人工抗原及其制备方法与应用
1.本发明涉及一种倒千里光碱的半抗原、人工抗原及其制备方法与应用,属于食品安全检测领域。
背景技术:
2.倒千里光碱是吡咯里西啶类生物碱的一种。2017年10月27日,世界卫生组织国际癌症研究机构公布的致癌物清单初步整理参考,倒千里光碱在3类致癌物清单中。吡咯里西啶类生物碱是诸多开花植物的次生代谢物,是目前已知的继马兜铃酸后的最重要的植物毒性成分,是影响牲畜、野生动物和人类的天然毒素。咯里西啶类生物碱主要分布在菊科、紫草科和豆科等植物中,其主要的靶器官为肝脏,可引起肝细胞出血性坏死、肝巨红细胞症及静脉闭塞症等,此外还具有肺脏毒性,致癌作用,致突变作用和神经毒性等。因吡咯里西啶类生物碱分布广泛,可以通过间接的食物污染如蜂蜜、谷物、牛奶、牧草等的污染或者直接通过含吡咯里西啶类生物碱的传统草药、滋补品、茶等对人类或牲畜生命造成极大的毒害。
3.针对吡咯里西啶类生物碱在人类食品及天然药物中的广泛存在和危害,许多国家或组织制定了相应的法规。我国新版药典中一些中药品种确实含有吡咯里西啶类生物碱。除了个别品种(如千里光),在质量标准中加强了有毒成分的控制,对于具有药食兼用的品种,相关研究则更少。现存的检测动植物食品中吡咯里西啶类生物碱的方法主要是仪器方法,包括高效液相色谱、气相色谱-质谱联用法、液相色谱-串联质谱法等,虽然色谱技术能够进行定性定量、高效率,高灵敏度的检测,但此类方法不能实现现场检测,难以推广普及。相较于色谱技术,基于抗原抗体的特异性结合,具有灵敏、快速、特异、简便等优点,近年来已广泛应用到食品安全检测中。
4.目前吡咯里西啶类生物碱的免疫学检测大多为仪器检测,而国内有关吡咯里西啶类生物碱检测试剂盒的开发还相对落后。因此设计免疫半抗原分子,开发一种简单、快捷、用于多种倒千里光碱检测的抗体显得尤为重要;更是为我国进出口食品中吡咯里西啶类有毒生物碱快速检测提供理论和技术依据,保障食品安全和人类健康。
技术实现要素:
5.本发明的目的是提供一种倒千里光碱半抗原、人工抗原及其制备方法与应用。
6.本发明所提供的倒千里光碱半抗原,其结构式如式ⅰ所示:
[0007][0008]
所述倒千里光碱半抗原可按照下述制备方法制备:
[0009]
在4-二甲氨基吡啶的催化下,倒千里光碱与琥珀酸酐进行反应即得。
[0010]
具体地,所述倒千里光碱与所述4-二甲氨基吡啶摩尔比为1:1~2;
[0011]
所述倒千里光碱与所述琥珀酸酐的摩尔比为1:1.2~1.5;
[0012]
所述反应温度室温(25℃左右),所述反应时间为4~5h。
[0013]
所述反应在二氯甲烷中进行;
[0014]
反应结束后,可通过硅胶柱收集,然后在35℃氮气下吹干。
[0015]
本发明还提供了一种倒千里光碱人工抗原,由所述倒千里光碱半抗原与载体蛋白偶联后得到;
[0016]
所述载体蛋白选自牛血清白蛋白、卵清蛋白和钥孔血蓝蛋白中任一种,优选牛血清白蛋白或卵清蛋白。
[0017]
所述倒千里光碱半抗原与所述载体蛋白的偶联摩尔比约为5:1;
[0018]
所述倒千里光碱人工抗原可以作为免疫原也可以作为包被原。
[0019]
可采用活泼酯法将所述载体蛋白偶联于所述半抗原的羧基碳上得到所述倒千里光碱人工抗原,具体步骤为:将所述倒千里光碱半抗原、n-羟基琥珀酰亚胺(nhs)、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc),溶于n,n-二甲基甲酰胺(dmf)中,室温搅拌过夜,得到a液;取所述载体蛋白溶于碳酸盐缓冲液中,得到b液;逐滴将所述a液滴入所述b液中,室温搅拌反应过夜,得到偶联物的混合液;混合液在pbs中透析三天,得到所述倒千里光碱人工抗原。
[0020]
所述倒千里光碱半抗原或所述倒千里光碱人工抗原具有下述应用:
[0021]
1)制备抗倒千里光碱抗体;
[0022]
2)检测食品或药品中倒千里光碱的残留。
[0023]
本发明还提供了一种倒千里光碱的单克隆抗体,通过所述倒千里光碱人工抗原免疫实验动物(雌性balb/c小鼠),经过细胞融合、筛选和体外诱生得到。
[0024]
所述倒千里光碱的单克隆抗体可用于制备倒千里光碱检测试剂或试剂盒。
[0025]
所述倒千里光碱的单克隆抗体具有下述应用:
[0026]
1)倒千里光碱的免疫检测;
[0027]
2)倒千里光碱免疫层析试纸条的制备;
[0028]
3)倒千里光碱的胶体金检测试纸条的制备。
[0029]
本发明提供了倒千里光碱半抗原、人工抗原及其制备方法,采用所述倒千里光碱人工抗原免疫动物,可得到效价高,灵敏度高并且可以同时识别倒千里光碱(rertsrsine,
rts)、阔叶千里光碱(platyphylline,pla)、千里光宁碱(senecionine,sen)、全缘千里光碱(integerrimine,int)、迷迭香宁碱(rosmarinine,ros)、春生千里光碱(senecivernine,sev)、新阔叶千里光碱(neoplatyphylline,neo)、菊三七胺(gynuramine,gyn)、野百合碱(monocrotaline,mct)的广谱性抗体。本发明提供的倒千里光碱半抗原及其制备的抗体,为建立快速、简便、价廉、灵敏的同时检测多种吡咯里西啶类生物碱残留的方法提供了新手段。
[0030]
本发明提供的半抗原制备方法简单,与载体蛋白的偶联物制备的单克隆抗体抗体对rts、pla、sen、int、ros、sev、neo、cyn、mct的检测灵敏度可分别达0.86、0.75、0.43、0.59、19.32、56.32、129.34、184.61、1003.95ng/ml,实用价值高。本发明在食品安全检测中具有良好的应用前景。
附图说明
[0031]
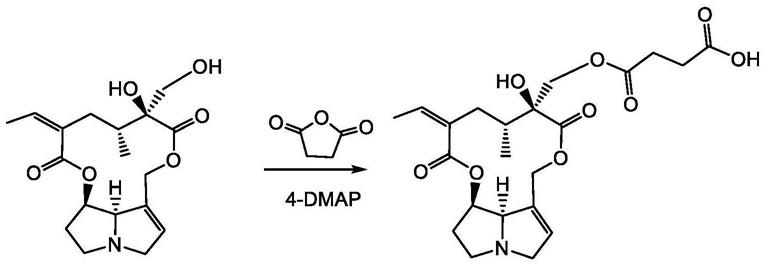
图1为制备本发明式i所示倒千里光碱半抗原的反应方程式。
[0032]
图2为本发明式i所示倒千里光碱半抗原的质谱图。
[0033]
图3为本发明半抗原与牛血清白蛋白偶联的maldi-tof-ms图,其中,图3(a)为牛血清白蛋白的maldi-tof-ms图,图3(b)为偶联物的maldi-tof-ms图。
[0034]
图4为本发明利用单克隆抗体检测9种倒千里光碱的标准曲线图,其中,图4(a)-图4(i)依次表示检测rts、sen、int、pla、sev、ros、cyn、neo、mct的标准曲线。
具体实施方式
[0035]
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
[0036]
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
[0037]
下述实施例中的定量试验,均设置三次重复实验,结果取平均值。实施例中所用的pbs缓冲液均为ph 7.4、0.01m的pbs缓冲液,碳酸盐缓冲液均为ph 9.6、0.05mol/l的碳酸钠缓冲液。
[0038]
下述实施例中,nhs为n-羟基琥珀酰亚胺的缩写,edc为1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐的缩写,dmf为n,n-二甲基甲酰胺的缩写。nhs、edc、牛血清白蛋白(albumin from bovine serum,bsa)、钥孔血蓝蛋白(keyhole limpet hemocyanin,klh)、卵清蛋白(ovalbumin,ova)以及弗氏完全佐剂、弗氏不完全佐剂均购自sigma公司。
[0039]
实施例1、倒千里光碱半抗原的制备和表征
[0040]
一、倒千里光碱半抗原的制备
[0041]
式i所示倒千里光碱半抗原的制备,,反应方程式如图1所示。
[0042]
(1)将35.1mg倒千里光碱与2.2mg 4-二甲氨基吡啶(dmap),完全溶解在10ml二氯甲烷中,其中,倒千里光碱与4-二甲氨基吡啶的摩尔比为1:2;
[0043]
(2)向反应液中添加10.7mg琥珀酸酐,在室温下,600r/min搅拌5小时后,通过硅胶柱收集化合物,倒千里光碱与琥珀酸酐的摩尔比为1:1.2。
[0044]
(3)将得到的化合物在35℃氮气下吹干,得到倒千里光碱半抗原37.9mg(84%)。
[0045]
二、倒千里光碱半抗原的表征
[0046]
质谱鉴定:式i所示倒千里光碱半抗原的质谱鉴定结果:ms m/z[m+h]
+
理论值:
451.2;实测值:452.45,与目标产物的分子量相吻合,质谱如图2所示。
[0047]
实施例2、倒千里光碱人工抗原的制备和表征
[0048]
免疫原与包被原的制备方法中,其区别在于载体蛋白的使用类型,免疫原载体蛋白主要采用bsa,包被原载体蛋白主要采用ova,所用偶联方法为活泼酯法。
[0049]
一、倒千里光碱人工抗原的合成和鉴定
[0050]
1、倒千里光碱人工抗原的制备
[0051]
(1)以半抗原与bsa投料比1:100计算,精确称取半抗原9mg,edc 8mg,nhs 5mg分别溶解于2ml dmf中,置于磁力搅拌器上室温搅拌过夜,即为溶液a液。
[0052]
(2)然后将22mg bsa、ova分别溶于5ml 0.05m碳酸盐缓冲液中,得到溶液b液
[0053]
(3)将溶液a缓慢滴加至溶液b液中,室温搅拌反应过夜,得到偶联物的混合液;混合液在0.01m pbs中透析三天,最终得到倒千里光碱人工抗原,-20℃保存。简称rts-hs-bsa、rts-hs-ova。
[0054]
2、倒千里光碱人工抗原的鉴定
[0055]
用基质辅助激光解吸电离飞行时间质谱(matrix-assisted laser desorption/ionization time of flight mass specrtsmetry,maldi-tof-ms)法测定rts-hs-bsa溶液中bsa与半抗原的结合比。结果见图3。
[0056]
结合比={m(偶联物)-m(蛋白质)}/m(半抗原)
[0057]
bsa的分子量为64771.30,式(i)半抗原的分子量为452.45,由质谱最高峰值分析偶联物的分子量为66991.13,经计算得出bsa与半抗原的结合比为4.9:1,即rts-hs-bsa中一个bsa分子上平均偶联4.9个半抗原。
[0058]
实施例3、倒千里光碱单克隆抗体的制备
[0059]
将实施例2制备的rts-hs-bsa人工抗原分别免疫8只6~8周龄balb/c雌性小鼠。使用0.01m pbs将各免疫原用稀释至1mg/ml,与等量的弗氏佐剂乳化,形成油包水结构。除首免采用弗氏完全佐剂外,其余加强免疫一律采用弗氏不完全佐剂,免疫剂量为100μg/只,颈背部皮内多点注射。4周后进行加强免疫并且每隔3周加免1次,共加免2次,改为颈背部皮下多点注射。在两次加免后的7~10天采每只小鼠的眼眶血离心取上清进行测定,选择抗血清效价与抑制均良好的小鼠,取脾细胞与骨髓瘤细胞融合,经过三次单细胞团亚克隆后,进行定株及扩大培养,采取体内诱生的方式获得抗体,并使用protein a免疫亲和柱进行纯化,最后保存于-20℃备用。
[0060]
实施例4、倒千里光碱抗血清的测定
[0061]
一、采用间接elisa方法检测抗血清效价
[0062]
具体操作步骤如下:
[0063]
(1)包被:将实施例2中的人工抗原rts-hs-ova用0.05m、ph 9.6碳酸盐缓冲液从15μg/ml进行倍比稀释,100μl/孔,置于37℃恒温培养箱孵育2h,甩干。
[0064]
(2)洗涤:洗涤液280μl/孔,洗涤2次,甩干。
[0065]
(3)封闭:封闭液150μl/孔,置于37℃恒温培养箱孵育1h后,甩干。
[0066]
(4)加样:每孔加入50μl pbs,然后将抗血清从1:1000开始进行倍比稀释,并50μl/孔加入到各稀释度的包被孔中,置于37℃恒温培养箱孵育30min,洗涤3次后甩干;加入1:5000稀释的hrp标记的羊抗鼠抗体,100μl/孔,置于37℃恒温培养箱孵育30min,洗涤5次甩
干。
[0067]
(5)显色:每孔加入100μl的tmb显色液,37℃避光反应15min。
[0068]
(6)终止和测定:每孔加入50μl终止液(2m h2so4),然后用酶标仪测定各孔的od
450
值。
[0069]
(7)结果判读:以od
450
值≥阴性对照孔的2.1倍(即p/n≥2.1)所对应的血清最高稀释倍数即为血清的elisa效价。
[0070]
二、最低检测限、半数抑制以及特异性的检测
[0071]
具体操作步骤如下:
[0072]
(1)用上述间接elisa方法确定以rts-hs-ova作为包被原,以rts-hs-klh免疫小鼠进行细胞融合生产抗体,以od
450
值在1.5左右时所对应的抗原和抗体浓度为最适工作浓度。
[0073]
(2)包被:将包被原用包被缓冲液稀释20000倍,100μl/孔,置于37℃恒温培养箱孵育2h。
[0074]
(3)洗涤和封闭:方法操作同上述间接elisa法。
[0075]
(4)分别配置标准溶液:将9种生物碱标准品用0.01mol/l,ph7.4的pbs溶液配制成2mg/ml的母液,然后,在加样前,再用0.01mol/l,ph7.4的pbs溶液倍比稀释成梯度为0、0.04、0.11、0.33、1、3、9、27ng/ml rts、pla、sen、int标准溶液,梯度为0、0.14、0.41、1.23、3.70、11.11、33.33、100ng/ml ros、sev标准溶液,梯度为0、1.4、4.1、12.3、37、111.11、333.33、1000ng/ml neo和cyn标准溶液,0、13.71、41.15、123.46、370.37、1111.11、3333.33、10000ng/ml mct标准溶液
[0076]
(5)加样:每孔加入50μl倍比稀释的各浓度标准品,然后再加入50μl/孔最适稀释倍数的抗体,37℃反应30min。充分洗涤后,加入1:5000稀释的hrp-羊抗鼠igg,100μl/孔,37℃反应30min。
[0077]
(6)显色反应:将酶标板取出,充分洗涤后,每孔加入100μl的tmb显色液,37℃避光反应15min。
[0078]
7)终止和测定:每孔加入50μl终止液以终止反应,然后用酶标仪测定各孔的od
450
值。
[0079]
8)数据处理:以各标准品浓度为横坐标,以各浓度对应的od
450nm
值为纵坐标,使用origin软件,按照四参数对数拟合绘制标准曲线,如图4所示,通过计算ic
50
值(半数抑制浓度)判定抗体对吡咯里西啶类生物碱是否具有识别。
[0080]
结果显示,所获得单克隆抗体对rts、pla、sen、int、ros、sev、neo、cyn、mct的检测灵敏度可分别达0.86、0.75、0.43、0.59、19.32、56.32、129.34、184.61、1003.95ng/ml。
[0081]
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之做一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1