有机硒化合物及其治疗用途的制作方法
1.本技术涉及药物化学领域,具体来说涉及式(i)化合物、包含所述式(i)化合物的药物组合物以及所述式(i)化合物在制备用于治疗或预防神经炎症相关疾病或症状的药物中的用途。
背景技术:
2.神经炎症会导致神经损伤,产生一系列病理生理变化,并导致相关神经疾病和症状发生。相关疾病主要是一组表现在行为、心理活动上的紊乱为主的神经系统疾病。
3.老年痴呆症是一种典型的神经炎症相关疾病,其为一种以记忆损伤为主的多种认知功能障碍的神经系统疾病,可分为三种:原发性痴呆、血管性痴呆、其它原因性痴呆。原发性痴呆包括阿尔兹海默病(alzheimers disease,ad)、帕金森氏病(parkinson’s disease,pd)和皮克病。阿尔兹海默病的主要病理特征为β样淀粉沉积、纤维缠结、基底核胆碱能神经元缺失、海马及皮层神经元广泛丢失及突触改变。最近的研究指出,出现活化的小胶质细胞是ad的另一病理特征。小胶质细胞是中枢神经系统的免疫细胞,作为常驻的免疫和吞噬细胞,在中枢神经系统发挥重要作用。在中枢神经系统的炎症进程中,多种因素可以诱发小胶质细胞的活化。活化的小胶质细胞可以释放包括一氧化氮(no)、白细胞介素il-1β、活性氧(ros)在内的大量神经毒性因子。研究表明,抑制神经炎症可成为防治ad的一个重要策略(cn110638854a)。
4.目前,一般认为神经炎症是导致都是多种神经系统疾病发生的重要原因。马春燕等指出,神经炎症机制是抑郁症的主要发生原因,炎症假说认为应激刺激引发炎症过程,并最终导致抑郁症的发生(中国医药导报,2017,14(14):33-35)。smith等在1991年提出炎症可参与抑郁症病理生理过程(barbara s beltz,michael f tlusty,jeanne l benton,et al.omega-3fatty acids upregulate adult neurogenesis[j].neurosci lett,2007,415(2):154-158.),这一学说也得到了大量研究结果的支持。
[0005]
帕金森病(parkinson’s disease,pd)是一种以中脑黑质致密部多巴胺能神经元进行性变性、缺失,以及路易小体形成为主要特征的中枢神经系统退行性疾病,其临床表现主要包括静止性震颤、运动迟缓、肌强直和姿势障碍等运动症状以及情绪低落、焦虑、睡眠障碍、认知障碍等非运动症状。大量的研究资料显示,小胶质细胞和星型胶质细胞介导的炎症反应在pd的发病过程中起着重要的作用。小胶质细胞是中枢神经系统内重要的免疫感受和效应细胞,黑质区是脑内小胶质细胞分布最丰富的脑区之一,黑质多巴胺能神经元对小胶质细胞介导的炎症反应极其敏感。在神经退行性疾病的发生和发展过程中,过度激活的小胶质细胞可产生一系列的炎性因子,如il-1β、ifn-γ、no、il-6、tnf-α等。这些炎性因子一方面可导致神经元的损伤和丢失,而受损的神经元会释放no和ros等,作用于小胶质细胞,促使其释放炎性因子,促进小胶质细胞的进一步激活,从而在神经元损伤和小胶质细胞激活之间形成恶性循环;另一面,这些炎性因子也可激活星型胶质细胞,促使星型胶质细胞释放炎性因子进一步损伤神经元。因此,如何有效抑制神经细胞的炎症反应,减轻胶质细胞
的过度活化成为治疗神经退行性疾病的潜在靶标(cn110623974a)。
[0006]
随着近年对多种神经系统病变如阿尔茨海默症、帕金森病、多发性硬化、脑梗塞、进行性肌肉萎缩症、帕金森病和亨廷顿舞蹈病等发病机制的深入探索,越来越多的研究结果表明,小胶质细胞激活介导的脑内慢性炎症反应是神经系统病变的病理特征之一(cn111116595a)。
[0007]
尽管已有研究为相关神经炎症相关疾病或症状的治疗阐明了一条途径,但现有化合物包括抗炎药,特别是非甾体抗炎剂仍普遍存在效力不足、安全性受限制等问题,还远远不能满足人类对于相关疾病预防和治疗的日益增长的需求。因此,开发出效果更好、结构类型更新颖的药物化合物,已成为迫切需要。
技术实现要素:
[0008]
本发明人经过大量实验研究,意外发现了一类有机硒衍生物,具有出乎意料的预防和治疗神经炎症相关疾病或症状的生物活性。所述化合物可有效用于多种相关疾病或症状的治疗和/或预防。
[0009]
基于上述发现,在第一方面,本发明提供了具有下式(i)结构的化合物:r-se-l-nr1r2r3(i)或其可药用盐,其中,r选自氰基、c1-c4烷基或卤代c1-c4烷基;l为1至4个碳原子的直链或支链化的亚烷基链;r1、r2、r3可相同或不同,各自独立地表示c1-c4烷基或羟基c1-c4烷基。在本发明的优选的实施方案中,r1、r2、r3均为c1-c4烷基或者r1、r2为c1-c4烷基且r3为羟基c1-c4烷基。更优选地,r1、r2、r3均为甲基或者r1、r2为甲基且r3为羟乙基。优选地,l为亚乙基(-(ch2)
2-)或亚丙基(-(ch2)
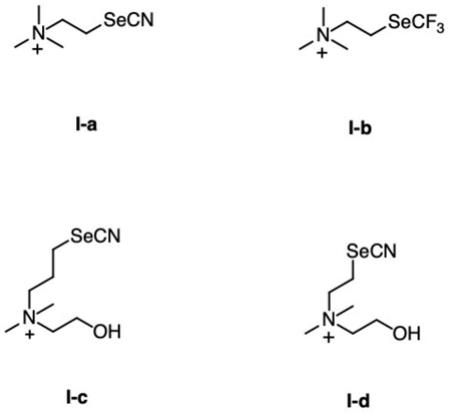
3-)。在本发明的优选的实施方案中,所述式(i)化合物为选自以下的化合物:或其可药用盐。
[0010]
在本发明的另一个方面,还提供了一种药物组合物,其包含本发明的化合物和任
选的药物载体或赋形剂。
[0011]
在本发明的又一个方面,上述药物组合物还可包含另外的活性药物成分,即第二药物,所述第二药物适于治疗医学上表明施用本发明化合物可治疗或预防的相同病症或相关病症。
[0012]
在本发明的另一方面,还提供了本发明的式(i)化合物在制备用于治疗或预防神经炎症相关疾病或症状的药物中的用途。
[0013]
本发明的多个实施方案提供了使用本发明的化合物、组合物或组合的方法,包括向需要治疗其不良状况的患者以足以向所述患者提供有益效果的剂量、频率和持续时间来施用所述化合物、组合物或组合。
附图说明
[0014]
图1是表明lps刺激bv2细胞显著增加no释放水平的图;
[0015]
图2是表明本发明化合物显著下调ros水平的效果的图;
[0016]
图3是表明本发明化合物显著降低促炎因子il-1β的释放水平的图。
具体实施方式
[0017]
术语“治疗”定义为为了对抵抗疾病、病症或障碍而对患者进行的处理和护理,其包括施用本发明化合物以预防症状或并发症的发作、或者减轻症状或并发症、或者治愈或消除疾病、病症或障碍。
[0018]
在本发明上下文中的“治疗”意指减轻与病症或疾病相关的症状,或者抑制这些症状的进一步发展或恶化,或者防止或预防所述疾病或病症。类似地,本文中使用的本发明化合物的“有效量”或“治疗有效量”指完全或部分减轻与所述病症或状况相关的症状、或者停止或减缓这些症状的进一步发展或恶化,或者预防或提供对所述病症或状况之预防的化合物的量。
[0019]
当将基团定义为“共价键”时,意指直接邻接该指定基团的基团通过共价键彼此连接。
[0020]
除非具体指出特定的立体化学或异构体形式,否则本发明化合物旨在包括结构的所有手性、非对映体、外消旋形式。在本发明中使用的化合物可以包括根据描述显而易见的任何或所有不对称原子的经富集或拆分的任何富集程度的光学异构体。可以分离或合成外消旋和非对映体混合物以及单独的光学异构体,以便基本上不含其对映体或非对映体,这些都在本发明的范围内。
[0021]
通常,“取代的”指本文中所定义的有机基团(其中包含有与氢原子键合的一个或多个键)被一个或多个与非氢原子键合的键取代,所述非氢原子即为取代基。
[0022]
本发明化合物的取代基(包括ra定义中的取代基)包括卤素、烷基(优选c
1-4
烷基,更优选c
1-2
烷基)、烷氧基(优选c
1-4
烷氧基,更优选c
1-2
烷氧基)、卤代c
1-4
烷氧基-(优选卤代c
1-2
烷氧基-)、氨基、酰基、c
1-4
烷基酰基-(优选c
1-2
烷基烷基酰基-)、酰氧基、c
1-4
烷基酰氧基-(优选c
1-2
烷基酰氧基-)、羧基、硝基、氰基、c
1-4
烷基氨基-(优选c
1-2
烷基氨基-)、卤代c
1-4
烷基(优选卤代c
1-2
烷基)、c
1-4
烷基氨基c
1-4
烷基-(优选c
1-2
烷基氨基c
1-2
烷基-)、羟基、羟基c
1-4
烷基-(优选羟基c
1-2
烷基-)、羟基c
1-4
烷基氨基-(优选羟基c
1-2
烷基氨基-)、c
3-6
环烷基、c2-4
链烯基。
[0023]
在本发明的取代基定义中,短线
“-”
表示某基团或取代基与结构式中其他部分相连接的成键位置。
[0024]
烷基包括具有1至约8个碳原子或在某些实施方案中为1至4个甚至更优选为1至2个碳原子的直链和支链烷基。直链烷基的实例包括具有1至8个、优选1至4个、更优选1-2个碳原子的那些,比如甲基、乙基、正丙基、正丁基、正戊基、正己基、正庚基和正辛基。支链烷基的实例包括但不限于异丙基、异丁基、仲丁基、叔丁基、新戊基、异戊基和2,2-二甲基丙基。代表性的取代烷基可以被任何上述基团取代一次或多次,所述上述基团例如氨基、羟基、氰基、羧基、硝基、硫基、烷氧基和卤素基团。同样,亚烷基意味着烷基具有两个成键位置,其可以是直链或支链形式。优选的亚烷基具有1至约8个碳原子、1至6个碳原子或1至4个碳原子,甚至1至3个碳原子或1至2个碳原子。
[0025]
环烷基为环状烷基,例如但不限于环丙基、环丁基、环戊基、环己基、环庚基和环辛基。在优选的实施方案中,所述环烷基具有3至8个环成员,而在其它一些实施方案中,环碳原子的数目为3至5、6或7个。环烷基进一步包括多环环烷基,例如但不限于降冰片基、金刚烷基、冰片基、莰烯基、异莰烯基和蒈烯基,以及稠环例如但不限于十氢萘基等。环烷基还包括被如上定义的直链或支链烷基取代的环。代表性的取代环烷基可以是单取代的或多于一次取代的,例如但不限于2,2-、2,3-、2,4-、2,5-或2,6-二取代的环己基或单-、二-或三-取代的降冰片基或环庚基,其可以被例如氨基、羟基、氰基、羧基、硝基、硫基、烷氧基和卤素基团取代。术语“环烯基”单独或组合时表示环状烯基。
[0026]
芳基为不包含杂原子的环状芳族烃。因此,芳基包括但不限于苯基、薁基、庚搭烯基(heptalenyl)、联苯基、二环戊二烯并苯基(indacenyl)、芴基、菲基、三亚苯基(triphenylenyl)、芘基、萘并萘基(naphthacenyl)、亚联苯基、蒽基和萘基。在某些实施方案中,芳基在该基团的环部分中包含6-14个碳。芳基可以是未取代或取代的,如上所定义。代表性的取代芳基可以是单取代的或多于一次取代的,例如但不限于2-、3-、4-、5-或6-取代的苯基或2-8取代的萘基,其可以被碳或非碳基团(如上述那些)取代。
[0027]
杂芳基是含有5个或更多个环成员的芳环化合物,其中一个或更多个环成员是杂原子,例如但不限于n、o和s。命名为c
2-杂芳基的杂芳基可以是具有两个碳原子和三个杂原子的5元环、具有两个碳原子和四个杂原子的6元环等。同样地,c
4-杂芳基可以是具有一个杂原子的5元环、具有2个杂原子的6元环等。碳原子数目加杂原子数目的总和等于环原子的总数。杂芳基包括但不限于例如以下的基团:吡咯基、吡唑基、三唑基、四唑基、噁唑基、异噁唑基、噻唑基、吡啶基、噻吩基、苯并噻吩基、苯并呋喃基、吲哚基、氮杂吲哚基、吲唑基、苯并咪唑基、氮杂苯并咪唑基、苯并噁唑基、苯并噻唑基、苯并噻二唑基、咪唑并吡啶基、异噁唑并吡啶基、硫杂萘基、嘌呤基、黄嘌呤基、腺嘌呤基、鸟嘌呤基、喹啉基、异喹啉基、四氢喹啉基、喹喔啉基和喹唑啉基。杂芳基可以是未取代的,或者可以是被如上所述基团取代的。代表性的取代杂芳基可以被如上所述的那些基团取代一次或多次。
[0028]
芳基和杂芳基的其它实例包括但不限于苯基、联苯基、茚基、萘基(1-萘基、2-萘基)、n-羟基四唑基、n-羟基三唑基、n-羟基咪唑基、蒽基(1-蒽基、2-蒽基、3-蒽基)、噻吩基(2-噻吩基、3-噻吩基)、呋喃基(2-呋喃基、3-呋喃基)、吲哚基、噁二唑基、异噁唑基、喹唑啉基、芴基、呫吨基、异茚满基、二苯甲基、吖啶基、噻唑基、吡咯基(2-吡咯基)、吡唑基(3-吡唑
基)、咪唑基(1-咪唑基、2-咪唑基、4-咪唑基、5-咪唑基)、三唑基(1,2,3-三唑-1-基、1,2,3-三唑-2-基、1,2,3-三唑-4-基、1,2,4-三唑-3-基)、噁唑基(2-噁唑基、4-噁唑基、5-噁唑基)、噻唑基(2-噻唑基、4-噻唑基、5-噻唑基)、吡啶基(2-吡啶基、3-吡啶基、4-吡啶基)、嘧啶基(2-嘧啶基、4-嘧啶基、5-嘧啶基、6-嘧啶基)、吡嗪基、哒嗪基(3-哒嗪基、4-哒嗪基、5-哒嗪基)、喹啉基(2-喹啉基、3
--
喹啉基、4-喹啉基、5-喹啉基、6-喹啉基、7-喹啉基、8-喹啉基)、异喹啉基(1-异喹啉基、3-异喹啉基、4-异喹啉基、5-异喹啉基、6-异喹啉基、7-异喹啉基、8-异喹啉基)、苯并[b]呋喃基(2-苯并[b]呋喃基、3-苯并[b]呋喃基、4-苯并[b]呋喃基、5-苯并[b]呋喃基、6-苯并[b]呋喃基、7-苯并[b]呋喃基)、2,3-二氢-苯并[b]呋喃基(2-(2,3-二氢-苯并[b]呋喃基)、3-(2,3-二氢-苯并[b]呋喃基)、4-(2,3-二氢-苯并[b]呋喃基)、5-(2,3-二氢-苯并[b]呋喃基)、6-(2,3-二氢-苯并[b]呋喃基)、7-(2,3-二氢-苯并[b]呋喃基)、苯并[b]噻吩基(2-苯并[b]噻吩基、3-苯并[b]噻吩基、4-苯并[b]噻吩基、5-苯并[b]噻吩基、6-苯并[b]噻吩基、7-苯并[b]噻吩基)、2,3-二氢-苯并[b]噻吩基、(2-(2,3-二氢-苯并[b]噻吩基)、3-(2,3-二氢-苯并[b]噻吩基)、4-(2,3-二氢-苯并[b]噻吩基)、5-(2,3-二氢-苯并[b]噻吩基)、6-(2,3-二氢-苯并[b]噻吩基)、7-(2,3-二氢-苯并[b]噻吩基)、吲哚基(1-吲哚基、2-吲哚基、3-吲哚基、4-吲哚基、5-吲哚基、6-吲哚基、7-吲哚基)、吲唑(1-吲唑基、3-吲唑基、4-吲唑基、5-吲唑基、6-吲唑基、7-吲唑基)、苯并咪唑基(1-苯并咪唑基、2-苯并咪唑基、4-苯并咪唑基、5-苯并咪唑基、6-苯并咪唑基、7-苯并咪唑基、8-苯并咪唑基)、苯并噁唑基(1-苯并噁唑基、2-苯并噁唑基)、苯并噻唑基(1-苯并噻唑基、2-苯并噻唑基、4-苯并噻唑基、5-苯并噻唑基、6-苯并噻唑基、7-苯并噻唑基)、咔唑基(1-咔唑基、2-咔唑基、3-咔唑基、4-咔唑基)等。
[0029]
更特别地,芳基和杂芳基可以包括苯基、异吲哚烷基(isoindolidinyl)、咪唑基、噁唑基、苯并咪唑基和苯并噁唑基;其中任何芳基或杂芳基可以是未取代的、单取代的或者独立地多取代的,例如用如本文定义的j基团取代。
[0030]
术语“烷氧基”指氧原子连接到如上述定义的包括环烷基在内的烷基上。直链烷氧基的实例包括但不限于甲氧基、乙氧基、丙氧基、丁氧基、戊氧基、己氧基等。支链烷氧基的实例包括但不限于异丙氧基、仲丁氧基、叔丁氧基、异戊氧基、异己氧基等。环烷氧基的实例包括但不限于环丙氧基、环丁氧基、环戊氧基、环己氧基等。
[0031]
本文使用的术语“卤素”包括氟、氯、溴和碘。“卤代烷基”包括单卤代烷基和多卤代烷基(其中所有卤原子可以相同或不同)。部分卤代的烷基是本文含义内的“卤代烷基”。卤代烷基的实例包括三氟甲基、1,1-二氯乙基、1,2-二氯乙基、1,3-二溴-3,3-二氟丙基等。
[0032]
本文中使用的术语“酰基”指包含羰基部分的基团,其中该基团经由该羰基碳原子键合。该羰基碳原子还键合至其它碳原子,其可以是烷基、芳基、芳烷基环烷基、环烷基烷基、杂环基、杂环基烷基、杂芳基、杂芳基烷基等的一部分。在其中羰基碳原子键合至氢的特定情况下,该基团是“甲酰基”,其为一种酰基(该术语如本文所定义)。其它的实例包括乙酰基、苯甲酰基、苯乙酰基、吡啶基乙酰基、肉桂酰基和丙烯酰基等。当包含键合至羰基碳原子的碳原子的基团包含卤素时,该基团称为“卤代酰基”。一个实例为三氟乙酰基。
[0033]
本领域众所周知的“盐”包括有机化合物,例如离子形式的羧酸、磺酸或胺与反离子的组合。例如,阴离子形式的酸可以与下述物质形成盐:阳离子如金属阳离子,例如钠、钾等;铵盐如nh
4+
或多种胺的阳离子,包括四烷基铵盐如四甲铵,或其它阳离子如三甲基硫鎓
等。“可药用”盐是由已批准用于人使用且通常无毒的离子形成的盐,比如盐酸盐或钠盐。“两性离子”是内盐,例如其可以在具有至少两个可电离基团的分子中形成,一个形成阴离子,另一个形成阳离子,其彼此达到平衡。例如,氨基酸(如甘氨酸)可以以两性离子形式存在。“两性离子”是本文含义内的盐。
[0034]“水合物”是以与水分子组合存在的化合物。所述组合物可以包含化学计量量的水,例如一水合物或二水合物,或者可以包含任意量的水。
[0035]“溶剂化物”是类似的组合物,不同点在于用不同于水的溶剂代替水。例如,甲醇或乙醇可以形成“醇化物”,其也可以是化学计量的或非化学计量的。
[0036]“互变异构体”是物质的两种形式,其仅仅在分子结构中的氢原子位置不同。
[0037]
本发明的另一个方面提供了包含本发明化合物和任选的药物载体或赋形剂的药物组合物或者包含除本发明化合物外还另外包含其他药物活性成分以及任选的载体的药物组合物。本发明的药物组合物可以通过常规技术制备,例如在remington:the science and practice of pharmacy,第19版,1995中所描述的方法,其通过引用并入本文。所述组合物可以以常规形式出现,例如胶囊、片剂、气雾剂、溶液剂、混悬剂或局部施用形式。
[0038]
典型的组合物包含本发明化合物和载体。例如,活性化合物通常与载体混合,或者被载体稀释,或者被密封在可以为安瓿、胶囊、小药囊(sachet)、纸或其它容器形式的载体内。当将活性化合物与载体混合时,或者当载体充当稀释剂时,所述载体可以为充当活性化合物的载体、赋形剂或介质的固体、半固体或液体材料。所述活性化合物可以吸附在颗粒状固体载体上(例如容纳在小药囊中)。合适的载体的一些实例为水、盐溶液、醇、聚乙二醇、聚羟基乙氧基化蓖麻油、花生油、橄榄油、明胶、乳糖、白土、蔗糖、糊精、碳酸镁、糖、环糊精、直链淀粉、硬脂酸镁、滑石、明胶、琼脂、果胶、阿拉伯胶、硬脂酸或纤维素的低级烷基醚、硅酸、脂肪酸、脂肪酸胺、脂肪酸甘油单酯和甘油二酯、季戊四醇脂肪酸酯、聚氧乙烯、羟甲基纤维素和聚乙烯吡咯烷酮。类似地,所述载体或稀释剂可以包括任何本领域已知的持续释放材料,例如单独的单硬脂酸甘油酯或二硬脂酸甘油酯或者其与蜡的混合物。
[0039]
所述制剂可以与不与所述活性化合物发生有害反应的辅助剂混合。这些添加剂可以包括润湿剂、乳化剂和助悬剂、影响渗透压的盐、缓冲剂和/或着色物质、防腐剂、甜味剂或调味剂。如果需要,还可以对所述组合物进行灭菌。
[0040]
施用途径可以是将本发明活性化合物有效地转运到适当的或期望的作用部位的任何途径,例如口服、经鼻、肺部、口含、皮下、皮内、透皮或肠胃外途径,例如直肠、贮库(depot)、皮下、静脉内、尿道内、肌内、鼻内、眼用溶液或软膏剂的途径,口服途径是优选的。
[0041]
如果使用固体载体用于口服施用,则该制剂可以是压片的,以粉剂或小丸形式置于硬明胶胶囊中,或者其可以是糖锭或锭剂的形式。如果使用液体载体,则所述制剂可以是糖浆剂、乳剂、软明胶胶囊或无菌可注射液体的形式,例如水性或非水性液体混悬剂或溶液剂。
[0042]
可注射的剂型通常包括水性混悬剂或油性混悬剂,其可以使用合适的分散剂或润湿剂和助悬剂来制备。可注射的形式可以是在溶液相中或者是用溶剂或稀释剂制备的混悬剂的形式。可接受的溶剂或载体包括无菌水、林格溶液或等渗盐水溶液。或者,可以应用无菌油作为溶剂或助悬剂。优选地,所述油或脂肪酸是不挥发性的,包括天然油或合成油、脂肪酸、甘油单酯、甘油二酯或甘油三酯。
[0043]
对于注射而言,所述制剂还可以是适于用上述的合适溶液重构的粉末。这些的实例包括但不限于冷冻干燥的、旋转干燥的或喷雾干燥的粉末,无定形粉末、颗粒、沉淀物或微粒。对于注射剂而言,所述制剂可以任选地包含稳定剂、ph调节剂、表面活性剂、生物利用度调节剂和这些试剂的组合。可以将所述化合物配制为用于通过注射进行胃肠外施用,例如通过推注或连续输注。用于注射的单位剂型可以在安瓿中或多剂量容器中。
[0044]
可以将本发明的制剂设计成在通过本领域熟知的方法施用至患者后能提供活性成分的快速、持续或延迟释放。因此,还可以将所述制剂配制成用于控释释放或缓慢释放。
[0045]
本发明的化合物在宽的剂量范围都是有效的。例如,在成年人的治疗中,可以使用每天约0.05至约5000mg、优选约1至约2000mg、更优选约2至约2000mg的剂量。典型的剂量为每天约10mg至约1000mg。在选择患者治疗方案时,其可常常须从较高的剂量开始,并且当病症得到控制时减少剂量。精确的剂量将取决于化合物的活性、施用方式、期望的治疗、施用的形式、待治疗的对象和待治疗对象的体重、及主管医师或兽医的偏好和经验。
[0046]
通常,将本发明化合物分配在单位剂型中,其每单位剂量包含约0.05mg至约1000mg活性成分和可药用载体。
[0047]
通常,适于口服、经鼻、肺部或透皮施用的剂型包括约125μg至约1250mg、优选约250μg至约500mg、更优选约2.5mg到约250mg的与可药用载体或稀释剂混合的所述化合物。
[0048]
剂型可以是每日一次、或每日一次以上例如每日两次或每日三次施用。或者,剂型可以少于每日一次的频率施用,例如每隔一天或每周,如果开处方的医师认为合适的话。
[0049]
药物组合物可以片剂、胶囊、粉剂、颗粒剂、锭剂、液体或胶状物形式。供口服的片剂和胶囊可以适于单位剂量用药的形式,并且可以含常规的赋形剂,这些例子有:结合剂如糖浆、阿拉伯树胶、凝胶、山梨醇、黄著胶、聚乙烯吡咯烷酮(pvp);填料如乳糖、糖类、玉米粉、磷酸钙、山梨醇或甘氨酸;片剂润滑剂如硬脂酸镁、二氧化硅、滑石、聚乙二醇或二氧化硅;崩解剂如马铃薯淀粉;可接受的润滑剂如月桂基硫酸钠。片剂可按照已知的常规制药实践中的方法进行包衣。口服液体制剂可以使水状或油状悬浮液、溶液、乳剂、糖浆或酊剂,也可制成一种干物质,在使用之前再用水或其它合适的载体重新调制。这些液体制剂可含有常规的添加剂,例如悬浮剂(如:山梨醇、糖浆、甲基纤维素、葡萄糖浆、明胶、经氢化的食用油脂)。乳化剂(如孵磷脂,山梨醇单油酸盐或阿拉伯树胶),非水相载体(包括食用油如杏仁油、精馏的椰子油、油脂如甘油、丙二醇或乙醇),防腐剂(如甲基或丙基对羟基苯甲酸或山梨酸),如果需要也可含有常规的风味剂或着色剂。
[0050]
本发明药物组合物中活性物质的百分比是可变的,因为必须使药物调剂制成一定合适比例的剂量,以获得理想的疗效。总之,本发明的药物制剂经口服或注射给药应按每70kg体重每天1至15毫克活性物质。以下说明性的而不是限制性的给出一些实施实施例。
[0051]
在本文中,提到式(i)化合物时,该术语包括其可药用盐。
[0052]
本发明提供了本发明式(i)化合物在制备用于治疗或预防神经炎症相关疾病或症状的药物中的用途。相应地,本发明提供了一种治疗或预防神经炎症相关疾病或症状的方法,包括向有此需要的对象(例如哺乳动物尤其是人)给予本发明所述的式(i)化合物。实施例
[0053]
以下结合具体的实施例对本发明的技术方案和应用作进一步说明:合成制备例
[0054]
实施例1:化合物i-a的制备反应式如下:
1.将氯化氯胆碱(200mg)溶于乙腈(10ml)中,加入硒氰酸钾(ksecn,273mg,)和碘化钾(ki,315mg),加热到100℃搅拌10小时,质谱监测反应基本完全,待溶液冷却至室温,抽滤,将母液旋干得到粗品。再将粗品溶于甲醇,加热回流,溶液变澄清,待溶液冷却至室温,过滤,将滤饼旋干,得到淡黄色晶体198mg,即化合物i-a,产率92%。
2.核磁共振1h nmr(400mhz,cdcl3):δ3.24(s,9h,3ch3),3.51-3.53(m,2h,ch2),3.88-3.92(m,2h,ch2)
3.esi-ms:194.0([m+1]
+
).实施例2:化合物i-b的制备反应式如下:
1.将i-a(200mg)溶于乙腈(10ml),加入三氟甲基三甲基硅烷(tmscf3,187mg)和碳酸铯(cs2co3,572mg),室温搅拌2小时,质谱显示反应完全,抽滤,母液旋干得粗品,将粗品溶于二氯甲烷(5ml),加热回流后,冷却至室温,抽滤,得到棕色固体133mg,即化合物i-b,产率90%。
2.核磁共振1h nmr(400mhz,cdcl3):δ3.21(s,9h,3ch3),3.41-3.44(m,2h,ch2),3.79-3.83(m,2h,ch2)
1.esi-ms:237.0([m+1]
+
).实施例3.化合物i-c的制备反应式如下:
3.将n,n-二甲基乙醇胺(1g)溶于无水乙醇(20ml)中,再加入1,3-二溴丙烷(2.5g),加热回流过夜,带溶液冷却至室温,旋干,得2.1克黄色油状物,即化合物ii,直接用于下一步。将化合物ii(2.1g)溶于乙腈(20ml),再加入ksecn(1.04g),加热到100℃回流过夜,待反应液冷却至室温,抽滤,滤饼用少量乙腈洗涤,将母液旋干,得黄黑色油状物。粗品通过制备tlc纯化(dcm/meoh=5:1),得到白色浑浊油状物370mg,即化合物i-c,产率65%。
4.核磁共振1h nmr(400mhz,cdcl3):δ2.44-2.52(m,2h,ch2),3.25(s,6h,2ch2),
3.22-3.26(m,2h,ch2),3.59-3.61(m,4h,2ch2),4.09-4.13(m,2h,ch2).
[0005]
esi-ms:238.1([m+1]
+
).实施例4.化合物4的制备反应式如下:
[0006]
将n,n-二甲基乙醇胺(1g)溶于无水乙醇(20ml)中,再加入1,2-二溴乙烷,加热回流过夜,溶液冷却至室温,旋干,得2.0克黄色油状物,即化合物iii,直接用于下一步反应。将化合物iii(2.0g)溶于乙腈(20ml)中,再加入ksecn(1.05g),加热到100℃回流过夜,待反应液冷却至室温,抽滤,滤饼用少量乙腈洗涤,将母液旋干,得黄色油状物133mg,即化合物i-d,产率60%。
[0007]
核磁共振1h nmr(400mhz,cdcl3):δ2.40-2.45(m,2h,ch2),3.22(s,6h,2ch3),3.24-3.27(m,2h,ch2),3.45-3.51(m,2h,ch2),4.11-4.14(m,2h,ch2).
[0008]
esi-ms:224.1([m+1]
+
).生物活性实验一、实验目的建立脂多糖(lps)诱导的小鼠神经胶质细胞(bv2细胞)的炎症模型,研究式i化合物对一氧化氮(no)、白细胞介素il-1β和活性氧(ros)在内的神经毒性因子的影响,考察本发明式化合物的抗老年痴呆作用。二、实验方法1,对lps激活的bv2细胞产生no的调节作用bv2细胞以每孔3x104个细胞接种于96孔板中,每孔100μl。过夜约12h,待细胞贴壁后,设立对照组、lps组、给药组(3、10、30μg/ml)(本发明实施例的化合物i-a,i-b,i-c和i-d),每组设3个平行孔。弃掉原有培养基,对照组重新加入100μl dmem培养基,lps组和给药组加入1μg/ml lps(dmem培养基稀释)处理24h后,继续弃掉原有培养基,对照组再次重新加入100μl dmem培养基,lps加入1μm dmso的100μl dmem培养基,给药组加入不同浓度(3、10、30μg/ml)的药物处理24小时。采用griess法测定细胞上清no水平,检测原理为水溶液中no易被氧化为亚硝酸盐(no
2-),no
2-与griess试剂发生重氮化及偶联反应生成紫红色化合物,no水平与此产物成正比,可根据呈色深浅定量分析,间接评定细胞上清液中no含量。实验结果如图1所示,与对照组(control)比较,在分别加入本发明实施例的化合物(i-a,i-b,i-c和i-d)后,在3μm,10μm和30μm浓度下处理24小时,结果发现no水平均显著下调,且比对照组具有更好的效果。2.对lps激活的bv2细胞产生ros的调节作用bv2细胞以每孔105个细胞接种于6孔板,每孔1500μl。过夜约12h,待细胞贴壁后,设立对照组、lps组、给药组(3、30μg/ml)(本发明实施例的化合物i-a,i-b,i-c和i-d),每组设3
个平行孔。弃掉原有培养基,对照组重新加入100μl dmem培养基,lps组和给药组加入1μg/ml lps(dmem培养基稀释)处理24h后,继续弃掉原有培养基,对照组再次重新加入100μl dmem培养基,lps加入1μm dmso的100μl dmem培养基,给药组加入不同浓度(3、30μg/ml)的药物进行处理24小时。加入dcfh-da法探针培养0.5h,利用dcfh-da法测定ros浓度。dcfh-da法实验原理为:dcfh-da本身没有荧光,可以自由穿过细胞膜,进入细胞后,可以被细胞内的酯酶水解生成dcfh。而dcfh不能通透细胞膜,从而使探针很容易被标记到细胞内。在活性氧存在的条件下,dcfh被氧化生成荧光物质dcf,绿色荧光强度与细胞内活性氧水平成正比,检测dcf的荧光就可以知道细胞内活性氧的水平。在激发波长502nm,发射波长530nm附近,使用荧光酶标仪检测dcf荧光,从而测定细胞内活性氧水平。实验结果如图2所示,相较于对照组(control组),lps组ros水平显著升高,相近于阳性对照组舒林酸(rosup)。在分别加入本发明实施例的化合物(i-a,i-b,i-c和i-d)后,在3μm和30μm浓度下处理48小时,结果发现ros水平均显著下调,且比阳性对照组舒林酸具有更好的效果。3.对lps激活的bv2细胞产生il-1β的调节作用bv2细胞以每孔105个细胞接种于6孔板,每孔1500μl。过夜约12h,待细胞贴壁后,设立对照组、lps组、给药组(3、30μg/ml)(本发明实施例的化合物i-a,i-b,i-c和i-d),每组设3个平行孔。弃掉原有培养基,对照组重新加入100μl dmem培养基,lps组和给药组加入1μg/ml lps(dmem培养基稀释)处理24h后,继续弃掉原有培养基,对照组再次重新加入100μldmem培养基,lps加入1μm dmso的100μl dmem培养基,给药组加入不同浓度(3、30μg/ml)的药物处理24小时。收集细胞上清,1500r/min离心5min去除悬浮细胞,吸取细胞上清液准备进行elisa实验测定炎性因子il-1β。应用elisa双抗体夹心法检测,原理为以纯化抗体包被微孔板形成固相化抗体,待测样本中的抗原与包被板中抗体发生特异性反应,再与辣根过氧化物酶(hrp)标记抗体结合,hrp酶可催化底物tmb成蓝色,并在酸性条件下变为黄色,根据颜色深浅和样品中抗原呈正比进行定量分析。实验结果如图3所示,相较于对照组(control组),bv2细胞经lps(1μg/ml)处理24h后促炎因子il-1β的释放水平明显增加。与lps处理组相比,加入本发明实施例的给药组(i-a,i-b,i-c,i-d)的促炎因子il-1β的释放水平明显下降,随药物浓度增大而降低。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1