一种联苯四氮唑丙酮加合物及其制备方法与流程
[0001]
本发明属于药物化学技术领域,特别涉及一种奥美沙坦酯新杂质联苯四氮唑丙酮加合物(i)及其制备方法。
背景技术:
[0002]
奥美沙坦酯(olmesartan medoxomil)是由日本sankyo(三共公司)和美国forest laboratories共同开发的一种特异性血管紧张素ⅱ受体(atⅰ型)拮抗剂,2002年5月以商品名在美国上市,用于治疗原发性高血压,具有剂量小、起效快、降压作用更强而持久、不良反应的发生率低等明显优点。其化学名为2,3-二羟基-2-丁烯基-4-(1-羟基-1-甲基乙基)-2-丙基-1-[4-(2-1h-四唑-5-苯基)苄基]咪唑-5-羧酸酯环-2,3-碳酸酯,结构式如下式:
[0003][0004]
在奥美沙坦酯的合成工艺中,我们发现,正常工艺条件下很容易产生一个未知杂质,特别是在某些工艺参数控制不到位的情况下,部分异常批次生产的奥美沙坦酯产品中该杂质含量甚至高达0.4%,因此有必要调查清楚该杂质的产生来源,解析出它的结构,并合成该杂质对照品以供后续的质量研究及工艺改进工作。
技术实现要素:
[0005]
本发明的目的在于提供一种奥美沙坦酯新的未知杂质联苯四氮唑丙酮加合物(i)及其制备方法,用于支持该杂质的质量研究及分析方法开发工作,并用于支持关于该杂质控制的奥美沙坦酯工艺改进。
[0006]
本发明首先提供了一种奥美沙坦酯新的未知杂质,命名为联苯四氮唑丙酮加合物,其结构式如下所示:
[0007][0008]
通过高分辨质谱液质联用(lc-hrms)及核磁共振结构表征,确定了奥美沙坦酯工艺中的一个关键未知杂质为联苯四氮唑丙酮加合物(i),并且该杂质未收载于任何官方药
典及文献报道中。
[0009]
本发明更进一步地对联苯四氮唑丙酮加合物(i)的核磁共振氢谱和核磁共振碳谱进行了解析,该化合物编号如下所示:
[0010][0011]
表1为联苯四氮唑丙酮加合物(i)核磁共振氢谱解析:
[0012]
表1
[0013]
质子类型化学位移(ppm)峰型归属h编号质子数c-h2.07sh-142c-h2.73th-173c-h2.74th-152c-h6.96dh-9/132c-h7.12dh-10/122c-h7.51ddh-41c-h7.53th-51c-h7.59dh-31c-h7.64dh-61
[0014]
表2为联苯四氮唑丙酮加合物(i)核磁共振碳谱解析:
[0015]
表2
[0016]
[0017][0018]
本发明提供的联苯四氮唑丙酮加合物(i)经高效液相-高分辨质谱联用仪器(hplc-hrms)检测,esi正离子模式其[m+h]
+
精确分子质量为293.1398,[m+k]
+
精确分子质量为331.0957,匹配分子式为c
17
h
16
n4o,匹配误差为0.34ppm。
[0019]
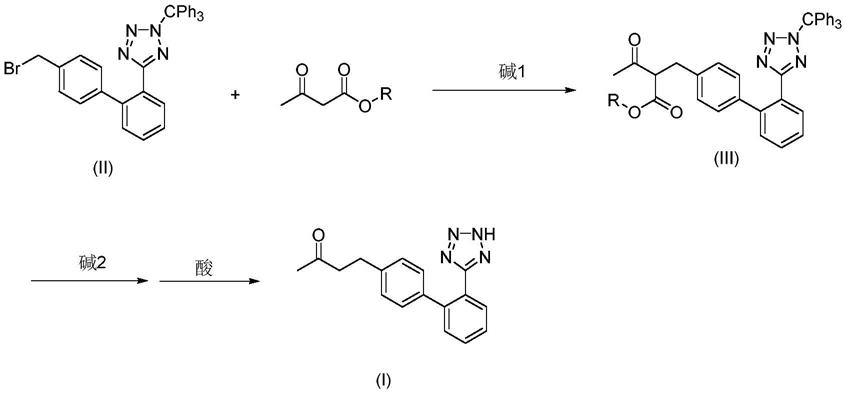
本发明的第二个方面是提供了一种联苯四氮唑丙酮加合物(i)的制备方法,合成反应式如下:
[0020][0021]
包括以下步骤:
[0022]
(1)4-溴甲基三苯基甲基联苯四氮唑(ii)与式iv化合物在碱1存在下,在有机溶剂中,发生缩合反应得到式iii化合物;
[0023]
(2)再向步骤1)得到的反应液中加入碱2进行水解反应;
[0024]
(3)在水解反应结束后加酸将反应体系调ph至0~5,再加热至20~60℃,得到联苯四氮唑丙酮加合物(i);
[0025]
其中式iv化合物中的r选自直链或支链的c1-c6烷基。
[0026]
优选地,所述步骤(1)中的碱1选自无机碱或有机碱的一种或多种;其中无机碱选自碳酸钾、碳酸氢钾、碳酸钠、碳酸氢钠、碳酸铵、碳酸氢铵、碳酸镁、氢氧化钠、氢氧化钾、氢氧化锂、氢氧化铯、氢氧化钙、氢化钠、氢化钾、氢化锂、氢化钙、氨基钠、磷酸钠或磷酸钾;更
进一步优选为碳酸钾和碳酸钠;有机碱选自四甲基碳酸铵、四甲基氢氧化铵、四丁基碳酸铵、三丁基苄基碳酸铵、叔丁醇钾、叔丁醇钠;更进一步优选为四甲基碳酸铵、四丁基碳酸铵、三丁基苄基碳酸铵。
[0027]
优选地,所述步骤(1)中式iv化合物、碱1与4-溴甲基三苯基甲基联苯四氮唑的摩尔比为1:1.5:1~10:10:1。
[0028]
优选地,所述步骤(1)的有机溶剂选自乙腈、丙酮、四氢呋喃和甲基叔丁基醚中的一种或多种。
[0029]
优选地,所述步骤(1)中反应温度为20~100℃,更进一步优选为60~80℃;反应时间为1~36小时;更进一步优选为12~18小时。
[0030]
优选地,所述步骤(2)中碱2选自无机碱或有机碱的一种或多种;其中无机碱选自氢氧化钠、氢氧化钾、氢氧化锂、氢氧化铯、氢氧化钙、氢化钠、氢化钾、氢化锂、氢化钙、氨基钠、碳酸钾、碳酸氢钾、碳酸钠、碳酸氢钠、磷酸钠或磷酸钾,优选为氢氧化钠、氢氧化钾、氢化钠、氢化钾、氢化锂及氢化钙;有机碱选自叔丁醇钾、叔丁醇钠、乙醇钠、乙醇钾、甲醇钠、甲醇钾,优选为甲醇钠、乙醇钠。
[0031]
优选地,所述步骤(2)中酸为无机酸或有机酸的一种或多种;其中无机酸选自盐酸、氢溴酸、硫酸、磷酸、高氯酸、高溴酸及硝酸,优选为硫酸、盐酸;有机酸选自甲酸、乙酸、甲磺酸、苯磺酸、对甲苯磺酸、三氟乙酸、三氯乙酸,优选为三氟乙酸、甲磺酸。
[0032]
优选地,所述步骤(2)的反应温度为10~65℃,优选为35~60℃;反应时间为0.5小时~24小时,优选为2小时~20小时;步骤3)的反应温度为10~65℃,优选为35~60℃;反应时间为0.5小时~3小时;步骤3)的ph范围优选为1~2。
[0033]
另一方面,本发明还提供了一种联苯四氮唑丙酮加合物(i)在改进奥美沙坦酯工艺及奥美沙坦酯质量研究中的用途。具体地可用于奥美沙坦酯粗品及成品分析过程中,以便对该杂质进行准确定位及外标法定量研究,具有很强的实际运用价值。同时,通过研究该杂质的产生机理,在奥美沙坦酯合成过程我们发现,由于反应物咪唑酯及三苯甲基溴代联苯四氮唑结构式相对复杂,在常规的溶剂中溶解度均不是太好,但我们通过溶剂筛选发现,丙酮对这些反应物及最终的产物均有良好的溶解性并且随着反应温度变化溶解度差异较大,因此丙酮非常适合当粗品工序的反应溶剂及结晶溶剂;同时我们进一步发现,不同的反应温度及反应时间下,不同批次的奥美沙坦酯粗品中联苯四氮唑丙酮加合物的含量会在0.45%到0.05%水平之间波动,因此合成出此联苯四氮唑丙酮加合物对照品可以更好地指导实际车间生产出含有联苯四氮唑丙酮加合物<0.1%的奥美沙坦酯成品,为奥美沙坦酯成品中联苯四氮唑丙酮加合物的杂质含量控制提供了杂质对照品,可以实现杂质的准确定量,具有较强的现实意义。
附图说明
[0034]
图1为联苯四氮唑丙酮加合物的核磁共振氢谱(400mhz);
[0035]
图2为联苯四氮唑丙酮加合物的核磁共振碳谱(400mhz);
[0036]
图3为联苯四氮唑丙酮加合物的高分辨质谱谱图。
[0037]
图4为奥美沙坦酯粗品中联苯四氮唑丙酮加合物杂质的hplc谱图。
具体实施方式
[0038]
下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。基于本发明中的实施例,本领域技术人员在没有作出创造性劳动前提下,任何对本发明的变换和变型都归属本发明的保护范围。
[0039]
联苯四氮唑丙酮加合物的检测色谱条件:
[0040]
色谱仪器:高效液相色谱仪配备紫外检测器
[0041]
色谱柱:waters symmetry c8 100
×
4.6mm,3.5μm
[0042]
缓冲液:2.04g磷酸二氢钾溶于1000ml水中,用浓磷酸调节ph值至3.4
[0043]
流动相a:缓冲液:乙腈=4:1(v/v)
[0044]
流动相b:缓冲液:乙腈=1:4(v/v)
[0045]
柱温:40℃
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
检测波长:250nm
[0046]
流速:1.0ml/min
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
进样量:10μl
[0047]
梯度表:
[0048][0049][0050]
稀释液:乙腈
[0051]
供试品溶液:称取25mg奥美沙坦酯粗品供试品,精密称定于25ml的容量瓶中,用稀释液溶解并稀释到刻度,混匀(供试品浓度:1.0mg/ml)。
[0052]
图4 hplc谱图结果显示在奥美沙坦酯粗品中联苯四氮唑丙酮加合物杂质的出峰时间为5.317min,峰面积比例为0.25%。
[0053]
按经标准品校正后的真实含量为0.25%
×
rrf(校正因子)=0.25%
×
0.72=0.18%。
[0054]
rrf(校正因子)计算过程:
[0055]
我们同时配置浓度均为10μg/ml奥美沙坦酯及联苯四氮唑丙酮加合物溶液,可见其紫外峰面积分别为7.85430及10.90884,由此我们计算rrf值如下:
[0056]
rrf=(uv
olmesartan medoxomil
/c
olmesartan medoxomil
)
÷
(uv
联苯四氮唑丙酮加成物
/c
联苯四氮唑丙酮加成物
)=(uv
olmesartan medoxomil
/u
联苯四氮唑丙酮加成物
)
÷
(c
olmesartan medoxomil
/
联苯四氮唑丙酮加成物
)=(7.85430/10.90884)
÷
(10μg/ml/10μg/ml)=0.72
[0057]
结果显示校正后的真实含量与表观含量有差异,使用联苯四氮唑丙酮加合物对照品能更真实地反映出奥美沙坦酯产品中的杂质水平。
[0058]
实施例1
[0059]
将1.0g 4-溴甲基三苯基甲基联苯四氮唑加入20ml乙腈中,接着加入1.25g碳酸钾及0.5g乙酰乙酸乙酯,加热升温至80℃反应10小时,冷却至室温,接着加入10ml 1mol/l的
氢氧化钠水溶液,加热至50℃继续搅拌反应18小时;得到的反应液冷却至室温,再用1mol/l盐酸溶液调节ph值至1.0,室温下继续搅拌10分钟,接着加热至50℃,搅拌反应3小时后,置于旋转蒸发仪下蒸去乙腈,接着再加入20ml二氯甲烷提取产生的化合物,分出有机层,置于旋转蒸发仪下蒸去二氯甲烷,得到的剩余物固体用柱层析方法[hp-silica正相硅胶,洗脱剂为二氯甲烷:甲醇=(20:1,v/v)]对目标产物进行分离,最终得到联苯四氮唑丙酮加合物0.37g,hplc纯度98.7%,产率70%。
[0060]
实施例2
[0061]
将1.0g 4-溴甲基三苯基甲基联苯四氮唑加入20ml丙酮中,接着加入1.1g碳酸钾及0.4g乙酰乙酸甲酯,加热升温至70℃反应12小时,冷却至60℃,接着加入15ml 1mol/l的氢氧化钠水溶液,继续搅拌反应18小时;得到的反应液冷却至室温,再用1mol/l盐酸溶液调节ph值至1.0,室温下继续搅拌10分钟,接着加热至50℃,搅拌反应3小时后,分出有机层,置于旋转蒸发仪下蒸去丙酮,接着再加入20ml二氯甲烷提取产生的化合物,置于旋转蒸发仪下蒸去二氯甲烷,得到的剩余物固体用柱层析方法[hp-silica正相硅胶,洗脱剂为二氯甲烷:甲醇=(15:1,v/v)]对目标产物进行分离,最终得到联苯四氮唑丙酮加合物0.38g,hplc纯度99.0%,产率72%。
[0062]
实施例3
[0063]
将1.0g 4-溴甲基三苯基甲基联苯四氮唑加入20ml乙腈中,接着加入1.0g碳酸钾及0.6g乙酰乙酸丙酯,加热升温至80℃反应10小时,冷却至室温,接着加入15ml 1mol/l的氢氧化钠水溶液,加热至50℃继续搅拌反应18小时;得到的反应液冷却至室温,再用1mol/l盐酸溶液调节ph值至1.2,室温下继续搅拌10分钟,接着加热至50℃,搅拌反应3小时后,置于旋转蒸发仪下蒸去乙腈,接着再加入20ml乙酸乙酯提取产生的化合物,分出有机层,置于旋转蒸发仪下蒸去二氯甲烷,得到的剩余物固体用柱层析方法[hp-silica正相硅胶,洗脱剂为二氯甲烷:甲醇=(20:1,v/v)]对目标产物进行分离,最终得到联苯四氮唑丙酮加合物0.36g,hplc纯度98.9%,产率68%。
[0064]
实施例4
[0065]
将1.0g 4-溴甲基三苯基甲基联苯四氮唑加入20ml乙腈中,接着加入1.2g碳酸钾及0.6g乙酰乙酸苯酯,加热升温至80℃反应10小时,冷却至室温,接着加入10ml 1mol/l的氢氧化钠水溶液,加热至50℃继续搅拌反应18小时;得到的反应液冷却至室温,再用1mol/l盐酸溶液调节ph值至1.2,室温下继续搅拌10分钟,接着加热至50℃,搅拌反应4小时后,置于旋转蒸发仪下蒸去乙腈,接着再加入20ml二氯甲烷提取产生的化合物,分出有机层,置于旋转蒸发仪下蒸去二氯甲烷,得到的剩余物固体用柱层析方法[hp-silica正相硅胶,洗脱剂为二氯甲烷:甲醇=(20:1,v/v)]对目标产物进行分离,最终得到联苯四氮唑丙酮加合物0.34g,hplc纯度99.2%,产率65%。
[0066]
实施例5
[0067]
将1.0g 4-溴甲基三苯基甲基联苯四氮唑加入20ml四氢呋喃中,接着加入1.0g碳酸钠及0.6g乙酰乙酸甲酯,加热升温至80℃反应10小时,冷却至室温,接着加入15ml1mol/l的氢氧化钠水溶液,加热至50℃继续搅拌反应18小时;得到的反应液冷却至室温,再用1mol/l盐酸溶液调节ph值至1.0,室温下继续搅拌10分钟,接着加热至50℃,搅拌反应3小时后,置于旋转蒸发仪下蒸去四氢呋喃,接着再加入20ml二氯甲烷提取产生的化合物,分出有
机层,置于旋转蒸发仪下蒸去二氯甲烷,得到的剩余物固体用柱层析方法[hp-silica正相硅胶,洗脱剂为二氯甲烷:甲醇=(15:1,v/v)]对目标产物进行分离,最终得到联苯四氮唑丙酮加合物0.37g,hplc纯度99.3%,产率71%。
[0068]
实施例6
[0069]
将1.0g 4-溴甲基三苯基甲基联苯四氮唑加入20ml甲基叔丁基醚中,接着加入1.25g碳酸钾及0.5g乙酰乙酸乙酯,加热升温至80℃反应10小时,冷却至室温,接着加入15ml1mol/l的氢氧化钾水溶液,加热至50℃继续搅拌反应18小时;得到的反应液冷却至室温,再用1mol/l硫酸溶液调节ph值至1.0,室温下继续搅拌10分钟,接着加热至50℃,搅拌反应2小时后,置于旋转蒸发仪下蒸去甲基叔丁基醚,接着再加入20ml乙酸乙酯提取产生的化合物,分出有机层,置于旋转蒸发仪下蒸去乙酸乙酯,得到的剩余物固体用柱层析方法[hp-silica正相硅胶,洗脱剂为二氯甲烷:甲醇=(15:1,v/v)]对目标产物进行分离,最终得到联苯四氮唑丙酮加合物0.38g,hplc纯度98.6%,产率72%。
[0070]
实施例7
[0071]
将20.0g 4-溴甲基三苯基甲基联苯四氮唑加入400ml乙腈中,接着加入18.0g碳酸钠及10g乙酰乙酸乙酯,加热升温至80℃反应10小时,冷却至室温,接着加入200ml 1mol/l的氢氧化钾水溶液,加热至50℃继续搅拌反应18小时;得到的反应液冷却至室温,再用1mol/l盐酸溶液调节ph值至1.0,室温下继续搅拌10分钟,接着加热至50℃,搅拌反应3小时后,置于旋转蒸发仪下蒸去乙腈,接着再加入350ml二氯甲烷提取产生的化合物,分出有机层,置于旋转蒸发仪下蒸去二氯甲烷,得到的剩余物再用二氯甲烷-甲醇混合溶液结晶,最终得到联苯四氮唑丙酮加合物6.82g,hplc纯度98.8%,产率65%。
[0072]
实施例8
[0073]
将20.0g 4-溴甲基三苯基甲基联苯四氮唑加入400ml丙酮中,接着加入22.0g碳酸钾及8g乙酰乙酸甲酯,加热升温至80℃反应10小时,冷却至室温,接着加入200ml 1mol/l的氢氧化钠水溶液,加热至50℃继续搅拌反应18小时;得到的反应液冷却至室温,再用1mol/l盐酸溶液调节ph值至1.0,室温下继续搅拌10分钟,接着加热至50℃,搅拌反应3小时后,置于旋转蒸发仪下蒸去丙酮,再加入400ml二氯甲烷提取产生的化合物,分出有机层,置于旋转蒸发仪下蒸去二氯甲烷,得到的剩余物再用二氯甲烷-甲醇混合溶液结晶,最终得到联苯四氮唑丙酮加合物7.76g,hplc纯度98.5%,产率74%。
[0074]
实施例9
[0075]
将20.0g 4-溴甲基三苯基甲基联苯四氮唑加入400ml乙腈中,接着加入42.7g四甲基碳酸铵及8.5g乙酰乙酸甲酯,加热升温至80℃反应10小时,冷却至室温,接着加入200ml 1mol/l的氢氧化钠水溶液,加热至45℃继续搅拌反应24小时;得到的反应液冷却至室温,再用1mol/l盐酸溶液调节ph值至1.0,室温下继续搅拌10分钟,接着加热至50℃,搅拌反应3小时后,置于旋转蒸发仪下蒸去乙腈,再加入400ml二氯甲烷提取产生的化合物,分出有机层,置于旋转蒸发仪下蒸去二氯甲烷,得到的剩余物再用二氯甲烷-甲醇混合溶液结晶,最终得到联苯四氮唑丙酮加合物7.55g,hplc纯度98.8%,产率72%。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1