微流控芯片与细胞筛选系统的制作方法
1.本实用新型涉及细胞筛选领域,尤其涉及一种微流控芯片与细胞筛选系统。
背景技术:
2.在各种生物检测场景中,需要利用细胞筛选装置从试样溶液中将目标细胞分离出来,以对目标细胞进行进一步的操作。其中的目标细胞可例如循环肿瘤细胞(circulating tumor cell,简称:ctc)。以ctc技术为代表的液体活检技术已经在肿瘤筛查、预后检测、药效评价等多方面开展应用。
3.现有的相关技术中,可采用微流控芯片实现细胞的筛选,具体的,可以从导入通道灌入试样溶液,试样溶液经过筛选部筛选过滤后,试样溶液中尺寸较小的非目标细胞可通过筛选部进入导出通道,而尺寸较大的目标细胞则被筛选部拦截,最终实现以ctc为例的目标细胞在微流控芯片中的富集。
4.然而,以ctc为例的目标细胞通常也具有一定形变弹性,其形变后可能挤过筛选部而进入导出通道,造成目标细胞易于漏出、截留率不够高的问题。
技术实现要素:
5.本实用新型提供一种微流控芯片与细胞筛选系统,以解决目标细胞易于漏出、截留率不够高的问题。
6.根据本实用新型的第一方面,提供了一种微流控芯片,包括:芯片主体,所述芯片主体内设有导入通道、导出通道,以及位于所述导入通道和所述导出通道之间的筛选部;
7.所述筛选部包括多个筛选单元,每个所述筛选单元包括一个容置腔和分别与所述容置腔连通的多个筛选通道;
8.所述导入通道与所述容置腔连通,所述容置腔与所述筛选通道入口端连通,所述筛选通道的出口段与所述导出通道连通;所述容置腔的宽度大于目标细胞的直径,所述筛选通道的宽度小于所述目标细胞的直径。
9.可选的,所述多个筛选通道分别具有不同的导流方向。
10.可选的,每个所述容置腔对应的所述筛选通道的数量为2。
11.可选的,所述多个筛选通道中至少一个筛选通道为第一通道;
12.在所述导出通道用于与所述第一通道连通的一段中,所述导出通道的导流方向与所述第一通道的导流方向之夹角为锐角。
13.可选的,所述筛选部设置于所述导入通道沿参考方向的一侧或两侧,其中,所述参考方向垂直于所述导入通道的导流方向。
14.可选的,在所述导入通道用于与所述容置腔连通的一段中,所述导入通道的导流方向与所述容置腔的导流方向之夹角为锐角,且所述容置腔的导流方向与对应的所述多个筛选通道之一的导流方向一致。
15.可选的,所述筛选通道的出口端形成有缓冲凹槽,以垂直于所述筛选通道的中心
线的平面为投影面,所述缓冲凹槽在所述投影面的投影区域覆盖并超出所述筛选通道在所述投影面的投影区域。
16.可选的,所述多个筛选单元包括多个第一筛选单元与多个第二筛选单元,所述多个第一筛选单元与所述多个第二筛选单元分别设于所述导入通道相对的两侧,其中,所述导入通道中的液体能够分别进入其两侧的第一筛选单元与第二筛选单元;
17.所述第一筛选单元中容置腔与导入通道的连通口为第一连通口,所述第二筛选单元中容置腔与导入通道的连通口为第二连通口;所述第一连通口与所述第二连通口在所述导入通道的中心线的方向错位分布。
18.可选的,所述筛选部还包括筛选间隙,所述筛选间隙位于所述筛选单元沿厚度方向的一侧,所述筛选间隙连接所述导入通道与所述导出通道,所述筛选间隙沿所述厚度方向的间隙距离小于或等于对应筛选通道的宽度。
19.根据本实用新型的第二方面,提供了一种细胞筛选系统,包括进样泵、废液收集装置以及如第一方面及其可选方案涉及的微流控芯片;
20.所述微流控芯片的导入通道与所述进样泵连接,所述微流控芯片的导出通道与所述废液收集装置连接。
21.本实用新型提供的微流控芯片与细胞筛选系统中,由于多个筛选通道分别与容置腔连通,进入容置腔的液体将分流至多个筛选通道,不同筛选通道的流体(即试样溶液)流动均会对容置腔中的目标细胞产生驱动作用,且不同筛选通道的驱动作用是将目标细胞驱动至不同筛选通道的,此时,由于一个目标细胞一次仅可能挤入一个筛选通道,任意之一筛选通道的驱动作用均会对其他筛选通道的驱动作用产生阻碍,相较而言,在将目标细胞引导至同一筛选通道的方案中,流体所产生的驱动作用不会受到该阻碍,可见,本实用新型中,通过多个筛选通道,可阻碍容置腔中的目标细胞轻易进入任意之一筛选通道,有效提高了筛选通道对目标细胞的截留能力,从而有助于降低目标细胞挤入筛选通道的可能性,提高截留率。
22.同时,相较于仅采用一个筛选通道的方案,多个筛选通道的分流可提升试样溶液的流通截面积,从而提高试样溶液流速的上限,进而,本实用新型可适用于更快的液体泵入速度,有助于提高检测效率,降低检测时间。
附图说明
23.为了更清楚地说明本实用新型实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本实用新型的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
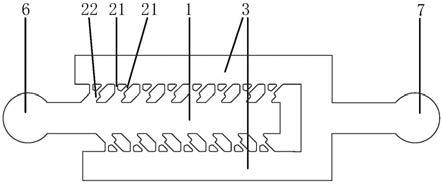
24.图1是本实用新型一实施例中微流控芯片的内部构造示意图一;
25.图2是本实用新型一实施例中主体层与封装层的结构示意图;
26.图3是图2中a
‑
a剖面、b
‑
b剖面剖开后主体层与封装层的结构示意图;
27.图4是本实用新型一实施例中微流控芯片的内部构造示意图一;
28.图5是本实用新型一实施例中主体层与封装层的结构示意图;
29.图6是图5中c
‑
c剖面、d
‑
d剖面剖开后主体层与封装层的结构示意图;
30.图7是本实用新型一实施例中微流控芯片的内部构造示意图二;
31.图8a与图8b是图7中e部分的放大示意图;
32.图9是本实用新型一实施例中微流控芯片的内部构造示意图三;
33.图10a与图10b是图9中f部分的放大示意图;
34.图11是本实用新型一实施例中微流控芯片的内部构造示意图四;
35.图12是本实用新型一实施例中微流控芯片的内部构造示意图五;
36.图13是本实用新型一实施例中微流控芯片的内部构造示意图六;
37.图14是本实用新型一实施例中微流控芯片的内部构造示意图七;
38.图15是本实用新型一实施例中微流控芯片的内部构造示意图八;
39.图16是本实用新型一实施例中微流控芯片的内部构造示意图九;
40.图17是本实用新型一实施例中微流控芯片的内部构造示意图十;
41.图18是本实用新型一实施例中微流控芯片的内部构造示意图十一。
42.附图标记说明:
[0043]1‑
导入通道;2
‑
筛选部;21
‑
筛选通道;22
‑
容置腔;221
‑
第一连通口;222
‑
第二连通口;223、224、225、226
‑
连通口;23
‑
缓冲凹槽;24
‑
凸起限位块;25
‑
筛选间隙;26
‑
间隙隔断部;3
‑
导出通道;4
‑
封装层;5
‑
主体层;6
‑
芯片进口;7
‑
芯片出口;8
‑
分流管道组件;9
‑
汇流管道组件。
具体实施方式
[0044]
下面将结合本实用新型实施例中的附图,对本实用新型实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本实用新型一部分实施例,而不是全部的实施例。基于本实用新型中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本实用新型保护的范围。
[0045]
本实用新型的说明书和权利要求书及上述附图中的术语“第一”、“第二”、“第三”“第四”等(如果存在)是用于区别类似的对象,而不必用于描述特定的顺序或先后次序。应该理解这样使用的数据在适当情况下可以互换,以便这里描述的本实用新型的实施例能够以除了在这里图示或描述的那些以外的顺序实施。此外,术语“包括”和“具有”以及他们的任何变形,意图在于覆盖不排他的包含,例如,包含了一系列步骤或单元的过程、方法、系统、产品或设备不必限于清楚地列出的那些步骤或单元,而是可包括没有清楚地列出的或对于这些过程、方法、产品或设备固有的其它步骤或单元。
[0046]
下面以具体地实施例对本实用新型的技术方案进行详细说明。下面这几个具体的实施例可以相互结合,对于相同或相似的概念或过程可能在某些实施例不再赘述。
[0047]
为了分离试样溶液中的目标细胞以便于后续观测或者检验,本实施例提供一种微流控芯片,微流控芯片的材质可以为透明材料,以便用于后续对目标细胞进行识别。
[0048]
请参考图1至图6,微流控芯片,包括:芯片主体,所述芯片主体内设有导入通道1、导出通道3与位于所述导入通道1和所述导出通道3之间的筛选部2。
[0049]
其中的筛选部,可理解为能够流通液体,从而对液体中的目标细胞进行筛选截留的任意结构,其中可以包括多个筛选单元,对应的,筛选部可理解为多个筛选单元阵列排布(例如沿单个方向排布)而形成的筛选单元的阵列。
[0050]
本实用新型实施例中,每个所述筛选单元包括一个容置腔22和分别与所述容置腔连通的多个筛选通道21。所述导入通道1与所述容置腔22连通,所述容置腔22与所述筛选通道21入口端连通,所述筛选通道21的出口段与所述导出通道3连通;所述容置腔22的宽度大于目标细胞的直径,所述筛选通道21的宽度小于所述目标细胞的直径。
[0051]
其中,由于多个筛选通道分别与容置腔连通,进入容置腔的液体将分流至多个筛选通道,不同筛选通道的流体(即试样溶液)流动均会对容置腔中的目标细胞产生驱动作用,且不同筛选通道的驱动作用是将目标细胞驱动至不同筛选通道的,此时,由于一个目标细胞一次仅可能挤入一个筛选通道,任意之一筛选通道的驱动作用均会对其他筛选通道的驱动作用产生阻碍,相较而言,在将目标细胞引导至同一筛选通道的方案中,流体所产生的驱动作用不会受到该阻碍,可见,本实用新型实施例中,通过多个筛选通道,可阻碍容置腔中的目标细胞轻易进入任意之一筛选通道,有效提高了筛选通道对目标细胞的截留能力,从而有助于降低目标细胞挤入筛选通道的可能性,提高截留率。
[0052]
同时,相较于仅采用一个筛选通道的方案,多个筛选通道的分流可提升试样溶液的流通截面积,从而提高试样溶液流速的上限,进而,本实用新型实施例可适用于更快的液体泵入速度,有助于提高检测效率,降低检测时间。
[0053]
在图示的微流控芯片中,导入通道1的中心线整体呈直线,在其他举例中,导入通道1的中心线的部分或全部也可以呈曲线,对应的,本实用新型实施例所适用的导入通道1的形状可以是呈直线的,也可以是呈非直线的,不论采用何种形状,均不脱离本实用新型实施例的范围。
[0054]
其中筛选通道21的数量可以为任意数量的,例如可以为图1至图3所示的两个,也可以为图4至图6所示的三个,还可以为四个以上,不论采用何种数量,均不脱离本实用新型实施例的范围。
[0055]
其中一种实施方式中,所述多个筛选通道分别具有不同的导流方向。其他部分举例中,所述多个筛选通道中两个或多个筛选通道的导流方向也可以是相同(或可理解为平行)的。
[0056]
其中筛选通道的导流方向,可理解为:试样溶液在筛选通道引导下的流向,也可理解为沿筛选通道中心线,且自导入通道至导出通道的方向,由于筛选通道通常是不发生弯曲的,故而,筛选通道的导流方向还可理解为;沿筛选通道两端中心的连线,且自导入通道至导出通道的方向。
[0057]
以图8b为例,其中的导流方向d13与导流方向d15即为对应筛选通道的导流方向,以图10b为例,其中的导流方向d23、导流方向d24与导流方向d25即为对应筛选通道的导流方向。
[0058]
此外,筛选通道的形状并不限于图中所示的长条形的,还可能是呈三角形或其他规则或不规则形状。不论采用何种形状,均不脱离本实用新型实施例的范围
[0059]
通过不同导流方向的筛选通道,可使得不同方向流动的流体(即试样溶液)对容置腔中的目标细胞产生不同方向、角度的驱动作用,进一步提高了单个筛选通道的驱动作用对其他筛选通道驱动作用的阻碍强度,从而进一步提高了筛选单元对目标细胞的截留能力,从而有助于进一步降低目标细胞挤入筛选通道的可能性,提高截留率。
[0060]
其中一种实施方式中,请参考图1至图6,所述筛选部设置于所述导入通道沿参考
方向(即图1、图4中自上而下的方向或自下而上的方向)的两侧,其中,所述参考方向垂直于所述导入通道的导流方向。部分未图示的实施方式中,所述筛选部也可仅设置于所述导入通道沿参考方向的一侧。
[0061]
其中一种实施方式中,请参考图1至图6、图7、图8a、图8b、图9、图10a与图10b,在所述导入通道1用于与所述容置腔22连通的一段中,所述导入通道1的导流方向与所述容置腔22的导流方向之夹角为锐角,且所述容置腔22的导流方向与对应的所述多个筛选通道21之一的导流方向一致。
[0062]
其中导入通道的导流方向,可理解为:试样溶液在导入通道引导下的整体流向,也可理解为沿导入通道中心线,且远离导入通道入口的方向。以图8b与图10b为例,其中的导流方向d11与导流方向d21即为导入通道的导流方向。
[0063]
其中容置腔的导流方向,可理解为试样溶液在容置腔引导下的整体流向,也可理解为沿容置腔的内壁,且远离导入通道的方向。以图8b与图10b为例,其中的导流方向d12与导流方向d22即为容置腔22的导流方向。
[0064]
具体举例中,容置腔22的导流方向与导入通道1的导流方向的夹角可例如为45度,例如图8b所示的容置腔22的导流方向d12与筛选通道的导流方向d15相同,且该导流方向d12与导入通道1的导流方向的夹角为45度;再例如图10b所示的容置腔22的导流方向d22与筛选通道的导流方向d25相同,且该导流方向d22与导入通道1的导流方向d21的夹角为45度。在其他举例中,也可选用其他锐角夹角。
[0065]
以上方案中,通过锐角夹角的设计,可避免试剂溶液离开导入通道1进入容置腔22时发生较大转向,使得细胞易于到达容置腔,从而更易于被截留。
[0066]
其中一种实施方式中,请参考图1至图6、图7、图8a、图8b、图9、图10a与图10b,所述多个筛选通道中至少一个筛选通道为第一通道;
[0067]
在所述导出通道用于与所述第一通道连通的一段中,所述导出通道的导流方向与所述第一通道的导流方向之夹角为锐角;其中的第一通道可例如图8b所示导流方向d15的筛选通道,也可例如图10b所示导流方向d25的筛选通道。
[0068]
通过以上配置,可减小筛选通道送出的试样溶液与导出通道中流通的试样溶液之间形成相互阻碍的作用力,以及不同筛选通道间送出液体之间相互阻碍的作用力,导出通道中试样溶液的流动可带走筛选通道出来的试样溶液,进而,该方案可有效提高流速。
[0069]
反之,如果筛选通道的导流方向与导出通道的导流方向大于90度,会形成逆向冲击,从而影响流速,不利于筛选通道内试样溶液流出,进一步的,导出通道中试样溶液易对容置腔中捕获的目标细胞(例如ctc细胞)造成反向冲击,导致目标细胞脱离容置腔。
[0070]
此外,一种举例中,针对于同一多通道筛选单元中任意的第一筛选通道与第二筛选通道,且所述第一筛选通道的出口端与所述第二筛选通道的出口端沿所述导出通道的导流方向依次分布,所述第一筛选通道的导流方向与导出通道的导流方向的夹角大于所述第二筛选通道的导流方向与导出通道的导流方向的夹角。
[0071]
以图8b为例,其中导流方向d13的筛选通道即为第一筛选通道,导流方向d15的筛选通道即为第二筛选通道;再以图10b为例,若以导流方向d23的筛选通道为第一筛选通道,则导流方向d24与导流方向d25的筛选通道均可作为第二筛选通道,若以导流方向d24的筛选通道为第一筛选通道,则导流方向d25的筛选通道可作为第二筛选通道。
[0072]
以上方案中,可避免沿导出通道3导流方向上靠后筛选通道的出液对靠前筛选通道的出液造成逆向冲刷,进一步保障了试样溶液的流速。
[0073]
其中一种实施方式中,请参考图2、图3与图5、图6,所述芯片主体包括主体层5与封装层4,所述筛选部2、所述导入通道1与所述导出通道3均设于所述主体层5。
[0074]
其中的封装层4可以是上封层也可以是下封层,封装层4具体可以是以贴膜工艺实现的膜层,也可以是以注塑工艺实现的键合盖板。任意工艺和材质而形成的封装层4均不脱离本实用新型实施例的范围。
[0075]
其中的主体层5中,所述筛选部2、所述导入通道1与所述导出通道3均可理解为在主体层5所形成的图案,例如可以是用凹凸形状相反的模仁制作形成的。任意工艺和材质而形成的主体层5均不脱离本实用新型实施例的范围。
[0076]
其中一种实施方式中,请参考图7、图8a、图9与图10a,所述筛选通道21的出口端形成有缓冲凹槽23,以垂直于所述筛选通道的中心线的平面为投影面,所述缓冲凹槽在所述投影面的投影区域覆盖并超出所述筛选通道在所述投影面的投影区域。以图8b为例,由于筛选通道的中心线即是沿筛选通道21的导流方向的,进而,以上所涉及的投影面也可理解为垂直于导流方向d15的平面。
[0077]
其中的缓冲凹槽23,可理解为下凹于导出通道3侧壁且处于筛选通道21端面处的凹槽,且该缓冲凹槽23的宽度大于筛选通道21的宽度。其中,缓冲凹槽23与筛选通道21的宽度(即沿宽度方向的尺寸),可理解为:对应的宽度方向同时垂直于对应筛选通道21的导流方向与所述筛选部2的厚度方向,该厚度方向既是筛选通道21的厚度方向,也是筛选单元的厚度方向,可理解为垂直于图2、图5所示的本体层5的连接封装层的表面,也可理解为同时垂直于所述筛选通道21的导流方向与所述导入通道1的中心线的方向,还可理解为芯片主体的厚度方向(即图2、图3、图5、图6中所示的上下方向)。
[0078]
具体举例中,该缓冲凹槽23的厚度(即厚度方向的尺寸)可以与筛选通道21的厚度相同或相近,缓冲凹槽23的导流方向可以与对应筛选通道21相同。
[0079]
以上方案中,由于筛选通道21和/或容置腔22被配置为倾斜后,通道长度变长了,这导致试样溶液中细胞流经狭窄且长的筛选通道时容易发生拥堵的问题,影响流速。因此,通过增加宽度较大的缓冲凹槽,可有利于缩短筛选通道长度,避免非目标细胞在过长的筛选通道中堵塞淤积,提高流速、提高检测效率。同时,通过缓冲凹槽23,也可以缓冲导出通道中液体的反冲压力,避免筛选通道处的淤积。
[0080]
其中一种实施方式中,请参考图11与图12,所述多个筛选单元包括多个第一筛选单元与多个第二筛选单元,所述多个第一筛选单元与所述多个第二筛选单元分别设于所述导入通道相对的两侧,其中,所述导入通道中的液体(即试样溶液)能够分别进入其两侧的第一筛选单元与第二筛选单元(例如图11与图12所示的上下两侧的筛选单元);
[0081]
所述第一筛选单元中容置腔与导入通道的连通口为第一连通口221,所述第二筛选单元中容置腔与导入通道的连通口为第二连通口222;所述第一连通口与所述第二连通口在所述导入通道的中心线的方向错位分布。
[0082]
同时,其中的多个第一筛选单元的多个第一连通口221是沿导入通道1的中心线依次分布的。进而,其中的错位,可理解为:除了首个或末尾一个第一连通口221,针对于任意一个第一连通口221,其关于导入通道1中心线对称的部位处于相邻的两个第二连通口之
间。
[0083]
另部分举例中,各第一连通口与各第二连通口可以是关于导入通道1的中心线对称分布的。
[0084]
相比于现有技术中对称设置或单侧设置筛选部的方案,以图11、图12为例的方案中,通过错位分布,可错开分流位置,导入通道全程可实现分流,避免了对称结构中间隔出现两侧相对壁的问题,提高了分流效率,同时,通过均衡的分压,最终可提高对目标细胞的截留率,减少了漏出的目标细胞(例如ctc)。
[0085]
另外,在管道中,流体的流动通常为层流,靠近管道中心的流体的流速更大,靠近管壁的流体的流速更小,左右两侧筛选部中筛选通道从侧向分流提供了侧向流速,因此,通过设置非对称通道可以降低流体中细胞错过两侧容置腔的概率。
[0086]
其中一种实施方式中,请参考图13与图14,同一筛选部中,至少部分容置腔22的连通口的宽度是不同的,其中连通口的宽度指对应容置腔22的入口端的沿所述导入通道1中心线方向的尺寸(即图13与图14中左右方向的尺寸),例如连通口223的宽度l1、连通口224的宽度l2、连通口225的宽度l3与连通口226的宽度l4,其中,宽度l1与宽度l2是不同的宽度,宽度l3与宽度l4是不同的宽度。
[0087]
进一步的,在同一筛选部中,连通口宽度的不同尺寸可以仅具有两种不同尺寸,也可具有三种或三种以上不同尺寸。
[0088]
进一步举例中,连通口宽度的尺寸变化可例如是沿导入通道1的导流方向自小变大而渐变的,也可以是先变大再变小的(也可理解为入口宽度被配置为两端位置的连通口宽度较窄,中间位置的连通口宽度较款)的变化趋势。
[0089]
以上方案中,由于目标细胞的大小在一定范围内也会存在差异,例如ctc大小在10
‑
20μm的范围内也存在差异,通过设置多种尺寸的入口宽度,有利于捕获不同尺寸的目标细胞。
[0090]
同时,经试验分析,目标细胞(例如ctc)主要集中卡在筛选部的沿导入通道1导流方向的开头和尾部,那么为了避免多个细胞在同一个容置腔中堆叠,将宽度配置为两端位置的入口宽度较窄,中间位置的入口宽度较宽,可以提高单个容置腔的单个细胞捕获效果。
[0091]
此外,其中容置腔、导流通道的截面形状可以是任意变化的,本领域任意已有或改进的变化均不脱离本实用新型实施例的范围。
[0092]
其中一种实施方式中,请参考图13至图15,所述筛选部2还包括筛选间隙25,所述筛选间隙25位于所述筛选单元(例如筛选通道21、容置腔22)沿厚度方向的一侧,所述筛选间隙25连接所述导入通道1与所述导出通道3,所述筛选间隙25沿厚度方向的间隙距离小于或等于对应筛选通道21的宽度。其中,筛选缝隙25可以设置在顶部,也可以设置在底部。
[0093]
现有相关技术中,导入通道1中的试样溶液只能通过筛选通道21进入导出通道3,但在以上方案中,在筛选部的一侧还增加了筛选间隙25,进而,导入通道1中的试样多了一条流入导出通道的路径,从而大大提高了芯片中试样溶液的流速,缩短检测时长。
[0094]
具体实施过程中,请参考图16,所述筛选间隙包括沿所述导入通道的中心线方向(即导入通道的导流方向)分布的至少两个间隙段,相邻的两个间隙段之间通过间隙隔断部26隔断,每个间隙段连接至少一个筛选通道21。
[0095]
在不采用隔断部的情况下,图15所示结构可能发生形变(制造或使用过程中而产
生的形变),进而,有可能导致筛选间隙变大漏出目标细胞,对应的,在以上方案中,通过间隙隔断部26的隔断,可通过支撑作用避免或降低形变的发生可能性,避免因此而导致的目标细胞漏出。
[0096]
进一步可选方案中,请参考图17,所述筛选间隙25中连接所述筛选通道的部分为第一间隙部分(即图15所示的对应筛选通道21下侧的间隙部分),所述筛选间隙中未连接所述筛选通道的部分为第二间隙部分,所述第一间隙部分的间隙距离小于所述第二间隙部分的间隙距离。为了实现该间隙距离,由于筛选部2设于主体层5,所述筛选间隙25可设于所述封装层4,所述封装层4还设有用于形成所述第一间隙部分的凸起限位块24。
[0097]
进一步举例中,其中的凸起限位块24的厚度(即沿筛选单元厚度方向的尺寸)可以例如为该间隙距离的一半。
[0098]
通过以上方案,通过凸起限位块24的设置,可避免在筛选间隙25于筛选通道21的连通区域形成大口径,从而避免或降低细胞漏出的可能性。此外,当筛选间隙25大于筛选通道宽度的一半且小于筛选通道的宽度时,凸起限位块24避免或降低细胞漏出可能性的作用将更为明显。
[0099]
进一步可选方案中,筛选间隙25的厚度方向的尺寸可以设置为比筛选通道21宽度小(例如小于8um),进一步的,筛选间隙25的厚度方向的尺寸可以优选为小于筛选通道21宽度的一半(例如小于4μm),通过该方案,也可避免在筛选通道和间隙连通区域出现大口径,从而避免或降低细胞漏出的可能性。
[0100]
其中一种实施方式中,请参考图18,所述芯片结构中还设有分流管道组件8,所述导入通道1的数量为多个;所述分流管道组件8的入口端连接芯片进口6;所述分流管道组件分别连接多个导入通道1的入口端;所述分流管道组件8用于通过至少一次分流将所述芯片进口10进入的液体送至所述多个导入通道1的入口端。
[0101]
其中一种实施方式中,请参考图18,所述芯片结构中还设有汇流管道组件9,所述导出通道3的数量为多个;所述汇流管道组件9的出口端连接芯片出口7;所述汇流管道组件9分别连接多个导出通道3的出口端;所述汇流管道组件9用于通过至少一次汇流将所述导出通道3送出的液体送至所述芯片出口7。
[0102]
以上方案中,通过分流与汇流,可提高各入口/出口管道的流体均匀性、压力均衡性,避免某个管道压力过大导致爆裂。
[0103]
进一步的,每级分流(即每次分流)都设置为1分2,且管道尺寸减半,其作用是为了均衡各入口通道的流量。提高均匀性,提高芯片进口初始速度。
[0104]
以ctc作为目标细胞为例,携带ctc的血液样本可流入导入通道,尺寸较小的普通正常血细胞从两侧或一侧的筛选流入导出通道,其中携带的ctc无法通过狭窄的筛选通道而被截留在筛选单元的容置腔中。
[0105]
试样溶液可以从芯片进口进入微流控芯片,由入液分流管道均匀分流至各入口通道。其中导入通道一端开口,用于导入试样溶液,另一端闭合,导入通道通过筛选部中的容置腔、筛选通道与导出通道连通,且筛选通道的宽度小于ctc的最小宽度,例如可优选为8μm,容置腔的宽度大于8μm,通常是单个ctc的直径。试样溶液中液体和尺寸较小的血细胞从导入通道“挤进”或“漏进”导出通道,尺寸较大的目标细胞(ctc)则因无法通过筛选通道,而被截留于导入通道和筛选部的容置器中。导出通道的血液样本经过出液分流管道汇聚于出
样口(即芯片出口),从而排出。
[0106]
本实用新型实施例还提供了一种细胞筛选系统,包括进样泵、废液收集装置以及以上可选方案所涉及的微流控芯片;
[0107]
所述微流控芯片的导入通道与所述进样泵连接,所述微流控芯片的导出通道与所述废液收集装置连接。
[0108]
可选的,所述的系统,还包括光源、图像采集装置和数据处理装置;
[0109]
所述光源用于照射所述微流控芯片;
[0110]
所述图像采集装置信号连接所述数据处理装置,所述图像采集装置用于在所述光源照射所述微流控芯片时采集所述微流控芯片的图像并传输给所述数据处理装置;
[0111]
所述数据处理装置根据所述图像进行所述目标细胞的识别。
[0112]
最后应说明的是:以上各实施例仅用以说明本实用新型的技术方案,而非对其限制;尽管参照前述各实施例对本实用新型进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本实用新型各实施例技术方案的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1