作为除草剂的吡唑取代的吡咯烷酮的制作方法
1.本发明涉及某些吡唑取代的吡咯烷酮,其n
‑
氧化物、盐和组合物,以及其用于控制不希望植被的方法。
背景技术:
2.控制不希望植被在实现高作物效率中是极其重要的。实现对杂草生长的选择性控制,尤其是在此类有用的作物尤其如稻、大豆、甜菜、玉蜀黍、马铃薯、小麦、大麦、番茄和种植作物中,是非常希望的。在此类有用的作物中的未加抑制的杂草生长可造成产量的显著下降,并且从而导致消费者的成本增加。在非作物区域中对不希望植被的控制也是重要的。为了这些目的,许多产品是可商购的,但持续需要更有效、较低成本、较低毒性、对环境更安全或具有不同的作用位点的新型化合物。
3.wo 2015/084796和wo 2016/196593披露了某些取代的环酰胺及其作为除草剂的用途。本发明的吡唑取代的吡咯烷酮未在这些出版物中披露。
技术实现要素:
4.本发明涉及一种具有式1的化合物,包括其所有立体异构体、n
‑
氧化物和盐,含有它们的农业组合物,以及它们作为除草剂的用途:
[0005][0006]
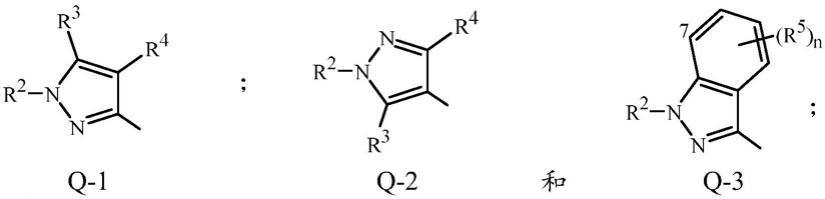
其中q选自由以下组成的组:
[0007][0008]
r1是h、c1‑
c6烷基、c1‑
c6卤代烷基、c3‑
c7环烷基或c4‑
c8环烷基烷基;
[0009]
r2是c1‑
c6烷基或c1‑
c6卤代烷基;
[0010]
r3是卤素、c1‑
c6烷基、c1‑
c6卤代烷基、c1‑
c6烷氧基或c1‑
c卤代烷氧基;
[0011]
y是o或s;
[0012]
r4是h、卤素、c1‑
c4烷基或c1‑
c4卤代烷基;
[0013]
r5是卤素、c1‑
c4烷基或c1‑
c4卤代烷基;
[0014]
n是1、2、3或4;
[0015]
r6是h、卤素、羟基、c1‑
c4烷氧基、c1‑
c4卤代烷基或c1‑
c4烷基;
[0016]
w是苯基或吡啶基,每个苯基或吡啶基任选地被至多5个r9取代;并且
[0017]
每个r9独立地是卤素、氰基、硝基、c1‑
c4烷基、c1‑
c4卤代烷基、c2‑
c4烯基、c2‑
c4卤代烯基、c2‑
c4炔基、c2‑
c4卤代炔基、c1‑
c4硝基烷基、c2‑
c4硝基烯基、c2‑
c4烷氧基烷基、c2‑
c4卤代烷氧基烷基、c3‑
c4环烷基、c3‑
c4卤代环烷基、环丙基甲基、甲基环丙基、c1‑
c4烷氧基、c1‑
c4卤代烷氧基、c2‑
c4烯氧基、c2‑
c4卤代烯氧基、c3‑
c4炔氧基、c3‑
c4卤代炔氧基、c3‑
c4环烷氧基、c1‑
c4烷硫基、c1‑
c4卤代烷硫基、c1‑
c4烷基亚磺酰基、c1‑
c4卤代烷基亚磺酰基、c1‑
c4烷基磺酰基、c1‑
c4卤代烷基磺酰基、羟基、甲酰基、c2‑
c4烷基羰基、c2‑
c4烷基羰基氧基、c1‑
c4烷基磺酰基氧基、c1‑
c4卤代烷基磺酰基氧基、氨基、c1‑
c4烷基氨基、c2‑
c4二烷基氨基、甲酰氨基、c2‑
c4烷基羰基氨基、
‑
sf5、
‑
scn、c3‑
c4三烷基甲硅烷基、三甲基甲硅烷基甲基或三甲基甲硅烷基甲氧基;
[0018]
前提是该化合物不是具有式1的化合物,其中q是q
‑
1;r1是h;r2是ch3;r3是c(ch3)3;r4是h;r6是h;y是o,w是在2
‑
位处被r9取代的苯基;并且r9是f。
[0019]
更具体地,本发明涉及一种具有式1的化合物(包括所有立体异构体)、其n
‑
氧化物或盐。本发明还涉及一种除草组合物,该除草组合物包含本发明的化合物(即以除草有效量)和至少一种选自由表面活性剂、固体稀释剂和液体稀释剂组成的组的组分。本发明还涉及一种用于控制不希望植被的生长的方法,该方法包括使植被或其环境与除草有效量的本发明的化合物(例如,作为本文所述的组合物)接触。
[0020]
本发明还包括一种除草混合物,该除草混合物包含(a)选自式1、其n
‑
氧化物和盐的化合物,以及(b)至少一种选自如下所述的(b1)至(b16)、以及(b1)至(b16)的化合物的盐的附加活性成分。
具体实施方式
[0021]
如本文所用,术语“包括”、“包含”、“内含”、“涵盖”、“具有”、“含有”、“包容”、“容纳”、“特征在于”或其任何其他变型旨在覆盖非排他性的包括,以任何明确指明的限定为条件。例如,包含一系列元素的组合物、混合物、工艺或方法不必仅限于那些元素,而是可以包括未明确列出的其它元素,或此类组合物、混合物、工艺或方法的其它固有元素。
[0022]
连接短语“由
……
组成”排除任何未指出的元素、步骤或成分。如果在权利要求中,则此类短语将使权利要求为封闭式,使其不包含除那些叙述的材料以外的材料,但与其相关的常规杂质除外。当短语“由
……
组成”出现在权利要求的特征部分,而非紧接前序部分时,则它仅仅限制所述特征部分中阐述的要素;其他元素不从整个权利要求中被排除。
[0023]
连接短语“基本上由...组成”用于限定除了字面披露的那些以外还包括材料、步骤、特征、组分、或元素的组合物或方法,前提是这些附加的材料、步骤、特征、组分、或元素不会实质影响请求保护的发明的基本和新颖特征。术语“基本上由
……
组成”居于“包含”和“由
……
组成”中间。
[0024]
当申请人已经用开放式术语如“包含着”定义了本发明或其一部分时,则应易于理解(除非另外指明),说明书应被解释为还使用术语“基本上由
……
组成”或“由
……
组成”描述本发明。
[0025]
此外,除非有相反的明确说明,否则“或”是指包含性的“或”,而不是指排他性的“或”。例如,条件a或者b通过以下中的任一项满足:a为真(或存在)且b为假(或不存在),a为假(或不存在)且b为真(或存在),并且a和b都为真(或存在)。
[0026]
同样,在本发明的元素或组分前的不定冠词“一个/一种(a/an)”关于元素或组分的例子(即,出现)的数量旨在是非限制性的。因此,“一个”或“一种”应理解为包括一个/一种或至少一个/一种,并且要素或组分的单数词语形式还包括复数,除非所述数字明显意指单数。
[0027]
如本文所提及的,单独或以词语的组合使用的术语“幼苗”是指由种子的胚芽发育的植物幼苗。
[0028]
如本文所提及的,单独使用或以诸如“阔叶杂草”的词语使用的术语“阔叶”是指双子叶或双子叶植物,用于描述以具有两个子叶的胚芽为特征的一类被子植物的术语。
[0029]
如本文所用,术语“烷基化剂”是指其中含碳基团通过碳原子键合到离去基团如卤化物或磺酸酯的化合物,该离去基团可通过亲核体与所述碳原子的键合而被置换。除非另外指明,否则术语“烷基化”不将含碳基团限制为烷基;烷基化剂中的含碳基团包括对于r3和r4指定的各种碳键合的取代基基团。
[0030]
在以上详述中,术语“烷基”,单独使用或在复合词如“烷硫基”或“卤代烷基”中使用,包括直链或支链烷基,诸如甲基、乙基、正丙基、异丙基、或不同的丁基、戊基、或己基异构体。“烯基”包括直链或支链的烯烃,诸如乙烯基、1
‑
丙烯基、2
‑
丙烯基、以及不同的丁烯基、戊烯基和己烯基异构体。“烯基”还包括聚烯,诸如1,3
‑
丁二烯基和2,4
‑
己二烯基。“炔基”包括直链或支链的炔烃,诸如乙炔基、1
‑
丙炔基、2
‑
丙炔基、以及不同的丁炔基、戊炔基和己炔基异构体。“炔基”还可包括由多个三键构成的部分,诸如2,5
‑
己二炔基。
[0031]“烷氧基”包括例如甲氧基、乙氧基、正丙氧基、异丙氧基和不同的丁氧基、戊氧基和己氧基异构体。“烷氧基烷基”表示烷基上的烷氧基取代。“烷氧基烷基”的实例包括ch3och2、ch3och2ch2、ch3ch2och2、ch3ch2ch2ch2och2和ch3ch2och2ch2。“烯氧基”包括直链或支链的烯氧基部分。“烯氧基”的实例包括h2c=chch2o、(ch3)2c=chch2o、(ch3)ch=chch2o、(ch3)ch=c(ch3)ch2o和ch2=chch2ch2o。“炔氧基”包括直链或支链的炔氧基部分。“炔氧基”的实例包括hc≡cch2o、ch3c≡cch2o和ch3c≡cch2ch2o。“烷硫基”包括支链或直链的烷硫基部分,诸如甲硫基、乙硫基、以及不同的丙硫基、丁硫基、戊硫基和己硫基异构体。“烷基亚磺酰基”包括烷基亚磺酰基的两种对映异构体。“烷基亚磺酰基”的实例包括ch3s(o)
‑
、ch3ch2s(o)
‑
、ch3ch2ch2s(o)
‑
、(ch3)2chs(o)
‑
以及不同的丁基亚磺酰基、戊基亚磺酰基和己基亚磺酰基异构体。“烷基磺酰基”的实例包括ch3s(o)2‑
、ch3ch2s(o)2‑
、ch3ch2ch2s(o)2‑
、(ch3)2chs(o)2‑
、以及不同的丁基磺酰基、戊基磺酰基和己基磺酰基异构体。“烷基氨基”、“二烷基氨基”等类似于上述实例进行定义。
[0032]“环烷基”包括例如环丙基、环丁基、环戊基和环己基。术语“烷基环烷基”表示环烷基部分上的烷基取代,并且包括例如乙基环丙基、异丙基环丁基、3
‑
甲基环戊基和4
‑
甲基环己基。术语“环烷基烷基”表示烷基部分上的环烷基取代。“环烷基烷基”的实例包括环丙基甲基、环戊基乙基、以及其他键合到直链或支链烷基上的环烷基部分。术语“环烷氧基”表示通过氧原子连接的环烷基,诸如环戊氧基和环己氧基。“环烷基烷氧基”表示通过附接至烷基链的氧原子连接的环烷基烷基。“环烷基烷氧基”的实例包括环丙基甲氧基、环戊基乙氧
基、以及其他键合到直链或支链烷氧基的环烷基部分。
[0033]
术语“卤素”,单独地或在复合词如“卤代烷基”中,或者当在描述如“被卤素取代的烷基”中使用时,包括氟、氯、溴或碘。此外,当在复合词如“卤代烷基”中使用时,或者当在描述如“被卤素取代的烷基”中使用时,所述烷基可以是被卤素原子(其可以是相同的或不同的)部分地或完全地取代的。“卤代烷基”或“被卤素取代的烷基”的实例包括f3c、clch2、cf3ch2和cf3ccl2。术语“卤代环烷基”、“卤代烷氧基”、“卤代烷硫基”、“卤代烷基亚磺酰基”、“卤代烷基磺酰基”、“卤代烯基”、“卤代炔基”等类似于术语“卤代烷基”定义。“卤代环烷基”的实例包括2
‑
氯环丙基和2
‑
溴环丁基。“卤代烷氧基”的实例包括cf3o
‑
、ccl3ch2o
‑
、hcf2ch2ch2o
‑
和cf3ch2o
‑
。“卤代烷硫基”的实例包括ccl3s
‑
、cf3s
‑
、ccl3ch2s
‑
和clch2ch2ch2s
‑
。“卤代烷基亚磺酰基”的实例包括cf3s(o)
‑
、ccl3s(o)
‑
、cf3ch2s(o)
‑
和cf3cf2s(o)
‑
。“卤代烷基磺酰基”的实例包括cf3s(o)2‑
、ccl3s(o)2‑
、cf3ch2s(o)2‑
和cf3cf2s(o)2‑
。“卤代烯基”的实例包括(cl)2c=chch2‑
和cf3ch2ch=chch2‑
。“卤代炔基”的实例包括hc≡cchcl
‑
、cf3c≡c
‑
、ccl3c≡c
‑
和fch2c≡cch2‑
。
[0034]“烷基羰基”表示键合到c(=o)部分上的直链或支链的烷基部分。“烷基羰基”的实例包括ch3c(=o)
‑
、ch3ch2ch2c(=o)
‑
和(ch3)2chc(=o)
‑
。“烷氧基羰基”的实例包括ch3oc(=o)
‑
、ch3ch2oc(=o)
‑
、ch3ch2ch2oc(=o)
‑
、(ch3)2choc(=o)
‑
和不同的丁氧基
‑
或戊氧基羰基异构体。
[0035]
在取代基中的碳原子的总数用“c
i
‑
c
j”前缀表示,其中i和j是从1至8的数。例如,c1‑
c4烷基磺酰基表示甲基磺酰基至丁基磺酰基;c2烷氧基烷基表示ch3och2‑
;c3烷氧基烷基表示例如ch3ch(och3)
‑
、ch3och2ch2‑
或ch3ch2och2‑
;并且c4烷氧基烷基表示被包含总共四个碳原子的烷氧基取代的烷基的各种异构体,实例包括ch3ch2ch2och2‑
和ch3ch2och2ch2‑
。
[0036]
当化合物被带有下标(其表示所述取代基的数目可以超过1)的取代基取代时,所述取代基(当它们超过1时)独立地选自所定义的取代基的组,例如,([r
(5))n
],n是1、2、3或4)。当基团含有可以为氢的取代基,例如(r1或r4)时,则当该取代基为氢时,公认这等同于所述基团是未取代的。与苯基或吡啶基有关的术语“任选地取代的”是指这样的基团,其为未取代的或具有至少一个不消除由未取代的类似物所拥有的生物活性的非氢取代基。如本文所用,除非另外指明,否则将应用下列定义。术语“任选地取代的”与短语“取代或未取代的”或与术语“(未)取代的”可互换使用。除非另外指明,否则任选地取代的基团可在基团的每个可取代的位置处具有取代基,并且每个取代彼此独立。
[0037]
如上所述,w可以是苯基或吡啶基,每个苯基或吡啶基任选地被至多5个r9取代。苯基或吡啶基的实例包括以下:
[0038]
示例1
[0039][0040][0041]
虽然在结构u
‑
1、u
‑
49、u
‑
50和u
‑
51中示出r9基团,但是应注意到,因为它们是任选的取代基,所以它们不必须存在。应注意到,当(r9)
r
与u基团之间的附接点示出为浮动时,
(r9)
r
可以附接至u基团的任何可用的碳原子。
[0042]
本领域中已知多种合成方法能够制备芳族和非芳族的杂环和环体系;对于广泛综述,参见comprehensive heterocyclic chemistry[综合杂环化学],a.r.katritzky和c.w.主编,pergamon press[培格曼出版社],牛津,1984的八卷集合和comprehensive heterocyclic chemistry ii[综合杂环化学ii],a.r.katritzky,c.w.rees和e.f.v.scriven主编,pergamon press[培格曼出版社],牛津,1996的十二卷集合。
[0043]
本发明的化合物可作为一种或多种立体异构体存在。多种立体异构体包括对映异构体、非对映异构体、阻转异构体和几何异构体。立体异构体为构成相同但它们的原子在空间中的排列不同的异构体,并且包括对映异构体、非对映异构体、顺
‑
反异构体(还称为几何异构体)和阻转异构体。阻转异构体起因于围绕单键的旋转受限制,其中旋转势垒足够高以允许同分异构物种的分离。本领域的技术人员将理解,一种立体异构体当相对于一种或多种其他立体异构体富集时,或当与一种或多种其他立体异构体分离时,可能更有活性和/或可能表现出有益的效果。另外,本领域的技术人员知道如何分离、富集和/或选择性地制备所述立体异构体。本发明的化合物可作为立体异构体的混合物、单独的立体异构体、或作为光学活性形式存在。
[0044]
例如,如下所示出的,通常在反式构型中发现c(o)nh(w)部分(键合至吡咯烷酮环的3
‑
位处的碳)和q(键合至环的4
‑
位处的碳)。这两个碳原子二者都具有手性中心。最普遍的一对对映体被描述为式1’和式1”。虽然本发明涉及所有立体异构体,但用于生物可操作性的优选对映异构体被确定为式1
′
(在本文也称为(3s,4r)或索引表a的“立体(3,4)”列中的“s,r”),其中酰胺(即c(o)nh(w))部分朝向观察者突出并且q部分远离观察者突出。对于立体异构现象的所有方面的综合讨论,参见ernest l.eliel和samuel h.wilen的stereochemistry of organiccompounds[有机化合物立体化学],john wiley&sons[约翰威立父子出版社],1994。
[0045][0046]
本文绘制的分子描述依照用于描绘立体化学的标准惯例。为了指明立体构型,从绘图平面伸出并且朝向观看者的键以实心楔形表示,其中该楔形的宽端连接至从绘图平面伸出朝向观看者的原子上。伸向绘图平面下方并且远离观察者的键由虚线楔形表示,其中该楔形的窄端连接到进一步远离观察者的原子上。等宽线表示相对于用实心或虚线楔形示出的键具有相对或中立方向的键;等宽线还可描述其中不旨在指明具体立体构型的分子或分子部分中的键。
[0047]
本发明包括外消旋混合物,例如等量的具有式1’和1
″
的对映异构体。此外,本发明包括与具有式1的对映异构体中的外消旋混合物相比富集的化合物。还包括具有式1(例如式1’和1”)的化合物的基本上纯的对映异构体。
[0048]
当对映异构体地富集时,一种对映异构体以比另一种更大的量存在,并且富集程
度可以通过定义为(2x
‑
1)
·
100%的对映异构体过量(“ee”)的表达来定义,其中x是混合物中占优势的对映异构体的摩尔分数(例如,20%的ee对应于对映异构体的60:40比率)。
[0049]
优选地,本发明的组合物具有更具活性异构体的至少50%的对映异构体过量;更优选地至少75%的对映异构体过量;还更优选地至少90%的对映异构体过量;并且最优选地至少94%的对映异构体(>99%ee)过量。特别值得注意的是更具活性的异构体的基本上对映异构体纯的实施例。
[0050]
具有式1的化合物可包含附加的手性中心。例如,取代基和其他分子成分如r2和r3本身可以含有手性中心。本发明包括外消旋混合物以及在这些附加的手性中心处富集的和基本上纯的立体构型。
[0051]
本发明的化合物由于围绕式1中的酰胺键(例如,c(o)nh(w))的旋转受限,因此可以作为一种或多种构象异构体存在。本发明包括构象异构体的混合物。此外,本发明包括相对于其他构象异构体富集一种构象异构体的化合物。
[0052]
具有式1的化合物典型地以多于一种形式存在,并且因此式1包括它们所代表的化合物的所有结晶和非结晶形式。非结晶形式包括为固体的实施例诸如蜡和树胶,以及为液体的实施例诸如溶液和熔融物。结晶形式包括代表基本上单晶类型的实施例和代表多晶型物(即不同结晶类型)的混合物的实施例。术语“多晶型物”是指可以以不同晶型结晶的化合物的具体晶型,这些晶型在晶格中具有不同的分子排列和/或构象。虽然多晶型物可具有相同的化学组成,但是它们也可以在组成上由于共结晶水或其他分子的存在或不存在而不同,该共结晶水或其他分子可弱结合或强结合在晶格内。多晶型物可以在此类化学、物理、和生物特性方面不同,诸如晶体形状、密度、硬度、颜色、化学稳定性、熔点、吸湿性、可悬浮性、溶解速率和生物利用度。本领域的技术人员将理解,相对于具有式1的相同化合物的另一种多晶型物或多晶型物的混合物,具有式1的化合物的具体多晶型物可以展现出有益效果(例如适合制备有用制剂,改善的生物性能)。具有式1的化合物的具体多晶型物的制备和分离可通过本领域技术人员已知的方法实现,包括例如采用所选溶剂和温度的结晶。对于多晶型现象的综合讨论,参见r.hilfiker编辑的制药工业的多晶型现象(polymorphism in the pharmaceutical 知dustry),wiley
‑
vch,魏因海姆(weinheim),2006。
[0053]
本领域的技术人员将理解,不是所有的含氮杂环都可以形成n
‑
氧化物,因为氮需要可用的孤电子对以氧化成氧化物;本领域的技术人员将认识到可形成n
‑
氧化物的那些含氮杂环。本领域技术人员还将认识到叔胺能够形成n
‑
氧化物。用于制备杂环和叔胺的n
‑
氧化物的合成方法是本领域的技术人员非常熟知的,包括使用过氧酸诸如过氧乙酸和间氯过氧苯甲酸(mcpba)、过氧化氢、烷基氢过氧化物诸如叔丁基氢过氧化物、过硼酸钠和二环氧乙烷诸如二甲基二环氧乙烷来氧化杂环和叔胺。用于制备n
‑
氧化物的这些方法已广泛描述和综述于文献中,参见例如:t.l.gilchrist,comprehensive organic synthesis[综合有机合成]中,第7卷,第748
‑
750页,s.v.ley编辑,pergamon press[培格曼出版社];m.tisler和b.stanovnik,comprehensive heterocyclic chemistry[综合杂环化学],第3卷,第18
‑
20页,a.j.boulton和a.mckillop编辑,培格曼出版社;m.r.grimmett和b.r.t.keene,advances in heterocyclic chemistry[杂环化学进展],第43卷,第149
‑
161页,a.r.katritzky编辑,academic press[学术出版社];m.tisler和b.stanovnik,advances in heterocyclic chemistry[杂环化学进展],第9卷,第285
‑
291页,a.r.katritzky和
a.j.boulton编辑,academic press[学术出版社];和g.w.h.cheeseman和e.s.g.werstiuk于advances in heterocyclic chemistry[杂环化学进展]中,第22卷,第390
‑
392页,a.r.katritzky和a.j.boulton编辑,academic press[学术出版社]。
[0054]
本领域的技术人员认识到,由于在环境中和在生理条件下化合物的盐与它们相应的非盐形式处于平衡,因此盐共享非盐形式的生物效用。因此,多种具有式1的化合物的盐可用于控制不希望的植被(即,是农业上适合的)。具有式1的化合物的盐包括与无机酸或有机酸形成的酸加成盐,所述酸如氢溴酸、盐酸、硝酸、磷酸、硫酸、乙酸、丁酸、富马酸、乳酸、马来酸、丙二酸、草酸、丙酸、水杨酸、酒石酸、4
‑
甲苯磺酸或戊酸。当具有式1的化合物包含酸性部分诸如羧酸或酚时,盐还包括与有机碱或无机碱形成的那些,所述碱诸如吡啶、三乙基胺或氨、或钠、钾、锂、钙、镁或钡的酰胺、氢化物、氢氧化物或碳酸盐。因此,本发明包括选自式1、其n
‑
氧化物和农业上合适的盐的化合物。
[0055]
如在发明内容中所述的本发明的实施例包括(即,其中如以下实施例中所用的式1包括其n
‑
氧化物和盐):
[0056]
实施例1.如在发明内容中所述的具有式1的化合物。
[0057]
实施例2.如实施例1所述的化合物,其中q选自由q
‑
1和q
‑
2组成的组。
[0058]
实施例3.如实施例1所述的化合物,其中q是q
‑
1。
[0059]
实施例4.如实施例1至3中任一项所述的化合物,其中y是o。
[0060]
实施例5.如实施例1至4中任一项所述的化合物,其中r1是h、c1‑
c6烷基、c1‑
c6卤代烷基或c4‑
c8环烷基烷基。
[0061]
实施例6.如实施例5所述的化合物,其中r1是h、c1‑
c4烷基、或c4‑
c5环烷基烷基。
[0062]
实施例7.如实施例6所述的化合物,其中r1是h、ch3或环丙基甲基。
[0063]
实施例8.如实施例7所述的化合物,其中r1是h或ch3。
[0064]
实施例9.如实施例8所述的化合物,其中r1是ch3。
[0065]
实施例10.如实施例1至9中任一项所述的化合物,其中r2是c1‑
c3烷基或c1‑
c3卤代烷基。
[0066]
实施例11.如实施例1至10中任一项所述的化合物,其中r2是c1‑
c2烷基或c1‑
c2卤代烷基。
[0067]
实施例12.如实施例11所述的化合物,其中r2是ch3或ch2cf3。
[0068]
实施例13.如实施例12所述的化合物,其中r2是ch3。
[0069]
实施例14.如实施例1至13中任一项所述的化合物,其中r3是卤素、c1‑
c6烷基或c1‑
c6卤代烷基。
[0070]
实施例15.如实施例14所述的化合物,其中r3是卤素、c1‑
c3烷基或c1‑
c3卤代烷基。
[0071]
实施例16.如实施例15所述的化合物,其中r3是cl、ch3或cf3。
[0072]
实施例17.如实施例16所述的化合物,其中r3是ch3或cf3。
[0073]
实施例18.如实施例17所述的化合物,其中r3是cf3。
[0074]
实施例19.如实施例1至18中任一项所述的化合物,其中r4是h或cl。
[0075]
实施例20.如实施例19所述的化合物,其中r4是h。
[0076]
实施例21.如实施例1至20中任一项所述的化合物,其中r5是f、cl或br。
[0077]
实施例22.如实施例21所述的化合物,其中r5是f或cl。
[0078]
实施例23.如实施例22所述的化合物,其中r5是f。
[0079]
实施例24.如实施例1至23中任一项所述的化合物,其中r6是h、卤素、羟基、c1‑
c4烷氧基或c1‑
c4烷基。
[0080]
实施例25.如实施例24所述的化合物,其中r6是h、cl、羟基、och3或ch3。
[0081]
实施例26.如实施例25所述的化合物,其中r6是h。
[0082]
实施例27.如实施例25所述的化合物,其中r6是cl。
[0083]
实施例28.如实施例25所述的化合物,其中r6是羟基。
[0084]
实施例29.如实施例25所述的化合物,其中r6是och3。
[0085]
实施例30.如实施例25所述的化合物,其中r6是ch3。
[0086]
实施例31.如实施例21至30中任一项所述的化合物,其中n是1、2或3。
[0087]
实施例32.如实施例31所述的化合物,其中n是1或2。
[0088]
实施例33.如实施例32所述的化合物,其中n是1。
[0089]
实施例34.如实施例1至33中任一项所述的化合物,其中w是苯基、3
‑
吡啶基或4
‑
吡啶基,每个苯基、3
‑
吡啶基或4
‑
吡啶基任选地被至多4个r9取代。
[0090]
实施例35.如实施例34所述的化合物,其中w是苯基或3
‑
吡啶基,每个苯基或3
‑
吡啶基任选地被至多3个r9取代。
[0091]
实施例36.如实施例35所述的化合物,其中w是被至多3个r9取代的苯基。
[0092]
实施例37.如实施例1至36中任一项所述的化合物,其中每个r9独立地是卤素、氰基、硝基、c1‑
c4烷基、c1‑
c4卤代烷基、c2‑
c4烷氧基烷基、c2‑
c4卤代烷氧基烷基、c3‑
c4环烷基、c3‑
c4卤代环烷基、环丙基甲基、甲基环丙基、c1‑
c4烷氧基、c1‑
c4卤代烷氧基、c3‑
c4环烷氧基、c1‑
c4烷硫基、c1‑
c4卤代烷硫基、c1‑
c4烷基亚磺酰基、c1‑
c4卤代烷基亚磺酰基、c1‑
c4烷基磺酰基、c1‑
c4卤代烷基磺酰基、羟基、甲酰基、c2‑
c4烷基羰基、c2‑
c4烷基羰基氧基、c1‑
c4烷基磺酰基氧基、c1‑
c4卤代烷基磺酰基氧基。
[0093]
实施例38.如实施例37所述的化合物,其中每个r9独立地是卤素、氰基、硝基、c1‑
c4烷基、c1‑
c4卤代烷基、c1‑
c4烷氧基、c1‑
c4烷硫基、c1‑
c4烷基亚磺酰基或c1‑
c4烷基磺酰基。
[0094]
实施例39.如实施例38所述的化合物,其中每个r9独立地是卤素、c1‑
c4烷基、c1‑
c4卤代烷基或c1‑
c4烷基磺酰基。
[0095]
实施例40.如实施例39所述的化合物,其中每个r9独立地是f、cl、ch3、cf3或so2ch3。
[0096]
实施例41.如实施例40所述的化合物,其中每个r9独立地是f或cf3。
[0097]
实施例42.如实施例34至41中任一项所述的化合物,其中r9在w的邻位、间位、或对位(相对于与式1的其余部分的连接)。
[0098]
实施例43.如实施例34至41中任一项所述的化合物,其中r9在w的邻位和间位(相对于与式1的其余部分的连接)。
[0099]
实施例44.如发明内容所述的化合物,其中当r1是c1‑
c6烷基时,r2是c1‑
c6卤代烷基。
[0100]
本发明的具体实施例是具有式1的化合物,其中y是o;r1是ch3;q是q
‑
1;r2是ch3;r3是cf3;r4是h;w是在2
‑
位处被1个r9和在3
‑
位被1个r9取代的苯基;两个r9独立地是f;并且r6是h。
[0101]
本发明还包括一种除草混合物,其包含(a)选自式1、其n
‑
氧化物和盐的化合物(如
发明内容中所描述的)和(b)至少一种选自以下项的附加活性成分:(b1)光系统ii抑制剂,(b2)乙酰羟酸合酶(ahas)抑制剂,(b3)乙酰辅酶a羧化酶(accase)抑制剂,(b4)生长素模拟物,(b5)5
‑
烯醇
‑
丙酮酸莽草酸
‑3‑
磷酸酯(epsp)合酶抑制剂,(b6)光系统i电子转向剂,(b7)原卟啉原氧化酶(ppo)抑制剂,(b8)谷氨酰胺合成酶(gs)抑制剂,(b9)极长链脂肪酸(vlcfa)延长酶抑制剂,(b10)生长素转运抑制剂,(b11)八氢番茄红素脱氢酶(pds)抑制剂,(b12)4
‑
羟基苯基
‑
丙酮酸双加氧酶(hppd)抑制剂,(b13)尿黑酸茄呢基转移酶(hst)抑制剂,(b14)纤维素生物合成抑制剂,(b15)其他除草剂,包括有丝分裂干扰剂、有机含砷化合物、磺草灵、溴丁酰草胺、环庚草醚、苄草隆、棉隆、2
‑
[(2,5
‑
二氯苯基)甲基]
‑
4,4
‑
二甲基
‑3‑
异噁唑烷酮、野燕枯、杀草隆、乙氧苯草胺、抑草丁、调节膦、杀木膦、海丹托西丁(hydantocidin)、威百亩、甲基杀草隆、油状物酸、噁嗪草酮、壬酸和稗草畏,(b16)(b1)至(b16)的化合物的除草剂安全剂和盐。
[0102]
本发明的实施例(包括实施例1至44以及本文所述的任何其他实施例)可以以任何方式组合,并且实施例中变量的描述不仅涉及具有式1的化合物,而且还涉及对于制备具有式1的化合物有用的中间体化合物。实施例1至44的组合如以下示出:
[0103]
实施例a.一种具有式1的化合物,其中
[0104]
r1是h、c1‑
c6烷基、c1‑
c6卤代烷基或c4‑
c8环烷基烷基;
[0105]
r2是c1‑
c3烷基或c1‑
c3卤代烷基;
[0106]
r3是卤素、c1‑
c6烷基或c1‑
c6卤代烷基;
[0107]
y是o;
[0108]
r4是h或cl;
[0109]
r5是f、cl或br;
[0110]
n是1、2或3;
[0111]
r6是h、卤素、羟基、c1‑
c4烷氧基或c1‑
c4烷基;
[0112]
w是苯基、3
‑
吡啶基或4
‑
吡啶基,每个苯基、3
‑
吡啶基或4
‑
吡啶基任选地被至多4个r9取代;并且
[0113]
每个r9独立地是卤素、氰基、硝基、c1‑
c4烷基、c1‑
c4卤代烷基、c2‑
c4烷氧基烷基、c2‑
c4卤代烷氧基烷基、c3‑
c4环烷基、c3‑
c4卤代环烷基、环丙基甲基、甲基环丙基、c1‑
c4烷氧基、c1‑
c4卤代烷氧基、c3‑
c4环烷氧基、c1‑
c4烷硫基、c1‑
c4卤代烷硫基、c1‑
c4烷基亚磺酰基、c1‑
c4卤代烷基亚磺酰基、c1‑
c4烷基磺酰基、c1‑
c4卤代烷基磺酰基、羟基、甲酰基、c2‑
c4烷基羰基、c2‑
c4烷基羰基氧基、c1‑
c4烷基磺酰基氧基、c1‑
c4卤代烷基磺酰基氧基。
[0114]
实施例b.如实施例a所述的化合物,其中
[0115]
q选自由q
‑
1和q
‑
2组成的组;
[0116]
r1是h、c4‑
c5环烷基烷基或c1‑
c4烷基;
[0117]
r2是c1‑
c2烷基或c1‑
c2卤代烷基;
[0118]
r3是卤素、c1‑
c3烷基或c1‑
c3卤代烷基;
[0119]
r4是h;
[0120]
n是1或2;
[0121]
r6是h、cl、羟基、och3或ch3;
[0122]
w是苯基或3
‑
吡啶基,每个苯基或3
‑
吡啶基任选地被至多3个r9取代;并且
[0123]
每个r9独立地是卤素、氰基、硝基、c1‑
c4烷基、c1‑
c4卤代烷基、c1‑
c4烷氧基、c1‑
c4烷硫基、c1‑
c4烷基亚磺酰基或c1‑
c4烷基磺酰基。
[0124]
实施例c.如实施例b所述的化合物,其中
[0125]
q是q
‑
1;
[0126]
r1是h、环丙基甲基或ch3;
[0127]
r2是ch3或ch2cf3;
[0128]
r3是cl、ch3或cf3;
[0129]
r6是h;
[0130]
w是被至多3个r9取代的苯基;并且
[0131]
每个r9独立地是卤素、c1‑
c4烷基、c1‑
c4卤代烷基或c1‑
c4烷基磺酰基。
[0132]
实施例d.如实施例c所述的化合物,其中
[0133]
r1是h或ch3;
[0134]
r2是ch3;
[0135]
r3是ch3或cf3;
[0136]
r6是h;
[0137]
每个r9独立地是f或cf3;并且
[0138]
r9在w的邻位、间位、或对位(相对于与式1的其余部分的连接)。
[0139]
具体的实施例是具有式1的化合物,即:
[0140]
(3s,4r)
‑
n
‑
(2,3
‑
二氟苯基)
‑1‑
甲基
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷甲酰胺。
[0141]
本发明还涉及一种用于控制不希望植被的方法,该方法包括向该植被所在地施用除草有效量的本发明的化合物(例如,作为本文所述的组合物)。应注意作为与使用方法有关的实施例是涉及上述实施例的化合物的那些。本发明的化合物特别可用于选择性地控制作物如小麦、大麦、玉蜀黍、大豆、向日葵、棉、油状物菜和稻以及特种作物如甘蔗、柑橘、水果和坚果作物中的杂草。
[0142]
另外值得注意作为实施例是包含上述实施例的化合物的本发明的除草组合物。
[0143]
本发明还包括一种除草混合物,所述除草混合物包含(a)选自式1、其n
‑
氧化物和盐的化合物和(b)至少一种选自以下项的附加活性成分:(b1)光系统ii抑制剂,(b2)乙酰羟酸合酶(ahas)抑制剂,(b3)乙酰辅酶a羧化酶(accase)抑制剂,(b4)生长素模拟物,(b5)5
‑
烯醇
‑
丙酮酸莽草酸
‑3‑
磷酸酯(epsp)合酶抑制剂,(b6)光系统i电子转向剂,(b7)原卟啉原氧化酶(ppo)抑制剂,(b8)谷氨酰胺合成酶(gs)抑制剂,(b9)极长链脂肪酸(vlcfa)延长酶抑制剂,(b10)生长素转运抑制剂,(b11)八氢番茄红素脱氢酶(pds)抑制剂,(b12)4
‑
羟基苯基
‑
丙酮酸双加氧酶(hppd)抑制剂,(b13)尿黑酸茄呢基转移酶(hst)抑制剂,(b14)纤维素生物合成抑制剂,(b15)其他除草剂,包括有丝分裂干扰剂、有机含砷化合物、磺草灵、溴丁酰草胺、环庚草醚、苄草隆、棉隆、野燕枯、杀草隆、乙氧苯草胺、抑草丁、调节膦、调节膦
‑
铵、海丹托西丁、威百亩、甲基杀草隆、油状物酸、噁嗪草酮、壬酸和稗草畏,和(b16)(b1)至(b16)的化合物的除草剂安全剂和盐。
[0144]“光系统ii抑制剂”(b1)是在q
b
‑
结合位置处结合到d
‑
1蛋白质上并因此在叶绿体类囊体膜中阻断电子从q
a
传输至q
b
的化学化合物。由穿过光系统ii被阻断的电子通过一系
列反应转移以形成毒性化合物,这些毒性化合物破坏细胞膜并造成叶绿体溶胀、膜渗漏,并最终造成细胞破裂。q
b
‑
结合位置具有三个不同的结合位点:结合位点a结合三嗪如莠去津、三嗪酮如环嗪酮、以及尿嘧啶如除草定,结合位点b结合苯基脲如敌草隆,并且结合位点c结合苯并噻二唑如灭草松、腈如溴苯腈以及苯基哒嗪如哒草特。光系统ii抑制剂的实例包括莠灭净、氨唑草酮、莠去津、灭草松、除草定、杀草全、溴苯腈、氯溴隆、杀草敏、绿麦隆、枯草隆、苄草隆、草净津、杀草隆、甜菜安、敌草净、噁唑隆、异戊净、敌草隆、磺噻隆、非草隆、伏草隆、环嗪酮、碘苯腈、异丙隆、异噁隆、环草定、利谷隆、苯嗪草酮、甲基苯噻隆、溴谷隆、甲氧隆、嗪草酮、绿谷隆、草不隆、甲氯酰草胺、苯敌草、扑灭通、扑草净、敌稗、扑灭津、氯苯哒醇(pyridafol)、哒草特、环草隆、西玛津、西草净、特丁噻草隆、特草定、特丁通、特丁津、去草净和草达津。
[0145]“ahas抑制剂”(b2)是抑制乙酰羟酸合酶(ahas)(也称为乙酰乳酸合酶(als))的化学化合物,并因此通过抑制蛋白质合成和细胞生长所需的支链脂族氨基酸诸如缬氨酸、亮氨酸和异亮氨酸的生产来杀死植物。ahas抑制剂的实例包括酰嘧磺隆、四唑嘧磺隆、苄嘧磺隆、双草醚钠盐、氯酯磺草胺、氯嘧磺隆、氯磺隆、醚磺隆、环丙嘧磺隆、双氯磺草胺、胺苯磺隆、乙氧嘧磺隆、啶嘧磺隆、双氟磺草胺、氟酮磺隆、唑嘧磺草胺、氟啶嘧磺隆、氟啶嘧磺隆钠、甲酰胺磺隆、氯吡嘧磺隆、咪草酸、甲氧咪草烟、甲咪唑烟酸、灭草烟、灭草喹、咪草烟、唑吡嘧磺隆、甲基碘磺隆(包括钠盐)、碘嗪磺隆(iofensulfuron)(2
‑
碘
‑
n
‑
[[(4
‑
甲氧基
‑6‑
甲基
‑
1,3,5
‑
三嗪
‑2‑
基)氨基]羰基]苯磺酰胺)、甲磺胺磺隆、嗪吡嘧磺隆(3
‑
氯
‑4‑
(5,6
‑
二氢
‑5‑
甲基
‑
1,4,2
‑
二噁嗪
‑3‑
基)
‑
n
‑
[[(4,6
‑
二甲氧基
‑2‑
嘧啶基)氨基]羰基]
‑1‑
甲基
‑
1h
‑
吡唑
‑5‑
磺酰胺)、磺草唑胺、甲磺隆、烟嘧磺隆、环氧嘧磺隆、五氟磺草胺、氟氯磺隆、丙苯磺隆钠、丙嗪嘧磺隆(2
‑
氯
‑
n
‑
[[(4,6
‑
二甲氧基
‑2‑
嘧啶基)氨基]羰基]
‑6‑
丙基咪唑并[1,2
‑
b]哒嗪
‑3‑
磺酰胺)、氟磺隆、吡嘧磺隆、嘧啶肟草醚、环酯草醚、嘧草醚、嘧硫草醚钠、砜嘧磺隆、甲嘧磺隆、磺酰磺隆、噻酮磺隆、噻吩磺隆、氟酮磺草胺(n
‑
[2
‑
[(4,6
‑
二甲氧基
‑
1,3,5
‑
三嗪
‑2‑
基)羰基]
‑6‑
氟苯基]
‑
1,1
‑
二氟
‑
n
‑
甲基甲磺酰胺)、醚苯磺隆、苯磺隆、三氟啶磺隆(包括钠盐)、氟胺磺隆和三氟甲磺隆。
[0146]“accase抑制剂”(b3)是抑制乙酰辅酶a羧化酶的化学化合物,该酶负责催化植物中脂质和脂肪酸合成的早期步骤。脂质是细胞膜的主要组分,并且没有脂质,则不能产生新细胞。乙酰辅酶a羧化酶的抑制和后续脂质生产的缺乏导致细胞膜完整性丧失,尤其是在活跃生长区域如分生组织中。最终幼苗和根茎生长停止,并且幼苗分生组织和根茎芽开始枯死。accase抑制剂的实例包括禾草灭、丁苯草酮、烯草酮、炔草酯、噻草酮、氰氟草酯、禾草灵、噁唑禾草灵、吡氟禾草灵、吡氟氯禾灵、唑啉草酯、环苯草酮、喔草酯、喹禾灵、稀禾定、得杀草和肟草酮,包括经解析形式,诸如精噁唑禾草灵、精吡氟禾草灵、精吡氟氯禾灵和精喹禾灵以及酯形式如炔草酯、氰氟草酯、禾草灵和精噁唑禾草灵。
[0147]
生长素是调节许多植物组织的生长的植物激素。“生长素模拟物”(b4)是模拟植物生长激素生长素的化合物,因此导致不受控制和无序的生长,从而导致易感物种的植物死亡。生长素模拟物的实例包括环丙嘧啶酸(6
‑
氨基
‑5‑
氯
‑2‑
环丙基
‑4‑
嘧啶羧酸)及其甲基和乙基酯及其钠盐和钾盐、氯氨吡啶酸、草除灵
‑
乙酯、草灭平、氯酰草膦、稗草胺、二氯吡啶酸、麦草畏、2,4
‑
d、2,4
‑
db、滴丙酸、氯氟吡氧乙酸、氟氯吡啶酯(halauxifen)(4
‑
氨基
‑3‑
氯
‑6‑
(4
‑
氯
‑2‑
氟
‑3‑
甲氧基苯基)
‑2‑
吡啶羧酸)、氟氯吡啶甲酯(halauxifen
‑
methyl)(4
‑
氨基
‑3‑
氯
‑6‑
(4
‑
氯
‑2‑
氟
‑3‑
甲氧基苯基)
‑2‑
吡啶羧酸甲酯)、mcpa、mcpb、2
‑
甲
‑4‑
氯丙酸、毒莠定、二氯喹啉酸、氯甲喹啉酸、2,3,6
‑
tba、绿草定、以及4
‑
氨基
‑3‑
氯
‑6‑
(4
‑
氯
‑2‑
氟
‑3‑
甲氧基苯基)
‑5‑
氟
‑2‑
吡啶羧酸甲酯。
[0148]“epsp合酶抑制剂”(b5)是抑制酶5
‑
烯醇
‑
丙酮酰莽草酸
‑3‑
磷酸酯合酶的化学化合物,该酶参与芳族氨基酸诸如酪氨酸、色氨酸和苯丙氨酸的合成。epsp抑制剂除草剂易于通过植物叶吸收并在韧皮部中易位至生长点。草甘膦是属于该组的相对非选择性苗后除草剂。草甘膦包括酯和盐,诸如铵盐、异丙基铵盐、钾盐、钠盐(包括倍半钠盐)和三甲基锍盐(可替代地称为草硫膦)。
[0149]“光系统i电子转向剂”(b6)是从光系统i中接收电子,并在数次循环之后产生羟基自由基的化合物。这些自由基极具反应性并易于破坏不饱和脂质,包括膜脂肪酸和叶绿素。这破坏细胞膜完整性,使得细胞和细胞器“渗漏”,从而导致快速叶片萎蔫和干枯,并最终导致植物死亡。该第二类型的光合成抑制剂的实例包括敌草快和百草枯。
[0150]“ppo抑制剂”(b7)是抑制酶原卟啉原氧化酶的化合物,其迅速地导致在植物中形成破坏细胞膜的高反应性化合物,从而导致细胞液渗出。ppo抑制剂的实例包括三氟羧草醚
‑
钠、唑啶草酮、双苯嘧草酮、甲羧除草醚、氟丙嘧草酯、唑酮草酯、三唑酮草酯、甲氧除草醚、吲哚酮草酯、异丙吡草酯、氟哒嗪草酯、氟胺草酯、丙炔氟草胺、乙羧氟草醚、氟噻甲草酯、氟磺胺草醚、氟硝磺酰胺(halosafen)、乳氟禾草灵、丙炔噁草酮、噁草酮、乙氧氟草醚、环戊噁草酮、氟唑草胺、双唑草腈、吡草醚、苯嘧磺草胺、甲磺草胺、噻二唑草胺、三氟草嗪(trifludimoxazin)(二氢
‑
1,5
‑
二甲基
‑6‑
硫基
‑3‑
[2,2,7
‑
三氟
‑
3,4
‑
二氢
‑3‑
氧代
‑4‑
(2
‑
丙
‑1‑
基)
‑
2h
‑
1,4
‑
苯并噁嗪
‑6‑
基]
‑
1,3,5
‑
三嗪
‑
2,4(1h,3h)
‑
二酮)和氟嘧硫草酯(n
‑
[2
‑
[[2
‑
氯
‑5‑
[3,6
‑
二氢
‑3‑
甲基
‑
2,6
‑
二氧基
‑4‑
(三氟甲基)
‑
1(2h)
‑
嘧啶基]
‑4‑
氟苯基]硫基]
‑1‑
氧代丙基]
‑
β
‑
丙氨酸甲酯)。
[0151]“gs抑制剂”(b8)是抑制谷氨酰胺合成酶的活性的化合物,植物使用该酶以将氨转化为谷氨酰胺。因此,氨累积并且谷氨酰胺水平降低。由于氨毒性和其他代谢过程所需的氨基酸的缺乏的联合效应,植物损害可能出现。gs抑制剂包括草胺磷及其酯和盐,诸如草胺磷和其他草胺瞵衍生物、草胺磷p((2s)
‑2‑
氨基
‑4‑
(羟基甲基氧膦基)丁酸)和双丙氨膦(bilanaphos)。
[0152]“极长链脂肪酸(vlcfa)延长酶抑制剂”(b9)是具有各种化学结构的除草剂,其抑制延长酶。延长酶是位于叶绿体中或附近的酶之一,其在极长链脂肪酸的生物合成中被涉及。在植物中,极长链脂肪酸是疏水聚合物的主要成分,其防止叶表面处的干燥并提供花粉粒的稳定性。此类除草剂包括乙草胺、甲草胺、莎稗磷、丁草胺、苯酮唑、二甲草胺、噻吩草胺、双苯酰草胺、异噁苯砜(fenoxasulfone)(3
‑
[[(2,5
‑
二氯
‑4‑
乙氧基苯基)甲基]磺酰基]
‑
4,5
‑
二氢
‑
5,5
‑
二甲基异噁唑)、四唑酰草胺、氟噻草胺、茚草酮、苯噻草胺、吡唑草胺、异丙甲草胺、萘丙胺、敌草胺、敌草胺
‑
m((2r)
‑
n,n
‑
二乙基
‑2‑
(1
‑
萘氧基)丙酰胺)、烯草胺(pethoxamid)、哌草磷、丙草胺、毒草胺、异丙草胺、罗克杀草砜(pyroxasulfone)和甲氧噻草胺,包括经解析形式诸如精异丙甲草胺和氯乙酰胺和氧乙酰胺。
[0153]“生长素传输抑制剂”(b10)是抑制植物中生长素传输的化学物质,诸如通过与生长素
‑
载体蛋白质结合。生长素传输抑制剂的实例包括氟吡草腙、萘草胺(也称为n
‑
(1
‑
萘基)
‑
邻氨甲酰基苯甲酸和2
‑
[(1
‑
萘基氨基)羰基]苯甲酸)。
[0154]“pds抑制剂(b11)”是在八氢番茄红素去饱和酶步骤时抑制类胡萝卜素生物合成途径的化合物。pds抑制剂的实例包括氟丁酰草胺、氟丁酰草胺
‑
m、吡氟酰草胺、氟啶草酮、氟咯草酮、呋草酮、氟草敏(norflurzon)和氟吡酰草胺。
[0155]“hppd抑制剂”(b12)是抑制4
‑
羟基
‑
苯基
‑
丙酮酸酯双加氧酶合成的生物合成的化学物质。hppd抑制剂的实例包括双环磺草酮、吡草酮、氟吡草酮(4
‑
羟基
‑3‑
[[2
‑
[(2
‑
甲氧基乙氧基)甲基]
‑6‑
(三氟甲基)
‑3‑
吡啶基]羰基]双环[3.2.1]辛
‑3‑
烯
‑2‑
酮)、芬奎诺酮(2
‑
[[8
‑
氯
‑
3,4
‑
二氢
‑4‑
(4
‑
甲氧基苯基)
‑3‑
氧代
‑2‑
喹喔啉基]羰基]
‑
1,3
‑
环己二酮)、异噁氯草酮、异噁唑草酮、甲基磺草酮、磺酰草吡脱、吡唑特、苄草唑、磺草酮、特呋三酮、环磺酮、tolpyralate(1
‑
[[1
‑
乙基
‑4‑
[3
‑
(2
‑
甲氧基乙氧基)
‑2‑
甲基
‑4‑
(甲基磺酰基)苯甲酰基]
‑
1h
‑
吡唑
‑5‑
基]氧基]乙基甲基碳酸酯)、苯吡唑草酮、5
‑
氯
‑3‑
[(2
‑
羟基
‑6‑
氧代
‑1‑
环己烯
‑1‑
基)羰基]
‑1‑
(4
‑
甲氧基苯基)
‑
2(1h)
‑
喹喔啉酮、4
‑
(2,6
‑
二乙基
‑4‑
甲基苯基)
‑5‑
羟基
‑
2,6
‑
二甲基
‑
3(2h)
‑
哒嗪酮、4
‑
(4
‑
氟苯基)
‑6‑
[(2
‑
羟基
‑6‑
氧代
‑1‑
环己烯
‑1‑
基)羰基]
‑2‑
甲基
‑
1,2,4
‑
三嗪
‑
3,5(2h,4h)
‑
二酮、5
‑
[(2
‑
羟基
‑6‑
氧代
‑1‑
环己烯
‑1‑
基)羰基]
‑2‑
(3
‑
甲氧基苯基)
‑3‑
(3
‑
甲氧基丙基)
‑
4(3h)
‑
嘧啶酮、2
‑
甲基
‑
n
‑
(4
‑
甲基
‑
1,2,5
‑
噁二唑
‑3‑
基)
‑3‑
(甲基亚磺酰基)
‑4‑
(三氟甲基)苯甲酰胺和2
‑
甲基
‑3‑
(甲基磺酰基)
‑
n
‑
(1
‑
甲基
‑
1h
‑
四唑
‑5‑
基)
‑4‑
(三氟甲基)苯甲酰胺。
[0156]“hst抑制剂”(b13)破坏植物将尿黑酸转化成2
‑
甲基
‑6‑
茄尼基
‑
1,4
‑
苯并醌的能力,从而破坏类胡萝卜素生物合成。hst抑制剂的实例包括氟啶草、氯草定、3
‑
(2
‑
氯
‑
3,6
‑
二氟苯基)
‑4‑
羟基
‑1‑
甲基
‑
1,5
‑
萘啶
‑
2(1h)
‑
酮、7
‑
(3,5
‑
二氯
‑4‑
吡啶基)
‑5‑
(2,2
‑
二氟乙基)
‑8‑
羟基吡咯并[2,3
‑
b]吡嗪
‑
6(5h)
‑
酮和4
‑
(2,6
‑
二乙基
‑4‑
甲基苯基)
‑5‑
羟基
‑
2,6
‑
二甲基
‑
3(2h)
‑
哒嗪酮。
[0157]
hst抑制剂还包括式a和b的化合物。
[0158][0159]
其中r
d1
是h、cl或cf3;r
d2
是h、cl或br;r
d3
是h或cl;r
d4
是h、cl或cf3;r
d5
是ch3、ch2ch3或ch2chf2;并且r
d6
是oh、或
‑
oc(=o)
‑
i
‑
pr;并且r
e1
是h、f、cl、ch3或ch2ch3;r
e2
是h或cf3;r
e3
是h、ch3或ch2ch3;r
e4
是h、f或br;r
e5
是cl、ch3、cf3、ocf3或ch2ch3;r
e6
是h、ch3、ch2chf2或c≡ch;r
e7
是oh、
‑
oc(=o)et、
‑
oc(=o)
‑
i
‑
pr或
‑
oc(=o)
‑
t
‑
bu;并且a
e8
是n或ch。
[0160]“纤维素生物合成抑制剂”(b14)抑制某些植物中的纤维素的生物合成。当对幼嫩或快速生长的植物出苗前施用或出苗后早期施用时,它们是最有效的。纤维素生物合成抑制剂的实例包括草克乐、敌草腈、氟胺草唑、三嗪茚草胺(n2‑
[(1r,2s)
‑
2,3
‑
二氢
‑
2,6
‑
二甲基
‑
1h
‑
茚
‑1‑
基]
‑6‑
(1
‑
氟乙基)
‑
1,3,5
‑
三嗪
‑
2,4
‑
二胺)、异噁酰草胺和三嗪氟草胺。
[0161]“其他除草剂”(b15)包括通过多种不同作用模式起作用的除草剂,诸如有丝分裂
干扰剂(例如,高效麦草氟甲酯和高效麦草氟异丙酯)、有机含砷化合物(例如,dsma和msma)、7,8
‑
二氢叶酸合成酶抑制剂、叶绿体类异戊二烯合成抑制剂和细胞壁生物合成抑制剂。其他除草剂包括具有未知作用模式或不落入(b1)至(b14)列出的具体类别中或通过以上列出的作用模式的组合起作用的那些除草剂。其他除草剂的实例包括苯草醚、磺草灵、杀草强、比克罗宗、溴丁酰草胺、环庚草醚、异噁草酮、苄草隆、cyclopyrimorate(6
‑
氯
‑3‑
(2
‑
环丙基
‑6‑
甲基苯氧基)
‑4‑
哒嗪基4
‑
吗啉羧酸酯)、杀草隆、野燕枯、乙氧苯草胺、伏草隆、抑草丁、调节膦、调节膦
‑
铵、棉隆、杀草隆、三唑酰草胺(1
‑
(2,4
‑
二氯苯基)
‑
n
‑
(2,4
‑
二氟苯基)
‑
1,5
‑
二氢
‑
n
‑
(1
‑
甲基乙基)
‑5‑
氧代
‑
4h
‑
1,2,4
‑
三唑
‑4‑
甲酰胺)、威百亩、甲基杀草隆、油状物酸、噁嗪草酮、壬酸、稗草畏和5
‑
[[(2,6
‑
二氟苯基)甲氧基]甲基]
‑
4,5
‑
二氢
‑5‑
甲基
‑3‑
(3
‑
甲基
‑2‑
噻吩基)异噁唑。
[0162]“除草剂安全剂”(b16)是加入除草剂制剂中以消除或减少除草剂对某些作物的植物性毒素效应的物质。这些化合物保护作物免受除草剂伤害,但通常不能防止除草剂控制不希望植被。除草剂安全剂的实例包括但不限于解草酮、解草酯、苄草隆、解草胺腈、环丙磺酰胺、杀草隆、二氯丙烯胺、大赛克农(dicyclonon)、增效磷(dietholate)、哌草丹、解草唑、解草啶、解草安、氟草肟、解草噁唑、双苯噁唑酸、吡唑解草酯、梅芬内(mephenate)、去草酮、萘二甲酸酐、解草腈、n
‑
(氨基羰基)
‑2‑
甲基苯磺酰胺和n
‑
(氨基羰基)
‑2‑
氟苯磺酰胺、1
‑
溴
‑4‑
[(氯甲基)磺酰基]苯、2
‑
(二氯甲基)
‑2‑
甲基
‑
1,3
‑
二氧戊环(mg 191)、4
‑
(二氯乙酰基)
‑1‑
氧杂
‑4‑
氮杂螺[4.5]癸烷(mon 4660)、2,2
‑
二氯
‑1‑
(2,2,5
‑
三甲基
‑3‑
噁唑烷基)
‑
乙酮和2
‑
甲氧基
‑
n
‑
[[4
‑
[[(甲基氨基)羰基]氨基]苯基]磺酰基]
‑
苯甲酰胺。
[0163]
具有式1的化合物可以通过合成有机化学领域已知的一般方法制备。如方案1
‑
19中描述的以下方法和变型中的一种或多种可用于制备具有式1的化合物。除非另外指明,以下具有式1
‑
28的化合物中的q、r1、r2、r3、y、r4、r5、n、r6、w和r9的定义如以上发明内容中所定义。除非另外指明,具有式1a、1b、1c、4a、5a、5a'、5a”、5c和8a的化合物是具有式1的化合物的子集,并且式1a、1b、1c、4a、5a、5a'、5a”、5c和8a的所有取代基如以上对于式1所定义。
[0164]
如方案1中所示,具有式1a的化合物(即其中y是o的具有式1的化合物)可以通过具有式2的酸与具有式3的胺在脱水偶联试剂的存在下的反应来制备,该脱水偶联试剂诸如丙基膦酸酐、二环己基碳二亚胺、n
‑
(3
‑
二甲基氨基丙基)
‑
n'
‑
乙基碳二亚胺、n,n'
‑
羰基二咪唑、2
‑
氯
‑
1,3
‑
二甲基咪唑鎓氯化物或2
‑
氯
‑1‑
甲基吡啶鎓碘化物。聚合物负载的试剂,如聚合物负载的环己基碳化二亚胺,也是合适的。这些反应典型地在从0℃
‑
60℃范围内的温度下在溶剂如二氯甲烷、乙腈、n,n
‑
二甲基甲酰胺或乙酸乙酯中,在碱例如三乙胺、n,n
‑
二异丙胺或1,8
‑
二氮杂二环[5.4.0]十一碳
‑7‑
烯的存在下进行。对于采用丙基膦酸酐的偶联条件,参见organic process research&development[有机加工研究与开发]2009,13,900
‑
906。
[0165]
方案1
[0166][0167]
如方案2中所示,具有式2的化合物可以通过具有式4的酯的水解通过本领域技术人员已知的方法来制备。水解用碱水溶液或酸水溶液典型地在共溶剂的存在下进行。用于反应的合适的碱包括但不限于氢氧化物如氢氧化钠和氢氧化钾,以及碳酸盐如碳酸钠和碳酸钾。用于反应的合适的酸包括但不限于无机酸如盐酸、氢溴酸和硫酸,以及有机酸如乙酸和三氟乙酸。多种多样的共溶剂适用于反应,包括但不限于甲醇、乙醇和四氢呋喃。反应在从
‑
20℃至溶剂的沸点、并且典型地从0℃至100℃的范围内的温度下进行。另外,具有式2的化合物(其中r1是h)可以通过烷基化反应进一步转化为具有式2的化合物(其中r1是烷基、卤代烷基、环烷基、环烷基烷基)。多种碱和烷基化剂是可能的,但优选的方法是在0℃下用在四氢呋喃中的过量叔丁醇钾处理具有式2的化合物(其中r1是h)并添加烷基化试剂。
[0168]
方案2
[0169][0170]
如方案3中所示,具有式4a的化合物(其中r1是h的具有式4的化合物)可以通过还原具有式5的化合物并且随后原位环化所得中间体胺来获得。用于还原具有式5的化合物中的脂肪族硝基的各种方法在文献中是已知的。本领域技术人员已知的方法包括在碳载钯或酸性介质中的雷尼镍、铁或锌金属(参见,例如,berichte der deutschen chemischen gesellschaft 1904,37,3520
‑
3525)和氢化铝锂的存在下的催化氢化。脂肪族硝基的还原还可以在诸如甲醇的质子源的存在下,用碘化钐(ii)来实现(参见例如,tetrahedron letters[四面体通讯]1991,32(14),1699
‑
1702)。可替代地,可以使用在镍催化剂如乙酸镍(ii)或氯化镍(ii)存在下的硼氢化钠(参见例如,四面体通讯1985,26(52),6413
‑
6416)。
[0171]
方案3
[0172][0173]
如方案4中所示,具有式5的化合物可以通过典型地在碱的存在下使具有式6的二
酯与具有式7的硝基烷反应来制备。用于反应的合适的碱包括碱金属低级醇盐如甲醇中的甲醇钠或乙醇中的乙醇钠。优选地,具有式6的二酯化合物和低级醇盐碱衍生自相同的醇。具有式6的化合物可以通过本领域技术人员已知的方法制备,例如通过醛和丙二酸酯的克脑文纳格尔缩合反应(参见例如g.jones,organic reactions[有机反应],第15卷,约翰威利父子出版社,1967)。
[0174]
方案4
[0175][0176]
具有式5a的化合物可以通过使具有式8的化合物与具有式9的丙二酸酯在碱的存在下反应来制备,如方案5中所示。用于该反应的合适的碱包括但不限于碱金属低级醇盐如甲醇中的甲醇钠或乙醇中的乙醇钠,或碱如在溶剂如四氢呋喃中的二(三甲基硅基)氨基锂、二(三甲基硅基)氨基钠和二异丙基氨基锂。典型地,该反应在从
‑
78℃至23℃的范围内进行。用于进行该转化的条件参见synthesis[合成]2005,2239
‑
2245。在不存在催化剂下在回流水中进行这种转化的条件在synthetic communications[合成通讯]2013,43,744
‑
748中有报道。
[0177]
方案5
[0178][0179]
具有式6的化合物可以通过具有式14的醛和具有式9的丙二酸酯的克脑文纳格尔缩合反应来制备,如方案6中所示。同样如方案6中所示,具有式8的化合物可以通过具有式14的醛和硝基甲烷的克脑文纳格尔缩合反应来制备。
[0180]
方案6
[0181][0182]
具有式5a'和5a”的化合物可以通过在手性催化剂的存在下和任选地在合适的碱的存在下使具有式8的硝基烯烃与具有式9的丙二酸酯反应来立体选择性地制备,如方案7中所示。合适的催化剂包括但不限于具有邻位二胺配体的ni(ii)如双[(r,r)
‑
n,n
’‑
二苄基
环己烷
‑
1,2
‑
二胺]二溴化镍(ii)、双[(s,s)
‑
n,n'
‑
二苄基环己烷
‑
1,2
‑
二胺]二溴化镍(ii)或具有手性1,1'
‑
二(四氢异喹啉)型二胺的溴化镍(ii)。用于该反应的合适的有机碱包括但不限于哌啶、吗啉、三乙胺、4
‑
甲基吗啉或n,n
‑
二异丙基乙胺。这种转化可以纯地或在溶剂如四氢呋喃、甲苯或二氯甲烷中完成。典型地,该反应在从
‑
78℃至80℃的范围内使用0至1当量的催化剂和任选地0至1当量的碱进行。实现该转化的条件已经报告于j.am.chem.soc.[美国化学学会杂志]2005,9958
‑
9959或eur.j.org.chem.[欧洲有机化学]2011,5441
‑
5446的条件中。具有式8的硝基烯烃可以通过本领域技术人员已知的方法由醛和硝基甲烷制备。
[0183]
方案7
[0184][0185]
如方案8中所示,具有式10的化合物可以通过使具有式11的化合物与具有式7的化合物在溶剂中在碱的存在下类似于方案4中描述的方法反应来制备。
[0186]
方案8
[0187][0188]
如方案9中所示,具有式10的化合物可以通过类似于方案5的方法使具有式8的硝基烯与具有式12的化合物反应来制备。
[0189]
方案9
[0190][0191]
如方案10中所示,具有式11a的化合物可以通过本领域技术人员已知的方法通过具有式12的丙二酰胺与具有式14的醛的反应来制备。还如方案10中所示,具有式12的丙二酰胺可以容易地通过本领域技术人员已知的方法由具有式13的低级烷基丙二酰氯如甲基丙二酰氯和具有式3的胺制备。
[0192]
方案10
[0193][0194]
如方案11中所示,具有式1b的化合物可以通过在碱的存在下具有式15的化合物与具有式16的异氰酸酯的反应来制备。可以用于本发明方法的碱的实例包括对于方案4的方法列出的那些。反应温度可以选自从
‑
78℃至所用的惰性溶剂的沸点的范围。典型地,该反应在范围从
‑
78℃至100℃的温度下在溶剂诸如甲苯中进行。
[0195]
方案11
[0196][0197]
如方案12中所示,具有式15的化合物可以通过在碱的存在下具有式17的化合物与相应的具有式18的亲电体的反应来制备。在式18中,g表示离去基团,即离核体。取决于r1的选择,用于该反应的合适的亲电体可以包括烷基卤化物诸如氯化物、溴化物和碘化物,烷基磺酸盐。用于反应的合适的碱包括无机碱如碱金属或碱土金属(例如,锂、钠、钾和铯)氢氧化物、醇盐、碳酸盐和磷酸盐,以及有机碱如三乙胺、n,n
‑
二异丙基乙胺和1,8
‑
二氮杂二环[5.4.0]十一碳
‑7‑
烯。各种溶剂适用于该反应,包括例如但不限于四氢呋喃、二氯甲烷、n,n
‑
二甲基甲酰胺、n,n
‑
二甲基乙酰胺、n
‑
甲基吡咯烷酮、乙腈、c2‑
c6醇和丙酮以及这些溶剂的混合物。该反应在范围从
‑
20℃至200℃、并且典型地在0℃与50℃之间的温度下进行。
[0198]
方案12
[0199][0200]
如方案13中所示,具有式17的化合物可以通过具有式2的酸的脱羧通过本领域技术人员已知的方法来制备。通过将具有式2的化合物在溶剂中加热,典型地在酸的存在下进行脱羧。用于该反应的合适的酸包括但不限于对甲苯磺酸。各种共溶剂适用于该反应,包括但不限于甲苯、乙酸异丙酯和甲基异丁基酮。该反应在范围从
‑
20℃至溶剂的沸点、并且典型地从0℃至150℃的温度下进行。
[0201]
方案13
[0202][0203]
如方案14所示,具有式1c的化合物(即其中r1是h并且y是s的具有式1的化合物)可以通过使具有式1a的化合物与至少一当量的硫化试剂(如劳森试剂、十硫化四磷或五硫化二磷)在溶剂(如四氢呋喃或甲苯)中反应来制备。典型地,该反应在范围从0℃至115℃的温度下进行。
[0204]
方案14
[0205][0206]
具有式8的化合物还可以由具有式19的硝基烯胺与具有式20的格式试剂或锂试剂的反应来制备,如方案15中详述的。参见severin的chem.ber.[化学学报]1969,102,2966
‑
71中该反应和条件的实例。格氏试剂和锂试剂可以通过在已知的或可商购的溴化物和碘化物上的卤素金属交换反应来制备。
[0207]
方案15
[0208][0209]
用作具有式6和8的化合物的起始材料的具有式14的醛和卤化物(制备具有式20的化合物的前体)是可商购的或本领域技术人员已知的。用于合成起始化合物(当q是q
‑
1时并且其中r4是烷基或卤代烷基)的有用方法在j.heterocyclic chem.[杂环化学杂志]1989,26,895
‑
98中找到。用于合成吡唑起始材料(其中q是q
‑
1或q
‑
2)的方法的综述在chem.rev.[化学评论]2011,111,6984
‑
7034和其中所引用的参考文献中找到。用于合成吲唑化合物(其中q是q
‑
3)的有用方法可以在世界专利申请wo 2011/050245和wo 2018/177781中以及在molecules[大分子]2018,23(11),2783和其中所引用的参考文献中找到。使吡唑在3
‑
、4
‑
、以及5
‑
位上官能化的金属化反应已经在慕尼黑大学(lmu)christina despotopoulou于2009年的论文和其中所引用的参考文献中详述。
[0210]
具有式14的化合物(其中q是q
‑
1并且r3是烷基或卤代烷基)的合成示于方案16中。可以使具有式21化合物与具有式22的化合物在碱的存在下反应以提供具有式23的中间体。
具有式23的化合物转而又可以通过与烷基肼反应被环化以形成吡唑啉(当r3是卤代烷基时)和吡唑(当r3是烷基时),其可以在一个步骤使用酸的水溶液被水解和脱水以提供具有式14的化合物(其中q是q
‑
1)。用于环化的碱可以是但不限于碱金属氢氧化物和低级醇盐如甲醇钠、叔丁醇钾和叔丁醇钠,碱金属氢化物如氢化钠、六甲基二硅基氨基钠、六甲基二硅基氨基钾、以及六甲基二硅基氨基锂。酸的水溶液(诸如但不限于盐酸、硫酸、乙酸和三氟乙酸)适用于水解/脱水步骤。
[0211]
方案16
[0212][0213]
合成具有式4的化合物的替代性路径示出于方案17中。具有式24的化合物与具有式25的丙烯酸酯的环加成产生具有受保护的硫代羰基的吡咯烷酮环体系(例如,具有式26的化合物)。硫代羰基可以在氧化条件下用试剂诸如过硫酸氢钾制剂和过氧化氢水解成羰基。对于进行这些环加成的条件和合成具有式24的化合物的方法,参见fishwick,tet.lett.[四面体通讯]1995,36,9409
‑
9412和引用文献诸如eur.j.org.chem.[欧洲有机化学]2001,3533
‑
3544。具有式25的丙烯酸酯可以通过具有式14的醛的维蒂希(wittig)或霍纳尔
‑
沃兹沃思
‑
埃蒙斯(horner
‑
emmons wadsworth)反应或者通过相应的卤化材料的赫克(heck)反应容易地制备。
[0214]
方案17
[0215][0216]
用于合成具有式1的化合物的另一有用的方法示出于方案18中。具有式27的硼酸与具有式28的不饱和吡咯烷酮的铑催化加成在铑催化剂的存在下直接得到具有式1的化合物(hayashi反应)。用于进行hayashi反应的多种条件和催化剂由frost等人在chem.soc.rev.[化学会评论]2010,39,2093
‑
2105和其中的参考文献中提供。该综述文章还描述了用于提供对映异构体纯的产物的条件。具有式28的不饱和吡咯烷酮可以由熟知的饱和吡咯烷酮通过许多类型的脱氢条件例如苯基硒化物消除来制备。
[0217]
方案18
[0218][0219]
本领域的技术人员认识到,各种官能团可被转变成其他以提供不同的具有式1的化合物。对于以简单且直接的方式说明官能团的相互转换的有价值的资源,参见larock,r.c.,comprehensive organic transformations:a guide to functional group preparations[综合有机转化:官能团制备的指引],第2版,wiley
‑
vch,纽约,1999。例如,用于制备具有式1的化合物的中间体可包含芳族硝基,这些芳族硝基可被还原成氨基,并且然后经由本领域熟知的反应(诸如桑德迈尔反应)被转换成各种卤化物,从而提供具有式1的化合物。在许多情况下,上述反应还可以以交替的顺序进行。
[0220]
应认识到,上述对于制备具有式1的化合物所描述的某些试剂和反应条件可能不与中间体中存在的某些官能团相容。在这些情况下,将保护/去保护序列或官能团相互转换结合到合成中将有助于获得所期望的产物。保护基团的使用和选择对于化学合成领域的技术人员将是显而易见的(参见,例如,greene,t.w.;wuts,p.g.m.protective groups in organic synthesis[有机合成中的保护基团],第2版;wiley:纽约,1991)。本领域的技术人员将认识到,在一些情况下,在按照任何单独方案中描绘的引入给定试剂后,可能需要进行没有详细描述的额外常规合成步骤以完成具有式1的化合物的合成。本领域的技术人员还将认识到,可能需要以与制备具有式1的化合物所具体呈现的顺序不同的顺序来进行以上方案中示出的步骤的组合。
[0221]
本领域的技术人员还将认识到,本文所述的具有式1的化合物和中间体可经受各种亲电反应、亲核反应、自由基反应、有机金属反应、氧化反应和还原反应以添加取代基或改性现有的取代基。
[0222]
无需进一步详尽说明,据信本领域技术人员使用前述说明可将本发明利用至其最大程度。以下非限制性实例是本发明的例示。以下实例中的步骤示出了在整体合成转化中每个步骤的程序,并且用于每个步骤的起始物质并不必须由其程序描述于其他实例或步骤中的具体制备试验来制备。百分比是按重量计,除了色谱溶剂混合物或除非另外指明之外。除非另外指明,色谱溶剂混合物的份数和百分比是按体积计。1h nmr谱以距四甲基硅烷的低场的ppm来报告;“s”意指单峰、“d”意指双重峰、“t”意指三重峰、“q”意指四重峰、“m”意指多重峰、“dd”意指两个双重峰、“br”意指宽峰、以及“br s”意指宽单峰。质谱(ms)报道为通过使用液相色谱法与质谱仪结合(lcms)使用大气压化学电离(ap+)观察到的通过向分子中加入h+(分子量为1)形成的最高同位素丰度母离子(m+1)或从分子损失h+(分子量为1)形成的(m
‑
1)的分子量,其中“amu”代表统一原子质量单位。
[0223]
合成实例1
[0224]
(3s,4r)
‑
n
‑
(2,3
‑
二氟苯基)
‑1‑
甲基
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷甲酰胺(化合物13)的制备
[0225]
步骤a:4,4
‑
二乙氧基
‑
1,1,1
‑
三氟
‑3‑
丁烯
‑2‑
酮的制备
[0226]
向在0℃下的原乙酸三乙酯(450g,2.77mol)和吡啶(550g,6.9mol)在二氯甲烷(3500ml)中的溶液中逐滴添加三氟乙酸酐(1135g,5.54mol)。将反应混合物在环境温度下搅拌过夜,然后用冷的饱和nahco3溶液淬灭,然后用水洗涤。将有机层经硫酸钠干燥、在减压下浓缩并在真空下干燥以提供呈油状物的标题化合物(500g,85%)。
[0227]1h nmr(300mhz,cdcl3)δ4.94(s,1h),4.37(q,2h),4.15(q,2h),1.46(t,3h),1.42(t,3h)。lc
‑
ms(esi)m/z 213(m+h)
+
。
[0228]
步骤b:(3e)
‑4‑
氨基
‑4‑
乙氧基
‑
1,1,1
‑
三氟
‑3‑
丁烯
‑2‑
酮的制备
[0229]
向在室温下的4,4
‑
二乙氧基
‑
1,1,1
‑
三氟
‑3‑
丁烯
‑2‑
酮(即步骤a中所获得的产物,500g,2.35mol)在乙腈(2500ml)中的溶液中逐滴添加nh4oh在水中的28%溶液(500ml)。将反应混合物在环境温度下搅拌过夜。在减压下去除溶剂,并添加二氯甲烷,然后用水洗涤。将有机层经硫酸钠干燥并在减压下浓缩以提供呈固体的标题化合物(325g,75%)。
[0230]1h nmr(300mhz,cdcl3)δ9.79(br,1h),5.66br,1h),5.13(s,1h),4.15(q,2h),1.38(t,3h)。lc
‑
ms(esi)m/z 184(m+h)
+
。
[0231]
步骤c:1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
胺的制备
[0232]
在环境温度下,向(3e)
‑4‑
氨基
‑4‑
乙氧基
‑
1,1,1
‑
三氟
‑3‑
丁烯
‑2‑
酮(即步骤b中所获得的产物,325g,1.76mol)和硫酸甲肼(1:1,299g,2.11mol)在乙醇(1500ml)中的悬浮液中添加三乙胺(285g,2.8mol)。将反应混合物加热并在95℃下搅拌7h。将反应混合物在减压下浓缩并将所得残余物用水稀释并用nahco3溶液使其成碱性并用二氯甲烷萃取。将有机萃取物经硫酸钠干燥,然后在减压下浓缩。将所得粗产物通过硅胶色谱法(用5%至25%乙酸乙酯/己烷作为洗脱液洗脱)纯化,以提供呈棕色低熔点固体的标题化合物(75g,25%)。
[0233]1h nmr(300mhz,cdcl3)δ5.94(s,1h),3.78(s,3h),3.67(br,2h)。lc
‑
ms(esi)m/z 166(m+h)
+
。
[0234]
步骤d:3
‑
碘
‑1‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑的制备
[0235]
在
‑
10℃下向1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
胺(75g,0.454mol)在盐酸(浓的,750ml)中的溶液中逐滴添加亚硝酸钠(38g,0.545mol)溶解于水(50ml)中的溶液。将反应混合物在
‑
10℃下搅拌30min,然后在
‑
10℃下逐滴添加碘化钾(162g,0.98mol)在水(200ml)中的溶液。在1h内使反应物质缓慢达到环境温度。将反应混合物用水和二氯甲烷稀释。添加硫代硫酸钠的饱和溶液,得到澄清溶液。将有机层分离、经硫酸钠干燥并在减压下浓缩。将粗产物通过硅胶色谱法(用在己烷中的5%至10%乙酸乙酯洗脱)纯化,以提供呈浅黄色液体的标题化合物(70g,55%)。
[0236]1h nmr(400mhz,cdcl3)δ4.01(d,j=0.61hz,3h)6.76(s,1h)。lc
‑
ms(esi)m/z 277(m+h)
+
。
[0237]
步骤e:1
‑
甲基
‑3‑
[(1e)
‑2‑
硝基乙烯基]
‑5‑
(三氟甲基)
‑
1h
‑
吡唑的制备
[0238]
在
‑
20℃下将异丙基氯化镁
‑
氯化锂复合物(在四氢呋喃中的1.3m溶液,293ml,0.382mmol)逐滴添加到在四氢呋喃(700ml)中的3
‑
碘
‑1‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑(即步骤d的产物,70g,0.254mol)中,并在相同温度下搅拌2h。添加1
‑
(二甲基氨基)
‑2‑
硝基乙烯(44.5g,0.382mol)在四氢呋喃(200ml)中的溶液,并在1h的时间段内将反应缓慢升温至室温。将反应小心地用盐酸水溶液(2m)淬灭,然后搅拌1h并用乙酸乙酯萃取。将有机层用盐
水洗涤、经硫酸钠干燥、过滤并浓缩至硅胶上以通过硅胶色谱法(用10%乙酸乙酯/石油状物醚洗脱)纯化,以提供呈黄色油状物的标题化合物(35g,62%)。
[0239]1h nmr(400mhz,cdcl3)δ7.89(d,j=13.7hz,1h),7.63(d,j=13.7hz,1h),6.88(s,1h),4.05(d,j=0.6hz,3h)。lc
‑
ms(esi)m/z 222(m+h)
+
。
[0240]
步骤f:2
‑
[(1s)
‑1‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
硝基乙基]丙二酸1,3
‑
二乙酯的制备
[0241]
向1
‑
甲基
‑3‑
[(1e)
‑2‑
硝基乙烯基]
‑5‑
(三氟甲基)
‑
1h
‑
吡唑(即步骤e中所获得的产物,35g,0.158mol)在甲苯(100ml)中的溶液中添加丙二酸二乙酯(32.8g,0.205mol),随后添加双[(1r,2r)
‑
n1,n2
‑
双(苯基甲基)
‑
1,2
‑
环己二胺
‑
n1,n2]二溴
‑
(oc
‑6‑
12)
‑
2镍(0.02当量,2.5g,3.16mmol),并将混合物在环境温度下搅拌16h。然后将反应混合物在减压下浓缩并将所得残余物通过柱色谱法(用25%乙酸乙酯/石油状物醚洗脱)纯化,以得到呈浅粉色
‑
黄色油状物的标题化合物(55g,92%)。
[0242]1h nmr:(400mhz,cdcl3)δ6.53(s,1h),5.01(dd,1h),4.88(dd,j=4.3,13.9hz,1h),4.35(dd,j=4.4,7.7,9.0hz,1h),4.22(q,2h),4.16(q,j=7.1hz,2h),3.90(s,3h),3.89(d,1h),1.26(t,3h),1.20(t,j=7.2hz,3h)。lc
‑
ms(esi)m/z 382(m+h)
+
。
[0243]
步骤g:(3r,4r)
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷羧酸乙酯的制备
[0244]
在0℃
‑
5℃(冰浴)下在氮气下向2
‑
[(1s)
‑1‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
硝基乙基]丙二酸1,3
‑
二乙酯(即步骤f中所获得的产物,55g,21.9mmol)在乙醇(500ml)中的溶液中添加氯化镍(ii)六水合物(5.45g,22.9mmol)。然后将硼氢化钠(2.5g,65.7mmol)分批添加(伴随鼓泡)至浅绿色
‑
蓝色溶液中。一旦添加第一份硼氢化钠,反应混合物就变成黑色。30min后,移除冷却并使反应混合物升温至环境温度。将反应混合物在环境温度下搅拌另外3h。将反应混合物在冰水浴中冷却至约5℃
‑
10℃,并用nh4cl溶液缓慢淬灭。将混合物用乙酸乙酯(2000ml)稀释,并通过硅藻土助滤剂床过滤,用若干份水和乙酸乙酯洗涤。将有机层分离,用水、饱和盐水溶液洗涤,经硫酸钠干燥并在减压下浓缩。将残余物通过柱色谱法(用50%乙酸乙酯/石油状物醚洗脱)纯化,以得到呈黄色油状物的标题化合物(23g,52%)。
[0245]1h nmr:(400mhz,cdcl3)δ6.91(br s,1h),6.47(s,1h),4.28(q,j=7.2hz,2h),4.14(q,1h),3.94(d,3h),3.80(d,j=1.0,9.0hz,1h),3.63(d,j=9.3hz,1h),3.52(dd,j=8.2,9.5hz,1h),1.32(t,j=7.2hz,3h)。lc
‑
ms(esi)m/z 306(m+h)
+
。
[0246]
步骤h:(3r,4r)
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷羧酸的制备
[0247]
在0℃下,向(3r,4r)
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷羧酸乙酯(即步骤g中所获得的产物,20g,65.5mmol)在甲醇和四氢呋喃的混合物(1:1,150ml)中的溶液中添加在50ml的水中的氢氧化锂(3.73g,98.3mmol)。然后将反应物质在环境温度下搅拌2h,然后用水稀释并用甲基叔丁基醚洗涤。将水层用盐酸水溶液(1.5n)酸化并用乙酸乙酯萃取。将乙酸乙酯层用饱和盐水溶液洗涤、经硫酸钠干燥并在减压下浓缩以提供呈淡黄色液体的14g的标题化合物(77%)。
[0248]1h nmr:(400mhz,cdcl3)δ6.59(s,1h),4.09(q,1h),3.94(s,3h),3.85
‑
3.77(m,
1h),3.72(d,j=10.0hz,1h),3.66
‑
3.58(m,1h)。lc
‑
ms(esi)m/z 278(m+h)
+
。
[0249]
步骤i:(3r,4r)
‑1‑
甲基
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷羧酸的制备
[0250]
在0℃下,将(3r,4r)
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷羧酸(即步骤h中所获得的产物,14g,50.5mmol)在干燥四氢呋喃(75ml)中的溶液添加至叔丁醇钾(在四氢呋喃中的1m溶液,126ml)在四氢呋喃(75ml)中的溶液中。在0℃下逐滴添加碘甲烷(7.2g,101mmol)。将反应混合物在环境温度下搅拌2h,然后用水稀释,用盐酸水溶液(1.5n)酸化并用乙酸乙酯萃取。将有机层用饱和盐水溶液洗涤、经硫酸钠干燥并在减压下浓缩以提供呈淡黄色液体的10g的标题化合物(68%)。
[0251]1h nmr:(400mhz,cdcl3)δ6.68(s,1h),3.97(q,1h),3.94(s,3h),3.76
‑
3.68(m,3h),2.99(s,3h)。lc
‑
ms(esi)m/z 292(m+h)
+
。
[0252]
步骤j:(3s,4r)
‑
n
‑
(2,3
‑
二氟苯基)
‑1‑
甲基
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷甲酰胺的制备
[0253]
在环境温度下,向(3r,4r)
‑1‑
甲基
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷羧酸(10g,34.3mmol)在乙酸乙酯(100ml)中的溶液中添加三乙胺(10.41g,103mmol)。在0℃下逐滴添加t3p(在乙酸乙酯中的50%溶液,32.7g,51.5mmol)。将反应物质在环境温度下搅拌12h,然后用水、饱和盐水溶液洗涤,经硫酸钠干燥并在减压下浓缩。将所获得的残余物通过柱色谱法(用50%乙酸乙酯/石油状物醚洗脱)纯化,以提供呈浅粉色固体的标题化合物(10g,68%)。
[0254]1h nmr:(400mhz,cdcl3)δ10.16(br s,1h),8.08
‑
8.01(m,1h),7.02(ddt,j=2.1,5.9,8.3hz,1h),6.93
‑
6.84(m,1h),6.69(s,1h),4.09(q,1h),3.94(s,3h),3.78(d,j=9.5hz,1h),3.76
‑
3.65(m,2h),2.98(s,3h)。lc
‑
ms(esi)m/z 403(m+h)
+
。
[0255]
合成实例2
[0256]
(3s,4r)
‑
n
‑
(2,3
‑
二氟苯基)
‑1‑
甲基
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷甲酰胺(化合物13)的替代制备
[0257]
步骤a:1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
羧醛的制备
[0258]
将1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
甲醇(6.7g)在二氯甲烷(60ml)中的搅拌溶液用冰浴冷却。在5分钟内分批添加氯铬酸吡啶(9.6g)。添加硅藻土助滤剂(15g),并将反应在环境温度下搅拌2.5h。将反应通过硅藻土助滤剂塞过滤,然后在16℃下在减压下浓缩。将所得黑色油状物吸收在乙醚中并通过二氧化硅塞,然后在16℃下在减压下浓缩以提供呈澄清油状物的标题化合物(4.8g)。
[0259]1h nmr(500mhz,cdcl3)δ9.95(s,1h),7.14(s,1h),4.11(m,3h)。
[0260]1‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
羧醛的替代制备
[0261]
步骤a1:5,5,5
‑
三氟
‑4‑
羟基
‑
1,1
‑
二甲氧基
‑3‑
戊烯
‑2‑
酮的制备
[0262]
在
‑
5℃下在氮气下,在30min内将甲基乙二醛1,1
‑
二甲基乙缩醛(17.7g)和三氟乙酸乙酯(27g)在乙醚(90ml)中的混合物逐滴添加至甲醇钠(在甲醇中30wt%,40g)在乙醚(210ml)中的搅拌溶液中。将反应在
‑
5℃与4℃之间的温度下搅拌2h,然后倒入浓盐酸(30ml)和冰屑(150g)的搅拌浆液中。将各层分离并用乙醚和甲基叔丁基醚萃取水相,然后将合并的有机萃取物用饱和氯化铵水溶液洗涤、经硫酸钠干燥并在减压下浓缩以提供呈浅
橙色油状物的标题化合物(30.5g),将其不经进一步纯化用于下一步骤。
[0263]1h nmr(500mhz,cdcl3,烯醇互变异构体)δ6.33(s,1h),4.82(s,1h),3.43(s,6h)。
[0264]
步骤a2:3
‑
(二甲氧基甲基)
‑
4,5
‑
二氢
‑1‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑5‑
醇的制备
[0265]
在
‑
5℃下在氮气下,在15min内将甲基肼(6.9g)在甲醇(75ml)中的溶液逐滴添加至5,5,5
‑
三氟
‑4‑
羟基
‑
1,1
‑
二甲氧基
‑3‑
戊烯
‑2‑
酮(即步骤a的产物,30.5g)在甲醇(150ml)中的搅拌溶液中。将反应混合物在
‑
5℃与4℃之间的温度下搅拌1h,然后在减压下浓缩以提供橙色油状物(34g)。将油状物在硅胶上层析,用在二氯甲烷中的0%
‑
30%甲基叔丁基醚洗脱,以提供呈浅黄色油状物的标题化合物(23.7g)。
[0266]1h nmr(500mhz,cdcl3)δ4.92(s,1h),3.43(s,3h),3.37(s,3h),3.25
‑
3.21(m,1h),2.99(s,3h),2.95
‑
2.92(m,1h)。
[0267]
步骤a3:1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
羧醛的制备
[0268]
在
‑
36℃下,在10min内将浓盐酸(100ml)逐滴添加至3
‑
(二甲氧基甲基)
‑
4,5
‑
二氢
‑1‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑5‑
醇(即步骤a2的产物,31.1g)在乙醚(300ml)中的搅拌溶液中。然后使反应混合物升温至室温并剧烈搅拌2h。然后分离各层并将水相用乙醚萃取两次。将合并的有机萃取物用饱和氯化铵水溶液(1
×
)洗涤、经硫酸钠干燥并在低于25℃下在减压下浓缩以提供呈浅黄色油状物的标题化合物(18.9g)。
[0269]1h nmr(500mhz,cdcl3)δ9.95(s,1h),7.14(s,1h),4.11(br s,3h)。
[0270]
步骤b:1
‑
甲基
‑3‑
[(1e)
‑2‑
硝基乙烯基]
‑5‑
(三氟甲基)
‑
1h
‑
吡唑的制备
[0271]
向1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
羧醛(即步骤a或a3的产物,4.8g)在甲醇(50ml)中的搅拌溶液中添加硝基甲烷(1.5ml)。将混合物冷却至
‑
5℃并在15min内逐滴添加用水(10ml)稀释的氢氧化钠水溶液(50wt%,2.3g),维持温度低于0℃。在0℃与5℃之间再继续搅拌3h,然后将反应混合物倒入1n盐酸水溶液(50ml)中。将反应混合物转移至分液漏斗并用乙酸乙酯(3
×
50ml)萃取水相。将合并的有机萃取物用盐水洗涤、经硫酸镁干燥并在减压下浓缩以提供黄色油状物(5.5g)。
[0272]
将由此获得的中间体(5.5g)吸收在甲苯(50ml)中。用干冰/丙酮浴将溶液冷却至
‑
10℃,并经由注射器添加甲磺酰氯(2.0ml)。然后在15min内逐滴添加三乙胺(7.3ml),维持温度在0℃或低于0℃。然后将所得溶液在相同温度下搅拌2h。将反应混合物倒入1n盐酸水溶液(60ml)中并转移至分液漏斗。将水相用乙酸乙酯(3
×
50ml)萃取,然后将合并的有机萃取物用盐水洗涤、经硫酸镁干燥并在减压下浓缩。将粗材料在硅胶上层析,用在己烷中的0%
‑
10%乙酸乙酯梯度洗脱,以提供呈琥珀色油状物的标题化合物(3.2g)。
[0273]1h nmr(500mhz,cdcl3)δ7.90
‑
7.87(m,1h),7.64
‑
7.62(m,1h),6.88(s,1h),4.06(m,3h)。
[0274]
步骤c:2
‑
[(1s)
‑1‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
硝基乙基]丙二酸1,3
‑
二乙酯的制备
[0275]
向1
‑
甲基
‑3‑
[(1e)
‑2‑
硝基乙烯基]
‑5‑
(三氟甲基)
‑
1h
‑
吡唑(即步骤b的产物,3.2g)和丙二酸二乙酯(3.3ml)在甲苯(25ml)中的搅拌混合物中添加双[(r,r)
‑
n,n'
‑
二苄基环己烷
‑
1,2
‑
二胺]溴化镍(ii)(如j.am.chem.soc.[美国化学会志]2005,127,9958
‑
9959中描述的制备;0.232g)。将所得溶液在环境温度下搅拌16h。然后在减压下除去挥发物以提
供呈琥珀色油状物的标题化合物(5.7g),将其不经纯化使用。
[0276]1h nmr(500mhz,cdcl3)δ6.53(s,1h),5.03
‑
4.98(m,1h),4.90
‑
4.86(m,1h),4.37
‑
4.33(m,1h),4.25
‑
4.14(m,4h),3.90
‑
3.88(m,4h),1.28
‑
1.19(m,6h)。
[0277]
步骤d:(3r,4r)
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷羧酸乙酯的制备
[0278]
将2
‑
[(1s)
‑1‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
硝基乙基]丙二酸1,3
‑
二乙酯(即步骤c的产物,5.7g)、氯化镍(ii)六水合物(3.55g)和乙醇(60ml)的搅拌混合物在冰浴中冷却并在10min内用硼氢化钠(1.7g)分批处理。将所得混合物在环境温度下搅拌18h。然后添加饱和氯化铵水溶液(100ml)和乙酸乙酯(100ml),并将混合物搅拌2h。分离各层,并将水层用乙酸乙酯(2
×
100ml)萃取。将合并的有机萃取物用饱和氯化铵溶液(100ml)和盐水(100ml)洗涤、经硫酸镁干燥并在减压下浓缩以提供呈粘性绿色油状物的标题化合物(5.2g),将其不经纯化使用。
[0279]1h nmr(500mhz,cdcl3)δ6.67(br s,1h),6.47(s,1h),4.30
‑
4.25(m,2h),4.16
‑
4.10(m,1h),3.94
‑
3.93(m,3h),3.81
‑
3.76(m,1h),3.63
‑
3.61(m,1h),3.54
‑
3.50(m,1h),1.33
‑
1.30(m,3h)。
[0280]
步骤e:(3r,4r)
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷羧酸的制备
[0281]
将(3r,4r)
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷羧酸乙酯(即步骤d的产物,5.2g)和氢氧化钠水溶液(50wt%,4.1g)在乙醇(50ml)中的混合物在环境温度下搅拌3h。然后将反应混合物用水(50ml)稀释并用乙醚(2
×
50ml)洗涤。将水相用浓盐酸酸化至ph 2并用乙酸乙酯(3
×
50ml)萃取。将合并的乙酸乙酯萃取物用盐水洗涤、经硫酸镁干燥并在减压下浓缩以提供呈白色固体的标题化合物(3.5g),将其不经进一步纯化使用。
[0282]1h nmr(500mhz,cdcl3)δ6.66(s,1h),6.34(br s,1h),4.08
‑
4.03(m,1h),3.94(m,3h),3.82
‑
3.78(m,1h),3.72
‑
3.67(m,2h)。
[0283]
步骤f:(3r,4r)
‑1‑
甲基
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷羧酸的制备
[0284]
将(3r,4r)
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷羧酸(即步骤e的产物,3.5g)在四氢呋喃(10ml)中的溶液逐滴添加至冰浴冷却的叔丁醇钾的悬浮液(1m,在四氢呋喃中,30.3ml)中,在添加期间维持温度低于5℃。将所得稠溶液在0℃下搅拌10min。经由注射器添加碘甲烷(1.34ml)并将反应在环境温度下再搅拌4h。在减压下除去溶剂,并将所得固体用水(50ml)和饱和碳酸氢钠水溶液(30ml)吸收并用乙醚(2
×
50ml)萃取。将水相用浓盐酸酸化至ph 2并用乙酸乙酯(3
×
50ml)萃取。将合并的乙酸乙酯萃取物用盐水洗涤、经硫酸镁干燥并在减压下浓缩以提供呈琥珀色油状物的标题化合物(3.5g)。
[0285]1h nmr(500mhz,cdcl3)δ6.68(s,1h),3.98
‑
3.88(m,4h),3.77
‑
3.67(m,3h),2.99(m,3h)。
[0286]
步骤g:(3s,4r)
‑
n
‑
(2,3
‑
二氟苯基)
‑1‑
甲基
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷甲酰胺的制备
[0287]
将(3r,4r)
‑1‑
甲基
‑4‑
[1
‑
甲基
‑5‑
(三氟甲基)
‑
1h
‑
吡唑
‑3‑
基]
‑2‑
氧代
‑3‑
吡咯烷
羧酸(即步骤f的产物,3.5g)、三乙胺(5ml)和2,3
‑
二氟苯胺(1.3ml)在二氯甲烷(40ml)中的混合物用冰浴冷却,并且然后用丙基膦酸酐(50wt%,在乙酸乙酯中,13.0g)处理。将所得混合物在环境温度下搅拌18h,然后在减压下浓缩。将粗材料在硅胶上层析,用在己烷中的0%
‑
50%乙酸乙酯梯度洗脱,以提供油状物状固体(2.3g)。然后将该材料用热己烷研磨以提供呈白色固体的标题化合物(2.1g)。
[0288]1h nmr(500mhz,cdcl3)δ10.16(br s,1h),8.06
‑
8.03(m,1h),7.03
‑
7.00(m,1h),6.91
‑
6.86(m,1h),6.69(s,1h),4.12
‑
4.06(m,1h),3.94(m,3h),3.79
‑
3.66(m,3h),2.98(m,3h)。
[0289]
通过本文所描述的程序与本领域已知的方法一起,可以制备表1至16中的下列化合物。以下缩写用于随后的表中:i意指异,me意指甲基,et意指乙基,pr意指丙基,i
‑
pr意指异丙基,ph意指苯基,ome意指甲氧基,oet意指乙氧基,sme意指甲硫基,s(o)me意指甲基亚磺酰基,以及s(o)2me意指甲基磺酰基。
[0290]
表1
[0291][0292]
r1是me,r6是h,w是ph(2
‑
f);y是o;并且q是;
[0293]
[0294][0295]
表2以与表1相同的方式构造,不同之处在于行标题“r1是me,r6是h,y是o,w是ph(2
‑
f);并且q是”被替换为以下表2列出的行标题(即w是ph(2,3
‑
二
‑
f);并且q是”)。因此,表2中的第一项是具有式1的化合物,其中r1是me,r6是h,y是o,w是ph(2,3
‑
二
‑
f);q是吡唑
‑3‑
基(1
‑
me,5
‑
cf3)。
[0296]
表3至16类似地构造。
[0297]
表行标题2r1是me,r6是h,y是o,w是ph(2,3
‑
二
‑
f);并且q是3r1是me,r6是h,y是o,w是ph(2,4
‑
二
‑
f);并且q是4r1是me,r6是h,y是o,w是ph(2,3,4
‑
三
‑
f);并且q是5r1是me,r6是h,y是o,w是ph(2
‑
cf3);并且q是6r1是me,r6是h,y是o,w是ph(2
‑
me);并且q是7r1是me,r6是h,y是o,w是ph(2
‑
no2);并且q是8r1是me,r6是h,y是o,w是ph(2
‑
cl);并且q是9r1是me,r6是h,y是o,w是ph(2
‑
so2me);并且q是10r1是me,r6是h,y是o,w是ph(2
‑
f,3
‑
cl);并且q是11r1是me,r6是h,y是o,w是ph(2
‑
some);并且q是12r1是me,r6是h,y是o,w是ph(2
‑
sme);并且q是13r1是me,r6是h,y是o,w是ph(2
‑
me,3
‑
f);并且q是14r1是me,r6是h,y是o,w是3
‑
吡啶基(2,6
‑
二
‑
f);并且q是15r1是me,r6是h,y是o,w是3
‑
吡啶基(2
‑
f);并且q是16r1是me,r6是h,y是o,w是2
‑
吡啶基(6
‑
f);并且q是
[0298]
本发明的化合物一般将用作组合物(即制剂)中的除草剂活性成分,其中至少一种选自由表面活性剂、固体稀释剂和液体稀释剂组成的组的附加组分,用作载体。选择该制剂或组合物成分,以与活性成分的物理特性、施用模式和环境因素诸如土壤类型、水分和温度一致。
[0299]
有用的制剂包括液体和固体组合物二者。液体组合物包括任选地可以被稠化成凝胶的溶液(包括可乳化的浓缩物)、悬浮液、乳液(包括微乳液、水包油状物乳液、可流动的浓
缩物和/或悬浮乳液)等。水性液体组合物的一般类型为可溶性浓缩物、悬浮液浓缩物、胶囊悬浮液、浓缩乳液、微乳液、水包油状物乳液、可流动的浓缩物和悬浮乳液。非水性液体组合物的一般类型为可乳化的浓缩物、可微乳化的浓缩物、可分散的浓缩物和油状物分散体。
[0300]
固体组合物的一般类型为粉剂、粉末、颗粒剂、球剂、粒料、锭剂、片剂、填充膜(包括种子包衣)等,它们可以是水可分散的(“可润湿的”)或水溶性的。由成膜溶液或可流动的悬浮液形成的膜和包衣特别可用于种子处理。活性成分可以被(微)包封并进一步形成为悬浮液或固体制剂;可替代地,活性成分的整个制剂可以被包封(或“包覆”)。包封可以控制或延迟活性成分的释放。可乳化的颗粒剂结合了可乳化的浓缩物制剂和干颗粒制剂两者的优点。高强度组合物主要用作进一步制剂的中间体。
[0301]
可喷雾的配制品通常在喷雾之前分散在适宜的介质中。此类液体和固体制剂被配制成在喷雾介质,通常为水,但偶尔另一种合适介质像芳族烃或石蜡烃或植物油状物中易于稀释的。喷雾体积的范围可以为每公顷从约一升至几千升,但更典型为在每公顷从约十至几百升的范围内。可喷雾的制剂可在槽中与水或另一种合适的介质混合,用于通过空气或地面施用来进行叶处理,或用于施用到植物的生长介质中。液体和干制剂可以直接计量加入滴灌系统中,或在种植期间计量加入垄沟中。
[0302]
制剂通常将含有总计达100重量百分比的在以下近似范围内的有效量的活性成分、稀释剂和表面活性剂。
[0303][0304][0305]
固体稀释剂包括,例如,粘土诸如膨润土、蒙脱土、凹凸棒石和高岭土、石膏、纤维素、二氧化钛、氧化锌、淀粉、糊精、糖(例如,乳糖、蔗糖)、二氧化硅、滑石、云母、硅藻土、脲、碳酸钙、碳酸钠和碳酸氢钠、以及硫酸钠。典型的固体稀释剂在watkins等人的handbook of insecticide dust diluents and carriers[杀昆虫剂粉剂稀释剂和载体手册],第2版,dorland books,考德威尔,新泽西州中有所描述。
[0306]
液体稀释剂包括,例如水、n,n
‑
二甲基烷酰胺(例如,n,n
‑
二甲基甲酰胺)、柠檬烯、二甲基亚砜、n
‑
烷基吡咯烷酮(例如,n
‑
甲基吡咯烷酮)、磷酸烷基酯(例如,磷酸三乙酯)、乙二醇、三甘醇、丙二醇、二丙二醇、聚丙二醇、碳酸亚丙酯、碳酸亚丁酯、石蜡(例如白矿物油状物、正链烷烃、异链烷烃)、烷基苯、烷基萘、甘油状物、三乙酸甘油状物酯、山梨醇、芳烃、脱芳构化脂族化合物、烷基苯、烷基萘、酮,诸如环己酮、2
‑
庚酮、异佛尔酮和4
‑
羟基
‑4‑
甲基
‑2‑
戊酮,乙酸酯,诸如乙酸异戊酯、乙酸己酯、乙酸庚酯、乙酸辛酯、乙酸壬酯、乙酸十三烷基酯和乙酸异冰片酯,其他酯,诸如烷基化乳酸酯、二元酯、苯甲酸烷基和芳基酯和γ
‑
丁内酯,以及可以是直链、支链、饱和或不饱和的醇,诸如甲醇、乙醇,正丙醇、异丙醇、正丁醇、异丁醇、正己醇、2
‑
乙基己醇、正辛醇、癸醇、异癸醇、异十八烷醇、鲸蜡醇、月桂醇、十三烷
醇、油状物醇、环己醇、四氢糠醇、双丙酮醇、甲酚和苄醇。液体稀释剂还包括饱和的和不饱和的脂肪酸(通常为c6‑
c
22
)的甘油状物酯,诸如植物种子和果实油状物(例如,橄榄油状物、蓖麻油状物、亚麻籽油状物、芝麻油状物、玉米油状物(玉蜀黍油状物)、花生油状物、葵花籽油状物、葡萄籽油状物、红花油状物、棉籽油状物、大豆油状物、油状物菜籽油状物、椰子油状物和棕榈仁油状物),动物源脂肪(例如,牛脂、猪脂、猪油状物、鱼肝油状物、鱼油状物),以及它们的混合物。液体稀释剂还包括烷基化(例如甲基化、乙基化、丁基化)脂肪酸,其中脂肪酸可以通过来自植物和动物来源的甘油状物酯的水解获得,并且可通过蒸馏纯化。典型的液体稀释剂在marsden,solvents guide[溶剂指南],第2版,interscience,纽约,1950中进行描述。
[0307]
本发明的固体和液体组合物经常包括一种或多种表面活性剂。当添加到液体中时,表面活性剂(也称为“表面活性试剂”)通常改变、最经常地降低液体的表面张力。根据表面活性剂分子中的亲水和亲脂基团的性质,表面活性剂可用作润湿剂、分散剂、乳化剂或消泡剂。
[0308]
表面活性剂可以分类为非离子的、阴离子的或阳离子的。可用于本发明组合物的非离子表面活性剂包括但不限于:醇烷氧基化物,诸如基于天然醇和合成醇(其可以是支链或直链的)并且由醇和环氧乙烷、环氧丙烷、环氧丁烷或其混合物制备的醇烷氧基化物;胺乙氧基化物、链烷醇酰胺和乙氧基化链烷醇酰胺;烷氧基化甘油状物三酯,诸如乙氧基化的大豆油状物、蓖麻油状物和油状物菜籽油状物;烷基酚烷氧基化物,诸如辛基酚乙氧基化物、壬基酚乙氧基化物、二壬基酚乙氧基化物和十二烷基酚乙氧基化物(由苯酚和环氧乙烷、环氧丙烷、环氧丁烷或它们混合物制备);由环氧乙烷或环氧丙烷制备的嵌段聚合物和其中末端嵌段由环氧丙烷制备的反式嵌段聚合物;乙氧基化脂肪酸;乙氧基化脂肪酯和油状物;乙氧基化甲酯;乙氧基化三苯乙烯基酚(包括由环氧乙烷、环氧丙烷、环氧丁烷或其混合物制备的那些);脂肪酸酯、甘油状物酯、基于羊毛脂的衍生物、多乙氧基化酯(如多乙氧基化脱水山梨糖醇脂肪酸酯、多乙氧基化山梨糖醇脂肪酸酯和多乙氧基化甘油状物脂肪酸酯);其他脱水山梨糖醇衍生物如脱水山梨糖醇酯;聚合物表面活性剂,诸如无规共聚物、嵌段共聚物、醇酸peg(聚乙二醇)树脂、接枝或梳型聚合物以及星型聚合物;聚乙二醇(pegs);聚乙二醇脂肪酸酯;硅酮基表面活性剂;和糖衍生物,诸如蔗糖酯、烷基多糖苷和烷基多糖。
[0309]
有用的阴离子表面活性剂包括但不限于:烷基芳基磺酸及其盐;羧化的醇或烷基酚乙氧基化物;二苯基磺酸酯衍生物;木质素和木质素衍生物,诸如木质素磺酸盐;马来酸或琥珀酸或它们的酸酐;烯烃磺酸酯;磷酸酯,诸如醇烷氧基化物的磷酸酯,烷基酚烷氧基化物的磷酸酯和苯乙烯基酚乙氧基化物的磷酸酯;基于蛋白质的表面活性剂;肌氨酸衍生物;苯乙烯基酚醚硫酸盐;油状物和脂肪酸的硫酸盐和磺酸盐;乙氧基化烷基酚的硫酸盐和磺酸盐;醇的硫酸盐;乙氧基化醇的硫酸盐;胺和酰胺的磺酸盐,诸如n,n
‑
烷基牛磺酸盐;苯、枯烯、甲苯、二甲苯以及十二烷基苯和十三烷基苯的磺酸盐;缩聚萘的磺酸盐;萘和烷基萘的磺酸盐;分馏石油状物的磺酸盐;磺基琥珀酰胺酸盐;以及磺基琥珀酸盐和它们的衍生物,诸如二烷基磺基琥珀酸盐。
[0310]
有用的阳离子表面活性剂包括但不限于:酰胺和乙氧基化酰胺;胺诸如n
‑
烷基丙二胺、三亚丙基三胺和二亚丙基四胺,和乙氧基化胺、乙氧基化二胺以及丙氧基化胺(由胺和环氧乙烷、环氧丙烷、环氧丁烷或它们的混合物制备);胺盐如乙酸铵和二胺盐;季铵盐如
季盐、乙氧基化季盐和二季盐;以及胺氧化物,诸如烷基二甲基胺氧化物和双
‑
(2
‑
羟乙基)
‑
烷基胺氧化物。
[0311]
还可用于本发明组合物的是非离子表面活性剂和阴离子表面活性剂的混合物、或非离子表面活性剂和阳离子表面活性剂的混合物。非离子表面活性剂、阴离子表面活性剂和阳离子表面活性剂及其推荐用途在多个已公布的参考文献中披露,这些参考文献包括mccutcheon分部,the manufacturing confectioner出版公司出版的mccutcheon’s emulsifiers and detergents[mccutcheon的乳化剂和洗涤剂],annual american and international editions[美国和国际年度版];sisely和wood,encyclopedia of surface active agents[表面活性剂百科全书],chemical publ.co.,inc.[化工出版社有限公司],纽约,1964;以及a.s.davidson和b.milwidsky,synthetic detergents[合成洗涤剂],第七版,约翰威利父子出版社,纽约,1987。
[0312]
本发明的组合物还可包含本领域技术人员已知为辅助制剂的制剂助剂和添加剂(其中一些也可被认为是起到固体稀释剂、液体稀释剂或表面活性剂作用)。此类制剂助剂和添加剂可控制:ph(缓冲剂)、加工过程中的起泡(消泡剂,诸如聚有机硅氧烷)、活性成分的沉降(悬浮剂)、粘度(触变增稠剂)、容器内的微生物生长(抗微生物剂)、产品冷冻(防冻剂)、颜色(染料/颜料分散体)、洗脱(成膜剂或粘着剂)、蒸发(蒸发阻滞剂)、以及其他配制品属性。成膜剂包括例如聚乙酸乙烯酯、聚乙酸乙烯酯共聚物、聚乙烯吡咯烷酮
‑
乙酸乙烯酯共聚物、聚乙烯醇、聚乙烯醇共聚物和蜡。制剂助剂和添加剂的实例包括mccutcheon分部,the manufacturing confectioner出版公司出版的mccutcheon’s volume 2:functional materials[mccutcheon第2卷:功能材料],国际和北美年度版;以及pct公开wo 03/024222中列出的那些。
[0313]
通常通过将活性成分溶于溶剂中或者通过在液体或干稀释剂中研磨将具有式1的化合物和任何其他活性成分结合到本发明组合物中。可通过简单地混合这些成分来制备包括可乳化的浓缩物的溶液。如果旨在用作可乳化的浓缩物的液体组合物的溶剂是与水不混溶的,通常加入乳化剂以使含有活性成分的溶剂在用水稀释时乳化。粒径多达2,000μm的活性成分浆料可以使用介质研磨机进行湿法研磨,以得到平均粒径低于3μm的颗粒。水性浆液可以制成成品悬浮液浓缩物(参见,例如,u.s.3,060,084)或通过喷雾干燥进一步加工以形成水可分散性颗粒剂。干制剂通常需要干研磨过程,其产生在2μm至10μm范围内的平均粒径。粉剂和粉末可以通过共混并且通常通过研磨(例如用锤磨机或流能磨)来制备。可以通过将活性物质喷雾在预成形的颗粒剂载体上或者通过附聚技术来制备颗粒剂和球剂。参见,browning,“agglomeration[附聚]”,chemical engineering[化学工程],1967年12月4日,第147
‑
48页;perry’s chemical engineer’s handbook[佩里化学工程师手册],第4版,mcgraw
‑
hill[麦格劳希尔集团],纽约,1963,第8
‑
57页及其后页,以及wo 91/13546。球剂可以如u.s.4,172,714中所述制备。水可分散性和水溶性颗粒剂可如在u.s.4,144,050、u.s.3,920,442和de 3,246,493中传授的来制备。片剂可以如在u.s.5,180,587、u.s.5,232,701和u.s.5,208,030中所传授的来制备。膜可以如在gb 2,095,558和u.s.3,299,566中所传授的来制备。
[0314]
关于制剂领域的进一步信息,参见t.s.woods,pesticide chemistry and bioscience,the food
–
environment challenge[农药化学与生物科学,食品与环境挑战]
中的“the formulator’s toolbox
–
product forms for modern agriculture[制剂工具箱
‑
现代农业产品形式]”,t.brooks和t.r.roberts编辑,proceedings of the9th international congress on pesticide chemistry[第九届农药化学国际会议论文集],the royal society of chemistry[皇家化学学会],剑桥,1999,第120
‑
133页。还可参见u.s.3,235,361,第6栏,第16行至第7栏,第19行和实施例10
‑
41;u.s 3,309,192,第5栏,第43行至第7栏,第62行和实施例8、12、15、39、41、52、53、58、132、138
‑
140、162
‑
164、166、167和169
‑
182;u.s.2,891,855,第3栏,第66行至第5栏,第17行和实例1
‑
4;klingman,weed control as a science[杂草控制科学],john wiley and sons,inc.[约翰威利父子公司],纽约,1961,第81
–
96页;hance等人,weed control handbook[杂草控制手册],第8版,blackwell scientific publications[布莱克威尔科学出版社],牛津,1989;和developments in formulation technology[制剂技术的发展],pjb publications[pjb出版公司],里士满,uk,2000。
[0315]
在下列实例中,全部百分比都是按重量计的,并且所有制剂以常规的方式制备。化合物编号是指索引表a中的化合物。无需进一步详尽说明,据信本领域技术人员使用前述说明可将本发明利用至其最大程度。因此,以下实例应被解释为仅仅是说明性的,并非以任何方式限制本披露。除非另外说明,否则百分比按重量计。
[0316]
实例a
[0317]
高强度浓缩物
[0318]
化合物13
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
98.5%
[0319]
二氧化硅气凝胶
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
0.5%
[0320]
合成无定形精细二氧化硅
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
1.0%
[0321]
实例b
[0322]
可润湿的粉末
[0323][0324]
实例c
[0325]
颗粒
[0326]
化合物13
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
10.0%
[0327]
凹凸棒石颗粒剂(低挥发性物质,0.71/0.30mm;u.s.s.号25
‑
50筛) 90.0%
[0328][0329]
实例d
[0330]
挤出球剂
[0331]
[0332][0333]
实例e
[0334]
可乳化的浓缩物
[0335]
化合物13
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
10.0%
[0336]
聚氧乙烯山梨糖醇六油状物酸酯
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
20.0%
[0337]
c6‑
c
10
脂肪酸甲酯
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
70.0%
[0338]
实例f
[0339]
微乳液
[0340][0341]
实例g
[0342]
悬浮液浓缩物
[0343][0344]
实例h
[0345]
在水中的乳液
[0346][0347]
实例i
[0348]
油状物分散体
[0349][0350]
本披露内容还包括以上实例a至i,不同之处在于将“化合物13”用如索引表a中所描述的以上“化合物1”、“化合物2”、“化合物3”、“化合物4”、“化合物5”、“化合物6”、“化合物7”、“化合物8”、“化合物9”、“化合物10”、“化合物11”、“化合物12”、“化合物14”、“化合物15”、“化合物16”、“化合物17”、“化合物18”、“化合物19”、“化合物20”、“化合物21”、“化合物22”、“化合物23”、“化合物24”、“化合物25”、“化合物26”、“化合物27”、“化合物28”、“化合物29”、“化合物30”、“化合物31”和“化合物32”代替。测试结果表明,本发明的化合物是高活性出苗前和/或出苗后除草剂和/或植物生长调节剂。本发明的化合物通常对于出苗后杂草控制(即在杂草从土壤中出苗之后施用)和出苗前杂草控制(即在杂草从土壤中出苗之前施用)显示出最高活性。在期望完全控治所有植被的区域,诸如在燃料储槽、工业仓储区域、停车场、露天汽车电影院、机场、河岸、灌溉与其他水道、广告牌与高速公路及铁路结构体周围,它们中许多对于广谱的出苗前和/或出苗后杂草控制具有效用。本发明的许多化合物经由下列方式可用于选择性控治作物/杂草混生中的禾草与阔叶杂草:借助在作物对比杂草中的选择性代谢,或通过在作物与杂草中的生理抑制位点处具有选择性活性,或通过在作物与杂草混生的环境之上或之中的选择性施放。本领域技术人员将认识到,在化合物或化合物组内,这些选择性因子的优选组合可通过进行常规生物和/或生物化学测定容易地确定。本发明的化合物可示出对重要农作物的耐受性,这些农作物包括但不限于苜蓿、大麦、棉、小麦、油状物菜、甜菜、玉米(玉蜀黍)、高粱、大豆、稻、燕麦、花生、蔬菜、番茄、马铃薯、多年生种植作物,包括咖啡、可可、油状物棕、橡胶、甘蔗、柑橘、葡萄、果树、坚果树、香蕉、车前草、菠萝、啤酒花、茶和树木诸如桉树和针叶树(例如火炬松)、以及草皮物类(例如肯塔基蓝草、圣奥古斯丁草、肯塔基牛毛草和百慕大草)。本发明的化合物可用于经基因转化或育种的作物,以掺入除草剂抗性,表达对无脊椎害虫具有毒性的蛋白质(诸如苏云金芽孢杆菌毒素)和/或表达其他有用的性状。本领域技术人员将理解,并不是所有的化合物对所有杂草都是同等有效的。可替代地,主题化合物可用于改变植物生长。
[0351]
由于本发明的化合物具有出苗前和出苗后除草活性,以通过杀灭或伤害植被或减缓其生长来控制不希望植被,通常由多种方法来有效地施用化合物,这些方法涉及使除草有效量的本发明的化合物、或包含所述化合物和表面活性剂、固体稀释剂或液体稀释剂中的至少一种的组合物接触不希望植被的叶子或其他部位,或接触不希望植被的环境,诸如土壤或水,该不希望植被生长于该环境中,或该环境包围该不希望植被的种子或其它繁殖体。
[0352]
本发明的化合物的除草有效量是由许多因素决定的。这些因素包括:所选择的制剂、施用方法、所存在植被的量和类型、生长条件等。通常,本发明的化合物的除草有效量为约0.001至20kg/ha,其中优选范围为约0.004至1kg/ha。本领域技术人员可以容易地确定希望的杂草控制水平所需的除草有效量。
[0353]
在一个常见的实施例中,将本发明的化合物通常以配制的组合物施用于包括希望植被(例如作物)和不期望植被(即杂草)的所在地,该希望植被和不希望植被二者均可为与
生长介质(例如土壤)接触的种子、幼苗和/或较大植物。在此所在地,可将包含本发明化合物的组合物直接施用于植物或其一部分,特别是不希望的植被,和/或施用于与植物接触的生长介质。
[0354]
虽然最典型地,本发明的化合物用于控制不希望植被,但是使希望的植被在经处理的所在地中与本发明的化合物接触可导致与期望植被的遗传性状的超加性或协同效应,包括通过基因修饰引入的性状。例如,对植食性害虫或植物病害的抗性、对生物胁迫/非生物胁迫的耐受性或贮存稳定性可比希望植被的遗传性状中所期望的更大。
[0355]
本发明的化合物还可与一种或多种其他生物学活性化合物或试剂混合以形成多组分杀虫剂,从而赋予甚至更广范围的农业保护,这些生物学活性化合物或试剂包括除草剂、除草剂安全剂、杀真菌剂、杀昆虫剂、杀线虫剂、杀菌剂、杀螨剂、生长调节剂诸如昆虫蜕皮抑制剂和生根刺激剂、化学不育剂、化学信息素、驱虫剂、引诱剂、信息素、取食刺激剂、植物营养素、其他生物学活性化合物或昆虫病原细菌、病毒或真菌。本发明化合物与其他除草剂的混合物可扩大抵抗附加杂草物种的活性范围,并且抑制任何抗性生物类型的增殖。因此,本发明还涉及包含具有式1的化合物(处于除草有效量)和至少一种附加生物活性化合物或试剂(处于生物学有效量)的组合物,并且该组合物可进一步包含表面活性剂、固体稀释剂或液体稀释剂中的至少一种。其他生物活性化合物或试剂可以配制到包含表面活性剂、固体或液体稀释剂中的至少一种的组合物中。对于本发明的混合物,可将一种或多种其他生物活性化合物或试剂与具有式1的化合物配制在一起以形成预混物,或者一种或多种其他生物活性化合物或试剂可与具有式1的化合物分开配制,并且在施用前将制剂组合在一起(例如在喷雾罐中),或可替代地,依次施用。
[0356]
以下除草剂中的一种或多种与本发明的化合物的混合物可尤其用于杂草控制:乙草胺、三氟羧草醚及其钠盐、苯草醚、丙烯醛(2
‑
丙烯醛)、甲草胺、禾草灭、莠灭净、氨唑草酮、酰嘧磺隆、环丙嘧啶酸及其酯(例如甲基、乙基)和盐(例如钠、钾)、氯氨吡啶酸、杀草强、氨基磺酸铵、莎稗磷、磺草灵、莠去津、四唑嘧磺隆、氟丁酰草胺、草除灵、草除灵乙酯、苯唑磺隆(bencarbazone)、氟草胺、呋草黄、苄嘧磺隆、地散磷、灭草松、双环磺草酮、吡草酮、氟吡草酮、甲羧除草醚、双丙氨膦、双草醚及其钠盐、除草定、溴丁酰草胺、溴酚肟、溴苯腈、溴苯腈辛酸酯、丁草胺、氟丙嘧草酯、抑草磷、丁乐灵、丁苯草酮、丁草特、苯酮唑、卡草胺、三唑酮草酯、儿茶素、甲氧除草醚、草灭平、氯溴隆、氯甲丹、杀草敏、氯嘧磺隆、绿麦隆、氯苯胺灵、氯磺隆、氯酞酸二甲酯、赛草青、吲哚酮草酯、环庚草醚、醚磺隆、氯酰草膦、环苯草酮、烯草酮、炔草酯、异噁草酮、稗草胺、二氯吡啶酸、二氯吡啶酸乙醇胺、氯酯磺草胺、苄草隆、氰草津、环草特、环吡瑞莫、环丙嘧磺隆、噻草酮、氰氟草酯、2,4
‑
d及其丁氧基酯、丁酯、异辛酯和异丙酯及其二甲基铵盐、二乙醇胺盐和三乙醇胺盐、杀草隆、茅草枯、茅草枯钠、棉隆、2,4
‑
db及其二甲基铵盐、钾盐和钠盐、甜菜安、敌草净、麦草畏及其二乙二醇铵盐、二甲基铵盐、钾盐和钠盐、敌草腈、滴丙酸、禾草灵、双氯磺草安、野燕枯硫酸二甲酯、吡氟草胺、氟吡草腙、噁唑隆、哌草丹、二甲草胺、异戊净、噻吩草胺、噻吩草胺
‑
p、噻节因、二甲胂酸及其钠盐、敌乐胺、特乐酚、双苯酰草胺、敌草快、氟硫草定、敌草隆、dnoc、草多索、eptc、戊草丹、乙丁烯氟灵、胺苯磺隆、乙嗪草酮、乙呋草黄、氯氟草醚、乙氧嘧磺隆、乙氧苯草胺、噁唑禾草灵、精噁唑禾草灵、异噁苯砜、芬奎诺酮、四唑酰草胺、非草隆、非草隆
‑
tca、麦草氟甲酯、麦草氟异丙酯、麦草氟甲酯、啶嘧磺隆、双氟磺草胺、吡氟禾草灵、精吡氟禾草灵、异丙吡草酯、
氟酮磺隆、氟吡磺隆、氟消草、氟噻草胺、氟哒嗪、氟哒嗪草酯、唑嘧磺草胺、氟胺草酯、丙炔氟草胺、伏草隆、乙羧氟草醚、氟胺草唑、氟啶嘧磺隆及其钠盐、抑草丁、芴醇丁酯、氟啶草酮、氟咯草酮、氯氟吡氧乙酸、呋草酮、氟噻甲草酯、氟磺胺草醚、甲酰胺磺隆、调节膦
‑
铵、草胺磷、草铵膦铵、精草胺磷、草甘膦及其盐诸如铵、异丙基铵、钾、钠(包括倍半钠)和三甲基锍(可替代地称为草硫膦)、氟氯吡啶酯、氟氯吡啶甲酯、氯吡嘧磺隆、氟吡乙禾灵、氟吡甲禾灵、环嗪酮、海丹托西丁、咪草酸、甲氧咪草烟、甲咪唑烟酸、灭草烟、灭草喹、灭草喹铵、咪草烟、咪草烟铵、唑吡嘧磺隆、茚草酮、三嗪茚草胺、碘嗪磺隆、甲基碘磺隆、碘苯腈、碘苯腈辛酸酯、碘苯腈钠、三唑酰草胺、异丙隆、异噁隆、异噁草胺、异噁唑草酮、异噁氯草酮、乳氟禾草灵、环草定、利谷隆、抑芽丹、mcpa及其盐(例如,mcpa
‑
二甲基铵、mcpa
‑
钾和mcpa
‑
钠、酯(例如,mcpa
‑2‑
乙基己基酯、mcpa
‑
丁氧乙酯)和硫酯(例如,mcpa
‑
乙硫酯)、mcpb及其盐(例如,mcpb
‑
钠)和酯(例如mcpb
‑
乙酯)、2
‑
甲
‑4‑
氯丙酸、精2
‑
甲
‑4‑
氯丙酸、苯噻草胺、氟磺酰草胺、甲磺胺磺隆、甲基磺草酮、威百亩钠、噁唑酰草胺、苯嗪草酮、吡唑草胺、嗪吡嘧磺隆、甲基苯噻隆、甲胂酸及其钙盐、单铵盐、单钠盐和二钠盐、甲基杀草隆、甲氧苯草隆、溴谷隆、异丙甲草胺、精异丙甲草胺、磺草唑胺、甲氧隆、嗪草酮、甲磺隆、草达灭、绿谷隆、萘丙胺、敌草胺、敌草胺
‑
m、萘草胺、草不隆、烟嘧磺隆、哒草伏、坪草丹、嘧苯胺磺隆、氨磺乐灵、丙炔噁草酮、噁草酮、环氧嘧磺隆、噁嗪草酮、乙氧氟草醚、百草枯二氯盐、克草猛、壬酸、二甲戊乐灵、五氟磺草胺、甲氯酰草胺、环戊噁草酮、氟草磺胺、烯草胺(pethoxamid)、百特胺(pethoxyamid)、苯敌草、毒莠定、毒莠定钾、氟吡酰草胺、唑啉草酯、哌草磷、丙草胺、氟嘧磺隆、氨基丙氟灵、环苯草酮、扑灭通、扑草净、毒草胺、敌稗、喔草酯、扑灭津、苯胺灵、异丙草胺、丙苯磺隆、丙嗪嘧磺隆、戊炔草胺、苄草丹、氟磺隆、双唑草腈、吡草醚、磺酰草吡脱、双唑草腈(pyrazogyl)、吡唑特、苄草唑、吡嘧磺隆、苯嘧磺草胺、稗草畏、达草特、环酯草醚、嘧草醚、嘧啶硫蕃(pyrimisulfan)、嘧硫草醚、嘧硫草醚钠、罗克杀草砜、甲氧磺草胺、二氯喹啉酸、氯甲喹啉酸、灭藻醌、喹禾灵、精喹禾灵、喹禾糠酯、砜嘧磺隆、嘧啶肟草醚、稀禾定、环草隆、西玛津、西草净、磺草酮、甲磺草胺、甲嘧磺隆、磺酰磺隆、2,3,6
‑
tba、tca、tca
‑
钠、牧草胺、特丁噻草隆、特呋三酮、环磺酮、得杀草、特草定、特丁通、特丁津、去草净、甲氧噻草胺、噻草啶、噻酮磺隆、噻吩磺隆、禾草丹、氟丙嘧草酯、仲草丹、托派拉雷(tolpyralate)、苯吡唑草酮、肟草酮、野麦畏、氟酮磺草胺、醚苯磺隆、三嗪氟草胺、苯磺隆、绿草定、三氯比、绿草定三乙铵、灭草环、草达津、三氟啶磺隆、三氟草嗪(trifludimoxazin)、氟乐灵、氟胺磺隆、三氟甲磺隆、灭草敌、3
‑
(2
‑
氯
‑
3,6
‑
二氟苯基)
‑4‑
羟基
‑1‑
甲基
‑
1,5
‑
萘啶
‑
2(1h)
‑
酮、5
‑
氯
‑3‑
[(2
‑
羟基
‑6‑
氧基
‑1‑
环己烯
‑1‑
基)羰基]
‑1‑
(4
‑
甲氧基苯基)
‑
2(1h)
‑
喹喔啉酮、2
‑
氯
‑
n
‑
(1
‑
甲基
‑
1h
‑
四唑
‑5‑
基)
‑6‑
(三氟甲基)
‑3‑
吡啶甲酰胺、7
‑
(3,5
‑
二氯
‑4‑
吡啶基)
‑5‑
(2,2
‑
二氟乙基)
‑8‑
羟基吡啶并[2,3
‑
b]吡嗪
‑
6(5h)
‑
酮)、4
‑
(2,6
‑
二乙基
‑4‑
甲基苯基)
‑5‑
羟基
‑
2,6
‑
二甲基
‑
3(2h)
‑
哒嗪酮)、5
‑
[[(2,6
‑
二氟苯基)甲氧基]甲基]
‑
4,5
‑
二氢
‑5‑
甲基
‑3‑
(3
‑
甲基
‑2‑
噻吩基)异噁唑(前述为methioxolin)、4
‑
(4
‑
氟苯基)
‑6‑
[(2
‑
羟基
‑6‑
氧基
‑1‑
环己烯
‑1‑
基)羰基]
‑2‑
甲基
‑
1,2,4
‑
三嗪
‑
3,5(2h,4h)
‑
二酮、4
‑
氨基
‑3‑
氯
‑6‑
(4
‑
氯
‑2‑
氟
‑3‑
甲氧基苯基)
‑5‑
氟
‑2‑
吡啶甲酸甲酯、2
‑
甲基
‑3‑
(甲基磺酰基)
‑
n
‑
(1
‑
甲基
‑
1h
‑
四唑
‑5‑
基)
‑4‑
(三氟甲基)苯甲酰胺以及2
‑
甲基
‑
n
‑
(4
‑
甲基
‑
1,2,5
‑
噁二唑
‑3‑
基)
‑3‑
(甲基亚磺酰基)
‑4‑
(三氟甲基)苯甲酰胺。其他除草剂还包括生物除草剂,诸如损毁链格孢(alternaria destruens simmons)、刺盘孢炭疽菌(colletotrichum gloeosporiodes(penz.)penz.&
sacc.)、稗内脐蠕孢菌(drechsiera monoceras)(mtb
‑
951)、疣孢漆斑菌(myrothecium verrucaria(albertini&schweinitz)ditmar:fries)、棕榈疫霉(phytophthora palmivora(butl.)butl.)和菥蓂柄锈菌(puccinia thlaspeos schub)。
[0357]
本发明的化合物还可与植物生长调节剂诸如艾维激素、n
‑
(苯基甲基)
‑
1h
‑
嘌呤
‑6‑
胺、丙酰芸苔素内酯、赤霉酸、赤霉素a4和a7、超敏蛋白、甲哌鎓、调环酸钙、茉莉酮、硝酚钠和抗倒酯
‑
甲基,以及植物生长改性生物体诸如蜡状芽孢杆菌(bacillus cereus)菌株bp01结合地使用。
[0358]
农用保护剂(即除草剂、除草剂安全剂、杀昆虫剂、杀真菌剂、杀线虫剂、杀螨剂、和生物试剂)的一般参考文献包括the pesticide manual[农药手册],第13版,c.d.s.tomlin编辑,british crop protection council[英国作物保护委员会],famham,surrey,u.k.,2003和the biopesticide manual[生物农药手册],第2版,l.g.copping编辑,英国作物保护委员会,farnham,surrey,u.k.,2001。
[0359]
对于其中使用这些不同混合组分中的一种或多种的实施例,这些混合组分通常以类似于单独使用混合物组分时的常规量的量使用。更具体地,在混合物中,活性成分通常以在产品标签上指明的仅使用活性成分的一半与全部施用量之间的施用量施用。这些量列在参考文献诸如the pesticide manual[农药手册]和the biopesticide manual[生物农药手册]中。这些不同混合组分(总量)与具有式1的化合物的重量比典型地在约1∶3000与约3000∶1之间。值得注意的是在约1∶300与约300∶1之间的重量比(例如在约1∶30与约30∶1之间的比率)。本领域技术人员可以通过简单的实验容易地确定所希望的生物活性谱所必需的活性成分的生物有效量。将明显的是,包含这些附加组分可使受控杂草谱扩展超出由单独的具有式1的化合物的控制谱。
[0360]
在某些情况下,本发明化合物与其他生物活性(特别是除草)化合物或试剂(即活性成分)的组合可导致对杂草的大于累加(即协同)的效应和/或对作物或其他期望植物的小于累加(即安全化)的效应。降低释放在环境中的活性成分的量,同时确保有效的有害生物防治一直是人们所希望的。使用较大量的活性成分以提供更有效的杂草控制而没有过度作物伤害的能力也是期望的。当除草活性成分以获得农艺上令人满意的杂草控制水平的施用率对杂草产生协同作用时,此类组合可有利地用于降低作物生产成本并且减少环境负荷。当除草活性成分的安全化发生于作物上时,此类组合可有利地用于通过减少杂草竞争而增加作物保护。
[0361]
值得注意的是本发明化合物与至少一种其他除草活性成分的组合。特别值得注意的是其他除草活性成分与本发明化合物具有不同作用位点的组合。在某些情况下,与至少一种具有相似控制范围但是不同作用位点的其他除草活性成分的组合对于抗性管理将是特别有利的。因此,本发明的组合物可以进一步包含(处于除草有效量的)至少一种具有相似控制范围但是不同作用位点的附加除草活性成分。
[0362]
本发明的化合物也可与诸如以下各项的除草剂安全剂结合使用以增加对某些作物的安全性:二丙烯草胺、解草酮、解草酯、苄草隆、解草胺腈、环丙磺酰胺、杀草隆、二氯丙烯胺、大赛克农、增效磷、哌草丹、解草唑、解草啶、解草安、氟草肟、解草噁唑、双苯噁唑酸、吡唑解草酯、梅芬内、去草酮、萘二甲酸酐(1,8
‑
萘二甲酸酐)、解草腈、n
‑
(氨基羰基)
‑
2甲基苯磺酰胺、n
‑
(氨基羰基)
‑2‑
氟苯磺酰胺、1
‑
溴
‑4‑
[(氯甲基)磺酰基]苯(bcs)、4
‑
(二氯乙酰
基)
‑1‑
氧杂
‑4‑
氮杂螺[4.5]癸烷(mon 4660)、2
‑
(二氯甲基)2
‑
甲基
‑
1,3二氧戊环(mg 191)、1,6
‑
二氢
‑1‑
(2
‑
甲氧基苯基)
‑6‑
氧基
‑2‑
苯基
‑5‑
嘧啶羧酸乙酯、2
‑
羟基
‑
n,n
‑
二甲基
‑6‑
(三氟甲基)吡啶
‑3‑
甲酰胺、以及3
‑
氧基
‑1‑
环己烯
‑
l
‑
基1
‑
(3,4
‑
二甲基苯基)
‑
l,6
‑
二氢
‑6‑
氧基
‑2‑
苯基
‑5‑
嘧啶羧酸酯、2,2
‑
二氯
‑1‑
(2,2,5
‑
三甲基
‑3‑
噁唑烷基)
‑
乙酮和2
‑
甲氧基
‑
n
‑
[[4
‑
[[(甲基氨基)羰基]氨基]苯基]磺酰基]
‑
苯甲酰胺。解毒有效量的除草剂安全剂可与本发明的化合物同时施用,或作为种子处理物施用。因此,本发明的一个方面涉及一种包含本发明的化合物和解毒有效量的除草剂安全剂的除草混合物。种子处理对于选择性杂草控制是特别有用的,因为它将解毒作用物理地限制在作物植物上。因此,本发明的特别有用的实施例是用于选择性控制作物中不希望的植被生长的方法,该方法包括使该作物的所在地与除草有效量的本发明的化合物接触,其中该作物自其长成的种子用解毒有效量的安全剂处理。解毒有效量的安全剂可以由本领域技术人员通过简单的实验容易地确定。
[0363]
本发明的化合物还可以与以下各项混合:(1)多核苷酸,包括但不限于dna、rna和/或化学修饰的核苷酸,这些核苷酸通过减量调节、干扰、抑制或沉默呈现除草效果的基因衍生的转录物来影响特定靶的量;或(2)多核苷酸,包括但不限于dna、rna和/或化学修饰的核苷酸,这些核苷酸通过减量调节、干扰、抑制或沉默呈现安全化效果的基因衍生的转录物来影响特定靶的量。
[0364]
值得注意的是一种组合物,该组合物包含本发明的化合物(以除草有效量)、至少一种选自由其他除草剂和除草剂安全剂组成的组的附加活性成分(以除草有效量)、以及至少一种选自由表面活性剂、固体稀释剂和液体稀释剂组成的组的组分。
[0365]
优选用于更好地控制不希望的植被(例如,更低的使用率,例如来自协同作用、更广谱的杂草控制、或增强的作物安全性)或者用于防止抗性杂草的发展的是本发明的化合物与选自由以下组成的组的除草剂的混合物:莠去津、四唑嘧磺隆、氟丁酰草胺、s
‑
氟丁酰草胺、苯并异噻唑啉酮、比克罗腙、唑酮草酯、氯嘧磺隆、氯磺隆
‑
甲基、异噁草酮、二氯吡啶酸钾、氯酯磺草胺、2
‑
[(2,5
‑
二氯苯基)甲基]
‑
4,4
‑
二甲基
‑3‑
异噁唑烷酮、胺苯磺隆、唑嘧磺草胺、4
‑
(4
‑
氟苯基)
‑6‑
[(2
‑
羟基
‑6‑
氧代
‑1‑
环己烯
‑1‑
基)羰基]
‑2‑
甲基
‑
1,2,4
‑
三嗪
‑
3,5
‑
(2h,4h)
‑
二酮、氟啶嘧磺隆、氟噻甲草酯、氟磺胺草醚、咪草烟、环草定、硝磺草酮、嗪草酮、甲磺隆、烯草胺、毒莠定、罗克杀草砜、二氯喹啉酸、玉嘧磺隆、精异丙甲草胺、甲磺草胺、噻吩磺隆、氟胺磺隆和苯磺隆。
[0366]
表a1列出了组分(a)与组分(b)的特定组合,说明了本发明的混合物、组合物和方法。组分(a)列中的化合物13标识在索引表a中。表a1的第二列列出了特定组分(b)化合物(例如第一行中的“2,4
‑
d”)。表a1的第三、第四和第五列列出了将组分(a)化合物典型地施用于田间生长作物的速率相对于组分(b)的重量比范围(即(a):(b))。因此,例如,表a1的第一行具体披露了组分(a)(即索引表a中的化合物13)与2,4
‑
d的组合典型地以在1:192
‑
6:1之间的重量比施用。表a1的其余行将被类似地构造。
[0367]
表a1
[0368]
[0369]
[0370]
[0371]
[0372]
[0373]
[0374][0375]
表a2如以上表a1相同构造,除了“组分(a)”列标题下面的条目被下文所示的相应组分(a)列条目替代。组分(a)列中的化合物1在索引表a中标识。因此,例如,在表a2中,“组分(a)”列标题下面的条目全都列举“化合物2”(即,索引表a中所标识的化合物2),并且表a2中的列标题下面的第一行具体披露了化合物2与2,4
‑
d的混合物。表a3至a31类似地构造。
[0376][0377]
优选用于更好地控制不希望的植被(例如,诸如来自协同作用的较低使用率、更广的受控杂草的范围或增强的作物安全性)或用于防止抗性杂草的发展的是本发明的化合物与选自由以下组成的组的除草剂的混合物:氯磺隆、胺苯磺隆、氯嘧磺隆、硝磺草酮、噻吩磺隆、氟啶嘧磺隆、苯磺隆、甲磺隆、氟胺磺隆、罗克杀草砜、唑啉草酯、环磺酮、甲氧磺草胺、异丙甲草胺和精异丙甲草胺。
[0378]
以下测试证明本发明的化合物对特定杂草的控制功效。然而,由化合物提供的杂草控制不限于这些物种。化合物描述参见索引表a和b。以下缩写用于随后的索引表中:et是乙基。(r)或(s)表示不对称碳中心的绝对手性。“rac.”意指外消旋混合物。“立体(3,4)”描述了吡咯烷酮环的3
‑
和4
‑
位的立体化学。缩写“cmpd.no.”代表“化合物编号”。缩写“ex.”代表“实例”并且后面是数字,该数字表示化合物在哪个合成实例中制备。作为通过使用大气压力化学电离(ap+)观察到的通过h+(分子量为1)加在分子上形成的最高同位素丰度母离子(m+1)的分子量以
±
0.5da内的估计精度报告质谱。
[0379]
索引表a
[0380][0381]
[0382][0383]
*1h nmr数据参见索引表b。
[0384]
**1h nmr数据参见合成实例。
[0385]
索引表b
[0386]
[0387]
[0388][0389]
本发明的生物学实例
[0390]
测试a
[0391]
出苗前方案
[0392]
将玉米(corn)(玉蜀黍(zea mays,zeamx))、大狗尾草(giant foxtail)(狗毛草(setaria faberii,setfa))、稗草(barnyardgrass)(稗子(echinochloa crus
‑
galli,echcg))、常春藤叶状牵牛花(ivy
‑
leaved morning glory)(碗仔花(ipomoea hederacea,ipohe))、红根苋(redroot pigweed)(反枝苋(amaranthus retroflexus,amare))和绒毛叶(velvetleaf)(苘麻(abutilon theophrasti,abuth))的种子播种在盆中的标准土壤中。在受控条件下在温室中(在24/16℃下,日/夜;14h光照;65%湿度)培养一天后,将植物用来源于工艺活性成分在含有0.5%吐温20(聚氧乙烯脱水山梨糖醇单月桂酸酯,cas rn 9005
‑
64
‑
5)的丙酮/水(50:50)溶液中的配制品的喷雾水溶液喷雾以得到最终剂量为15.625、62.5或250g/ha的测试化合物。
[0393]
然后将测试植物在受控条件下在温室中(在24/16℃下,日/夜;14h光照;65%湿度)生长并且每天浇水两次。13天后,评估测试(100=对植物的完全损害;0=对植物没有损害)。结果如下所示。
[0394]
出苗后方案
[0395]
将玉米(corn)(玉蜀黍(zea mays,zeamx))、大狗尾草(giant foxtail)(狗毛草(setaria faberii,setfa))、稗草(barnyardgrass)(稗子(echinochloa crus
‑
galli,echcg))、常春藤叶状牵牛花(ivy
‑
leaved morning glory)(碗仔花(ipomoea hederacea,ipohe))、红根苋(redroot pigweed)(反枝苋(amaranthus retroflexus,amare))和绒毛叶(velvetleaf)(苘麻(abutilon theophrasti,abuth))的种子播种在盆中的标准土壤中。在受控条件下在温室中(在24/16℃下,日/夜;14h光照;65%湿度)培养8天后,将植物用来源于工艺活性成分在含有0.5%吐温20(聚氧乙烯脱水山梨糖醇单月桂酸酯,cas rn 9005
‑
64
‑
5)的丙酮/水(50:50)溶液中的配制品的喷雾水溶液喷雾以得到最终剂量为15.625、62.5或250g/ha的测试化合物。
[0396]
然后将测试植物在受控条件下在温室中(在24/16℃下,日/夜;14h光照;65%湿度)生长并且每天浇水两次。13天后,评估测试(100=对植物的完全损害;0=对植物没有损害)。结果如下所示。
[0397]
表a:出苗前(250g/ha)
[0398][0399][0400]
表a:出苗后(250g/ha)
[0401]
化合物编号amareabuthsetfaechcgzeamxipohe20080904003200909080042020909090205008080006106070706010700808080080080808030
9009090500100109090703011008090400120000001400908080501500000016007070001750080808001800707080501930080801002020080800022008080803023008080803024008080405025008080304026009090805027300707010202850070700029400606001030100505000312008080040320080801010
[0402]
表a:出苗前(62.5g/ha)
[0403]
化合物编号amareabuthsetfaechcgzeamxipohe100000020090900032009010060042009090401050030200062070909020070080803020800909040209009090001001090907030110090900012000000140090801040150000001600808000
1710090100700180090906010190090900020600808000221009090200230090902010240090100300250109010000260090907030270080901002800807000290030701003000010003100808010032006050100
[0404]
表a:出苗后(62.5g/ha)
[0405]
[0406][0407]
表a:出苗前(15.625g/ha)
[0408]
[0409][0410]
表a:出苗后(15.625g/ha)
[0411]
[0412][0413]
测试b
[0414]
将选自以下项的植物物种的种子种植到粉砂壤土中,并用配制在包含表面活性剂的非植物毒性溶剂混合物中的测试化学品进行出苗前处理:黑草(alopecurus myosuroides)、意大利黑麦草(lolium multiflorum)、冬小麦(冬小麦,triticum aestivum)、玉米(zea mays)、大(lg)马唐草(digitaria sanguinalis)、大狗尾草(setaria faberi)、约翰逊草(sorghum halepense)、豚草(普通豚草,ambrosia elatior)、大豆(glycine max)、稗草(echinochloa crus
‑
galli)、苋菜藤子(普通苋菜藤子,amaranthus rudis)、长芒苋(amaranthus palmeri)和苏里南草(brachiaria decumbens)。
[0415]
将经处理的植物与对照物在温室中保持19至21天,之后将所有物种与对照物比较并且视觉评估。总结于表b中的植株响应评级基于0至100的标度,其中0为无效果并且100为完全控制。
[0416]
[0417][0418][0419]
测试c
[0420]
将选自以下项的植物物种的种子种植到粉砂壤土中并用配制在包含表面活性剂的非植物毒性溶剂混合物中的测试化学品进行出苗前处理:玉米(zea mays)、大豆(glycine max)、绒毛叶(abutilon theophrasti)、长芒苋(amaranthus palmeri)、苋菜藤子(普通苋菜藤子,amaranthus rudis)、苏里南草(brachiaria decumbens)、大(lg)马唐草(digitaria sanguinalis)、秋黍子(panicum dichotomiflorum)、大狗尾草(setaria faberi)、豚草(普通豚草,ambrosia elatior)、稗草(echinochloa crus
‑
galli)、龙葵(e.black nightshade)(solanum ptycanthum)、以及小蓬草(conyza canadensis)。
[0421]
将经处理的植物与对照物在温室中保持19至21天,之后将所有物种与对照物比较并且视觉评估。总结于表c中的植株响应评级基于0至100的标度,其中0为无效果并且100为完全控制。
[0422][0423][0424]
测试d
[0425]
通过将活性成分溶解在有机溶剂和乳化剂的混合物中来制备含有50g/l测试化学品的制剂,表中提供了详细信息。然后将该制剂与少量、可变量的丙酮混合以帮助溶解,然后添加0.2%v/v佐剂的水溶液作为水性稀释剂,以形成含有预定浓度的活性成分的喷雾水溶液。
[0426][0427]
然后在一天的培养后(对于出苗前)或在约12天的培养后(对于出苗后),将该喷雾
水溶液喷雾至已经用除草剂安全剂处理过种子的植物(包括玉米和小麦)上。植物由播种在标准土壤中的种子生长,在受控条件(在24/18℃或20/16℃下,日/夜;16h光照;65%湿度)下放置在温室中。喷雾施用后,植物然后在相同条件下在温室中生长并每天浇水两次。出苗后15天以及出苗前20daa后,评估测试(100=对植物的完全损害;0=对植物无损害)。
[0428][0429][0430]
表d1:“谷物”出苗前
[0431]
[0432][0433]
表d1:“谷物”出苗前(续)
[0434]
[0435][0436]
[0437]
表d1:“谷物”出苗前(续)
[0438][0439]
表d1:“谷物”出苗前(续)
[0440][0441][0442]
表d2:“谷物”出苗后
[0443][0444]
表d2:“谷物”出苗后(续)
[0445]
[0446][0447]
表d3:“玉米”出苗前
[0448]
[0449][0450]
表d3:“玉米”出苗前(续)
[0451]
[0452]
[0453][0454]
表d3:“玉米”出苗前(续)
[0455][0456]
表d3:“玉米”出苗前(续)
[0457]
[0458][0459]
表d4:“玉米”出苗后
[0460][0461]
表d4:“玉米”出苗后(续)
[0462]
[0463][0464]
表d4:“玉米”出苗后(续)
[0465][0466]
表d4:“玉米”出苗后(续)
[0467]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1