非典型蛋白激酶C的抑制剂和其在治疗hedgehog途径依赖性癌症中的用途的制作方法
非典型蛋白激酶c的抑制剂和其在治疗hedgehog途径依赖性癌症中的用途
1.关于联邦赞助的研究或开发的声明
2.本发明是根据美国国立卫生研究院授予的合同ar054780在政府支持下完成的。政府对本发明享有一定的权利。
发明领域
3.本发明涉及用于治疗hedgehog途径依赖性癌症和病症的疗法。特别地,本发明涉及用非典型蛋白激酶c(apkc)iota的抑制剂治疗hedgehog途径依赖性癌症和病症的方法。
4.发明背景
5.hedgehog(hh)信号传导途径在后生动物的发育和肿瘤发生中起关键作用。已经鉴定出三种哺乳动物hh基因:sonic hedgehog(shh)、desert hedgehog(dhh)和indian hedgehog(ihh)。这些蛋白质是分泌性蛋白质,通过拮抗受体patched(人中ptch1或ptch2)起作用。ptch部分地通过拮抗smoothened(smo)(激活转录因子gli的g蛋白偶联受体)的活性起作用。当shh与ptch结合时,ptch介导的smo抑制解除,容许smo促进gli依赖性转录。在发育期间,hh诱导的smo活性促进祖细胞的增殖、迁移和分化,以使器官发育模式形成。然而,hh途径信号传导的失调,例如通过ptch失活突变或smo激活突变,与癌症有关(toftgard,r.hedgehog signaling in cancer.cell mol.life sci.,57:1720-1731(2000))。肿瘤上皮细胞的肿瘤生长和维持需要hh靶基因的诱导,并且hh途径信号传导与许多上皮性肿瘤的肿瘤转移有关。例如,基底细胞癌(bcc)的启动和扩增需要高水平的hh途径信号传导。
6.仍然需要更好的方法来治疗hh途径相关的癌症和疾病。
7.发明概述
8.提供了治疗hedgehog途径依赖性癌症的方法。该方法的方面包括抑制由hedgehog途径信号传导促进的hedgehog途径依赖性癌症生长、增殖和/或转移。特别地,公开了用apkc iota的抑制剂治疗hedgehog途径依赖性癌症的方法。
9.在一个方面,提供了治疗受试者hedgehog途径依赖性癌症的方法,该方法包括向所述受试者施用治疗有效量的包含crt0422839或crt0364436或其药学上可接受的盐的组合物。
10.在某些实施方案中,癌症包含组成型活性hedgehog途径。在一个实施方案中,癌症是基底细胞癌(bcc)。在一些实施方案中,癌症是转移性的。
11.可以在一段时间内向受试者施用多个治疗周期。例如,可以向受试者施用治疗至少3个月、至少6个月、至少9个月、或至少12个月或更长。优选地,向受试者施用多个治疗周期,其时间段足以实现至少部分肿瘤响应或更优选地实现完全肿瘤响应。在某些实施方案中,根据每日给药方案或间歇性施用包含crt0422839或crt0364436或其药学上可接受的盐的组合物。
12.在某些实施方案中,该方法进一步包括施用另外的抗癌疗法诸如但不限于手术、
化学疗法、放射疗法、免疫疗法、生物疗法或其组合。
13.在某些实施方案中,施用的组合物进一步包含药学上可接受的赋形剂。
14.在某些实施方案中,该方法进一步包括施用组蛋白脱乙酰酶(hdac)抑制剂联合crt0422839或crt0364436或其药学上可接受的盐。示例性的hdac抑制剂包括异羟肟酸诸如伏立诺他、贝利司他、帕比司他、吉维司他(givinostat)、达西司他(laq824)和曲古抑菌素a;倍半萜内酯类(sesquiterpene lactone)诸如欧苷菊、环状四肽类诸如trapoxin b;缩肽类诸如罗米地辛以及苯甲酰胺类诸如恩提诺特(entinostat)(ms-275)、泰克地那林(tacedinaline)(ci994)和莫西司他(mocetinostat)。在一个实施方案中,hdac抑制剂是伏立诺他。
15.在某些实施方案中,受试者是哺乳动物,例如人或非人灵长类、啮齿动物、农场动物或宠物。
16.在某些实施方案中,crt0422839或crt0364436或其药学上可接受的盐以足以降低受试者中hedgehog途径依赖性癌细胞的生存力的量施用。
17.在某些实施方案中,crt0422839或crt0364436或其药学上可接受的盐以足以减少受试者的hedgehog途径依赖性癌细胞中gli 1 mrna的产生的量施用。
18.在某些实施方案中,crt0422839或crt0364436或其药学上可接受的盐以足以减少受试者中hedgehog途径依赖性癌细胞的生长和细胞增殖的量施用。
19.另一方面,提供了抑制hedgehog途径依赖性癌细胞生长或增殖的方法,该方法包括将hedgehog途径依赖性癌细胞与有效量的crt0422839或crt0364436或其药学上可接受的盐接触。
20.在某些实施方案中,hedgehog途径依赖性癌细胞是bcc细胞。
21.在某些实施方案中,hedgehog途径依赖性癌细胞包含组成型活性hedgehog途径。
22.在某些实施方案中,hedgehog途径依赖性癌细胞是体内或体外的。
23.在某些实施方案中,hedgehog途径依赖性癌细胞是哺乳动物(例如,人或非人灵长类、啮齿动物、农场动物或宠物)癌细胞。
24.在某些实施方案中,该方法进一步包括将hedgehog途径依赖性癌细胞与hdac抑制剂接触。
25.在另一方面,提供了包含crt0422839或crt0364436或其药学上可接受的盐的组合物,用于治疗hedgehog途径依赖性癌症。在一些实施方案中,该组合物进一步包含hdac抑制剂。在一个实施方案中,hdac抑制剂是伏立诺他。
26.在另一方面,提供了包含crt0422839或crt0364436或其药学上可接受的盐的组合物,用于治疗基底细胞癌。在一些实施方案中,该组合物进一步包含hdac抑制剂。在一个实施方案中,hdac抑制剂是伏立诺他。
27.附图简述
28.当连同附图阅读以下详细描述时,可以最好地理解本发明。要强调的是,按照惯例,附图的各种特征不按比例。相反,为了清楚,各种特征的尺寸经任意扩大或缩小。附图中包括以下图。
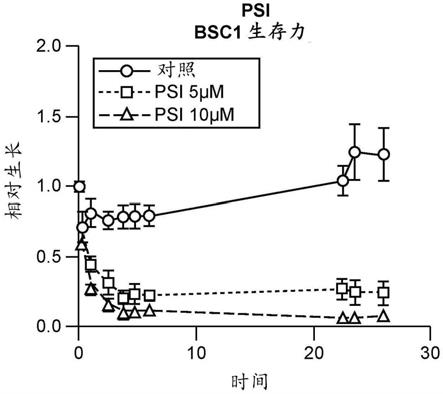
29.图1a-1d显示非典型蛋白激酶iota(apkcι)抑制剂调控bcc细胞生存力。在鼠bcc细胞系(bsc1)中测试了化合物crt0422839和crt0364436对bcc生存力的影响,并与已知的肽
抑制剂psi结果进行比较,psi之前在mirza et al.(jci insight(2017)2(21):e97071)中描述。显示了用apkc抑制剂psi(图1a)、crt0329868(图1b)、crt0364436(图1c)或crt0422839(图1d)以1μm和10μm的浓度处理后,bsci细胞生存力。
30.图2a和2b显示了用psi、crt0329868、crt0422839或crt0364436处理鼠bcc细胞系(bsc1)对gli1 mrna表达水平的影响,gli 1 mrna是shh途径输出的标志物,其经测量以进一步记录bcc生长和shh途径信号传导的抑制。显示了用化合物以1μm和10μm的浓度处理6小时(图2a)或24小时(图2b)后的结果。
31.图3a-3b显示了apkcι抑制剂crt0364436/tev-44229(图3a)和crt0422839/tev-47448(图3b)的化学结构和特性。
32.发明详述
33.在描述本方法和组合物之前,将应当理解本发明不限于所描述的特定方法或组合物,照此当然可以变化。还应理解,本文所用的术语仅用于描述特定实施方案的目的,而不意图值将限制,因为本发明的范围将仅由所附权利要求限制。
34.在提供值范围处,除非上下文另有明确规定,应当理解,还具体公开了该范围的上下限之间的每个中间值,到下限单位的十分之一。在规定范围内的任何规定值或中间值和该规定范围内的任何其他规定或中间值之间的每个较小范围都涵盖在本发明内。这些较小量程的上下限可以独立地包括或不包括在该范围内,受制于规定的范围内任何具体排除的限制,界限之一、两者都不或两者都包括在较小范围内的每个范围也涵盖在本发明内。在包括一个或两个界限的范围处,排除这些包括的界限之一或两者的范围也包括在本发明中。
35.除非另有定义,本文使用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常理解的相同的含义。尽管在本发明的实践或测试中可以使用与本文描述的那些相似或等同的任何方法和材料,现在描述一些潜在的和优选的方法和材料。本文提及的所有出版物通过引用并入本文以公开和描述与出版物所引用的相关的方法和/或材料。应当理解,在存在矛盾的情况下,本公开取代并入的出版物的任何公开。
36.如本领域技术人员在阅读本公开后所显而易见的是,本文描述和说明的单独实施方案中的每一个都具有分立的组分和特征,这些组分和特征可以容易地与其他几个实施方案中的任一个的特征分离或组合,而不脱离本发明的范围或精神。任何叙述的方法都可以按照所叙述的事件的顺序或以逻辑上可能的任何其他顺序来执行。
37.必须注意,如本文所用的和在所附权利要求中,单数形式“一个”、“一种”和“该”包括复数指代物,除非上下文另有明确规定。因此,例如,提及“一个细胞”包括多个此类细胞,以及提及“该抑制剂”包括提及一种或多种抑制剂及其等同物,例如,本领域技术人员已知的化合物或药物,如此等等。
38.提供本文讨论的出版物仅是为了它们在本技术的申请日之前的公开。凭借在先发明,本文中的任何文字都不应解释为承认本发明没有资格早于所述出版物。此外,提供的出版日期可能与实际出版日期不同,其可能需要独立确认。
39.术语“约”,特别是关于给定的量,意指涵盖正负百分之五的偏差。
40.术语“肿瘤”、“癌症”和“瘤形成”可互换使用,是指其生长、增殖或存活大于正常对应细胞生长、增殖或存活的细胞或细胞群,例如,细胞增殖性、过度增殖性或分化性病症。通常,生长是不受控制的。术语“恶性”是指对附近组织的侵袭。术语“转移”或继发性、反复性
或复发性肿瘤、癌症或瘤形成是指肿瘤、癌症或瘤形成向受试者体内的其他位点、位置或区域扩散或播散,其中该位点、位置或区域与原发肿瘤或癌症不同。瘤形成、肿瘤和癌症包括良性、恶性、转移性和非转移性类型,并且包括瘤形成、肿瘤或癌症的任何阶段(i、ii、iii、iv或v)或等级(g1、g2、g3等),或正在进展、恶化、稳定或缓解的瘤形成、肿瘤、癌症或转移。特别地,术语“肿瘤”、“癌症”和“瘤形成”包括癌,诸如鳞状细胞癌、腺癌、腺鳞癌、间变性癌、大细胞癌和小细胞癌。
41.术语“hedgehog途径依赖性癌症”包括任何依赖hedgehog途径激活或与hedgehog途径异常激活相关的癌症诸如但不限于基底细胞癌、髓母细胞瘤、横纹肌肉瘤、小细胞肺癌、视网膜母细胞瘤、胃和上消化道癌症、骨肉瘤、胰腺癌、乳腺癌、结肠癌、卵巢癌、脑癌、乳腺癌症、甲状腺癌和前列腺癌。
[0042]“抗肿瘤活性”意指细胞增殖速率的降低,并因此降低现有肿瘤或治疗期间出现的肿瘤的生长速率,和/或破坏现有瘤形成(肿瘤)细胞或新形成的瘤形成细胞,并因此减小治疗期间肿瘤的整体大小。可以使用动物模型,诸如人肾细胞癌的异种移植模型评估这种活性。参见,例如pulkkanen et al.,in vivo(2000)14:393-400和everitt et al.,toxicol.lett.(1995)82-83:621-625中关于动物模型的描述。
[0043]
apkc iota抑制剂(例如,crt0422839或crt0364436)的“治疗有效剂量或量”意指如本文所述,施用apkc iota抑制剂时,或另外施用组蛋白脱乙酰酶抑制剂(例如伏立诺他)联合apkc iota抑制剂时,引起积极治疗响应(诸如抗肿瘤活性)的量。另外,“有效量”的apkc iota抑制剂可以抑制hedgehog途径依赖性癌细胞的生长、增殖和/或转移,和/或减少hedgehog途径依赖性癌细胞中gli 1mrna的产生,和/或降低hedgehog途径依赖性癌细胞的生存力。
[0044]
本文使用的术语“肿瘤响应”意指所有可测量的病变的减少或消除。肿瘤响应的标准基于who报告标准[who胶板印刷出版物(who offset publication),48-世界卫生组织(48-world health organization),日内瓦,瑞士(1979)]。理想地,应该在每次评估时测量所有一维或二维可测量的病变。当任何器官中存在多个病变时,这种测量可能是不可能的,并且,在这种情况下,应该选择最多6个代表性病变(如果有的话)。
[0045]
如本文所用,术语“完全响应”(cr)意指所有临床可检测的恶性疾病的完全消失,其通过至少相隔4周的2次评估确定。
[0046]
如本文所用,术语“部分响应”(pr)意指所有可测量疾病的最长垂直直径的乘积总和比基线降低50%或更多,而没有可评估疾病的进展并且没有任何新病变的证据,如通过至少相隔4周的至少两次连续评估确定的。评估应显示溶解性病变的尺寸部分减少、溶解性病变的重新钙化或原始病变(blastic lesions)的密度降低。在转移性疾病位点观察到短暂的炎症并不罕见。表现出尺寸增加的单独病变未必取消pr的资格,除非在至少相隔28天进行的两次连续测量中记录了该增加。
[0047]“药学上可接受的赋形剂或载体”是指可以任选地包含在组合物中并且对患者不引起显著的不良毒理学反应的赋形剂。
[0048]“药学上可接受的盐”包括但不限于氨基酸盐、用无机酸制备的盐,诸如氯化物、硫酸盐、磷酸盐、磷酸氢盐、溴化物和硝酸盐,或由任一种前述的相应无机酸形式制备的盐,例如盐酸盐等,或用有机酸制备的盐,诸如苹果酸盐、马来酸盐、富马酸盐、酒石酸盐、琥珀酸
盐、乙基琥珀酸盐、柠檬酸盐、醋酸盐、乳酸盐、甲磺酸盐、苯甲酸盐、抗坏血酸盐、对甲苯磺酸盐、棕榈酸盐(palmoate)、水杨酸盐和硬脂酸盐,以及依托酸盐(estolate)、葡庚糖酸盐和乳糖醛酸盐。类似地,含有药学上可接受的阳离子的盐包括但不限于钠、钾、钙、铝、锂和铵(包括取代的铵)。
[0049]
如本文所用,术语“治疗(treatment)”、“治疗(treating)”等是指获得期望的药理学和/或生理学效应。该效应在完全或部分预防疾病或其症状的方面可以是预防性的,和/或在关于部分或完全治愈疾病和/或由该疾病引起的不良反应的方面可以是治疗性的。如本文所用,“治疗”涵盖了哺乳动物(特别是人)中的疾病的任何治疗,并且包括:(a)增加存活时间;(b)降低因疾病死亡的风险;(c)预防疾病在可能倾向于患该疾病但尚未被诊断为患有该疾病的受试者中发生;(d)抑制疾病,即阻止其发展(例如,降低疾病进展率);和(e)缓解疾病,即引起疾病消退。
[0050]“基本上纯的”通常是指分离物质(例如,化合物、分子、试剂),使得该物质占其所在样品的大部分百分比。通常在样品中,基本上纯的组分占样品的50%,优选80%-85%,更优选90-95%。
[0051]
术语“受试者”、“个体”和“患者”在本文中可互换使用,是指期望诊断、预后、治疗或疗法的任何哺乳动物受试者,特别是人。用于治疗目的的“哺乳动物”是指归类为哺乳动物的任何动物,包括人、家养和农场动物以及动物园、竞技或宠物动物,诸如狗、马、猫、牛、绵羊、山羊、猪等。在一些情况下,本发明的方法发现了在实验动物、兽医应用和疾病动物模型开发中的用途,包括但不限于啮齿动物,包括小鼠、大鼠和仓鼠;灵长类,和转基因动物。
[0052]
方法
[0053]
公开了用apkc iota的抑制剂治疗hedgehog途径依赖性癌症的方法。在一些实施方案中,apkc iota的抑制剂联合hdac1的抑制剂使用。不受特定理论的束缚,apkc磷酸化gli1转录因子,导致gli1的染色质结合和导致hedgehog途径激活的基因转录的激活。gli1活性受其核输入的调节所控制。也就是说,gli1在其不活跃的核纤层和其活跃的核质之间移动。apkc iota激活gli1的机制似乎涉及hdac1到gli1的募集,其中gli1由hdac1介导的脱乙酰作用激活。因此,apkc iota的抑制剂和hdac1的抑制剂可能在治疗hedgehog途径依赖性癌症中有用。
[0054]
虽然本发明的方法针对现有肿瘤的治疗,人们认识到该方法在预防治疗期间出现进一步的肿瘤生长中有用。
[0055]
非典型蛋白激酶c iota的抑制剂
[0056]
如上文所解释的,本发明的方法包括施用apkc iota的抑制剂。apkc iota的示例性抑制剂包括crt0422839(tev-47448)和crt0364436(tev-44229)或其药学上可接受的盐。
[0057]
crt0422839具有化学式:
[0058][0059]
crt0364436具有化学式:
[0060][0061]
此类apkc iota抑制剂在治疗hedgehog途径依赖性癌症中具有抗肿瘤活性。特别地,这些apkc iota抑制剂具有抑制hedgehog途径依赖性癌细胞的生长、增殖和转移、减少
hedgehog途径依赖性癌细胞中gli 1 mrna的产生,以及降低hedgehog途径依赖性癌细胞的生存力的能力(见实施例)。
[0062]
hdac1的抑制剂
[0063]
在某些实施方案中,用apkc iota抑制剂和hdac1抑制剂实施联合治疗。示例性的hdac1抑制剂包括异羟肟酸诸如伏立诺他、贝林司他、帕比司他、吉维司他、达西司他(laq824)和曲古抑菌素a;倍半萜内酯类诸如欧苷菊、环状四肽类诸如trapoxinb;缩肽类诸如罗米地辛以及苯甲酰胺类诸如恩提诺特(ms-275)、泰克地那林(ci994)和莫西司他。在一些实施方案中,使用选择性抑制hdac1而不影响其他hdac类别的抑制剂,诸如欧苷菊。
[0064]
hedgehog信号传导途径的抑制
[0065]
如本文所述,单独或联合hdac抑制剂的apkc iota抑制剂的使用抑制hh途径信号传导。抑制,意指降低、抑制、减少、减弱或拮抗该途径的活性。例如,可能想要在其中hh途径过度活跃或组成型活跃的细胞(例如癌细胞)中,例如在包含smo基因中的激活突变或者ptch或sufu基因中的失活突变的细胞中,或在其中过表达途径激活物诸如shh/ihh配体、smo或gli1/2的细胞中,用apkc iota抑制剂和/或hdac抑制剂抑制hh途径信号传导。促进hedgehog信号传导途径异常激活的其他突变是众所周知的并且由本领域技术人员可以容易地确定。关于与hedgehog信号传导异常激活相关的突变的综述,特别是癌症中牵涉的突变,参见,例如,pellegrini et al.(2017)int.j.mol.sci.18(11)pii:e2485,bao et al.(2018)mol.nutr.food res.62(1),levanat et al.(2017)curr.pharm.des.23(1):73-94,laukkanen et al.(2016)anticancer agents med.chem.16(3):309-317,suzman et al.(2015)cancers(basel).7(4):1983-1993,holikova et al.(2004)int.j.dermatol.43(12):865-869,wetmore(2003)curr.opin.genet.dev.13(1):34-42,bale(2002)annu.rev.genomics hum.genet.3:47-65,lacour et al.(2002)br.j.dermatol.146 suppl 61:17-19,wicking et al.(2001)cancer lett.173(1):1-7,and daya-grosjean et al.(2005)cancer lett.225(2):181-192;通过引用并入本文。
[0066]
在实施主题方法时,将单独或联合hdac抑制剂的apkc iota抑制剂以有效量,即有效抑制hh途径信号传导的量提供给细胞。从生化上讲,apkc iota抑制剂和/或hdac抑制剂的有效量或有效剂量是足以抑制细胞中hh途径信号传导30%或更多、40%或更多、50%或更多、60%或更多、70%或更多、80%或更多、90%或更多、100%或更多、200%或更多,或者500%或更多的量。换言之,与有效量或有效剂量的apkc iota抑制剂或hdac抑制剂接触的细胞中hh信号传导途径的活性将为尚未与有效量/剂量的apkc iota抑制剂和/或hdac抑制剂接触的细胞中观察到的活性的约70%或更少、约60%或更少、约50%或更少、约40%或更少、约30%或更少、约20%或更少、约10%或更少、约5%或更少,或将为约0%,即可以忽略。换言之,将使hh途径信号传导改变约0.5倍或更多、1倍或更多、2倍或更多、5倍或更多、8倍或更多,或者10倍或更多。
[0067]
apkc iota抑制剂或hdac抑制剂抑制细胞活性的量可以通过分子生物学领域的普通技术人员已知的多种方式确定。例如,细胞中磷酸化转录因子gli的量可以通过western印迹测量;与glidna靶序列结合的量可以通过电泳迁移率测定(emsa)来测量;通常由hh信号传导激活的转录因子例如ptchl、ptch2、hhipl、nhk2和rab34的表达量可以通过以下测量,例如通过测量作为gli转录靶标的基因的rna或蛋白质水平,或通过用包含与报告蛋白
诸如萤光素酶、egfp等可操作地连接的gli响应性启动子的核酸载体转染/感染细胞并且定性或定量测量产生的报告蛋白的量。以这种方式,可以证实apkc iota抑制剂或hdac抑制剂的抑制作用。
[0068]
在临床意义上,apkc iota抑制剂或hdac抑制剂的有效剂量是,当施用合适的时间段,通常至少约一周,并且可能约两周,或更长,多达约4周、8周或更长的时期时,将证明与hh信号传导途径的非期望活性相关的症状改变的剂量。例如,apkc iota抑制剂或hdac抑制剂的有效剂量是当施用合适的时间段,通常至少约一周,并且可以是约两周,或更长,多达约4周、8周或更长的时期时,将在患有癌症的患者中减缓、停止或逆转肿瘤生长和转移的剂量。本领域技术人员将理解,可以在该时间段施用初始剂量,然后是维持剂量,在一些情况下,维持剂量将是以降低的剂量。
[0069]
计算待施用的apkc iota抑制剂或hdac抑制剂的有效量或有效剂量在本领域普通技术人员的技能范围内,并且对本领域技术人员来说将是常规的。更不用说,最终的待施用量将取决于多种因素,包括施用途径、待治疗的病症或病况的性质以及患者之间不同的因素。有能力的临床医生将能够根据需要确定治疗药剂的有效量以向患者施用,以停止或逆转疾病状况的进展。利用ld
50
动物数据和药物的其他可用信息,临床医生可以根据施用途径确定个体的最大安全剂量。例如,考虑到治疗组合物正在施用到更大的体液中,静脉内施用的剂量可能大于鞘内或局部施用的剂量。类似地,从身体迅速清除的组合物可以以更高剂量或以重复剂量施用,以便维持治疗浓度。利用普通技能,有能力的临床医生将能够在常规临床试验过程中优化特定治疗的剂量。
[0070]
主题方法可用于在体外和体内细胞中抑制hh途径信号传导——并因此抑制与hh途径信号传导相关的细胞活性。例如,可以使任何细胞(其中hh途径信号传导是非期望的),例如癌细胞(其中不受控制的hh途径信号传导促进增殖或转移),与apkc iota抑制剂和/或hdac抑制剂接触。细胞可以来自任何哺乳动物物种,例如鼠、啮齿动物、犬、猫、马、牛、绵羊、灵长类、人等。
[0071]
如果主题方法在体外进行,细胞可以来自建立的细胞系或者它们可以是原代细胞,其中“原代细胞”、“原代细胞系”和“原代培养物”在本文中可互换使用以指已经衍生自受试者并容许在体外生长有限的培养物传代(即,分裂)次数的细胞和细胞培养物。例如,原代培养物是可能已经传代0次、1次、2次、4次、5次、10次或15次,但比足以通过危机阶段的次数,的培养物。通常,本发明的原代细胞系在体外维持少于10代。
[0072]
如果细胞是原代细胞,它们可以通过任何方便的方法从个体收获。例如,可以通过单采术、白细胞去除术、密度梯度分离等收获细胞,例如血细胞,例如白细胞。作为另一个实例,可以通过活体组织检查收获细胞,例如皮肤、肌肉、骨髓、脾脏、肝脏、胰腺、肺、肠、胃、神经系统组织等。可以使用合适的溶液来分散或悬浮收获的细胞。这种溶液将通常是平衡盐溶液,例如生理盐水、pbs、汉克氏平衡盐溶液等,其方便地补充有胎牛血清或其他天然存在的因子,结合可接受的低浓度缓冲液(一般为5-25mm)。方便的缓冲液包括hepes、磷酸盐缓冲液、乳酸盐缓冲液等。细胞可以立即使用,或者它们可以长期贮存、冷冻,解冻并能够再次使用。在这种情况下,细胞通常会在10%dmso、50%血清、40%缓冲培养基或如本领域所常用的一些其他此类溶液中冷冻,以在这种冷冻温度下保存细胞,并以如本领域公知的用于解冻冷冻培养细胞的方式解冻。
[0073]
apkc iota抑制剂或hdac抑制剂可以溶解在水或醇或诸如dmso或dmf的溶剂中,并在提供给细胞之前稀释到水或合适的缓冲液中。
[0074]
为了调控hh途径信号传导,可以向细胞提供apkc iota抑制剂或hdac抑制剂约30分钟至约24小时,例如,1小时、1.5小时、2小时、2.5小时、3小时、3.5小时、4小时、5小时、6小时、7小时、8小时、12小时、16小时、18小时、20小时或从约30分钟到约24小时的任何其他时间段,其可以以约每天到约每4天的频率重复,例如每1.5天、每2天、每3天或从约每天到约每四天的任何其他频率。可以向受试细胞提供一次或多次药剂,例如一次、两次、三次或多于三次,并且每次接触事件后容许细胞与药剂一起温育一段时间,例如16-24小时,在该时间后,将培养基更换为新鲜培养基并进一步培养细胞。
[0075]
细胞与apkc iota抑制剂或hdac抑制剂的接触可以发生在促进细胞存活的任何培养基中和任何培养条件下。例如,细胞可以悬浮在任何方便的合适的营养培养基中,诸如iscove改良的dmem或rpmi 1640,其补充有胎牛血清或热灭活山羊血清(约5-10%)、l-谷氨酰胺、硫醇(特别是2-巯基乙醇)和抗生素(例如青霉素和链霉素)。培养物可能含有细胞对其响应的生长因子。如本文所定义的,生长因子是能够通过对跨膜受体的特异性作用促进培养物中或完整组织中细胞存活、生长和/或分化的分子。生长因子包括多肽和非多肽因子。促进细胞存活的条件通常允许非同源末端连接和同源重组。
[0076]
本技术中用于研究和治疗的感兴趣的癌细胞包括癌前(例如,良性)、恶性、转移前、转移性和非转移性细胞,其中癌性表型由hh途径信号传导促进。换句话说,hh途径信号传导(以及在许多情况下,不受调节的hh途径信号传导)使个体中的细胞倾向于变为癌性,或者诱导或增强个体中的癌症症状,例如肿瘤生长和转移。在许多此类情况下,相对于健康细胞中观察到的信号传导水平,肿瘤细胞中hh途径信号传导升高,例如,超过健康细胞中hh途径信号传导的量2倍或更高、3倍或更高、4倍或更高、6倍或更高、8倍或更高、10倍或更高、20倍或更高,或者50倍或更高。hh信号传导的水平可以通过任何方便的方法(例如,如本领域已知的或如本文所描述的)来测量。
[0077]
在一些应用中,采用apkc iota抑制剂或hdac抑制剂在体内调控hh途径信号传导,例如抑制肿瘤生长或转移以治疗癌症。在这些体内实施方案中,将apkc iota抑制剂或hdac抑制剂直接施用于个体。apkc iota调控剂可以通过如下所述的本领域中许多公知的方法中的任一种来施用。
[0078]
配制剂
[0079]
可以将apkc iota抑制剂(例如,crt0422839或crt0364436)或hdac抑制剂掺入多种配制剂中。更具体地,apkc iota抑制剂或hdac抑制剂可以通过联合合适的药学上可接受的载体或稀释剂而配制成药物组合物。药物制剂是在药学上可接受的载体中包含一种或多种apkc iota抑制剂和/或hdac抑制剂的组合物。“药学上可接受的载体”可以是联邦或州政府的管理机构批准的或在u.s.药典或其他普遍认可的药典中列出的用于哺乳动物,诸如人的媒介物。术语“媒介物”是指稀释剂、佐剂、赋形剂或载体,其与本发明的化合物一起配制用于向哺乳动物施用。此类药物媒介物可以是脂质,例如脂质体,例如脂质体树枝状聚合物;液体,诸如水和油,包括石油、动物、植物或合成来源的那些,诸如花生油、大豆油、矿物油、芝麻油等,盐水;阿拉伯树胶、明胶、淀粉糊、滑石、角蛋白、胶体硅、尿素等。此外,可以使用辅助剂、稳定剂、增稠剂、润滑剂和着色剂。药物组合物可以配制成固体、半固体、液体或
气体形式的制剂,诸如片剂、胶囊剂、粉剂、颗粒剂、软膏剂、溶液、栓剂、注射剂、吸入剂、凝胶剂、微球和气雾剂。因此,apkc iota抑制剂和/或hdac抑制剂的施用可以通过多种方式实现,包括透皮、皮内、口服、含服、直肠、肠胃外、腹膜内、皮内、气管内等施用。活性剂在施用后可以是系统性的,或者可以通过使用区域施用、壁内施用或使用在植入位点处表现出保持活性剂量的植入物而局部化。活性剂可配制成用于即时活性或可配制成用于持续释放。
[0080]
对于一些病况,特别是中枢神经系统病况,可能需要配制穿过血脑屏障(bbb)的药剂。药物递送通过血脑屏障(bbb)的一种策略需要通过渗透方式(诸如甘露醇或白三烯)或通过使用血管活性物质(例如缓激肽)生化上破坏bbb。使用bbb开放将特定药剂靶向脑肿瘤的潜力也是选择。当组合物通过血管内注射施用时,bbb破坏剂可以与本发明的治疗组合物共同施用。穿过bbb的其他策略可能需要使用内源性转运系统,包括小窝蛋白-1介导的转胞吞作用、载体介导的转运体(诸如葡萄糖和氨基酸载体)、受体介导的胰岛素或转铁蛋白的转胞吞作用,以及主动外排转运体(诸如p-糖蛋白)。活性转运部分也可以与用于本发明的治疗化合物缀合以促进穿过血管内皮壁的转运。或者,治疗药剂在bbb后的药物递送可以通过局部递送,例如通过鞘内递送,例如通过ommaya储液器(参见例如美国专利号5,222,982和5385582,通过引用并入本文);通过团注,例如通过注射器,例如经玻璃体内或经颅内;通过连续输注,例如通过套管插入法,例如用对流(参见例如美国申请号20070254842,通过引用并入本文);或通过植入已可逆地附着药剂的装置(参见例如美国申请号20080081064和20090196903,通过引用并入本文)。
[0081]
为了包含在药物中,apkc iota抑制剂和/或hdac抑制剂可以从合适的商业来源获得。作为一般性观点,每剂肠胃外施用的apkc iota抑制剂和/或hdac抑制剂的总药学上有效量将在可通过剂量响应曲线测量的范围内。
[0082]
对于有或没有hdac抑制剂的基于apkc iota抑制剂的疗法,即用于治疗性施用的制剂,可以是无菌的。通过无菌过滤膜(例如0.2μm膜)过滤很容易实现无菌。治疗组合物通常放置于具有无菌进入孔的容器中,例如静脉内溶液袋或具有可由皮下注射针头穿透的塞子的小瓶。包含apkc iota抑制剂和/或hdac抑制剂的组合物可以作为水溶液或作为重建用冻干配制剂贮存在单位或多剂量容器,例如密封安瓿或小瓶中。作为冻干制剂的实例,10ml小瓶装5ml无菌过滤的1%(w/v)化合物水溶液,并将所得混合物冻干。通过使用抑菌注射用水重建冻干化合物来制备输注溶液。或者,apkc iota抑制剂和/或hdac抑制剂可以配制成用于局部施用的洗剂。
[0083]
药物组合物可包括(取决于期望的配制剂)药学上可接受的、无毒的稀释剂载体,其定义为通常用以配制用于动物或人施用的药物组合物的载体。选择稀释剂以便不影响组合的生物活性。此类稀释剂的实例是蒸馏水、缓冲水、生理盐水、pbs、林格氏溶液、葡萄糖溶液和汉克氏溶液。此外,药物组合物或制剂可包括其他载体、佐剂或无毒、非治疗性、非免疫原性的稳定剂、赋形剂等。组合物还可包括额外物质以接近生理条件,诸如ph调节和缓冲剂、毒性调节剂、润湿剂和去污剂。
[0084]
组合物还可以包含多种稳定剂中的任一种,诸如抗氧化剂。当药物组合物包含多肽时,多肽可以与各种熟知的化合物络合,该化合物增强多肽的体内稳定性,或以其他方式增强其药理特性(例如,增加多肽的半衰期、降低其毒性,增强溶解度或吸收)。这种改性或络合剂的实例包括硫酸盐、葡萄糖酸盐、柠檬酸盐和磷酸盐。组合物的核酸或多肽也可以与
增强其体内特性的分子络合。此类分子包括,例如碳水化合物、多胺、氨基酸、其他肽、离子(例如钠、钾、钙、镁、锰)和脂质。
[0085]
关于适合于各种类型施用的制剂的进一步指导可以在remington'spharmaceutical sciences,mace publishing company,philadelphia,pa.,17th ed.(1985)中找到。对于药物递送方法的简要综述,参见langer,science 249:1527-1533(1990)。
[0086]
可以施用药物组合物用于预防性和/或治疗性治疗。活性成分的毒性和治疗功效可以根据细胞培养物和/或实验动物中的标准制药规程来确定,包括,例如,确定ld50(对50%群体致死的剂量)和ed50(在50%群体中治疗有效的剂量)。毒性和治疗作用之间的剂量比是治疗指数,它可以表示为比值ld50/ed50。表现出大治疗指数的疗法是优选的。
[0087]
从细胞培养和/或动物研究中获得的数据可用于为人制定一系列剂量。活性成分的剂量通常在包括具有低毒性的ed50的循环浓度范围内。剂量可以在此范围内变化,其取决于所采用的剂型和所采用的给药途径。
[0088]
用于配制药物组合物的组分优选具有高纯度并且基本上不含潜在的有害污染物(例如,至少国家食品(nf)级,通常至少分析级,并且更通常至少药物级)。此外,意图在体内使用的组合物通常是无菌的。就给定化合物在使用前必须合成来说,所得产物通常基本上不含任何在合成或纯化过程中可能存在的潜在毒性剂,特别是任何内毒素。用于肠胃外施用的组合物也是无菌的、基本上等渗的并且在gmp条件下制备。
[0089]
除了其他药剂之外,还可以提供apkc iota抑制剂和/或hdac抑制剂。例如,在治疗由hh途径信号传导促进的癌症的方法中,apkc iota抑制剂和/或hdac抑制剂可以与其他已知的癌症疗法共同施用。
[0090]
施用
[0091]
可根据本文所述方法治疗的hedgehog途径依赖性癌症包括依赖于hedgehog途径激活或与hedgehog途径异常激活或组成型激活相关的任何癌症,诸如但不限于,基底细胞癌、髓母细胞瘤、横纹肌肉瘤、小细胞肺癌、视网膜母细胞瘤、胃和上消化道癌症、骨肉瘤、胰腺癌、乳腺癌、结肠癌、卵巢癌、脑癌、乳腺癌症、甲状腺癌和前列腺癌。
[0092]
单独或联合hdac抑制剂和/或任选地其他抗癌剂施用至少一种治疗有效剂量的apkc iota抑制剂(例如,crt0422839或crt0364436)。这些药剂中的每一种的“治疗有效剂量或量”意指当施用时引起关于个体hedgehog途径依赖性癌症治疗的积极治疗响应的量。特别感兴趣的是提供了如本文所定义的抗肿瘤效应的这些药剂的量。“积极治疗响应”意指根据本发明接受治疗的个体表现出个体正在接受疗法所针对的hedgehog途径依赖性癌症的一种或多种症状的改善。
[0093]
因此,例如,“积极治疗响应”将是与疗法(例如,使用apkc iota抑制剂的疗法或使用apkc iota抑制剂和hdac抑制剂和/或任选地其他抗癌剂的联合疗法)关联的疾病的改善,和/或与疗法关联的疾病的一种或多种症状的改善。因此,例如,积极治疗响应将指疾病中以下一项或多项改善:(1)肿瘤尺寸减小;(2)癌细胞数量减少;(3)抑制(即在一定程度上减缓,优选停止)肿瘤生长;(4)抑制(即在一定程度上减缓,优选停止)癌细胞浸润到周围器官中;(5)抑制(即在一定程度上减缓,优选停止)肿瘤转移;和(6)在一定程度上缓解与癌症相关的一种或多种症状。
[0094]
这种治疗响应可以进一步表征为改善的程度。因此,例如,改进可以表征为完全响应。“完全响应”是指经体格检查、实验室、核和放射学研究(即ct(计算机断层扫描术)和/或mri(磁共振成像)),以及对进入研究时的所有初始异常或阳性部位进行重复的其他非侵入性规程所确认的所有可测量或可评估疾病的所有症状和体征消失的记录。或者,疾病的改善可归类为是部分响应。“部分响应”是指当与治疗前测量值相比时,所有可测量病变的垂直直径的乘积之和减少50%以上(仅对于可评估响应的患者,部分响应不适用)。
[0095]
在某些实施方案中,将根据每日给药方案或间歇性施用单独或联合hdac抑制剂和任选地其他抗癌剂的多个治疗有效剂量的apkc iota抑制剂。例如,治疗有效剂量的施用可以每周一天、每周两天、每周三天、每周四天或每周五天等等。“间歇性”施用意指施用治疗有效剂量可以,例如,每隔一天、每两天、每三天等等。例如,在一些实施方案中,将每周两次地或每周三次地施用单独或联合hdac抑制剂和/或任选地其他抗癌剂的apkc iota抑制剂持续延长的时间段,例如持续1、2、3、4、5、6、7、8...10...15...24周,等等。“每周两次地”或“每周两次”意指在从给药第一周的第1天开始的7天时期内向受试者施用两个治疗有效剂量的正在讨论的药剂,剂量之间最少72小时以及最多96小时。“每周三次地”或“每周三次”意指在7天时期内向受试者施用三个治疗有效剂量,容许剂量之间最少48小时以及剂量之间最多72小时。出于本发明的目的,这种类型的给药称为“间歇性”疗法。根据本发明的方法,受试者可以接受间歇性疗法(即,每周两次地或每周三次地施用治疗有效剂量),持续一个或多个周周期,直到实现期望的治疗响应。药剂可以通过如下文所述的任何可接受的施用途径施用。
[0096]
在某些实施方案中,施用具有apkc iota抑制剂和hdac抑制剂以及任选地其他抗癌剂的联合疗法。apkc iota抑制剂可以在hdac抑制剂之前、同时或之后给药。如果与hdac抑制剂同时提供,则apkc iota抑制剂可以在相同或不同的组合物中提供。因此,这两种药剂可以通过同时治疗的方式呈递给个体。“同时治疗”意指向人受试者施用,使得在接受治疗的受试者中引起物质组合的治疗作用。例如,根据特定给药方案,可以通过施用至少一种治疗有效剂量的包含apkc iota抑制剂的药物组合物和至少一种治疗有效剂量的包含至少一种hdac抑制剂的药物组合物来实现同时治疗。类似地,可以以至少一个治疗剂量施用apkc iota抑制剂和/或hdac抑制剂和任选地其他抗癌剂。单独的药物组合物的施用可以在相同时间(即同时)或在不同时间(即依次、以任一顺序、在同一天或在不同天)进行,只要在接受治疗的对象中引起这些物质组合的治疗作用。
[0097]
在某些实施方案中,apkc iota抑制剂在施用hdac抑制剂之前持续短暂时期施用并且在hdac抑制剂治疗停止后继续持续短暂时期以确保治疗期间受试者体内apkc iota抑制剂的水平充足,以抑制gli1和hdac1的结合以及gli1和hedgehog信号传导途径的激活。例如,向受试者施用apkc iota抑制剂可以开始于在施用第一剂hdac抑制剂前一周,并持续到在施用最后一剂hdac抑制剂后一周。
[0098]
在其他实施方案中,包含诸如apkc iota抑制剂和/或hdac抑制剂和/或任选地其他抗癌剂的药剂的药物组合物是持续释放制剂,或是使用持续释放装置施用的制剂。此类装置在本领域中是公知的,并且包括例如透皮贴剂和微型可植入式泵,其可以在各种剂量下以连续的、稳态的方式提供随时间的药物递送,以用非持续释放的药物组合物实现持续释放作用。
[0099]
包含apkc iota抑制剂和/或hdac抑制剂和任选地其他抗癌剂的药物组合物可以依照本领域已知的任何医学上可接受的方法使用相同或不同的给药途径施用。合适的施用途径包括肠胃外施用,诸如皮下(sc)、腹膜内(ip)、肌内(im)、静脉内(iv)或输注、口服、肺部、鼻、局部、透皮、瘤内和塞药。当组合物经肺部递送施用时,调整治疗有效剂量使得诸如apkc iota抑制剂和/或hdac抑制剂的药剂在血流中的可溶性水平等同于用经肠胃外(例如sc、ip、im或iv)施用治疗有效剂量而获得的水平。在一些实施方案中,包含apkc iota抑制剂和/或hdac抑制剂和任选地其他抗癌剂的药物组合物通过im或sc注射(特别是通过im或sc注射局部至肿瘤)施用。在一些实施方案中,apkc iota抑制剂和/或hdac抑制剂以及任选地其他抗癌剂例如在贴剂上或在凝胶中局部施用。
[0100]
在一些实施方案中,apkc iota抑制剂和/或hdac抑制剂以及任选地其他抗癌剂通过输注或通过局部注射施用,例如通过以约50mg/h至约400mg/h的速率输注,包括约75mg/h至约375mg/h、约100mg/h至约350mg/h、约150mg/h至约350mg/h、约200mg/h至约300mg/h、约225mg/h至约275mg/h。示例性的输注速率可实现期望的治疗剂量,例如约0.5mg/m2/天至约10mg/m2/天的,包括约1mg/m2/天至约9mg/m2/天、约2mg/m2/天至约8mg/m2/天、约3mg/m2/天至约7mg/m2/天、约4mg/m2/天至约6mg/m2/天、约4.5mg/m2/天至约5.5mg/m2/天。施用(例如,通过输注)可以在期望的时期内重复,例如在约1天至约5天的时期内重复或每几天,例如,约5天、约1个月内、约2个月等重复一次。apkc iota抑制剂和/或hdac抑制剂也可以在其他治疗干预诸如手术干预以去除癌细胞之前、之时或之后施用。apkc iota抑制剂和/或hdac抑制剂也可以作为联合疗法的一部分施用,在联合疗法中向受试者施用免疫疗法、化学疗法、放射疗法或生物疗法中的至少一种。
[0101]
影响待施用的各种组合物的各自量的因素包括但不限于施用方式、施用频率(即,每天或间歇性施用,诸如每周两次或三次)、接受治疗的特定疾病、疾病的严重性、疾病史、个体是否正在接受另一种治疗剂的同时治疗,以及正在接受治疗的个体的年龄、身高、体重、健康和身体状况。通常,随着正在接受治疗的受试者体重的增加,优选更高剂量的该药剂。
[0102]
apkc iota抑制剂和/或hdac抑制剂和任选地其他抗癌剂的个体剂量通常不低于对受试者产生可测量效应所需的量,并且可以基于apkc iota抑制剂和/或hdac抑制剂和任选地其他抗癌剂及其副产物的吸收、分布、代谢和排泄(“adme”)的药物代谢动力学和药理学,以及因此基于受试者体内组合物的分布来确定。这包括考虑施用途径以及剂量,可以为局部(为了主要地局部效应在期望作用的地方直接应用)、肠内(当保留在部分消化道时,为了全身或局部效应经消化道应用),或肠胃外(为了全身或局部效应通过消化道以外的途径应用)应用进行调整。例如,apkc iota抑制剂(例如,crt0422839或crt0364436)的施用可以是局部的或通过注射,例如静脉内、肌内或瘤内注射或其组合。
[0103]
在受试者体内apkc iota抑制剂的分布及其相应的生物活性通常从存在于感兴趣的靶标处的apkc iota抑制剂的比例进行评估。例如,一旦施用apkc iota抑制剂,其可以与糖缀合物或其他生物靶标一起累积,使物质聚集在癌细胞和癌组织中。因此,施用apkc iota抑制剂以便随时间在感兴趣的靶标中累积的给药方案可以是容许较低个体剂量的策略的一部分。这也可能意味着,例如,相对于从体外测定计算的有效浓度,可以将在体内清除较慢的apkc iota抑制剂的剂量降低(例如,体外有效量近似于mm浓度,相对于低于mm体
内浓度)。
[0104]
作为实例,有效剂量或给药方案可以从用于抑制apkc激酶活性和/或gli1激活、和/或hedgehog途径的激活和/或细胞增殖和/或细胞迁移/侵袭的给定apkc iota抑制剂的ic
50
精确计量。“ic
50”意指在体外50%抑制所需的药物浓度。或者,有效量可以从给定的apkc iota抑制剂浓度的ec
50
精确计量。“ec
50”意指获得体内最大效应的50%所需的血浆浓度。在相关实施方案中,剂量也可以基于ed50(有效剂量)来确定。
[0105]
一般而言,有效量通常不超过计算出的ic
50
的200倍。通常,相比计算出的ic
50
,施用的apkc iota抑制剂的量低于约200x、低于约150x、低于约100x,并且许多实施方案低于约75x、低于约60x、50x、45x、40x、35x、30x、25x、20x、15x、10x,甚至低于约8x或2x。在一个实施方案中,有效量为计算出的ic
50
的约1x至50x,有时为计算ic
50
的约2x至40x、约3x至30x或约4x至20x。在其他实施方案中,有效量与计算出的ic
50
相同,并且在某些实施方案中,有效量为大于计算出的ic
50
的量。
[0106]
效应量通常不超过计算出的ec
50
的100倍。例如,相比计算出的ec
50
,施用的apkc iota抑制剂的量低于约100x、低于约50x、低于约40x、35x、30x或25x,并且许多实施方案低于约20x、低于约15x甚至低于约10x、9x、9x、7x、6x、5x、4x、3x、2x或1x。有效量可以为计算出的ec
50
的约1x至30x,有时为计算出的ec
50
的约1x至20x,或约1x至10x。有效量也可以与计算出的ec
50
相同或大于计算出的ec
50
。ic
50
可以通过在体外抑制apkc激酶活性和/或gli1激活、和/或细胞增殖和/或细胞迁移/侵袭来计算。
[0107]
为了实现功效,apkc iota抑制剂的水平必须高于特定水平持续特定时间。功效是剂量依赖性的,更高水平的apkc iota抑制剂有助于更大的抗肿瘤效应。为了使毒性最小化,apkc iota抑制剂的水平可以在特定时间内保持在某个水平以下并且持续特定时间(“休息期”容许清除apkc iota抑制剂)。也就是说,,药物保持在一定水平以下直至给予下一次剂量之前的一定时间。多次剂量之间更短的休息时间会导致更大毒性。
[0108]
在某些实施方案中,治疗患有hedgehog途径依赖性癌症的患者的方法包括用单独或联合hdac抑制剂和/或任选地其他抗癌剂的apkc iota抑制剂的治疗周期,随后是休息期,在休息期内不施用apkc iota抑制剂和/或hdac抑制剂以容许患者从apkc iota抑制剂和/或hdac抑制剂的不需要的效应中“恢复”。多剂量的apkc iota抑制剂和/或hdac抑制剂可以根据每日给药方案或间歇性给药,随后是休息期。
[0109]
在依照前述给药方案接受治疗的受试者表现出部分响应或在延长的缓解期后复发时,可能需要后续治疗过程以实现疾病的完全缓解。因此,在第一治疗期的休息时期(a period of time off)后,受试者可以接受一个或多个另外的治疗期,其包括单独或联合hdac抑制剂和任选地其他抗癌剂施用apkc iota抑制剂。治疗期之间的这种休息时期在本文中称为中止时间段。人们认识到,中止时间段的长度取决于用这些治疗剂治疗的任何先前治疗期所达到的肿瘤响应的程度(即,完全相对于部分)。
[0110]
应用
[0111]
由失调的hh途径信号传导促进的癌症的一个实例是基底细胞癌(bcc)。bcc肿瘤具有升高的gli水平,并且针对bcc的分子靶向药物集中于拮抗smo和减少gli mrna。一个这样的实例是环巴胺,一种抑制smo的植物生物碱。模型系统(体外和体内)显示环巴胺有效地抑制bcc,但环巴胺的临床应用显示出会妨碍其使用的严重副作用。另一种在转移性bcc肿瘤
中已经显示出良好功效的smo拮抗剂是维莫德吉(vismodegib)。其他治疗包括手术、化学疗法、免疫疗法(诸如南欧大戟(euphorbia peplus),咪喹莫特,aldara)和放射疗法。在某些情况下,bcc对smo拮抗剂有抗性,因为hh途径中的激活突变在下游或是smo的上位,或者癌细胞已经发展出对smo拮抗剂的抗性。主题方法可以应用于此类癌症。
[0112]
由失调的hh途径信号传导促进的病症的另一个实例是基底细胞痣综合征(bcns),也称为gorlin综合征,其标志为数十至数百个bcc的发展的罕见多系统疾病。具有bcns的受试者遗传了ptch1的缺陷拷贝。bcns是罕见疾病,在人群中具有每56,000-164,000人中1病例的患病率,没有有效和可耐受治疗。因此,治疗或预防bcc肿瘤的药物对于患有bcns的受试者是感兴趣的。
[0113]
主题方法和组合物可用于治疗或预防两个临床人群中的bcc:i)具有遗传性bcc肿瘤的患者,例如具有基底细胞痣综合征的患者;和ii)一般人群中具有散发性bcc肿瘤的患者。在美国,bcc是最常见的癌症,每年诊断出100万个新病例。尽管bcc很少致命,但它们在受累个体中的高发病率和频繁复发可导致显著的发病率。目前,皮肤癌的发病率逐年上升,皮肤癌的治疗使国家卫生服务承受了巨大的负担。目前,没有bcc预防的有效疗法,因为在随机对照试验中尚未显示防晒霜可减少bcc的发展。
[0114]
由失调的hh途径信号传导促进的癌症的另一个实例是髓母细胞瘤。髓母细胞瘤是高度恶性的原发性脑肿瘤,起源于小脑或后颅窝。髓母细胞瘤是最常见的恶性脑肿瘤,占新诊断的病例的14.5%。髓母细胞瘤通常在第四脑室附近,脑干和小脑之间形成。髓母细胞瘤的已知疗法包括化学疗法,例如洛莫司汀、顺铂、卡铂、长春新碱或环磷酰胺和维莫德吉中的一种或多种。主题方法可以应用于对smo拮抗剂有抗性(或已经产生抗性)的髓母细胞瘤。
[0115]
由失调的hh途径信号传导促进的癌症的另一个实例是横纹肌肉瘤。横纹肌肉瘤是一种肉瘤(结缔组织癌症),其中的癌细胞被认为是由骨骼肌祖细胞产生。它可以在任何解剖位置找到。大多数发生在天然缺乏骨骼肌的区域,诸如头、颈和泌尿生殖道。横纹肌肉瘤的诊断依赖于对朝向骨骼肌细胞分化的识别。蛋白质myod1和肌细胞生成素是通常存在于发育中的骨骼肌细胞中的转录因子蛋白质,其在肌肉成熟后消失并变得受神经支配。因此,myod1和肌细胞生成素通常不存在于正常骨骼肌中,并且可以充当横纹肌肉瘤的有用免疫组织化学标志物。横纹肌肉瘤的治疗包括化学疗法、放射疗法,和有时手术。
[0116]
其他组织中的hedgehog途径依赖性癌症,包括其他组织中对smo拮抗剂有抗性的hedgehog途径依赖性癌症变体,也可以通过主题方法治疗。这些包括,例如,小细胞肺癌、胰腺癌、结肠直肠癌、卵巢癌和前列腺癌的亚型,所有这些亚型已经显示对hedgehog途径的阻断剂响应。
[0117]
试剂盒
[0118]
提供了包含一个或多个容器的试剂盒,该容器容纳组合物,所述组合物包含至少一种apkc iota抑制剂(例如,crt0422839或crt0364436)和/或hdac抑制剂和/或任选地一种或多种用于治疗hedgehog途径依赖性癌症的其他抗癌剂。组合物可以是液体形式或可以是冻干的。用于组合物的合适容器包括例如瓶、小瓶、注射器和试管。容器可以由多种材料制成,包括玻璃或塑料。容器可以具有无菌进入孔(例如,容器可以是静脉内溶液袋或具有可由皮下注射针穿透的塞子的小瓶)。
[0119]
该试剂盒还可包括第二容器,该容器包含药学上可接受的缓冲液,诸如磷酸盐缓
冲盐水、林格氏溶液或葡萄糖溶液。它还可以包含对终端用户有用的其他材料,包括其他药学上可接受的配制溶液,诸如缓冲液、稀释剂、过滤器、针头和注射器或其他递送装置。递送装置可以预先填充有组合物。
[0120]
该试剂盒还可以包括包装说明书,该说明书包含使用包含apkc iota抑制剂和/或hdac抑制剂的组合物治疗受试者hedgehog途径依赖性癌症的方法的书面说明。包装说明书可以是未经批准的包装说明书草稿,也可以是经食品和药物管理局(fda)或其他监管机构批准的包装说明书。或者,可以在已记录信息的计算机可读介质(例如软盘、cd、dvd、闪存驱动器等)上提供说明,或者可以在网站地址上呈现说明,其可以经由互联网访问删除已站点上的信息来使用。为治疗受试者hedgehog途径依赖性癌症提供说明的任何方便方法可以存在于试剂盒中。
实施例
[0121]
提出以下实施例是为了为本领域普通技术人员提供如何制作和使用本发明的完整公开和描述,并不意图限制本发明人认作他们发明的范围也不意图代表以下实验是全部或唯一进行的实验。已做出努力确保关于所用数字(例如数量、温度等)的准确性,但应该考虑一些实验误差和偏差。除非另有说明,部分为重量部分,分子量为质量平均分子量,温度为摄氏温度,以及压力是在大气压或接近大气压。
[0122]
分子和细胞生物化学的一般方法可以在以下这些标准教科书中找到:molecular cloning:a laboratory manual,3rd ed.(sambrook et al.,harbor laboratory press 2001);short protocols in molecular biology,4th ed.(ausubel et al.eds.,john wiley&sons 1999);protein methods(bollag et al.,john wiley&sons 1996);nonviral vectors for gene therapy(wagner et al.eds.,academic press 1999);viral vectors(kaplift&loewy eds.,academic press 1995);immunology methods manual(i.lefkovits ed.,academic press 1997);和cell and tissue culture:laboratory procedures in biotechnology(doyle&griffiths,john wiley&sons 1998),其公开内容通过引用并入本文。本公开中提及的用于基因操作的试剂、克隆载体和试剂盒可从商业供应商获得,例如biorad、stratagene、invitrogen、sigma-aldrich和clontech。
[0123]
实施例1
[0124]
bcc细胞模型中的hedgehog途径调控
[0125]
简介
[0126]
为了生存和生长,基底细胞癌(bcc)需要高水平的hedgehog(hh)信号传导(chang et al.(2012)arch.dermatol.148(11):1324-1325、atwood et al.(2015)cancer cell 27(3):342-353、atwood et al.(2013)nature 494(7438):484-488、hutchin et al.(2005)genes dev.19(2):214-223)。hh途径的激活涉及hh配体与patched-1结合,从而减轻对smoothened(smo)的抑制。这导致转录因子gli家族的激活,最终促进hh靶基因(包括gli1本身)的转录。最近fda已经批准smo抑制剂用于bcc治疗,但耐药性已经作为显著问题而发生(chang et al.,同上;atwood et al.(2015),同上;sekulic et al.(2012)n.engl.j.med.366(23):2171-21791)。由于bcc一致地依赖于hh途径进行生长(atwood et al.(2015),同上),抗性bcc进化以使用途径内在突变以及gli激活的非经典机制来规避smo
水平的药理学阻断(atwood et al.(2015),同上;atwood et al.(2013),同上;)。
[0127]
最近,我们将非典型过度激活鉴定为bcc中耐药性的强大机制(atwood et al.(2013),同上;)。gli1锌指结构域的apkc磷酸化导致染色质结合、基因转录和在smo和patched-1输入下游的hh途径激活。此外,gli促进apkc的转录,与gli形成另一个正反馈回路。这种非经典hh信号传导途径的过度激活驱动了晚期bcc中的途径激活和维莫德吉(vismodegib)逃逸(atwood et al.(2013),同上;)。apkc的小分子抑制剂,变构的(erdogan et al.(2006)j.biol.chem.281(38):28450-28459)或正构的(et al.(2013)biochem.j.451(2):329-342),正在开发中但尚未应用于治疗bcc。
[0128]
在smo下游,通过p300进行乙酰化和随后的去乙酰化进一步调节gli蛋白。组蛋白去乙酰化酶1/2(hdac1/2)分别在k518和k757处对gli1/2的去乙酰化是染色质结合和基因转录所需的gli转录因子核成熟过程中的关键步骤(canettieri et al.(2010)nat.cell biol.12(2):132-142)。hdac1本身是gli的转录靶标,创建hh信号传导的第三正反馈回路。特别令人感兴趣的是,已经提议hdac抑制用于治疗许多hh驱动的癌症(canettieri et al.,同上;coni et al.(2017)sci rep.7:44079;zhao et al.(2014)pharmacol.res.perspect.2(3):e00043;coni et al.(2013)plos one 8(6):e65718)。hdac抑制剂通过改变组蛋白-dna复合物和改变非组蛋白的乙酰化状态来阻断生长并促进细胞凋亡(falkenberg et al.(2014)nat.rev.drug discov.13(9):673-691)。伏立诺他是i/ii类hdac抑制剂,目前fda已经批准用于治疗皮肤淋巴瘤(mann et al.(2007)clin.cancer res.13(8):2318-2322)。不幸的是,hdac抑制受其广泛的细胞毒性性质阻碍。由于缺乏经过验证的靶点和临床开发的成本,从头药物发现仍然是挑战性的(hoelder et al.(2012)mol.oncol.6(2):155-176)。
[0129]
在此我们显示apkc iota抑制剂crt0422839和crt0364436调控bcc细胞生存力并降低gli1 mrna的水平,与gli途径调控一致。
[0130]
结果
[0131]
为了在体外研究apkc iota抑制对bcc的功效,用增加剂量的crt0422839或crt0364436处理鼠bcc细胞系。经crt0422839或crt0364436处理导致bcc生长和生存力的剂量依赖性降低(图1c和1d)。将bcc生存力与经apkc抑制剂psi(图1a)和crt0329868(图1b)处理的生存力(如先前mirza等人(mirza et al.(jci insight(2017)2(21)pii:e97071;在此通过引用整体并入)所述)进行比较。此外,经crt0422839或crt0364436处理导致gli1 mrna水平的剂量依赖性降低(图2a和2b)。
[0132]
实施例2
[0133]
apkc iota的生化激酶测定
[0134]
使用imap fp渐进结合系统(molecular devices r8127)在384孔黑色、非结合、平底测定板(corning 3575)中测量化合物抑制apkc iota激酶活性的能力。测定混合物(最终体积=10μl)含有20mm tris-hcl(ph 7.5)、150μm atp、10mm mgcl2、0.01%triton x-100、250μm egta、1mm dtt、15pm pkcι(emd millipore 14-505)、100nm fam-pkcε-假底物(molecular devices rp7548)、0.1%dmso和各种浓度的测试化合物crt0422839和crt0364436。使用biomek nx针工具(beckman coulter)将化合物稀释液(在100%dmso中制
备)以100nl添加到测定板。通过添加atp(milliporesigmaa7699)启动酶反应,然后将板在25℃恒温箱中温育1小时。将20μl等份式样的imap检测试剂(1:400于85%1x结合缓冲液a和15%1x结合缓冲液b中)添加到每个孔中,然后在25℃下温育2小时。然后,使用perkinelmer envision 2102多标记读板器(perkinelmer),使用fp双镜、fp480激发滤光片以及p-pol 535和s-pol 535发射滤光片测量fp。使用activitybase(idbs)进行数据分析。通过在xlfit4(idbs)中绘制与化合物浓度的log10相对的百分比抑制对并拟合4参数逻辑模型(顶部和底部分别限制为100和0)来计算ic50值。
[0135]
前述仅说明了本发明的原理。应当理解,本领域的技术人员将能够设计出各种布置,体现本发明的原理并且包括在其精神和范围内,尽管本文没有明确描述或显示。此外,本文引用的所有实例和条件语言主要意图帮助读者理解本发明的原理和发明人为促进本领域所贡献的概念,并且将解释为不限于这些具体引用的实例和状况。此外,叙述本发明的原理、方面和实施方案及其具体实施例的本文所有陈述意图涵盖其结构和功能等同物。此外,此类等同物意图包括当前已知的等同物和未来开发的等同物,即,所开发的执行相同功能的任何元素,而不管结构。因此,本发明的范围并不意图限于本文所示和描述的示例性实施方案。相反,本发明的范围和精神由所附权利要求体现。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1